Centre d expertise en analyse environnementale du Québec GRILLE D ÉVALUATION MICROBIOLOGIE
|
|
|
- Bernard Boisvert
- il y a 8 ans
- Total affichages :
Transcription
1 Centre d expertise en analyse environnementale du Québec Programme d accréditation des laboratoires d analyse GRILLE D ÉVALUATION MICROBIOLOGIE Nom du laboratoire : N o du laboratoire : l évaluation : Évaluateur-évaluatrice : DR-12-GAM Édition : 14 juillet 2014
2 1 LOCAUX ET ENVIRONNEMENT 1.1 AMÉNAGEMENT C NC Superficie de plancher d au moins 20 m 2 par personne (incluant les services connexes). Espace de réception des échantillons (fonctionnel, espace adéquat). Espace d'entreposage (rangé, classé, emplacement et espace adéquats). Espace de réfrigération (rangé, emplacement adéquat, volume et nombre adéquats). Espace de préparation des milieux de culture (surface de comptoir suffisante, aménagement fonctionnel et rangé). Salle de lavage et de stérilisation (fonctionnelle, rangée). Séparation efficace entre les zones avoisinantes lorsque des activités incompatibles s'y déroulent (structure, mur, ventilation, aménagement). Aménagement dans des locaux séparés pour les secteurs d'activité de chimie, de microbiologie et de toxicologie (activités communes non compatibles dans le même espace ou le même local). Contrôle de l'accès aux aires du laboratoire (verrou de sécurité, séparation structurale, identification). Espace de travail d'analyse (surface suffisante, 1 m 2 par personne, fonctionnel). L'ordre du laboratoire : rangement en général, allée dans le laboratoire, corridor d'accès au laboratoire, tables de travail, poste de travail. 1.2 PROPRETÉ C NC Propreté des équipements, du laboratoire (le cas échéant, un service d'entretien). Rotation des désinfectants utilisés (planchers et surfaces de travail). Instructions disponibles. DR-12-GAM Page 3 de 55
3 C NC Calendrier d'entretien Vérification de la disponibilité du calendrier d'entretien des locaux, des équipements et des tables de travail. Enregistrement du nom du désinfectant utilisé pour le nettoyage. 1.3 CONDITIONS AMBIANTES C NC La température ambiante doit se situer entre 16 C et 27 C là où se déroulent les analyses. Vérifications de l impact des conditions ambiantes sur les méthodes Température ambiante Instructions disponibles. Disponibilité du registre de température du laboratoire principal et enregistrement une fois par jour ouvrable (vérifier si l horaire de travail inclut le samedi et le dimanche). Page 4 de 55 DR-12-GAM
4 1.4 QUALITÉ DE L'ENVIRONNEMENT C NC Air ambiant Vérification mensuelle, du mois d'avril à octobre, et au trimestre le reste de l'année, de la qualité bactériologique de l'air ambiant (un résultat < 15 UFC/1000 cm 2 est jugé satisfaisant). Instructions disponibles (temps d exposition : entre 16,5 et 18 minutes) (enregistrement des mesures de correction) Surfaces de travail Vérification trimestrielle de la stérilité des surfaces de travail. La stérilité des tables de travail doit être vérifiée mensuellement (un résultat < 25 UFC/25 cm 2 est jugé satisfaisant). Instructions disponibles (enregistrement des mesures de correction). Incubateurs (3.3.2). Tables de travail. Réception des échantillons. Réfrigérateurs (3.4.2). DR-12-GAM Page 5 de 55
5 2 MATÉRIEL ET RÉACTIFS 2.1 MEMBRANES FILTRANTES C OBS Vérification de la bonne diffusion du milieu de culture, non diffusion de l encre du quadrillé et absence de région hydrophobe. C NC La conservation d'une copie de la fiche technique de chaque lot utilisé et l'enregistrement des numéros de lot ainsi que la date de la première utilisation Vérification et enregistrement de la conformité des colonies aux caractéristiques des protocoles analytiques pour chaque nouveau lot en utilisant les différents milieux de culture employés pour la technique de la membrane filtrante Instructions disponibles La mesure et l'enregistrement du pourcentage de récupération. Le pourcentage de récupération des membranes filtrantes doit être supérieur à 80 % Instructions disponibles. Page 6 de 55 DR-12-GAM
6 2.2 VERRERIE ET AUTRES ÉLÉMENTS C NC Les instructions de lavage sont disponibles et affichées dans le laboratoire Vérification de l'adéquation des étapes de lavage manuel (lavage au détergent, rinçage à l'eau chaude du robinet, dernier rinçage à l'eau distillée ou déminéralisée) Le détergent utilisé pour la méthode de lavage manuel de la verrerie doit être sans phosphate et de ph neutre Vérification et enregistrement trimestriels de la présence de résidus inhibiteurs acides ou alcalins sur différents articles et lorsque les instructions de lavage ou le détergent sont changés La solution de bleu de bromothymol est conservée à l abri de la lumière. Vérification des contenants de prélèvement. Instructions disponibles (enregistrement des mesures de correction). DR-12-GAM Page 7 de 55
7 2.3 MILIEUX DE CULTURE ET RÉACTIFS C NC Le laboratoire doit maintenir un inventaire à jour des produits déshydratés et des réactifs. Le registre doit contenir les renseignements suivants : nom du manufacturier, numéro de lot du produit, date de réception, date d'expiration Instructions disponibles Vérification et enregistrement du pourcentage de récupération des nouveaux lots de milieux de culture à la réception et après six mois d'utilisation (ouverture du contenant). Vérifier si tous les milieux sont inclus tels que MI agar et DC medium. Le pourcentage de récupération doit être supérieur à 80 %. (S assurer que l inoculum utilisé est dans les limites de quantification de la méthode) Vérification et enregistrement de la sélectivité des milieux à l'aide de souches de contrôle positives et négatives aux mêmes périodes. Vérifier si tous les milieux sont inclus (MI agar, DC medium, XLT4, etc.) Instructions disponibles Vérification et enregistrement de la sélectivité des nouveaux lots de substrats enzymatiques à l aide de souches de contrôle positives et négatives. Souches de coliformes (ex. : Citrobacter), E.coli et souche négative (ex. : Pseudomonas) Instructions disponibles Le registre de la préparation des milieux doit contenir les renseignements suivants : identification du milieu, date de préparation, date d expiration de la préparation, numéro de lot, test de stérilité, ph final, initiales de l'analyste (voir annexe I) Page 8 de 55 DR-12-GAM
8 2.4 EAU DE RINÇAGE OU DE DILUTION (tampon phosphate, eau peptonée ou eau déminéralisée stérile) Le registre doit contenir les éléments suivants pour chacun des lots de bouteilles : date de préparation, date d'expiration, numéro de lot, test de stérilité, ph (lorsque requis), volume d'eau de dilution après stérilisation (lorsque requis), initiales de l'analyste. Le ph doit satisfaire aux critères des méthodes d'analyse Instructions disponibles. C NC 2.5 EAU DÉMINÉRALISÉE OU DISTILLÉE C NC Dénombrement et enregistrement sur une base mensuelle des bactéries hétérotrophes aérobies ou anaérobies facultatives (un résultat d'eau fraîche < 1000 UFC/ml est jugé satisfaisant) Enregistrement des mesures de correction Vérification des méthodes d'entreposage de l'eau déminéralisée ou distillée (une semaine dans un contenant stérilisé ou entretien régulier effectué) Instructions d entretien disponibles et affichées au laboratoire. DR-12-GAM Page 9 de 55
9 C NC Vérification et enregistrement des résultats des paramètres énumérés ci-dessous selon les fréquences établies Disponibilité des résultats dans le laboratoire de microbiologie. Blanc d analyse de COT, métaux, azote ammoniacal effectué en n utilisant pas le même système d eau déminéralisée ou distillée (ex. : autre laboratoire, eau différente achetée, etc.). Analyses COT, métaux, azote ammoniacal réalisées dans un laboratoire accrédité. Enregistrement des mesures de correction. Paramètres Fréquence Résultat attendu Conductivité 1 / semaine < 2 µmhos/cm à 25 C ph (1) 1 / semaine 5,5-7,5 Chlore résiduel 1 / mois < 0,1 mg/l Carbone organique total 1 / 6 mois (2) < 1 mg/l Métaux 1 / année (2) < 0,05 mg/l Métaux totaux (3) 1 / année (2) 0,1 mg/l Azote ammoniacal 1 / 6 mois < 0,1 mg/l (1) Lorsque la conductivité de l'eau est inférieure à 1 µmho/cm à 25 C, la mesure du ph peut être problématique. (2) Plus fréquemment, si des problèmes surviennent dans les travaux d'analyse. (3) Cd, Cr, Cu, Ni, Pb, Zn 2.6 CONTENANTS DE PRÉLÈVEMENT C NC Vérification de l'adéquation des exigences lorsque le laboratoire a recours à des pharmacies comme dépositaires de contenants de prélèvement (présence d un sceau de sécurité, note d avertissement aux clients pour l intégrité de l échantillon, protection des contenants) Identification des lots de contenants de prélèvement placés en consigne Instructions disponibles. Page 10 de 55 DR-12-GAM
10 C NC Vérification et enregistrement de la stérilité d'au moins un contenant par lot de stérilisation et un minimum de 2 % des contenants Vérification de la stérilité d un minimum de 2 % des contenants préstérilisés d un lot obtenu d un fabricant (incluant les bouteilles «Colilert» si celles-ci sont utilisées pour l échantillonnage) Instructions disponibles pour préparation des contenants, la préparation de la solution de thiosulfate de sodium ainsi que la vérification de la stérilité (bouillon riche non sélectif) Enregistrement de la date d'expiration des contenants de prélèvement (numéro de lot, date d'expiration) Vérification de l utilisation d un scellé adéquat ou identification de la date d expiration sur chaque contenant (120 jours) Vérification et enregistrement de la teneur en thiosulfate de sodium d au moins un contenant par lot obtenu d un fabricant (incluant les bouteilles «Colilert» si celles-ci sont utilisées pour l échantillonnage). La concentration minimale doit être d environ 29 mg/l en sodium Instructions disponibles pour la vérification de la teneur en thiosulfate de sodium. DR-12-GAM Page 11 de 55
11 2.7 SOUCHES DE CONTRÔLE C NC Liste à jour des souches de contrôle (ATCC ou équivalent) Instructions et registre de conservation et de manipulation des souches de contrôle Instructions et registre de la vérification des caractères phénotypiques et de l'activité biochimique des souches de contrôle entre chaque utilisation À chaque nouvelle culture d une souche à partir d un disque bactrol, d un culti-loop, d un «cryobille», d une décongélation, etc. et au minimum une fois par année. 2.8 RÉACTIFS DE CONFIRMATION ET D'IDENTIFICATION C NC Instructions et registre du contrôle de tous les réactifs utilisés pour la confirmation et l identification des colonies (fréquence adéquate : à la réception et périodique selon l utilisation du réactif). Page 12 de 55 DR-12-GAM
12 3 ÉQUIPEMENTS C NC Vérification de l application de la procédure. Vérification de la disponibilité au laboratoire des manuels fournis par le fabricant. Vérification ou étalonnage de l équipement avant la mise en service (réception, réparation ou prêt). Identification des équipements hors d usage et de l état d étalonnage (lorsque requis). Processus d identification de problèmes et enregistrement des mesures de correction. 3.1 SYSTÈME D'INVENTAIRE DES ÉQUIPEMENTS C NC Le registre doit contenir les informations suivantes : type d'équipement, numéro d'inventaire, modèle et numéro de série, nom du manufacturier, endroit où est placé l'équipement, date de réception, état à la réception (neuf, usagé, remis en état de fonctionnement), date de mise en service. Instructions disponibles. 3.2 AUTOCLAVE C NC Enregistrement des informations suivantes pour chaque cycle de stérilisation : date, durée et température de stérilisation, matériel stérilisé, réaction du ruban thermosensible, initiales du préposé Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible Vérification et enregistrement du bon fonctionnement et de l'efficacité de stérilisation mensuellement avec un indicateur biologique Instructions disponibles. DR-12-GAM Page 13 de 55
13 3.3 INCUBATEURS ET BAINS-MARIE C NC Nettoyage des incubateurs et bains-marie Enregistrement de la température deux fois par jour d'utilisation Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible. Pour les incubateurs, les thermomètres sont à l intérieur et baignent dans l eau ou le glycérol. Conformité des thermomètres aux exigences analytiques (3.5.2) Enregistrement du taux d'humidité de l'incubateur une fois par jour Vérification annuelle de l efficacité des incubateurs et bains-marie, et enregistrement des résultats (ex. : incubateurs : 4 coins et centre de chaque étagère, en utilisation ; bains-marie : 4 coins côtés et centre, en utilisation) Instructions disponibles (utilisation d un deuxième thermomètre pour la vérification aux différents endroits en comparaison avec le thermomètre du contrôle journalier, enregistrement des deux températures). Critères d acceptabilité selon les méthodes (enregistrement des mesures de correction). Page 14 de 55 DR-12-GAM
14 3.4 RÉFRIGÉRATEURS C NC Vérification de l'identification du matériel entreposé (date d'expiration du matériel périssable) Nettoyage périodique des réfrigérateurs et élimination du matériel périmé Enregistrement de la température une fois par jour Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible. Les thermomètres sont à l intérieur et baignent dans l eau ou le glycérol. Conformité des thermomètres aux exigences analytiques (3.5.2). DR-12-GAM Page 15 de 55
15 3.5 THERMOMÈTRES C NC Vérification et enregistrement de l'étalonnage annuellement (incluant le thermomètre infrarouge) Instructions disponibles. Vérification aux températures d utilisation. Thermomètre de référence (graduation de 0,1 C). Critères d acceptabilité. Enregistrement des thermomètres dans l inventaire ou identification unique et liste des thermomètres. État d étalonnage (identification). 3.6 ÉQUIPEMENTS DE FILTRATION C NC Bon état et propreté de l'équipement de filtration Vérification de l'utilisation d une solution de silicone non bactéricide lorsque les entonnoirs de filtration sont en métal (six mois) Vérification de la toxicité de la solution de silicone utilisée. Les résultats sont conservés Enregistrement du calibrage des entonnoirs à la réception et annuellement (support à filtre muni d une grille) Instructions de calibrage disponibles. Identification des entonnoirs. Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible. Page 16 de 55 DR-12-GAM
16 3.7 STÉRILISATEURS U.V. POUR DÉSINFECTION DES ÉQUIPEMENTS DE FILTRATION Enregistrement du bon fonctionnement des lampes hebdomadairement C NC Enregistrement des tests d'efficacité germicide deux fois par année (> 99 %) Instructions de réalisation disponibles (enregistrement des mesures de correction). Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible. 3.8 ph-mètre C NC Vérification de la procédure d'étalonnage et enregistrement hebdomadaire des résultats (saturation de l'électrode, tampons utilisés) Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible. Instructions d'étalonnage disponibles. Enregistrement hebdomadaire de la pente et de la date de vérification de l'appareil. DR-12-GAM Page 17 de 55
17 3.9 BALANCES C NC Vérification du calibrage trimestriellement et enregistrement des résultats Instructions d étalonnage (poids de référence certifiés). Un étalonnage par une firme externe ne remplace pas le besoin de vérifier le calibrage sur une base trimestrielle. Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible. Identification des balances (liste d inventaire des balances) et état d étalonnage MICROPIPETTES C NC Vérification de l étalonnage annuellement et enregistrement des résultats Instructions d étalonnage. Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible. Identification des micropipettes (liste d inventaire des micropipettes) et état d étalonnage. C NC 3.11 Appareil UV servant à l observation de la fluorescence pour l obtention d un résultat analytique Vérification deux fois par année du bon fonctionnement de l appareil et enregistrement des résultats Instructions de vérification. Instructions d'entretien disponibles et gestion adéquate des défectuosités. Registre d'entretien et de réparation disponible. Page 18 de 55 DR-12-GAM
18 4 MÉTHODES D ANALYSE 4.1 CALENDRIER DES CONTRÔLES DE LA QUALITÉ C NC Vérification de la présence dans le laboratoire d'un calendrier des contrôles de la qualité. Calendrier placé à la vue du personnel. Calendrier contenant une liste des contrôles, la fréquence et les initiales de la personne qui réalise le travail. 4.2 CONTRÔLE DE LA STÉRILITÉ C NC Vérification et enregistrement sur la feuille de travail de la stérilité de l'équipement de filtration à une fréquence régulière. Les contrôles devront tenir compte des paramètres analysés, de la méthode utilisée et de la sélectivité des milieux 1 par 10 échantillons minimum Vérification et enregistrement sur la feuille de travail de la stérilité, à une fréquence régulière, selon les prescriptions des méthodes autres que la méthode de la membrane filtrante Incorporation à la gélose (1/10), présence/absence (par série d analyses), coliphages (au début et à la fin de chaque série plus 1/10). DR-12-GAM Page 19 de 55
19 4.3 CONTRÔLE DE LA MÉTHODE D'ANALYSE C NC Coliformes totaux (colonies atypiques) : méthode de la membrane filtrante pour l eau potable Confirmation et enregistrement d un minimum de deux colonies atypiques (< 30 colonies atypiques) et d une colonie par morphologie coloniale différente Confirmation et enregistrement de 10 % des colonies atypiques jusqu à concurrence de cinq colonies (> 30 colonies atypiques) et d une colonie par morphologie coloniale différente Escherichia coli (domaine 30) : méthode de la membrane filtrante pour les eaux brutes conformément au RQEP (articles 22 et 53) lorsque le milieu de culture utilisé n est pas à détection directe de la bactérie Confirmation et enregistrement d un minimum de deux colonies typiques (< 30 colonies typiques) et d une colonie par morphologie coloniale différente Confirmation et enregistrement de 10 % des colonies typiques jusqu à concurrence de cinq colonies (> 30 colonies typiques) et d une colonie par morphologie coloniale différente Page 20 de 55 DR-12-GAM
20 C NC Méthode de la membrane filtrante Autres paramètres Le laboratoire doit posséder des moyens pour confirmer la présence de microorganismes des paramètres coliformes totaux, Escherichia coli, coliformes fécaux, entérocoques, Staphylococcus aureus et Pseudomonas aeruginosa, ou les identifier, s il est accrédité pour analyser ces paramètres. Le laboratoire doit déterminer une fréquence de confirmation des colonies typiques pour chaque paramètre Autres méthodes (seulement lors de la réalisation d une série d analyses) Méthode de présence/absence par substrat enzymatique Contrôle positif pour coliformes totaux (autre que E. coli) Minimum une fois/semaine. Contrôle positif pour E. coli Minimum une fois/semaine. Confirmation d un échantillon positif Minimum une fois/semaine (coliformes totaux). Par ONPG ou identification biochimique et cytochrome oxydase (souche positive acceptée). Confirmation d un échantillon positif Minimum une fois/semaine (E. coli). Par autre test MUG ou identification biochimique et cytochrome oxydase (souche positive acceptée). Enregistrement des résultats. DR-12-GAM Page 21 de 55
21 4.4 VALIDATION, VÉRIFICATION ET SUIVI DE LA PERFORMANCE DES MÉTHODES UTILISÉES Procédure locale de validation Référence au DR-12-VMM. Protocole de réalisation de la réplicabilité, de la répétabilité et du pourcentage de récupération. Procédure de vérification annuelle des données de validation avec mention des critères d acceptabilité retenus (égaux ou inférieurs à 2 CVR). Procédure de suivi des compétences du personnel avec mention des critères d acceptabilité retenus (égaux ou inférieurs à 2 CVR). Essai de réplicabilité et duplicata interanalyste par paramètre pour chaque nouvel analyste. Registres utilisés pour l enregistrement des données et résultats. Le personnel qui n effectue que des filtrations est évalué par un essai de réplicabilité et un duplicata interanalyste pour chaque type de matrice. Traçabilité des données brutes de validation et des échantillons utilisés pour la performance et la sélectivité de la méthode C NC Vérifications des méthodes utilisées C NC A. Méthode de la membrane filtrante (étapes communes) Numérotation de l'échantillon versus feuille de travail. Stérilisation de l'équipement de filtration (minuterie). Homogénéisation de l échantillon. Volume pour filtration et dilution (selon la nature de l échantillon). Dépôt du filtre sur le support. Filtration de l'échantillon. Rinçage des entonnoirs. Dépôt du filtre sur la gélose. Page 22 de 55 DR-12-GAM
22 DOMAINES 1 et 31 : COLIFORMES TOTAUX Vérifications des méthodes utilisées C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), limite de quantification, aspect des colonies, limite de la méthode (faux positif, faux négatif), etc. Évaluation de la compétence des analystes annuellement. Contrôle de stérilité (fréquence et milieu). Incubation (température et durée). Lecture, calculs et interprétation des résultats. Méthode de confirmation des colonies et calculs. Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire , ou VALIDATION C NC Évaluation de la nouvelle méthode ou comparaison de la performance de la nouvelle méthode avec celle qui est remplacée à l aide de 20 échantillons positifs différents ou plus, comprenant chaque matrice analysée. Réplicabilité. Répétabilité. Pourcentage de récupération. Performance (sensibilité, spécificité, taux de faux positifs, taux de faux négatifs). Sélectivité. Vérification des données de validation annuellement (4.4.5) CONTRÔLE À EXERCER C NC Duplicata intraanalyste avec échantillons naturels ensemencés avec l organisme cible (un duplicata par paramètre par 50 échantillons). Au moins un duplicata intraanalyste par paramètre doit être effectué chaque année. Duplicata trimestriel interanalyste avec des matrices naturellement contaminées. Comparaison annuelle de lecture d un échantillon naturellement positif pour l ensemble des analystes. DR-12-GAM Page 23 de 55
23 DOMAINES 1 et 30 : Escherichia coli Vérifications des méthodes utilisées C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), limite de quantification, aspect des colonies, limite de la méthode (faux positif, faux négatif), etc. Évaluation de la compétence des analystes annuellement. Contrôle de stérilité (fréquence et milieu). Incubation (température et durée). Lecture, calculs et interprétation des résultats. Méthode de confirmation des colonies et calculs. Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire , ou VALIDATION C NC Évaluation de la nouvelle méthode ou comparaison de la performance de la nouvelle méthode avec celle qui est remplacée à l aide de 20 échantillons positifs différents ou plus, comprenant chaque matrice analysée. Réplicabilité. Répétabilité. Pourcentage de récupération. Performance (sensibilité, spécificité, taux de faux positifs, taux de faux négatifs). Sélectivité. Vérification des données de validation annuellement (4.4.5) CONTRÔLE À EXERCER C NC Duplicata intraanalyste avec échantillons naturels ensemencés avec l organisme cible (un duplicata par paramètre par 50 échantillons). Au moins un duplicata intraanalyste par paramètre doit être effectué chaque année. Duplicata trimestriel interanalyste avec des matrices naturellement contaminées. Comparaison annuelle de lecture d un échantillon naturellement positif pour l ensemble des analystes. Page 24 de 55 DR-12-GAM
24 DOMAINE 30 : Coliformes fécaux Vérifications des méthodes utilisées C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), limite de quantification, aspect des colonies, limite de la méthode (faux positif, faux négatif), etc. Évaluation de la compétence des analystes annuellement. Contrôle de stérilité (fréquence et milieu). Incubation (température et durée). Lecture, calculs et interprétation des résultats. Méthode de confirmation des colonies et calculs. Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire , ou VALIDATION C NC Évaluation de la nouvelle méthode ou comparaison de la performance de la nouvelle méthode avec celle qui est remplacée à l aide de 20 échantillons positifs différents ou plus, comprenant chaque matrice analysée. Réplicabilité. Répétabilité. Pourcentage de récupération. Performance (sensibilité, spécificité, taux de faux positifs, taux de faux négatifs). Sélectivité. Vérification des données de validation annuellement (4.4.5) CONTRÔLE À EXERCER C NC Duplicata intraanalyste avec échantillons naturels ensemencés avec l organisme cible (un duplicata par paramètre par 50 échantillons). Au moins un duplicata intraanalyste par paramètre doit être effectué chaque année. Duplicata trimestriel interanalyste avec des matrices naturellement contaminées. Comparaison annuelle de lecture d un échantillon naturellement positif pour l ensemble des analystes. DR-12-GAM Page 25 de 55
25 DOMAINE 2 : ENTÉROCOQUES Vérifications des méthodes utilisées C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), limite de quantification, aspect des colonies, limite de la méthode (faux positif, faux négatif), etc. Évaluation de la compétence des analystes annuellement. Contrôle de stérilité (fréquence et milieu). Incubation (température et durée). Lecture, calculs et interprétation des résultats. Méthode de confirmation des colonies et calculs. Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire , ou VALIDATION C NC Évaluation de la nouvelle méthode ou comparaison de la performance de la nouvelle méthode avec celle qui est remplacée à l aide de 20 échantillons positifs différents ou plus, comprenant chaque matrice analysée. Réplicabilité. Répétabilité. Pourcentage de récupération. Performance (sensibilité, spécificité, taux de faux positifs, taux de faux négatifs). Sélectivité. Vérification des données de validation annuellement (4.4.5) CONTRÔLE À EXERCER C NC Duplicata intraanalyste avec échantillons naturels ensemencés avec l organisme cible (un duplicata par paramètre par 50 échantillons). Au moins un duplicata intraanalyste par paramètre doit être effectué chaque année. Duplicata trimestriel interanalyste avec des matrices naturellement contaminées. Comparaison annuelle de lecture d un échantillon naturellement positif pour l ensemble des analystes. Page 26 de 55 DR-12-GAM
26 DOMAINE 3 : Staphylococcus aureus Vérifications des méthodes utilisées C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), limite de quantification, aspect des colonies, limite de la méthode (faux positif, faux négatif), etc. Évaluation de la compétence des analystes annuellement. Contrôle de stérilité (fréquence et milieu). Incubation (température et durée). Lecture, calculs et interprétation des résultats. Méthode de confirmation des colonies et calculs. Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire , ou VALIDATION C NC Évaluation de la nouvelle méthode ou comparaison de la performance de la nouvelle méthode avec celle qui est remplacée à l aide de 20 échantillons positifs différents ou plus, comprenant chaque matrice analysée. Réplicabilité. Répétabilité. Pourcentage de récupération. Performance (sensibilité, spécificité, taux de faux positifs, taux de faux négatifs). Sélectivité. Vérification des données de validation annuellement (4.4.5) CONTRÔLE À EXERCER C NC Duplicata intraanalyste avec échantillons naturels ensemencés avec l organisme cible (un duplicata par paramètre par 50 échantillons). Au moins un duplicata intraanalyste par paramètre doit être effectué chaque année. Duplicata trimestriel interanalyste avec des matrices naturellement contaminées. Comparaison annuelle de lecture d un échantillon naturellement positif pour l ensemble des analystes. DR-12-GAM Page 27 de 55
27 DOMAINE 3 : Pseudomonas aeruginosa Vérifications des méthodes utilisées C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), limite de quantification, aspect des colonies, limite de la méthode (faux positif, faux négatif), etc. Évaluation de la compétence des analystes annuellement. Contrôle de stérilité (fréquence et milieu). Incubation (température et durée). Lecture, calculs et interprétation des résultats. Méthode de confirmation des colonies et calculs. Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire , ou VALIDATION C NC Évaluation de la nouvelle méthode ou comparaison de la performance de la nouvelle méthode avec celle qui est remplacée à l aide de 20 échantillons positifs différents ou plus, comprenant chaque matrice analysée. Réplicabilité. Répétabilité. Pourcentage de récupération. Performance (sensibilité, spécificité, taux de faux positifs, taux de faux négatifs). Sélectivité. Vérification des données de validation annuellement (4.4.5) CONTRÔLE À EXERCER C NC Duplicata intraanalyste avec échantillons naturels ensemencés avec l organisme cible (un duplicata par paramètre par 50 échantillons). Au moins un duplicata intraanalyste par paramètre doit être effectué chaque année. Duplicata trimestriel interanalyste avec des matrices naturellement contaminées. Comparaison annuelle de lecture d un échantillon naturellement positif pour l ensemble des analystes. Page 28 de 55 DR-12-GAM
28 DOMAINE 36 : Escherichia coli Matières solides Vérifications des méthodes utilisées C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), limite de quantification, aspect des colonies, limite de la méthode (faux positif, faux négatif), etc. Évaluation de la compétence des analystes annuellement. Homogénéisation de l échantillon, pesée (50 g) et mélange dans eau stérile. Utilisation d un mélangeur. Méthode utilisée pour établir le poids sec (minimum une nuit à 105 C). Dilution : respect des critères P2 < UFC/g (b.s.). Contrôle de stérilité (fréquence et milieu). Incubation (température et durée). Lecture, calculs avec prise en compte du poids sec : E. coli UFC/g (b.s.) et interprétation des résultats. Méthode de confirmation des colonies et calculs. Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire , ou VALIDATION C NC Évaluation de la nouvelle méthode ou comparaison de la performance de la nouvelle méthode avec celle qui est remplacée à l aide de 20 échantillons positifs différents ou plus, comprenant chaque matrice analysée. Réplicabilité. Répétabilité. Pourcentage de récupération. Performance (sensibilité, spécificité, taux de faux positifs, taux de faux négatifs). Sélectivité. Vérification des données de validation annuellement (4.4.5). DR-12-GAM Page 29 de 55
29 CONTRÔLE À EXERCER C NC Duplicata intraanalyste avec échantillons naturels ensemencés avec l organisme cible (un duplicata par paramètre par 50 échantillons). Au moins un duplicata intraanalyste par paramètre doit être effectué chaque année. Duplicata trimestriel interanalyste avec des matrices naturellement contaminées. Comparaison annuelle de lecture d un échantillon naturellement positif pour l ensemble des analystes. Page 30 de 55 DR-12-GAM
30 5.6 ÉCHANTILLON N o 1 N d'échantillon dans le registre Milieux de culture préparation ph Stérilité Nom du client N o lot m-endo prélèvement N o lot m-fc réception N o lot MI Agar Date d'analyse N o lot DC medium Température de l échantillon à l arrivée (EP) N o lot m-pac Paramètres demandés N o lot Baird- Parker Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + N o lot Date Stérilité Eau de rinçage N o lot Eau de dilution N o lot Rapport d'analyse Paramètre Unités Eau stérile N o lot Membranes filt. Date Récupération N o lot Signature Confirmation Eau déminéralisée ph Conductivité Date : Incubation T ( C) AM PM AM PM Incubateur n o 35 Incubateur n o Calculs Calcul du poids sec pour le domaine 36 Bain n o 44,5 Bain n o Bain n o Initiales de la personne qui vérifie les calculs DR-12-GAM Page 31 de 55
31 ÉCHANTILLON N o 2 N d'échantillon dans le registre Milieux de culture préparation ph Stérilité Nom du client N o lot m-endo prélèvement N o lot m-fc réception N o lot MI Agar Date d'analyse N o lot DC medium Température de l échantillon à l arrivée (EP) N o lot m-pac Paramètres demandés N o lot Baird- Parker Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + N o lot Date Stérilité Eau de rinçage N o lot Eau de dilution N o lot Rapport d'analyse Paramètre Unités Eau stérile N o lot Membranes filt. Date Récupération N o lot Signature Confirmation Eau déminéralisée ph Conductivité Date : Incubation T ( C) AM PM AM PM Incubateur n o 35 Incubateur n o Calculs Calcul du poids sec pour le domaine 36 Bain n o 44,5 Bain n o Bain n o Initiales de la personne qui vérifie les calculs Page 32 de 55 DR-12-GAM
32 ÉCHANTILLON N o 3 N d'échantillon dans le registre Milieux de culture préparation ph Stérilité Nom du client N o lot m-endo prélèvement N o lot m-fc réception N o lot MI Agar Date d'analyse N o lot DC medium Température de l échantillon à l arrivée (EP) N o lot m-pac Paramètres demandés N o lot Baird- Parker Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + N o lot Date Stérilité Eau de rinçage N o lot Eau de dilution N o lot Rapport d'analyse Paramètre Unités Eau stérile N o lot Membranes filt. Date Récupération N o lot Signature Confirmation Eau déminéralisée ph Conductivité Date : Incubation T ( C) AM PM AM PM Incubateur n o 35 Incubateur n o Calculs Calcul du poids sec pour le domaine 36 Bain n o 44,5 Bain n o Bain n o Initiales de la personne qui vérifie les calculs DR-12-GAM Page 33 de 55
33 ÉCHANTILLON N o 4 N d'échantillon dans le registre Milieux de culture préparation ph Stérilité Nom du client N o lot m-endo prélèvement N o lot m-fc réception N o lot MI Agar Date d'analyse N o lot DC medium Température de l échantillon à l arrivée (EP) N o lot m-pac Paramètres demandés N o lot Baird- Parker Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + N o lot Date Stérilité Eau de rinçage N o lot Eau de dilution N o lot Rapport d'analyse Paramètre Unités Eau stérile N o lot Membranes filt. Date Récupération N o lot Signature Confirmation Eau déminéralisée ph Conductivité Date : Incubation T ( C) AM PM AM PM Incubateur n o 35 Incubateur n o Calculs Calcul du poids sec pour le domaine 36 Bain n o 44,5 Bain n o Bain n o Initiales de la personne qui vérifie les calculs Page 34 de 55 DR-12-GAM
34 ÉCHANTILLON N o 5 N d'échantillon dans le registre Milieux de culture préparation ph Stérilité Nom du client N o lot m-endo prélèvement N o lot m-fc réception N o lot MI Agar Date d'analyse N o lot DC medium Température de l échantillon à l arrivée (EP) N o lot m-pac Paramètres demandés N o lot Baird- Parker Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + N o lot Date Stérilité Eau de rinçage N o lot Eau de dilution N o lot Rapport d'analyse Paramètre Unités Eau stérile N o lot Membranes filt. Date Récupération N o lot Signature Confirmation Eau déminéralisée ph Conductivité Date : Incubation T ( C) AM PM AM PM Incubateur n o 35 Incubateur n o Calculs Calcul du poids sec pour le domaine 36 Bain n o 44,5 Bain n o Bain n o Initiales de la personne qui vérifie les calculs DR-12-GAM Page 35 de 55
35 DOMAINES 2 et 5 : BHAA Méthode par incorporation à la gélose C NC Connaissances théoriques : définitions, milieux de culture (propriétés), limite de quantification, etc. Évaluation de la compétence des analystes annuellement. Préparation, vérification du ph et stérilité du milieu avant utilisation. Numérotation de l'échantillon versus feuille de travail. Vérification de la température de la gélose fondue, 3 heures max. à 45 C Homogénéisation de l échantillon. Volume pour incorporation et dilution (au moins 1 et 0,1 ml). Contrôle de stérilité (fréquence et milieu). Incubation (température et durée). Lecture, calculs et interprétation des résultats (compteur de colonies). Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire , ou VALIDATION C NC Évaluation de la nouvelle méthode ou comparaison de la performance de la nouvelle méthode avec celle qui est remplacée à l aide de 20 échantillons positifs différents ou plus, comprenant chaque matrice analysée. Réplicabilité. Répétabilité. Vérification des données de validation annuellement (4.4.5) CONTRÔLE À EXERCER C NC Duplicata intraanalyste avec échantillons naturels ensemencés avec l organisme cible (un duplicata par paramètre par 50 échantillons). Au moins un duplicata intraanalyste par paramètre doit être effectué chaque année. Duplicata trimestriel interanalyste avec des matrices naturellement contaminées. Comparaison annuelle de lecture d un échantillon naturellement positif pour l ensemble des analystes. Page 36 de 55 DR-12-GAM
36 5.6 ÉCHANTILLON N o 1 N d'échantillon dans le registre Milieux de culture préparation ph Stérilité Nom du client N o lot R2A prélèvement N o lot réception Incubation T ( C) AM PM AM PM Date d'analyse Incubateur n o 35 Paramètres demandés Incubateur n o Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + Eau déminéralisée ph Conductivité Date : Rapport d'analyse Unités Signature ÉCHANTILLON N o 2 N d'échantillon dans le registre Milieux de culture préparation ph Stérilité Nom du client N o lot R2A prélèvement N o lot réception Incubation T ( C) AM PM AM PM Date d'analyse Incubateur n o 35 Paramètres demandés Incubateur n o Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + Eau déminéralisée ph Conductivité Date : Rapport d'analyse Unités Signature DR-12-GAM Page 37 de 55
37 DOMAINE 4 : COLIFORMES TOTAUX et E. coli SUBSTRAT ENZYMATIQUE Méthode de présence/absence C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), interférences et limite de la méthode (faux positif, faux négatif), etc. Formation du personnel et autorisations pour la réalisation de la méthode. Numérotation de l'échantillon versus feuille de travail. Contrôle de stérilité (fréquence). Utilisation d eau déminéralisée stérile. Homogénéisation de l échantillon. Volume et mise du réactif. Incubation (température et durée). Lecture et interprétation des résultats. Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire CONTRÔLE À EXERCER C NC Contrôle positif au minimum une fois par semaine d analyse. Page 38 de 55 DR-12-GAM
38 5.6 ÉCHANTILLON N o 1 N d'échantillon dans le registre Réactif N o lot Nom du client Colilert prélèvement Colilert réception Date Stérilité Date d'analyse Eau stérile N o lot Température de l échantillon à l arrivée Incubation T ( C) AM PM AM PM Paramètres demandés Incubateur n o 35 Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + Incubateur n o Rapport d'analyse Paramètre Signature DR-12-GAM Page 39 de 55
39 ÉCHANTILLON N o 2 N d'échantillon dans le registre Réactif N o lot Nom du client Colilert prélèvement Colilert réception Date Stérilité Date d'analyse Eau stérile N o lot Température de l échantillon à l arrivée Incubation T ( C) AM PM AM PM Paramètres demandés Incubateur n o 35 Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + Incubateur n o Rapport d'analyse Paramètre Signature Page 40 de 55 DR-12-GAM
40 ÉCHANTILLON N o 3 N d'échantillon dans le registre Réactif N o lot Nom du client Colilert prélèvement Colilert réception Date Stérilité Date d'analyse Eau stérile N o lot Température de l échantillon à l arrivée Incubation T ( C) AM PM AM PM Paramètres demandés Incubateur n o 35 Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + Incubateur n o Rapport d'analyse Paramètre Signature DR-12-GAM Page 41 de 55
41 ÉCHANTILLON N o 4 N d'échantillon dans le registre Réactif N o lot Nom du client Colilert prélèvement Colilert réception Date Stérilité Date d'analyse Eau stérile N o lot Température de l échantillon à l arrivée Incubation T ( C) AM PM AM PM Paramètres demandés Incubateur n o 35 Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + Incubateur n o Rapport d'analyse Paramètre Signature Page 42 de 55 DR-12-GAM
42 ÉCHANTILLON N o 5 N d'échantillon dans le registre Réactif N o lot Nom du client Colilert prélèvement Colilert réception Date Stérilité Date d'analyse Eau stérile N o lot Température de l échantillon à l arrivée Incubation T ( C) AM PM AM PM Paramètres demandés Incubateur n o 35 Feuille de travail Paramètres bruts Volumes analysés Ctrl stérilité Ctrl + Incubateur n o Rapport d'analyse Paramètre Signature DR-12-GAM Page 43 de 55
43 DOMAINE 6 : COLIPHAGES Méthode de détection des virus coliphages MS2 (mâle spécifique F+) Enrichissement en deux étapes Connaissances théoriques : définitions, principes, interférences et limite de la méthode. Formation du personnel et autorisations pour la réalisation de la méthode. Numérotation de l'échantillon versus feuille de travail. Préparation d une culture en phase log de la souche hôte (E. coli F amp), bouillon avec ampicilline. Homogénéisation de l échantillon (100 ml). Préparation des échantillons et ajouts des suppléments Précaution pour le mélange. Contrôle de stérilité à faire au début et à la fin de chaque série d analyse + un à chaque tranche de 10 (avant le contrôle positif ou les contrôles de matrices). Contrôle positif ou contrôles de matrices à la fin de chaque série. Incubation (température 36 C et durée environ heures). Préparation des géloses pour le «spot-test». Homogénéisation des échantillons après la première incubation. Inoculation des géloses absorption (filtration suggérée avec Acrodisc). Incubation (36 C, heures). Lecture et interprétation des résultats (zone de lyse : claire). Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire. C NC Page 44 de 55 DR-12-GAM
44 N d'échantillon dans le registre Nom du client prélèvement réception 5.6 ÉCHANTILLON N o 1 Milieux de culture N o lot TSB N o lot gélose pour spot-test N o lot préparation ph Stérilité Date d'analyse Incubation T ( C) AM PM AM PM Paramètres demandés Feuille de travail Paramètres bruts Volumes analysés Témoin Ctrl + Incubateur n o Incubateur n o Eau déminéralisée 36 ph Conductivité Rapport d analyse Paramètre Date : Signature DR-12-GAM Page 45 de 55
45 DOMAINE 35 : SALMONELLES Méthode de présence/absence pour salmonelles C NC Connaissances théoriques : définitions, milieux de culture (propriétés et préparation), norme (salmonelles non détectées dans 10 g humides pour résidus ayant une siccité 15 % ou dans 50 g humides pour les autres), etc. Formation du personnel et autorisations pour la réalisation de la méthode. Numérotation de l'échantillon versus feuille de travail. Préparation de l échantillon : Échantillon solide : homogénéisation de l échantillon, pesée (10 ou 50 g) et mélange avec TSB (utilisation d un mélangeur), vérification du ph; Échantillon liquide très chargé : homogénéisation de l échantillon, volume (50 ml) et mélange avec TSB (450 ml), vérification du ph; Échantillon liquide : filtration de l échantillon et dépôt de la membrane dans le TSB, analyse 1 échantillon : 4 TSB. Incubation (36 ºC, 24 ± 2 h). Contrôle positif ou contrôle de matrice (chaque échantillon, un tube pour chaque dilution) et contrôle de stérilité (par série d analyses). Dépôt d inoculum sur gélose MSRV. Incubation (42 + 0,5 C, h). Les boîtes de Pétri ne doivent pas être incubées à l envers. Attendre 48 h avant de déclarer un résultat négatif. Lecture (halo blanchâtre de croissance à l extérieur du site d inoculation). Repiquage des salmonelles (prendre au moins 2 inoculums à l intérieur de la gélose) sur XLT4. Incubation (36 ºC, 24 ± 2 h). Lecture (colonies noires, roses avec ou sans centre noir ou jaune avec ou sans centre noir). Confirmation (oxydase et galerie d identification). Réalisation des différentes étapes selon la méthode écrite disponible au laboratoire. Page 46 de 55 DR-12-GAM
46 5.6 ÉCHANTILLON N o 1 N d'échantillon dans le registre Milieux de culture préparation ph Stérilité Nom du client N o lot Col. TSB prélèvement N o lot Col. MSRV réception N o lot XLT4 Date d'analyse N o lot Paramètres demandés Feuille de travail Paramètres Rapport d'analyse bruts Volumes/poids analysés Ctrl stérilité Ctrl + Paramètre Unités Eau déminéralisée ph Conductivité Date : Incubation T ( C) AM PM AM PM Incubateur n o Incubateur n o Incubateur n o Confirmation Signature DR-12-GAM Page 47 de 55
47 4.5 CONFORMITÉ RÈGLEMENTAIRE RQEP (2001) (Annexe II de SCA-02) Réseaux avec 21 personnes et plus : C NC Escherichia coli : Transmission automatique des résultats obtenus par dénombrement direct de la bactérie E. coli sans confirmation; Modification non permise des résultats transmis en rapport préliminaire lors de la transmission du rapport officiel. Coliformes totaux : Transmission des résultats après confirmation des colonies atypiques seulement (résultats < 200 UFC/100 ml); Éviter la transmission de rapport préliminaire avant la confirmation. Suivi d un rapport final après confirmation (possibilité de résultats différents pouvant entraîner de la confusion). Colonies atypiques : Transmission automatique des résultats sans confirmation pour les résultats suivants : Colonies atypiques > 200 UFC/100 ml, TNC ou TNI. Lors d un résultat > 200 UFC/100 ml, ne pas inscrire de résultat pour les coliformes totaux. Colonies atypiques et résultats TNI sur milieux combinés Résultat > 200 UFC/100 ml colonies atypiques, aucune colonie de E. coli et absence de confluence : Émission d un résultat de > 200 colonies atypiques, aucun résultat pour les coliformes totaux et 0 UFC/100 ml pour E. coli. Il s'agira d'un résultat non conforme. Le laboratoire doit transmettre immédiatement les résultats à l'exploitant et dans les meilleurs délais possibles pendant les heures ouvrables à la direction régionale et à la direction de la santé publique. Résultat > 200 UFC/100 ml colonies atypiques, présence d au moins une colonie de E. coli et absence de confluence : Émission d un résultat > 200 colonies atypiques, aucun résultat à coliformes totaux et inscrire le nombre de colonies observées par UFC/100 ml pour E. coli. Le résultat doit être transmis immédiatement par téléphone à l'exploitant, à la direction régionale et à la direction de la santé publique. Résultat TNI (confluence importante) et aucune colonie de E. coli : Émission d un résultat TNI pour les coliformes totaux et E. coli. Il s'agit d'un résultat non conforme pour E. coli. Le résultat doit être transmis immédiatement par téléphone à l'exploitant, à la direction régionale et à la direction de la santé publique. Résultat TNI (confluence importante) et présence de colonie de E. coli : Émission d un résultat TNI pour les coliformes totaux et pour E. coli (inscrire le nombre de colonies observées). Il s'agit d'un résultat positif pour E. coli. Le résultat doit être transmis immédiatement par téléphone à l'exploitant, à la direction régionale et à la direction de la santé publique. Page 48 de 55 DR-12-GAM
48 4.5.2 Petits réseaux ou puits individuels : C NC Avis immédiat d eau non potable et d ébullition avant consommation si détection d organismes pathogènes ou indicateurs d une contamination d origine fécale, d entérocoques ou de virus coliphages. Recommandation de procéder à une désinfection, d évaluer des sources de contamination et d effectuer un nouvel échantillonnage lorsque l eau contient > 10 coliformes totaux/100 ml, > 200 atypiques/100 ml. DR-12-GAM Page 49 de 55
49 5 TRAÇABILITÉ DE L INFORMATION (PALA 4.13, 5.8 ET 5.10) C NC Vérification de l application des procédures ou instructions. Enregistrement des observations, des données et des calculs au moment où ils sont effectués et vérification pour déterminer s ils peuvent être liés à l opération concernée. Modification des enregistrements originaux de façon à ne pas rendre illisible l original, valeur correcte inscrite à côté et initiales pour autorisation des changements. Calculs et transfert de données vérifiés de façon systématique. Pour les enregistrements électroniques, le laboratoire doit démontrer qu il respecte toutes les exigences prévues à la présente section. 5.1 ÉCHANTILLONNAGE ET CONSERVATION DES ÉCHANTILLONS C NC Disponibilité d'un dépliant dans lequel est décrite la technique de prélèvement des échantillons pour le client (retour au laboratoire, type, contenant, etc.). Pour les échantillons assujettis au Règlement sur la qualité de l eau potable, vérifier si les dépliants ou les protocoles pour la technique de prélèvement sont à jour avec la version officielle du RQEP, annexe 4 : Normes de prélèvement et de conservation des échantillons d eau. Pour les échantillons assujettis au Règlement sur la qualité de l eau des piscines et autres bassins artificiels, vérifier si les dépliants ou les protocoles pour la technique de prélèvement sont à jour avec la version officielle du DR : Méthodes de prélèvement, de conservation et d analyse des échantillons relatifs à l évaluation de la qualité de l eau des piscines et autres bassins artificiels. Les échantillons doivent toujours être prélevés dans des contenants stériles à large ouverture (DR-09-05). Le laboratoire possède des glacières et des agents réfrigérants (RQEP, annexe 4 et DR-09-05). Le nettoyage des glacières s effectue sur une base régulière (DR-12-SCA-02 et DR-09-05). Les échantillons destinés à l analyse microbiologique sont conservés idéalement à une température d environ 4 ºC entre le moment du prélèvement et la réception au laboratoire (DR-12-SCA-02). La mesure de la température est réalisée à l arrivée des échantillons au laboratoire à l aide d un thermomètre à infrarouge (non applicable pour les échantillons prélevés moins d une heure avant l arrivée au laboratoire s ils sont conservés dans les conditions de refroidissement requises) (DR-12-SCA-02). La température des échantillons ne dépasse pas 12 C (soit 10 C plus 2 C). Le cas échéant, le responsable du système de distribution est avisé du dépassement de ce critère de température pour le sensibiliser aux problèmes potentiels (DR-12-SCA-02). Page 50 de 55 DR-12-GAM
Les Bonnes Pratiques Hygiéniques dans l Industrie Alimentaire
 Les Bonnes Pratiques Hygiéniques dans l Industrie Alimentaire 1- Hygiène du personnel Lors de l'embauche à l entreprise, toute personne affectée au travail et à la manipulation des produits est soumise
Les Bonnes Pratiques Hygiéniques dans l Industrie Alimentaire 1- Hygiène du personnel Lors de l'embauche à l entreprise, toute personne affectée au travail et à la manipulation des produits est soumise
RAPID Salmonella/Gélose 356-3961 356-3963 356-4705
 356-3961 356-3963 356-4705 DOMAINE D APPLICATION La gélose RAPID Salmonella est un milieu chromogénique utilisé pour la recherche des Salmonella spp. lors de l'analyse des produits d alimentation humaine
356-3961 356-3963 356-4705 DOMAINE D APPLICATION La gélose RAPID Salmonella est un milieu chromogénique utilisé pour la recherche des Salmonella spp. lors de l'analyse des produits d alimentation humaine
CATALOGUE DE PRESTATIONS FORMATION ET CONSEILS
 (1/30pages) CATALOGUE DE PRESTATIONS FORMATION ET CONSEILS ANNEE : 2015 Date de mise à jour : 09/03/2015 1 - Microbiologie des eaux - Microbiologie des aliments Formation technique de Microbiologie HYGIÈNE
(1/30pages) CATALOGUE DE PRESTATIONS FORMATION ET CONSEILS ANNEE : 2015 Date de mise à jour : 09/03/2015 1 - Microbiologie des eaux - Microbiologie des aliments Formation technique de Microbiologie HYGIÈNE
Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire
 1 2 3 4 Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire Partie 1 Chapitre 3: Locaux et matériel 5 6 7 8 9 10 11 12 13 PRINCIPE Les locaux et le matériel doivent être situés,
1 2 3 4 Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire Partie 1 Chapitre 3: Locaux et matériel 5 6 7 8 9 10 11 12 13 PRINCIPE Les locaux et le matériel doivent être situés,
Science et technique. La température et la durée de stockage sont des facteurs déterminants. Viande bovine et micro-organisme pathogène
 Science et technique Viande bovine et micro-organisme pathogène La température et la durée de stockage sont des facteurs déterminants La contamination des carcasses lors des opérations d abattage et la
Science et technique Viande bovine et micro-organisme pathogène La température et la durée de stockage sont des facteurs déterminants La contamination des carcasses lors des opérations d abattage et la
Sensibilisation des opérateurs à l hygiène des aliments
 Sensibilisation des opérateurs à l hygiène des aliments Le respect des bonnes pratiques d hygiène de fabrication, par chaque opérateur, constitue le préalable à toute démarche de maîtrise de la sécurité
Sensibilisation des opérateurs à l hygiène des aliments Le respect des bonnes pratiques d hygiène de fabrication, par chaque opérateur, constitue le préalable à toute démarche de maîtrise de la sécurité
Construire un plan de nettoyage et de désinfection
 Construire un plan de nettoyage et de désinfection Docteur Régine POTIÉ-RIGO Médecin du Travail Mlle Laetitia DAVEZAT IPRP Ingénieur Hygiène/Sécurité Mme Laetitia MARCHE Technicienne des services généraux
Construire un plan de nettoyage et de désinfection Docteur Régine POTIÉ-RIGO Médecin du Travail Mlle Laetitia DAVEZAT IPRP Ingénieur Hygiène/Sécurité Mme Laetitia MARCHE Technicienne des services généraux
formations professionnelles fin 2014 / début 2015 hygiène alimentaire en restauration collective audit, conseil et formation professionnelle
 audit, conseil et formation professionnelle Stage 1 Bonnes pratiques d hygiène en restauration collective 19 et 26 novembre Stage 2 Règles d hygiène lors du service 3 décembre Stage 3 Le nettoyage et la
audit, conseil et formation professionnelle Stage 1 Bonnes pratiques d hygiène en restauration collective 19 et 26 novembre Stage 2 Règles d hygiène lors du service 3 décembre Stage 3 Le nettoyage et la
Décrets, arrêtés, circulaires
 Décrets, arrêtés, circulaires TEXTES GÉNÉRAUX MINISTÈRE DE LA SANTÉ ET DES SOLIDARITÉS Arrêté du 11 janvier 2007 relatif aux limites et références de qualité des eaux brutes et des eaux destinées à la
Décrets, arrêtés, circulaires TEXTES GÉNÉRAUX MINISTÈRE DE LA SANTÉ ET DES SOLIDARITÉS Arrêté du 11 janvier 2007 relatif aux limites et références de qualité des eaux brutes et des eaux destinées à la
Objet : Critères microbiologiques applicables aux auto-contrôles sur les carcasses d'animaux de boucherie. Destinataires d'exécution
 Ordre de méthode Direction générale de l'alimentation Sous-direction de la sécurité sanitaire des aliments Bureau des établissements d'abattage et de découpe 251 rue de Vaugirard 75 732 PARIS CEDEX 15
Ordre de méthode Direction générale de l'alimentation Sous-direction de la sécurité sanitaire des aliments Bureau des établissements d'abattage et de découpe 251 rue de Vaugirard 75 732 PARIS CEDEX 15
Centre d expertise en analyse environnementale du Québec GRILLE D ÉVALUATION SYSTÈME DE MANAGEMENT
 Centre d expertise en analyse environnementale du Québec Programme d accréditation des laboratoires d analyse GRILLE D ÉVALUATION SYSTÈME DE MANAGEMENT Nom du laboratoire : N o du laboratoire : Date de
Centre d expertise en analyse environnementale du Québec Programme d accréditation des laboratoires d analyse GRILLE D ÉVALUATION SYSTÈME DE MANAGEMENT Nom du laboratoire : N o du laboratoire : Date de
Les piscines à usage collectif Règles sanitaires. à usage collectif
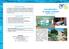 Déclaration d ouverture La déclaration d ouverture d une piscine (accompagnée d un dossier justificatif) est à adresser en 3 exemplaires à la mairie d implantation de l établissement et un exemplaire en
Déclaration d ouverture La déclaration d ouverture d une piscine (accompagnée d un dossier justificatif) est à adresser en 3 exemplaires à la mairie d implantation de l établissement et un exemplaire en
β-galactosidase A.2.1) à 37 C, en tampon phosphate de sodium 0,1 mol/l ph 7 plus 2-mercaptoéthanol 1 mmol/l et MgCl 2 1 mmol/l (tampon P)
 bioch/enzymo/tp-betagal-initiation-michaelis.odt JF Perrin maj sept 2008-sept 2012 page 1/6 Etude de la β-galactosidase de E. Coli : mise en évidence d'un comportement Michaélien lors de l'hydrolyse du
bioch/enzymo/tp-betagal-initiation-michaelis.odt JF Perrin maj sept 2008-sept 2012 page 1/6 Etude de la β-galactosidase de E. Coli : mise en évidence d'un comportement Michaélien lors de l'hydrolyse du
Méthodes de laboratoire Évaluation de structures mycologiques par examen microscopique
 Méthodes de laboratoire Évaluation de structures mycologiques par examen microscopique MÉTHODE ANALYTIQUE 360 Applicabilité Cette méthode est utilisée pour l évaluation semi-quantitative des structures
Méthodes de laboratoire Évaluation de structures mycologiques par examen microscopique MÉTHODE ANALYTIQUE 360 Applicabilité Cette méthode est utilisée pour l évaluation semi-quantitative des structures
5. Matériaux en contact avec l eau
 Monitoring de la qualité Microbiologique de l eau potable dans les réseaux de distributions Intérêt de l utilisation d un kit de mesure rapide de la flore totale UTLISATIONS 1. Surveillance de Réseau mixte
Monitoring de la qualité Microbiologique de l eau potable dans les réseaux de distributions Intérêt de l utilisation d un kit de mesure rapide de la flore totale UTLISATIONS 1. Surveillance de Réseau mixte
Registres de fermentation lente. Critères d inspection
 Chapitre 15 - tâches liées traitement non-thermique Chapitre 15 - tâches liées traitement non-thermique Registres de fermentation lente 1.15.0.3204 Registres de fermentation lente Registres Un échantillon
Chapitre 15 - tâches liées traitement non-thermique Chapitre 15 - tâches liées traitement non-thermique Registres de fermentation lente 1.15.0.3204 Registres de fermentation lente Registres Un échantillon
La réalisation d essais en réacteur pilote en vue d une demande d homologation de digestat
 La réalisation d essais en réacteur pilote en vue d une demande d homologation de digestat M CORDELIER, JF. LASCOURREGES, C. PEYRELASSE, C.LAGNET, P.POUECH 4 ième Journées Industrielles Méthanisation 4
La réalisation d essais en réacteur pilote en vue d une demande d homologation de digestat M CORDELIER, JF. LASCOURREGES, C. PEYRELASSE, C.LAGNET, P.POUECH 4 ième Journées Industrielles Méthanisation 4
Peroxyacide pour l'hygiène dans les industries agroalimentaires
 P3-oxonia active Description Peroxyacide pour l'hygiène dans les industries agroalimentaires Qualités Le P3-oxonia active est efficace à froid. Il n'est ni rémanent ni polluant. Il ne contient pas d'acide
P3-oxonia active Description Peroxyacide pour l'hygiène dans les industries agroalimentaires Qualités Le P3-oxonia active est efficace à froid. Il n'est ni rémanent ni polluant. Il ne contient pas d'acide
4. Conditionnement et conservation de l échantillon
 1. Objet S-II-3V1 DOSAGE DU MERCURE DANS LES EXTRAITS D EAU RÉGALE Description du dosage du mercure par spectrométrie d absorption atomique de vapeur froide ou par spectrométrie de fluorescence atomique
1. Objet S-II-3V1 DOSAGE DU MERCURE DANS LES EXTRAITS D EAU RÉGALE Description du dosage du mercure par spectrométrie d absorption atomique de vapeur froide ou par spectrométrie de fluorescence atomique
CODEX ŒNOLOGIQUE INTERNATIONAL. SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012)
 SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012) 1. OBJET, ORIGINE ET DOMAINE D APPLICATION Le sucre de raisin est obtenu exclusivement à partir du
SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012) 1. OBJET, ORIGINE ET DOMAINE D APPLICATION Le sucre de raisin est obtenu exclusivement à partir du
Décrire l'ensemble des mesures de maîtrise et des mesures de surveillance dans des procédures ou modes opératoires portés à la connaissance de tous.
 DEMARCHE HACCP EN CUISINE CENTRALE Alimentation GROSJEAN L, Vénissieux Juin 2010 Objectif La démarche HACCP (de l'américain Hazard Analysis Critical Control Point) est une méthode préventive visant à maîtriser
DEMARCHE HACCP EN CUISINE CENTRALE Alimentation GROSJEAN L, Vénissieux Juin 2010 Objectif La démarche HACCP (de l'américain Hazard Analysis Critical Control Point) est une méthode préventive visant à maîtriser
PROPOSITION TECHNIQUE ET FINANCIERE
 Avenue des Etangs Narbonne, F-11100, France Votre correspondant : Romain CRESSON INRA Transfert Environnement Avenue des Etangs Narbonne, F-11100, France Tel: +33 (0)4 68 46 64 32 Fax: +33 (0)4 68 42 51
Avenue des Etangs Narbonne, F-11100, France Votre correspondant : Romain CRESSON INRA Transfert Environnement Avenue des Etangs Narbonne, F-11100, France Tel: +33 (0)4 68 46 64 32 Fax: +33 (0)4 68 42 51
évaluation des risques professionnels
 évaluation des professionnels Inventaire des Etablissement : Faculté de Médecine Unité de travail : Laboratoire de Biochimie Médicale Année : 2013 Locaux Bureaux Salle de Microscopie Culture cellulaire
évaluation des professionnels Inventaire des Etablissement : Faculté de Médecine Unité de travail : Laboratoire de Biochimie Médicale Année : 2013 Locaux Bureaux Salle de Microscopie Culture cellulaire
PREPARATION (NETTOYAGE, DESINFECTION ET STERILISATION) D AIGUILLES MEDICALES, DE RACCORDS, DE ROBINETS ET D AIGUILLES CHIRURGICALES A SUTURE UNIMED
 U N I M E D S.A. CM/07.12.04 NETSTERIL.SPN Approuvé par/le: Claude Borgeaud / 08.10.13 PREPARATION (NETTOYAGE, DESINFECTION ET STERILISATION) D AIGUILLES MEDICALES, DE RACCORDS, DE ROBINETS ET D AIGUILLES
U N I M E D S.A. CM/07.12.04 NETSTERIL.SPN Approuvé par/le: Claude Borgeaud / 08.10.13 PREPARATION (NETTOYAGE, DESINFECTION ET STERILISATION) D AIGUILLES MEDICALES, DE RACCORDS, DE ROBINETS ET D AIGUILLES
AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE
 AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE CONCOURS EXTERNE Session 2005 TRAVAUX PRATIQUES DE BIOCHIMIE PHYSIOLOGIE ALCOOL ET FOIE L éthanol, psychotrope puissant, est absorbé passivement dans l intestin
AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE CONCOURS EXTERNE Session 2005 TRAVAUX PRATIQUES DE BIOCHIMIE PHYSIOLOGIE ALCOOL ET FOIE L éthanol, psychotrope puissant, est absorbé passivement dans l intestin
Traitement de l eau par flux dynamique
 GmbH Traitement de l eau par flux dynamique afin de réduire les impuretés microbiologiques afin d empêcher l apparition de nouveaux germes dans les eaux de consommation et de process et Nouveau avec certificat
GmbH Traitement de l eau par flux dynamique afin de réduire les impuretés microbiologiques afin d empêcher l apparition de nouveaux germes dans les eaux de consommation et de process et Nouveau avec certificat
CATALOGUE D'ESSAIS INTERLABORATOIRES AGLAE 2015 BIOLOGIE MEDICALE
 Ensemble pour s'améliorer CATALOGUE D'ESSAIS INTERLABORATOIRES AGLAE 2015 BIOLOGIE MEDICALE Association AGLAE Parc des Pyramides 427 rue des Bourreliers 59320 Hallennes lez Haubourdin +33 (0)3 20 16 91
Ensemble pour s'améliorer CATALOGUE D'ESSAIS INTERLABORATOIRES AGLAE 2015 BIOLOGIE MEDICALE Association AGLAE Parc des Pyramides 427 rue des Bourreliers 59320 Hallennes lez Haubourdin +33 (0)3 20 16 91
Solutions pour le calibrage et l entretien Gamme complète d accessoires indispensables
 Solutions laboratoires Solutions pour les laboratoires Tampons ph Étalons de conductivité Solutions de mesure redox et O 2 dissous Solutions de mesure ISE Solutions de maintenance Solutions pour le calibrage
Solutions laboratoires Solutions pour les laboratoires Tampons ph Étalons de conductivité Solutions de mesure redox et O 2 dissous Solutions de mesure ISE Solutions de maintenance Solutions pour le calibrage
3: Clonage d un gène dans un plasmide
 3: Clonage d un gène dans un plasmide Le clonage moléculaire est une des bases du génie génétique. Il consiste à insérer un fragment d'adn (dénommé insert) dans un vecteur approprié comme un plasmide par
3: Clonage d un gène dans un plasmide Le clonage moléculaire est une des bases du génie génétique. Il consiste à insérer un fragment d'adn (dénommé insert) dans un vecteur approprié comme un plasmide par
Détermination de la sensibilité aux antibiotiques. Méthode EUCAST de diffusion en gélose
 Détermination de la sensibilité aux antibiotiques Méthode EUCAST de diffusion en gélose Version Sommaire Page Modifications des documents Abréviations et terminologie 1 Introduction 4 2 Préparation des
Détermination de la sensibilité aux antibiotiques Méthode EUCAST de diffusion en gélose Version Sommaire Page Modifications des documents Abréviations et terminologie 1 Introduction 4 2 Préparation des
AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS
 AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS CONCOURS EXTERNE ÉPREUVES D ADMISSION session 2010 TRAVAUX PRATIQUES DE CONTRE-OPTION DU SECTEUR A CANDIDATS DES SECTEURS B ET C
AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS CONCOURS EXTERNE ÉPREUVES D ADMISSION session 2010 TRAVAUX PRATIQUES DE CONTRE-OPTION DU SECTEUR A CANDIDATS DES SECTEURS B ET C
PROCÉDURE. Code : PR-DSI-000-31
 Code : PR-DSI-000-31 PROCÉDURE Instance responsable : Direction des soins infirmiers Approuvée par : Diane Benoit Présentée et adoptée au comité de direction le : 16 janvier 2013 Entrée en vigueur le :
Code : PR-DSI-000-31 PROCÉDURE Instance responsable : Direction des soins infirmiers Approuvée par : Diane Benoit Présentée et adoptée au comité de direction le : 16 janvier 2013 Entrée en vigueur le :
Hygiène alimentaire en restauration collective
 Catalogue de formations 2012 Audit, conseil et formation Hygiène alimentaire en restauration collective Laboratoire Départemental de la Côte-d'Or 1 2 3 4 5 6 7 8 Sommaire Sensibilisation à l hygiène alimentaire
Catalogue de formations 2012 Audit, conseil et formation Hygiène alimentaire en restauration collective Laboratoire Départemental de la Côte-d'Or 1 2 3 4 5 6 7 8 Sommaire Sensibilisation à l hygiène alimentaire
Contexte réglementaire en hygiène alimentaire
 Contexte réglementaire en hygiène alimentaire 1 Réforme de la législation communautaire pour la restauration collective Approche traditionnelle = obligation de moyens Réglementation Arrêté Ministériel
Contexte réglementaire en hygiène alimentaire 1 Réforme de la législation communautaire pour la restauration collective Approche traditionnelle = obligation de moyens Réglementation Arrêté Ministériel
Demande chimique en oxygène
 Table des matières Introduction Réactifs DCO Azote et phosphore HI 83214 HI 83099 HI 839800 HI 3898 Page J3 J5 J6 J7 J8 J10 J11 J1 Tableau comparatif Paramètre Photomètre Photomètre Thermo-réacteur Trousse
Table des matières Introduction Réactifs DCO Azote et phosphore HI 83214 HI 83099 HI 839800 HI 3898 Page J3 J5 J6 J7 J8 J10 J11 J1 Tableau comparatif Paramètre Photomètre Photomètre Thermo-réacteur Trousse
Annexe A : Tableau des exigences
 E1 E1.1 E1.2 E1.3 E1.4 E1.5 E1.6 Exigences générales production Les végétaux destinés à la consommation humaine doivent être cultivés au Québec. Les végétaux destinés à la consommation humaine doivent
E1 E1.1 E1.2 E1.3 E1.4 E1.5 E1.6 Exigences générales production Les végétaux destinés à la consommation humaine doivent être cultivés au Québec. Les végétaux destinés à la consommation humaine doivent
Rapport de stage. «Travail préparatoire à l estimation du coût d une bonne qualité des eaux de baignade sur le littoral Aquitain»
 GRAPE-CEEP Rapport de stage «Travail préparatoire à l estimation du coût d une bonne qualité des eaux de baignade sur le littoral Aquitain» Vallette Jean-Vincent Master II Gestion des Ressources Naturelles
GRAPE-CEEP Rapport de stage «Travail préparatoire à l estimation du coût d une bonne qualité des eaux de baignade sur le littoral Aquitain» Vallette Jean-Vincent Master II Gestion des Ressources Naturelles
Détermination des métaux : méthode par spectrométrie de masse à source ionisante au plasma d argon
 Centre d'expertise en analyse environnementale du Québec MA. 200 Mét. 1.2 Détermination des métaux : méthode par spectrométrie de masse à source ionisante au plasma d argon 2014-05-09 (révision 5) Comment
Centre d'expertise en analyse environnementale du Québec MA. 200 Mét. 1.2 Détermination des métaux : méthode par spectrométrie de masse à source ionisante au plasma d argon 2014-05-09 (révision 5) Comment
SECURITE SANITAIRE DES ALIMENTS
 PREFET DES PYRENEES-ATLANTIQUES Direction Départementale de la Protection des Populations des Pyrénées-Altantiques SECURITE SANITAIRE DES ALIMENTS Quelques règles à respecter, secteur de la remise directe
PREFET DES PYRENEES-ATLANTIQUES Direction Départementale de la Protection des Populations des Pyrénées-Altantiques SECURITE SANITAIRE DES ALIMENTS Quelques règles à respecter, secteur de la remise directe
33-Dosage des composés phénoliques
 33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
Matériel de laboratoire
 Matériel de laboratoire MATERIAUX UTILISE... 1 L'APPAREILLAGE DE LABORATOIRE... 1 a) Les récipients à réaction... 2 b) La verrerie Graduée... 2 MATERIEL DE FILTRATION... 6 FILTRATION SOUS VIDE AVEC UN
Matériel de laboratoire MATERIAUX UTILISE... 1 L'APPAREILLAGE DE LABORATOIRE... 1 a) Les récipients à réaction... 2 b) La verrerie Graduée... 2 MATERIEL DE FILTRATION... 6 FILTRATION SOUS VIDE AVEC UN
Test d immunofluorescence (IF)
 Test d immunofluorescence (IF) 1.1 Prélèvement du cerveau et échantillonnage Avant toute manipulation, il est fondamental de s assurer que tout le personnel en contact avec un échantillon suspect soit
Test d immunofluorescence (IF) 1.1 Prélèvement du cerveau et échantillonnage Avant toute manipulation, il est fondamental de s assurer que tout le personnel en contact avec un échantillon suspect soit
Service de Biothérapies
 AP-HP Service de Biothérapies Pr. D. Klatzmann Service de Biothérapies Activités de l unité de thérapie cellulaire Dr. Hélène Trébéden-Negre Plan Définition de la thérapie cellulaire Les autogreffes de
AP-HP Service de Biothérapies Pr. D. Klatzmann Service de Biothérapies Activités de l unité de thérapie cellulaire Dr. Hélène Trébéden-Negre Plan Définition de la thérapie cellulaire Les autogreffes de
Ministère des affaires sociales, de la santé et des droits des femmes
 Ministère des affaires sociales, de la santé et des droits des femmes Direction générale de la santé Sous-direction «Prévention des risques liés à l environnement et à l alimentation» Bureau «Qualité des
Ministère des affaires sociales, de la santé et des droits des femmes Direction générale de la santé Sous-direction «Prévention des risques liés à l environnement et à l alimentation» Bureau «Qualité des
Rapport de synthèse (études préliminaire, d extension et interlaboratoire conduites selon la norme EN ISO 16140)
 Laboratoire de Touraine biomérieux Rapport de synthèse (études préliminaire, d extension et interlaboratoire conduites selon la norme EN ISO 16140) Validation de la méthode «ONE DAY» pour la recherche
Laboratoire de Touraine biomérieux Rapport de synthèse (études préliminaire, d extension et interlaboratoire conduites selon la norme EN ISO 16140) Validation de la méthode «ONE DAY» pour la recherche
POLITIQUE ET LIGNES DIRECTRICES EN MATIERE DE TRACABILITE DES RESULTATS DE MESURE
 BELAC 2-003 Rev 1-2014 POLITIQUE ET LIGNES DIRECTRICES EN MATIERE DE TRACABILITE DES RESULTATS DE MESURE Les versions des documents du système de management de BELAC telles que disponibles sur le site
BELAC 2-003 Rev 1-2014 POLITIQUE ET LIGNES DIRECTRICES EN MATIERE DE TRACABILITE DES RESULTATS DE MESURE Les versions des documents du système de management de BELAC telles que disponibles sur le site
GESTION DE STOCK. July 2009. Hilde De Boeck
 GESTION DE STOCK July 2009 Hilde De Boeck Table des matières Introduction Organisation du stock centrale 1. Gestionnaire de stock 2. Stockage: - Les Conditions - Rangement des produits 3. Les outils de
GESTION DE STOCK July 2009 Hilde De Boeck Table des matières Introduction Organisation du stock centrale 1. Gestionnaire de stock 2. Stockage: - Les Conditions - Rangement des produits 3. Les outils de
Hygiène alimentaire en restauration collective
 1 2 3 4 5 6 7 Catalogue 2011 Audit, conseil et formation Hygiène alimentaire en restauration collective Laboratoire Départemental de la Côte-d'Or Sommaire 1 2 3 4 5 6 7 Sensibilisation à l hygiène alimentaire
1 2 3 4 5 6 7 Catalogue 2011 Audit, conseil et formation Hygiène alimentaire en restauration collective Laboratoire Départemental de la Côte-d'Or Sommaire 1 2 3 4 5 6 7 Sensibilisation à l hygiène alimentaire
Chapitre 7 Les solutions colorées
 Chapitre 7 Les solutions colorées Manuel pages 114 à 127 Choix pédagogiques. Ce chapitre a pour objectif d illustrer les points suivants du programme : - dosage de solutions colorées par étalonnage ; -
Chapitre 7 Les solutions colorées Manuel pages 114 à 127 Choix pédagogiques. Ce chapitre a pour objectif d illustrer les points suivants du programme : - dosage de solutions colorées par étalonnage ; -
RAPPORT AUDIT HYGIENE AVXX-0XX-XXX
 Date: SITE: Heure: par: MENTION GLOBAL DE L'AUDIT: NOMBRE D'ECARTS CONSTATES: ECARTS CONSTATES: 1. RESPONSABILITÉ DE LA DIRECTION / DÉFINITION & CONTRÔLE DES RÈGLES D HYGIÈNE 1.1 Déclaration de l'établissement
Date: SITE: Heure: par: MENTION GLOBAL DE L'AUDIT: NOMBRE D'ECARTS CONSTATES: ECARTS CONSTATES: 1. RESPONSABILITÉ DE LA DIRECTION / DÉFINITION & CONTRÔLE DES RÈGLES D HYGIÈNE 1.1 Déclaration de l'établissement
(aq) sont colorées et donnent à la solution cette teinte violette, assimilable au magenta.»
 Chapitre 5 / TP 1 : Contrôle qualité de l'eau de Dakin par dosage par étalonnage à l'aide d'un spectrophotomètre Objectif : Vous devez vérifier la concentration massique d'un désinfectant, l'eau de Dakin.
Chapitre 5 / TP 1 : Contrôle qualité de l'eau de Dakin par dosage par étalonnage à l'aide d'un spectrophotomètre Objectif : Vous devez vérifier la concentration massique d'un désinfectant, l'eau de Dakin.
Laboratoire Eau de Paris. Analyses et Recherche
 Laboratoire Eau de Paris Analyses et Recherche L eau, un aliment sous contrôle public Pour Eau de Paris, approvisionner la capitale en eau, c est garantir à ses 3 millions d usagers une ressource de qualité,
Laboratoire Eau de Paris Analyses et Recherche L eau, un aliment sous contrôle public Pour Eau de Paris, approvisionner la capitale en eau, c est garantir à ses 3 millions d usagers une ressource de qualité,
Dénomination de l installation : Adresse du système de refroidissement :
 1 Carnet de suivi du système de refroidissement Dénomination de l installation : Adresse du système de refroidissement : 2 Mode d emploi du carnet de suivi Le carnet de suivi du système de refroidissement
1 Carnet de suivi du système de refroidissement Dénomination de l installation : Adresse du système de refroidissement : 2 Mode d emploi du carnet de suivi Le carnet de suivi du système de refroidissement
Liste de contrôle d auto-évaluation pour le niveau de confinement 1 pour les phytoravageurs
 Bureau du confinement des biorisques et de la sécurité Office of Biohazard, Containment and Safety Direction générale des sciences Science Branch 59, promenade Camelot 59 Camelot Drive Ottawa ON K1A 0Y9
Bureau du confinement des biorisques et de la sécurité Office of Biohazard, Containment and Safety Direction générale des sciences Science Branch 59, promenade Camelot 59 Camelot Drive Ottawa ON K1A 0Y9
Critères pour les méthodes de quantification des résidus potentiellement allergéniques de protéines de collage dans le vin (OIV-Oeno 427-2010)
 Méthode OIV- -MA-AS315-23 Type de méthode : critères Critères pour les méthodes de quantification des résidus potentiellement allergéniques de protéines de collage (OIV-Oeno 427-2010) 1 Définitions des
Méthode OIV- -MA-AS315-23 Type de méthode : critères Critères pour les méthodes de quantification des résidus potentiellement allergéniques de protéines de collage (OIV-Oeno 427-2010) 1 Définitions des
HYGIENE EN RESTAURATION COLLECTIVE
 HYGIENE EN RESTAURATION COLLECTIVE Dr Erick KEROURIO DIRECTION DEPARTEMENTALE DE LA PROTECTION DES POPULATIONS DE L ESSONNE Le cadre réglementaire LA RESTAURATION COLLECTIVE Notion de «clientèle» captive
HYGIENE EN RESTAURATION COLLECTIVE Dr Erick KEROURIO DIRECTION DEPARTEMENTALE DE LA PROTECTION DES POPULATIONS DE L ESSONNE Le cadre réglementaire LA RESTAURATION COLLECTIVE Notion de «clientèle» captive
Masse volumique et densité relative à 20 C
 Méthode OIV-MA-AS2-01A Méthodes Type I Masse volumique et densité relative à 20 C 1. Définition La masse volumique est le quotient de la masse d'un certain volume de vin ou de moût à 20 C par ce volume.
Méthode OIV-MA-AS2-01A Méthodes Type I Masse volumique et densité relative à 20 C 1. Définition La masse volumique est le quotient de la masse d'un certain volume de vin ou de moût à 20 C par ce volume.
MEDIACLAVE. La stérilisation rapide, reproductible et sûre des milieux
 MEDIACLAVE La stérilisation rapide, reproductible et sûre des milieux MEDIACLAVE La stérilisation rapide, reproductible et sûre des milieux Les milieux de culture bactérienne sont très largement utilisé,
MEDIACLAVE La stérilisation rapide, reproductible et sûre des milieux MEDIACLAVE La stérilisation rapide, reproductible et sûre des milieux Les milieux de culture bactérienne sont très largement utilisé,
SECURITE SANITAIRE ET RESTAURATION COLLECTIVE A CARACTERE SOCIAL
 SECURITE SANITAIRE ET RESTAURATION COLLECTIVE A CARACTERE SOCIAL Références réglementaires : Règlement N 178/2002 établissant les principes généraux et les prescriptions générales de la législation alimentaire
SECURITE SANITAIRE ET RESTAURATION COLLECTIVE A CARACTERE SOCIAL Références réglementaires : Règlement N 178/2002 établissant les principes généraux et les prescriptions générales de la législation alimentaire
GUIDE DE LAVAGE, DÉSINFECTION ET SÉCHAGE DES PORCHERIES
 GUIDE DE LAVAGE, DÉSINFECTION ET SÉCHAGE DES PORCHERIES Document de référence Publication Fédération des producteurs de porcs du Québec 555, boulevard Roland-Therrien, bureau 120 Longueuil (Québec) J4H
GUIDE DE LAVAGE, DÉSINFECTION ET SÉCHAGE DES PORCHERIES Document de référence Publication Fédération des producteurs de porcs du Québec 555, boulevard Roland-Therrien, bureau 120 Longueuil (Québec) J4H
de l Université Laval Orientations et exigences générales et techniques de construction
 de l Université Laval Orientations et exigences générales et techniques de construction Guide de conception de projets GC-3.2.4 Fabrication et distribution de l'air comprimé et de l'eau réfrigérée (11/2007)
de l Université Laval Orientations et exigences générales et techniques de construction Guide de conception de projets GC-3.2.4 Fabrication et distribution de l'air comprimé et de l'eau réfrigérée (11/2007)
HI 991x. Contrôleurs Industriel mural de ph et EC. HI 9910 Contrôleur de ph mural avec point de consigne simple et dosage proportionnel
 HI 991x Contrôleurs Industriel mural de ph et EC HI 9910 Contrôleur de ph mural avec point de consigne simple et dosage proportionnel HI 9910 est un contrôleur de ph avec point de consigne unique pour
HI 991x Contrôleurs Industriel mural de ph et EC HI 9910 Contrôleur de ph mural avec point de consigne simple et dosage proportionnel HI 9910 est un contrôleur de ph avec point de consigne unique pour
I. Définitions et exigences
 I. Définitions et exigences Classes d indicateurs chimiques [1] Stérilisation : synthèse des normes ayant trait Exigences générales : Chaque indicateur doit porter un marquage clair mentionnant le type
I. Définitions et exigences Classes d indicateurs chimiques [1] Stérilisation : synthèse des normes ayant trait Exigences générales : Chaque indicateur doit porter un marquage clair mentionnant le type
L eau à l intérieur des bâtiments: aspects règlementaires
 L eau à l intérieur des bâtiments: aspects règlementaires 01 La règlementation concernant la qualité des eaux destinées à la consommation humaine s applique sans restriction aux installations d eau à l
L eau à l intérieur des bâtiments: aspects règlementaires 01 La règlementation concernant la qualité des eaux destinées à la consommation humaine s applique sans restriction aux installations d eau à l
Indicateur d'unité Voyant Marche/Arrêt
 Notice MESURACOLOR Colorimètre à DEL Réf. 22020 Indicateur d'unité Voyant Marche/Arrêt Indicateur Etalonnage Bouton Marche/Arrêt Indicateur de sélection de la longueur d'onde Indicateur de mode chronomètre
Notice MESURACOLOR Colorimètre à DEL Réf. 22020 Indicateur d'unité Voyant Marche/Arrêt Indicateur Etalonnage Bouton Marche/Arrêt Indicateur de sélection de la longueur d'onde Indicateur de mode chronomètre
Metrohm. ph-mètre 780 ph-/ionomètre 781. Un nouveau concept qui fait référence. Analyse des ions
 Metrohm Analyse des ions ph-mètre 780 ph-/ionomètre 781 Un nouveau concept qui fait référence Des fonctions multiples faciles à utiliser Le ph-mètre 780 et le ph-/ionomètre 781 associent la qualité Metrohm
Metrohm Analyse des ions ph-mètre 780 ph-/ionomètre 781 Un nouveau concept qui fait référence Des fonctions multiples faciles à utiliser Le ph-mètre 780 et le ph-/ionomètre 781 associent la qualité Metrohm
Paquet hygiène : Le règlement 852/2004 relatif à l hygiène des denrées alimentaires
 Paquet hygiène : Le règlement 852/2004 relatif à l hygiène des denrées alimentaires Applicable au 1 er janvier 2006 Objectif : Etablit les règles générales en matière d hygiène, est directement applicable
Paquet hygiène : Le règlement 852/2004 relatif à l hygiène des denrées alimentaires Applicable au 1 er janvier 2006 Objectif : Etablit les règles générales en matière d hygiène, est directement applicable
CATALOGUE DE FORMATION. Qualité Hygiène et Sécurité Alimentaire. Au service des professionnels des métiers de bouche sur tout le territoire national
 Qualité Hygiène et Sécurité Alimentaire 2015 Au service des professionnels des métiers de bouche sur tout le territoire national CATALOGUE DE FORMATION Enregistré sous le numéro 53350863735 auprès du Préfet
Qualité Hygiène et Sécurité Alimentaire 2015 Au service des professionnels des métiers de bouche sur tout le territoire national CATALOGUE DE FORMATION Enregistré sous le numéro 53350863735 auprès du Préfet
TRAVAUX PRATIQUESDE BIOCHIMIE L1
 TRAVAUX PRATIQUESDE BICHIMIE L1 PRINTEMPS 2011 Les acides aminés : chromatographie sur couche mince courbe de titrage Etude d une enzyme : la phosphatase alcaline QUELQUES RECMMANDATINS IMPRTANTES Le port
TRAVAUX PRATIQUESDE BICHIMIE L1 PRINTEMPS 2011 Les acides aminés : chromatographie sur couche mince courbe de titrage Etude d une enzyme : la phosphatase alcaline QUELQUES RECMMANDATINS IMPRTANTES Le port
A B C Eau Eau savonneuse Eau + détergent
 1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
Le premier dispositif 4 en 1.
 TETHYS H10 Le premier dispositif 4 en 1. Décontamination, nettoyage, désinfection et séchage en un seul passage pour un flux de travail plus simple, plus rapide et plus efficace. Tethys H10 est le premier
TETHYS H10 Le premier dispositif 4 en 1. Décontamination, nettoyage, désinfection et séchage en un seul passage pour un flux de travail plus simple, plus rapide et plus efficace. Tethys H10 est le premier
 Règlement sur les conditions de production et de conservation à la ferme et sur la qualité... Page 1 sur 11 Éditeur officiel du Québec À jour au 1er novembre 2014 Ce document a valeur officielle. chapitre
Règlement sur les conditions de production et de conservation à la ferme et sur la qualité... Page 1 sur 11 Éditeur officiel du Québec À jour au 1er novembre 2014 Ce document a valeur officielle. chapitre
Choisir et utiliser un détecteur de gaz pour le travail en espace clos.
 entreposage Choisir et utiliser un détecteur de gaz pour le travail en espace clos. Un détecteur de gaz contribue à déterminer les mesures de prévention et l équipement de protection nécessaires dans le
entreposage Choisir et utiliser un détecteur de gaz pour le travail en espace clos. Un détecteur de gaz contribue à déterminer les mesures de prévention et l équipement de protection nécessaires dans le
FICHES INFORMATIVES HYGIENE DU PERSONNEL
 LE GOUVERNEMENT DU GRAND-DUCHÉ DE LUXEMBOURG Direction de la Santé FICHES INFORMATIVES HYGIENE DU PERSONNEL Un plan d hygiène permet de garantir la propreté du personnel et éviter toutes contaminations
LE GOUVERNEMENT DU GRAND-DUCHÉ DE LUXEMBOURG Direction de la Santé FICHES INFORMATIVES HYGIENE DU PERSONNEL Un plan d hygiène permet de garantir la propreté du personnel et éviter toutes contaminations
EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points)
 Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
Une solution parfaitement adaptée
 INFORMATIONS ANALYSE EN CONTINU DES NITRATES NISE SC / NITRATAX SC NOUVEAU! ME SU RE DES N I T R AT ES EN LIGNE Une solution parfaitement adaptée Sondes de nitrate utilisant les technologies UV et électrodes
INFORMATIONS ANALYSE EN CONTINU DES NITRATES NISE SC / NITRATAX SC NOUVEAU! ME SU RE DES N I T R AT ES EN LIGNE Une solution parfaitement adaptée Sondes de nitrate utilisant les technologies UV et électrodes
Dosage des sucres par CLHP dans les vins (Oeno 23/2003)
 Méthode OIV-MA-AS311-03 Méthode Type II Dosage des sucres par CLHP dans les vins (Oeno 23/2003) 1. DOMAINE D'APPLICATION Cette recommandation spécifie une méthode de dosage du fructose, du glucose et du
Méthode OIV-MA-AS311-03 Méthode Type II Dosage des sucres par CLHP dans les vins (Oeno 23/2003) 1. DOMAINE D'APPLICATION Cette recommandation spécifie une méthode de dosage du fructose, du glucose et du
Hygiène alimentaire. Introduction
 Direction des études Mission Santé-sécurité au travail dans les fonctions publiques (MSSTFP) Hygiène alimentaire Introduction Le temps de travail ne permet pas souvent aux salariés de déjeuner chez eux
Direction des études Mission Santé-sécurité au travail dans les fonctions publiques (MSSTFP) Hygiène alimentaire Introduction Le temps de travail ne permet pas souvent aux salariés de déjeuner chez eux
inspection, nettoyage et désinfection
 Réservoirs et canalisations d eau destinée à la consommation humaine : inspection, nettoyage et désinfection GUIDE TECHNIQUE Ce guide a été réalisé à l initiative du ministère chargé de la santé MINISTÈRE
Réservoirs et canalisations d eau destinée à la consommation humaine : inspection, nettoyage et désinfection GUIDE TECHNIQUE Ce guide a été réalisé à l initiative du ministère chargé de la santé MINISTÈRE
DÉTERMINATION DU POURCENTAGE EN ACIDE D UN VINAIGRE. Sommaire
 BACCALAURÉAT SÉRIE S Épreuve de PHYSIQUE CHIMIE Évaluation des compétences expérimentales Sommaire I. DESCRIPTIF DU SUJET DESTINÉ AUX PROFESSEURS... 2 II. LISTE DE MATÉRIEL DESTINÉE AUX PROFESSEURS ET
BACCALAURÉAT SÉRIE S Épreuve de PHYSIQUE CHIMIE Évaluation des compétences expérimentales Sommaire I. DESCRIPTIF DU SUJET DESTINÉ AUX PROFESSEURS... 2 II. LISTE DE MATÉRIEL DESTINÉE AUX PROFESSEURS ET
HACCP et sécurité sanitaire des aliments
 HACCP et sécurité sanitaire des aliments 1. A votre avis, comment cet accident aurait-il pu être évité? En identifiant les risques alimentaires potentiels liés à l activité de conserverie artisanale et
HACCP et sécurité sanitaire des aliments 1. A votre avis, comment cet accident aurait-il pu être évité? En identifiant les risques alimentaires potentiels liés à l activité de conserverie artisanale et
Cafetière. Mode d Emploi. 1Notice cafetière v1.0
 Cafetière Mode d Emploi 1Notice cafetière v1.0 SOMMAIRE 1 CONSIGNES DE SÉCURITÉ... 3 2INSTALLATION DE L APPAREIL EN TOUTE SÉCURITÉ...4 3PRECAUTION CONCERNANT L UTILISATION DE L APPAREIL...5 4DESCRIPTION
Cafetière Mode d Emploi 1Notice cafetière v1.0 SOMMAIRE 1 CONSIGNES DE SÉCURITÉ... 3 2INSTALLATION DE L APPAREIL EN TOUTE SÉCURITÉ...4 3PRECAUTION CONCERNANT L UTILISATION DE L APPAREIL...5 4DESCRIPTION
Une production économique! Echangeur d ions TKA
 Une eau totalement déminéralisée Une production économique! Echangeur d ions TKA Eau déminéralisée pour autoclaves, laveurs, analyseurs automatiques, appareils d'eau ultra pure... SYSTÈMES DE PURIFICATION
Une eau totalement déminéralisée Une production économique! Echangeur d ions TKA Eau déminéralisée pour autoclaves, laveurs, analyseurs automatiques, appareils d'eau ultra pure... SYSTÈMES DE PURIFICATION
Registre des dossiers et des mesures correctives du programme LCQ
 Programme Lait canadien de qualité des Producteurs laitiers du Canada Registre des dossiers et des mesures correctives du programme LCQ Utiliser avec le Registre et le Calendrier de DGI pour des dossiers
Programme Lait canadien de qualité des Producteurs laitiers du Canada Registre des dossiers et des mesures correctives du programme LCQ Utiliser avec le Registre et le Calendrier de DGI pour des dossiers
TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY)
 TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY) Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste Direction de l innovation scientifique et technologique Au Laboratoire
TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY) Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste Direction de l innovation scientifique et technologique Au Laboratoire
Ouverture d un pavillon médical : Mesures mises en œuvre pour la mise en eau et suivi bactériologique
 Ouverture d un pavillon médical : Mesures mises en œuvre pour la mise en eau et suivi bactériologique Congrès de la SF2H - 9 Juin 2011 S. Coudrais Biohygiéniste Unité d Hygiène et Epidémiologie - Groupement
Ouverture d un pavillon médical : Mesures mises en œuvre pour la mise en eau et suivi bactériologique Congrès de la SF2H - 9 Juin 2011 S. Coudrais Biohygiéniste Unité d Hygiène et Epidémiologie - Groupement
Analyse des risques points critiques pour leur maîtrise (HACCP)
 59 Chapitre 11 Analyse des risques points critiques pour leur maîtrise (HACCP) 11.1 PRINCIPES DE BASE DE L HACCP... 59 11.2 APPLICATION DES PRINCIPES HACCP À LA PURIFICATION DES MOLLUSQUES BIVALVES...
59 Chapitre 11 Analyse des risques points critiques pour leur maîtrise (HACCP) 11.1 PRINCIPES DE BASE DE L HACCP... 59 11.2 APPLICATION DES PRINCIPES HACCP À LA PURIFICATION DES MOLLUSQUES BIVALVES...
VERITAS TUNISIE CATALOGUE ANALYSES LABORATOIRE
 VERITAS TUNISIE CATALOGUE ANALYSES LABORATOIRE Agro-alimentaire et Environnement SOMMAIRE Page Introduction 1 Analyses microbiologiques 5 Microbiologie des aliments 6 Microbiologie des eaux 7 Microbiologie
VERITAS TUNISIE CATALOGUE ANALYSES LABORATOIRE Agro-alimentaire et Environnement SOMMAIRE Page Introduction 1 Analyses microbiologiques 5 Microbiologie des aliments 6 Microbiologie des eaux 7 Microbiologie
Moisture Analyzers. Dessicateur. http://www.aandd.jp
 Moisture Analyzers MS-70/MX-50 MF-50/ML-50 Dessicateur http://www.aandd.jp Sélectionnez le d application Tes SRA Dessicateurs A&D MS-70/MX-5 MS -70/MX-5 SHS Un chauffage rapide et uniforme grâce à une
Moisture Analyzers MS-70/MX-50 MF-50/ML-50 Dessicateur http://www.aandd.jp Sélectionnez le d application Tes SRA Dessicateurs A&D MS-70/MX-5 MS -70/MX-5 SHS Un chauffage rapide et uniforme grâce à une
LES INCONTOURNABLES DE L HYGIENE ALIMENTAIRE EN RESTAURANT SATELLITE
 LES INCONTOURNABLES DE L HYGIENE ALIMENTAIRE EN RESTAURANT SATELLITE Direction Départementale de la Protection des Populations De Seine-Saint-Denis (DDPP 93) - Immeuble l Européen - 5 et 7 promenade Jean
LES INCONTOURNABLES DE L HYGIENE ALIMENTAIRE EN RESTAURANT SATELLITE Direction Départementale de la Protection des Populations De Seine-Saint-Denis (DDPP 93) - Immeuble l Européen - 5 et 7 promenade Jean
1.3 Recherche de contaminants au cours de la production de Saccharomyces boulardii
 Série STL Biochimie génie biologique EPREUVE PRATIQUE 1. CONTROLE MICROBIOLOGIQUE DE PROBIOTIQUES Les préparations de probiotiques sont utilisées préventivement comme additifs dans l alimentation humaine
Série STL Biochimie génie biologique EPREUVE PRATIQUE 1. CONTROLE MICROBIOLOGIQUE DE PROBIOTIQUES Les préparations de probiotiques sont utilisées préventivement comme additifs dans l alimentation humaine
Hygiène alimentaire en restauration
 2 0 1 5 Catalogue de formations Audit, conseil et formation Hygiène alimentaire en restauration Laboratoire Départemental de la Côte-d'Or (LDCO) Sommaire 1A 1B 23 4 5 6 7A 7B 8 Sensibilisation à l hygiène
2 0 1 5 Catalogue de formations Audit, conseil et formation Hygiène alimentaire en restauration Laboratoire Départemental de la Côte-d'Or (LDCO) Sommaire 1A 1B 23 4 5 6 7A 7B 8 Sensibilisation à l hygiène
Acides et bases. Acides et bases Page 1 sur 6
 Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
FICHE 1 Fiche à destination des enseignants
 FICHE 1 Fiche à destination des enseignants 1S 8 (b) Un entretien d embauche autour de l eau de Dakin Type d'activité Activité expérimentale avec démarche d investigation Dans cette version, l élève est
FICHE 1 Fiche à destination des enseignants 1S 8 (b) Un entretien d embauche autour de l eau de Dakin Type d'activité Activité expérimentale avec démarche d investigation Dans cette version, l élève est
Avant propos. Nicole KLEIN Directrice Générale Agence Régionale de Santé d Aquitaine. ARS Aquitaine - mai 2010 3
 Avant propos Exploiter une piscine pour offrir aux usagers les meilleures conditions d'hygiène et de confort, tel doit être le souci de chaque responsable. En application du code de la santé publique,
Avant propos Exploiter une piscine pour offrir aux usagers les meilleures conditions d'hygiène et de confort, tel doit être le souci de chaque responsable. En application du code de la santé publique,
Calcaire ou eau agressive en AEP : comment y remédier?
 Calcaire ou eau agressive en AEP : comment y remédier? Les solutions techniques Principes et critères de choix Par Sébastien LIBOZ - Hydrogéologue Calcaire ou eau agressive en AEP : comment y remédier?
Calcaire ou eau agressive en AEP : comment y remédier? Les solutions techniques Principes et critères de choix Par Sébastien LIBOZ - Hydrogéologue Calcaire ou eau agressive en AEP : comment y remédier?
PARTIE 4 PROCESSUS DE SURVEILLANCE DES PRODUITS CERTIFIES MODIFICATIONS ET EVOLUTION
 REGLES DE CERTIFICATION MARQUE NFPOSTES DE SECURITE MICROBIOLOGIQUE PARTIE 4 PROCESSUS DE SURVEILLANCE DES PRODUITS CERTIFIES MODIFICATIONS ET EVOLUTION SOMMAIRE 4.1. Processus de surveillance des produits
REGLES DE CERTIFICATION MARQUE NFPOSTES DE SECURITE MICROBIOLOGIQUE PARTIE 4 PROCESSUS DE SURVEILLANCE DES PRODUITS CERTIFIES MODIFICATIONS ET EVOLUTION SOMMAIRE 4.1. Processus de surveillance des produits
Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu.
 Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu. Auteur : Dr. Wulfran FORTIN Professeur Agrégé de Sciences Physiques TZR -
Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu. Auteur : Dr. Wulfran FORTIN Professeur Agrégé de Sciences Physiques TZR -
Assurance qualité du côté de l'entreprise (1) pour l'utilisation de systèmes de peintures intumescentes
 Assurance qualité du côté de l'entreprise (1) pour l'utilisation de systèmes de peintures intumescentes sur acier (en tant qu'annexe 3 de la publication SZS C2.5 «Peintures intumescentes» reconnue officiellement
Assurance qualité du côté de l'entreprise (1) pour l'utilisation de systèmes de peintures intumescentes sur acier (en tant qu'annexe 3 de la publication SZS C2.5 «Peintures intumescentes» reconnue officiellement
UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure
 UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure APPEL D OFFRES OUVERT SUR OFFRES DE PRIX 08/ENS/24 BORDEREAU DES PRIX-DETAIL ESTIMATIF Lot n 2 : Achat et installation de matériel pour l enseignement
UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure APPEL D OFFRES OUVERT SUR OFFRES DE PRIX 08/ENS/24 BORDEREAU DES PRIX-DETAIL ESTIMATIF Lot n 2 : Achat et installation de matériel pour l enseignement
