PURIFICATION DE COMPOSÉS
|
|
|
- Aurélie Lessard
- il y a 5 ans
- Total affichages :
Transcription
1 PURIFICATION DE COMPOSÉS A. Composés liquides miscibles I. Distillation fractionnée Dans l'industrie, la tour de distillation, surmontant la chaudière, est constituée d'une superposition de n plateaux. À chaque étage s'établissent des équilibres d'ébullition et de condensation. La tour est alimentée en continu. Le plateau choisi est celui dont la composition est la plus proche de celle de la charge. Au laboratoire, on utilise une colonne à distiller (colonne Vigreux par exemple) dont les aspérités intérieures freinent la montée de la vapeur et rendent possible l'établissement des équilibres. Pour simplifier l étude, on considère que le mélange à purifier n est constitué que de deux composés A et B. 1. Absence d'azéotrope : À une température donnée, le liquide est plus riche que la vapeur en constituant le moins volatil; la vapeur monte de l'étage (n-1) à l'étage n, elle se refroidit et donc se condense en enrichissant le liquide de l'étage n en constituant le plus volatil; le trop-plein s'écoule vers l'étage (n-1) de température plus élevée; il s'y vaporise partiellement en émettant une vapeur plus riche en constituant le plus volatil et en laissant un liquide plus pauvre en constituant le plus volatil. Rq. Au lycée, le chauffage est assuré par un chauffe-ballon. Dans le montage ci-dessus, on utilise un bain d huile comme dans certains concours. Attention de ne pas mettre de l eau dans un tel bain! Globalement, la vapeur monte dans la colonne en se refroidissant et en s'enrichissant en constituant le plus volatil; le liquide descend en se réchauffant et en s'enrichissant en constituant le moins volatil. 1
2 Si le nombre de plateaux est suffisant, on obtiendra la vapeur du constituant le plus volatil en haut de colonne (sa condensation par un réfrigérant descendant donne le distillat) et le liquide du constituant le moins volatil en bas de colonne (résidu de distillation). La position du réservoir du thermomètre placé en tête de colonne est capitale si l on veut que la température lue ait un sens. Il faut que le milieu du réservoir soit au niveau de la partie basse de la tubulure latérale qui part vers le réfrigérant droit, donc un peu plus bas que sur le schéma précédent. On chauffe un mélange liquide de composition x B. La première bulle de vapeur apparaît à la températuret N, sa composition est y 1 B (N 1 ). La vapeur monte dans le Vigreux et s y refroidit à la température T N pour donner un liquide de 2 même composition en équilibre avec une vapeur de composition y B (N 2 ) qui monte dans la colonne. Ce double processus (vaporisationliquéfaction) se poursuit, les vapeurs s enrichissent en composé le plus volatil. Si le nombre de plateau est suffisant seule la vapeur de B parvient au sommet de la colonne et le distillat ne contient que B pur. Un Vigreux de 25 cm correspond à 2 plateaux théoriques environ. La figure ci-dessus schématise de manière simplifiée l évolution de la température en tête de colonne. La fraction 1 peut contenir des impuretés très volatiles, on la recueille dans une poubelle. Quand on observe un palier de température (que l on note sur le compte-rendu), on recueille le composé B dans un récipient propre et sec. Dès que la température change, on recueille le distillat dans la poubelle (fraction 3). Lorsque l on observe un nouveau palier de température (noté lui aussi), un nouveau récipient propre et sec permet de récupérer le composé le moins volatil Rq. En réalité les courbes ne sont pas linéaires et l on observe un léger décrochement de température entre les fractions 2 et 3 du au refroidissement du Vigreux. 2. Présence d azéotrope On ne peut pas obtenir les deux corps purs; on ne peut obtenir que l'azéotrope et l'un des corps purs. On ne travaille que sur l'un des fuseaux (le système ne comporte qu'une phase liquide et qu'une phase vapeur!). C'est la composition initiale du mélange à distiller qui détermine le "fuseau de travail". Pour un azéotrope à maximum de température, l'azéotrope se comporte comme le composé le moins volatil et constituera le résidu de distillation. 2
3 Le rendement de ce mode de purification est très faible, donc cette méthode est peu utilisée. On peut faire appel à une distillation fractionnée de mélange ternaire, mais c est une autre histoire. II. Distillation simple Cette méthode de séparation peut être mise en œuvre lorsque les températures d ébullition des deux composés sont très différentes. L écart doit être supérieur à 80 C. L utilisation de l évaporateur rotatif en est une illustration car le solvant est nettement plus volatil que le composé synthétisé. B. Composés liquides non miscibles 1. Hydrodistillation Rq. Si la quantité d eau initiale est suffisante l ampoule de coulée isobare n est pas indispensable. La difficulté est que l on ne connaît pas à l avance la quantité nécessaire. Regardez attentivement le schéma de cette ampoule : la surface libre du liquide est horizontale et la partie inférieure de la tubulure est en dessous du robinet! Le thermomètre en tête de colonne n est pas indispensable. L'hydrodistillation est utilisable pour deux constituants non miscibles à l'état liquide (l'eau et souvent un composé organique). Elle ne nécessite pas de colonne à distiller. Le chauffage modéré du système permet la production d'une vapeur à une température constante égale à la température de l'hétéroazéotrope (ceci tant que les deux liquides subsistent). Cette température est simultanément inférieure aux températures d'ébullition, à la pression considérée, des deux liquides purs; en effet, l'ébullition se produit dès que la somme des pressions de vapeur saturante des deux liquides est égale à la pression extérieure. Le rapport des fractions molaires des deux constituants dans la vapeur formée est égal au rapport de leurs pressions de vapeur saturante à la température de l'hétéroazéotrope. La vapeur est continuellement condensée par un réfrigérant descendant et les constituants liquides obtenus sont recueillis puis séparés à l'aide d'une ampoule à décanter. Cette méthode permet notamment d'extraire un composé organique d'un brut réactionnel à une température suffisamment faible pour éviter des dégradations de ce composé. 3
4 L'hydrodistillation peut aussi servir à déplacer des réactions : les réactions d'estérification et d'acétalisation sont thermodynamiquement peu favorisées : on les déplace en évacuant l'eau formée du milieu réactionnel à l'aide de toluène (par exemple). L interprétation des courbes n est pas reprise ici, c est du cours! 2) Entraînement à la vapeur d'eau Le principe est le même mais on fait passer de la vapeur d'eau dans le brut réactionnel; cette circulation apporte l'eau et la chaleur (par condensation partielle de l'eau); on a alors production d'une vapeur contenant la substance à extraire et l'eau. Cette méthode permet par exemple d'extraire le limonène de l'écorce d'orange ou l'essence de lavande des fleurs de lavande. Parfois, on chauffe aussi le ballon contenant le système à traiter. 4
5 3. Extraction liquide/liquide Il s agit d une technique usuelle en chimie qui permet d isoler le produit d intérêt en le faisant passer depuis une phase liquide (brut réactionnel) dans un autre phase liquide non miscible à la première et dans lequel il est soluble. On utilise pour cela une ampoule à décanter. Dans la suite, on se limite à une phase aqueuse (assimilé au brut réactionnel) et à une phase organique (solvant d extraction). La répartition du produit entre ces deux phase est décrite par un équilibre de partage : A (aq) = A (org) caractérisé par une constante d équilibre nommée coefficient de partage. [ A( org) ] eq Son expression est : K = avec des notations évidentes. A [ ( aq) ] eq Le rendement d extraction est maximal à l équilibre. Il convient donc d agiter vivement et plusieurs fois l ampoule à décanter. On démontre que pour un volume donné de solvant extracteur, on a intérêt à opérer plusieurs lavages avec des fractions de volume plutôt qu un seul lavage avec tout le volume. Généralement, les phases organiques réunies sont lavées par des solutions aqueuses pour éliminer les impuretés. Durant ces opérations de lavage le produit d intérêt ne change pas de phase. Un composé ionique (chlorure de sodium le plus souvent peut être ajouté à la phase aqueuse. Cette étape de relargage permet de déshydrater la phase organique en mobilisant les molécules d eau encore piégées dans la phase organique et de diminuer la solubilité du produit d intérêt dans la phase aqueuse. Quelques règles de bon usage de l ampoule à décanter : - Éviter les surpressions. Pour cela ne pas fermer l ampoule tant qu un dégagement gazeux est perceptible et ouvrir le robinet dès que vous avez retourné l ampoule avant toute agitation. Ne pas oublier de refermer le robinet avant agitation - Lorsque l on ouvre le robinet, diriger l extrémité vers une hotte ou vers un mur, en tous cas vers un espace libre. - Agiter vivement l ampoule en tenant son bouchon appuyé dans la paume de la main et déplaçant l ampoule parallèlement à elle-même et inclinée de 45 afin d éviter que du liquide ne s accumule vers le robinet et soit chassé lors de l ouverture. 5
6 C. Composés solides : Recristallisation Lors d'une synthèse organique, le produit d intérêt P à obtenir s'est généralement solidifié brutalement, soit au cours de sa formation parce qu'il est insoluble dans son milieu d'obtention, soit lors d'un refroidissement rapide, soit par un ajout d'eau, soit par acidification (précipitation d'un acide carboxylique par acidification de la solution de carboxylate). La solidification ne s'est donc pas effectuée sous contrôle thermodynamique et le solide en se formant a emprisonné différents composés : des molécules de solvant, des molécules des réactifs ou de catalyseurs désormais qualifiées d'impuretés. I. Principe de la recristallisation La recristallisation est une technique de purification des solides qui consiste à dissoudre le solide brut dans le minimum de solvant S à ébullition. Ci-dessous, le composé à purifier est nommé P ou A. T P constante T fus (A) L (= A + S) T eb (S) T 1 N N' L + A (s) 20 C 15 C H J O O' O'' R R' R" P x S (O'') xs (R'') x S La purification par recristallisation est possible si P et le solvant S choisi pour la recristallisation sont non miscibles à l'état solide. Le diagramme liquide-solide ci-dessus est schématique et se limite à la partie du liquidus relative à l équilibre P (s) = P (dis) On remarque que cette partie du liquidus peut être interprétée comme une courbe de solubilité : la proportion de P diminue dans la phase liquide saturée si la température diminue (la dissolution de P dans S est donc endothermique). Le chauffage de P en présence de solvant S permet de dissoudre P : le point représentant le système se déplace de O vers N situé dans le domaine du liquide. Pour pouvoir totalement dissoudre P dans le minimum de solvant, il faut élever le plus possible la température du système. La température T 1 qu'il faut atteindre est donc la température à partir de laquelle le solvant commence à bouillir : T 1 = T eb (S) (attention, cette température n'est pas la température d'ébullition du solvant pur). Pour des raisons cinétiques, T N est légèrement supérieure à T 1. On refroidit ensuite lentement de manière à avoir un contrôle proche du contrôle thermodynamique. Quand T = T 1, le solide P commence à se former. On peut alors refroidir plus rapidement. Si on laisse la température diminuer, une plus grande quantité de P solide se forme (en conformité avec le théorème des moments) et il subsiste du P dissous dans le solvant. Une fois la température souhaitée atteinte, on filtre et on essore le solide. 6
7 A priori, on a intérêt à diminuer fortement la température pour minimiser la perte en P puisque la solubilité de P diminue lorsque la température diminue. Mais, il ne faut surtout pas refroidir jusqu'à la température de l'eutectique car les deux solides (P et S) se forment alors. On filtre pour récupérer P solide, la fraction restant en solution étant a priori perdue. On voit donc qu'il est nécessaire d'arriver à une température finale la plus faible possible, sans atteindre l'eutectique, de manière à limiter la perte en composé P. On doit utiliser le minimum de solvant pour perdre le minimum de P car pour une même température finale de refroidissement, la quantité de P restant en solution est proportionnelle au volume de solvant. II. Prise en compte des impuretés L approche binaire est simpliste car il y a aussi des impuretés, mais l idée générale reste la même. Il peut arriver, cas assez rare, que des impuretés restent insolubles à chaud. Dans ce cas, on effectue une première filtration à chaud pour les éliminer. La purification nécessite que les impuretés solubles à chaud restent solubles à froid. Concrètement, cela signifie que le point représentant le système dans un diagramme solvant-impureté se situe dans le domaine du liquide à la température finale. Lors de la recristallisation, P solide se forme et les impuretés restent en solution. Si le refroidissement est suffisamment lent, les impuretés ne sont pas piégées par la phase solide de P qui se forme, on obtient donc P pur ou contenant un peu de solvant. On filtre puis on sèche le composé P à l'étuve pour éliminer le solvant. III. Critères de choix du solvant Le solvant et P ne doivent pas réagir chimiquement l'un avec l'autre! Le composé P doit être soluble à chaud et très peu soluble à froid : il ne faut donc pas un trop bon solvant. Les impuretés doivent êtres solubles dans le solvant à chaud comme à froid. Le solvant doit être assez volatil pour être éliminé par séchage à l'étuve, mais ne doit pas avoir une température d ébullition trop faible car la différence de solubilité de P dans S à ébullition et à froid varie comme l écart de température entre l ambiante et la température d ébullition du solvant. Des solvants usuels de recristallisation : eau, éthanol, éthanoate d'éthyle Lorsque l on ne trouve pas un «bon» solvant de recristallisation, on utilise un mélange de deux solvants miscibles. On les choisit de manière à ce qu ils aient des températures d ébullition proches et possèdent de grandes différences dans leur propriétés de solubilisation de P. (dans un, P est très soluble, dans l autre, très peu soluble). On dissout d abord P dans le bon solvant à ébullition puis on ajoute progressivement le mauvais solvant (toujours à ébullition) lentement jusqu à observer un trouble, c est-àdire un début de précipitation. On laisse ensuite refroidir lentement. IV. Que répondre aux concours? Le principe d'une purification par recristallisation est souvent demandé et il serait difficile et non rentable d'expliquer tout ce qui précède à l écrit ; à l oral on vous écoutera ou on vous interrompra. Le minimum à dire à l écrit : La recristallisation est une technique de purification des solides qui consiste à dissoudre le solide brut dans le minimum de solvant S à ébullition. On laisse ensuite refroidir lentement jusqu'à l'apparition des premiers grains de solide puis on refroidit plus rapidement. On filtre et on essore. Le solvant et le produit d intérêt P ne doivent pas réagir chimiquement l'un avec l'autre. Le composé P doit être soluble à chaud et très peu soluble à froid dans S. Les impuretés doivent êtres solubles dans le solvant à chaud comme à froid. On filtre sous vide puis on sèche le solide à l'étuve. On peut contrôler la nature de P et sa pureté par mesure de la température de fusion au banc KÖFLER. 7
8 V. Réalisation On reconnaît le montage de chauffage à reflux. L ampoule de coulée isobare n est pas indispensable. On peu ajouter le solvant manquant par le haut du réfrigérant en prenant toutes les précautions nécessaires : ôter le système de chauffage, ajouter le solvant, essuyer les bords du réfrigérant, remettre le chauffage. On peut partir de trois volumes de liquide pour un volume de solide, sauf indication contraire du protocole), puis chauffer à reflux (réfrigérant à eau). Si, après quelques minutes d'ébullition, tout le solide n'est pas dissous, on ajoute un peu de solvant et on chauffe et on procède ainsi jusqu'à dissolution complète du solide (le solide qui ne se serait pas dissous resterait impur). On peut mettre un agitateur dans le ballon, mais il faut le retirer dès que l on cesse définitivement le chauffage. S'il subsiste des impuretés insolubles, on filtre à chaud en récupérant le filtrat dans un récipient propre. On laisse refroidir lentement. P cristallise et les impuretés restent en solution. Si le solide n apparaît pas, on peut essayer - de plonger le ballon dans un bain d eau glacée voire un mélange glace/chlorure de sodium, - de gratter l extérieur du ballon avec une baguette de verre, - si rien ne se passe après les deux essais précédents, gratter l intérieur du ballon avec une baguette de verre : des microcristaux de verre sont crées jouant le rôle de points de nucléation, mais on peut y perdre en pureté. La raison principale de la non-recristallisation est d origine cinétique. Le système est dans un état métastable 8
TECHNIQUES DE BASE EN CHIMIE ORGANIQUE
 TECHNIQUES DE BASE EN CHIMIE ORGANIQUE La synthèse organique suit en général le schéma suivant : Synthèse Séparation des produits Caractérisation du produit Pur? Oui Fin. Evaluation du rendement Non Purification
TECHNIQUES DE BASE EN CHIMIE ORGANIQUE La synthèse organique suit en général le schéma suivant : Synthèse Séparation des produits Caractérisation du produit Pur? Oui Fin. Evaluation du rendement Non Purification
Savoir écouter, assimiler : s approprier
 PCSI TP-DI Chimie organique INITIATION A LA CHIMIE ORGANIQUE Travail élève : savoirs et actions Compétences attendues Au début du TP, quelques explications orales sur le déroulement de la séance, sur le
PCSI TP-DI Chimie organique INITIATION A LA CHIMIE ORGANIQUE Travail élève : savoirs et actions Compétences attendues Au début du TP, quelques explications orales sur le déroulement de la séance, sur le
Synthèse et propriétés des savons.
 Synthèse et propriétés des savons. Objectifs: Réaliser la synthèse d'un savon mise en évidence de quelques propriétés des savons. I Introduction: 1. Présentation des savons: a) Composition des savons.
Synthèse et propriétés des savons. Objectifs: Réaliser la synthèse d'un savon mise en évidence de quelques propriétés des savons. I Introduction: 1. Présentation des savons: a) Composition des savons.
Suivi d une réaction lente par chromatographie
 TS Activité Chapitre 8 Cinétique chimique Suivi d une réaction lente par chromatographie Objectifs : Analyser un protocole expérimental de synthèse chimique Analyser un chromatogramme pour mettre en évidence
TS Activité Chapitre 8 Cinétique chimique Suivi d une réaction lente par chromatographie Objectifs : Analyser un protocole expérimental de synthèse chimique Analyser un chromatogramme pour mettre en évidence
Exemples d utilisation de G2D à l oral de Centrale
 Exemples d utilisation de G2D à l oral de Centrale 1 Table des matières Page 1 : Binaire liquide-vapeur isotherme et isobare Page 2 : Page 3 : Page 4 : Page 5 : Page 6 : intéressant facile facile sauf
Exemples d utilisation de G2D à l oral de Centrale 1 Table des matières Page 1 : Binaire liquide-vapeur isotherme et isobare Page 2 : Page 3 : Page 4 : Page 5 : Page 6 : intéressant facile facile sauf
EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points)
 Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage
 PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage I) Qu'est-ce qu'un savon et comment le fabrique-t-on? D'après épreuve BAC Liban 2005 Physique-Chimie dans la cuisine Chapitre 3 1/6 1- En vous
PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage I) Qu'est-ce qu'un savon et comment le fabrique-t-on? D'après épreuve BAC Liban 2005 Physique-Chimie dans la cuisine Chapitre 3 1/6 1- En vous
TECHNIQUES: Principes de la chromatographie
 TECHNIQUES: Principes de la chromatographie 1 Définition La chromatographie est une méthode physique de séparation basée sur les différentes affinités d un ou plusieurs composés à l égard de deux phases
TECHNIQUES: Principes de la chromatographie 1 Définition La chromatographie est une méthode physique de séparation basée sur les différentes affinités d un ou plusieurs composés à l égard de deux phases
CHROMATOGRAPHIE SUR COUCHE MINCE
 CHROMATOGRAPHIE SUR COUCHE MINCE I - PRINCIPE La chromatographie est une méthode physique de séparation de mélanges en leurs constituants; elle est basée sur les différences d affinité des substances à
CHROMATOGRAPHIE SUR COUCHE MINCE I - PRINCIPE La chromatographie est une méthode physique de séparation de mélanges en leurs constituants; elle est basée sur les différences d affinité des substances à
Calcaire ou eau agressive en AEP : comment y remédier?
 Calcaire ou eau agressive en AEP : comment y remédier? Les solutions techniques Principes et critères de choix Par Sébastien LIBOZ - Hydrogéologue Calcaire ou eau agressive en AEP : comment y remédier?
Calcaire ou eau agressive en AEP : comment y remédier? Les solutions techniques Principes et critères de choix Par Sébastien LIBOZ - Hydrogéologue Calcaire ou eau agressive en AEP : comment y remédier?
Matériel de laboratoire
 Matériel de laboratoire MATERIAUX UTILISE... 1 L'APPAREILLAGE DE LABORATOIRE... 1 a) Les récipients à réaction... 2 b) La verrerie Graduée... 2 MATERIEL DE FILTRATION... 6 FILTRATION SOUS VIDE AVEC UN
Matériel de laboratoire MATERIAUX UTILISE... 1 L'APPAREILLAGE DE LABORATOIRE... 1 a) Les récipients à réaction... 2 b) La verrerie Graduée... 2 MATERIEL DE FILTRATION... 6 FILTRATION SOUS VIDE AVEC UN
- pellicule de fruits qui a un rôle de prévention contre l'évaporation, le développement de moisissures et l'infection par des parasites
 LES LIPIDES Quelles Sont les Idées Clés? Les lipides sont les huiles et les graisses de la vie courante. Ils sont insolubles dans l eau. Pour les synthétiser, une réaction : l Estérification. Pour les
LES LIPIDES Quelles Sont les Idées Clés? Les lipides sont les huiles et les graisses de la vie courante. Ils sont insolubles dans l eau. Pour les synthétiser, une réaction : l Estérification. Pour les
Fiche 23 : Au laboratoire
 Fiche 23 : Au laboratoire 05/03/2007 Au laboratoire Le port de la blouse est obligatoire. Le port des lunettes ou surlunettes est obligatoire (attention au port des lentilles de contact, autorisé mais
Fiche 23 : Au laboratoire 05/03/2007 Au laboratoire Le port de la blouse est obligatoire. Le port des lunettes ou surlunettes est obligatoire (attention au port des lentilles de contact, autorisé mais
Les solutions. Chapitre 2 - Modèle. 1 Définitions sur les solutions. 2 Concentration massique d une solution. 3 Dilution d une solution
 Chapitre 2 - Modèle Les solutions 1 Définitions sur les solutions 1.1 Définition d une solution : Une solution est le mélange homogène et liquide d au moins deux espèces chimiques : Le soluté : c est une
Chapitre 2 - Modèle Les solutions 1 Définitions sur les solutions 1.1 Définition d une solution : Une solution est le mélange homogène et liquide d au moins deux espèces chimiques : Le soluté : c est une
Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu.
 Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu. Auteur : Dr. Wulfran FORTIN Professeur Agrégé de Sciences Physiques TZR -
Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu. Auteur : Dr. Wulfran FORTIN Professeur Agrégé de Sciences Physiques TZR -
Etudier le diagramme température-pression, en particulier le point triple de l azote.
 K4. Point triple de l azote I. BUT DE LA MANIPULATION Etudier le diagramme température-pression, en particulier le point triple de l azote. II. BASES THEORIQUES Etats de la matière La matière est constituée
K4. Point triple de l azote I. BUT DE LA MANIPULATION Etudier le diagramme température-pression, en particulier le point triple de l azote. II. BASES THEORIQUES Etats de la matière La matière est constituée
33-Dosage des composés phénoliques
 33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
Mesures calorimétriques
 TP N 11 Mesures calorimétriques - page 51 - - T.P. N 11 - Ce document rassemble plusieurs mesures qui vont faire l'objet de quatre séances de travaux pratiques. La quasi totalité de ces manipulations utilisent
TP N 11 Mesures calorimétriques - page 51 - - T.P. N 11 - Ce document rassemble plusieurs mesures qui vont faire l'objet de quatre séances de travaux pratiques. La quasi totalité de ces manipulations utilisent
direct serve EN DE NI ES PT CZ SK www.moulinex.com
 FR direct serve EN DE NI ES PT CZ SK www.moulinex.com 4 3 2 1 71mm 5 6 7 1 2 3 4 5 6 OK Click NO 7 8 9 150ml 10 Nous vous remercions d avoir choisi un appareil de la gamme Moulinex. CONSIGNES DE SECURITE
FR direct serve EN DE NI ES PT CZ SK www.moulinex.com 4 3 2 1 71mm 5 6 7 1 2 3 4 5 6 OK Click NO 7 8 9 150ml 10 Nous vous remercions d avoir choisi un appareil de la gamme Moulinex. CONSIGNES DE SECURITE
La Plateforme GALA. Un projet régional structurant. avec le pôle Cancer-Bio-Santé pour la recherche et l'innovation en galénique CPER 2007-2013
 La Plateforme GALA Un projet régional structurant CPER 2007-2013 avec le pôle Cancer-Bio-Santé pour la recherche et l'innovation en galénique Labellisé en avril 2009 Plateforme GALA : quel rôle? Principe
La Plateforme GALA Un projet régional structurant CPER 2007-2013 avec le pôle Cancer-Bio-Santé pour la recherche et l'innovation en galénique Labellisé en avril 2009 Plateforme GALA : quel rôle? Principe
CODEX ŒNOLOGIQUE INTERNATIONAL. SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012)
 SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012) 1. OBJET, ORIGINE ET DOMAINE D APPLICATION Le sucre de raisin est obtenu exclusivement à partir du
SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012) 1. OBJET, ORIGINE ET DOMAINE D APPLICATION Le sucre de raisin est obtenu exclusivement à partir du
SP. 3. Concentration molaire exercices. Savoir son cours. Concentrations : Classement. Concentration encore. Dilution :
 SP. 3 Concentration molaire exercices Savoir son cours Concentrations : Calculer les concentrations molaires en soluté apporté des solutions désinfectantes suivantes : a) Une solution de 2,0 L contenant
SP. 3 Concentration molaire exercices Savoir son cours Concentrations : Calculer les concentrations molaires en soluté apporté des solutions désinfectantes suivantes : a) Une solution de 2,0 L contenant
AIDE-MÉMOIRE LA THERMOCHIMIE TABLE DES MATIERES
 Collège Voltaire, 2014-2015 AIDE-MÉMOIRE LA THERMOCHIMIE http://dcpe.net/poii/sites/default/files/cours%20et%20ex/cours-ch2-thermo.pdf TABLE DES MATIERES 3.A. Introduction...2 3.B. Chaleur...3 3.C. Variation
Collège Voltaire, 2014-2015 AIDE-MÉMOIRE LA THERMOCHIMIE http://dcpe.net/poii/sites/default/files/cours%20et%20ex/cours-ch2-thermo.pdf TABLE DES MATIERES 3.A. Introduction...2 3.B. Chaleur...3 3.C. Variation
L eau liquide a des propriétés
 Eau à l état gazeux ELLE EXISTE SOUS DIFFERENTES FORMES OU ETATS Eau à l état solide ELLE PEUT PASSER D UN ETAT À L AUTRE CYCLE DE L EAU Eau à l état liquide Elle dissout Faire des mélanges NOUS UTILISONS
Eau à l état gazeux ELLE EXISTE SOUS DIFFERENTES FORMES OU ETATS Eau à l état solide ELLE PEUT PASSER D UN ETAT À L AUTRE CYCLE DE L EAU Eau à l état liquide Elle dissout Faire des mélanges NOUS UTILISONS
FICHE 1 Fiche à destination des enseignants
 FICHE 1 Fiche à destination des enseignants 1S 8 (b) Un entretien d embauche autour de l eau de Dakin Type d'activité Activité expérimentale avec démarche d investigation Dans cette version, l élève est
FICHE 1 Fiche à destination des enseignants 1S 8 (b) Un entretien d embauche autour de l eau de Dakin Type d'activité Activité expérimentale avec démarche d investigation Dans cette version, l élève est
1 ère partie : tous CAP sauf hôtellerie et alimentation CHIMIE ETRE CAPABLE DE. PROGRAMME - Atomes : structure, étude de quelques exemples.
 Référentiel CAP Sciences Physiques Page 1/9 SCIENCES PHYSIQUES CERTIFICATS D APTITUDES PROFESSIONNELLES Le référentiel de sciences donne pour les différentes parties du programme de formation la liste
Référentiel CAP Sciences Physiques Page 1/9 SCIENCES PHYSIQUES CERTIFICATS D APTITUDES PROFESSIONNELLES Le référentiel de sciences donne pour les différentes parties du programme de formation la liste
THE SEPARATION OF A TRACER FOR THE RADIOCHEM1CAL ANALYSIS OF RADIUM 226.
 CEA-R 2419 - BUTAYE Michel ISOLEMENT D'UN TRACEUR POUR L'ANALYSE RAJDIOCHIMIQUE DU RADIUM 226. 223 Sommaire.- Ce rapport décrit une méthode d'isolement du Ra à partir d'un minerai d'uranium et son utilisation
CEA-R 2419 - BUTAYE Michel ISOLEMENT D'UN TRACEUR POUR L'ANALYSE RAJDIOCHIMIQUE DU RADIUM 226. 223 Sommaire.- Ce rapport décrit une méthode d'isolement du Ra à partir d'un minerai d'uranium et son utilisation
Exercices sur le thème II : Les savons
 Fiche d'exercices Elève pour la classe de Terminale SMS page 1 Exercices sur le thème : Les savons EXERCICE 1. 1. L oléine, composé le plus important de l huile d olive, est le triglycéride de l acide
Fiche d'exercices Elève pour la classe de Terminale SMS page 1 Exercices sur le thème : Les savons EXERCICE 1. 1. L oléine, composé le plus important de l huile d olive, est le triglycéride de l acide
Propriétés thermodynamiques du mélange. Eau-Ammoniac-Hélium
 International Renewable Energy Congress November 5-7, 2010 Sousse, Tunisia Propriétés thermodynamiques du mélange Eau-Ammoniac-Hélium Chatti Monia 1, Bellagi Ahmed 2 1,2 U.R. Thermique et Thermodynamique
International Renewable Energy Congress November 5-7, 2010 Sousse, Tunisia Propriétés thermodynamiques du mélange Eau-Ammoniac-Hélium Chatti Monia 1, Bellagi Ahmed 2 1,2 U.R. Thermique et Thermodynamique
DEMANDE DE BREVET EUROPEEN. PLASSERAUD 84, rue d'amsterdam, F-75009 Paris (FR)
 Patentamt JEuropâisches European Patent Office @ Numéro de publication: 0 1 1 0 7 5 4 Office européen des brevets ^ ^ DEMANDE DE BREVET EUROPEEN Numéro de dépôt: 83402133.9 Int. Cl.3: C 07 C 103/183, C
Patentamt JEuropâisches European Patent Office @ Numéro de publication: 0 1 1 0 7 5 4 Office européen des brevets ^ ^ DEMANDE DE BREVET EUROPEEN Numéro de dépôt: 83402133.9 Int. Cl.3: C 07 C 103/183, C
FACTEURS INFLUENÇANT LA QUALITÉ DU CAFÉ-BOISSON 1 - CAFÉ 2 - TORRÉFACTION 3 - CONSERVATION 4 - EAU 5 - MOUTURE 6 - DOSAGE 7 - TYPE DE PRÉPARATION
 FACTEURS INFLUENÇANT LA QUALITÉ DU CAFÉ-BOISSON 1 - CAFÉ 2 - TORRÉFACTION 3 - CONSERVATION 4 - EAU 5 - MOUTURE 6 - DOSAGE 7 - TYPE DE PRÉPARATION 1 1. CAFÉ La qualité du café vert dépend : De l espèce
FACTEURS INFLUENÇANT LA QUALITÉ DU CAFÉ-BOISSON 1 - CAFÉ 2 - TORRÉFACTION 3 - CONSERVATION 4 - EAU 5 - MOUTURE 6 - DOSAGE 7 - TYPE DE PRÉPARATION 1 1. CAFÉ La qualité du café vert dépend : De l espèce
Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire
 1 2 3 4 Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire Partie 1 Chapitre 3: Locaux et matériel 5 6 7 8 9 10 11 12 13 PRINCIPE Les locaux et le matériel doivent être situés,
1 2 3 4 Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire Partie 1 Chapitre 3: Locaux et matériel 5 6 7 8 9 10 11 12 13 PRINCIPE Les locaux et le matériel doivent être situés,
GUIDE D INSTRUCTION. Montage Entretien
 GUIDE D INSTRUCTION Montage Entretien INSTRUCTIONS PARTICULIÈRES Dès réception des marchandises, veuillez vérifier le bon état de l'emballage. Veuillez mentionner tout dégât éventuel de transport sur le
GUIDE D INSTRUCTION Montage Entretien INSTRUCTIONS PARTICULIÈRES Dès réception des marchandises, veuillez vérifier le bon état de l'emballage. Veuillez mentionner tout dégât éventuel de transport sur le
UTILISATION DES SÉDIMENTS VALORISÉS : exemple de la plate-forme expérimentale SOLINDUS pour le pré-traitement des produits de dragage
 UTILISATION DES SÉDIMENTS VALORISÉS : exemple de la plate-forme expérimentale SOLINDUS pour le pré-traitement des produits de dragage Dr H. Bréquel, Responsable département Recherche 1 1 /20 CONTEXTE ET
UTILISATION DES SÉDIMENTS VALORISÉS : exemple de la plate-forme expérimentale SOLINDUS pour le pré-traitement des produits de dragage Dr H. Bréquel, Responsable département Recherche 1 1 /20 CONTEXTE ET
EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points)
 BAC S 2011 LIBAN http://labolycee.org EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points) Les parties A et B sont indépendantes. A : Étude du fonctionnement d un spectrophotomètre
BAC S 2011 LIBAN http://labolycee.org EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points) Les parties A et B sont indépendantes. A : Étude du fonctionnement d un spectrophotomètre
Masse volumique et densité relative à 20 C
 Méthode OIV-MA-AS2-01A Méthodes Type I Masse volumique et densité relative à 20 C 1. Définition La masse volumique est le quotient de la masse d'un certain volume de vin ou de moût à 20 C par ce volume.
Méthode OIV-MA-AS2-01A Méthodes Type I Masse volumique et densité relative à 20 C 1. Définition La masse volumique est le quotient de la masse d'un certain volume de vin ou de moût à 20 C par ce volume.
TP : Suivi d'une réaction par spectrophotométrie
 Nom : Prénom: n groupe: TP : Suivi d'une réaction par spectrophotométrie Consignes de sécurité de base: Porter une blouse en coton, pas de nu-pieds Porter des lunettes, des gants (en fonction des espèces
Nom : Prénom: n groupe: TP : Suivi d'une réaction par spectrophotométrie Consignes de sécurité de base: Porter une blouse en coton, pas de nu-pieds Porter des lunettes, des gants (en fonction des espèces
Exemple de cahier de laboratoire : cas du sujet 2014
 Exemple de cahier de laboratoire : cas du sujet 2014 Commentaires pour l'évaluation Contenu du cahier de laboratoire Problématique : Le glucose est un nutriment particulièrement important pour le sportif.
Exemple de cahier de laboratoire : cas du sujet 2014 Commentaires pour l'évaluation Contenu du cahier de laboratoire Problématique : Le glucose est un nutriment particulièrement important pour le sportif.
COMMENT CONSTRUIRE UN CRIB A MAÏS?
 COMMENT CONSTRUIRE UN CRIB A MAÏS? Par Philippe et Marie-Noëlle LENOIR Un couple du Volontaires du Progrès qui travaille à GALIM Département des Bamboutos, Province de l Ouest, nous adresse cette fiche
COMMENT CONSTRUIRE UN CRIB A MAÏS? Par Philippe et Marie-Noëlle LENOIR Un couple du Volontaires du Progrès qui travaille à GALIM Département des Bamboutos, Province de l Ouest, nous adresse cette fiche
L eau dans le corps. Fig. 6 L eau dans le corps. Cerveau 85 % Dents 10 % Cœur 77 % Poumons 80 % Foie 73 % Reins 80 % Peau 71 % Muscles 73 %
 24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
Premier principe : bilans d énergie
 MPSI - Thermodynamique - Premier principe : bilans d énergie page 1/5 Premier principe : bilans d énergie Table des matières 1 De la mécanique à la thermodynamique : formes d énergie et échanges d énergie
MPSI - Thermodynamique - Premier principe : bilans d énergie page 1/5 Premier principe : bilans d énergie Table des matières 1 De la mécanique à la thermodynamique : formes d énergie et échanges d énergie
1. Identification de la substance / préparation et de la société / entreprise. Peinture Aimant
 Page: 1 de 6 1. Identification de la substance / préparation et de la société / entreprise. Nom du produit: Utilisations: Identification de l'entreprise: Peinture dispersion à base d'eau pour l'usage intérieur.
Page: 1 de 6 1. Identification de la substance / préparation et de la société / entreprise. Nom du produit: Utilisations: Identification de l'entreprise: Peinture dispersion à base d'eau pour l'usage intérieur.
4. Conditionnement et conservation de l échantillon
 1. Objet S-II-3V1 DOSAGE DU MERCURE DANS LES EXTRAITS D EAU RÉGALE Description du dosage du mercure par spectrométrie d absorption atomique de vapeur froide ou par spectrométrie de fluorescence atomique
1. Objet S-II-3V1 DOSAGE DU MERCURE DANS LES EXTRAITS D EAU RÉGALE Description du dosage du mercure par spectrométrie d absorption atomique de vapeur froide ou par spectrométrie de fluorescence atomique
A B C Eau Eau savonneuse Eau + détergent
 1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
Fiche de révisions sur les acides et les bases
 Fiche de révisions sur les s et les s A Définitions : : espèce chimique capable de libérer un (ou plusieurs proton (s. : espèce chimique capable de capter un (ou plusieurs proton (s. Attention! Dans une
Fiche de révisions sur les s et les s A Définitions : : espèce chimique capable de libérer un (ou plusieurs proton (s. : espèce chimique capable de capter un (ou plusieurs proton (s. Attention! Dans une
NORME CODEX POUR LES SUCRES 1 CODEX STAN 212-1999
 CODEX STAN 212-1999 Page 1 de 5 NORME CODEX POUR LES SUCRES 1 CODEX STAN 212-1999 1. CHAMP D'APPLICATION ET DESCRIPTION La présente norme vise les sucres énumérés ci-après destinés à la consommation humaine
CODEX STAN 212-1999 Page 1 de 5 NORME CODEX POUR LES SUCRES 1 CODEX STAN 212-1999 1. CHAMP D'APPLICATION ET DESCRIPTION La présente norme vise les sucres énumérés ci-après destinés à la consommation humaine
Bundesdruckerei Berlin
 Europaisches Patentamt European Patent Office Office européen des brevets @ Numéro de publication : 0 359 622 A1 DEMANDE DE BREVET EUROPEEN (S) Numéro de dépôt: 89402410.8 @ Date de dépôt: 05.09.89 (g)
Europaisches Patentamt European Patent Office Office européen des brevets @ Numéro de publication : 0 359 622 A1 DEMANDE DE BREVET EUROPEEN (S) Numéro de dépôt: 89402410.8 @ Date de dépôt: 05.09.89 (g)
pka D UN INDICATEUR COLORE
 TP SPETROPHOTOMETRIE Lycée F.BUISSON PTSI pka D UN INDIATEUR OLORE ) Principes de la spectrophotométrie La spectrophotométrie est une technique d analyse qualitative et quantitative, de substances absorbant
TP SPETROPHOTOMETRIE Lycée F.BUISSON PTSI pka D UN INDIATEUR OLORE ) Principes de la spectrophotométrie La spectrophotométrie est une technique d analyse qualitative et quantitative, de substances absorbant
Partie 2 La santé Notions:
 Partie 2 La santé Notions: Chapitre 8. Analyse des signaux périodiques 8.1. Introduction Qu'est ce qu'un phénomène périodique? Activité: Bordas 2010, p14 / Bordas 2014, p22 8.2. Les phénomènes périodiques
Partie 2 La santé Notions: Chapitre 8. Analyse des signaux périodiques 8.1. Introduction Qu'est ce qu'un phénomène périodique? Activité: Bordas 2010, p14 / Bordas 2014, p22 8.2. Les phénomènes périodiques
2 e partie de la composante majeure (8 points) Les questions prennent appui sur six documents A, B, C, D, E, F (voir pages suivantes).
 SUJET DE CONCOURS Sujet Exploitation d une documentation scientifique sur le thème de l énergie 2 e partie de la composante majeure (8 points) Les questions prennent appui sur six documents A, B, C, D,
SUJET DE CONCOURS Sujet Exploitation d une documentation scientifique sur le thème de l énergie 2 e partie de la composante majeure (8 points) Les questions prennent appui sur six documents A, B, C, D,
BACCALAURÉAT TECHNOLOGIQUE
 BACCALAURÉAT TECHNOLOGIQUE Série : Sciences et Technologies de Laboratoire Spécialité : Biotechnologies SESSION 2015 Sous-épreuve écrite de Biotechnologies Coefficient de la sous-épreuve : 4 Ce sujet est
BACCALAURÉAT TECHNOLOGIQUE Série : Sciences et Technologies de Laboratoire Spécialité : Biotechnologies SESSION 2015 Sous-épreuve écrite de Biotechnologies Coefficient de la sous-épreuve : 4 Ce sujet est
Session 2011 PHYSIQUE-CHIMIE. Série S. Enseignement de Spécialité. Durée de l'épreuve: 3 heures 30 - Coefficient: 8
 PYSCSLl BACCALAU Session 20 PHYSIQUE-CHIMIE Série S Enseignement de Spécialité Durée de l'épreuve: 3 heures 30 - Coefficient: 8 L'usage des calculatrices est autorisé. Ce sujet ne nécessite pas de feuille
PYSCSLl BACCALAU Session 20 PHYSIQUE-CHIMIE Série S Enseignement de Spécialité Durée de l'épreuve: 3 heures 30 - Coefficient: 8 L'usage des calculatrices est autorisé. Ce sujet ne nécessite pas de feuille
Etablissement Recevant du Public (ERP) de 5 ème catégorie avec locaux à sommeil
 Notice de sécurité Etablissement Recevant du Public (ERP) de 5 ème catégorie avec locaux à sommeil Cette notice a été établie à l'attention des exploitants d Etablissements Recevant du Public (ERP), afin
Notice de sécurité Etablissement Recevant du Public (ERP) de 5 ème catégorie avec locaux à sommeil Cette notice a été établie à l'attention des exploitants d Etablissements Recevant du Public (ERP), afin
Mario Geiger octobre 08 ÉVAPORATION SOUS VIDE
 ÉVAPORATION SOUS VIDE 1 I SOMMAIRE I Sommaire... 2 II Évaporation sous vide... 3 III Description de l installation... 5 IV Travail pratique... 6 But du travail... 6 Principe... 6 Matériel... 6 Méthodes...
ÉVAPORATION SOUS VIDE 1 I SOMMAIRE I Sommaire... 2 II Évaporation sous vide... 3 III Description de l installation... 5 IV Travail pratique... 6 But du travail... 6 Principe... 6 Matériel... 6 Méthodes...
TS1 TS2 02/02/2010 Enseignement obligatoire. DST N 4 - Durée 3h30 - Calculatrice autorisée
 TS1 TS2 02/02/2010 Enseignement obligatoire DST N 4 - Durée 3h30 - Calculatrice autorisée EXERCICE I : PRINCIPE D UNE MINUTERIE (5,5 points) A. ÉTUDE THÉORIQUE D'UN DIPÔLE RC SOUMIS À UN ÉCHELON DE TENSION.
TS1 TS2 02/02/2010 Enseignement obligatoire DST N 4 - Durée 3h30 - Calculatrice autorisée EXERCICE I : PRINCIPE D UNE MINUTERIE (5,5 points) A. ÉTUDE THÉORIQUE D'UN DIPÔLE RC SOUMIS À UN ÉCHELON DE TENSION.
' Département de Chimie Analytique, Académie de Médecine, 38 rue Szewska,
 J. Phys. IVFrance 11 (2001) O EDP Sciences, Les Ulis Limites des solutions solides dans le système binaire CdBr2-AgBr A. Wojakowska, A. Gorniak and W. ~awel' Laboratoire d'analyse Thermique, Département
J. Phys. IVFrance 11 (2001) O EDP Sciences, Les Ulis Limites des solutions solides dans le système binaire CdBr2-AgBr A. Wojakowska, A. Gorniak and W. ~awel' Laboratoire d'analyse Thermique, Département
THEME 2. LE SPORT CHAP 1. MESURER LA MATIERE: LA MOLE
 THEME 2. LE SPORT CHAP 1. MESURER LA MATIERE: LA MOLE 1. RAPPEL: L ATOME CONSTITUANT DE LA MATIERE Toute la matière de l univers, toute substance, vivante ou inerte, est constituée à partir de particules
THEME 2. LE SPORT CHAP 1. MESURER LA MATIERE: LA MOLE 1. RAPPEL: L ATOME CONSTITUANT DE LA MATIERE Toute la matière de l univers, toute substance, vivante ou inerte, est constituée à partir de particules
Titre alcalimétrique et titre alcalimétrique complet
 Titre alcalimétrique et titre alcalimétrique complet A Introduction : ) Définitions : Titre Alcalimétrique (T.A.) : F m / L T.A. T.A.C. Définition : C'est le volume d'acide (exprimé en ml) à 0,0 mol.l
Titre alcalimétrique et titre alcalimétrique complet A Introduction : ) Définitions : Titre Alcalimétrique (T.A.) : F m / L T.A. T.A.C. Définition : C'est le volume d'acide (exprimé en ml) à 0,0 mol.l
ProSimPlus HNO3 Résumé des nouvelles fonctionnalités, décembre 2008
 ProSimPlus HNO3 Résumé des nouvelles fonctionnalités, décembre 2008 Cette page présente un résumé des derniers développements effectués dans le logiciel ProSimPlus HNO3. Ceux-ci correspondent à de nouvelles
ProSimPlus HNO3 Résumé des nouvelles fonctionnalités, décembre 2008 Cette page présente un résumé des derniers développements effectués dans le logiciel ProSimPlus HNO3. Ceux-ci correspondent à de nouvelles
Étape 1 : Balancer la chimie de l'eau
 Étape 1 : Balancer la chimie de l'eau Au printemps surtout et durant l'été, il sera important de contrôler et d'ajuster certain paramètres qui constituent la chimie de l'eau. Cet étape est bien souvent
Étape 1 : Balancer la chimie de l'eau Au printemps surtout et durant l'été, il sera important de contrôler et d'ajuster certain paramètres qui constituent la chimie de l'eau. Cet étape est bien souvent
FICHE DE DONNEES DE SECURITE
 PAGE 1/7 DATE DE MISE A JOUR : 16/11/2011 1/ - IDENTIFICATION DU PRODUIT ET DE LA SOCIETE Identification du produit : Gaines, films, housses, et/ou sacs transparents et colorés en polyéthylène. Famille
PAGE 1/7 DATE DE MISE A JOUR : 16/11/2011 1/ - IDENTIFICATION DU PRODUIT ET DE LA SOCIETE Identification du produit : Gaines, films, housses, et/ou sacs transparents et colorés en polyéthylène. Famille
SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION)
 Terminale S CHIMIE TP n 2b (correction) 1 SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION) Objectifs : Déterminer l évolution de la vitesse de réaction par une méthode physique. Relier l absorbance
Terminale S CHIMIE TP n 2b (correction) 1 SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION) Objectifs : Déterminer l évolution de la vitesse de réaction par une méthode physique. Relier l absorbance
FONTANOT CREE UNE LIGNE D ESCALIERS IMAGINÉE POUR CEUX QUI AIMENT LE BRICOLAGE.
 STILE FONTANOT CREE UNE LIGNE D ESCALIERS IMAGINÉE POUR CEUX QUI AIMENT LE BRICOLAGE. 2 3 Magia. Une gamme de produits qui facilitera le choix de votre escalier idéal. 4 06 Guide pour la sélection. 16
STILE FONTANOT CREE UNE LIGNE D ESCALIERS IMAGINÉE POUR CEUX QUI AIMENT LE BRICOLAGE. 2 3 Magia. Une gamme de produits qui facilitera le choix de votre escalier idéal. 4 06 Guide pour la sélection. 16
LABORATOIRES DE CHIMIE Techniques de dosage
 LABORATOIRES DE CHIMIE Techniques de dosage Un dosage (ou titrage) a pour but de déterminer la concentration molaire d une espèce (molécule ou ion) en solution (généralement aqueuse). Un réactif de concentration
LABORATOIRES DE CHIMIE Techniques de dosage Un dosage (ou titrage) a pour but de déterminer la concentration molaire d une espèce (molécule ou ion) en solution (généralement aqueuse). Un réactif de concentration
Comprendre l efflorescence
 Février 2006 Bulletin technique 4 BULLETIN TECHNIQUE Le Conseil Canadien des Systèmes d Isolation et de Finition Extérieure (SIFE) / (416) 499-4000 Comprendre l efflorescence Nous avons tous déjà observé
Février 2006 Bulletin technique 4 BULLETIN TECHNIQUE Le Conseil Canadien des Systèmes d Isolation et de Finition Extérieure (SIFE) / (416) 499-4000 Comprendre l efflorescence Nous avons tous déjà observé
Présentation générale des principales sources d énergies fossiles.
 Présentation générale des principales sources d énergies fossiles. Date : 19/09/2012 NOM / Name SIGNATURE Etabli / Prepared Vérifié / Checked Approuvé /Approved G J-L & R-SENE R.SENE R.SENE Sommaire 1.
Présentation générale des principales sources d énergies fossiles. Date : 19/09/2012 NOM / Name SIGNATURE Etabli / Prepared Vérifié / Checked Approuvé /Approved G J-L & R-SENE R.SENE R.SENE Sommaire 1.
LE SPECTRE D ABSORPTION DES PIGMENTS CHLOROPHYLLIENS
 Fiche sujet-élève Les végétaux chlorophylliens collectent l énergie lumineuse grâce à différents pigments foliaires que l on peut classer en deux catégories : - les chlorophylles a et b d une part, - les
Fiche sujet-élève Les végétaux chlorophylliens collectent l énergie lumineuse grâce à différents pigments foliaires que l on peut classer en deux catégories : - les chlorophylles a et b d une part, - les
GUIDE DE BONNES PRATIQUES POUR LA COLLECTE DE PILES ET ACCUMULATEURS AU LUXEMBOURG
 GUIDE DE BONNES PRATIQUES POUR LA COLLECTE DE PILES ET ACCUMULATEURS AU LUXEMBOURG Version 1.0 1 Avant-propos Ce guide de bonnes pratiques a été préparé pour fournir des informations concernant la collecte
GUIDE DE BONNES PRATIQUES POUR LA COLLECTE DE PILES ET ACCUMULATEURS AU LUXEMBOURG Version 1.0 1 Avant-propos Ce guide de bonnes pratiques a été préparé pour fournir des informations concernant la collecte
Construire un plan de nettoyage et de désinfection
 Construire un plan de nettoyage et de désinfection Docteur Régine POTIÉ-RIGO Médecin du Travail Mlle Laetitia DAVEZAT IPRP Ingénieur Hygiène/Sécurité Mme Laetitia MARCHE Technicienne des services généraux
Construire un plan de nettoyage et de désinfection Docteur Régine POTIÉ-RIGO Médecin du Travail Mlle Laetitia DAVEZAT IPRP Ingénieur Hygiène/Sécurité Mme Laetitia MARCHE Technicienne des services généraux
K W = [H 3 O + ] [OH - ] = 10-14 = K a K b à 25 C. [H 3 O + ] = [OH - ] = 10-7 M Solution neutre. [H 3 O + ] > [OH - ] Solution acide
![K W = [H 3 O + ] [OH - ] = 10-14 = K a K b à 25 C. [H 3 O + ] = [OH - ] = 10-7 M Solution neutre. [H 3 O + ] > [OH - ] Solution acide K W = [H 3 O + ] [OH - ] = 10-14 = K a K b à 25 C. [H 3 O + ] = [OH - ] = 10-7 M Solution neutre. [H 3 O + ] > [OH - ] Solution acide](/thumbs/20/420627.jpg) La constante d autoprotolyse de l eau, K W, est égale au produit de K a par K b pour un couple acide/base donné : En passant en échelle logarithmique, on voit donc que la somme du pk a et du pk b d un
La constante d autoprotolyse de l eau, K W, est égale au produit de K a par K b pour un couple acide/base donné : En passant en échelle logarithmique, on voit donc que la somme du pk a et du pk b d un
BACCALAURÉAT GÉNÉRAL PHYSIQUE-CHIMIE
 BAALAURÉAT GÉNÉRAL SESSIN 2015 PYSIQUE-IMIE Série S Durée de l épreuve : 3 heures 30 oefficient : 6 L usage de la calculatrice est autorisé e sujet ne nécessite pas de feuille de papier millimétré Le sujet
BAALAURÉAT GÉNÉRAL SESSIN 2015 PYSIQUE-IMIE Série S Durée de l épreuve : 3 heures 30 oefficient : 6 L usage de la calculatrice est autorisé e sujet ne nécessite pas de feuille de papier millimétré Le sujet
BREVET DE TECHNICIEN SUPÉRIEUR QUALITÉ DANS LES INDUSTRIES ALIMENTAIRES ET LES BIO-INDUSTRIES
 ~--------------~~-----~- ----~-- Session 2009 BREVET DE TECNICIEN SUPÉRIEUR QUALITÉ DANS LES INDUSTRIES ALIMENTAIRES ET LES BIO-INDUSTRIES U22 - SCIENCES PYSIQUES Durée: 2 heures Coefficient : 3 Les calculatrices
~--------------~~-----~- ----~-- Session 2009 BREVET DE TECNICIEN SUPÉRIEUR QUALITÉ DANS LES INDUSTRIES ALIMENTAIRES ET LES BIO-INDUSTRIES U22 - SCIENCES PYSIQUES Durée: 2 heures Coefficient : 3 Les calculatrices
Stockage de chaleur solaire par sorption : Analyse et contrôle du système à partir de sa simulation dynamique
 Stockage de chaleur solaire par sorption : Analyse et contrôle du système à partir de sa simulation dynamique Kokouvi Edem N TSOUKPOE 1, Nolwenn LE PIERRÈS 1*, Lingai LUO 1 1 LOCIE, CNRS FRE3220-Université
Stockage de chaleur solaire par sorption : Analyse et contrôle du système à partir de sa simulation dynamique Kokouvi Edem N TSOUKPOE 1, Nolwenn LE PIERRÈS 1*, Lingai LUO 1 1 LOCIE, CNRS FRE3220-Université
Extraction Assistée par Ultrasons
 Extraction Assistée par Ultrasons Extraction par ultrasons au laboratoire Deux types d équipements à ultrasons sont couramment utilisés dans le laboratoire. Le premier est le bain de nettoyage à ultrasons
Extraction Assistée par Ultrasons Extraction par ultrasons au laboratoire Deux types d équipements à ultrasons sont couramment utilisés dans le laboratoire. Le premier est le bain de nettoyage à ultrasons
L inégale répartition de l énergie solaire est à l origine des courants atmosphériques
 L inégale répartition de l énergie solaire est à l origine des courants atmosphériques I/ Objectif : Dans la partie 2 du programme de seconde «enjeux planétaires contemporains : énergie et sol», sous partie
L inégale répartition de l énergie solaire est à l origine des courants atmosphériques I/ Objectif : Dans la partie 2 du programme de seconde «enjeux planétaires contemporains : énergie et sol», sous partie
Feuille de garde contenant les suppléments nationaux à la feuille des données de sécurités UE OLDO AKTIV OX
 Version 002 Révisée le: 26.03.1997 Feuille de garde contenant les suppléments nationaux à la feuille des données de sécurités UE OLDO AKTIV OX Total de pages (la feuille de garde inclus) : 5 1. IDENTIFICATON
Version 002 Révisée le: 26.03.1997 Feuille de garde contenant les suppléments nationaux à la feuille des données de sécurités UE OLDO AKTIV OX Total de pages (la feuille de garde inclus) : 5 1. IDENTIFICATON
PROPOSITION TECHNIQUE ET FINANCIERE
 Avenue des Etangs Narbonne, F-11100, France Votre correspondant : Romain CRESSON INRA Transfert Environnement Avenue des Etangs Narbonne, F-11100, France Tel: +33 (0)4 68 46 64 32 Fax: +33 (0)4 68 42 51
Avenue des Etangs Narbonne, F-11100, France Votre correspondant : Romain CRESSON INRA Transfert Environnement Avenue des Etangs Narbonne, F-11100, France Tel: +33 (0)4 68 46 64 32 Fax: +33 (0)4 68 42 51
NOTICE TECHNIQUE D INSTALLATION & D UTILISATION
 NOTICE TECHNIQUE D INSTALLATION & D UTILISATION Plafond filtrant Lumispace Il est important de lire attentivement cette notice avant la maintenance du plafond Lumispace Ce document doit être remis au client
NOTICE TECHNIQUE D INSTALLATION & D UTILISATION Plafond filtrant Lumispace Il est important de lire attentivement cette notice avant la maintenance du plafond Lumispace Ce document doit être remis au client
Périodiquement, nettoyer les surfaces de l unité pour les maintenir dans une condition sanitaire et ce, aussi souvent que nécessaire.
 Périodiquement, nettoyer les surfaces de l unité pour les maintenir dans une condition sanitaire et ce, aussi souvent que nécessaire. Laver les surfaces à l aide d une solution d eau tiède et de savon,
Périodiquement, nettoyer les surfaces de l unité pour les maintenir dans une condition sanitaire et ce, aussi souvent que nécessaire. Laver les surfaces à l aide d une solution d eau tiède et de savon,
LYCEE TECHNIQUE PIERRE EMILE MARTIN - 18 026 BOURGES ETUDE D UN TRAITEMENT DE SURFACE
 TP. TET LYCEE TECHNIQUE PIERRE EMILE MARTIN - 18 026 BOURGES GENIE ELECTROTECHNIQUE Durée : 3 heures Tp relais statique 10-11 RELAIS STATIQUE S.T.I. Pré-requis : Laboratoire des systèmes Cours sur les
TP. TET LYCEE TECHNIQUE PIERRE EMILE MARTIN - 18 026 BOURGES GENIE ELECTROTECHNIQUE Durée : 3 heures Tp relais statique 10-11 RELAIS STATIQUE S.T.I. Pré-requis : Laboratoire des systèmes Cours sur les
LA PERTE DE CONSCIENCE
 CES QUELQUES NOTIONS PEUVENT SAUVER DES VIES. PENSEZ Y SV D URGENCES Pompiers et service médical urgent : 100 Police : 101 L'HEMORRAGIE Comment reconnaître une hémorragie? Le sang s'écoule abondamment
CES QUELQUES NOTIONS PEUVENT SAUVER DES VIES. PENSEZ Y SV D URGENCES Pompiers et service médical urgent : 100 Police : 101 L'HEMORRAGIE Comment reconnaître une hémorragie? Le sang s'écoule abondamment
A QUOI SERT LE NIVEAU DE CUVE?
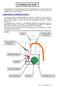 LE NIVEAU DE CUVE Les explications et les schémas qui suivent correspondent à ce que j ai compris du fonctionnement du carburateur MIKUNI qui équipe les BETA trial. Elles sont aussi valables pour les autres
LE NIVEAU DE CUVE Les explications et les schémas qui suivent correspondent à ce que j ai compris du fonctionnement du carburateur MIKUNI qui équipe les BETA trial. Elles sont aussi valables pour les autres
Sur une aire de stationnement, accessible par tranche de 50 places.
 Handicap : Les normes d'accessibilité La loi du 11 février 2005 est l'une des principales lois sur les droits des personnes handicapées, depuis la loi de 1975. Elle réaffirme que les locaux d habitation,
Handicap : Les normes d'accessibilité La loi du 11 février 2005 est l'une des principales lois sur les droits des personnes handicapées, depuis la loi de 1975. Elle réaffirme que les locaux d habitation,
L énergie sous toutes ses formes : définitions
 L énergie sous toutes ses formes : définitions primaire, énergie secondaire, utile ou finale. Quelles sont les formes et les déclinaisons de l énergie? D après le dictionnaire de l Académie française,
L énergie sous toutes ses formes : définitions primaire, énergie secondaire, utile ou finale. Quelles sont les formes et les déclinaisons de l énergie? D après le dictionnaire de l Académie française,
Enseignement secondaire
 Enseignement secondaire Classe de IIIe Chimie 3e classique F - Musique Nombre de leçons: 1.5 Nombre minimal de devoirs: 4 devoirs par an Langue véhiculaire: Français I. Objectifs généraux Le cours de chimie
Enseignement secondaire Classe de IIIe Chimie 3e classique F - Musique Nombre de leçons: 1.5 Nombre minimal de devoirs: 4 devoirs par an Langue véhiculaire: Français I. Objectifs généraux Le cours de chimie
ÉJECTEURS. CanmetÉNERGIE Juillet 2009
 ÉJECTEURS CanmetÉNERGIE Juillet 2009 ÉJECTEURS 1 ÉJECTEURS INTRODUCTION Les éjecteurs sont activés par la chaleur perdue ou la chaleur provenant de sources renouvelables. Ils sont actionnés directement
ÉJECTEURS CanmetÉNERGIE Juillet 2009 ÉJECTEURS 1 ÉJECTEURS INTRODUCTION Les éjecteurs sont activés par la chaleur perdue ou la chaleur provenant de sources renouvelables. Ils sont actionnés directement
VEILLE RÉGLEMENTAIRE Sécurité des personnes Fiche VRE.30
 VEILLE RÉGLEMENTAIRE Sécurité des personnes Fiche VRE.30 Incendie Code du Travail R4216-1 à R4216-7 ; R4216-11 à R4216-34 Code du Travail R4225-8 Code du Travail R4227-34 à R4227-36 Code du Travail R4227-1
VEILLE RÉGLEMENTAIRE Sécurité des personnes Fiche VRE.30 Incendie Code du Travail R4216-1 à R4216-7 ; R4216-11 à R4216-34 Code du Travail R4225-8 Code du Travail R4227-34 à R4227-36 Code du Travail R4227-1
UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure
 UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure APPEL D OFFRES OUVERT SUR OFFRES DE PRIX 08/ENS/24 BORDEREAU DES PRIX-DETAIL ESTIMATIF Lot n 2 : Achat et installation de matériel pour l enseignement
UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure APPEL D OFFRES OUVERT SUR OFFRES DE PRIX 08/ENS/24 BORDEREAU DES PRIX-DETAIL ESTIMATIF Lot n 2 : Achat et installation de matériel pour l enseignement
A Global Solution For Green Buildings.
 A Global Solution For Green Buildings. www.greenfumehood.com an product SORBONNES GREENFUMEHOOD Sécurité, performance, économies d énergie et respect de l environnement ehood m u F n e Gre tre des concen
A Global Solution For Green Buildings. www.greenfumehood.com an product SORBONNES GREENFUMEHOOD Sécurité, performance, économies d énergie et respect de l environnement ehood m u F n e Gre tre des concen
Mesure de la teneur en alcool
 37 Mesure de la teneur en alcool 1 Rôle de l alcool dans les vins 285 1.1. Sur le plan organoleptique 285 1.2. Sur le plan biologique 285 1.3. Sur le plan réglementaire 285 1.4. Sur le plan commercial
37 Mesure de la teneur en alcool 1 Rôle de l alcool dans les vins 285 1.1. Sur le plan organoleptique 285 1.2. Sur le plan biologique 285 1.3. Sur le plan réglementaire 285 1.4. Sur le plan commercial
I. Introduction: L énergie consommée par les appareils de nos foyers est sous forme d énergie électrique, facilement transportable.
 DE3: I. Introduction: L énergie consommée par les appareils de nos foyers est sous forme d énergie électrique, facilement transportable. Aujourd hui, nous obtenons cette énergie électrique en grande partie
DE3: I. Introduction: L énergie consommée par les appareils de nos foyers est sous forme d énergie électrique, facilement transportable. Aujourd hui, nous obtenons cette énergie électrique en grande partie
FICHE DE DONNÉES DE SÉCURITÉ conformément au Règlement (CE) nº1907/2006 REACH Nom : KR-G KR-G
 KR-G Page 1 de 5 1. IDENTIFICATION DE LA SUBSTANCE/PRÉPARATION ET DE LA SOCIÉTÉ/ENTREPRISE 1.1 Identificateur de produit : Nom du produit : KR-G 1.2 Utilisations identifiées pertinentes de la substance
KR-G Page 1 de 5 1. IDENTIFICATION DE LA SUBSTANCE/PRÉPARATION ET DE LA SOCIÉTÉ/ENTREPRISE 1.1 Identificateur de produit : Nom du produit : KR-G 1.2 Utilisations identifiées pertinentes de la substance
LE CHAUFFAGE. Peu d entretien. Entretien. fréquent. Peu d entretien. Pas d entretien. Pas d entretien. Entretien. fréquent. Peu d entretien.
 LE CHAUFFAGE 1. LE CHAUFFAGE ELECTRIQUE Le chauffage électrique direct ne devrait être utilisé que dans les locaux dont l isolation thermique est particulièrement efficace. En effet il faut savoir que
LE CHAUFFAGE 1. LE CHAUFFAGE ELECTRIQUE Le chauffage électrique direct ne devrait être utilisé que dans les locaux dont l isolation thermique est particulièrement efficace. En effet il faut savoir que
Sommaire. Séquence 2. La pression des gaz. Séance 1. Séance 2. Séance 3 Peut-on comprimer de l eau? Séance 4 Je fais le point sur la séquence 2
 Sommaire La pression des gaz Séance 1 Comprimer de l air Séance 2 Mesurer la pression d un gaz Séance 3 Peut-on comprimer de l eau? Séance 4 Je fais le point sur la séquence 2 24 Cned, Physique - Chimie
Sommaire La pression des gaz Séance 1 Comprimer de l air Séance 2 Mesurer la pression d un gaz Séance 3 Peut-on comprimer de l eau? Séance 4 Je fais le point sur la séquence 2 24 Cned, Physique - Chimie
Herrebout-Vermander N.V. S.A.
 Pag. 1/5 Herrebout-Vermander N.V. S.A. Kuurne, mai 2002 rev. Janvier 2005 Le parquetteur est parti, et qu'est-ce qu'on fait maintenant Félicitations avec votre nouveau Le parquet est un revêtement de sol
Pag. 1/5 Herrebout-Vermander N.V. S.A. Kuurne, mai 2002 rev. Janvier 2005 Le parquetteur est parti, et qu'est-ce qu'on fait maintenant Félicitations avec votre nouveau Le parquet est un revêtement de sol
La gravure. *lagravureparvoiehumide *lagravuresèche
 La gravure Après avoir réalisé l étape de masquage par lithographie, il est alors possible d effectuer l étape de gravure. L étape de gravure consiste à éliminer toutes les zones non protégées par la résine
La gravure Après avoir réalisé l étape de masquage par lithographie, il est alors possible d effectuer l étape de gravure. L étape de gravure consiste à éliminer toutes les zones non protégées par la résine
MODE D EMPLOI DU DROPER FIELD 1000
 MODE D EMPLOI DU DROPER FIELD 1000 PROMOVET sarl ZAC de la Route de Beauraing, 1 08600 GIVET (France) info @ promovet.fr 1 / 10 Table des matières 1 Description du Droper Field 1000 2 2 Utilisation du
MODE D EMPLOI DU DROPER FIELD 1000 PROMOVET sarl ZAC de la Route de Beauraing, 1 08600 GIVET (France) info @ promovet.fr 1 / 10 Table des matières 1 Description du Droper Field 1000 2 2 Utilisation du
TS 31 ATTAQUE DE FOURMIS!
 FICHE 1 Fiche à destination des enseignants TS 31 ATTAQUE DE FOURMIS! Type d'activité ECE Notions et contenus du programme de Terminale S Compétences exigibles du programme de Terminale S TYPE ECE Evaluation
FICHE 1 Fiche à destination des enseignants TS 31 ATTAQUE DE FOURMIS! Type d'activité ECE Notions et contenus du programme de Terminale S Compétences exigibles du programme de Terminale S TYPE ECE Evaluation
PHYSIQUE Discipline fondamentale
 Examen suisse de maturité Directives 2003-2006 DS.11 Physique DF PHYSIQUE Discipline fondamentale Par l'étude de la physique en discipline fondamentale, le candidat comprend des phénomènes naturels et
Examen suisse de maturité Directives 2003-2006 DS.11 Physique DF PHYSIQUE Discipline fondamentale Par l'étude de la physique en discipline fondamentale, le candidat comprend des phénomènes naturels et
