NOTICE : INFORMATION DE L UTILISATEUR. GADOVIST 1,0 mmol/ml, solution injectable. Gadobutrol
|
|
|
- Violette Mathieu
- il y a 8 ans
- Total affichages :
Transcription
1 NOTICE : INFORMATION DE L UTILISATEUR GADOVIST 1,0 mmol/ml, solution injectable Gadobutrol Veuillez lire attentivement l'intégralité de cette notice avant d utiliser ce médicament car elle contient des informations importantes pour vous. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions, interrogez votre médecin ou la personne qui va vous administrer GADOVIST (le radiologue) ou le personnel de l hôpital / du centre d IRM. Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre radiologue. Ceci s applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4. Dans cette notice : 1. Qu'est-ce que GADOVIST 1,0 mmol/ml, solution injectable et dans quels cas est-il utilisé? 2. Quelles sont les informations à connaître avant d utiliser GADOVIST 1,0 mmol/ml, solution injectable? 3. Comment utiliser GADOVIST 1,0 mmol/ml, solution injectable? 4. Quels sont les effets indésirables éventuels? 5. Comment conserver GADOVIST 1,0 mmol/ml, solution injectable? 6. Informations supplémentaires. 1. QU EST-CE QUE GADOVIST 1,0 mmol/ml, solution injectable ET DANS QUELS CAS EST-IL UTILISE? Classe pharmacothérapeutique : Produit de contraste paramagnétique. GADOVIST est un produit de contraste destiné à l imagerie par résonance magnétique (IRM) à visée diagnostique des territoires crâniens, rachidiens et des vaisseaux. GADOVIST peut aussi aider le médecin à caractériser le type d anomalie (bénigne ou maligne) connue ou suspectée dans le foie ou les reins. GADOVIST peut également être utilisé pour l IRM des anomalies d autres régions du corps. Il facilite la visualisation des structures ou des lésions anormales et aide à différencier les tissus sains des tissus malades. Il est indiqué chez les adultes et les enfants de tout âge (y compris les nouveau-nés à terme). Comment agit GADOVIST L IRM est une technique d imagerie médicale à visée diagnostique basée sur les différences de réaction des molécules d eau entre les tissus normaux et les tissus anormaux. Cet examen est réalisé avec un système complexe utilisant un champ magnétique et des ondes radio. Un ordinateur enregistre l activité et la traduit sous forme d images. GADOVIST est administré par injection dans une veine. Ce médicament est à usage diagnostique uniquement et ne vous sera administré que par des professionnels de santé ayant l expérience de la pratique clinique de l IRM. 2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D UTILISER GADOVIST 1,0 mmol/ml, solution injectable? N utilisez JAMAIS GADOVIST 1,0 mmol/ml, solution injectable si : Date de mise à jour : Page 1 sur 10
2 vous êtes allergique au gadobutrol ou à l un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6). Avertissements et précautions : Prévenez votre médecin avant que GADOVIST 1,0 mmol/ml solution injectable ne vous soit administré, si : vous souffrez d une allergie ou si vous avez des antécédents d allergie (par exemple, rhume des foins, urticaire) ou d asthme, vous avez des antécédents de réaction à un quelconque produit de contraste, vous présentez une fonction rénale altérée, vous souffrez d une maladie cérébrale avec convulsions (troubles épileptiques) ou d une autre maladie du système nerveux, vous portez un stimulateur cardiaque (pacemaker) ou si vous avez un implant ou des agrafes contenant du fer dans votre corps. Votre médecin décidera si l examen peut être réalisé ou non. Des réactions de type allergique pouvant entraîner des problèmes cardiaques, des difficultés à respirer ou des réactions au niveau de la peau peuvent survenir après l utilisation de GADOVIST. La survenue de réactions graves est possible. La plupart de ces réactions surviennent dans la demi-heure suivant l administration de GADOVIST, c est pourquoi vous serez gardé(e) en observation après l examen. Des cas de réactions retardées (survenant de quelques heures à plusieurs jours suivant l administration) ont été rapportés (voir la rubrique 4). Reins/Foie Prévenez votre médecin si vos reins ne fonctionnent pas correctement, vous avez récemment bénéficié ou allez prochainement bénéficier d une greffe du foie. Votre médecin peut vous prescrire un examen sanguin afin de vérifier le fonctionnement de vos reins avant de prendre la décision de vous prescrire GADOVIST, particulièrement si vous êtes âgé de 65 ans ou plus. Nouveau-nés et nourrissons En raison de l immaturité de la fonction rénale des nouveau-nés jusqu à l âge de 4 semaines et des nourrissons jusqu à l âge d un an, GADOVIST ne doit être administré à ces patients qu après un examen approfondi de la situation par le médecin. Autres médicaments et GADOVIST Informez votre médecin si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament. Grossesse et allaitement Demandez conseil à votre médecin avant de prendre tout médicament. Grossesse Vous devez prévenir votre médecin si vous pensez être enceinte ou si vous envisagez de l être car GADOVIST ne doit pas être administré au cours de la grossesse, sauf en cas de stricte nécessité. Allaitement Prévenez votre médecin si vous allaitez ou prévoyez d allaiter. Votre médecin déterminera avec vous si vous pouvez poursuivre l allaitement ou si vous devez l interrompre pendant une période de 24 heures après l administration de GADOVIST. GADOVIST 1,0 mmol/ml, solution injectable contient du sodium : Date de mise à jour : Page 2 sur 10
3 Ce médicament contient moins de 23 mg de sodium par dose (calculé pour une dose moyenne administrée à une personne de 70 kg) c est-à-dire qu il est «pratiquement sans sel». 3. COMMENT UTILISER GADOVIST 1,0 mmol/ml, solution injectable? GADOVIST est injecté dans une veine à l aide d une petite aiguille par un professionnel de santé. Votre IRM peut commencer immédiatement. Après l injection, vous serez gardé(e) en observation pendant au moins une demi-heure. Posologie usuelle La dose de GADOVIST la mieux adaptée pour vous dépendra de votre poids ainsi que de la partie du corps examinée par IRM: Chez l adulte, une seule injection de 0,1 millilitre de GADOVIST par kilogramme de masse corporelle est généralement suffisante (pour une personne de 70 kg, la dose est donc de 7 millilitres), cependant une injection supplémentaire pouvant aller jusqu à 0,2 millilitre par kg de masse corporelle pourra vous être administrée dans les 30 minutes suivant la première injection. La dose totale pouvant être administrée est de 0,3 millilitre de GADOVIST par kg de masse corporelle. De plus amples renseignements concernant l'administration et la manipulation de GADOVIST sont donnés à la fin de la notice. Utilisation dans des populations particulières L'utilisation de GADOVIST n est pas recommandée chez les patients qui ont des troubles rénaux sévères et chez les patients qui ont récemment eu ou doivent prochainement bénéficier d une greffe du foie. Si l administration de GADOVIST est cependant nécessaire, vous ne devrez recevoir qu une seule dose au cours d un examen et ne pas faire l objet d un second examen IRM avec injection de produit de contraste avant au moins sept jours. Utilisation chez les nouveau-nés, nourrissons, enfants et adolescents Chez les enfants de tout âge (y compris les nouveau-nés à terme), une seule dose de 0,1 millilitre de GADOVIST par kg de masse corporelle est recommandée pour tout examen (voir rubrique 1). En raison de l immaturité de la fonction rénale chez le nouveau-né jusqu à l âge de 4 semaines et chez le nourrisson jusqu à l âge d un an, GADOVIST ne doit être administré qu après un examen approfondi de la situation par le médecin. Les nouveau-nés et les nourrissons ne doivent recevoir qu une seule dose au cours d un examen et ne pas faire l objet d un second examen IRM avec injection de produit de contraste avant au moins sept jours. Sujets âgés Il n est pas nécessaire d adapter la dose si vous avez 65 ans ou plus, mais une analyse de sang pourra être faite afin de vérifier le fonctionnement de vos reins. Si vous avez reçu plus de GADOVIST 1.0 mmol/ml, solution injectable que vous n auriez dû: Le risque de surdosage est peu probable. En cas de surdosage, le médecin instaurera un traitement des symptômes associés et pourra recourir à une hémodialyse pour éliminer GADOVIST de votre organisme. Il n a pas été établi que l hémodialyse puisse prévenir le risque de Fibrose Systémique Néphrogénique (FSN ; voir rubrique 4) ni la traiter. Dans certains cas, le médecin contrôlera votre coeur. Date de mise à jour : Page 3 sur 10
4 Si vous avez d'autres questions sur l'utilisation de ce médicament, demandez plus d informations à votre médecin ou votre radiologue. 4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS? Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, bien que tout le monde n y soit pas sujet. Les effets indésirables les plus graves (ayant mis en jeu le pronostic vital ou ayant eu une issue fatale dans certains cas) sont : le cœur qui s arrête de battre (arrêt cardiaque) et les réactions sévères de type allergique (anaphylactoïdes) incluant arrêt respiratoire et choc anaphylactoïde. De plus, pour les effets indésirables suivants, des évolutions fatales ou ayant mis en jeu le pronostic vital ont été observées dans certains cas: Essoufflement (dyspnée), perte de conscience, réactions sévères de type allergique, baisse importante de la pression artérielle pouvant aller jusqu au collapsus, arrêt respiratoire, liquide dans les poumons, gonflement de la bouche et de la gorge, pression artérielle basse. Dans de rares cas : des réactions de type allergique (hypersensibilité et anaphylaxie) peuvent se produire, y compris des réactions sévères (choc anaphylactique) nécessitant une prise en charge médicale immédiate. Si vous remarquez: un gonflement du visage, des lèvres, de la langue ou de la gorge, une toux et des éternuements, des difficultés à respirer, des démangeaisons, un écoulement nasal, une urticaire (éruption cutanée ressemblant à celle d une piqûre d orties) veuillez prévenir immédiatement le personnel du service d IRM. Ces symptômes peuvent être les premiers signes d une réaction sévère. Votre examen pourra être interrompu et vous pourrez nécessiter un traitement supplémentaire. Des réactions de type allergique retardées, survenant quelques heures à plusieurs jours après que vous ayez reçu GADOVIST, ont été observées dans de rares cas. Si vous présentez une telle réaction, prévenez immédiatement votre médecin ou votre radiologue. Les effets indésirables les plus fréquemment observés (survenant chez 5 patients sur 1000 ou plus) sont : des maux de tête, une sensation de malaise (nausées) et des étourdissements. La plupart des effets indésirables sont légers à modérés. Les effets indésirables éventuels qui ont été observés lors des études cliniques avant la commercialisation de GADOVIST sont listés ci-dessous, selon leur probabilité de survenue : Fréquents (pouvant affecter jusqu à 1 personne sur 10) maux de tête, sensation de malaise (nausées). Peu fréquents (pouvant affecter jusqu à 1 personne sur 100) réactions de type allergique, par exemple : Date de mise à jour : Page 4 sur 10
5 - pression artérielle basse, - urticaire, - gonflement du visage, - gonflement (œdème) des paupières, - bouffées de chaleur. La fréquence des réactions de type allergique suivantes est inconnue : - réaction de type allergique sévère (choc anaphylactoïde), - baisse importante de la pression artérielle pouvant mener à un collapsus (choc), - arrêt respiratoire, - liquide dans les poumons, - difficultés à respirer (bronchospasme), - bleuissement des lèvres, - gonflement de la bouche et de la gorge, - gonflement de la gorge, - augmentation de la pression artérielle, - douleurs dans la poitrine, - gonflement du visage, de la gorge, de la bouche, des lèvres et/ou de la langue (angioœdème), - conjonctivite, - augmentation de la transpiration, - toux, - éternuements, - sensation de brûlures, - pâleur de la peau (pâleur), étourdissements, troubles du goût, engourdissement et fourmillement, essoufflement (dyspnée), vomissements, rougeur de la peau (érythème), démangeaisons (prurit incluant un prurit généralisé), éruption cutanée (incluant éruption cutanée généralisée, taches rouges petites et plates [rash maculaire], petites lésions surélevées et limitées [rash papulaire], éruption qui démange [rash prurigineux]), réactions diverses au point d injection (par exemple : débordement vers les tissus environnants, brûlure, froid, chaud, rougeur, rash, douleur ou bleus), sensation de chaleur. Rares (pouvant affecter jusqu à 1 personne sur 1000) évanouissement, convulsions, troubles de l odorat, accélération du rythme cardiaque, palpitations, bouche sèche, sensation générale de malaise (malaise), sensation de froid. Autres effets indésirables rapportés après l autorisation de mise sur le marché de GADOVIST avec une fréquence indéterminée (la fréquence ne peut pas être évaluée à partir des données disponibles) : cœur qui s arrête de battre (arrêt cardiaque), des cas de fibrose systémique néphrogénique FSN (durcissement de la peau qui peut également affecter les tissus mous et les organes internes) ont été rapportés. Date de mise à jour : Page 5 sur 10
6 Des variations des tests sanguins de la fonction rénale (par exemple, augmentation de la créatinine sérique) ont été observées après l'administration de GADOVIST. Déclaration des effets secondaires Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre radiologue. Ceci s applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via l Agence nationale de sécurité du médicament et des produits de santé (Ansm) et le réseau des Centres Régionaux de Pharmacovigilance. Site internet: En signalant les effets indésirables, vous contribuez à fournir davantage d informations sur la sécurité du médicament. 5. COMMENT CONSERVER GADOVIST 1,0 mmol/ml, solution injectable? Tenir ce médicament hors de la vue et de la portée des enfants. N utilisez pas ce médicament après la date de péremption indiquée sur l étiquette et sur l'étui en carton après «EXP». La date de péremption fait référence au dernier jour du mois. Ce médicament ne requiert pas de conditions particulières de stockage. La stabilité physico-chimique et microbiologique du produit après ouverture a été démontrée pendant 24 heures à C. Toutefois, d un point de vue microbiologique, il est préférable d utiliser le produit immédiatement. Ce médicament est une solution limpide, incolore à jaune pâle. Ne l 'utilisez pas en cas de changement important de coloration, de présence de particules ou si l emballage apparaît défectueux. Les médicaments ne doivent pas être jetés au tout-à-l égout ou avec les ordures ménagères. Le professionnel de santé éliminera ce médicament lorsqu il ne sera plus utilisé. Ces mesures permettront de protéger l environnement. 6. INFORMATIONS SUPPLEMENTAIRES Ce que contient GADOVIST 1,0 mmol/ml, solution injectable? La substance active est : le gadobutrol. 1 ml de solution injectable contient 604,72 mg de gadobutrol (correspondant à 1,0 mmol de gadobutrol contenant 157,25 mg de gadolinium). 1 flacon de 2 ml contient 1209,44 mg de gadobutrol, 1 flacon de 7,5 ml contient 4535,4 mg de gadobutrol, 1 flacon de 15 ml contient 9070,8 mg de gadobutrol, 1 flacon de 30 ml contient 18141,6 mg de gadobutrol. 1 flacon de 65 ml contient 39306,8 mg de gadobutrol. Les autres composants sont : le calcobutrol sodique (voir fin de la rubrique 2), le trométamol, l acide chlorhydrique 1N et l eau pour préparations injectables. Qu est-ce que GADOVIST 1,0 mmol/ml, solution injectable et contenu de l emballage extérieur? GADOVIST est une solution injectable limpide, incolore à jaune pâle. Chaque boîte contient : 1 ou 3 flacons de 2 ml de solution injectable, 1 ou 10 flacons de 7,5, 15 ou 30 ml de solution injectable, Date de mise à jour : Page 6 sur 10
7 1 ou 10 flacons contenant 65 ml de solution injectable (en flacons de 100 ml). Toutes les présentations peuvent ne pas être commercialisées. Titulaire BAYER HEALTHCARE 220 Avenue de la Recherche LOOS FRANCE Exploitant BAYER HEALTHCARE 220 Avenue de la Recherche LOOS FRANCE Fabricant BAYER PHARMA AG Müllerstrasse Berlin ALLEMAGNE Ce médicament est autorisé dans les Etats Membres de l'espace Economique Européen sous les noms suivants : Allemagne, Autriche Belgique, Danemark, Finlande, Grèce, Italie, Luxembourg, Norvège, Portugal, Suède Croatie Espagne France Irlande Pays-Bas Royaume-Uni GADOVIST 1,0 mmol/ml Injektionslösung GADOVIST Gadovist 1,0 mmol/ml otopina za injekciju GADOVIST 1 mmol/ml solución inyectable en vial GADOVIST 1,0 mmol/ml, solution injectable GADOVIST 1,0 mmol/ml Solution for Injection GADOVIST 1,0 mmol/ml, oplossing voor injectie GADOVIST 1.0 mmol/ml solution for injection La dernière date à laquelle cette notice a été révisée est Août Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l Ansm (France) Les informations suivantes sont destinées exclusivement aux professionnels de santé: - Insuffisance rénale Avant l administration de GADOVIST, il est recommandé de procéder à des examens de laboratoire chez tous les patients afin de rechercher une altération de la fonction rénale. Des cas de fibrose systémique néphrogénique (FSN) ont été rapportés après injection de certains produits de contraste contenant du gadolinium chez des patients ayant une insuffisance rénale sévère aiguë ou chronique (clairance de la créatinine < 30 ml/min/ 1, 73 m²). Les patients devant bénéficier d une transplantation hépatique sont particulièrement à risque, car l incidence de l insuffisance rénale aiguë est élevée dans ce groupe. Etant donné qu il est possible que des cas de FSN surviennent avec Date de mise à jour : Page 7 sur 10
8 GADOVIST, ce produit ne doit être administré aux patients présentant une insuffisance rénale sévère ou aux patients durant la période pré ou post-opératoire d une transplantation hépatique qu après une évaluation approfondie du rapport bénéfice/risque et que si le diagnostic est indispensable et ne peut être obtenu par d autres moyens que l IRM avec injection de gadolinium. S il est nécessaire d administrer GADOVIST, la dose ne doit pas excéder 0,1 mmol/kg de masse corporelle. Ne pas administrer plus d une dose au cours de l examen IRM. En raison du manque d information sur les administrations répétées, les injections de GADOVIST ne doivent pas être réitérées sauf si l intervalle entre les injections est d au moins 7 jours. L élimination rénale de gadobutrol pouvant être altérée chez les sujets âgés, il est particulièrement important de rechercher un dysfonctionnement rénal chez les sujets âgés de 65 ans et plus. La réalisation d une hémodialyse peu de temps après l administration de GADOVIST pourrait faciliter l élimination de ce produit de l organisme. Il n est pas établi que l instauration d une hémodialyse puisse prévenir ou traiter la FSN chez les patients qui ne sont pas déjà hémodialysés. - Grossesse et allaitement GADOVIST ne doit pas être utilisé pendant la grossesse à moins que la situation clinique de la patiente ne nécessite l administration de gadobutrol. Le médecin et la mère allaitante doivent décider s il faut poursuivre l allaitement ou le suspendre pendant les 24 heures suivant l administration de GADOVIST. - Réactions d hypersensibilité Comme pour les autres agents de contraste administrés par voie intraveineuse, l utilisation de GADOVIST peut s accompagner de réactions anaphylactoïdes/d hypersensibilité ou d autres réactions idiosyncrasiques, se traduisant par des manifestations cardiovasculaires, respiratoires ou cutanées, potentiellement sévères, allant même jusqu au choc. Les patients souffrant de maladies cardio-vasculaires sont plus susceptibles que les autres de présenter une évolution grave ou fatale lors d une réaction d hypersensibilité sévère. Le risque de développer des réactions d hypersensibilité peut être augmenté en cas : - de précédente réaction aux produits de contraste, - d antécédents d asthme bronchique, - d antécédents de troubles allergiques. Chez les patients présentant un terrain allergique, la décision d utiliser GADOVIST ne doit être prise qu après une évaluation particulièrement attentive du rapport bénéfice/risque. La plupart de ces réactions surviennent dans la demi-heure suivant l administration. Aussi, il est recommandé de garder le patient en observation après examen. Il est impératif d avoir à disposition le traitement médicamenteux nécessaire à la prise en charge de réactions d hypersensibilité; il faut également être prêt pour la mise en place immédiate de mesures d urgence. Des réactions retardées (de quelques heures à plusieurs jours après l administration) ont été rarement observées. - Troubles épileptiques Comme avec les autres produits de contraste contenant du gadolinium, des précautions particulières s'imposent en cas de seuil épileptogène bas. - Surdosage Date de mise à jour : Page 8 sur 10
9 En cas de surdosage accidentel, une surveillance cardiovasculaire (incluant un ECG) et un contrôle de la fonction rénale sont recommandés à titre de précaution. En cas de surdosage chez les patients présentant une insuffisance rénale, GADOVIST peut être éliminé par hémodialyse. Après 3 séances d hémodialyse, environ 98 % de l agent de contraste est éliminé du corps. Toutefois, il n est pas démontré que l hémodialyse soit appropriée dans la prévention de la fibrose systémique néphrogénique (FSN). - Avant l injection : Ce produit n est destiné qu à un usage unique. Ce médicament est une solution limpide, incolore à jaune pâle. Elle doit être contrôlée visuellement juste avant utilisation. GADOVIST ne doit pas être utilisé en cas de changement important de coloration, de présence de particules ou d emballage défectueux. - Instructions d utilisation GADOVIST ne doit être prélevé dans la seringue qu'immédiatement avant utilisation. Le bouchon de caoutchouc ne doit jamais être perforé plus d une fois. Tout produit de contraste restant après un examen doit être éliminé. Si le produit de contraste doit être administré à l'aide d'un injecteur automatique, sa compatibilité avec l'utilisation envisagée doit être démontrée par le fabricant du dispositif médical. Les instructions complémentaires des fabricants des appareils utilisés doivent être rigoureusement respectées. Toute solution restante, non utilisée après un examen, doit être jetée conformément aux réglementations nationales en vigueur. Durée de conservation après première ouverture du récipient Il faut jeter toute solution injectable qui n a pas été utilisée lors d un examen. La stabilité physico-chimique et microbiologique du produit après ouverture a été démontrée pendant 24 heures à C. Toutefois, d'un point de vue microbiologique, il est préférable d utiliser le produit immédiatement. S'il n'est pas utilisé immédiatement, la durée et les conditions de conservation jusqu'à l'utilisation sont de la seule responsabilité de l'utilisateur. L étiquette détachable de traçabilité placée sur les flacons doit être collée dans le dossier du patient afin de permettre la traçabilité du produit de contraste à base de gadolinium administré. La dose administrée doit également être enregistrée. En cas d utilisation de dossier médical électronique, le nom du produit, le numéro de lot et la dose administrée doivent être enregistrés dans le dossier du patient. Posologie Adultes Indications dans le SNC : La dose recommandée chez l adulte est de 0,1 mmol par kg de masse corporelle (mmol/kg), ce qui équivaut à 0,1 ml/kg de la solution à 1,0 M. En cas de forte suspicion clinique d une lésion non confirmée à l IRM ou si des informations plus précises peuvent modifier la prise en charge thérapeutique du patient, une seconde injection pouvant aller jusqu à 0,2 ml/kg au maximum peut être effectuée dans les 30 minutes suivant la première injection. Date de mise à jour : Page 9 sur 10
10 IRM du corps entier (à l exception de l Angiographie par Résonance Magnétique) : De manière générale, l administration de 0,1 ml de GADOVIST par kg de masse corporelle est suffisante pour apporter une réponse à la question clinique. Angiographie par Résonance Magnétique : Image d'un seul champ d'acquisition: 7,5 ml pour un patient de moins de 75 kg, 10 ml pour un patient de 75 kg et plus (équivalent à 0,1-0,15 mmol/kg). Image de plusieurs champs d acquisition: 15 ml pour un patient de moins de 75 kg, 20 ml pour un patient de 75 kg ou plus (équivalent à 0,2-0,3 mmol/kg). Population pédiatrique Pour les enfants de tout âge (y compris les nouveau-nés à terme), la dose recommandée est de 0,1 mmol de gadobutrol par kg de masse corporelle (équivalent à 0,1 ml de GADOVIST par kg de masse corporelle) pour toutes les indications (voir rubrique 1). En raison de l immaturité de la fonction rénale chez le nouveau-né jusqu à l âge de 4 semaines et chez le nourrisson jusqu à l âge d un an, GADOVIST ne doit être administré à ces patients qu après un examen approfondi de la situation et à une dose n excédant pas 0,1 mmol/kg de masse corporelle. Ne pas administrer plus d une dose au cours de l examen IRM. En raison du manque d information sur les administrations répétées, les injections de GADOVIST ne doivent pas être réitérées sauf si l intervalle entre les injections est d au moins 7 jours. Imagerie La dose nécessaire est administrée en bolus par voie intraveineuse. L examen IRM avec rehaussement du contraste peut débuter immédiatement après l injection (dans un délai dépendant des séquences d IRM utilisées et du protocole d examen). Le rehaussement optimal du signal est observé pendant le premier passage artériel en angiographie par résonance magnétique et dans les 15 minutes suivant l injection de GADOVIST pour les indications du SNC (ce délai dépendant du type de lésion ou de tissu). Les séquences pondérées en T1 sont particulièrement adaptées aux examens avec injection d un produit de contraste gadoliné. De plus amples renseignements concernant l utilisation de GADOVIST sont donnés à la rubrique 3 de la notice. Date de mise à jour : Page 10 sur 10
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR. Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant
 B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
PIL Décembre 2009. Autres composants: acide tartrique, macrogol 4000, macrogol 1000, macrogol 400, butylhydroxyanisol.
 Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique PERDOLAN - PÉDIATRIE
 Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
NOTICE : INFORMATION DE L'UTILISATEUR. DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc
 NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
NOTICE: INFORMATION DE L UTILISATEUR. Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain)
 NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
Stelara (ustekinumab)
 Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine
 KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR. Delphi 0,1 % crème Acétonide de triamcinolone
 NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés Bisacodyl
 NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
Atrovent HFA 20 mcg/bouffée solution pour inhalation en flacon pressurisé (bromure d'ipratropium)
 NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
NOTICE: INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés. Bisacodyl
 NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
Résonance magnétique (IRM)
 (IRM) Le médecin a prescrit une résonance magnétique (IRM) et vous vous demandez en quoi consiste cet examen. Afin de répondre à vos questions, voici quelques informations. But de l examen Les examens
(IRM) Le médecin a prescrit une résonance magnétique (IRM) et vous vous demandez en quoi consiste cet examen. Afin de répondre à vos questions, voici quelques informations. But de l examen Les examens
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
NOTICE : INFORMATION DE L UTILISATEUR. Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés. sumatriptan
 NOTICE : INFORMATION DE L UTILISATEUR Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés sumatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament. - Gardez
NOTICE : INFORMATION DE L UTILISATEUR Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés sumatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament. - Gardez
NOTICE : INFORMATION DE L UTILISATEUR. Flunarizine
 NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
Exemple de Projet d Accueil Individualisé ELEVE CONCERNE
 Exemple de Projet d Accueil Individualisé Circulaire projet d accueil n 2003-135 du 08/09/2003 (Bulletin Officiel n 34 du 18/9/2003) Circulaire restauration scolaire n 2001-118 du 25/06/2001(BO Spécial
Exemple de Projet d Accueil Individualisé Circulaire projet d accueil n 2003-135 du 08/09/2003 (Bulletin Officiel n 34 du 18/9/2003) Circulaire restauration scolaire n 2001-118 du 25/06/2001(BO Spécial
Bien vous soigner. avec des médicaments disponibles sans ordonnance. juin 2008. Douleur. de l adulte
 Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
MONOGRAPHIE DE PRODUIT
 MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
NOTICE: INFORMATION DE L UTILISATEUR. Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl)
 NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
La Dysplasie Ventriculaire Droite Arythmogène
 1 La Dysplasie Ventriculaire Droite Arythmogène Document rédigé par l équipe pluridisciplinaire du centre de référence pour les maladies cardiaques héréditaires (Paris), en collaboration avec des patients
1 La Dysplasie Ventriculaire Droite Arythmogène Document rédigé par l équipe pluridisciplinaire du centre de référence pour les maladies cardiaques héréditaires (Paris), en collaboration avec des patients
Notice : Informations de l utilisateur. Pantomed 20 mg comprimés gastro-résistants. Pantoprazole
 Notice : Informations de l utilisateur Pantomed 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations
Notice : Informations de l utilisateur Pantomed 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations
Point d Information. Le PRAC a recommandé que le RCP soit modifié afin d inclure les informations suivantes:
 Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
NOTICE. ANSM - Mis à jour le : 25/03/2014. Dénomination du médicament. PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole
 NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
Humira Solution pour injection dans un injecteur prérempli
 Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
NOTICE: INFORMATION DE L UTILISATEUR. Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan
 NOTICE: INFORMATION DE L UTILISATEUR Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan Veuillez lire attentivement l'intégralité de cette notice avant
NOTICE: INFORMATION DE L UTILISATEUR Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan Veuillez lire attentivement l'intégralité de cette notice avant
NOTICE : INFORMATIONS DE L'UTILISATEUR. PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole
 NOTICE : INFORMATIONS DE L'UTILISATEUR PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole Veuillez lire attentivement l'intégralité de cette notice car elle contient des informations importantes
NOTICE : INFORMATIONS DE L'UTILISATEUR PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole Veuillez lire attentivement l'intégralité de cette notice car elle contient des informations importantes
1 La scintigraphie myocardique au Persantin ou Mibi Persantin
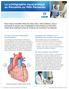 La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
QUESTIONNAIRE SUR LA SANTE RESPIRATOIRE ET ALLERGIQUE DES ECOLIERS ET LEUR ENVIRONNEMENT SCOLAIRE
 Santé et pollution intérieure dans les écoles : Réseau d observation en Europe QUESTIONNAIRE SUR LA SANTE RESPIRATOIRE ET ALLERGIQUE DES ECOLIERS ET LEUR ENVIRONNEMENT SCOLAIRE A compléter par les enfants
Santé et pollution intérieure dans les écoles : Réseau d observation en Europe QUESTIONNAIRE SUR LA SANTE RESPIRATOIRE ET ALLERGIQUE DES ECOLIERS ET LEUR ENVIRONNEMENT SCOLAIRE A compléter par les enfants
Conseils aux patients* Lutter activement. *pour les patients ayant subi une opération de remplacement de la hanche ou du genou
 Conseils aux patients* Lutter activement contre la thrombose *pour les patients ayant subi une opération de remplacement de la hanche ou du genou 2 Mentions légales Directeur de la publication : Bayer
Conseils aux patients* Lutter activement contre la thrombose *pour les patients ayant subi une opération de remplacement de la hanche ou du genou 2 Mentions légales Directeur de la publication : Bayer
La prise en charge de votre insuffisance cardiaque
 G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre insuffisance cardiaque Vivre avec une insuffisance cardiaque Décembre 2007 Pourquoi ce guide? Votre médecin traitant
G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre insuffisance cardiaque Vivre avec une insuffisance cardiaque Décembre 2007 Pourquoi ce guide? Votre médecin traitant
Notice : information de l utilisateur. Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine
 Notice : information de l utilisateur Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine Veuillez lire attentivement cette notice avant de prendre ce médicament
Notice : information de l utilisateur Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine Veuillez lire attentivement cette notice avant de prendre ce médicament
NOTICE : INFORMATION DE L UTILISATEUR. Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants. Acide acétylsalicylique
 NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
Bleu comme un Schtroumpf Démarche d investigation
 TP Bleu comme un Schtroumpf Démarche d investigation Règles de sécurité Blouse, lunettes de protection, pas de lentilles de contact, cheveux longs attachés. Toutes les solutions aqueuses seront jetées
TP Bleu comme un Schtroumpf Démarche d investigation Règles de sécurité Blouse, lunettes de protection, pas de lentilles de contact, cheveux longs attachés. Toutes les solutions aqueuses seront jetées
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013
 NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
NOTICE : INFORMATION DE L UTILISATEUR. Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés. ambrisentan
 NOTICE : INFORMATION DE L UTILISATEUR Version 17 Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés ambrisentan Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR Version 17 Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés ambrisentan Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR. Pantogastrix 20 mg comprimés gastro-résistants Pantoprazole
 NOTICE : INFORMATION DE L UTILISATEUR Pantogastrix 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations
NOTICE : INFORMATION DE L UTILISATEUR Pantogastrix 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations
Leucémies de l enfant et de l adolescent
 Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Conseils pour le traitement des douleurs persistantes
 Page -1- Conseils pour le traitement des douleurs persistantes Ce qu'il faut savoir avant tout, c'est que les douleurs persistantes sont des "douleurs particulières", qui doivent donc être traitées en
Page -1- Conseils pour le traitement des douleurs persistantes Ce qu'il faut savoir avant tout, c'est que les douleurs persistantes sont des "douleurs particulières", qui doivent donc être traitées en
Qu est-ce que la fibrillation auriculaire? (FA)
 Qu est-ce que la fibrillation auriculaire? (FA) Qu est-ce que la fibrillation auriculaire? La fibrillation auriculaire (FA) est le trouble du rythme le plus répandu. Certains signaux du cœur deviennent
Qu est-ce que la fibrillation auriculaire? (FA) Qu est-ce que la fibrillation auriculaire? La fibrillation auriculaire (FA) est le trouble du rythme le plus répandu. Certains signaux du cœur deviennent
NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine
 NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament.
NOTICE. DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine
 NOTICE ANSM Mis à jour le : 08/06/2010 Dénomination du médicament DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine Encadré Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE ANSM Mis à jour le : 08/06/2010 Dénomination du médicament DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine Encadré Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE. TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé
 NOTICE ANSM Mis à jour le : 15/07/2014 Dénomination du médicament Encadré TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient
NOTICE ANSM Mis à jour le : 15/07/2014 Dénomination du médicament Encadré TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient
Etablissement Français du Sang
 Etablissement Français du Sang LE LIEN ENTRE LA GÉNÉROSITÉ DES DONNEURS DE SANG ET LES BESOINS DES MALADES Document de préparation à l entretien médical préalable au don de sang Partie médicale La sécurité
Etablissement Français du Sang LE LIEN ENTRE LA GÉNÉROSITÉ DES DONNEURS DE SANG ET LES BESOINS DES MALADES Document de préparation à l entretien médical préalable au don de sang Partie médicale La sécurité
Vous et votre traitement anticoagulant par AVK (antivitamine K)
 Ce carnet a été réalisé sous la coordination de l Agence française de sécurité sanitaire des produits de santé (Afssaps). Vous et votre traitement anticoagulant par AVK (antivitamine K) Carte à découper
Ce carnet a été réalisé sous la coordination de l Agence française de sécurité sanitaire des produits de santé (Afssaps). Vous et votre traitement anticoagulant par AVK (antivitamine K) Carte à découper
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT
 IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
Notice : information de l utilisateur
 Notice : information de l utilisateur ALIMTA 100 mg poudre pour solution à diluer pour perfusion ALIMTA 500 mg poudre pour solution à diluer pour perfusion Pemetrexed Veuillez lire attentivement l'intégralité
Notice : information de l utilisateur ALIMTA 100 mg poudre pour solution à diluer pour perfusion ALIMTA 500 mg poudre pour solution à diluer pour perfusion Pemetrexed Veuillez lire attentivement l'intégralité
Un environnement sans fumée pour vos enfants. Comment y parvenir?
 Un environnement sans fumée pour vos enfants. Comment y parvenir? Renseignements sur la fumée secondaire et tertiaire Qu est-ce que la fumée secondaire? La fumée secondaire est une combinaison de fumée
Un environnement sans fumée pour vos enfants. Comment y parvenir? Renseignements sur la fumée secondaire et tertiaire Qu est-ce que la fumée secondaire? La fumée secondaire est une combinaison de fumée
La vaccination, une bonne protection
 Vaccin contre l hépatite A et l hépatite B La personne qui reçoit ce vaccin se protège contre l hépatite A, l hépatite B et leurs complications. L hépatite A et l hépatite B sont des infections du foie
Vaccin contre l hépatite A et l hépatite B La personne qui reçoit ce vaccin se protège contre l hépatite A, l hépatite B et leurs complications. L hépatite A et l hépatite B sont des infections du foie
MONOGRAPHIE. tocilizumab. Solution concentrée à 20 mg/ml pour perfusion. Solution à 162 mg/0,9 ml pour injection. Norme reconnue
 MONOGRAPHIE Pr ACTEMRA tocilizumab Solution concentrée à 20 mg/ml pour perfusion Solution à 162 mg/0,9 ml pour injection Norme reconnue Inhibiteur du récepteur d interleukine Le traitement par ACTEMRA
MONOGRAPHIE Pr ACTEMRA tocilizumab Solution concentrée à 20 mg/ml pour perfusion Solution à 162 mg/0,9 ml pour injection Norme reconnue Inhibiteur du récepteur d interleukine Le traitement par ACTEMRA
Repères. Gestion des défibrillateurs automatisés externes
 Repères Gestion des défibrillateurs automatisés externes Juin 2014 Défibrillateurs automatisés externes grand public : Recommandations à suivre Vous êtes une entreprise, une structure accueillant du public
Repères Gestion des défibrillateurs automatisés externes Juin 2014 Défibrillateurs automatisés externes grand public : Recommandations à suivre Vous êtes une entreprise, une structure accueillant du public
vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé)
 EMA/90006/2015 EMEA/H/C/001104 Résumé EPAR à l intention du public vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé) Le présent document est un résumé du rapport européen public d évaluation
EMA/90006/2015 EMEA/H/C/001104 Résumé EPAR à l intention du public vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé) Le présent document est un résumé du rapport européen public d évaluation
Le traitement du paludisme d importation de l enfant est une urgence
 Le traitement du paludisme d importation de l enfant est une urgence Dominique GENDREL Necker-Enfants Malades Traiter en urgence en présence de trophozoïtes Plus de 80% des paludismes d importation en
Le traitement du paludisme d importation de l enfant est une urgence Dominique GENDREL Necker-Enfants Malades Traiter en urgence en présence de trophozoïtes Plus de 80% des paludismes d importation en
NOTICE. PANTOPRAZOLE MYLAN CONSEIL 20 mg, comprimé gastro résistant
 NOTICE ANSM Mis à jour le : 05/09/2014 Dénomination du médicament Encadré PANTOPRAZOLE MYLAN CONSEIL 20 mg, comprimé gastro résistant Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE ANSM Mis à jour le : 05/09/2014 Dénomination du médicament Encadré PANTOPRAZOLE MYLAN CONSEIL 20 mg, comprimé gastro résistant Veuillez lire attentivement cette notice avant de prendre ce médicament.
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT 2. COMPOSITION QUALITATIVE ET QUANTITATIVE 3. FORME PHARMACEUTIQUE 4. DONNEES CLINIQUES 4.1. Indications thérapeutiques 4.2.
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT 2. COMPOSITION QUALITATIVE ET QUANTITATIVE 3. FORME PHARMACEUTIQUE 4. DONNEES CLINIQUES 4.1. Indications thérapeutiques 4.2.
Rougeole, Oreillons Rubéole et Coqueluche
 Rougeole, Oreillons Rubéole et Coqueluche Comment protéger vos enfants? La seule protection efficace : la vaccination R.O.R COQUELUCHE ANNUAIRE Livret élaboré en partenariat avec : Conseil Général du Loir-et-Cher
Rougeole, Oreillons Rubéole et Coqueluche Comment protéger vos enfants? La seule protection efficace : la vaccination R.O.R COQUELUCHE ANNUAIRE Livret élaboré en partenariat avec : Conseil Général du Loir-et-Cher
Votre guide des définitions des maladies graves de l Assurance maladies graves express
 Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
NOTICE : INFORMATIONS DU PATIENT. Keforal 500 mg comprimés pelliculés. Céfalexine monohydratée
 NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
L eau dans le corps. Fig. 6 L eau dans le corps. Cerveau 85 % Dents 10 % Cœur 77 % Poumons 80 % Foie 73 % Reins 80 % Peau 71 % Muscles 73 %
 24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE
 GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
The consent form is also available in English.
 Université McGill et hôpitaux affiliés Centre universitaire de santé McGill (CUSM) Hôpital général juif - Sir Mortimer B. Davis The Sir Mortimer B. Davis - Jewish General Hospital Centre hospitalier de
Université McGill et hôpitaux affiliés Centre universitaire de santé McGill (CUSM) Hôpital général juif - Sir Mortimer B. Davis The Sir Mortimer B. Davis - Jewish General Hospital Centre hospitalier de
Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène
 NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
MINISTERE DE LA SANTE ET DES SOLIDARITES DIRECTION GENERALE DE LA SANTE- DDASS DE SEINE MARITIME
 Département des situations d urgence sanitaire Personne chargée du dossier : Evelyne FALIP/Nicole BOHIC Tél : 01 40 56 59 65/02 32 18 31 66 evelyne.falip@sante.gouv.fr MINISTERE DE LA SANTE ET DES SOLIDARITES
Département des situations d urgence sanitaire Personne chargée du dossier : Evelyne FALIP/Nicole BOHIC Tél : 01 40 56 59 65/02 32 18 31 66 evelyne.falip@sante.gouv.fr MINISTERE DE LA SANTE ET DES SOLIDARITES
Le VIH et votre apparence physique
 Le VIH et votre apparence physique Le VIH et votre apparence physique Les personnes séropositives subissent-elles souvent des changements de l apparence physique? Il est difficile de dire avec exactitude
Le VIH et votre apparence physique Le VIH et votre apparence physique Les personnes séropositives subissent-elles souvent des changements de l apparence physique? Il est difficile de dire avec exactitude
MEDICAMENTS CONTENANT L ASSOCIATION DEXTROPROPOXYPHENE / PARACETAMOL :
 REPUBLIQUE FRANÇAISE Juin 2009 MEDICAMENTS CONTENANT L ASSOCIATION DEXTROPROPOXYPHENE / PARACETAMOL : Recommandation de l EMEA de retrait de ces médicaments à la suite de l évaluation européenne et avis
REPUBLIQUE FRANÇAISE Juin 2009 MEDICAMENTS CONTENANT L ASSOCIATION DEXTROPROPOXYPHENE / PARACETAMOL : Recommandation de l EMEA de retrait de ces médicaments à la suite de l évaluation européenne et avis
Protéger. son animal. la gamme FRONTLINE. grâce à la gamme. Contre les puces et les tiques. Efficace plusieurs semaines (1) Résistant à la pluie,
 la gamme Frontline Contre les puces et les tiques Efficace plusieurs semaines (1) Résistant à la pluie, aux bains et aux shampooings (2) Protéger son animal grâce à la gamme FRONTLINE La gamme FRONTLINE
la gamme Frontline Contre les puces et les tiques Efficace plusieurs semaines (1) Résistant à la pluie, aux bains et aux shampooings (2) Protéger son animal grâce à la gamme FRONTLINE La gamme FRONTLINE
Protégeons-nous ensemble!
 Grippe saisonnière. Protégeons-nous ensemble! Informations importantes pour vous et votre famille. www.sevaccinercontrelagrippe.ch www.ofsp.admin.ch B C Qu est-ce que la grippe saisonnière et quels en
Grippe saisonnière. Protégeons-nous ensemble! Informations importantes pour vous et votre famille. www.sevaccinercontrelagrippe.ch www.ofsp.admin.ch B C Qu est-ce que la grippe saisonnière et quels en
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
RECOMMANDATIONS OFFICIELLES - DEFIBRILLATEURS AUTOMATISES EXTERNES
 RECOMMANDATIONS OFFICIELLES - DEFIBRILLATEURS AUTOMATISES EXTERNES SOMMAIRE : Définitions DAE / DSA / DEA. Les accessoires recommandés. Notion de système d information pour les secours spécialisés. Les
RECOMMANDATIONS OFFICIELLES - DEFIBRILLATEURS AUTOMATISES EXTERNES SOMMAIRE : Définitions DAE / DSA / DEA. Les accessoires recommandés. Notion de système d information pour les secours spécialisés. Les
Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés
 Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Developé pour le Centre
Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Developé pour le Centre
Questionnaire Médical
 Nom et prénom(s) de l élève: Date de naissance: Questionnaire Médical Ce formulaire est à compléter, avant de commencer l année scolaire, pour les nouveaux élèves ainsi que pour les élèves poursuivant
Nom et prénom(s) de l élève: Date de naissance: Questionnaire Médical Ce formulaire est à compléter, avant de commencer l année scolaire, pour les nouveaux élèves ainsi que pour les élèves poursuivant
Comment ça va? Quand ça ne va pas. 4 comment ça va?
 Comment ça va? 1 Voici quatre dialogues. Dites à quelle situation de communication correspond chacun d eux. Situation a) : consultation chez un médecin. Situation b) : salutations dans la rue, par simple
Comment ça va? 1 Voici quatre dialogues. Dites à quelle situation de communication correspond chacun d eux. Situation a) : consultation chez un médecin. Situation b) : salutations dans la rue, par simple
Ce que les femmes enceintes doivent savoir au sujet de la grippe H1N1 (appelée grippe porcine auparavant)
 Ce que les femmes enceintes doivent savoir au sujet de la grippe H1N1 (appelée grippe porcine auparavant) 3 mai 2009, 15 h HNE Sur cette page : Que dois-je faire si je contracte ce nouveau virus et que
Ce que les femmes enceintes doivent savoir au sujet de la grippe H1N1 (appelée grippe porcine auparavant) 3 mai 2009, 15 h HNE Sur cette page : Que dois-je faire si je contracte ce nouveau virus et que
L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ
 L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ Plan de la présentation Introduction L enfant Le cathéter court La voie veineuse centrale La voie intra-osseuse Plan de la présentation Le
L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ Plan de la présentation Introduction L enfant Le cathéter court La voie veineuse centrale La voie intra-osseuse Plan de la présentation Le
Date: Avant de commencer, nous aimerions savoir à qui nous devons un immense MERCI! pour t avoir référé à nous
 1 457 route 105, unité 2 Chelsea (QC) J9B 1L2 (819) 827-4499 Fax : (819) 827-4459 Drmartine4kids@hotmail.com www.chelseachiro.com Formulaire pour les nouveaux Petits Date: Avant de commencer, nous aimerions
1 457 route 105, unité 2 Chelsea (QC) J9B 1L2 (819) 827-4499 Fax : (819) 827-4459 Drmartine4kids@hotmail.com www.chelseachiro.com Formulaire pour les nouveaux Petits Date: Avant de commencer, nous aimerions
NOTICE: INFORMATION DE L UTILISATEUR
 NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
Questionnaire santé et soins médicaux pour les moins de 16 ans
 _0_ An Vag Enq N adresse N individuel... Prénom Année de naissance (réservé enquêteur) Questionnaire santé et soins médicaux pour les moins de 6 ans Enquête sur la Santé et la Protection Sociale 00 Prénom
_0_ An Vag Enq N adresse N individuel... Prénom Année de naissance (réservé enquêteur) Questionnaire santé et soins médicaux pour les moins de 6 ans Enquête sur la Santé et la Protection Sociale 00 Prénom
Se préparer à une angiographie artérielle
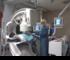 Se préparer à une angiographie artérielle Table des matières Sujet Page Qu est-ce que l athérosclérose?... 1 Durcissement graduel des artères (athérosclérose)... 2 Pourquoi dois-je subir une angiographie
Se préparer à une angiographie artérielle Table des matières Sujet Page Qu est-ce que l athérosclérose?... 1 Durcissement graduel des artères (athérosclérose)... 2 Pourquoi dois-je subir une angiographie
Anémie et maladie rénale chronique. Phases 1-4
 Anémie et maladie rénale chronique Phases 1-4 Initiative de qualité en matière d issue des maladies rénales de la National Kidney Foundation Saviez-vous que l initiative de qualité en matière d issue des
Anémie et maladie rénale chronique Phases 1-4 Initiative de qualité en matière d issue des maladies rénales de la National Kidney Foundation Saviez-vous que l initiative de qualité en matière d issue des
INFORMATION À DESTINATION DES PROFESSIONNELS DE SANTÉ LE DON DU VIVANT
 INFORMATION À DESTINATION DES PROFESSIONNELS DE SANTÉ LE DON DU VIVANT QUELS RÉSULTATS POUR LE RECEVEUR? QUELS RISQUES POUR LE DONNEUR? DONNER UN REIN DE SON VIVANT PEUT CONCERNER CHACUN /////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////
INFORMATION À DESTINATION DES PROFESSIONNELS DE SANTÉ LE DON DU VIVANT QUELS RÉSULTATS POUR LE RECEVEUR? QUELS RISQUES POUR LE DONNEUR? DONNER UN REIN DE SON VIVANT PEUT CONCERNER CHACUN /////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////
NOTICE : INFORMATION DU PATIENT. MAALOX CONTROL 20 mg comprimés gastro-résistants Pantoprazole
 NOTICE : INFORMATION DU PATIENT MAALOX CONTROL 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations
NOTICE : INFORMATION DU PATIENT MAALOX CONTROL 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations
Livret des nouveaux anticoagulants oraux. Ce qu il faut savoir pour bien gérer leur utilisation
 Livret des nouveaux anticoagulants oraux Ce qu il faut savoir pour bien gérer leur utilisation DONNÉES DU PATIENT Nom Adresse Tél MÉDECIN TRAITANT Nom Adresse Tél SPÉCIALISTE Nom Hôpital Tél MÉDICAMENT
Livret des nouveaux anticoagulants oraux Ce qu il faut savoir pour bien gérer leur utilisation DONNÉES DU PATIENT Nom Adresse Tél MÉDECIN TRAITANT Nom Adresse Tél SPÉCIALISTE Nom Hôpital Tél MÉDICAMENT
Le guide du bon usage des médicaments
 Le guide du bon usage des médicaments Les médicaments sont là pour vous aider mais......ils ont parfois du mal à vivre ensemble. Votre médecin et votre pharmacien peuvent adapter votre traitement pour
Le guide du bon usage des médicaments Les médicaments sont là pour vous aider mais......ils ont parfois du mal à vivre ensemble. Votre médecin et votre pharmacien peuvent adapter votre traitement pour
QU EST-CE QUE LA TUBERCULOSE?
 QU EST-CE QUE LA TUBERCULOSE? Information pour les patients TABLE DES MATIÈRES INTRODUCTION 1 LA TUBERCULOSE GÉNÉRALITÉS 1.1 Qu est-ce que la tuberculose? 1.2 La tuberculose est-elle toujours contagieuse?
QU EST-CE QUE LA TUBERCULOSE? Information pour les patients TABLE DES MATIÈRES INTRODUCTION 1 LA TUBERCULOSE GÉNÉRALITÉS 1.1 Qu est-ce que la tuberculose? 1.2 La tuberculose est-elle toujours contagieuse?
Notice : ROACCUTANE. AcnéFight. Consultez :
 Consultez : Notice : ROACCUTANE AcnéFight Retrouvez l évolution de mes traitements Roaccutane sur ce site : http://montraitementroaccutane.over-blog.com/ NOTICE : INFORMATION DE L UTILISATEUR ISOCURAL
Consultez : Notice : ROACCUTANE AcnéFight Retrouvez l évolution de mes traitements Roaccutane sur ce site : http://montraitementroaccutane.over-blog.com/ NOTICE : INFORMATION DE L UTILISATEUR ISOCURAL
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr ELIQUIS MD Comprimés d apixaban Le présent dépliant constitue la troisième dernière partie de la monographie publiée à la suite de l homologation d ELIQUIS
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr ELIQUIS MD Comprimés d apixaban Le présent dépliant constitue la troisième dernière partie de la monographie publiée à la suite de l homologation d ELIQUIS
L'œsophage L'œsophage est un tube musculaire qui traverse de la bouche à l'estomac. Causes
 L'œsophage est un tube musculaire qui traverse de la bouche à l'estomac. Chez l'adulte moyen, il fait 25 cm à 30 cm (10 po à 14 po) de long et environ 2 cm (moins d'un pouce) de large. L'œsophage est constitué
L'œsophage est un tube musculaire qui traverse de la bouche à l'estomac. Chez l'adulte moyen, il fait 25 cm à 30 cm (10 po à 14 po) de long et environ 2 cm (moins d'un pouce) de large. L'œsophage est constitué
http://agence-prd.ansm.sante.fr/php/ecodex/notice/n0230847.htm NOTICE IPRAALOX 20 mg, comprimé gastro-résistant Pantoprazole
 NOTICE ANSM - Mis à jr le : 30/09/2013 Dénomination du médicament IPRAALOX 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant de prendre ce médicament
NOTICE ANSM - Mis à jr le : 30/09/2013 Dénomination du médicament IPRAALOX 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant de prendre ce médicament
DIAMICRON MR (Gliclazide) Monographie de produit Page 1 de 5
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr DIAMICRON MR Gliclazide Comprimés à libération modifiée de 30 mg Comprimés sécables à libération modifiée de 60 mg Le présent dépliant constitue la troisième
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr DIAMICRON MR Gliclazide Comprimés à libération modifiée de 30 mg Comprimés sécables à libération modifiée de 60 mg Le présent dépliant constitue la troisième
EURO DEFI PADS 52502000IU9I 2012/10
 EURO DEFI PADS 52502000IU9I 2012/10 PLAQUES MULTI-FONCTIONS JETABLES EURODEFIPADS NOTICE D UTILISATION DESCRIPTION DU PRODUIT Les plaques multifonctions jetables EURODEFIPADS sont composées de deux électrodes
EURO DEFI PADS 52502000IU9I 2012/10 PLAQUES MULTI-FONCTIONS JETABLES EURODEFIPADS NOTICE D UTILISATION DESCRIPTION DU PRODUIT Les plaques multifonctions jetables EURODEFIPADS sont composées de deux électrodes
Maladie de Hodgkin ou lymphome de Hodgkin
 Maladie de Hodgkin ou lymphome de Hodgkin Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca MALADIE DE HODGKIN Ce que vous devez savoir Même si vous entendez parler du
Maladie de Hodgkin ou lymphome de Hodgkin Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca MALADIE DE HODGKIN Ce que vous devez savoir Même si vous entendez parler du
Pourquoi une femme-enceinte présente un certain nombre de douleurs inconnues jusqu'à lors?
 Pourquoi une femme-enceinte présente un certain nombre de douleurs inconnues jusqu'à lors? elle va pour cela créer des éléments chargées de transmettre un message à son corps (les hormones) : la «relaxine»
Pourquoi une femme-enceinte présente un certain nombre de douleurs inconnues jusqu'à lors? elle va pour cela créer des éléments chargées de transmettre un message à son corps (les hormones) : la «relaxine»
Diabète Type 2. Épidémiologie Aspects physiques Aspects physiologiques
 Diabète Type 2 Épidémiologie Aspects physiques Aspects physiologiques Épidémiologie 90% de tous les cas de diabètes Environ 1 personne sur 20 est atteinte Diabète gras Facteur de risque majeur pour les
Diabète Type 2 Épidémiologie Aspects physiques Aspects physiologiques Épidémiologie 90% de tous les cas de diabètes Environ 1 personne sur 20 est atteinte Diabète gras Facteur de risque majeur pour les
Traitements topiques. Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames. Soulagent les démangeaisons.
 SANS ORDONNANCE Solutions pour le bain et la douche : Huiles Farine d avoine Sels d Epsom Sels de al Mer Morte Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames.
SANS ORDONNANCE Solutions pour le bain et la douche : Huiles Farine d avoine Sels d Epsom Sels de al Mer Morte Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames.
NOTICE: INFORMATION DE L UTILISATEUR
 NOTICE: INFORMATION DE L UTILISATEUR MIGARD 2,5 mg comprimés pelliculés frovatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR MIGARD 2,5 mg comprimés pelliculés frovatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
Les différentes maladies du coeur
 Auteur : Dr Pascal AMEDRO Les différentes maladies du coeur 1. Le cœur normal L oxygène capté dans l air va dans les poumons, où le sang «bleu» est alors oxygéné et devient «rouge». Il est conduit par
Auteur : Dr Pascal AMEDRO Les différentes maladies du coeur 1. Le cœur normal L oxygène capté dans l air va dans les poumons, où le sang «bleu» est alors oxygéné et devient «rouge». Il est conduit par
Le don de moelle osseuse :
 DON DE MOELLE OSSEUSE Le don de moelle osseuse : se décider aujourd hui, s engager pour longtemps LA MOELLE OSSEUSE ET SA GREFFE La moelle osseuse C est le tissu mou dans le centre du corps des os qui
DON DE MOELLE OSSEUSE Le don de moelle osseuse : se décider aujourd hui, s engager pour longtemps LA MOELLE OSSEUSE ET SA GREFFE La moelle osseuse C est le tissu mou dans le centre du corps des os qui
Comprendre la mort cérébrale
 Comprendre la mort cérébrale Imprimeur de la Reine pour l Ontario, 2010. Adaptation et reproduction autorisées. 1 Comprendre la mort cérébrale Il est difficile d imaginer une expérience plus douloureuse
Comprendre la mort cérébrale Imprimeur de la Reine pour l Ontario, 2010. Adaptation et reproduction autorisées. 1 Comprendre la mort cérébrale Il est difficile d imaginer une expérience plus douloureuse
