Notice: Information de l utilisateur. Humalog 200 UI/ml, solution injectable en stylo prérempli insuline lispro
|
|
|
- Amandine Guérard
- il y a 8 ans
- Total affichages :
Transcription
1 Notice: Information de l utilisateur Humalog 200 UI/ml, solution injectable en stylo prérempli insuline lispro Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour vous. - Gardez cette notice. Vous pourriez avoir besoin de la relire. - Si vous avez d autres questions, interrogez votre médecin ou votre pharmacien. - Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres. - Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4. Que contient cette notice?: 1. Qu'est-ce qu Humalog 200 UI/ml KwikPen et dans quel cas est-il utilisé 2. Quelles sont les informations à connaître avant d'utiliser Humalog 200 UI/ml KwikPen 3. Comment utiliser Humalog 200 UI/ml KwikPen 4. Quels sont les effets indésirables éventuels 5. Comment conserver Humalog 200 UI/ml KwikPen 6. Contenu de l emballage et autres informations 1. Qu'est-ce qu Humalog 200 UI/ml KwikPen et dans quel cas est-il utilisé Humalog 200 UI/ml KwikPen est utilisé dans le traitement du diabète. Humalog agit plus rapidement que l'insuline humaine normale car l insuline lispro a été légèrement modifiée par rapport à l insuline humaine. L insuline lispro est étroitement apparentée à l insuline humaine qui est une hormone naturelle produite par le pancréas. Vous êtes diabétique lorsque votre pancréas ne produit pas suffisamment d'insuline pour réguler le niveau de glucose dans votre sang. Humalog remplace votre propre insuline et assure un contrôle du glucose à long terme. Son action est très rapide et plus courte que celle d'une insuline rapide (2 à 5h). Vous utiliserez normalement Humalog 15 minutes avant ou après un repas. Votre médecin peut vous prescrire Humalog 200 UI/ml KwikPen ainsi qu une insuline d'action plus prolongée. Une notice spécifique accompagne cette autre insuline. Ne changez pas d'insuline sauf sur prescription de votre médecin. Humalog 200 UI/ml KwikPen doit être réservé pour le traitement des adultes atteints de diabète nécessitant des doses quotidiennes de plus de 20 unités d'insuline à action rapide. 2. Quelles sont les informations à connaître avant d'utiliser Humalog 200 UI/ml KwikPen N utilisez JAMAIS Humalog 200 UI/ml KwikPen - Si vous êtes allergique à l insuline lispro ou à l un des autres composants contenus dans ce médicament mentionnés dans la rubrique 6. 1
2 - Si vous estimez qu'une hypoglycémie (abaissement du sucre dans le sang) est imminente. Il est indiqué plus loin dans cette notice comment prendre en charge une hypoglycémie légère (voir rubrique 3 : Si vous avez pris plus d Humalog que vous n auriez dû). Avertissements et précautions La solution injectable contenue dans votre stylo prérempli Humalog 200 UI/ml KwikPen doit être injectée UNIQUEMENT avec ce stylo prérempli. Ne pas transférer l insuline lispro dans une seringue à partir de votre Humalog 200 UI/ml KwikPen. Les graduations sur la seringue d'insuline n indiqueront pas correctement votre dose. Un surdosage grave peut survenir, entraînant un abaissement du sucre dans le sang, ce qui peut mettre votre vie en danger. Ne pas transférer l insuline de votre Humalog 200 UI/ml KwikPen dans tout autre dispositif d administration comme les pompes à insuline. NE PAS mélanger la solution injectable contenue dans votre stylo prérempli Humalog 200 UI/ml KwikPen avec tout autre insuline ou tout autre médicament. Humalog 200 UI/ml KwikPen solution injectable ne doit pas être dilué. Si votre glycémie est bien contrôlée par votre insuline actuelle, vous pourriez ne pas ressentir les symptômes annonciateurs de l'hypoglycémie. Ces symptômes sont énumérés à la rubrique 4 de cette notice. Réfléchissez soigneusement à l heure à laquelle vous prendrez vos repas, à la fréquence et à l intensité de vos exercices physiques. Vous devez étroitement surveiller les niveaux de sucre dans votre sang grâce à des tests fréquents de votre glycémie. Quelques patients ayant présenté des hypoglycémies après passage d'une insuline animale à une insuline humaine ont rapporté que les symptômes annonciateurs d hypoglycémie étaient moins prononcés ou différents de ceux provoqués par une insuline animale. En cas d'hypoglycémies fréquentes ou si vous avez des difficultés à les reconnaître, parlez-en avec votre médecin. Si vous répondez par l'affirmative à l'une des questions suivantes, informez-en votre médecin, pharmacien ou personnel infirmier. - Etes-vous récemment tombé malade? - Avez-vous des problèmes rénaux ou hépatiques? - Faites-vous davantage d'exercice que d'habitude? Si vous envisagez de vous rendre à l'étranger, pensez à en informer votre médecin, pharmacien ou personnel infirmier. Le décalage horaire pourrait vous contraindre à modifier vos heures d injection et de repas par rapport à vos heures habituelles. Certains patients avec un diabète de type II ancien et une maladie cardiaque ou un antécédent d accident vasculaire cérébral, qui étaient traités avec la pioglitazone et l insuline ont développé une insuffisance cardiaque. Informez votre médecin le plus rapidement possible si vous avez des signes d insuffisance cardiaque tels qu un essoufflement inhabituel ou une augmentation rapide de poids ou un gonflement localisé (œdème). Autres médicaments et Humalog 200 UI/ml KwikPen Vos besoins en insuline peuvent être différents si vous prenez une pilule contraceptive, des corticostéroïdes, un traitement substitutif par hormones thyroïdiennes, des hypoglycémiants oraux (par exemple, metformine, acarbose, sulfamides hypoglycémiants, pioglitazone, empagliflozine, inhibiteurs du DPP-4 tels que sitagliptine ou saxagliptine) de l acide acétylsalicylique, des sulfamides antibactériens, des analogues de la somatostatine (tels que octréotide, utilisée pour traiter une maladie peu fréquente liée à une sécrétion trop élevée d hormone de croissance) 2
3 des "bêta-2 stimulants" tels que salbutamol ou terbutaline pour traiter l asthme ou la ritodrine utilisée pour prévenir l accouchement prématuré, des bêtabloquants pour traiter l hypertension artérielle, ou certains antidépresseurs (inhibiteurs de la mono-amine oxydase ou inhibiteurs sélectifs de la recapture de la sérotonine), le danazol (médicament agissant sur l ovulation), certains inhibiteurs de conversion de l angiotensine, utilisés pour traiter certaines maladies du cœur ou l hypertension artérielle (ex. captopril, enalapril) et des médicaments spécifiques pour traiter l hypertension artérielle, les lésions rénales dues au diabète et certains problèmes cardiaques (antagonistes des récepteurs de l angiotensine II). Informez votre médecin si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament. (voir également la rubrique Avertissements et précautions ). Humalog avec de l alcool Vos niveaux de sucre dans le sang peuvent soit augmenter soit diminuer si vous buvez de l alcool. Par conséquent, la quantité d'insuline nécessaire, peut être modifiée. Grossesse et allaitement Etes-vous enceinte ou l'envisagez-vous? Allaitez-vous? Les besoins en insuline diminuent généralement durant les trois premiers mois de grossesse et augmentent au cours des six autres mois. Si vous allaitez, l'administration de votre insuline devra peut-être être adaptée ainsi que votre régime alimentaire. Demandez conseil à votre médecin avant de prendre tout médicament. Conduite de véhicules et utilisation de machines Vos capacités de concentration et vos réflexes peuvent être diminués en cas d hypoglycémie. Vous devez y penser dans toutes les situations où vous pourriez mettre votre vie en danger ou celle d autres personnes, comme la conduite automobile ou l utilisation de machines. Vous devez interroger votre médecin sur vos capacités à conduire si vous avez : de fréquents épisodes d hypoglycémie, des symptômes annonciateurs d hypoglycémie diminués ou absents. 3. Comment utiliser Humalog 200 UI/ml KwikPen Vérifiez toujours la désignation et le type d'insuline figurant sur le conditionnement et sur l'étiquette du stylo pré-rempli délivré par votre pharmacien. Assurez-vous que vous avez le stylo d Humalog 200 UI/ml KwikPen prescrit par votre médecin. Veillez à toujours prendre ce médicament en suivant exactement les indications de votre médecin. Vérifiez auprès de votre médecin en cas de doute. Humalog 200 UI/ml KwikPen est pour les patients prenant plus de 20 unités quotidiennes d insuline d action rapide. Ne pas transférer l insuline dans une seringue à partir de votre Humalog 200 UI/ml KwikPen. Les graduations sur la seringue d'insuline n indiqueront pas correctement la dose. Un surdosage grave peut survenir, entraînant un abaissement du sucre dans le sang, ce qui peut mettre votre vie en danger. 3
4 Ne pas utiliser Humalog 200 UI/ml KwikPen solution injectable dans une pompe à insuline. Posologie Vous devez normalement injecter Humalog dans les 15 minutes précédant ou suivant un repas. Si besoin, vous pouvez pratiquer l injection juste après le repas. Votre médecin vous aura avisé de la dose exacte de l'injection, de son heure et de sa fréquence. Ces consignes vous sont exclusivement réservées. Observez-les scrupuleusement et rendez-vous régulièrement chez votre médecin. Si vous changez de type d'insuline (par exemple, passage d'une insuline humaine ou animale à une présentation Humalog), vous pouvez nécessiter un changement de dose. Ce changement peut être effectué lors de la première injection ou progressivement sur plusieurs semaines ou plusieurs mois. Injectez Humalog sous la peau (sous-cutanée). Préparation d'humalog 200 UI/ml KwikPen Humalog est une solution et il n'est donc pas nécessaire de la mélanger. Vous ne devez l'utiliser que si elle a l'apparence de l'eau. Le liquide doit être transparent, incolore et exempt de toutes particules. Vérifiez l apparence avant chaque injection. Réglage du stylo KwikPen (consultez votre manuel d'utilisation) Lavez-vous d'abord les mains. Lisez les instructions pour l'utilisation de votre stylo à insuline pré-rempli et suivez-les attentivement. En voici quelques-unes : Utilisez une aiguille propre (les aiguilles ne sont pas fournies). Purgez votre stylo KwikPen avant chaque utilisation. La purge permet de vérifier que l insuline sort et permet de chasser les bulles d'air de votre stylo KwikPen. Il peut persister quelques petites bulles d'air, sans conséquence, dans le stylo. Toutefois, si la taille des bulles est trop importante, la dose injectée pourrait être affectée. Injection d'humalog Avant de procéder à l'injection, nettoyez la peau selon les instructions que l on vous a données. Injectez sous la peau comme on vous l'a appris. Après l'injection, laissez l'aiguille sous la peau pendant 5 secondes afin de vous assurer que vous avez injecté votre dose en totalité. Ne frottez pas l'endroit où vous venez de faire l'injection. Assurez-vous que vous injectez à une distance d'au moins 1 cm de la dernière injection et que vous observez une rotation des emplacements d'injection, comme on vous l'a appris. Quel que soit le site d injection utilisé, les bras, les cuisses, les fesses ou l abdomen, Humalog agira toujours plus rapidement que l insuline humaine rapide. Ne pas injecter Humalog 200 UI/ml KwikPen solution injectable directement dans une veine (par voie intraveineuse). Après l'injection Une fois l'injection terminée, dévissez l'aiguille du stylo KwikPen en utilisant le capuchon extérieur de l'aiguille. Cette opération permet de maintenir l'insuline stérile et empêche les fuites. Elle empêche également toute entrée d'air dans le stylo et l obstruction de l'aiguille. Ne partagez pas vos aiguilles. Ne partagez pas votre stylo. Replacez le capuchon sur votre stylo. Injections ultérieures A chaque utilisation du stylo KwikPen, vous devez utiliser une nouvelle aiguille. Avant chaque injection, chassez les bulles d'air. Vous pouvez vous assurer de la quantité d'insuline restante en tenant le stylo KwikPen l'aiguille pointée vers le haut. N'utilisez plus le stylo KwikPen lorsqu il est vide. Eliminez votre stylo selon les recommandations des professionnels de santé. 4
5 Si vous avez pris plus d Humalog que vous n auriez dû Si vous avez pris plus d Humalog que vous n auriez dû, un abaissement du taux de sucre dans le sang peut survenir. Vérifiez votre taux de sucre. Si votre glycémie est basse (hypoglycémie légère), consommez des préparations glucosées, du sucre ou des boissons sucrées. Puis, consommez des fruits, des biscuits ou un sandwich selon les conseils de votre médecin et reposez-vous. Ceci vous permettra généralement de maîtriser une hypoglycémie légère ou un surdosage mineur d'insuline. En cas d'aggravation, si votre respiration est superficielle et si votre peau devient pâle, avisez-en immédiatement votre médecin. Une injection de glucagon peut traiter une hypoglycémie assez grave. Prenez du glucose ou du sucre après l'injection de glucagon. Si vous n'obtenez aucune réaction au glucagon, un traitement hospitalier sera nécessaire. Demandez à votre médecin des renseignements concernant le glucagon. Si vous oubliez d utiliser Humalog Si vous prenez moins d Humalog que vous n auriez dû, une augmentation du taux de sucre dans le sang peut survenir. Vérifiez votre taux de sucre. Si une hypoglycémie (pas assez de sucre dans le sang) ou une hyperglycémie (trop de sucre dans le sang) n est pas traitée, il peut s'ensuivre des complications sérieuses telles que céphalées, envie de vomir (nausées), vomissements, perte d eau (déshydratation), évanouissements, coma voire même décès (voir la rubrique 4 «Quels sont les effets indésirables éventuels»). Trois recommandations simples pour éviter une hypoglycémie ou une hyperglycémie : Ayez toujours avec vous des seringues et un flacon d'humalog 100 UI/ml supplémentaire ou un stylo de rechange et des cartouches supplémentaires, au cas où vous perdriez ou endommageriez votre stylo KwikPen. Ayez toujours avec vous un document indiquant que vous êtes diabétique. Ayez toujours du sucre avec vous. Si vous arrêtez d utiliser Humalog Si vous prenez moins d Humalog que vous n auriez dû, une augmentation du taux de sucre dans le sang peut survenir. Ne changez pas d insuline sauf sur prescription de votre médecin. Si vous avez d autres questions sur l utilisation de ce médicament, demandez plus d informations à votre médecin ou à votre pharmacien. 4. Quels sont les effets indésirables éventuels Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde. Une allergie grave est rare (peut affecter jusqu à 1 personne sur 1000). En voici les symptômes : éruption généralisée sur tout le corps baisse de la tension artérielle difficultés de respiration accélération du pouls respiration sifflante de type asthmatique transpiration Si vous pensez avoir ce type d allergie à l insuline avec Humalog, contactez un médecin. L allergie locale est fréquente (peut affecter jusqu à 1 personne sur 10). Elle peut se manifester par une rougeur, un œdème et des démangeaisons au point d'injection. Cette réaction disparaît habituellement en quelques jours voire quelques semaines. Consultez votre médecin si ceci vous arrive. 5
6 La lipodystrophie (épaississement ou cicatrices sur la peau) est peu fréquente (peut affecter jusqu à 1 personne sur 100). Si vous observez un épaississement de la peau ou des marques au point d'injection, consultez votre médecin. Un œdème (par exemple, gonflement au niveau des bras, des chevilles ; rétention d eau) a été rapporté en particulier au début du traitement par insuline ou lors d un changement du traitement pour améliorer le contrôle de votre glycémie. Déclaration des effets secondaires Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance. En signalant les effets indésirables, vous contribuez à fournir davantage d informations sur la sécurité du médicament. Problèmes courants du diabète Hypoglycémie Hypoglycémie (pas assez de sucre dans le sang) signifie qu'il n'y a pas suffisamment de sucre dans le sang et peut être provoquée par : une dose trop élevée d'humalog ou d'une autre insuline ; le fait que vous sautiez ou retardiez vos repas ou changiez de régime alimentaire ; des exercices ou des activités intenses juste avant ou après un repas ; une infection ou une maladie (en particulier des diarrhées ou vomissements) ; des changements de vos besoins en insuline ; ou une insuffisance rénale ou hépatique en voie d'aggravation ; Les boissons alcoolisées ainsi que certains médicaments sont susceptibles d'influencer votre glycémie (voir rubrique 2). Les premiers symptômes de l'hypoglycémie apparaissent habituellement rapidement et comprennent : fatigue accélération du pouls nervosité ou tremblements malaise maux de tête sueurs froides Lorsque vous n êtes pas certain de votre capacité à en reconnaître les symptômes précurseurs, évitez toute situation, comme la conduite de véhicule, dans laquelle vous ou d autres personnes pourraient être exposées à un risque du fait de votre hypoglycémie. Hyperglycémie et acidocétose diabétique Hyperglycémie (trop de sucre dans le sang) signifie que vous n'avez pas suffisamment d'insuline. L hyperglycémie peut être provoquée par le fait que : vous n'avez pas pris votre dose d'humalog ou d'une autre insuline ; vous prenez moins d'insuline que la dose prescrite par votre médecin ; votre alimentation dépasse de beaucoup les limites permises par votre régime alimentaire ; vous avez de la fièvre, une infection ou êtes en état de stress. L'hyperglycémie peut entraîner une acidocétose diabétique. Les premiers symptômes se manifestent lentement. Parmi ceux-ci, citons les suivants : 6
7 somnolence absence d'appétit rougeur au visage odeur acétonique de l'haleine soif sensation de malaise Les symptômes graves sont une respiration difficile et un pouls rapide. Consultez votre médecin immédiatement. En cas de maladie Si vous êtes malade et plus particulièrement, si vous vous sentez malade ou si vous avez des nausées, vos besoins en insuline pourront être différents. Même si vous ne vous alimentez pas normalement, vous avez néanmoins toujours besoin d'insuline. Testez vos urines ou votre sang, suivez les instructions qui vous ont été données dans ce cas et consultez votre médecin. 5. Comment conserver Humalog 200 UI/ml KwikPen Tenir ce médicament hors de la vue et de la portée des enfants. Ne pas utiliser Humalog 200 UI/ml KwikPen après la date de péremption mentionnée sur l étiquette et l emballage. La date de péremption fait référence au dernier jour de ce mois. Avant la première utilisation, conserver votre Humalog 200 UI/ml KwikPen au réfrigérateur (entre 2 C et 8 C). Ne pas congeler. Conserver votre Humalog 200 UI/ml KwikPen en cours d utilisation à température ambiante (entre 15 C et 30 C) et jeter-le après 28 jours. Ne pas exposer à une chaleur excessive ou au soleil. Ne laissez pas votre stylo KwikPen en cours d'utilisation au réfrigérateur. Le stylo KwikPen ne doit pas être conservé avec l aiguille vissée dessus. Ne pas utiliser Humalog 200 UI/ml KwikPen, si la solution est colorée ou si elle contient des particules.vous devez l utiliser uniquement si elle a l apparence de l eau. Vérifiez cela avant chaque injection. Les médicaments ne doivent pas être jetés au tout à l égout ou avec les ordures ménagères. Demandez à votre pharmacien ce qu il faut faire des médicaments inutilisés. Ces mesures permettront de protéger l environnement. 6. Contenu de l emballage et autres informations Que contient Humalog KwikPen 200 UI/ml, solution injectable - La substance active est l insuline lispro. Chaque ml de solution contient 200 unités (UI) d insuline lispro. Chaque stylo prérempli (3 ml) contient 600 unités (UI) d insuline lispro. - Les autres composants sont : le métacrésol, le glycérol, le trométamol, l oxyde de zinc et l eau pour préparations injectables. L'hydroxyde de sodium ou l'acide chlorhydrique peuvent avoir été utilisés pour ajuster le ph. Qu est-ce qu Humalog 200 UI/ml KwikPen et contenu de son emballage extérieur Humalog 200 UI/ml KwikPen, solution injectable est une solution aqueuse, stérile, transparente, incolore et contient 200 unités internationales d insuline lispro par millilitre (200 UI/ml) de solution injectable. La contenance d'humalog 200 UI/ml KwikPen est de 600 unités internationales (3 millilitres). Les stylos 7
8 Humalog 200 UI/ml KwikPen sont conditionnés par boîte de 1, 2 ou 5 stylos pré-remplis ou en emballage multiple de 2 x 5 stylos pré-remplis. Toutes les présentations peuvent ne pas être commercialisées. Le stylo KwikPen contient simplement une cartouche intégrée. Vous ne pouvez plus utiliser le stylo pré-rempli lorsqu'il est vide. Titulaire de l'autorisation de mise sur le marché Eli Lilly Nederland B.V., Grootslag 1-5, 3991 RA Houten, Pays-Bas. Fabricant Lilly France SAS, Rue du Colonel Lilly, Fegersheim, France. Pour toute information complémentaire concernant ce médicament, veuillez prendre contact avec le représentant local du titulaire de l autorisation de mise sur le marché : France Lilly France S.A.S. Tél: +33-(0) La dernière date à laquelle cette notice a été révisée est 30 septembre Des informations détaillées sur ce médicament sont disponibles sur le site internet de l Agence européenne du médicament 8
NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR. Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant
 B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
Notice publique PERDOLAN - PÉDIATRIE
 Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
NOTICE : INFORMATION DE L'UTILISATEUR. DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc
 NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
DIABÈTe De TYPe 1 Petit guide pour les parents et les enfants.
 DIABÈTe De TYPe 1 Petit guide pour les parents et les enfants. Guide pour comprendre et aborder sereinement l apparition du diabète de type 1. Sommaire Le contrôle glycémique 04 Qu est-ce que le taux d
DIABÈTe De TYPe 1 Petit guide pour les parents et les enfants. Guide pour comprendre et aborder sereinement l apparition du diabète de type 1. Sommaire Le contrôle glycémique 04 Qu est-ce que le taux d
PIL Décembre 2009. Autres composants: acide tartrique, macrogol 4000, macrogol 1000, macrogol 400, butylhydroxyanisol.
 Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Guide d injection de l insuline
 Guide d injection de l insuline Table des matières Introduction........................2 Instruments d injection d insuline........3 Glycémie Hyperglycémie..........................15 Table des matières
Guide d injection de l insuline Table des matières Introduction........................2 Instruments d injection d insuline........3 Glycémie Hyperglycémie..........................15 Table des matières
NOTICE: INFORMATION DE L UTILISATEUR. Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain)
 NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine
 KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
1 La scintigraphie myocardique au Persantin ou Mibi Persantin
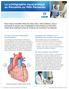 La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
Insulinothérapie et diabète de type 1
 Insulinothérapie et diabète de type 1 Introduction: la molécule d insuline L instauration de l insulinothérapie Dispositif d administration de l insuline Les propriétés de l insuline Insuline et schémas
Insulinothérapie et diabète de type 1 Introduction: la molécule d insuline L instauration de l insulinothérapie Dispositif d administration de l insuline Les propriétés de l insuline Insuline et schémas
Stelara (ustekinumab)
 Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
NOTICE: INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés. Bisacodyl
 NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
Diabète de type 1: Informations destinées aux enseignants
 Diabète de type 1: Informations destinées aux enseignants Le diabète chez les jeunes Le diabète de type 1 est une maladie très difficile à affronter, surtout quand on est jeune. Malheureusement, si quelque
Diabète de type 1: Informations destinées aux enseignants Le diabète chez les jeunes Le diabète de type 1 est une maladie très difficile à affronter, surtout quand on est jeune. Malheureusement, si quelque
NOTICE : INFORMATION DE L UTILISATEUR. Delphi 0,1 % crème Acétonide de triamcinolone
 NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR. Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl)
 NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR. Flunarizine
 NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
DIAMICRON MR (Gliclazide) Monographie de produit Page 1 de 5
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr DIAMICRON MR Gliclazide Comprimés à libération modifiée de 30 mg Comprimés sécables à libération modifiée de 60 mg Le présent dépliant constitue la troisième
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr DIAMICRON MR Gliclazide Comprimés à libération modifiée de 30 mg Comprimés sécables à libération modifiée de 60 mg Le présent dépliant constitue la troisième
NOTICE : INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés Bisacodyl
 NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
La prise en charge de votre insuffisance cardiaque
 G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre insuffisance cardiaque Vivre avec une insuffisance cardiaque Décembre 2007 Pourquoi ce guide? Votre médecin traitant
G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre insuffisance cardiaque Vivre avec une insuffisance cardiaque Décembre 2007 Pourquoi ce guide? Votre médecin traitant
Atrovent HFA 20 mcg/bouffée solution pour inhalation en flacon pressurisé (bromure d'ipratropium)
 NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
Brûlures d estomac. Mieux les comprendre pour mieux les soulager
 Brûlures d estomac Mieux les comprendre pour mieux les soulager Définition et causes Brûlures d estomac Mieux les comprendre pour mieux les soulager Vous arrive-t-il de ressentir une douleur à l estomac
Brûlures d estomac Mieux les comprendre pour mieux les soulager Définition et causes Brûlures d estomac Mieux les comprendre pour mieux les soulager Vous arrive-t-il de ressentir une douleur à l estomac
Diabète Type 2. Épidémiologie Aspects physiques Aspects physiologiques
 Diabète Type 2 Épidémiologie Aspects physiques Aspects physiologiques Épidémiologie 90% de tous les cas de diabètes Environ 1 personne sur 20 est atteinte Diabète gras Facteur de risque majeur pour les
Diabète Type 2 Épidémiologie Aspects physiques Aspects physiologiques Épidémiologie 90% de tous les cas de diabètes Environ 1 personne sur 20 est atteinte Diabète gras Facteur de risque majeur pour les
TROISIÈME PARTIE : INFORMATION POUR LE PATIENT
 TROISIÈME PARTIE : INFORMATION POUR LE PATIENT REBIF (Interféron bêta-1a) Solution pour injection dans des seringues préremplies Ce livret représente la troisième partie de la «Monographie de produit»
TROISIÈME PARTIE : INFORMATION POUR LE PATIENT REBIF (Interféron bêta-1a) Solution pour injection dans des seringues préremplies Ce livret représente la troisième partie de la «Monographie de produit»
Le diabète pédiatrique : Un guide pour la famille
 Montreal Children s Le diabète pédiatrique : Un guide pour la famille Ce guide est pour : Le but de ce guide est de vous aider, vous et votre famille, à mieux comprendre le diabète et à gérer les soins
Montreal Children s Le diabète pédiatrique : Un guide pour la famille Ce guide est pour : Le but de ce guide est de vous aider, vous et votre famille, à mieux comprendre le diabète et à gérer les soins
L APS ET LE DIABETE. Le diabète se caractérise par un taux de glucose ( sucre ) trop élevé dans le sang : c est l hyperglycémie.
 1. Qu est-ce que le diabète? L APS ET LE DIABETE Le diabète se caractérise par un taux de glucose ( sucre ) trop élevé dans le sang : c est l hyperglycémie. Cette hyperglycémie est avérée si à 2 reprises
1. Qu est-ce que le diabète? L APS ET LE DIABETE Le diabète se caractérise par un taux de glucose ( sucre ) trop élevé dans le sang : c est l hyperglycémie. Cette hyperglycémie est avérée si à 2 reprises
Notice : information de l utilisateur. Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine
 Notice : information de l utilisateur Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine Veuillez lire attentivement cette notice avant de prendre ce médicament
Notice : information de l utilisateur Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine Veuillez lire attentivement cette notice avant de prendre ce médicament
Le guide du bon usage des médicaments
 Le guide du bon usage des médicaments Les médicaments sont là pour vous aider mais......ils ont parfois du mal à vivre ensemble. Votre médecin et votre pharmacien peuvent adapter votre traitement pour
Le guide du bon usage des médicaments Les médicaments sont là pour vous aider mais......ils ont parfois du mal à vivre ensemble. Votre médecin et votre pharmacien peuvent adapter votre traitement pour
Notice : information de l utilisateur
 Notice : information de l utilisateur ALIMTA 100 mg poudre pour solution à diluer pour perfusion ALIMTA 500 mg poudre pour solution à diluer pour perfusion Pemetrexed Veuillez lire attentivement l'intégralité
Notice : information de l utilisateur ALIMTA 100 mg poudre pour solution à diluer pour perfusion ALIMTA 500 mg poudre pour solution à diluer pour perfusion Pemetrexed Veuillez lire attentivement l'intégralité
L autogestion de l insulinothérapie basale plus 1
 L autogestion de l insulinothérapie basale plus 1 Le traitement combiné insuline basale et hypoglycémiants oraux est un traitement éprouvé et efficace pour amorcer en douceur l insulinothérapie. Il est
L autogestion de l insulinothérapie basale plus 1 Le traitement combiné insuline basale et hypoglycémiants oraux est un traitement éprouvé et efficace pour amorcer en douceur l insulinothérapie. Il est
Patchs contre la douleur contenant des dérivés de morphine. Réponses aux questions les plus fréquentes
 Patchs contre la douleur contenant des dérivés de morphine Réponses aux questions les plus fréquentes Introduction Quel objectif? Ce document constitue une aide dans la gestion au quotidien de votre douleur.
Patchs contre la douleur contenant des dérivés de morphine Réponses aux questions les plus fréquentes Introduction Quel objectif? Ce document constitue une aide dans la gestion au quotidien de votre douleur.
NOTICE. TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé
 NOTICE ANSM Mis à jour le : 15/07/2014 Dénomination du médicament Encadré TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient
NOTICE ANSM Mis à jour le : 15/07/2014 Dénomination du médicament Encadré TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient
Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés
 Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Developé pour le Centre
Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Developé pour le Centre
Sportifs et médicaments Questions et réponses
 Sportifs et médicaments Questions et réponses Que puis-je faire pour éviter d'être contrôlé positif suite à la prise d'un médicament? Il y a deux façons de se procurer des médicaments : soit sur ordonnance
Sportifs et médicaments Questions et réponses Que puis-je faire pour éviter d'être contrôlé positif suite à la prise d'un médicament? Il y a deux façons de se procurer des médicaments : soit sur ordonnance
NOTICE: INFORMATION DE L UTILISATEUR. Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan
 NOTICE: INFORMATION DE L UTILISATEUR Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan Veuillez lire attentivement l'intégralité de cette notice avant
NOTICE: INFORMATION DE L UTILISATEUR Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan Veuillez lire attentivement l'intégralité de cette notice avant
NOTICE. DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine
 NOTICE ANSM Mis à jour le : 08/06/2010 Dénomination du médicament DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine Encadré Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE ANSM Mis à jour le : 08/06/2010 Dénomination du médicament DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine Encadré Veuillez lire attentivement cette notice avant de prendre ce médicament.
Humira Solution pour injection dans un injecteur prérempli
 Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
NOTICE: INFORMATION DE L UTILISATEUR
 NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
Certaines situations de trafic peuvent-elles provoquer un risque accru d hypoglycémie?
 P a g e 1 Comment savoir que vous présentez une hypoglycémie? La plupart des personnes diabétiques sentent rapidement lorsque leur taux de glycémie est trop bas (inférieur à 60 mg/dl). Les premiers symptômes
P a g e 1 Comment savoir que vous présentez une hypoglycémie? La plupart des personnes diabétiques sentent rapidement lorsque leur taux de glycémie est trop bas (inférieur à 60 mg/dl). Les premiers symptômes
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE
 GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
Vous et votre traitement anticoagulant par AVK (antivitamine K)
 Ce carnet a été réalisé sous la coordination de l Agence française de sécurité sanitaire des produits de santé (Afssaps). Vous et votre traitement anticoagulant par AVK (antivitamine K) Carte à découper
Ce carnet a été réalisé sous la coordination de l Agence française de sécurité sanitaire des produits de santé (Afssaps). Vous et votre traitement anticoagulant par AVK (antivitamine K) Carte à découper
BIEN VIVRE AVEC MON DIABÈTE
 BIEN VIVRE AVEC MON DIABÈTE 2 e édition révisée BIEN VIVRE AVEC MON DIABÈTE 2 e édition révisée Stéphane Tardif Infirmier clinicien spécialisé en enseignement diabétique Avec la collaboration de l équipe
BIEN VIVRE AVEC MON DIABÈTE 2 e édition révisée BIEN VIVRE AVEC MON DIABÈTE 2 e édition révisée Stéphane Tardif Infirmier clinicien spécialisé en enseignement diabétique Avec la collaboration de l équipe
Livret des nouveaux anticoagulants oraux. Ce qu il faut savoir pour bien gérer leur utilisation
 Livret des nouveaux anticoagulants oraux Ce qu il faut savoir pour bien gérer leur utilisation DONNÉES DU PATIENT Nom Adresse Tél MÉDECIN TRAITANT Nom Adresse Tél SPÉCIALISTE Nom Hôpital Tél MÉDICAMENT
Livret des nouveaux anticoagulants oraux Ce qu il faut savoir pour bien gérer leur utilisation DONNÉES DU PATIENT Nom Adresse Tél MÉDECIN TRAITANT Nom Adresse Tél SPÉCIALISTE Nom Hôpital Tél MÉDICAMENT
Carnet de suivi Lithium
 Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT
 IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
Avenue du Président François Mitterrand 76405 FECAMP Service pédiatrie Tel 02.35.10.92.01. Guide du patient, porteur d un diabète de type 1
 Avenue du Président François Mitterrand 76405 FECAMP Service pédiatrie Tel 02.35.10.92.01 Guide du patient, porteur d un diabète de type 1 1 Madame, Monsieur, Votre enfant vient d être hospitalisé dans
Avenue du Président François Mitterrand 76405 FECAMP Service pédiatrie Tel 02.35.10.92.01 Guide du patient, porteur d un diabète de type 1 1 Madame, Monsieur, Votre enfant vient d être hospitalisé dans
Le VIH et votre apparence physique
 Le VIH et votre apparence physique Le VIH et votre apparence physique Les personnes séropositives subissent-elles souvent des changements de l apparence physique? Il est difficile de dire avec exactitude
Le VIH et votre apparence physique Le VIH et votre apparence physique Les personnes séropositives subissent-elles souvent des changements de l apparence physique? Il est difficile de dire avec exactitude
Traitements topiques. Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames. Soulagent les démangeaisons.
 SANS ORDONNANCE Solutions pour le bain et la douche : Huiles Farine d avoine Sels d Epsom Sels de al Mer Morte Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames.
SANS ORDONNANCE Solutions pour le bain et la douche : Huiles Farine d avoine Sels d Epsom Sels de al Mer Morte Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames.
NOTICE : INFORMATION DE L UTILISATEUR. Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés. ambrisentan
 NOTICE : INFORMATION DE L UTILISATEUR Version 17 Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés ambrisentan Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR Version 17 Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés ambrisentan Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR. Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés. sumatriptan
 NOTICE : INFORMATION DE L UTILISATEUR Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés sumatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament. - Gardez
NOTICE : INFORMATION DE L UTILISATEUR Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés sumatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament. - Gardez
J aimerais garder les hypoglycémies sous contrôle - Que puis-je faire?
 Simon Equilibré grâce à sa pompe depuis 2004 J aimerais garder les hypoglycémies sous contrôle - Que puis-je faire? L hypoglycémie peut être l une des préoccupations majeures des diabétiques de type 1,
Simon Equilibré grâce à sa pompe depuis 2004 J aimerais garder les hypoglycémies sous contrôle - Que puis-je faire? L hypoglycémie peut être l une des préoccupations majeures des diabétiques de type 1,
vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé)
 EMA/90006/2015 EMEA/H/C/001104 Résumé EPAR à l intention du public vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé) Le présent document est un résumé du rapport européen public d évaluation
EMA/90006/2015 EMEA/H/C/001104 Résumé EPAR à l intention du public vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé) Le présent document est un résumé du rapport européen public d évaluation
Conseils pour le traitement des douleurs persistantes
 Page -1- Conseils pour le traitement des douleurs persistantes Ce qu'il faut savoir avant tout, c'est que les douleurs persistantes sont des "douleurs particulières", qui doivent donc être traitées en
Page -1- Conseils pour le traitement des douleurs persistantes Ce qu'il faut savoir avant tout, c'est que les douleurs persistantes sont des "douleurs particulières", qui doivent donc être traitées en
Le diabète de type 1 UNSPF. Ségolène Gurnot
 Le diabète de type 1 UNSPF Ségolène Gurnot Juin 2013 Légende Entrée du glossaire Abréviation Référence Bibliographique Référence générale Table des matières Introduction 5 I - Introduction 7 A. Quelle
Le diabète de type 1 UNSPF Ségolène Gurnot Juin 2013 Légende Entrée du glossaire Abréviation Référence Bibliographique Référence générale Table des matières Introduction 5 I - Introduction 7 A. Quelle
Notice : Information de l utilisateur. Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable interféron bêta-1b
 Notice : Information de l utilisateur Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable interféron bêta-1b Veuillez lire attentivement cette notice avant d utiliser ce médicament
Notice : Information de l utilisateur Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable interféron bêta-1b Veuillez lire attentivement cette notice avant d utiliser ce médicament
Boughanmi Hajer. JAOUA Noureddine. Membre du bureau exécutif de l OTEF
 Organisation Tunisienne pour L Éducation et de la Famille Elaboré par Diabète infantile Boughanmi Hajer Encadré par : Licence appliquée en Biotechnologie JAOUA Noureddine Membre du bureau exécutif de l
Organisation Tunisienne pour L Éducation et de la Famille Elaboré par Diabète infantile Boughanmi Hajer Encadré par : Licence appliquée en Biotechnologie JAOUA Noureddine Membre du bureau exécutif de l
Le diabète de type 1
 www.reperessante.mu Le guide qui préserve votre capital Bien-être Le diabète de type 1 Numéro proposé gratuitement par : avec le soutien de : Message d Abdullah Dustagheer Président de T1 Diams L association
www.reperessante.mu Le guide qui préserve votre capital Bien-être Le diabète de type 1 Numéro proposé gratuitement par : avec le soutien de : Message d Abdullah Dustagheer Président de T1 Diams L association
BRICOLAGE. Les précautions à prendre
 BRICOLAGE Les précautions à prendre Chaque année, près de 300 000 personnes arrivent aux Urgences à la suite d un accident de bricolage et/ou de jardinage. Respecter quelques règles simples de prévention
BRICOLAGE Les précautions à prendre Chaque année, près de 300 000 personnes arrivent aux Urgences à la suite d un accident de bricolage et/ou de jardinage. Respecter quelques règles simples de prévention
TRAITEMENTS MEDICAMENTEUX DU DIABETE DE TYPE 2 (Hors Insuline) MAREDIA Dr Marc DURAND
 TRAITEMENTS MEDICAMENTEUX DU DIABETE DE TYPE 2 (Hors Insuline) MAREDIA Dr Marc DURAND PHYSIOPATHOLOGIE DE L HYPERGLYCEMIE DU DT2 Tube digestif Pancréas endocrine α β Tissu adipeux cellules β insuline cellules
TRAITEMENTS MEDICAMENTEUX DU DIABETE DE TYPE 2 (Hors Insuline) MAREDIA Dr Marc DURAND PHYSIOPATHOLOGIE DE L HYPERGLYCEMIE DU DT2 Tube digestif Pancréas endocrine α β Tissu adipeux cellules β insuline cellules
Vivez votre féminité sans souffrir.
 Vivez votre féminité sans souffrir. PERDOFEMINA (lysinate d ibuprofène) est un médicament pour les adultes et les enfants à partir de 12 ans. Pas d utilisation prolongée sans avis médical. Ne pas administrer
Vivez votre féminité sans souffrir. PERDOFEMINA (lysinate d ibuprofène) est un médicament pour les adultes et les enfants à partir de 12 ans. Pas d utilisation prolongée sans avis médical. Ne pas administrer
«Je suis diabétique» Informations sur la prise en charge d enfants diabétiques à l école. Pour les parents et les enseignants
 «Je suis diabétique» Informations sur la prise en charge d enfants diabétiques à l école Pour les parents et les enseignants C est parti! Compréhensible et compacte: par le biais de cette brochure, parents
«Je suis diabétique» Informations sur la prise en charge d enfants diabétiques à l école Pour les parents et les enseignants C est parti! Compréhensible et compacte: par le biais de cette brochure, parents
NOTICE : INFORMATION DE L UTILISATEUR. Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants. Acide acétylsalicylique
 NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
Qu est-ce que la fibrillation auriculaire? (FA)
 Qu est-ce que la fibrillation auriculaire? (FA) Qu est-ce que la fibrillation auriculaire? La fibrillation auriculaire (FA) est le trouble du rythme le plus répandu. Certains signaux du cœur deviennent
Qu est-ce que la fibrillation auriculaire? (FA) Qu est-ce que la fibrillation auriculaire? La fibrillation auriculaire (FA) est le trouble du rythme le plus répandu. Certains signaux du cœur deviennent
Rougeole, Oreillons Rubéole et Coqueluche
 Rougeole, Oreillons Rubéole et Coqueluche Comment protéger vos enfants? La seule protection efficace : la vaccination R.O.R COQUELUCHE ANNUAIRE Livret élaboré en partenariat avec : Conseil Général du Loir-et-Cher
Rougeole, Oreillons Rubéole et Coqueluche Comment protéger vos enfants? La seule protection efficace : la vaccination R.O.R COQUELUCHE ANNUAIRE Livret élaboré en partenariat avec : Conseil Général du Loir-et-Cher
Médicaments et alcool?
 Médicaments et alcool? Parlez-en à votre pharmacien évitez les cocktails à risque... Médicaments et alcool? évitez les cocktails à risque! Consommer de l alcool quand on prend des médicaments n est pas
Médicaments et alcool? Parlez-en à votre pharmacien évitez les cocktails à risque... Médicaments et alcool? évitez les cocktails à risque! Consommer de l alcool quand on prend des médicaments n est pas
que dois-tu savoir sur le diabète?
 INVENTIV HEALTH COMMUNICATIONS - TERRE NEUVE - FRHMG00277 - Avril 2013 - Lilly - Tous droits de reproduction réservés. que dois-tu savoir sur le diabète? Lilly France 24 boulevard Vital Bouhot CS 50004-92521
INVENTIV HEALTH COMMUNICATIONS - TERRE NEUVE - FRHMG00277 - Avril 2013 - Lilly - Tous droits de reproduction réservés. que dois-tu savoir sur le diabète? Lilly France 24 boulevard Vital Bouhot CS 50004-92521
MONOGRAPHIE. tocilizumab. Solution concentrée à 20 mg/ml pour perfusion. Solution à 162 mg/0,9 ml pour injection. Norme reconnue
 MONOGRAPHIE Pr ACTEMRA tocilizumab Solution concentrée à 20 mg/ml pour perfusion Solution à 162 mg/0,9 ml pour injection Norme reconnue Inhibiteur du récepteur d interleukine Le traitement par ACTEMRA
MONOGRAPHIE Pr ACTEMRA tocilizumab Solution concentrée à 20 mg/ml pour perfusion Solution à 162 mg/0,9 ml pour injection Norme reconnue Inhibiteur du récepteur d interleukine Le traitement par ACTEMRA
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MEDICAMENT ImmunoGam, 312 UI/ml, solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque ml contient 312 UI d'immunoglobuline
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MEDICAMENT ImmunoGam, 312 UI/ml, solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque ml contient 312 UI d'immunoglobuline
DIABETE ET SPORT. Dominique HUET Hopital Saint Joseph PARIS
 DIABETE ET SPORT Dominique HUET Hopital Saint Joseph PARIS DIABETE TYPE 1#TYPE 2 Jeunes sportifs Risque hypoglycémie Adaptation schémas Autosurveillance +++ Sports souvent sources de difficultés Contre
DIABETE ET SPORT Dominique HUET Hopital Saint Joseph PARIS DIABETE TYPE 1#TYPE 2 Jeunes sportifs Risque hypoglycémie Adaptation schémas Autosurveillance +++ Sports souvent sources de difficultés Contre
Bien vous soigner. avec des médicaments disponibles sans ordonnance. juin 2008. Douleur. de l adulte
 Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
MONOGRAPHIE DE PRODUIT
 MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
NOTICE : INFORMATIONS DU PATIENT. Keforal 500 mg comprimés pelliculés. Céfalexine monohydratée
 NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
diabète Le diabète est l assimilation, de glucose (sucre) apporté par On peut être diabétique sans
 Tout savoir sur le Le est une maladie chronique incurable qui se traduit par une élévation anormale du taux de sucre dans le sang. Sans traitement approprié, cette maladie peut être à l origine de graves
Tout savoir sur le Le est une maladie chronique incurable qui se traduit par une élévation anormale du taux de sucre dans le sang. Sans traitement approprié, cette maladie peut être à l origine de graves
Vous avez subi une ICT.
 Vous avez subi une ICT. Apprenez comment éviter d en subir une autre. Vous avez subi une ict. apprenez comment éviter d en subir une autre. Une ischémie cérébrale transitoire (ou ICT) est une urgence médicale.
Vous avez subi une ICT. Apprenez comment éviter d en subir une autre. Vous avez subi une ict. apprenez comment éviter d en subir une autre. Une ischémie cérébrale transitoire (ou ICT) est une urgence médicale.
Fiche de synthèse. Learn. Les points essentiels pour l accompagnement d un patient diabétique. Parcours : Prise en charge du diabète à l officine
 Les points essentiels pour l accompagnement d un patient diabétique Dans toutes les situations Privilégiez la phase de découverte Savoir comment le patient et/ou l accompagnant perçoivent le diabète. Permettre
Les points essentiels pour l accompagnement d un patient diabétique Dans toutes les situations Privilégiez la phase de découverte Savoir comment le patient et/ou l accompagnant perçoivent le diabète. Permettre
Le VIH et votre foie
 Le VIH et votre foie Le VIH et votre foie Que dois-je savoir au sujet de mon foie? Votre foie joue un rôle incroyablement important. Il filtre votre sang en éliminant les substances nocives (toxiques)
Le VIH et votre foie Le VIH et votre foie Que dois-je savoir au sujet de mon foie? Votre foie joue un rôle incroyablement important. Il filtre votre sang en éliminant les substances nocives (toxiques)
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR. APO-CITALOPRAM Comprimés de citalopram USP
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr APO-CITALOPRAM Comprimés de citalopram USP Cette notice est la troisième partie de la monographie du produit APO-CITALOPRAM, publiée lorsque le médicament
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr APO-CITALOPRAM Comprimés de citalopram USP Cette notice est la troisième partie de la monographie du produit APO-CITALOPRAM, publiée lorsque le médicament
Recherche et textes Gilles Landry et Diane Labelle
 Recherche et textes Gilles Landry et Diane Labelle Collaboration Le comité de lecture des participants et participantes de Lettres en main. Hélène Ranger et Esther Filion de Lettres en main. Chantal Martin,
Recherche et textes Gilles Landry et Diane Labelle Collaboration Le comité de lecture des participants et participantes de Lettres en main. Hélène Ranger et Esther Filion de Lettres en main. Chantal Martin,
Itraconazole Sandoz 100 mg gélules Itraconazole
 Notice Itraconazole Sandoz 100 mg gélules Itraconazole Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire
Notice Itraconazole Sandoz 100 mg gélules Itraconazole Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire
VOUS et VOTRE NOUVEAU TRAITEMENT anticoagulant Eliquis, Pradaxa, Xarelto
 VOUS et VOTRE NOUVEAU TRAITEMENT anticoagulant Eliquis, Pradaxa, Xarelto Carnet-conseils appartenant à :.... Adresse :......................... Tel :............................ Médecin Généraliste : Adresse
VOUS et VOTRE NOUVEAU TRAITEMENT anticoagulant Eliquis, Pradaxa, Xarelto Carnet-conseils appartenant à :.... Adresse :......................... Tel :............................ Médecin Généraliste : Adresse
ACTUALITES THERAPEUTIQUES DANS LE DIABETE DE TYPE 2. Docteur R.POTIER
 ACTUALITES THERAPEUTIQUES DANS LE DIABETE DE TYPE 2 Docteur R.POTIER DEFINITION DU DIABETE soit : Syndrome polyuro-polydipsique + amaigrissement + 1 glycémie > 2g/L 2 glycémies à jeun > 1,26g/l 1 glycémie
ACTUALITES THERAPEUTIQUES DANS LE DIABETE DE TYPE 2 Docteur R.POTIER DEFINITION DU DIABETE soit : Syndrome polyuro-polydipsique + amaigrissement + 1 glycémie > 2g/L 2 glycémies à jeun > 1,26g/l 1 glycémie
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR. ANDROGEL Gel de testostérone à 1 %
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR ANDROGEL Gel de testostérone à 1 % Le présent dépliant constitue la troisième et dernière partie d une «monographie de produit» publiée à la suite de l
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR ANDROGEL Gel de testostérone à 1 % Le présent dépliant constitue la troisième et dernière partie d une «monographie de produit» publiée à la suite de l
Vivre avec l insuffisance cardiaque Information pour les patients et leur famille
 Vivre avec l insuffisance cardiaque Information pour les patients et leur famille EPICORE CENTRE Division of Cardiology 213 Heritage Medical Research Centre University of Alberta Edmonton, AB T6G 2S2 Phone:
Vivre avec l insuffisance cardiaque Information pour les patients et leur famille EPICORE CENTRE Division of Cardiology 213 Heritage Medical Research Centre University of Alberta Edmonton, AB T6G 2S2 Phone:
Enfants et adolescents diabétiques Problématiques courantes en médecine générale dominique.beckers@uclouvain.be
 Enfants et adolescents diabétiques Problématiques courantes en médecine générale dominique.beckers@uclouvain.be Hyperglycémies Acido-cétose = Insulinopénie * Au moment du diagnostic (dépistage) * Lors
Enfants et adolescents diabétiques Problématiques courantes en médecine générale dominique.beckers@uclouvain.be Hyperglycémies Acido-cétose = Insulinopénie * Au moment du diagnostic (dépistage) * Lors
Se préparer à une angiographie artérielle
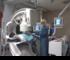 Se préparer à une angiographie artérielle Table des matières Sujet Page Qu est-ce que l athérosclérose?... 1 Durcissement graduel des artères (athérosclérose)... 2 Pourquoi dois-je subir une angiographie
Se préparer à une angiographie artérielle Table des matières Sujet Page Qu est-ce que l athérosclérose?... 1 Durcissement graduel des artères (athérosclérose)... 2 Pourquoi dois-je subir une angiographie
Le VIH et votre cœur
 Le VIH et votre cœur Le VIH et votre cœur Que dois-je savoir au sujet de mon cœur? Les maladies cardiovasculaires représentent une des cause les plus courante de décès, elles incluent: les maladies coronariennes,
Le VIH et votre cœur Le VIH et votre cœur Que dois-je savoir au sujet de mon cœur? Les maladies cardiovasculaires représentent une des cause les plus courante de décès, elles incluent: les maladies coronariennes,
Guide d'auto administration des soins destiné aux personnes atteintes du diabète
 Guide d'auto administration des soins destiné aux personnes atteintes du diabète Avec le soutien d'une subvention sans restriction de French Version 1 Lorsque le diagnostic est celui du diabète...........03
Guide d'auto administration des soins destiné aux personnes atteintes du diabète Avec le soutien d'une subvention sans restriction de French Version 1 Lorsque le diagnostic est celui du diabète...........03
Diabetes Service. Diabète et exercice physique
 Diabetes Service Diabète et exercice physique Diabète et Exercice Physique La présente brochure a pu être réalisée grâce à l aimable collaboration du: Dr. B. Jandrain, Médecine Interne, Diabétologie, Consultant
Diabetes Service Diabète et exercice physique Diabète et Exercice Physique La présente brochure a pu être réalisée grâce à l aimable collaboration du: Dr. B. Jandrain, Médecine Interne, Diabétologie, Consultant
Lecteur éditeur de chèques. i2200. Manuel utilisateur. Solutions de transactions et de paiement sécurisées
 Manuel utilisateur Lecteur éditeur de chèques i2200 Solutions de transactions et de paiement sécurisées Ingenico 2200 Avant Propos Merci d avoir choisi le Lecteur Editeur de chèque nouvelle génération
Manuel utilisateur Lecteur éditeur de chèques i2200 Solutions de transactions et de paiement sécurisées Ingenico 2200 Avant Propos Merci d avoir choisi le Lecteur Editeur de chèque nouvelle génération
Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène
 NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE
 CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE BAXTER_CLINIMIX N9G15 E et N12G20E_Avis CT_14-02-2007.pdf BAXTER_CLINIMIX N9G15E N12G20E N14G30 N17G35_Avis CT_12-12-2001.pdf BAXTER_CLINIMIX changement
CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE BAXTER_CLINIMIX N9G15 E et N12G20E_Avis CT_14-02-2007.pdf BAXTER_CLINIMIX N9G15E N12G20E N14G30 N17G35_Avis CT_12-12-2001.pdf BAXTER_CLINIMIX changement
En savoir plus sur le diabète
 En savoir plus sur le diabète 2 Qu est-ce que le diabète? Le diabète se caractérise par un excès de sucre dans le sang, on appelle cela l hyperglycémie. Le diabète est une maladie chronique qui survient
En savoir plus sur le diabète 2 Qu est-ce que le diabète? Le diabète se caractérise par un excès de sucre dans le sang, on appelle cela l hyperglycémie. Le diabète est une maladie chronique qui survient
Exercices pour renforcer les muscles abdominaux après l accouchement
 Exercices pour renforcer les muscles abdominaux après l accouchement Pendant la grossesse, les muscles du ventre, appelés abdominaux, s étirent beaucoup et perdent souvent de la force. Il est important
Exercices pour renforcer les muscles abdominaux après l accouchement Pendant la grossesse, les muscles du ventre, appelés abdominaux, s étirent beaucoup et perdent souvent de la force. Il est important
Information pour les patients dialysés qui prennent du chlorhydrate de sévélamer (RENAGEL)
 Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament RENAGEL de certaines conditions. Le plan obligatoire de minimalisation des risques en Belgique, dont cette information
Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament RENAGEL de certaines conditions. Le plan obligatoire de minimalisation des risques en Belgique, dont cette information
CARDIOLOGIE LA MÉDICATION POUR L'INSUFFISANCE CARDIAQUE
 CARDIOLOGIE LA MÉDICATION POUR L'INSUFFISANCE CARDIAQUE La médication est importante, elle aidera à améliorer le travail du cœur et à éliminer le surplus d'eau. Il est important de prendre la médication
CARDIOLOGIE LA MÉDICATION POUR L'INSUFFISANCE CARDIAQUE La médication est importante, elle aidera à améliorer le travail du cœur et à éliminer le surplus d'eau. Il est important de prendre la médication
NOTICE. ANSM - Mis à jour le : 25/03/2014. Dénomination du médicament. PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole
 NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
Pourquoi une femme-enceinte présente un certain nombre de douleurs inconnues jusqu'à lors?
 Pourquoi une femme-enceinte présente un certain nombre de douleurs inconnues jusqu'à lors? elle va pour cela créer des éléments chargées de transmettre un message à son corps (les hormones) : la «relaxine»
Pourquoi une femme-enceinte présente un certain nombre de douleurs inconnues jusqu'à lors? elle va pour cela créer des éléments chargées de transmettre un message à son corps (les hormones) : la «relaxine»
L eau dans le corps. Fig. 6 L eau dans le corps. Cerveau 85 % Dents 10 % Cœur 77 % Poumons 80 % Foie 73 % Reins 80 % Peau 71 % Muscles 73 %
 24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
