Imitrex 20 mg Solution pour pulvérisation nasale : Spray à usage unique pour administration intranasale. Le dispositif délivre 20 mg de
|
|
|
- Beatrice Gamache
- il y a 8 ans
- Total affichages :
Transcription
1 Société pharmaceutique (GLAXOSMITHKLINE) 1. DÉNOMINATION DU MÉDICAMENT Imitrex 10 mg Solution pour pulvérisation nasale. Imitrex 20 mg Solution pour pulvérisation nasale. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Imitrex 10 mg Solution pour pulvérisation nasale : Spray à usage unique pour administration intranasale. Le dispositif délivre 10 mg de sumatriptan dans 0,1 ml de solution aqueuse tamponnée. Imitrex 20 mg Solution pour pulvérisation nasale : Spray à usage unique pour administration intranasale. Le dispositif délivre 20 mg de sumatriptan dans 0,1 ml de solution aqueuse tamponnée. Pour la liste complète des excipients, voir rubrique FORME PHARMACEUTIQUE Solution pour pulvérisation nasale. Liquide limpide jaune pâle à jaune foncé, en flacons de verre dans un spray nasal à usage unique. 4. DONNÉES CLINIQUES 4.1 Indications thérapeutiques Imitrex Solution pour pulvérisation nasale est indiqué dans le traitement aigu des crises de migraine avec ou sans aura. 4.2 Posologie et mode d'administration Imitrex Solution pour pulvérisation nasale ne doit pas être utilisé en prophylaxie. La dose recommandée d Imitrex ne doit pas être dépassée. Imitrex est recommandé en monothérapie pour le traitement aigu d'une crise de migraine et ne doit pas être administré concomitamment avec l ergotamine ou des dérivés de l ergotamine (y compris le méthysergide) (voir rubrique 4.3). Il est conseillé de prendre Imitrex dès que possible après le début de la céphalée migraineuse, mais il est également efficace quel que soit le stade de la crise auquel il est administré. Adultes (18 ans et plus) La dose optimale d'imitrex Solution pour pulvérisation nasale est de 20 mg administrée dans une seule narine. Toutefois, vu la variabilité inter/intra patient tant des crises de migraine que de l'absorption du sumatriptan, une dose de 10 mg peut être efficace chez certains patients. Le patient qui ne répond pas à la première dose ne doit pas prendre une seconde dose au cours de la même crise. Toutefois, la crise pourra être traitée avec du paracétamol, de l acide acétylsalicylique ou des anti-inflammatoires non stéroïdiens. Imitrex pourra être utilisé pour les crises suivantes. Si le patient a répondu à la première dose mais que les symptômes réapparaissent, une seconde dose peut être prise dans les 24 heures suivantes à condition de respecter un intervalle d'au moins deux heures entre les deux administrations. Ne pas utiliser plus de deux doses d Imitrex Solution pour pulvérisation nasale à 20 mg par 24 heures. Adolescents (12 à 17 ans) L'utilisation du sumatriptan chez les adolescents doit se faire sous la recommandation d'un spécialiste ou d'un médecin généraliste expérimenté dans le traitement de la migraine, en tenant compte des lignes de conduites locales. La dose recommandée d'imitrex Solution pour pulvérisation nasale est de 10 mg administrée dans une seule narine. Le patient qui ne répond pas à la première dose ne doit pas prendre une seconde dose d'imitrex au cours de la même crise. Toutefois, la crise pourra être traitée avec du paracétamol, de l acide acétylsalicylique ou des anti-inflammatoires non stéroïdiens. Imitrex pourra être utilisé pour les crises suivantes.
2 Si le patient a répondu à la première dose mais que les symptômes réapparaissent, une seconde dose peut être prise dans les 24 heures suivantes à condition de respecter un intervalle d'au moins 2 heures entre les deux administrations. Ne pas utiliser plus de deux doses d Imitrex Solution pour pulvérisation nasale à 10 mg par 24 heures. Enfants (de moins de 12ans) L utilisation d Imitrex Solution n est pas recommandée chez les enfants de moins de 12 ans car il n y a pas de données suffisantes concernant l'innocuité et l'efficacité. Sujets âgés (de plus de 65 ans) Il n'y a pas de données concernant l'utilisation d'imitrex Solution pour pulvérisation nasale chez les patients de plus de 65 ans. La pharmacocinétique n'a pas été suffisamment étudiée chez les patients âgés. L'utilisation du sumatriptan n'est donc pas recommandée avant que l'on ne dispose de données supplémentaires. 4.3 Contre-indications Hypersensibilité au sumatriptan ou à l'un des excipients mentionnés à la rubrique 6.1. Le sumatriptan ne doit pas être administré aux patients qui ont eu un infarctus du myocarde ou qui souffrent d'une cardiomyopathie ischémique, d'un vasospasme coronarien (angor de Prinzmetal), d'une atteinte vasculaire périphérique ou aux patients présentant des symptômes ou des signes évoquant une cardiomyopathie ischémique. Le sumatriptan ne doit pas être administré aux patients présentant des antécédents d'accident vasculaire cérébral (AVC) ou d'accidents ischémiques transitoires (AIT). Le sumatriptan ne doit pas être administré à des patients présentant une insuffisance hépatique sévère. L'utilisation du sumatriptan est contre-indiquée chez des patients souffrant d hypertension modérée ou sévère et chez des patients souffrant d hypertension légère non contrôlée. L'administration concomitante d'ergotamine ou de dérivés de l'ergotamine (y compris le méthysergide) ou d un triptan/agoniste des récepteurs de la 5-hydroxytryptamine 1 (5-HT 1 ) est contre-indiquée (voir rubrique 4.5). L administration concomitante d inhibiteurs de la monoamine oxydase (IMAO) et de sumatriptan est contre-indiquée. Imitrex ne doit pas être utilisé pendant les deux semaines qui suivent l'arrêt d'un traitement par des inhibiteurs de la monoamine oxydase. 4.4 Mises en garde spéciales et précautions d'emploi Imitrex Solution pour pulvérisation nasale ne doit être utilisé qu'après avoir clairement établi le diagnostic de migraine. Le sumatriptan n'est pas indiqué pour le traitement des migraines hémiplégiques, basilaires ou ophtalmiques. Avant d initier un traitement avec sumatriptan, il est nécessaire d'exclure des affections neurologiques potentiellement graves (par exemple : AVC, AIT) si le patient présente des symptômes atypiques ou s il n a pas reçu un diagnostic approprié pour l utilisation de sumatriptan. Après administration, le sumatriptan peut être associé à des symptômes transitoires dont des douleurs thoraciques et une sensation d'oppression, qui peuvent être intenses et englober la gorge (voir rubrique 4.8). Lorsque ces symptômes évoquent une maladie cardiaque ischémique, l administration du sumatriptan doit être interrompue et des investigations appropriées seront réalisées. Le sumatriptan ne peut être administré à des patients présentant des facteurs de risque de maladie cardiaque ischémique, y compris les patients qui sont des fumeurs invétérés ou qui utilisent des thérapies de substitution de nicotine, sans évaluation cardiovasculaire préalable (voir rubrique 4.3). Une attention particulière est requise pour les femmes post-ménopausées et les hommes de plus de 40 ans présentant les facteurs de risque susmentionnés. Néanmoins, ces examens peuvent ne pas identifier tous les patients atteints d une affection cardiaque et, dans de très rares cas, des patients sans atteinte cardiovasculaire sous-jacente ont eu un problème cardiaque grave ainsi que des adolescents (voir rubrique 4.8). Le sumatriptan doit être administré avec précaution aux patients souffrant d hypertension légère contrôlée, étant donné qu on a observé des élévations transitoires de la tension artérielle et de la résistance vasculaire périphérique chez une faible proportion de patients (voir rubrique 4.3). Après la mise sur le marché, il y a eu de rares rapports décrivant des cas de patients présentant un syndrome sérotoninergique (y compris altération de l état mental, instabilité autonome et troubles neuromusculaires) après l utilisation d un inhibiteur sélectif de la recapture de la sérotonine (ISRS) et de sumatriptan. Un syndrome sérotoninergique a été rapporté après traitement simultané par des triptans et des inhibiteurs de la recapture de la sérotonine et de la noradrénaline (IRSN).
3 Si un traitement concomitant par du sumatriptan et ISRS/IRSN est indiqué, une observation adéquate du patient est conseillée (voir rubrique 4.5). Le sumatriptan doit être administré avec précaution chez les patients atteints d'affections pouvant modifier significativement l'absorption, le métabolisme ou l'excrétion du médicament, par exemple en cas d'insuffisance hépatique (insuffisance légère à modérée (Grade Child Pugh A ou B) ; voir rubrique 5.2) ou insuffisance de la fonction rénale (voir rubrique 5.2). Le sumatriptan doit être utilisé avec précaution chez les patients avec des antécédents de convulsions ou d autres facteurs de risque qui diminuent le seuil de la crise convulsive, car des crises d épilepsie ont été rapportées en association avec le sumatriptan (voir rubrique 4.8). Les patients présentant une hypersensibilité connue aux sulfamidés, peuvent présenter des réactions allergiques après administration de sumatriptan. Ces réactions peuvent aller de l'hypersensibilité cutanée à la réaction anaphylactique. Les données concernant une allergie croisée sont limitées, cependant la prudence est recommandée avant d utiliser le sumatriptan chez ces patients. Des effets indésirables peuvent être plus habituels lors de l utilisation concomitante de triptans avec des préparations à base d herbes contenant du millepertuis (Hypericum perforatum). L utilisation prolongée de tout type d antalgique contre les céphalées peut aggraver celles-ci. En présence de cette situation, ou en cas de suspicion, il convient de consulter un médecin et d interrompre le traitement. Le diagnostic de céphalées par abus d antalgiques (CAA) doit être envisagé chez les patients qui présentent des céphalées fréquentes ou quotidiennes malgré (ou à cause de) la prise régulière de médicaments contre les céphalées. 4.5 Interactions avec d'autres médicaments et autres formes d'interactions On n'a pas mis en évidence d'interaction avec le propranolol, la flunarizine, le pizotifène ou l'alcool. Les données concernant l'interaction avec les médicaments contenant de l'ergotamine ou un autre triptan/agoniste des récepteurs 5- HT 1 sont limitées. Un risque accru de vasospasme coronarien est théoriquement possible. L'administration concomitante de ces deux produits est donc contre-indiquée (voir rubrique 4.3). Le délai à respecter entre l utilisation de sumatriptan et de préparations renfermant de l ergotamine ou un autre triptan/agoniste des récepteurs 5-HT 1 n est pas connu. Ceci dépend des doses et du type des produits utilisés. Les effets peuvent être additifs. Il est conseillé d attendre au moins 24 heures après l utilisation de préparations à base d ergotamine ou un autre triptan/agoniste des récepteurs 5-HT 1 avant d administrer du sumatriptan. Inversement, il est conseillé d attendre au moins 6 heures après la prise de sumatriptan avant d administrer un produit à base d ergotamine et au moins 24 heures avant d administrer un autre triptan/agoniste des récepteurs 5-HT 1. Une interaction peut également se produire entre le sumatriptan et les IMAOs. L'administration concomitante de ces deux produits est donc contre-indiquée (voir rubrique 4.3). Après la mise sur le marché, il y a eu de rares rapports décrivant des cas de patients présentant un syndrome sérotoninergique (y compris altération de l état mental, instabilité autonome et troubles neuromusculaires) après l administration d ISRS et de sumatriptan. Un syndrome sérotoninergique a également été rapporté après traitement simultané par des triptans et des IRSN (voir rubrique 4.4). 4.6 Fécondité, grossesse et allaitement Grossesse Des données de pharmacovigilance provenant de l utilisation du sumatriptan par plus de femmes au cours du premier trimestre de leur grossesse sont disponibles. Bien que les informations fournies par ces données soient insuffisantes pour tirer des conclusions définitives, elles n indiquent pas d augmentation du risque d anomalies congénitales. Les expériences relatives à l utilisation du sumatriptan au cours du deuxième et du troisième trimestre de la grossesse sont limitées. Les études expérimentales menées chez l animal n'ont pas mis en évidence d effets tératogènes directs, ni d effets délétères sur le développement péri- et post-natal. Cependant, la viabilité embryo-foetale peut être affectée chez les lapins (voir rubrique 5.3). L administration de sumatriptan ne doit être envisagée que si le bénéfice escompté pour la mère est supérieur à tout risque éventuel pour le foetus. Allaitement On a démontré qu après administration s.c., le sumatriptan est excrété dans le lait maternel. L exposition du nourrisson au produit peut être minimisée en évitant l allaitement pendant 12 heures après le traitement. Pendant cette durée le lait maternel doit être abandonné. 4.7 Effets sur l'aptitude à conduire des véhicules et à utiliser des machines Les effets sur l aptitude à conduire des véhicules et à utiliser des machines n ont pas été étudiés. Une somnolence due à la migraine ou
4 à au traitement par le sumatriptan peut survenir. Ceci peut influencer l'aptitude à conduire des véhicules et à utiliser des machines. 4.8 Effets indésirables Les effets indésirables sont listés ci-dessous par système d organe et par fréquence. Les fréquences sont définies de la manière suivante : très fréquent ( 1/10), fréquent ( 1/100, <1/10), peu fréquent ( 1/1000, <1/100), rare ( 1/10000, <1/1000), très rare (<1/10000), fréquence indéterminée (ne peut être estimée sur base des données disponibles). Certains symptômes rapportés comme effets indésirables peuvent être liés à la migraine. Des événements indésirables rapportés chez l adulte ont également été observés chez l adolescent. Ces effets indésirables incluent de très rares rapports décrivant des cas de vasospasme coronaire et d infarctus du myocarde (voir rubrique 4.4). Affections du système immunitaire Fréquence indéterminée : Réactions d hypersensibilité allant de l hypersensibilité cutanée (par exemple urticaire) à des réactions anaphylactiques. Affections du système nerveux Très fréquent : Dysgueusie/goût désagréable. Fréquent : Vertiges, somnolence, troubles sensitifs notamment des paresthésies et de l hypoesthésie Fréquence indéterminée: Crises d épilepsie. Bien que certaines de ces crises se soient produites chez des patients présentant des antécédents d épilepsie ou des facteurs favorisants, des cas ont été rapportés chez des patients ne présentant aucune prédisposition. Trémor, dystonie, nystagmus, scotome. Affections oculaires Fréquence indéterminée : Scintillements, diplopie, diminution de l acuité visuelle. Perte de vision, incluant des cas de déficiences permanentes. Cependant, ces troubles visuels peuvent également apparaître au cours de la crise migraineuse elle-même. Affections cardiaques Fréquence indéterminée: Bradycardie, tachycardie, palpitations, arythmies cardiaques, signes d ischémie transitoire à l ECG, spasmes coronariens, angor, infarctus du myocarde (voir rubriques 4.3 et 4.4). Affections vasculaires Fréquent : Augmentations transitoires de la pression artérielle survenant juste après le traitement, bouffées de chaleur. Fréquence indéterminée : Hypotension, syndrome de Raynaud. Affections respiratoires, thoraciques et médiastinales Fréquent : Après administration de sumatriptan solution pour pulvérisation nasale, une irritation légère et transitoire ou une sensation de brûlure au niveau du nez ou de la gorge, et de l épistaxis ont été rapportés. Dyspnée. Affections gastro-intestinales Fréquent : Des nausées et des vomissements sont survenus chez certains patients mais il n est pas clair si ces effets sont liés au sumatriptan ou à la condition sous-jacente. Fréquence indéterminée: Colite ischémique. Fréquence indéterminée: Diarrhée. Affections musculo-squelettiques et du tissu conjonctif Fréquent : Sensations de lourdeur (habituellement transitoires, mais peuvent être intenses et affecter n importe quelle partie du corps, y compris la poitrine et la gorge). Myalgie Fréquence indéterminée: Raideur de la nuque. Fréquence indéterminée: Arthralgie. Troubles généraux et anomalies au site d administration Fréquent : Douleur, sensations de chaleur ou de froid, de pression ou d oppression (ces effets sont habituellement transitoires, mais peuvent être intenses et affecter n importe quelle partie du corps, y compris la poitrine et la gorge). Sensations de faiblesse, fatigue (ces deux effets sont le plus souvent d intensité faible à modérée et transitoires). Investigations Très rare : Des perturbations mineures des tests de la fonction hépatique ont été occasionnellement observées. Affections psychiatriques Fréquence indéterminée: Anxiété. Affections de la peau et du tissu sous-cutané Fréquence indéterminée: Hyperhidrose.
5 Déclaration des effets indésirables suspectés La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration: Belgique Agence fédérale des médicaments et des produits de santé Division Vigilance EUROSTATION II Place Victor Horta, 40/40 B-1060 Bruxelles Site internet: Luxembourg Direction de la Santé Division de la Pharmacie et des Médicaments Villa Louvigny Allée Marconi L-2120 Luxembourg Site internet: Surdosage Des doses uniques de sumatriptan allant jusqu'à 40 mg par voie intranasale, dépassant 16 mg par voie sous-cutanée et de 400 mg par voie orale n'ont pas entraîné d'effets indésirables autres que ceux mentionnés. Dans les études cliniques, des volontaires ont reçu 20 mg de sumatriptan par voie intranasale 3 fois par jour pendant 4 jours sans présenter d'effets indésirables significatifs. En cas de surdosage, le patient doit être gardé sous surveillance pendant au moins 10 heures et si nécessaire, un traitement standard de soutien doit être instauré. L'effet de l'hémodialyse ou de la dialyse péritonéale sur les concentrations plasmatiques de sumatriptan n'est pas connu. 5. PROPRIÉTÉS PHARMACOLOGIQUES 5.1 Propriétés pharmacodynamiques Groupe pharmacothérapeutique : agonistes sélectifs des récepteurs à la 5-HT 1. Code ATC : N02CC01. Le sumatriptan est un agoniste sélectif des récepteurs vasculaires à la 5-hydroxytryptamine-1 (5-HT 1d ) sans effet sur les autres soustypes de récepteurs 5-HT (5-HT 2 à 5-HT 7 ). Les récepteurs vasculaires 5-HT 1d sont localisés principalement au niveau des vaisseaux sanguins crâniens et induisent une vasoconstriction. Chez l'animal, le sumatriptan provoque une vasoconstriction sélective de la circulation artérielle carotidienne. La circulation artérielle carotidienne vascularise les tissus extracrâniens et intracrâniens tels que les méninges et on pense que la dilatation et/ou la formation d'un œdème au niveau de ces vaisseaux pourraient être le mécanisme sousjacent de la migraine chez l'homme. De plus, les études chez l'animal suggèrent une inhibition de l'activité du nerf trijumeau par le sumatriptan. Ces deux actions (vasoconstriction crânienne et inhibition de l'activité du nerf trijumeau) peuvent contribuer à l'action antimigraineuse du sumatriptan chez l'homme. La réponse clinique débute 15 minutes après l'administration d'une dose de 20 mg par voie intranasale. Etant donné sa voie d administration, Imitrex Solution pour pulvérisation nasale convient particulièrement aux patients présentant des nausées et vomissements pendant la crise de migraine. L'importance de l'effet du traitement est plus faible chez les adolescents par comparaison aux adultes. 5.2 Propriétés pharmacocinétiques Après administration intranasale, le sumatriptan est rapidement absorbé, le temps médian pour atteindre les concentrations plasmatiques maximales étant de 1,5 heures (intervalle : 0,25-3) chez les adultes et de 2 heures (intervalle : 0,5-3) chez les adolescents. Après une dose de 20 mg, la concentration maximale moyenne est de 13 ng/ml. La biodisponibilité moyenne par voie intranasale par rapport à l'administration sous-cutanée est d'environ 16 %, ceci étant du en partie au métabolisme pré-systémique. La liaison aux protéines plasmatiques est faible (14-21 %), le volume moyen de distribution est de 170 litres. La demi-vie d'élimination est d'environ 2 heures. La clairance plasmatique totale moyenne est d'environ 1160 ml/min et la clairance plasmatique rénale moyenne est d'environ 260 ml/min. Une étude pharmacocinétique chez les adolescents (12-17 ans) a montré que la concentration plasmatique maximale moyenne était de 13,9 ng/ml et que la demi-vie d'élimination moyenne était d'environ 2 heures après administration intranasale d'une dose de 20 mg. La modélisation pharmacocinétique de la population étudiée a montré que la clairance et le volume de distribution augmentaient tous les
6 deux en fonction de la taille chez la population adolescente, résultant en une exposition plus élevée chez les adolescents de faible poids corporel. La clairance non rénale représente environ 80 % de la clairance totale. Le sumatriptan est essentiellement éliminé par métabolisme oxydatif via la monoamine oxydase A. Le métabolite principal, l'analogue acide indolacétique du sumatriptan, est principalement excrété dans les urines sous formes d'acide libre et glucuroconjuguée. Il n'a pas d'activité 5-HT 1 ou 5-HT 2 connue. Des métabolites mineurs n'ont pas été identifiés. Le profil pharmacocinétique du sumatriptan par voie intranasale ne semble pas être significativement modifié par la crise de migraine. Populations particulières Personnes âgées (de plus de 65 ans) La cinétique chez les patients âgés a été insuffisamment étudiée pour justifier une différence possible de la cinétique entre les sujets âgés et les volontaires jeunes. Insuffisance hépatique La pharmacocinétique du sumatriptan a été étudiée après l administration d une dose orale (50 mg) et d une dose sous-cutanée (s.c. 6 mg) chez 8 patients atteints d insuffisance hépatique légère à modérée appariés en termes de sexe, d âge et de poids avec 8 sujets sains. Après une dose orale, les concentrations plasmatiques de sumatriptan (ASC et Cmax) ont presque doublé (augmentation d environ 80 %) chez les patients atteints d une insuffisance hépatique légère à modérée par rapport aux sujets témoins avec fonction hépatique normale. Aucune différence n a été constatée entre les patients insuffisants hépatiques et les sujets témoins après la dose s.c. Ceci indique qu une insuffisance hépatique légère à modérée réduit la clairance présystémique et augmente la biodisponibilité et l exposition au sumatriptan par rapport à une fonction hépatique normale. Après administration orale, la clairance présystémique est réduite chez les patients atteints d insuffisance hépatique légère à modérée, tandis que les concentrations plasmatiques, mesurées sur la base de la Cmax et de l ASC, ont pratiquement doublé. Une certaine proportion du spray nasal étant avalée, les patients atteints d insuffisance hépatique légère à modérée pourraient également présenter des concentrations plus élevées, mais dans une moindre mesure que celles observées après une administration orale. (Voir rubrique 4.4, Mises en garde spéciales et précautions d emploi). La pharmacocinétique du sumatriptan chez les patients atteints d insuffisance hépatique grave n a pas été étudiée (voir rubrique 4.3 Contre-indications et rubrique 4.4 Mises en garde spéciales et précautions d emploi). 5.3 Données de sécurité précliniques Dans les études évaluant le pouvoir irritant local et oculaire, aucune irritation nasale n'a été observée chez l'animal de laboratoire après administration de sumatriptan en spray nasal et aucune irritation oculaire n'a été observée après application directe du spray sur les yeux des lapins. Des études expérimentales de toxicité aigue et chronique n ont pas mis en évidence d effets toxiques aux doses thérapeutiques utilisées chez l homme. Lors des études de fertilité chez le rat, on a observé une diminution du taux de réussite des inséminations lors d expositions à des doses largement supérieures aux doses maximales pour l homme. Chez les lapins, on a observé une embryoléthalité sans effets tératogènes marqués. Le sumatriptan est dépourvu d activité génotoxique et carcinogène in vitro et dans les études animales. 6. DONNÉES PHARMACEUTIQUES 6.1 Liste des excipients - Phosphate monopotassique - Phosphate disodique anhydre - Acide sulfurique - Hydroxyde de sodium - Eau purifiée 6.2 Incompatibilités Pas d application. 6.3 Durée de conservation 3 ans. 6.4 Précautions particulières de conservation A conserver à une température ne dépassant pas 30 C. Ne pas congeler. A conserver dans sa plaquette scellée, de préférence dans la boîte, à l'abri de la lumière.
7 6.5 Nature et contenu de l emballage extérieur Le récipient consiste en un flacon en verre type I Ph.Eur. avec un bouchon en caoutchouc et un applicateur. Imitrex 10 mg Solution pour pulvérisation nasale: spray à usage unique contenant 0,1ml de solution. Boîtes de 1, 2, 4, 6, 12 ou 18 sprays. Imitrex 20 mg Solution pour pulvérisation nasale: spray à usage unique contenant 0,1ml de solution. Boîtes de 1, 2, 4, 6, 12 ou 18 sprays. Toutes les présentations peuvent ne pas être commercialisées. 6.6 Précautions particulières d élimination Pas d exigences particulières. 7. TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHÉ GlaxoSmithKline Pharmaceuticals s.a./n.v. Site Apollo Avenue Pascal, B-1300 Wavre 8. NUMÉROS D'AUTORISATION DE MISE SUR LE MARCHÉ Imitrex 10mg Solution pour pulvérisation nasale : BE Imitrex 20mg Solution pour pulvérisation nasale : BE DATE DE PREMIÈRE AUTORISATION/DE RENOUVELLEMENT DE L'AUTORISATION Date de première autorisation Imitrex 10mg Solution pour pulvérisation nasale : 05/05/1997 Imitrex 20mg Solution pour pulvérisation nasale : 05/05/1997 Date de dernier renouvellement : Imitrex 10mg Solution pour pulvérisation nasale : 14/06/2006 Imitrex 20mg Solution pour pulvérisation nasale : 14/06/ DATE DE MISE À JOUR DU TEXTE 11/2014 (version 31) MODE DE DELIVRANCE : Sur prescription médicale Classification ATC5 Classe N02CC01 Description SYSTEME NERVEUX CENTRAL ANALGESIQUES ANTIMIGRAINEUX AGONISTES DES RECEPTEURS 5HT1 SELECTIFS (TRIPTANS) SUMATRIPTAN Prix Nom Conditionnement CNK Prix Rb Type IMITREX solution pour pulvérisation nasale 10 mg et 20 mg 6 SPRAY 10MG ,80 D Original IMITREX solution pour pulvérisation nasale 10 mg et 20 mg 6 SPRAY 20MG ,40 D Original
IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie
 1 sur 6 13/09/2010 16:58 Mis à jour : 23/02/2009 1. DENOMINATION DU MEDICAMENT IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
1 sur 6 13/09/2010 16:58 Mis à jour : 23/02/2009 1. DENOMINATION DU MEDICAMENT IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT 2. COMPOSITION QUALITATIVE ET QUANTITATIVE 3. FORME PHARMACEUTIQUE 4. DONNEES CLINIQUES 4.1. Indications thérapeutiques 4.2.
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT 2. COMPOSITION QUALITATIVE ET QUANTITATIVE 3. FORME PHARMACEUTIQUE 4. DONNEES CLINIQUES 4.1. Indications thérapeutiques 4.2.
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT NARATRIPTAN ARROW 2,5 mg, comprimé pelliculé 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Naratriptan..2,50 mg Sous forme de
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT NARATRIPTAN ARROW 2,5 mg, comprimé pelliculé 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Naratriptan..2,50 mg Sous forme de
NOTICE: INFORMATION DE L UTILISATEUR. Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan
 NOTICE: INFORMATION DE L UTILISATEUR Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan Veuillez lire attentivement l'intégralité de cette notice avant
NOTICE: INFORMATION DE L UTILISATEUR Sumatriptan Teva 50 mg comprimés pelliculés Sumatriptan Teva 100 mg comprimés pelliculés sumatriptan Veuillez lire attentivement l'intégralité de cette notice avant
Les triptans. quel casse-tête! Kim Messier et Michel Lapierre. Vous voulez prescrire des triptans? Lisez ce qui suit!
 Fédération des médecins omnipraticiens du Québec Les triptans quel casse-tête! Kim Messier et Michel Lapierre Vous voulez prescrire des triptans? Lisez ce qui suit! Les triptans, des agonistes sélectifs
Fédération des médecins omnipraticiens du Québec Les triptans quel casse-tête! Kim Messier et Michel Lapierre Vous voulez prescrire des triptans? Lisez ce qui suit! Les triptans, des agonistes sélectifs
RELPAX. hydrobromure d élétriptan
 RELPAX hydrobromure d élétriptan * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques * Conclusion * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques *
RELPAX hydrobromure d élétriptan * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques * Conclusion * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques *
NOTICE : INFORMATION DE L UTILISATEUR. Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés. sumatriptan
 NOTICE : INFORMATION DE L UTILISATEUR Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés sumatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament. - Gardez
NOTICE : INFORMATION DE L UTILISATEUR Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés sumatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament. - Gardez
ANNEXE 1116 NOTICE : INFORMATION DE L ' UTILISATEUR. ZOlMITRIPTAN ARCHIE SAMUEL 2,5 mg, comprimé orodispersible. Zolmitriptan
 ANNEXE 1116 NOTICE : INFORMATION DE L ' UTILISATEUR 1 Dénomination du médicament ZOlMITRIPTAN ARCHIE SAMUEL 2,5 mg, comprimé orodispersible 1 Encadré Zolmitriptan Veuillez lire attentivement l'intégralité
ANNEXE 1116 NOTICE : INFORMATION DE L ' UTILISATEUR 1 Dénomination du médicament ZOlMITRIPTAN ARCHIE SAMUEL 2,5 mg, comprimé orodispersible 1 Encadré Zolmitriptan Veuillez lire attentivement l'intégralité
NOTICE: INFORMATION DE L UTILISATEUR
 NOTICE: INFORMATION DE L UTILISATEUR MIGARD 2,5 mg comprimés pelliculés frovatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR MIGARD 2,5 mg comprimés pelliculés frovatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
Monographie de produit
 Monographie de produit Pr FROVA MD Comprimés de succinate de frovatriptan frovatriptan à 2,5 mg Agoniste des récepteurs de sous-type 5-HT 1 Antimigraineux Endo Pharmaceuticals, Inc. 100 Endo Boulevard
Monographie de produit Pr FROVA MD Comprimés de succinate de frovatriptan frovatriptan à 2,5 mg Agoniste des récepteurs de sous-type 5-HT 1 Antimigraineux Endo Pharmaceuticals, Inc. 100 Endo Boulevard
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
NOTICE : INFORMATION DE L'UTILISATEUR. DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc
 NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
Atrovent HFA 20 mcg/bouffée solution pour inhalation en flacon pressurisé (bromure d'ipratropium)
 NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
DU BON USAGE DES TRIPTANS DANS LA MIGRAINE
 DU BON USAGE DES TRIPTANS DANS LA MIGRAINE SEPTEMBRE 2009 A. AUTRET, TOURS au moins 5 crises : de MIGRAINE SANS AURA 4 72 heures, 2 des caractères : 1 signe d accompagnement : modérée ou sévère, pulsatile,
DU BON USAGE DES TRIPTANS DANS LA MIGRAINE SEPTEMBRE 2009 A. AUTRET, TOURS au moins 5 crises : de MIGRAINE SANS AURA 4 72 heures, 2 des caractères : 1 signe d accompagnement : modérée ou sévère, pulsatile,
MONOGRAPHIE DE PRODUIT
 MONOGRAPHIE DE PRODUIT Pr AMERGE (naratriptan sous forme de chlorhydrate de naratriptan) Comprimés à 1 mg et à 2,5 mg Agoniste des récepteurs 5-HT 1 Antimigraineux GlaxoSmithKline Inc. 7333 Mississauga
MONOGRAPHIE DE PRODUIT Pr AMERGE (naratriptan sous forme de chlorhydrate de naratriptan) Comprimés à 1 mg et à 2,5 mg Agoniste des récepteurs 5-HT 1 Antimigraineux GlaxoSmithKline Inc. 7333 Mississauga
LES ANTIMIGRAINEUX. Médicaments de la crise et médicaments de fond
 LES ANTIMIGRAINEUX Migraine : maladie qui peut être handicapante selon fréquence, durée, intensité des crises, signes d accompagnement (digestifs), retentissement sur la vie quotidienne, professionnelle,
LES ANTIMIGRAINEUX Migraine : maladie qui peut être handicapante selon fréquence, durée, intensité des crises, signes d accompagnement (digestifs), retentissement sur la vie quotidienne, professionnelle,
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT. Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl par comprimé enrobé.
 RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1. Dé nomination du mé dicame nt Bisolax 5 mg comprimés enrobés. 2. Composition qualitative e t quantitative Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1. Dé nomination du mé dicame nt Bisolax 5 mg comprimés enrobés. 2. Composition qualitative e t quantitative Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl
Notice : information de l utilisateur. Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine
 Notice : information de l utilisateur Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine Veuillez lire attentivement cette notice avant de prendre ce médicament
Notice : information de l utilisateur Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine Veuillez lire attentivement cette notice avant de prendre ce médicament
TRAITEMENT DE LA MIGRAINE. programme aux résidents de neurologie
 TRAITEMENT DE LA MIGRAINE programme aux résidents de neurologie LA MIGRAINE Classification I.H.S. 1.1 Migraine sans aura 1.2 Migraine avec aura 1.2.1 Migraine avec aura typique 1.2.2 Migraine avec aura
TRAITEMENT DE LA MIGRAINE programme aux résidents de neurologie LA MIGRAINE Classification I.H.S. 1.1 Migraine sans aura 1.2 Migraine avec aura 1.2.1 Migraine avec aura typique 1.2.2 Migraine avec aura
Migraine : traitement de la crise. Comment utiliser les triptans?
 Migraine : traitement de la crise Comment utiliser les triptans? 6 ème congrès national de lutte contre la douleur 19-20 Mars Alger Alain Serrie Service de Médecine de la douleur, médecine palliative et
Migraine : traitement de la crise Comment utiliser les triptans? 6 ème congrès national de lutte contre la douleur 19-20 Mars Alger Alain Serrie Service de Médecine de la douleur, médecine palliative et
La migraine. Foramen ovale perméable. Infarctus cérébral (surtout chez la femme)
 La migraine 1/Introduction : Céphalée primaire (sans lésion sous-jacente). Deux variétés principales: Migraine sans aura (migraine commune). Migraine avec aura (migraine accompagnée). Diagnostic: interrogatoire
La migraine 1/Introduction : Céphalée primaire (sans lésion sous-jacente). Deux variétés principales: Migraine sans aura (migraine commune). Migraine avec aura (migraine accompagnée). Diagnostic: interrogatoire
XARELTO (RIVAROXABAN) 2,5 MG - 15 MG - 20 MG, COMPRIMÉS PELLICULÉS GUIDE DE PRESCRIPTION
 Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament Xarelto 2,5 mg; 15 mg et 20 mg de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique
Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament Xarelto 2,5 mg; 15 mg et 20 mg de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique
NOTICE: INFORMATION DE L UTILISATEUR. Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain)
 NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
MIGRAINE - TRAITEMENT
 MIGRAINE - TRAITEMENT Restauration d une bonne qualité de vie Adapté à chaque patient Reposant sur trois axes : éviction des facteurs déclenchants traitement de crise traitement prophylactique ANAES 2002
MIGRAINE - TRAITEMENT Restauration d une bonne qualité de vie Adapté à chaque patient Reposant sur trois axes : éviction des facteurs déclenchants traitement de crise traitement prophylactique ANAES 2002
PIL Décembre 2009. Autres composants: acide tartrique, macrogol 4000, macrogol 1000, macrogol 400, butylhydroxyanisol.
 Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique PERDOLAN - PÉDIATRIE
 Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
MONOGRAPHIE DE PRODUIT
 MONOGRAPHIE DE PRODUIT Pr AXERT comprimés de malate d almotriptan 6,25 mg et 12,5 mg d almotriptan Agoniste des récepteurs 5-HT 1 Traitement antimigraineux Cette monographie de produit est la propriété
MONOGRAPHIE DE PRODUIT Pr AXERT comprimés de malate d almotriptan 6,25 mg et 12,5 mg d almotriptan Agoniste des récepteurs 5-HT 1 Traitement antimigraineux Cette monographie de produit est la propriété
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine
 KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR. Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants. Acide acétylsalicylique
 NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
Carnet de suivi Lithium
 Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013
 NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
Dossier d information sur les bêtabloquants
 Dossier d information sur les bêtabloquants Septembre 2014 I. Rappel sur les récepteurs bêta-adrénergiques Il y a actuellement 3 sortes de récepteurs bêta-adrénergiques connus: - Les récepteurs 1 qui sont
Dossier d information sur les bêtabloquants Septembre 2014 I. Rappel sur les récepteurs bêta-adrénergiques Il y a actuellement 3 sortes de récepteurs bêta-adrénergiques connus: - Les récepteurs 1 qui sont
Céphalées. 1- Mise au point sur la migraine 2- Quand s inquiéter face à une céphalée. APP du DENAISIS
 Céphalées 1- Mise au point sur la migraine 2- Quand s inquiéter face à une céphalée EPU DENAIN -14 novembre 2006 Dr Kubat-Majid14 novembre 2006 Dr KUBAT-MAJID Céphalées 1 Mise au point sur la migraine
Céphalées 1- Mise au point sur la migraine 2- Quand s inquiéter face à une céphalée EPU DENAIN -14 novembre 2006 Dr Kubat-Majid14 novembre 2006 Dr KUBAT-MAJID Céphalées 1 Mise au point sur la migraine
NOTICE : INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés Bisacodyl
 NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène
 NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
Point d Information. Le PRAC a recommandé que le RCP soit modifié afin d inclure les informations suivantes:
 Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
ÉVALUATION DE LA PERSONNE ATTEINTE D HYPERTENSION ARTÉRIELLE
 ÉVALUATION DE LA PERSONNE ATTEINTE D HYPERTENSION ARTÉRIELLE PRISE EN CHARGE SYSTÉMATISÉE DES PERSONNES ATTEINTES D HYPERTENSION ARTÉRIELLE SOCIÉTÉ QUÉBÉCOISE D HYPERTENSION ARTÉRIELLE 23 ÉVALUATION DE
ÉVALUATION DE LA PERSONNE ATTEINTE D HYPERTENSION ARTÉRIELLE PRISE EN CHARGE SYSTÉMATISÉE DES PERSONNES ATTEINTES D HYPERTENSION ARTÉRIELLE SOCIÉTÉ QUÉBÉCOISE D HYPERTENSION ARTÉRIELLE 23 ÉVALUATION DE
SEROTONINE ET MEDICAMENTS
 Chapitre 9 SEROTONINE ET MEDICAMENTS Item 176 : Prescription et surveillance des Psychotropes Item 262 : Migraine et algies de la face La sérotonine et les médicaments interférant avec les systèmes sérotoninergiques
Chapitre 9 SEROTONINE ET MEDICAMENTS Item 176 : Prescription et surveillance des Psychotropes Item 262 : Migraine et algies de la face La sérotonine et les médicaments interférant avec les systèmes sérotoninergiques
NOTICE: INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés. Bisacodyl
 NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
Migraine et Abus de Médicaments
 Migraine et Abus de Médicaments Approches diagnostiques et thérapeutiques des Céphalées Chroniques Quotidiennes Pr D. DEPLANQUE Département de Pharmacologie médicale EA 1046, Institut de Médecine Prédictive
Migraine et Abus de Médicaments Approches diagnostiques et thérapeutiques des Céphalées Chroniques Quotidiennes Pr D. DEPLANQUE Département de Pharmacologie médicale EA 1046, Institut de Médecine Prédictive
Bien vous soigner. avec des médicaments disponibles sans ordonnance. juin 2008. Douleur. de l adulte
 Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
COMMISSION DE LA TRANSPARENCE AVIS. 23 mai 2012
 COMMISSION DE LA TRANSPARENCE AVIS 23 mai 2012 SEGLOR 5 mg, gélule B/30 (CIP: 321 899-8) SEGLOR LYOC 5 mg, lyophilisat oral B/30 (CIP: 334 062-4) Laboratoire UCB PHARMA dihydroergotamine (mésilate de)
COMMISSION DE LA TRANSPARENCE AVIS 23 mai 2012 SEGLOR 5 mg, gélule B/30 (CIP: 321 899-8) SEGLOR LYOC 5 mg, lyophilisat oral B/30 (CIP: 334 062-4) Laboratoire UCB PHARMA dihydroergotamine (mésilate de)
 Les Migraines et les céphalées. Dr G.Hinzelin Migraines et Céphalées Migraines et Céphalées La migraine représente entre 5 à 18% de la population française selon le sexe et en fonction des études. Est
Les Migraines et les céphalées. Dr G.Hinzelin Migraines et Céphalées Migraines et Céphalées La migraine représente entre 5 à 18% de la population française selon le sexe et en fonction des études. Est
NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR. Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant
 B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
La migraine ANEPF ANEPF ANEPF. Chapitre 5. ANEPF Migraine 23/10/02 15:47 Page 1 NEPF ANEPF ANEPF ANEPF ANEPF ANEPF ANEPF ANEPF ANEPF ANEPF AN
 Migraine 23/10/02 15:47 Page 1 Chapitre 5 N N F La migraine 1 AN PF PF Migraine 23/10/02 15:47 Page 2 Chapitre 5 : La migraine Deuxième Partie AN ANE F La migraine est une affection très fréquente, souvent
Migraine 23/10/02 15:47 Page 1 Chapitre 5 N N F La migraine 1 AN PF PF Migraine 23/10/02 15:47 Page 2 Chapitre 5 : La migraine Deuxième Partie AN ANE F La migraine est une affection très fréquente, souvent
Observation. Merci à l équipe de pharmaciens FormUtip iatro pour ce cas
 Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Les nouveaux triptans dans la migraine
 Les nouveaux triptans dans la migraine J.M. Senard*, N. Fabre** P O I N T S F O R T S P O I N T S F O R T S Comme le sumatriptan, ce sont des agonistes sérotoninergiques 5HT1B/D ayant une action périphérique
Les nouveaux triptans dans la migraine J.M. Senard*, N. Fabre** P O I N T S F O R T S P O I N T S F O R T S Comme le sumatriptan, ce sont des agonistes sérotoninergiques 5HT1B/D ayant une action périphérique
La migraine : quelle prise de tête!
 La migraine : quelle prise de tête! Introduction La migraine est une véritable «prise de tête» pour les personnes qui en souffrent! Bien au-delà d un mal physique, cette réelle maladie engendre également
La migraine : quelle prise de tête! Introduction La migraine est une véritable «prise de tête» pour les personnes qui en souffrent! Bien au-delà d un mal physique, cette réelle maladie engendre également
Diabète Type 2. Épidémiologie Aspects physiques Aspects physiologiques
 Diabète Type 2 Épidémiologie Aspects physiques Aspects physiologiques Épidémiologie 90% de tous les cas de diabètes Environ 1 personne sur 20 est atteinte Diabète gras Facteur de risque majeur pour les
Diabète Type 2 Épidémiologie Aspects physiques Aspects physiologiques Épidémiologie 90% de tous les cas de diabètes Environ 1 personne sur 20 est atteinte Diabète gras Facteur de risque majeur pour les
Carte de soins et d urgence
 Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION. 10 octobre 2001
 COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
Votre guide des définitions des maladies graves de l Assurance maladies graves express
 Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
NOTICE : INFORMATION DE L UTILISATEUR. Delphi 0,1 % crème Acétonide de triamcinolone
 NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine
 NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament.
La prise en charge de votre insuffisance cardiaque
 G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre insuffisance cardiaque Vivre avec une insuffisance cardiaque Décembre 2007 Pourquoi ce guide? Votre médecin traitant
G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre insuffisance cardiaque Vivre avec une insuffisance cardiaque Décembre 2007 Pourquoi ce guide? Votre médecin traitant
neurogénétique Structures sensibles du crâne 11/02/10 Classification internationale des céphalées:2004
 11/02/10 Structures sensibles du crâne neurogénétique Cheveux Cuir chevelu Tissu sous cutané Périoste Os Dure mère Méninges molles Cerveau vaisseaux MIGRAINE:PHYSIOPATHOLOGIE MIGRAINE:PHYSIOPATHOLOGIE
11/02/10 Structures sensibles du crâne neurogénétique Cheveux Cuir chevelu Tissu sous cutané Périoste Os Dure mère Méninges molles Cerveau vaisseaux MIGRAINE:PHYSIOPATHOLOGIE MIGRAINE:PHYSIOPATHOLOGIE
Information transmise sous l autorité de l Agence fédérale des médicaments et des produits de santé
 Les Direct Healthcare Professional Communications (DHPC) sont des courriers envoyés aux professionnels de la santé par les firmes pharmaceutiques, afin de les informer de risques potentiels apparus lors
Les Direct Healthcare Professional Communications (DHPC) sont des courriers envoyés aux professionnels de la santé par les firmes pharmaceutiques, afin de les informer de risques potentiels apparus lors
CEPHALEES CHRONIQUES QUOTIDIENNES AVEC ABUS MEDICAMENTEUX
 CEPHALEES CHRONIQUES QUOTIDIENNES AVEC ABUS MEDICAMENTEUX Groupe de travail du RRDBN Y.Perier, A.S.Sergent, E.Touchard, V.Lepelletier, S.Sladek FMC 2009 1 PLAN Migraine sans aura Epidémiologie Critères
CEPHALEES CHRONIQUES QUOTIDIENNES AVEC ABUS MEDICAMENTEUX Groupe de travail du RRDBN Y.Perier, A.S.Sergent, E.Touchard, V.Lepelletier, S.Sladek FMC 2009 1 PLAN Migraine sans aura Epidémiologie Critères
Mieux informé sur la maladie de reflux
 Information destinée aux patients Mieux informé sur la maladie de reflux Les médicaments à l arc-en-ciel Mise à jour de l'information: septembre 2013 «Maladie de reflux» Maladie de reflux La maladie de
Information destinée aux patients Mieux informé sur la maladie de reflux Les médicaments à l arc-en-ciel Mise à jour de l'information: septembre 2013 «Maladie de reflux» Maladie de reflux La maladie de
NOTICE : INFORMATION DE L UTILISATEUR. Acidozol 10 mg, gélules gastro-résistantes Oméprazole
 La notice, 1/4/2014 NOTICE : INFORMATION DE L UTILISATEUR Acidozol 10 mg, gélules gastro-résistantes Oméprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient
La notice, 1/4/2014 NOTICE : INFORMATION DE L UTILISATEUR Acidozol 10 mg, gélules gastro-résistantes Oméprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES :
 FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
Protéger. son animal. la gamme FRONTLINE. grâce à la gamme. Contre les puces et les tiques. Efficace plusieurs semaines (1) Résistant à la pluie,
 la gamme Frontline Contre les puces et les tiques Efficace plusieurs semaines (1) Résistant à la pluie, aux bains et aux shampooings (2) Protéger son animal grâce à la gamme FRONTLINE La gamme FRONTLINE
la gamme Frontline Contre les puces et les tiques Efficace plusieurs semaines (1) Résistant à la pluie, aux bains et aux shampooings (2) Protéger son animal grâce à la gamme FRONTLINE La gamme FRONTLINE
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR. APO-CITALOPRAM Comprimés de citalopram USP
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr APO-CITALOPRAM Comprimés de citalopram USP Cette notice est la troisième partie de la monographie du produit APO-CITALOPRAM, publiée lorsque le médicament
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr APO-CITALOPRAM Comprimés de citalopram USP Cette notice est la troisième partie de la monographie du produit APO-CITALOPRAM, publiée lorsque le médicament
Recommandation Pour La Pratique Clinique
 Recommandation Pour La Pratique Clinique Prise en charge diagnostique et thérapeutique de la migraine chez l adulte ( et chez l enfant) : aspects cliniques (et économiques) Octobre 2002 1 La migraine de
Recommandation Pour La Pratique Clinique Prise en charge diagnostique et thérapeutique de la migraine chez l adulte ( et chez l enfant) : aspects cliniques (et économiques) Octobre 2002 1 La migraine de
Les troubles non moteurs de la maladie de Parkinson. Comprendre la maladie de Parkinson
 Les troubles non moteurs de la maladie de Parkinson Comprendre la maladie de Parkinson La maladie de Parkinson se définit classiquement par des troubles moteurs. Néanmoins, de nombreux autres symptômes,
Les troubles non moteurs de la maladie de Parkinson Comprendre la maladie de Parkinson La maladie de Parkinson se définit classiquement par des troubles moteurs. Néanmoins, de nombreux autres symptômes,
E04a - Héparines de bas poids moléculaire
 E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
Monographie d Abbott-Citalopram Page 52 de 57 Date de révision : 5 septembre 2014 et numéro de contrôle : 177396
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Abbott-Citalopram Comprimés de citalopram USP (sous forme de bromhydrate de citalopram) Le présent dépliant constitue la troisième et dernière partie d
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Abbott-Citalopram Comprimés de citalopram USP (sous forme de bromhydrate de citalopram) Le présent dépliant constitue la troisième et dernière partie d
1 - Que faut-il retenir sur les anticoagulants oraux?
 La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
MIGRAINES. Diagnostic. A rechercher aussi. Critères IHS de la migraine. Type d aura. Particularités chez l enfant. Paraclinique.
 MIGRAINES Diagnostic Critères IHS de la migraine SANS AURA : 5 crises 4-72 heures sans traitement 2 caractéristiques suivantes : Unilatérales Pulsatiles Modérées ou sévères Aggravation par activités physiques
MIGRAINES Diagnostic Critères IHS de la migraine SANS AURA : 5 crises 4-72 heures sans traitement 2 caractéristiques suivantes : Unilatérales Pulsatiles Modérées ou sévères Aggravation par activités physiques
CYMBALTA (duloxétine) CYMBALTA 30 mg, gélule gastro-résistante : Corps blanc opaque imprimé 30 mg et coiffe bleu opaque imprimée 9543.
 CYMBALTA (duloxétine) FORMES ET PRESENTATIONS CYMBALTA 30 mg, gélule gastro-résistante : Corps blanc opaque imprimé 30 mg et coiffe bleu opaque imprimée 9543. CYMBALTA 60 mg, gélule gastro-résistante :
CYMBALTA (duloxétine) FORMES ET PRESENTATIONS CYMBALTA 30 mg, gélule gastro-résistante : Corps blanc opaque imprimé 30 mg et coiffe bleu opaque imprimée 9543. CYMBALTA 60 mg, gélule gastro-résistante :
NOTICE: INFORMATION DE L UTILISATEUR. Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl)
 NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
Nouveaux Anti-thrombotiques. Prof. Emmanuel OGER Pharmacovigilance Pharmaco-épidémiologie Faculté de Médecine Université de Rennes 1
 Nouveaux Anti-thrombotiques Prof. Emmanuel OGER Pharmacovigilance Pharmaco-épidémiologie Faculté de Médecine Université de Rennes 1 Classification Antithrombines directes o Ximélagatran EXANTA o Désirudine
Nouveaux Anti-thrombotiques Prof. Emmanuel OGER Pharmacovigilance Pharmaco-épidémiologie Faculté de Médecine Université de Rennes 1 Classification Antithrombines directes o Ximélagatran EXANTA o Désirudine
COMMISSION DE LA TRANSPARENCE AVIS. 18 janvier 2006
 COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
I.TRAITEMENT DE CRISE -ANTALGIQUES SIMPLES -ANTINFLAMMATOIRES BIPROFENID -TRIPTANS
 TRAITEMENT DE LA MIGRAINE I.TRAITEMENT DE CRISE -ANTALGIQUES SIMPLES PARACETAMOL PEU OU PAS EFFICACE ASSOCIATIONS ASPIRINE-METOCLOPRAMIDE (CEPHALGAN MIGPRIV ) -ANTINFLAMMATOIRES -TRIPTANS BIPROFENID 1
TRAITEMENT DE LA MIGRAINE I.TRAITEMENT DE CRISE -ANTALGIQUES SIMPLES PARACETAMOL PEU OU PAS EFFICACE ASSOCIATIONS ASPIRINE-METOCLOPRAMIDE (CEPHALGAN MIGPRIV ) -ANTINFLAMMATOIRES -TRIPTANS BIPROFENID 1
Migraine et mal de tête : des "casse-tête"
 Migraine et mal de tête : des "casse-tête" Tous concernés! De quoi s agit-il? Les migraines ne doivent pas être confondues avec les céphalées de tension, communément appelées les "maux de tête". En effet,
Migraine et mal de tête : des "casse-tête" Tous concernés! De quoi s agit-il? Les migraines ne doivent pas être confondues avec les céphalées de tension, communément appelées les "maux de tête". En effet,
La migraine : une maladie qui se traite
 La migraine : une maladie qui se traite L évolution natuelle de la migraine Maladie fluctuante+++ Modification des symptômes avec l âge ++ : Moins de crises sévères Caractère pulsatile moins fréquent Plus
La migraine : une maladie qui se traite L évolution natuelle de la migraine Maladie fluctuante+++ Modification des symptômes avec l âge ++ : Moins de crises sévères Caractère pulsatile moins fréquent Plus
NOTICE : INFORMATION DE L UTILISATEUR. Flunarizine
 NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
Humira Solution pour injection dans un injecteur prérempli
 Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 1. DENOMINATION DU MEDICAMENT ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT GAVISCONELL FRUITS DE LA PASSION SANS SUCRE, poudre orale en sachet-dose édulcorée à l'aspartam, au xylitol et à l'acésulfame
1. DENOMINATION DU MEDICAMENT ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT GAVISCONELL FRUITS DE LA PASSION SANS SUCRE, poudre orale en sachet-dose édulcorée à l'aspartam, au xylitol et à l'acésulfame
Fiche de transparence
 Supplément aux Folia Pharmacotherapeutica Centre Belge d Information Pharmacothérapeutique Fiche de transparence Antimigraineux Mai 2012 LES FICHES DE TRANSPARENCE But Les Fiches de transparence ont pour
Supplément aux Folia Pharmacotherapeutica Centre Belge d Information Pharmacothérapeutique Fiche de transparence Antimigraineux Mai 2012 LES FICHES DE TRANSPARENCE But Les Fiches de transparence ont pour
Le problème de la première ou nouvelle. céphalée. Il faudra avant tout :
 Les céphalées Le problème de la première ou nouvelle Il faudra avant tout : céphalée Rechercher des signes d alarme Rechercher avant tout le caractère secondaire de la céphalée Signes d alarme Début après
Les céphalées Le problème de la première ou nouvelle Il faudra avant tout : céphalée Rechercher des signes d alarme Rechercher avant tout le caractère secondaire de la céphalée Signes d alarme Début après
Notice : Informations de l utilisateur. Pantomed 20 mg comprimés gastro-résistants. Pantoprazole
 Notice : Informations de l utilisateur Pantomed 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations
Notice : Informations de l utilisateur Pantomed 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT
 IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
Céphalées vues aux Urgences. Dominique VALADE Centre d Urgence des Céphalées Hôpital Lariboisière PARIS
 Céphalées vues aux Urgences Dominique VALADE Centre d Urgence des Céphalées Hôpital Lariboisière PARIS Deux Objectifs aux Urgences Identifier les céphalées à risque vital Optimiser le traitement des céphalées
Céphalées vues aux Urgences Dominique VALADE Centre d Urgence des Céphalées Hôpital Lariboisière PARIS Deux Objectifs aux Urgences Identifier les céphalées à risque vital Optimiser le traitement des céphalées
Item 182 : Accidents des anticoagulants
 Item 182 : Accidents des anticoagulants COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Cruralgie par hématome
Item 182 : Accidents des anticoagulants COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Cruralgie par hématome
Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS)
 Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS) Édition Conseil du médicament www.cdm.gouv.qc.ca Coordination Anne Fortin, pharmacienne Élaboration Conseil du médicament Fédération
Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS) Édition Conseil du médicament www.cdm.gouv.qc.ca Coordination Anne Fortin, pharmacienne Élaboration Conseil du médicament Fédération
TRAITEMENT DES MAUX DE TÊTE PAR EMDR INTÉGRÉ
 TRAITEMENT DES MAUX DE TÊTE PAR EMDR INTÉGRÉ «Un atelier de deux jours en spécialité EMDR» Présenté par Dr Steven MARCUS,, Ph.D 30 AVRIL & 1er MAI 2011 A PARIS SAMEDI 30 AVRIL : 9H - 16H30 - DIMANCHE 1ER
TRAITEMENT DES MAUX DE TÊTE PAR EMDR INTÉGRÉ «Un atelier de deux jours en spécialité EMDR» Présenté par Dr Steven MARCUS,, Ph.D 30 AVRIL & 1er MAI 2011 A PARIS SAMEDI 30 AVRIL : 9H - 16H30 - DIMANCHE 1ER
Traitement actuel de la migraine
 Traitement actuel de la migraine Pr M. AIT- KACI - AHMED Chef du Service de Neurologie E.H.S Ali Aït Idir (Alger) Alger, 04 Juin 2009 Importance du sujet 1. Sur le plan médical - 12 à 15 % de la population
Traitement actuel de la migraine Pr M. AIT- KACI - AHMED Chef du Service de Neurologie E.H.S Ali Aït Idir (Alger) Alger, 04 Juin 2009 Importance du sujet 1. Sur le plan médical - 12 à 15 % de la population
La prise en charge de votre artérite des membres inférieurs
 G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre artérite des membres inférieurs Vivre avec une artérite des membres inférieurs Novembre 2007 Pourquoi ce guide? Votre
G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre artérite des membres inférieurs Vivre avec une artérite des membres inférieurs Novembre 2007 Pourquoi ce guide? Votre
GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral intramusculaire
 ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
Les NOACs en situation de crise
 Les NOACs en situation de crise Vanderhofstadt Quentin Stagiaire en médecine interne (CHHF) Février 2013 Supervision : Dr Guillen 1 Les NOACs en situation de crise Pourquoi un staff à ce sujet R/ de plus
Les NOACs en situation de crise Vanderhofstadt Quentin Stagiaire en médecine interne (CHHF) Février 2013 Supervision : Dr Guillen 1 Les NOACs en situation de crise Pourquoi un staff à ce sujet R/ de plus
mal de tête d installation subite 12/10 Éliminer une céphalée secondaire
 LES CÉPHALÉES 4 e Forum Département de médecine familiale et de médecine d urgence St-Georges de Beauce le 29 mai 2009 Les céphalées: objectifs Appliquer un algorithme diagnostique des céphalées Reconnaître
LES CÉPHALÉES 4 e Forum Département de médecine familiale et de médecine d urgence St-Georges de Beauce le 29 mai 2009 Les céphalées: objectifs Appliquer un algorithme diagnostique des céphalées Reconnaître
Lorraine Waechter - http://fichesecn.wordpress.com/ ITEM 262 : MIGRAINE CLINIQUE
 ITEM 262 : MIGRAINE CLINIQUE Terrain Anamnèse Critères diagnostiques IHS Migraine sans aura = Migraine commune Critères diagnostiques IHS Migraine avec aura = Migraine accompagnée Aura - Argument de fréquence
ITEM 262 : MIGRAINE CLINIQUE Terrain Anamnèse Critères diagnostiques IHS Migraine sans aura = Migraine commune Critères diagnostiques IHS Migraine avec aura = Migraine accompagnée Aura - Argument de fréquence
Programme pour les patients traités par les nouveaux anti-coagulants oraux.
 Programme P H A R M A C O pour les patients traités par les nouveaux anti-coagulants oraux. AG Caffin 1, Y Chabi 1, C Sévin 2, B Leclere 3, C Debelmas 4, G Camus 1, X Bohand 1 1 Hôpital d Instruction des
Programme P H A R M A C O pour les patients traités par les nouveaux anti-coagulants oraux. AG Caffin 1, Y Chabi 1, C Sévin 2, B Leclere 3, C Debelmas 4, G Camus 1, X Bohand 1 1 Hôpital d Instruction des
Programme de prise en charge et de suivi en anticoagulothérapie
 Programme de prise en charge et de suivi en anticoagulothérapie (PEACE) Médecins réviseurs : Dr Steve Brulotte, cardiologue, CSSSAD-Lévis Dr Daniel D Amours, cardiologue, CHU Dr Guy Boucher, cardiologue,
Programme de prise en charge et de suivi en anticoagulothérapie (PEACE) Médecins réviseurs : Dr Steve Brulotte, cardiologue, CSSSAD-Lévis Dr Daniel D Amours, cardiologue, CHU Dr Guy Boucher, cardiologue,
1 La scintigraphie myocardique au Persantin ou Mibi Persantin
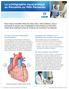 La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI
 LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI? LA MÉTHAMPHÉTAMINE est un produit stupéfiant illicite, synthétisé à partir de substances chimiques, également connu sous le nom de «crystal» ou «crystalmet», «ice»,
LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI? LA MÉTHAMPHÉTAMINE est un produit stupéfiant illicite, synthétisé à partir de substances chimiques, également connu sous le nom de «crystal» ou «crystalmet», «ice»,
2015-01-29 OBJECTIFS QUOI DE NEUF, DOC? EN PÉDIATRIE MIGRAINE TRIPTANS EN PÉDIATRIE MIGRAINES STRATÉGIES DE TRAITEMENT
 OBJECTIFS QUOI DE NEUF, DOC? EN PÉDIATRIE Sophie Bergeron, MD Département de pédiatrie Hôpital de Gatineau Triptan en pédiatrie Comprendre la pathophysiologie de la migraine Connaître les différentes approches
OBJECTIFS QUOI DE NEUF, DOC? EN PÉDIATRIE Sophie Bergeron, MD Département de pédiatrie Hôpital de Gatineau Triptan en pédiatrie Comprendre la pathophysiologie de la migraine Connaître les différentes approches
Les nouveaux anticoagulants oraux (NAC)
 Les nouveaux anticoagulants oraux (NAC) Dr Jean-Marie Vailloud Cardiologue libéral/ salarié (CHU/clinique) Pas de lien d'intérêt avec une entreprise pharmaceutique Adhérent à l'association Mieux Prescrire
Les nouveaux anticoagulants oraux (NAC) Dr Jean-Marie Vailloud Cardiologue libéral/ salarié (CHU/clinique) Pas de lien d'intérêt avec une entreprise pharmaceutique Adhérent à l'association Mieux Prescrire
