Compte rendu de séance
|
|
|
- Marie-Claire Bergeron
- il y a 7 ans
- Total affichages :
Transcription
1 Compte rendu de séance Numero unique de document :CSST Date document : 31/03/2014 Direction : INFHEP Pôle : Maladies Infectieuses Personne en charge : Nathalie Morgensztejn /Caroline S le COMITE SCIENTIFIQUE SPECIALISE TEMPORAIRE «ANTIVIRAUX DANS L HEPATITE C» N 1 Statut (mentionner si Nom des participants Président, membre, /secrétaire, rédacteur, /excusé évaluateur) ANTONINI Teresa Membre BARDOU Marc Membre BARRE Jérôme Membre COUZIGOU Patrice Membre MASSY-GUILLEMANT Nathalie Membre ROZENBAUM Willy Membre SELLIER Pierre Membre VITTECOQ Daniel Membre DELFRAISSY Jean-François Expert auditionné DHUMEAUX Daniel Expert auditionné par téléphone le 13/02/14 DIALLO Alpha Expert auditionné De LEDINGHEN Victor Expert auditionné PAWLOTSKY Jean-Michel Expert auditionné par téléphone le 13/02/14 PETROV-SANCHEZ Ventzislava Expert auditionné POL Stanislas Expert auditionné Copie Points Sujets abordés Initiales évaluateur Action : mentionner pour audition, information, adoption ou discussion 1. Introduction 1.1 Adoption de l ordre du jour Non 1.2 Adoption du CR de Sans objet Non Avis EU nécessaire avant publication Mentionner Oui non Liens DPI Mention ner Oui non 2. Dossiers thématiques 2.1 Sans objet /147 boulevard Anatole France - F Saint-Denis Cedex - Tél.: +33 (0)
2 3. Dossiers Produits Substances (National) 3.1 Sans objet Dossiers Produits Substances (Europe) 4.1 Daclatasvir, mise en place d une ATU de cohorte 4.2 Simeprevir, élargissement de l ATU de cohorte 5. Tour de Table Pour discussion Pour discussion Déroulement de la séance Nom du dossier Dossier thématique Dossiers Produits Substances (National) Dossiers Produits Substances (Europe) Numéro de dossier NL Horaire de passage DACLATASVIR Sans objet Nom, Prénom DPI > 1 an Type de lien Niveau lien Période Traitement en séance Tous les Experts auditionnés sont sortis de la salle : - JF. Delfraissy - A. Diallo - V. De Ledinghen - V. Petrov-Sanchez - S. Pol Si DPI > 1 an DPI actualisée en séance Si niveau 1 Si niveau 2 Critères de passage Besoin d une connaissance terrain sur des pratiques Besoin d un avis collégial ou complémentaire / Absence de consensus interne et / ou avis complémentaire Caractère innovant du dossier Impact majeur de santé publique Références documentaires Sans objet Page 2/9
3 Nom du dossier Dossier thématique Dossiers Produits Substances (National) Dossiers Produits Substances (Europe) Numéro de dossier NL Horaire de passage SIMEPREVIR Sans objet Nom, Prénom DPI > 1 an Tous les Experts auditionnés sont sortis de la salle : - JF. Delfraissy - A. Diallo - V. De Ledinghen - V. Petrov-Sanchez - S. Pol Type de lien Niveau lien Période Traitement en séance Si DPI > 1 an DPI actualisée en séance Si niveau 1 Si niveau 2 Critères de passage Besoin d une connaissance terrain sur des pratiques Besoin d un avis collégial ou complémentaire / Absence de consensus interne et / ou avis complémentaire Caractère innovant du dossier Impact majeur de santé publique Références documentaires Sans objet ation de la problématique (pour les 2 dossiers) Contexte : La dynamique très évolutive du développement des nouveaux antiviraux dans l hépatite C et la publication récente de résultats très encourageants d associations d antiviraux sans interféron suscitent des attentes majeures au sein de la communauté scientifique et des patients, comme en témoigne les demandes croissantes d ATU nominative reçues depuis début janvier Dans ce contexte, un comité scientifique spécialisé temporaire a été réuni pour l examen de 2 dossiers de demande d ATU de cohorte permettant de répondre à la demande forte d accès précoce à des associations d antiviraux sans interféron chez les patients à un stade avancé de la maladie. Il s agit d une demande d ATU de cohorte pour le DACLATASVIR (en association à sofosbuvir) et une demande d élargissement de l ATU de cohorte du SIMEPREVIR (en association à sofosbuvir). A noter que ces deux antiviraux font actuellement l objet de demandes d AMM en cours d évaluation au niveau européen. Le Comité scientifique est constitué d experts spécialisés dans le domaine de l hépatite C et de la transplantation hépatique, de cliniciens infectiologues, d un pharmacologue et d un représentant d un centre régional de pharmacovigilance. De plus, des experts ont également été auditionnés, compte tenu de l intérêt scientifique majeur de leur expertise et compte tenu du fait qu il n a pas été possible de trouver d'expert de compétence équivalente dans le domaine concerné et qui n'ait pas de conflit d'intérêts. Page 3/9
4 Les experts suivants ont été auditionnés : - Des représentants de l ANRS : le Pr Jean François DELFRAISSY (Directeur ANRS), le Pr Stanislas POL (en tant que responsable scientifique de la cohorte Hepather), Ventzislava PETROV-SANCHEZ (Responsable du Service de Recherches fondamentale, clinique et thérapeutique sur les hépatites virales) et Alpha DIALLO (Responsable du Service des Vigilances des Recherches cliniques) ; - Le Pr Victor de LEDINGHEN, en tant que représentant de l AFEF ; - Le Pr Jean Michel PAWLOTSKY, en tant que représentant du CNR sur les Hépatites B et C (auditionné par téléphone le 13/02/2014); - Le Pr Daniel DHUMEAUX, en tant que coordonateur du rapport d'expertise et président du comité de suivi du plan hépatites (auditionné par téléphone le 13/02/2014). La réunion s est articulée autour d une présentation par l ANSM des données cliniques disponibles sur les deux produits et d un bilan des demandes d ATU reçues à ce jour. Une présentation a également été faite par les représentants de l ANRS et de l AFEF puis une synthèse des principaux éléments recueillis auprès des experts auditionnés par téléphone a été présentée par l ANSM. Une discussion a ensuite été engagée avec les membres du comité, en l absence des personnes auditionnées, portant en particulier sur la population cible et le schéma de traitement. A. Donnés sur le Daclatasvir Le Daclatasvir est le 1er représentant de la classe des inhibiteurs du complexe de réplication de la protéine non structurale NS5A du VHC. Depuis le 16 janvier (date à laquelle l'amm de sofosbuvir a été ratifiée par l'union Européenne et ont été publiés dans le NEJM des résultats concernant l association de sofosbuvir et daclatasvir sans interféron), un afflux de demande d accès précoce à cette association a été reçu par l ANSM nécessitant la mise en place rapide d une ATU de cohorte. A noter que dans l attente, des ATU nominatives sont octroyées chez les patients les plus gravement atteints ne pouvant attendre la mise en place de l ATU de cohorte, tels que les patients en récidive après une transplantation hépatique ou présentant des signes de décompensation hépatique. Ainsi, alors que 108 demandes avaient été reçues entre juillet et décembre 2013, 372 demandes d ATU ont été reçues dans la courte période du 1er janvier au 13 février Parmi ces dernières, 141 ont été octroyées chez des patients greffés ou ayant une cirrhose décompensée (ainsi que quelques cas de patients présentant une cryoglobulinémie très sévère) et 231 demandes (principalement des patients avec une cirrhose compensée) ont été mises en attente de la mise en place de l ATU de cohorte. L indication proposée par les laboratoires BMS dans le cadre de l ATU de cohorte, déposée en décembre 2013, est la suivante: «DACLATASVIR utilisé dans le cadre de l ATU de cohorte est indiqué en association avec d autres antiviraux dans le traitement de l hépatite C chronique chez les adultes à risque de décompensation ou de décès et ayant une espérance de vie inférieure à 12 mois en l absence de traitement.» De la présentation des données, il est admis que cet antiviral présente des caractéristiques intéressantes au plan virologique avec une activité pangénotypique (bien que son activité semble inférieure chez les génotypes 2 et 3 en comparaison au génotype 1). Son profil pharmacocinétique est également intéressant permettant une utilisation en cas d insuffisance hépatique (y compris sévère) ou d insuffisance rénale/hémodialyse sans ajustement posologique. Les données d interaction disponibles montrent l absence d interaction significative avec le sofosbuvir et avec les immunosuppresseurs. Il est nécessaire d'ajuster la dose de daclatasvir à 30mg en cas de coadministration avec Atazanavir/r et à 90mg en cas de co-administration avec l'efavirenz. L activité antivirale de daclatasvir dans l hépatite C chronique a été explorée dans différents schémas d association (en association à peginterferon alpha ou lambda, en association à d autres antiviraux directs tels que sofosbuvir, asunaprévir et BMS ). Les données cliniques d association de daclatasvir avec sofosbuvir reposent à ce jour sur une étude de phase II (AI444040, publiée dans le NEJM en janvier 2014). Cette étude, randomisée, a été conduite en ouvert chez 211 patients infectés par un génotype 1, 2 ou 3, naïfs de traitement ou en échec à un inhibiteur de protéase. Aucun de ces patients ne présentait de cirrhose histologique. La durée de traitement était de semaines avec ou sans ribavirine. Page 4/9
5 Des taux de réponse virologique soutenue (RVS) très élevés ont été rapportés dans cette étude : La RVS à 12 semaines après l arrêt (RVS 12 ) était de 91 à 98% selon les génotypes. Dans cette étude, il n a pas été montré d impact sur l efficacité des sous-types G1a versus G1b, du polymorphisme IL28 ou de l utilisation ou non de la ribavirine. De même il ne semble pas y avoir eu d impact des variants NS5A pré-existants sur l efficacité du traitement. Concernant la sécurité d emploi, les données non cliniques n ont pas révélé de préoccupations majeures. De même, les données cliniques portant sur 6000 patients exposés au cours du développement dont 1000 exposés à la dose recommandée dans les principales études de phase II/III du dossier d AMM, suggèrent un profil de risque favorable. Les données de sécurité d emploi sont toutefois limitées chez les patients cirrhotiques (n=70 patients environ). Concernant plus particulièrement l association de daclatasvir à sofosbuvir, les effets indésirables les plus fréquents étaient : fatigue, céphalées, nausée, arthralgie et diarrhée. Un total de 15 patients (7%) ont présenté un effet indésirable grave et 2 patients (<1%) ont arrêté le traitement du fait d un effet indésirable. L ajout de la ribavirine à sofosbuvir et daclatasvir a entrainé une baisse du taux d hémoglobine : 30% dans les bras de traitement contenant de la ribavirine versus 3% dans les bras sans ribavirine. A noter qu un cas d insuffisance biventriculaire aiguë d évolution fatale a été rapporté chez un patient traité par sofosbuvir et ribavirine puis sofosbuvir et daclatasvir dans le cadre d une ATU. Bien qu aucun signal de toxicité cardiaque ne puisse être confirmé à ce jour, un message pour attirer la vigilance des prescripteurs a été ajouté dans les courriers accompagnant les ATU nominatives et sera également inclus dans le PUT de Daclatasvir. B. Donnés sur le Simeprevir Le simeprevir est le 3 ème représentant de la classe des inhibiteurs de la sérine protéase NS3/4A du VHC, après le télaprevir et le boceprevir. Par rapport à ces derniers, son activité est étendue en plus du génotype 1 au VHC de génotype 4, dont la prévalence s accroît en Europe, en particulier en France. En octobre 2013, une ATU de cohorte a été mise en place dans l indication suivante: «Traitement de l'hépatite C chronique (HCC) due au virus de génotype 4, en association avec le peg-interféron alfa et la ribavirine, chez les adultes ayant une maladie hépatique compensée avec un stade de fibrose F4 (cirrhose), avec ou sans co-infection par le virus de l'immunodéficience humaine de type 1 (VIH-1), en échec après traitement par interféron (pégylé ou non) avec ou sans ribavirine». Au 12 février 2014, 41 patients avaient été inclus dans cette ATU de cohorte. Par ailleurs, plusieurs demandes d ATU ont été reçues pour des patients ne rentrant pas dans le cadre de l ATU de cohorte motivant un élargissement de cette ATU; il s agit principalement de patients infectés par un génotype 1 ou de patients ne pouvant recevoir d interféron pour lesquels les prescripteurs souhaitent avoir un accès précoce à simeprevir en association à sofosbuvir. Au total, 52 demandes d ATU nominatives ont été reçues par l ANSM dans ce contexte. Huit ont été octroyées chez des patients dont le pronostic vital était engagé à très court terme du fait d une cirrhose décompensée (stade Child Pugh B) et 46 ont été mises en attente de l élargissement de l ATU de cohorte. L indication revendiquée par le laboratoire dans sa demande d élargissement déposée en janvier 2014 est la suivante : «SIMEPREVIR, utilisé dans le cadre de l ATU de Cohorte, est indiqué dans le traitement de l'hépatite C chronique (HCC) due au virus de génotype 1 ou 4, en association avec d autres médicaments, chez les patients adultes ayant une maladie hépatique à un stade avancé, avec ou sans co-infection par le virus de l'immunodéficience humaine (VIH) et pour lesquels il n existe pas d alternatives therapeutiques appropriées». Au plan pharmacodynamique, le simeprevir présente un niveau de résistance croisée avec le telaprevir et le boceprevir sur le génotype 1. De plus, le polymorphisme Q80K caractérisé par une prévalence significative parmi les patients infectés par un VHC de génotype 1a (19% en Europe), a été identifié comme étant un facteur péjoratif de réponse virologique au siméprevir chez ces patients (différence d environ 30% observée dans les études de phase III en association avec pegifn+ribavirine). L impact de ce polymorphisme dans un schéma d association au sofosbuvir semble moins marqué mais ne peut être exclus à ce stade. Cette problématique soulève la question de la recherche du polymorphisme Q80K avant l initiation du traitement chez les patients infectés par un VHC de génotype 1a. Page 5/9
6 Le profil pharmacocinétique du siméprévir a été caractérisé chez l insuffisant rénal et hépatique, avec un risque de majoration de l exposition/toxicité chez les patients avec une insuffisance hépatique sévère. Au plan des interactions médicamenteuses, sa co-administration avec les immunosuppresseurs n apparaît pas nécessiter d ajustement posologique. La possibilité de co-administration avec les antirétroviraux du VIH est limitée. En effet, en raison de l induction des enzymes du CYP3A [efavirenz, étravirine, névirapine] ou inhibition [inhibiteurs de protéases «boostées» par le ritonavir], des modifications des concentrations plasmatiques du simeprevir sont attendues. Les seules coadministrations possibles sont avec le raltegravir, la rilpivirine, le tenofovir et les inhibiteurs nucléosidiques de la transcriptase inverse du VIH. L association au maraviroc n est pas documentée. Les études cliniques ont principalement été conduites chez les patients infectés par un VHC de génotype 1. Sur la base des données des études de phase III, l ajout du simeprévir à la bithérapie pégylée permet, de façon comparable à ce qui été observé avec boceprevir et telaprevir, d augmenter significativement le taux de guérison chez les patients G1 naïfs ou rechuteurs (RVS de 80% chez ces patients, représentant un gain de 30-40% par rapport à la bithérapie). Les données cliniques d association de simeprevir avec sofosbuvir reposent à ce jour sur une étude de phase II (COSMOS, chez des patients infectés par un génotype 1). Cette étude, randomisée, a été conduite en ouvert chez 167 patients infectés par un génotype 1a ou 1b : 80 répondeurs nuls à un précédent traitement par pegifn+ribavirine au stade de fibrose F0-F2 (cohorte 1) et 87 patients répondeurs nuls ou naïfs de traitement présentant une fibrose F3 ou une cirrhose (cohorte 2). La durée de traitement était de 12 ou 24 semaines avec ou sans ribavirine. Des taux de réponse virologique soutenue (RVS) très élevés ont été rapportés dans cette étude. La RVS à 12 semaines après l arrêt (RVS 12 ) était > 90% dans la cohorte 1 et les données de RVS 8 disponibles à ce jour pour la cohorte 2 indiquent également des taux de réponse très élevés chez les patients ayant une fibrose avancée : RVS 8 >90%. Dans cette étude, il n a pas été montré d impact de la durée de traitement ou de l utilisation ou non de la ribavirine. Aucun rebond virologique n a été rapporté. A noter que tous les patients ayant rechuté (n=4) étaient infectés par un virus de génotype 1a et présentaient la mutation Q80K. L association de sofosbuvir et simeprevir n a pas été spécifiquement testé chez les patients infectés par un génotype 4 à ce jour. Une étude est en cours associant simeprevir à pegifn+ribavirine chez les patients infectés par un VHC de génotype 4 (étude RESTORE portant sur environ 100 patients naïfs et prétraités, dont des patients répondeurs nuls et cirrhotiques). Bien que les données disponibles soient à ce stade préliminaires, les données de réponse virologique rapide sous traitement vont dans le sens d une efficacité comparable à celle observée chez les patients infectés par un VHC de génotype 1. En particulier, les données disponibles chez les patients naïfs et rechuteurs montrent des taux de RVS 12 élevés chez ces patients, de 88% et 91%, respectivement. Compte tenu du fait que sofosbuvir est actif sur les génotype 4 et que simeprevir semble avoir une activité comparable sur le génotype 1 et 4 (et de plus, la mutation Q80K ne semble pas être prévalente chez les patients infectés par un G4); l extrapolation des résultats de COSMOS aux patients infectés par un génotype 4 a été admise (notamment au niveau européen). Chez les patients co-infectés VIH-VHC, les résultats préliminaires d une étude réalisée chez les patients co-infectés VIH-VHC de génotype 1 (C212, n= 106 patients naïfs de traitement ou prétraités suggèrent une efficacité comparable aux patients mono-infectés (à l instar de ce qui a été précédemment rapporté avec les autres inhibiteurs de protéase). Au plan de la sécurité d emploi : Les études non cliniques n ont pas révélé de préoccupations majeures. Plus de 1000 patients ont reçu du siméprévir 150mg par jour pendant 12 semaines. L ajout du siméprévir à la bithérapie peginterféron alfa + ribavirine n apparaît pas dégrader significativement le profil de sécurité d emploi déjà connu avec ces produits. Son profil de tolérance se caractérise en particulier par un risque d hyperbilirubinémie, de réactions cutanées (principalement des rashs non sévères), des prurits, et des réactions de photosensibilité nécessitant des mesures de protection solaire. De plus, un risque de dyspnée en particulier chez le sujet de plus de 45 ans a été identifié. Par ailleurs, bien que les données soient encore limitées, le profil de sécurité d emploi du traitement par siméprévir chez les patients co-infectés par le VIH et le VHC semble comparable à celui décrit chez les mono-infectés. Enfin, environ 200 patients ayant un score de Métavir F3-F4 ont reçu du siméprévir en association à PegIFN et ribavirine. Comme attendu, le risque d hyperbilirubinémie et d anémie est augmenté dans cette population de patients par rapport aux patients ayant un score Métavir F0-F2. Page 6/9
7 Concernant plus particulièrement, les données de tolérance de l association de simeprevir à sofosbuvir, les données disponibles de l étude COSMOS n ont pas révélé de craintes particulières, y compris chez les 41 patients cirrhotiques inclus dans cette étude. Les effets indésirables les plus fréquemment rapportés ont été la fatigue et les céphalées. C. Auditions Jean-François Delfraissy a rappelé l importance des cohortes observationnelles mises en place par l ANRS telles ANRS CO 22 HEPATHER et ANRS CO 23 CUPILT. Ces cohortes, de même que la cohorte ANRS CO 13 HEPAVIH chez les patients coinfectés, sont des outils pour le recueil des informations sur l utilisation des nouveaux antiviraux du VHC dans le cadre des ATU et lors des premières années de commercialisation. L objectif est de recueillir des informations sur l utilisation des nouveaux antiviraux dans les populations plus difficiles à traiter qui n ont généralement pas été inclus dans les essais cliniques, que sont les patients bénéficiant d un traitement sous ATU ou ayant une AMM récente, et permettre d`obtenir rapidement des données pour ces patients, mais aussi de poser des questions de recherche. A l instar de la cohorte CUPIC, qui a inclus environ 55% des patients ayant reçu du boceprevir ou du telaprévir en ATU, il est anticipé que 50-60% des patients des ATUs de Cohorte seront inclus dans les cohortes de suivi HEPATHER et CUPILT. Pour rappel, la cohorte HEPATHER est une cohorte française observationnelle qui a pour objectif d inclure patients ( patients infectés par le VHB et infectés par le VHC) afin de mesurer les bénéfices et les risques associés aux différentes modalités de prise en charge thérapeutique des hépatites B et C et en identifier les déterminants individuels, virologiques, environnementaux et sociaux. En février 2014, patients étaient inclus dans 23 centres. La cohorte CUPILT est un observatoire des patients transplantés hépatiques présentant une récidive virale C traités par un nouvel agent antiviral direct. Au 14 février, 60 patients étaient inclus dans cette cohorte. Par ailleurs, l importance du recueil des événements indésirables dans cette population de patients ayant une maladie hépatique avancée a été rappelée. Néanmoins, Jean-François Delfraissy a souligné que le recueil systématique des événements indésirables de grade 1-2, très fréquents dans cette population, était perçu comme lourd, notamment dans les services de réanimation. Des assouplissements ont été demandés par l ANRS sur les modalités de ce recueil dans la cohorte CUPILT ou d'autres cohortes de même type. Victor de Lédinghen a présenté, au titre de l AFEF, une synthèse d avis d experts sur les traitements à recommander en 2014 chez les patients à un stade avancé de la maladie tels ceux ciblés dans les ATUs. Un panel de 10 experts a participé. Il apparait une certaine hétérogénéité dans les réponses quant aux schémas et principalement quant à la durée de traitement et l ajout ou non de ribavirine. Par contre, certains éléments font consensus et rejoignent les avis des autres experts présents à la réunion du CSST et ceux auditionnés par téléphone. Globalement, les éléments suivants semblent faire consensus parmi les membres présents et auditionnés : - Population cible de l ATU doit inclure les patients à un stade avancé de la maladie, c'est-à-dire ceux avec une cirrhose mais aussi ceux présentant un stade de fibrose avancée/pré-cirrhotique. La façon la plus appropriée de définir cette population a par contre été un point de discussion. Par ailleurs, il a été souligné à plusieurs reprises l importance d inclure les patients présentant des manifestations extrahépatiques ou les patients greffés rénaux dans l indication de l ATU. De plus, les patients en attente de transplantation hépatique sont également ciblés dans l ATU. Il est admis que ces patients doivent être traités avec le traitement le plus efficace d emblée, soit sofosbuvir en association à un autre inhibiteur direct. Par ailleurs, il a été souligné que les patients en attente de transplantation rénale étaient également en besoin urgent de traitement compte tenu de l intérêt d éradiquer le virus avant la greffe rénale et devaient être inclus dans l ATU de daclatasvir (les propriétés pharmacocinétiques de cette molécule permettant cette utilisation). Les patients présentant une rechute post-greffe doivent pouvoir bénéficier d un traitement efficace de façon précoce. - Place de la ribavirine : Si les experts mentionnent que l interféron ne semble plus avoir de place dans les nouvelles stratégies thérapeutiques, la ribavirine pourrait quant à elle garder un intérêt pour optimiser la réponse au traitement dans certaines situations, notamment chez les patients cirrhotiques. Par contre, il semble faire consensus que les données disponibles à ce jour ne permettent pas de statuer de façon définitive sur l intérêt ou non de la ribavirine. L ajout de la ribavirine dans le schéma thérapeutique doit être évalué au cas par cas par le prescripteur. Page 7/9
8 L utilisation du simeprévir chez les patients infectés par un génotype 1a soulève des interrogations. Il a été souligné qu il semble plus prudent de prescrire sofosbuvir+daclatasvir dans cette situation compte tenu du potentiel impact négatif du polymorphisme Q80K sur la réponse au traitement chez les patients infectés par un génotype 1a. Le Pr Pawlotsky précise qu aujourd hui, il est difficile d apprécier l intérêt d un génotypage (Q80K ou mutants NS5A) avant la mise sous traitement par simeprevir ou daclatasvir. On devrait pour ces deux molécules avoir, selon lui, la même attitude c est à dire soit faire un génotypage systématiquement avant la mise en route du traitement soit ne pas le rechercher et dans ce cas un patient G1a devrait pouvoir recevoir sofosbuvir en association à simeprevir, au même titre que sofosbuvir en association à daclatasvir. A noter que le CNR est en train de développer un test de recherche de la mutation Q80K. Enfin, les experts se sont également interrogés sur le coût de ces nouvelles molécules. Toutefois, il a été précisé que ce n était pas le lieu pour une telle discussion. Les membres auditionnés sont sortis de la salle. Il pourrait être nécessaire de façon exceptionnelle de notifier l ATU de cohorte de Daclatasvir avant le passage en «Commission d évaluation initiale du rapport entre les bénéfices et les risques des produits de santé» compte tenu de la date de la commission (13 mars 2014) et de l intérêt de mettre rapidement en place cette ATU pour donner un accès précoce à ces associations aux patients qui sont à un stade avancé de la maladie. Questions posées (pour les 2 dossiers) Les questions posées aux membres étaient les suivantes : 1. Définition de la population cible pour chacune des associations au regard des alternatives disponibles à ce jour 2. Définition du cadre de l ATU et de son suivi (fiches de suivi) pour chacune des associations 3. Pour chacune des associations, peut-on considérer qu il existe un schéma thérapeutique à privilégier à ce jour en termes de durée et d adjonction de ribavirine Votes : sans objet Nombre de votants sur nombre global Nombre d avis favorables Nombre d avis défavorables Nombre d abstention Avis relatif aux questions posées A l issue de la discussion, les membres du groupe ont estimé que : - l indication de l ATU de cohorte de Daclatasvir devait être la suivante : «Daclatasvir utilisé dans le cadre d une ATU de Cohorte, est indiqué pour le traitement de patients adultes atteints d infection virale C chronique : - ant une maladie à un stade avancé (avec fibrose hépatique F3/F4 ou présentant des manifestations extrahépatiques du VHC) et pour lesquels il n existe pas d alternatives thérapeutiques appropriées ou - Sont sur liste d attente pour une transplantation hépatique ou rénale ou - Ont subi une transplantation hépatique et présentent une récurrence de l infection par le virus de l hépatite C. Page 8/9
9 Pour l activité en fonction du génotype du virus de l hépatite C (VHC), voir rubriques 4.4 et 5.1». - Concernant la posologie, il a été décidé de faire les recommandations suivantes (pour toutes les situations, y compris chez les patients en attente de greffe) : «Daclatasvir doit être utilisé en association avec le sofosbuvir 400 mg comprimé (un comprimé par jour) pendant une durée de 24 semaines de traitement. Les données limitées de l essai AI ne permettent pas de conclure sur l intérêt de l ajout de la ribavirine dans le schéma thérapeutique. Le schéma optimal chez les patients à un stade avancé reste à déterminer». Les membres du CSST sont en faveur d un schéma de traitement limité à 24 semaines chez les patients en attente de transplantation, avec retraitement en cas de rechute, au regard de l absence de recul en termes de tolérance sur des durées d exposition de plus de 6 mois. - De même pour simeprevir, les membres du groupe ont estimé que l ATU de cohorte de simeprevir pouvait être élargie comme suit : "SIMEPREVIR, utilisé dans le cadre de l'atu de cohorte, est indiqué dans le traitement de l'hépatite C chronique (HCC) due au virus de génotype 1b et 4, en association avec d'autres médicaments, chez les adultes ayant une maladie hépatique à un stade avancé (avec fibrose hépatique F3/F4 ou présentant des manifestations extra-hépatiques du VHC) et pour lesquels il n'existe pas d'alternatives thérapeutiques appropriées". A noter que les patients co-infectés VIH-VHC sont inclus dans l ATU de cohorte bien que n apparaissant pas stricto sensu dans le libellé de l indication. Avis majoritaires Le comité est en faveur de la mise en place d une ATU de cohorte pour le Daclatasvir (en association à sofosbuvir) et d un élargissement de l ATU de cohorte pour le Siméprévir (en association à sofosbuvir) dans les indications mentionnées ci-dessus. Avis minoritaires Proposition d action : Par Échéance Page 9/9
Bonne lecture!! et si vous souhaitez consulter le document de l AFEF dans son intégralité, c est ici
 Un résumé des recommandations éditées par l AFEF le 1 er juin 2015 Les recommandations de l AFEF vont plus loin que celles de l EASL. Le Pr Victor De Lédinghen, du CHU de Bordeaux, et secrétaire général
Un résumé des recommandations éditées par l AFEF le 1 er juin 2015 Les recommandations de l AFEF vont plus loin que celles de l EASL. Le Pr Victor De Lédinghen, du CHU de Bordeaux, et secrétaire général
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION. 10 octobre 2001
 COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
COMMISSION DE LA TRANSPARENCE. 10 décembre 2008
 COMMISSION DE LA TRANSPARENCE AVIS 10 décembre 2008 VIRAFERONPEG 50 µg/ 0.5 ml, poudre et solvant pour solution injectable B/1 : code CIP 355 189.3 B/4 : code CIP 355 191.8 VIRAFERONPEG, stylo pré-rempli
COMMISSION DE LA TRANSPARENCE AVIS 10 décembre 2008 VIRAFERONPEG 50 µg/ 0.5 ml, poudre et solvant pour solution injectable B/1 : code CIP 355 189.3 B/4 : code CIP 355 191.8 VIRAFERONPEG, stylo pré-rempli
Marseille 25 octobre 2012 Accompagnement du traitement chez les co-infectés VHC-VIH en pratique
 Marseille 25 octobre 2012 Accompagnement du traitement chez les co-infectés VHC-VIH en pratique Dominique Larrey Service d Hépatogastroenterologie et transplantation Hôpital Saint Eloi CHU Montpellier
Marseille 25 octobre 2012 Accompagnement du traitement chez les co-infectés VHC-VIH en pratique Dominique Larrey Service d Hépatogastroenterologie et transplantation Hôpital Saint Eloi CHU Montpellier
Le Comité Scientifique a traité les questions suivantes : «Association reconnue d utilité publique» - 1 -
 - 1 - Prise de position de l'association Française pour l'etude du Foie (AFEF) sur les trithérapies (Peg-IFN + ribavirine + inhibiteur de protéase) dans la prise en charge des malades atteints d'hépatite
- 1 - Prise de position de l'association Française pour l'etude du Foie (AFEF) sur les trithérapies (Peg-IFN + ribavirine + inhibiteur de protéase) dans la prise en charge des malades atteints d'hépatite
L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015
 L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015 Objectifs de la présentation Décrire l évolution clinique et la prise en charge d
L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015 Objectifs de la présentation Décrire l évolution clinique et la prise en charge d
Actualités sur le Virus de l'hépatite C
 CBP CHRU Lille Actualités sur le Virus de l'hépatite C 2.0 ANNE GOFFARD UNIVERSITÉ LILLE 2 DROIT ET SANTÉ FACULTÉ DES SCIENCES PHARMACEUTIQUES ET BIOLOGIQUES DE LILLE 2012 Table des matières I - Épidémiologie
CBP CHRU Lille Actualités sur le Virus de l'hépatite C 2.0 ANNE GOFFARD UNIVERSITÉ LILLE 2 DROIT ET SANTÉ FACULTÉ DES SCIENCES PHARMACEUTIQUES ET BIOLOGIQUES DE LILLE 2012 Table des matières I - Épidémiologie
Traitement de l hépatite C: données récentes
 Traitement de l hépatite C: données récentes J.-P. BRONOWICKI (Vandœuvre-lès-Nancy) Tirés à part : Jean-Pierre Bronowicki Service d Hépatogastroentérologie, CHU de Nancy, 54500 Vandœuvre-lès-Nancy. Le
Traitement de l hépatite C: données récentes J.-P. BRONOWICKI (Vandœuvre-lès-Nancy) Tirés à part : Jean-Pierre Bronowicki Service d Hépatogastroentérologie, CHU de Nancy, 54500 Vandœuvre-lès-Nancy. Le
Hépatite C, les nouveaux traitements
 Hépatite C, les nouveaux traitements Dr Ghassan Riachi CHU de Rouen QDN 2014 Revue de presse p L hépatite C est une maladie curable Peginterferon + DAAs 2011 Standard Interferon 1991 + Ribavirin 1998 2001
Hépatite C, les nouveaux traitements Dr Ghassan Riachi CHU de Rouen QDN 2014 Revue de presse p L hépatite C est une maladie curable Peginterferon + DAAs 2011 Standard Interferon 1991 + Ribavirin 1998 2001
Communiqué de presse. Direction Communication Externe/Interne Sylvie Nectoux TEL : 01 44 34 65 73 Email : sylvie.nectoux@boehringeringelheim.
 Les données des études pivots de phase III STARTVerso démontrent l'efficacité du faldaprevir * dans des populations de patients difficiles à guérir telles que celles co-infectées par le VIH et celles avec
Les données des études pivots de phase III STARTVerso démontrent l'efficacité du faldaprevir * dans des populations de patients difficiles à guérir telles que celles co-infectées par le VIH et celles avec
LES CO-INFECTIONS VIH-VHC. EPIDEMIOLOGIE, INTERFERENCES. Patrice CACOUB La Pitié Salpêtrière, Paris
 LES CO-INFECTIONS VIH-VHC. EPIDEMIOLOGIE, INTERFERENCES Patrice CACOUB La Pitié Salpêtrière, Paris 8 Avant l introduction des traitements antirétroviraux hautement actifs (HAART), la majorité des patients
LES CO-INFECTIONS VIH-VHC. EPIDEMIOLOGIE, INTERFERENCES Patrice CACOUB La Pitié Salpêtrière, Paris 8 Avant l introduction des traitements antirétroviraux hautement actifs (HAART), la majorité des patients
Place du médecin généraliste dans la gestion du traitement de l hépatite C C. Buffet*
 Entretiens de Bichat 26 sept. 2013 Salle 352 A 17 h 30 18 h 30 Place du médecin généraliste dans la gestion du traitement de l hépatite C C. Buffet* * Hépatologue, Université Paris XI, Centre de compétence
Entretiens de Bichat 26 sept. 2013 Salle 352 A 17 h 30 18 h 30 Place du médecin généraliste dans la gestion du traitement de l hépatite C C. Buffet* * Hépatologue, Université Paris XI, Centre de compétence
Résistance du virus de l hépatite C aux nouveaux traitements anti-viraux
 14 ème forum SOS Hépatites, Lyon Résistance du virus de l hépatite C aux nouveaux traitements anti-viraux Dr. Sylvie LARRAT Laboratoire de Virologie CHU Grenoble Hépatite C chronique 180 millions de porteurs
14 ème forum SOS Hépatites, Lyon Résistance du virus de l hépatite C aux nouveaux traitements anti-viraux Dr. Sylvie LARRAT Laboratoire de Virologie CHU Grenoble Hépatite C chronique 180 millions de porteurs
Hépatite C une maladie silencieuse..
 Hépatite C une maladie silencieuse.. F. Bally Centre de Maladies Infectieuses et Epidémiologie Institut Central des Hôpitaux Valaisans Histoire Années 70 Hépatite non-a-non-b = hépatite post-transfusionelle
Hépatite C une maladie silencieuse.. F. Bally Centre de Maladies Infectieuses et Epidémiologie Institut Central des Hôpitaux Valaisans Histoire Années 70 Hépatite non-a-non-b = hépatite post-transfusionelle
Compte-rendu de la réunion du 19 septembre 2013
 Secrétariat des Commissions Commission évaluation initiale du rapport entre les bénéfices et les risques des produits de santé N 4 Compte-rendu de la réunion du 19 septembre 2013 PARTICIPANTS Membres de
Secrétariat des Commissions Commission évaluation initiale du rapport entre les bénéfices et les risques des produits de santé N 4 Compte-rendu de la réunion du 19 septembre 2013 PARTICIPANTS Membres de
PRISE EN CHARGE DE L HEPATITE CHRONIQUE C EN 2009
 PRISE EN CHARGE DE L HEPATITE CHRONIQUE C EN 2009 CHU BAB EL OUED DR OSMANE DR MAHIOU PR NAKMOUCHE Evolution du traitement de hépatite c Découverte du génome de l HVC 1989 1989 1989 Evolution du traitement
PRISE EN CHARGE DE L HEPATITE CHRONIQUE C EN 2009 CHU BAB EL OUED DR OSMANE DR MAHIOU PR NAKMOUCHE Evolution du traitement de hépatite c Découverte du génome de l HVC 1989 1989 1989 Evolution du traitement
HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI. http://www.infectiologie.org.tn
 HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI LES MOYENS THERAPEUTIQUES Les interférons La ribavirine Les nouveaux produits INTERFERONS 1957: activité antivirale Interférence
HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI LES MOYENS THERAPEUTIQUES Les interférons La ribavirine Les nouveaux produits INTERFERONS 1957: activité antivirale Interférence
Traitements de l hépatite B
 Traitements de l hépatite B S Matheron Service des maladies infectieuses et tropicales A Hôpital Bichat-Claude Bernard Virus de l hépatite B: histoire naturelle Contage Hépatite aigüe 70% asymptomatique
Traitements de l hépatite B S Matheron Service des maladies infectieuses et tropicales A Hôpital Bichat-Claude Bernard Virus de l hépatite B: histoire naturelle Contage Hépatite aigüe 70% asymptomatique
Place de l interféron dans le traitement de l hépatite B chez le patient co-infecté VIH
 Place de l interféron dans le traitement de l hépatite B chez le patient co-infecté VIH Lionel PIROTH CHU Dijon, Université de Bourgogne Tours juin 2012 Un problème? VIH-VHB Piroth L et al, J Hepatol,
Place de l interféron dans le traitement de l hépatite B chez le patient co-infecté VIH Lionel PIROTH CHU Dijon, Université de Bourgogne Tours juin 2012 Un problème? VIH-VHB Piroth L et al, J Hepatol,
Mme BORGHI Monique Infirmière ETP Mme ALEXIS Françoise Hopital Archet I Infectiologie/Virologie Clinique
 Mme BORGHI Monique Infirmière ETP Mme ALEXIS Françoise Hopital Archet I Infectiologie/Virologie Clinique Une hépatite est une inflammation du foie causée soit par des substances toxiques (médicaments,
Mme BORGHI Monique Infirmière ETP Mme ALEXIS Françoise Hopital Archet I Infectiologie/Virologie Clinique Une hépatite est une inflammation du foie causée soit par des substances toxiques (médicaments,
Hépatite chronique B Moyens thérapeutiques
 Hépatite chronique B Moyens thérapeutiques Dr Olfa BAHRI Laboratoire de Virologie Clinique Institut Pasteur de Tunis INTRODUCTION Plus de 300. 10 6 porteurs chroniques de VHB dans le monde Hépatite chronique
Hépatite chronique B Moyens thérapeutiques Dr Olfa BAHRI Laboratoire de Virologie Clinique Institut Pasteur de Tunis INTRODUCTION Plus de 300. 10 6 porteurs chroniques de VHB dans le monde Hépatite chronique
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
Traitement des hépatites virales
 Traitement des hépatites virales Philippe Sogni Hépato-gatroentérologie gatroentérologie,, Hôpital Cochin et Faculté de Médecine Paris 5 Sogni 1 Hépatite chronique C Sogni 2 Prévalence en France des Ac..
Traitement des hépatites virales Philippe Sogni Hépato-gatroentérologie gatroentérologie,, Hôpital Cochin et Faculté de Médecine Paris 5 Sogni 1 Hépatite chronique C Sogni 2 Prévalence en France des Ac..
Les hépatites virales chroniques B et C
 Les hépatites virales chroniques B et C www.aqodad.ma Service d hépato-gastroentérologie CHU HASSAN II; Fès 6èmes journées médicales d Al Hoceima; Le 28 09 2013 1 Introduction Problème majeur de santé
Les hépatites virales chroniques B et C www.aqodad.ma Service d hépato-gastroentérologie CHU HASSAN II; Fès 6èmes journées médicales d Al Hoceima; Le 28 09 2013 1 Introduction Problème majeur de santé
Traitement des hépatites h chroniques virales B et C
 Traitement des hépatites h chroniques virales B et C Dr Joanna POFELSKI Service d hépatod pato-gastroentérologierologie CH d Annecyd Particularités? Virus hépatotropes / cytopathogènes : lésions hépatiques
Traitement des hépatites h chroniques virales B et C Dr Joanna POFELSKI Service d hépatod pato-gastroentérologierologie CH d Annecyd Particularités? Virus hépatotropes / cytopathogènes : lésions hépatiques
Co-infection HVB HVC CO-infection VIH HVB et HVC
 Co-infection HVB HVC CO-infection VIH HVB et HVC Abdelfattah CHAKIB Faculté de médecine et de pharmacie de Casablanca Service des maladies infectieuses, CHU Ibn Rochd 06 61 42 91 64 afchakib@gmail.com
Co-infection HVB HVC CO-infection VIH HVB et HVC Abdelfattah CHAKIB Faculté de médecine et de pharmacie de Casablanca Service des maladies infectieuses, CHU Ibn Rochd 06 61 42 91 64 afchakib@gmail.com
Christian TREPO, MD, PhD
 PEG INTERFERON MONOTHERAPI E Christian TREPO, MD, PhD Unmet medical needs in chronic HBV infection Inhibition of viral replication Normalisation of ALT Improvement in liver necroinflammation Improvement
PEG INTERFERON MONOTHERAPI E Christian TREPO, MD, PhD Unmet medical needs in chronic HBV infection Inhibition of viral replication Normalisation of ALT Improvement in liver necroinflammation Improvement
Traitement des hépatites virales B et C
 Traitement des hépatites virales B et C GFMER Yaoundé 26 Novembre 2007 Dr José M Bengoa foie cirrhotique foie normal Vitesse de développement de la fibrose fibrose VHD VHB VHC années Indications au traitement
Traitement des hépatites virales B et C GFMER Yaoundé 26 Novembre 2007 Dr José M Bengoa foie cirrhotique foie normal Vitesse de développement de la fibrose fibrose VHD VHB VHC années Indications au traitement
1. Différentes hépatites/ différents traitements
 III. Traitements 55 1. Différentes hépatites/ différents traitements Se faire soigner 1.1 Traitements des hépatites virales D après les expériences pratiques et la littérature scientifique, le traitement
III. Traitements 55 1. Différentes hépatites/ différents traitements Se faire soigner 1.1 Traitements des hépatites virales D après les expériences pratiques et la littérature scientifique, le traitement
Hépatite = inflammation du foie. Pr Bronowicki CHU Nancy - 17.11.2011 Conférence mensuelle - section de Forbach
 Hépatite = inflammation du foie Pr Bronowicki CHU Nancy - 17.11.2011 Conférence mensuelle - section de Forbach 1 Hépatites virales chroniques 2 Histoire naturelle Hépatite aiguë Guérison Hépatite chronique
Hépatite = inflammation du foie Pr Bronowicki CHU Nancy - 17.11.2011 Conférence mensuelle - section de Forbach 1 Hépatites virales chroniques 2 Histoire naturelle Hépatite aiguë Guérison Hépatite chronique
Conférence de consensus Traitement de l hépatite C
 Sociétés savantes copromotrices Avec la participation de FEDERATION NATIONALE DES POLES DE REFERENCES ET RESEAUX HEPATITES Conférence de consensus Traitement de l hépatite C Mercredi 27 et jeudi 28 février
Sociétés savantes copromotrices Avec la participation de FEDERATION NATIONALE DES POLES DE REFERENCES ET RESEAUX HEPATITES Conférence de consensus Traitement de l hépatite C Mercredi 27 et jeudi 28 février
Hépatite B. Le virus Structure et caractéristiques 07/02/2013
 Hépatite B Le virus Structure et caractéristiques o o o Famille des Hepadnaviridae Genre orthohepadnavirus Enveloppé, capside icosaédrique, 42 nm 1 Le virus Structure et caractéristiques En microscopie
Hépatite B Le virus Structure et caractéristiques o o o Famille des Hepadnaviridae Genre orthohepadnavirus Enveloppé, capside icosaédrique, 42 nm 1 Le virus Structure et caractéristiques En microscopie
LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B
 LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B Actualisation février 2009 Ce document est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service communication
LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B Actualisation février 2009 Ce document est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service communication
Y a-t-il une place pour un vaccin thérapeutique contre l hépatite B? H. Fontaine, Unité d Hépatologie Médicale, Hôpital Cochin
 Y a-t-il une place pour un vaccin thérapeutique contre l hépatite B? H. Fontaine, Unité d Hépatologie Médicale, Hôpital Cochin Objectifs thérapeutiques Inhibition de la réplication virale Négativation
Y a-t-il une place pour un vaccin thérapeutique contre l hépatite B? H. Fontaine, Unité d Hépatologie Médicale, Hôpital Cochin Objectifs thérapeutiques Inhibition de la réplication virale Négativation
COMMISSION DE LA TRANSPARENCE. Avis. 23 mai 2007
 COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
Mon traitement n a pas marché.
 tirer profit des différents traitements et soins disponibles être hépatant 13 Mon traitement n a pas marché. Que faire? Nous voulons informer sur l hépatite C, lutter pour une meilleure prise en charge
tirer profit des différents traitements et soins disponibles être hépatant 13 Mon traitement n a pas marché. Que faire? Nous voulons informer sur l hépatite C, lutter pour une meilleure prise en charge
Avis 6 novembre 2013
 COMMISSION DE LA TRANSPARENCE Avis 6 novembre 2013 ISENTRESS, comprimé à croquer 25 mg Flacon de 60 comprimés (CIP : 3400926992408) ISENTRESS, comprimé à croquer sécable 100 mg Flacon de 60 comprimés (CIP
COMMISSION DE LA TRANSPARENCE Avis 6 novembre 2013 ISENTRESS, comprimé à croquer 25 mg Flacon de 60 comprimés (CIP : 3400926992408) ISENTRESS, comprimé à croquer sécable 100 mg Flacon de 60 comprimés (CIP
Le VIH et votre foie
 Le VIH et votre foie Le VIH et votre foie Que dois-je savoir au sujet de mon foie? Votre foie joue un rôle incroyablement important. Il filtre votre sang en éliminant les substances nocives (toxiques)
Le VIH et votre foie Le VIH et votre foie Que dois-je savoir au sujet de mon foie? Votre foie joue un rôle incroyablement important. Il filtre votre sang en éliminant les substances nocives (toxiques)
Item 169 : Évaluation thérapeutique et niveau de preuve
 Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
TRAITEMENT DE L HÉPATITE B
 TRAITEMENT DE L HÉPATITE B P Mathurin Service d Hépatogastroentérologie Pr Paris Hôpital Claude Hurriez CHRU Lille CRITERES VIROLOGIQUES ET HISTOIRE NATURELLE 1 OBJECTIF THERAPEUTIQUE: Séroconversion HBe
TRAITEMENT DE L HÉPATITE B P Mathurin Service d Hépatogastroentérologie Pr Paris Hôpital Claude Hurriez CHRU Lille CRITERES VIROLOGIQUES ET HISTOIRE NATURELLE 1 OBJECTIF THERAPEUTIQUE: Séroconversion HBe
Traitement des Hépatites Chroniques Virales B et C
 Réunion Tunisienne de Consensus Organisée par La Société Tunisienne de Gastro-entérologie Sous l égide de La Société Tunisienne des Sciences Médicales Traitement des Hépatites Chroniques Virales B et C
Réunion Tunisienne de Consensus Organisée par La Société Tunisienne de Gastro-entérologie Sous l égide de La Société Tunisienne des Sciences Médicales Traitement des Hépatites Chroniques Virales B et C
F ZOULIM. Traitement du VHB : Interféron ou anti-viraux
 F ZOULIM Traitement du VHB : Interféron ou anti-viraux - Connaître les objectifs du traitement - Connaître les résultats immédiats et à long terme des traitements - Savoir choisir une option thérapeutique
F ZOULIM Traitement du VHB : Interféron ou anti-viraux - Connaître les objectifs du traitement - Connaître les résultats immédiats et à long terme des traitements - Savoir choisir une option thérapeutique
Traitement des hépatites virales
 Traitement des hépatites virales IFMT Séminaire hépatites mai 2006. IFMT-MS-Sémin Hépatites-2006 1 Principes de base 1. Hépatites aigues : on ne traite pas! (VHA, VHE, VHB aigue) aucun traitement n a fait
Traitement des hépatites virales IFMT Séminaire hépatites mai 2006. IFMT-MS-Sémin Hépatites-2006 1 Principes de base 1. Hépatites aigues : on ne traite pas! (VHA, VHE, VHB aigue) aucun traitement n a fait
Thérapeutique anti-vhc et travail maritime. O. Farret HIA Bégin
 Thérapeutique anti-vhc et travail maritime O. Farret HIA Bégin Introduction «L hépatite C est une maladie le plus souvent mineure, mais potentiellement cancérigène, qu on peut ne pas traiter et surveiller
Thérapeutique anti-vhc et travail maritime O. Farret HIA Bégin Introduction «L hépatite C est une maladie le plus souvent mineure, mais potentiellement cancérigène, qu on peut ne pas traiter et surveiller
GUIDE AFFECTION DE LONGUE DURÉE. Hépatite chronique B
 GUIDE AFFECTION DE LONGUE DURÉE Hépatite chronique B Octobre 2006 Ce guide médecin est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service communication 2 avenue du Stade de France F 93218
GUIDE AFFECTION DE LONGUE DURÉE Hépatite chronique B Octobre 2006 Ce guide médecin est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service communication 2 avenue du Stade de France F 93218
HEPATITES VIRALES 22/09/09. Infectieux. Mme Daumas
 HEPATITES VIRALES 22/09/09 Mme Daumas Infectieux Introduction I. Hépatite aigu II. Hépatite chronique III. Les différents types d hépatites A. Hépatite A 1. Prévention de la transmission 2. Vaccination
HEPATITES VIRALES 22/09/09 Mme Daumas Infectieux Introduction I. Hépatite aigu II. Hépatite chronique III. Les différents types d hépatites A. Hépatite A 1. Prévention de la transmission 2. Vaccination
Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE. Hépatite chronique B
 Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE Hépatite chronique B Février 2015 Ce document est téléchargeable sur : www.has-sante.fr Haute Autorité de Santé Service des
Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE Hépatite chronique B Février 2015 Ce document est téléchargeable sur : www.has-sante.fr Haute Autorité de Santé Service des
Lettre à l éditeur. Résistance du VIH aux Antirétroviraux : Quoi de neuf au Mali? Quelles. perspectives?
 Lettre à l éditeur Résistance du VIH aux Antirétroviraux : Quoi de neuf au Mali? Quelles perspectives? HIV Antiretroviral Drug Resistance: What s new in Mali? What is the future? Maiga AI 1,2, Sangare
Lettre à l éditeur Résistance du VIH aux Antirétroviraux : Quoi de neuf au Mali? Quelles perspectives? HIV Antiretroviral Drug Resistance: What s new in Mali? What is the future? Maiga AI 1,2, Sangare
Accès aux antiviraux contre les hépatites dans les pays à bas et moyens revenus : produire localement des génériques. Maurice Cassier CNRS CERMES3
 Accès aux antiviraux contre les hépatites dans les pays à bas et moyens revenus : produire localement des génériques Maurice Cassier CNRS CERMES3 Production de génériques dans les PVD et accessibilité
Accès aux antiviraux contre les hépatites dans les pays à bas et moyens revenus : produire localement des génériques Maurice Cassier CNRS CERMES3 Production de génériques dans les PVD et accessibilité
Août 2010. a thérapie. antirétrovirale. pour les adultes infectés par le VIH. Guide pour les professionnels de la santé du Québec
 Août 2010 a thérapie antirétrovirale pour les adultes infectés par le VIH Guide pour les professionnels de la santé du Québec Août 2010 a thérapie antirétrovirale pour les adultes infectés par le VIH
Août 2010 a thérapie antirétrovirale pour les adultes infectés par le VIH Guide pour les professionnels de la santé du Québec Août 2010 a thérapie antirétrovirale pour les adultes infectés par le VIH
USAGERS DE DROGUE ET VHC ADIJA CHAMPAGNOLE MARDI 17 MARS
 USAGERS DE DROGUE ET VHC ADIJA CHAMPAGNOLE MARDI 17 MARS RAPPELS Répartition des patients VHC 15% Nosocomial 20% Autres + Inconnue 3% Activité prof. 37 % Transfusion 1 % sexuel 25 % Toxicomanie IV D'après
USAGERS DE DROGUE ET VHC ADIJA CHAMPAGNOLE MARDI 17 MARS RAPPELS Répartition des patients VHC 15% Nosocomial 20% Autres + Inconnue 3% Activité prof. 37 % Transfusion 1 % sexuel 25 % Toxicomanie IV D'après
HEPATITES VIRALES CHRONIQUES ET AIGUES
 HEPATITES VIRALES CHRONIQUES ET AIGUES INFORMATIONS Pré-requis : Durée de l'item : Auteur(s) : Professeur Louis Buscail (mail : ) Objectifs : RAPPEL : LE DIAGNOSTIC D HEPATITE CHRONIQUE La fréquence de
HEPATITES VIRALES CHRONIQUES ET AIGUES INFORMATIONS Pré-requis : Durée de l'item : Auteur(s) : Professeur Louis Buscail (mail : ) Objectifs : RAPPEL : LE DIAGNOSTIC D HEPATITE CHRONIQUE La fréquence de
TRAITEMENT ACTUEL DE L HÉPATITE C : PLACE DE LA RIBAVIRINE
 Évaluation thérapeutique : TRAITEMENT ACTUEL DE L HÉPATITE C : PLACE DE LA RIBAVIRINE 1. Évaluation clinique 2. Évaluation pharmaco-économique 5 É d i t o r i a l Depuis 10 ans, date à laquelle le virus
Évaluation thérapeutique : TRAITEMENT ACTUEL DE L HÉPATITE C : PLACE DE LA RIBAVIRINE 1. Évaluation clinique 2. Évaluation pharmaco-économique 5 É d i t o r i a l Depuis 10 ans, date à laquelle le virus
L. Clivaz Mariotti. Médecine interne FMH RFSM
 L. Clivaz Mariotti Médecine interne FMH RFSM Conflits d intérêts Pas de conflit d intérêt Première partie : problèmes somatiques courants Problèmes cutanés Problèmes nutritionnels Problèmes dentaires Problèmes
L. Clivaz Mariotti Médecine interne FMH RFSM Conflits d intérêts Pas de conflit d intérêt Première partie : problèmes somatiques courants Problèmes cutanés Problèmes nutritionnels Problèmes dentaires Problèmes
Définition de l Infectiologie
 Définition de l Infectiologie Discipline médicale clinique Spécialisée. Prise en charge des Maladies Infectieuses et Tropicales. Actuelles, émergentes ou ré-émergentes. Référents dans le cadre d un maillage
Définition de l Infectiologie Discipline médicale clinique Spécialisée. Prise en charge des Maladies Infectieuses et Tropicales. Actuelles, émergentes ou ré-émergentes. Référents dans le cadre d un maillage
Pathologie VIH. Service maladies infectieuses Archet 1. Françoise ALEXIS, infirmière Monique BORGHI, infirmière 15 octobre 2013
 Pathologie VIH Service maladies infectieuses Archet 1 Françoise ALEXIS, infirmière Monique BORGHI, infirmière 15 octobre 2013 Les traitements antirétroviraux Sont classés en 5 familles selon leur mode
Pathologie VIH Service maladies infectieuses Archet 1 Françoise ALEXIS, infirmière Monique BORGHI, infirmière 15 octobre 2013 Les traitements antirétroviraux Sont classés en 5 familles selon leur mode
Journée Mondiale des Hépatites
 2 Bulletin d information de REVIH-STS Réseau de Santé VIH - Hépatites - Toxicomanies en Savoie Journée Mondiale des Hépatites Sommaire Edito / Pôle hépatites.p.1 Education thérapeutique / Nutrition...p.2
2 Bulletin d information de REVIH-STS Réseau de Santé VIH - Hépatites - Toxicomanies en Savoie Journée Mondiale des Hépatites Sommaire Edito / Pôle hépatites.p.1 Education thérapeutique / Nutrition...p.2
Bon usage. Mise au point
 Bon usage Mise au point Évaluation et prise en charge des troubles psychiatriques chez les patients adultes infectés par le virus de l hépatite C et traités par (peg) interféron alfa et ribavirine Mai
Bon usage Mise au point Évaluation et prise en charge des troubles psychiatriques chez les patients adultes infectés par le virus de l hépatite C et traités par (peg) interféron alfa et ribavirine Mai
Nouvelles thérapeutiques du VHC: progrès vers l éradication virale
 Nouvelles thérapeutiques du VHC: progrès vers l éradication virale Fabien Zoulim Service d hépatologie, Hospices Civils de Lyon & Laboratoire des Hépatites, INSERM U1052 Université de Lyon, France Prévalence
Nouvelles thérapeutiques du VHC: progrès vers l éradication virale Fabien Zoulim Service d hépatologie, Hospices Civils de Lyon & Laboratoire des Hépatites, INSERM U1052 Université de Lyon, France Prévalence
ACTUALITES THERAPEUTIQUES. Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012
 ACTUALITES THERAPEUTIQUES Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012 Traitement de fond Objectifs: Réduire le nombre de poussées Arrêter ou freiner la progression du handicap Les traitements disponibles
ACTUALITES THERAPEUTIQUES Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012 Traitement de fond Objectifs: Réduire le nombre de poussées Arrêter ou freiner la progression du handicap Les traitements disponibles
Virus de l hépatite B
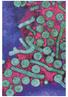 Virus de l hépatite B Virus de l hépatite B Hépatite aiguë B Virus de l hépatite B Hépatite aiguë B Persistance de l antigène HBs 10% - 90% Virus de l hépatite B Hépatite aiguë B faible ou absente Persistance
Virus de l hépatite B Virus de l hépatite B Hépatite aiguë B Virus de l hépatite B Hépatite aiguë B Persistance de l antigène HBs 10% - 90% Virus de l hépatite B Hépatite aiguë B faible ou absente Persistance
MONOGRAPHIE. Pr PEGASYS. peginterféron alfa-2a injectable. Seringues préremplies : 180 µg/0,5 ml. Flacons à usage unique : 180 µg/1 ml
 MONOGRAPHIE Pr PEGASYS peginterféron alfa2a injectable Seringues préremplies : 180 µg/0,5 ml Flacons à usage unique : 180 µg/1 ml Autoinjecteur ProClick : 180 µg/0,5 ml Modificateur de la réponse biologique
MONOGRAPHIE Pr PEGASYS peginterféron alfa2a injectable Seringues préremplies : 180 µg/0,5 ml Flacons à usage unique : 180 µg/1 ml Autoinjecteur ProClick : 180 µg/0,5 ml Modificateur de la réponse biologique
Une forte dynamique des prescriptions de ces nouveaux anti-coagulants oraux
 27 novembre 2013 Nouveaux anti-coagulants oraux : une étude de l Assurance Maladie souligne la dynamique forte de ces nouveaux médicaments et la nécessité d une vigilance accrue dans leur utilisation Les
27 novembre 2013 Nouveaux anti-coagulants oraux : une étude de l Assurance Maladie souligne la dynamique forte de ces nouveaux médicaments et la nécessité d une vigilance accrue dans leur utilisation Les
Prise en charge thérapeutique des personnes infectées par le VIH
 Prise en charge thérapeutique des personnes infectées par le VIH 2004 Prise en charge thérapeutique des personnes infectées par le VIH Rapport 2004 Recommandations du groupe d experts Sous la direction
Prise en charge thérapeutique des personnes infectées par le VIH 2004 Prise en charge thérapeutique des personnes infectées par le VIH Rapport 2004 Recommandations du groupe d experts Sous la direction
Détection et prise en charge de la résistance aux antirétroviraux
 Détection et prise en charge de la résistance aux antirétroviraux Jean Ruelle, PhD AIDS Reference Laboratory, UCLouvain, Bruxelles Corata 2011, Namur, 10 juin 2011 Laboratoires de référence SIDA (Belgique)
Détection et prise en charge de la résistance aux antirétroviraux Jean Ruelle, PhD AIDS Reference Laboratory, UCLouvain, Bruxelles Corata 2011, Namur, 10 juin 2011 Laboratoires de référence SIDA (Belgique)
Mise à jour VIH Revue des données récentes concernant les nouveaux traitements antiviraux
 Mise à jour VIH Revue des données récentes concernant les nouveaux traitements antiviraux Soutenu par une bourse indépendante de formation de ViiV Healthcare. www.medscape.org/viewarticle/826417 Mise à
Mise à jour VIH Revue des données récentes concernant les nouveaux traitements antiviraux Soutenu par une bourse indépendante de formation de ViiV Healthcare. www.medscape.org/viewarticle/826417 Mise à
Le titrage de l AgHBs: un témoin du statut du patient et de la réponse au traitement. Denis Ouzan Institut Arnault Tzanck, Saint-Laurent-du-Var
 Le titrage de l AgHBs: un témoin du statut du patient et de la réponse au traitement Denis Ouzan Institut Arnault Tzanck, Saint-Laurent-du-Var Objectifs pédagogiques Connaitre les problèmes pratiques posés
Le titrage de l AgHBs: un témoin du statut du patient et de la réponse au traitement Denis Ouzan Institut Arnault Tzanck, Saint-Laurent-du-Var Objectifs pédagogiques Connaitre les problèmes pratiques posés
Comité d organisation
 Workshop Comité d organisation Khadija Akarid Abdelkrim Benbouzid Abdellah Badou Nadia Bouhaddioui Zakaria Chraïbi Hassan Fellah Jamal Hafid Fouad Seghrouchni Faculté polydisciplinaire de Safi Laboratoire
Workshop Comité d organisation Khadija Akarid Abdelkrim Benbouzid Abdellah Badou Nadia Bouhaddioui Zakaria Chraïbi Hassan Fellah Jamal Hafid Fouad Seghrouchni Faculté polydisciplinaire de Safi Laboratoire
Tabac et VIH : descendre au bon arrêt!
 >> Hiver 2013 - Printemps 2014 #87 Tabac et VIH : descendre au bon arrêt! Remaides Québec numéro 18 Forum après forum, bataille après bataille 2 >> Sommaire REMAIDES #87 I 08 12 04 Courrier 05 Edito VHC
>> Hiver 2013 - Printemps 2014 #87 Tabac et VIH : descendre au bon arrêt! Remaides Québec numéro 18 Forum après forum, bataille après bataille 2 >> Sommaire REMAIDES #87 I 08 12 04 Courrier 05 Edito VHC
Observation. Merci à l équipe de pharmaciens FormUtip iatro pour ce cas
 Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Mise à jour du formulaire pour les régimes de médicaments du Nouveau-Brunswick
 Bulletin n 902 le 6 mars 2015 Mise à jour du formulaire pour les régimes de médicaments du Nouveau-Brunswick Cette mise à jour du formulaire pour les régimes de médicaments du Nouveau-Brunswick entre en
Bulletin n 902 le 6 mars 2015 Mise à jour du formulaire pour les régimes de médicaments du Nouveau-Brunswick Cette mise à jour du formulaire pour les régimes de médicaments du Nouveau-Brunswick entre en
Conflits d intérêt P-M Girard
 Télaprévir en association avec peg-interféron alfa/ribavirine chez les patients co-infectés VIH/VHC : résultats finaux 24 semaines après fin de traitement (RVS24) Essai VX 110 Pierre-Marie Girard 1, Vincent
Télaprévir en association avec peg-interféron alfa/ribavirine chez les patients co-infectés VIH/VHC : résultats finaux 24 semaines après fin de traitement (RVS24) Essai VX 110 Pierre-Marie Girard 1, Vincent
Document de synthèse : Hépatite B et hépatite C. Sommaire :
 Document de synthèse : Hépatite B et hépatite C Sommaire : Au Canada, l hépatite B et l hépatite C demeurent de graves enjeux de santé publique en raison de taux de prévalence élevés, de coûts élevés pour
Document de synthèse : Hépatite B et hépatite C Sommaire : Au Canada, l hépatite B et l hépatite C demeurent de graves enjeux de santé publique en raison de taux de prévalence élevés, de coûts élevés pour
Normes canadiennes pour la lutte antituberculeuse
 Normes canadiennes pour la lutte antituberculeuse 7 ième édition Chapitre 10 : La tuberculose et le virus de l immunodéficience humaine Normes canadiennes pour la lutte antituberculeuse, 7 ième édition
Normes canadiennes pour la lutte antituberculeuse 7 ième édition Chapitre 10 : La tuberculose et le virus de l immunodéficience humaine Normes canadiennes pour la lutte antituberculeuse, 7 ième édition
GASTRO-ENTEROLOGIE. Variabilité. A des entrées. B des sites anatomiques. C inter-individuelle. D intra-individuelle
 GASTRO-ENTEROLOGIE Variabilité A des entrées B des sites anatomiques 2 l externe + 2 l interne 15 litres sécrétion-absorption entrée 2 l duodénum 4 l grêle 3 l côlon 0,3 l anus 0,3 l œsophage 10" estomac
GASTRO-ENTEROLOGIE Variabilité A des entrées B des sites anatomiques 2 l externe + 2 l interne 15 litres sécrétion-absorption entrée 2 l duodénum 4 l grêle 3 l côlon 0,3 l anus 0,3 l œsophage 10" estomac
Virus de l hépatite C
 Virus de l hépatite C Dr Dominique Bettinger Laboratoire de Virologie CHU Saint Jacques Besançon Le 17 Avril 2004 Historique La transfusion en masse a été à l origine de nbreuses hépatites post-transfusionnelles
Virus de l hépatite C Dr Dominique Bettinger Laboratoire de Virologie CHU Saint Jacques Besançon Le 17 Avril 2004 Historique La transfusion en masse a été à l origine de nbreuses hépatites post-transfusionnelles
Hépatite. du dépistage au traitement. Questions et réponses. L hépatite C Dépistage, clinique, prise en charge et conseils aux patients
 DOCUMENT À L USAGE DES PATIENTS Également disponible : L hépatite C Dépistage, clinique, prise en charge et conseils aux patients (document à l usage des professionnels de santé) Document édité et diffusé
DOCUMENT À L USAGE DES PATIENTS Également disponible : L hépatite C Dépistage, clinique, prise en charge et conseils aux patients (document à l usage des professionnels de santé) Document édité et diffusé
Prophylaxie infectieuse après exposition professionnelle
 1 Prophylaxie infectieuse après exposition professionnelle Introduction Le personnel soignant est régulièrement confronté au risque de contamination par le virus de l immunodéficience humaine (VIH) mais
1 Prophylaxie infectieuse après exposition professionnelle Introduction Le personnel soignant est régulièrement confronté au risque de contamination par le virus de l immunodéficience humaine (VIH) mais
C comme Cirrhose. être hépatant7. apprendre à vivre avec une cirrhose
 BROCHURE BLEUE comprendre et m adapter aux différentes situations de la maladie être hépatant7 C comme Cirrhose apprendre à vivre avec une cirrhose Nous voulons informer sur l hépatite C, lutter pour une
BROCHURE BLEUE comprendre et m adapter aux différentes situations de la maladie être hépatant7 C comme Cirrhose apprendre à vivre avec une cirrhose Nous voulons informer sur l hépatite C, lutter pour une
INTERFERON Traitement adjuvant du mélanome à haut risque de récidive. Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper
 INTERFERON Traitement adjuvant du mélanome à haut risque de récidive Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper Pourquoi proposer un TTT adjuvant? Probabilité de survie à 10 ans en fonction
INTERFERON Traitement adjuvant du mélanome à haut risque de récidive Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper Pourquoi proposer un TTT adjuvant? Probabilité de survie à 10 ans en fonction
Actualités sur l hépatite C. 20 Janvier 2004
 Actualités sur l hépatite C 20 Janvier 2004 Guérison sans séroconversion? CONTAMINATION 4 à 12 semaines HEPATITE AIGUE 15-45 % 55-85 % GUERISON ARN VHC- 25-40% INFECTION CHRONIQUE ARN VHC+ 60-75% ALAT
Actualités sur l hépatite C 20 Janvier 2004 Guérison sans séroconversion? CONTAMINATION 4 à 12 semaines HEPATITE AIGUE 15-45 % 55-85 % GUERISON ARN VHC- 25-40% INFECTION CHRONIQUE ARN VHC+ 60-75% ALAT
Quantification de l AgHBs Pouquoi? Quand?
 Quantification de l AgHBs Pouquoi? Quand? Michelle Martinot-Peignoux Service d Hépatologie Hôpital Beaujon Université Paris-Diderot INSERM U-773/CRB3 Clichy-France Plan Introduction Applications Cliniques
Quantification de l AgHBs Pouquoi? Quand? Michelle Martinot-Peignoux Service d Hépatologie Hôpital Beaujon Université Paris-Diderot INSERM U-773/CRB3 Clichy-France Plan Introduction Applications Cliniques
Hépatite B. Risques, prévention et traitement. Prof. Dr méd. Stefan Zeuzem. European Liver Patients Association
 Prof. Dr méd. Stefan Zeuzem Hépatite B Risques, prévention et traitement European Liver Patients Association F. De Renesselaan, 57 B - 3800 Sint-Truiden, Belgium email: contact@elpa-info.org Chère patiente,
Prof. Dr méd. Stefan Zeuzem Hépatite B Risques, prévention et traitement European Liver Patients Association F. De Renesselaan, 57 B - 3800 Sint-Truiden, Belgium email: contact@elpa-info.org Chère patiente,
Plan. Introduction. Les Nouveaux Anticoagulants Oraux et le sujet âgé. Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or
 Plan Introduction Les Nouveaux Anticoagulants Oraux et le sujet âgé Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or Introduction NACO: une actualité brûlante! AVK: Plus forte incidence
Plan Introduction Les Nouveaux Anticoagulants Oraux et le sujet âgé Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or Introduction NACO: une actualité brûlante! AVK: Plus forte incidence
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
L investigation chez la personne infectée par le VIH
 P O U R Q U O I P A R L E R D U V I H E N 2 0 0 4? 2 L investigation chez la personne infectée par le VIH quand et comment utiliser les différents tests de laboratoire? par Harold Dion Paul, un homme de
P O U R Q U O I P A R L E R D U V I H E N 2 0 0 4? 2 L investigation chez la personne infectée par le VIH quand et comment utiliser les différents tests de laboratoire? par Harold Dion Paul, un homme de
Comprimé Comprimé ovale, sécable, blanc à blanc cassé, portant l inscriptions «TMC» gravée sur une face. Le comprimé peut être divisé en doses égales.
 1. DÉNOMINATION DU MÉDICAMENT INTELENCE 25 mg comprimés 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque comprimé contient 25 mg d. Excipient à effet notoire : chaque comprimé contient 40 mg de lactose.
1. DÉNOMINATION DU MÉDICAMENT INTELENCE 25 mg comprimés 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque comprimé contient 25 mg d. Excipient à effet notoire : chaque comprimé contient 40 mg de lactose.
Les analyses virologiques pour le diagnostic et la prise en charge thérapeutique de l infection au VHC
 Les analyses virologiques pour le diagnostic et la prise en charge thérapeutique de l infection au VHC Donald Murphy, PhD Laboratoire de santé publique du Québec PNMVS, Montréal, 15 octobre 2013 Plan de
Les analyses virologiques pour le diagnostic et la prise en charge thérapeutique de l infection au VHC Donald Murphy, PhD Laboratoire de santé publique du Québec PNMVS, Montréal, 15 octobre 2013 Plan de
Diagnostic et suivi virologique des hépatites virales B et C. Marie-Laure Chaix Virologie Necker
 Diagnostic et suivi virologique des hépatites virales B et C Marie-Laure Chaix Virologie Necker OUTILS DIAGNOSTIQUES VHC Transaminases Recherche des Anticorps! Tests indirects - Anticorps! ELISA! RIBA
Diagnostic et suivi virologique des hépatites virales B et C Marie-Laure Chaix Virologie Necker OUTILS DIAGNOSTIQUES VHC Transaminases Recherche des Anticorps! Tests indirects - Anticorps! ELISA! RIBA
COMMISSION DE LA TRANSPARENCE. Avis. 3 septembre 2008
 COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
Hépatite. Dépistage, clinique, prise en charge et conseils aux patients DOCUMENT À L USAGE DES PROFESSIONNELS DE SANTÉ
 DOCUMENT À L USAGE DES PROFESSIONNELS DE SANTÉ Hépatite C Dépistage, clinique, prise en charge et conseils aux patients Etat des connaissances : Août 2001 Table des matières 4page 4 8page 8 Indications
DOCUMENT À L USAGE DES PROFESSIONNELS DE SANTÉ Hépatite C Dépistage, clinique, prise en charge et conseils aux patients Etat des connaissances : Août 2001 Table des matières 4page 4 8page 8 Indications
Traitement de l hépatite C chez le sujet infecté par le VIH Actualités 2004
 Traitement de l hépatite C chez le sujet infecté par le VIH Actualités 2004 Pr C. PERRONNE Service des Maladies Infectieuses et Tropicales Hôpital Raymond Poincaré Faculté de Médecine Paris - Ile de France
Traitement de l hépatite C chez le sujet infecté par le VIH Actualités 2004 Pr C. PERRONNE Service des Maladies Infectieuses et Tropicales Hôpital Raymond Poincaré Faculté de Médecine Paris - Ile de France
Author Disclosures DT Dieterich V Soriano KE Sherman P-M Girard JK Rockstroh J Henshaw, R Rubin, M Bsharat, and N Adda MS Sulkowski
 Télaprévir en association avec peginterféron alfa-2a/ribavirine chez les patients co-infectés VIH/VHC : analyse intermédiaire 12 semaines après traitement (RVS12) Essai VX 110 Pierre-Marie Girard 1, Vincent
Télaprévir en association avec peginterféron alfa-2a/ribavirine chez les patients co-infectés VIH/VHC : analyse intermédiaire 12 semaines après traitement (RVS12) Essai VX 110 Pierre-Marie Girard 1, Vincent
27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013
 27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013 Les Nouveaux Anticoagulants Oraux (NACO) dans la maladie thrombo embolique veineuse INTRODUCTION Thrombose veineuse
27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013 Les Nouveaux Anticoagulants Oraux (NACO) dans la maladie thrombo embolique veineuse INTRODUCTION Thrombose veineuse
Nouveaux développements en recherche sur le VHC et leurs répercussions sur la pratique de première ligne
 Nouveaux développements en recherche sur le VHC et leurs répercussions sur la pratique de première ligne Marie-Louise Vachon, M.D., M.Sc. Microbiologiste-Infectiologue CHUQ- Centre Hospitalier de l Université
Nouveaux développements en recherche sur le VHC et leurs répercussions sur la pratique de première ligne Marie-Louise Vachon, M.D., M.Sc. Microbiologiste-Infectiologue CHUQ- Centre Hospitalier de l Université
Révision des descriptions génériques Comment monter un dossier?
 DISPOSITIFS MEDICAUX Révision des descriptions génériques Comment monter un dossier? Guide pour le dossier déposé par les fabricants/distributeurs Adopté en séance de la CEPP* le 13 juillet 2005 *CEPP
DISPOSITIFS MEDICAUX Révision des descriptions génériques Comment monter un dossier? Guide pour le dossier déposé par les fabricants/distributeurs Adopté en séance de la CEPP* le 13 juillet 2005 *CEPP
Point d Information. Le PRAC a recommandé que le RCP soit modifié afin d inclure les informations suivantes:
 Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Lecture historique et prospective du rôle de la barrière génétique
 Lecture historique et prospective du rôle de la barrière génétique Clotilde Allavena NANTES Symposium JANSSEN JNI 2011, Toulouse Jusqu en 1996, la montée en puissance Bithérapie 2 NUCs Trithérapie 2 NUCs
Lecture historique et prospective du rôle de la barrière génétique Clotilde Allavena NANTES Symposium JANSSEN JNI 2011, Toulouse Jusqu en 1996, la montée en puissance Bithérapie 2 NUCs Trithérapie 2 NUCs
Pierre-Yves Comtois, Marc Leclerc, Bruno Lemay, Karina Ortega Révision scientifique : Benoît Lemire, pharmacien
 P RTAIL VIH / sida du Québec Hépatite C Retour sur les symposiums hépatite C 2012 Pierre-Yves Comtois, Marc Leclerc, Bruno Lemay, Karina Ortega Révision scientifique : Benoît Lemire, pharmacien Le 3 et
P RTAIL VIH / sida du Québec Hépatite C Retour sur les symposiums hépatite C 2012 Pierre-Yves Comtois, Marc Leclerc, Bruno Lemay, Karina Ortega Révision scientifique : Benoît Lemire, pharmacien Le 3 et
Cas clinique 2. Florence JOLY, Caen François IBORRA, Montpellier
 Cas clinique 2 Florence JOLY, Caen François IBORRA, Montpellier Cas clinique Patient de 60 ans, ATCD: HTA, IDM en 2007, hypercholestérolémie Juin 2008: Toux, dyspnée (sous 02) et anorexie progressive Bilan
Cas clinique 2 Florence JOLY, Caen François IBORRA, Montpellier Cas clinique Patient de 60 ans, ATCD: HTA, IDM en 2007, hypercholestérolémie Juin 2008: Toux, dyspnée (sous 02) et anorexie progressive Bilan
