Résumé. Mots clés : Cancers mammaires, immunohistochimie, HER2, RE/RP, hormonosensibilité, chimiorésistance.
|
|
|
- Edmond Pothier
- il y a 8 ans
- Total affichages :
Transcription
1 Résumé Le cancer du sein constitue un problème majeur de santé publique, à la fois dans les pays industrialisés, et dans les pays en voie de développement où son incidence ne cesse d augmenter d année en année, en Algérie ce cancer représente 50% des cancers gynécologiques. Le type histologique des cancers est un élément important pour la conduite thérapeutique et le pronostic, dans un premier temps nous nous sommes intéressés à l étude anatomopathologique des prélèvements mammaires. Les tumeurs malignes du sein les plus rencontrées furent les adénocarcinomes développés à partir des canaux galactophores qui représentent 98% des tumeurs malignes du sein. La technique immunohistochimique (IHC) est d un très grand apport pour le diagnostic en oncologie : pour aider à classer une tumeur dans sa catégorie, pour identifier l origine d une métastase et, dans certains cas, pour aider à établir la malignité d une lésion. Nous avons travaillé sur 39 carcinomes mammaires infiltrants fixés et inclus en paraffine, les anticorps primaires ont été choisis en fonction de l antigène recherché. Notre étude a pour but en premier lieu de confirmer, par l immunohistochimie, l étude histologique et en deuxième lieu, la mise en place de cette techniques en vue de déterminer l hormonosensibilité (récepteurs hormonaux RH), et la chimiorésistance (oncogène HER2), mais aussi de différencier entre les carcinomes (EMA et Cytokératine positifs), et les sarcomes (vimentine positif). Concernent nos résultats, 20,51% des 39 carcinomes mammaires sont RE+/RP+, avec une intensité de marquage allant de 50 à 80%, alors que 37,5% sont HER2+, pour les marqueurs confirmant la nature épithéliale des tumeurs (EMA Cytokératine), nous avons obtenu des positivités confirmant le diagnostic de l étude histologique, en retenant comme positives, les valeurs supérieures à 10% des cellules marquées. Les cellules carcinomateuses qui surexpriment l HER2 est de mauvais pronostic, cette même tumeur est caractérisée par l absence des récepteurs hormonaux, qui eux par contre sont de bon pronostic et facteur prédictif d une réponse à l hormonothérapie. Mots clés : Cancers mammaires, immunohistochimie, HER2, RE/RP, hormonosensibilité, chimiorésistance.
2 Ac : Anticorps AEC : 3-Amino-9-Ethyl-Carbazole AEP : Atypie Epithéliale Plane AF-1 : Activation de facteur de transcription1 AFAQAP : Association Française d Assurance Qualité en Anatomie Pathologique Ag : Antigène AI : Index apoptotique AP-1 : Protéine activatrice-1 APS : Autopalpation des seins BRCA1 et BRCA2 : Breast Cancer 1et 2 CCI : Carcinome canalaire infiltrant CCIS : Carcinome canalaire in situ CDK : Cyclin Dependant Kinase CLI : Carcinome lobulaire infiltrant CLIS : Carcinome lobulaire in situ CO : Contraception orale DAB : 3,3-Diaminobenzidine DBD : Binding Domain DIN : Ductal Intra-epithelial Néoplasia EGF : Epithelial grow factor enos : Endothéliale NO synthase ERE : Elément de réponse aux œstrogènes FGF : Fibroblast growth factor FSH : Folliculo Stimulating Hormone GnRH : Gonadotrophin Releasing Hormon HCA : Hyperplasie canalaire atypique HCS : Hyperplasie canalaire simple HER : Humen Epithélial Grow Factor Receptor HSP : Heat shock protein" ou Hsp IA : Inhibiteurs de l aromatase IHC : Immunohistochimie IMC ; Index de masse corporelle l IGF-1 : insulin-like growth factor LBD : Ligand Binding Domain LH : Luteinizing Hormone MAKK-MEK : Mitogen activated phosphoryled kinase kinase) MAPKK : Mitogen activated phosphoryled kinase kinase MFK : Maladie fibrokystique MGG: May-Grünwald-Giemsa MORE : Multiple Outcomes of Raloxifene Evaluation trial NL : Néoplasie Lobulaire NSABP : National Surgical Adjuvant Breast Project) OMS : Organisation mondiale de la santé PAP : Péroxydase-anti-peroxydase PDK1-PRK2 : 3 phospho-inosotide dependant proteine kinase PI3K : Phospho-inositol triphosphate kinase PRL : Prolactine PTEN : phosphatase and tensin homologue deleted on chromosome ten RAR : Acide rétinoïque trans (RAR), Ras: Rous avian sarcoma RB : Rétinoblastome RE : Récepteurs d œstrogène REGF : Receptor l epidermal growth factor RH : Récepteurs hormonaux RP : récepteur à la progestérone RTK : Les récepteurs doués d activité de tyrosine kinase (RTK) SARM : Modulateurs sélectifs des récepteurs des œstrogènes SBR : Scarff Bloom et Richardson SHBG : Sex hormone-binding globulin SO : Suppression ovarienne SPHH : Système Porte Hypothalamo- Hypophysaire STAR : Study of Tamoxifen and Raloxifene TP : Pumeurs phyllode TR : Récepteur des hormones thyroïdiennes TSH : Traitement hormonal substitutif UTDL : Uunité terminale ductulobulaire VEGF: Vascular endothelial grow factor V-erbB : Virus de l érythroblastose aviaire
3 Figure 1 : Coupe au niveau de la glande mammaire... 4 Figure 2 : Unité terminale ductulobulaire... 6 Figure 3 : Réseau vasculaire de la glande mammaire... 7 Figure 4 : Réseau lymphatique de la glande mammaire... 9 Figure 5 : Lobes et lobules mammaires Figure 6 : Coupe histologique pour identifier les cellules myoépithéliales (M) autour des alvéoles (A) et les vaisseaux sanguins (b) Figure 7 : Localisation de la glande hypothalamo-hypophysaire Figure 8 : Concentrations hormonales de l axe hypothalamo-hypophysaire au cours d un cycle sexuel chez la femme (en absence de fécondation) Figure 9 : Niveau d action hormonale chez la femme Figure 10 : Les voies de signalisation cellulaire par la liaison du ligand à l HER Figure 11 : Cascade de réponse induite par le stimuli externe et réponse physiologique qui en découle Figure 12 : Les voies de signalisation cellulaire induite par l IGF Figure 13 : Structure des différents récepteurs aux hormones stéroïdes Figure 14 : Structure d un récepteur à l œstrogène Figure 15 : Voie de signalisation par l œstradiol Figure 16 : Passage du récepteur inactif au récepteur actif grâce au dé ancrage des protéines Hsp Figure 17 : Activation dépendante par l hormone et indépendante par l EGF et MAP-Kinase Figure 18 : Conformations tridimensionnelle du récepteur à l œstradiol Figure 19 : Activation des récepteurs en présence du ligand dans le cas normale, activation independante dans la division cellulaire excessive Figure 20 : Mécanismes d activation des récepteurs des œstrogènes Figure 21 : Réponse primaire et secondaire induite par les récepteurs nucléaires Figure 22 : Passage d un Cancer Canalaire in situ au Stade d Evolution Infiltrante Figure 23 : Carcinome canalaire in situ. Coloration HE. Gr X Figure 24 : Carcinome lobulaire in situ coloration HE. Gr X Figure 25 : Evolution d un carcinome canalaire et métastases... 67
4 Figure 26 : Passage d un carcinome lobulaire in situ au stade d évolution de cancer invasif Figure 27 : Transformation de proto-oncogènes qui codent pour les protéines de cellules normales en oncogènes Figure 28 : Trois différentes voies de mutation d un proto-oncogène en oncogène Figure 29 : Représentation schématique du rôle des protéines p53 et prb, codées par les antioncogènes p53 et Rb, dans la régulation de croissance des cellules normales du sein Figure 30 : Classification en stade du cancer du sein Figure 31 : Images mammographiques cliché de face et de profil Figure 32 : Image échographique d une patiente atteinte d un cancer du sein Figure 33 : Conduite chirurgicales après dépistage mammographique pour femmes ménopausées et femmes jeunes Figure 34 : Structure biochimique du SERM Figure 35 : Action agoniste et antagoniste du SERM Figure 36 : L origine hormonale de pathologies bénignes Figure 37 : Facteurs favorisants l apparition d un cancer du sein Figure 38: Structure d un anticorps Figure 39: Anticorps monoclonaux, liaison à un épitope spécifique Figure 40 : Anticorps polyclonaux, liaison à des épitopes différents Figure 41 : Anticorps primaire conjugué à l anticorps secondaire Figure 42 : Mode d action de la peroxydase Figure 43 : Immunoperoxydase simple Figure 44 : Système biotine/streptavidine Figure 45 : Méthode immunoenzymatique de type streptavidine-biotine-peroxydase Figure 46 : Algorithme pour la sélection des patientes en France et dans la plupart des pays Figure 47 : Automate d'inclusion : Leica TP 1040» Figure 48 : Protocole d inclusion, de coupe et de collage des coupes Figure 49 : Protocole de coloration hémalun éosine Figure 50 : Répartition des carcinomes selon l âge des patientes Figure 51 : Pourcentage des patientes ménopausées et non ménopausées Figure 52 : Répartition des carcinomes selon la taille de la tumeur Figure 53 : Répartition des carcinomes selon l envahissement ganglionnaire
5 Figure 54 : Répartition des carcinomes selon le grade histopronostique de Scarff et Bloom SBR Figure 55 : Répartition des carcinomes selon le type histologique Figure 56 : Répartition selon le grade histopronostic de SBR des CCI Figure 57 : Répartition selon le grade histopronostique de SBR des CLI Figure 58 : Répartition selon le grade histopronostique de SBR des CCLI Figure 59 : Répartition selon le grade histopronostique de SBR des tumeurs phyllode Figure 60 : Valeurs de positivité et négativité des récepteurs hormonaux Figure 61 : Valeurs des récepteurs hormonaux pris individuellement Figure 62: Valeurs des récepteurs hormonaux pris individuellement Figure 63 : Pourcentage d expression de la protéine HER2 chez des femmes atteintes d un carcinome infiltrant
6 Tableau I : Classifications de densité et variations en fonction de l âge Tableau II : Propriétés notoires des hormones stéroïdes de mammifères Tableau III : Action hormonale sur la glande mammaire Tableau IV : Classification prise en considération pour le diagnostic Tableau V : Le grading histopronostique d Elston Ellis 1999 (Index de Nottingam) Tableau VI : Classification TNM des cancers mammaires Tableau VII : Relation entre la taille de la tumeur et la survie de 10 ans Tableau VIII : Réduction de rechute et de mortalité chez les femmes non ménopausées 116 Tableau IX : Cancer du sein métastatique : éléments aidant au choix du traitement Général Tableau X : Taux d incidence annuelle brute suivant l âge en France et en Europe pour habitants Tableau XI : Taux d incidence standardisés des cancers du sein pour en Algérie 121 Tableau XII : Taux d incidence standardisés des cancers du sein dans le monde pour habitants Tableau XIII : Répartition du cancer du sein par sexe à Sidi Bel Abbés (1998) Tableau XIV : Pourcentage des cancers mammaires selon l aspect morphologiques dans la wilaya de Sidi Bel Abbés (1998) Tableau XV : Répartition des cancers gynécologiques selon la localisation à Sidi Bel Abbés Tableau XVI : Caractéristiques des deux chromogènes de la peroxydase Tableau XVII : Protocole d inclusion des prélèvements de cancer du sein Tableau XVIII : Protocole de coloration Hémalun-éosine Tableau XIX : Techniques de démasquage d antigènes Tableau XX : Evaluation des récepteurs hormonaux Tableau XXI : Valeurs de positivité et de négativité pour chaque récepteur hormonal1. 76 Tableau XXII : Guide d interprétation des résultats immunohistochimiques Tableau XXIII : Valeurs de dosage de l HER2 dans les carcinomes mammaires Tableau XXIV : Valeurs de dosage de p53 pour les 24 cas de carcinomes mammaires
7 RESUME I. INTRODUCTION... 1 CHAPITRE I : ANATOMIE ET PHYSIOLOGIE DU SEIN 1. Anatomie de la glande mammaire Vascularisation de la glande mammaire Attaches et limites Histologie de la glande mammaire Involution et densité mammaire Biologie descriptive de la glande mammaire Fonctions physiologiques de la glande mammaire «l allaitement» Régulation hormonale et cycle sexuel de la femme Contrôle hormonale de la croissance canaliculaire mammaire Au cours du cycle menstruel Pendant la grossesse Pendant la lactation Ménopause Récepteurs hormonaux au niveau de la glande mammaire Récepteurs transmembranaires Récepteurs doués d activité de tyrosine kinase Récepteurs HER a. Fonction physiologique...28 b. Transduction du signal : les seconds messagers...31 b.1. Voie Ras/Raf/MEK/MAPK-ERK...31 b.2. Voie PI3K/PTEN/AKT/mTor...31 c. Altération des récepteurs de la famille HER2 dans le cancer du sein R-EGF (HER1) et sa signalisation Libération de facteurs de croissance transformants...35
8 Expression tumorale du REGF dans le cancer du sein Relation REGF et RE dans la cancer du sein Régulation par endocytose des récepteurs portés à la surface de la cellule Récepteurs intracellulaire «stéroïdiens» Structure générale des récepteurs nucléaires Récepteur à l œstradiol et voie de signalisation Transconformation des récepteurs d œstrogènes Dimérisation du récepteur Activation de la transcription dépendante des œstrogènes Activation ligand indépendante Activation ERE indépendante Activation non génomique Gènes induits Facteurs de transcriptions assujettis à des hormones liposolubles Récepteurs hormonaux en pathologie mammaire Etiologie hormonale du cancer du sein Facteurs hormonaux chez la femme avant et après ménopause Chez la femme ménopausée Rôle carcinogène des hormones sexuelles Autres hormones Prolactine Insuline, IGF CHAPITRE II : PATHOLOGIES MAMMAIRES ET LEURS CLASSIFICATIONS 1. Les maladies bénignes du sein Le cancer mammaire Le cancer in situ Carcinome non infiltrant, carcinome canalaire in situ (CCIS) CCIS de haut grade nucléaire...64
9 CCIS de bas grade nucléaire CCIS de grade intermédiaire Type mixte Carcinome non infiltrant, Carcinome lobulaire in situ (CLIS) Mode d extension des tumeurs malignes invasives Carcinome canalaire infiltrant (CCI)...69 Carcinome canalaire infiltrant avec composante intracanalaire prédominante Carcinome lobulaire infiltrant (CLI)...69 Carcinome mucineux...69 Carcinome médullaire (à stroma lymphoïde)...70 Carcinome papillaire...70 Carcinome tubuleux...70 Carcinome adénoïde kystique...70 Carcinome sécrétant (juvénile)...70 Carcinome apocrine...70 Carcinome métaplasique...70 Autres variétés (carcinome riche en lipides, carcinome à petites cellules, carcinome à cellules en bague à chaton, etc.) Maladie de Paget du mamelon Les tumeurs phyllode du sein Mécanismes de déclenchement tumorale Activation des signaux de croissance et des oncogènes Oncogènes et anti-oncogène Mécanismes d activation des oncogènes Anti-oncogènes ou gènes suppresseurs de tumeur Contrôle du cycle cellulaire par les gènes suppresseurs de tumeur P Mécanisme d action des anti-oncogènes Inhibition des signaux anti-prolifératifs Altérations des gènes suppresseurs de cancers...81
10 3.3. Contrôle génétique et rapport avec le cycle cellulaire : La famille bcl Aspect génétique des cancers mammaires Prédispositions héréditaires au cancer du sein : BRCA1 et BRCA Les altérations moléculaires constitutionnelles dans les cancers mammaires Anti-œstrogènes (Tamoxiféne) et mutations de BRCA1/BRCA Les formes héréditaires de cancer du sein liées à BRCA1 et BRCA2 sont elles sensibles aux œstrogènes? Œstrogéno-induction de BRCA Aspects biologiques de l implication de BRCA1 et 2 dans les cancers mammaires REα et BRCA BRCA1 et expression des RE : un lien paradoxal? Hétérogénéité phénotypique des cancers mammaires Conseil génétique Classifications des cancers mammaires Classification des lésions pré-invasives et des carcinomes in situ...89 Hyperplasie canalaire simple (HCS)...90 Hyperplasie canalaire atypique (HCA)...90 Carcinome canalaire in situ (CCIS) Classification de Tavassoli Classification selon le grade histologique (SBR = Scarff Bloom et Richardson) Classification TNM internationale Classification en stade...94 CHAPITRE III : DEPISTAGE ET TRAITEMENTS DES CANCERS MAMMAIRES 1. Méthodes de diagnostique Mammographie Echographie...100
11 1.3. Cytoponction Dépistage précoce des cancers mammaires et traitements Terminologie et principes généraux du dépistage Dépistage de la maladie et identification des personnes Dépistage des cancers : dépistage des lésions précancéreuses Efficacité du dépistage Différents types de dépistages Le dépistage individuel Le dépistage de masse Les recommandations actuelles pour le dépistage précoce du cancer du sein Traitement du cancer du sein Chirurgie Curage axillaire Ganglion sentinelle Radiothérapie Chimiothérapie Hormonothérapie Hormonothérapie du cancer du sein métastatique Pour les femmes non ménopausées a. Inhibiteurs de l aromatase (IA) b. Œstrogènes et SERM c. Le tamoxifène et le raloxifène Femmes ménopausées Anti-œstrogènes a. Inhibiteurs de l aromatase b. Progestatifs CHAPITRE IV : EPIDEMIOLOGIE ET FACTEURS DE RISQUES DES CANCERS MAMMAIRES 1. Epidémiologie du cancer du sein Epidémiologie descriptive mondiale...119
12 1.2. Epidémiologie du cancer du sein en Europe Epidémiologie du cancer du sein en Afrique Epidémiologie du cancer du sein en Algérie Comparaison nationale et internationale A l échelle nationale A l échelle internationale Données d incidence du cancer du sein dans la wilaya de Sidi Bel Abbés, Periode Les facteurs de risques du cancer du sein L âge Le Sexe Les femmes obèses L exposition à l hormone oestrogène endogène La pilule anticonceptionnelle L hormonothérapie post-ménopause Les rayons-x et la mammographie Prévention CHAPITRE V : IMMUNOHISTOCHIMIE ET CANCERS MAMMAIRES 1. L immnohistochimie, valeurs diagnostiques, et pronostiques Anticorps monoclonaux Anticorps polyclonaux Système PAP Système Biotine/Streptavidine Avantages de la technique de démasquage des antigènes Apport de l immunohistochimie dans les cancers mammaires Immunohistochimie diagnostique Immunohistochimie pronostique et prédictive Corrélation entre la FISH et l IHC L immunohistochimie en anatomie pathologique mammaire Applications pratiques...144
13 Apport de l immunohistochimie dans le diagnostic différentiel Les facteurs biologiques et moléculaires déterminés par l immunohistochimie Récepteurs hormonaux Règles techniques Règles d interprétations Rédaction du compte rendu L oncogène HER2 (HER2-neu ou c-erbb2 ou neu) Règles techniques Règles d interprétations HER2 et pronostic HER2 et prédiction de la réponse à la chimiothérapie La protéine p P53 et pronostic Les marqueurs de prolifération Valeur pronostique et prédictive du Ki Autres Facteurs influençant le pronostic La présence des récepteurs d œstrogènes et de progestérones Le matériel génétique des cellules Absence de diploïdie ADN Haut degré de multiplication «Phase S» Présence de certains «neu oncogènes» Présence de certains «Facteurs de croissance» CHAPITRE VI : MATERIEL ET METHODES 1. La population étudiée Méthodes Prise en charge d un prélèvement mammaire Examen macroscopique et prélèvements pour l'étude histologique Pièces d'exérèse d une tumeur palpable...151
14 Mastectomie Curage axillaire Préparation tissulaire Méthodes utilisées pour la technique immunohistochimique Préparation tissulaire Etape de la préparation des coupes incluses en paraffine pour l IHC Fixation Inclusion en paraffine Coupes au microtome Séchage des lames Déparaffinage et réhydratation Réalisation de la technique IHC standard Démasquage antigénique Avantages de la technique de démasquage des antigènes Blocage des peroxydases endogènes Application de l anticorps primaire Révélation Révélation aux chromogènes Contre coloration Montage et observation Lecture des lames Méthode de lecture des lames en immunohistochimie Protocole de détection des récepteurs hormonaux sur tissus inclus en paraffine-lsab2 - Démasquage micro-onde et bain-marie Préparation des anticorps Déparaffinage et réhydratation Démasquage antigénique à la chaleur Pour RE Pour RP Immunomarquage...163
15 Blocage des peroxydases endogènes Anticorps primaire Anticorps secondaire Chromogène Contre coloration Observation au microscope Protocole de détection de l HER2 sur tissus inclus en paraffine. Démasquage au bain-marie Protocole de marquage Lecture des lames Protocole de détection de l Actnine, EMA, Cytokératine, Vimentine, P Déparaffinage et réhydratation Démasquage antigénique à la chaleur Immunomarquage Blocage des peroxydases endogènes Anticorps primaire Anticorps secondaire Chromogène Contre coloration Observation au microscope CHAPITRE VII : RESULTATS ET DISCUSSION 1. Résultats de l étude histologique Le sexe L âge Le statut hormonal Le stade clinique selon la classification TNM Taille Envahissement ganglionnaire Le grade histopronostic Répartition selon le type histologique Pour les carcinome canalaire infiltrant CCI...173
16 Pour les Carcinome Lobulaire Infiltrant CLI Pour les carcinome canalaire et lobulaire infiltrant CCLI Pour les tumeurs phyllode Résultats de l étude immunohistochimique Etude immunohistochimique des récepteurs hormonaux (RH) Etude immunohistochimique de l oncogène HER2 et de l anti-oncogène P Interprétation de l étude histologique Interprétation de l étude immunohistochimique CONCLUSION... REFERENCES BIBLIOGRAPHIQUES... ANNEXE
17 Introduction REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET POPULAIRE MINISTERE DE L ENSEIGNEMENT SUPERIEUR ET DE LA RECHERCHE SCIENTIFIQUE UNIVERSITE DJILLALI LIABES FACULTE DES SCIENCES DEPARTEMENT DE BIOLOGIE MAGISTER DE BIOLOGIE CELLULAIRE OPTION : BIOLOGIE DE LA CELLULE NORMALE ET PATHOLOGIQUE «CAS DES CANCERS» Mémoire de Magister Soutenu par Mme Hammar K. devant le jury composé de : Président : Examinateur : Examinateur : Promoteur : Pr. Tou A Pr. Tadjeddine A Dr. Bendahmane M Pr. Moulessehoul S Année universitaire :
18 Introduction Annexe 1 Matériel utilisé Etuve Chambre humide complète Microscope optique Microtome de type Minot Four pour chauffer Réfrigérateur Micro-onde (750 Watt) Balance analytique Bacs et paniers pour solutions (en verre/en plastique) Portoir pour lames (en verre/en métal) Bain-marie Micropipettes Becher, lames dégraissées, et gélatinées, lamelles Tubes à hémolyse Ruban ph Cuves à coloration Pinces à lames et lamelles Pissette d'eau neutre Plateau émaillé ou inox Microscope hund WETZLAR muni d un appareil numérique type JVC (color video camera), acquisition vidéo. En plus du matériel précédemment décrit on a besoin d un graveur pour cercler les prélèvements ou d un stylo spécial Dako Cytomation «Dako Pen». 2
19 Introduction ANNEXE 2 Produits utilisés pour le protocole d inclusion dans de la paraffine Formol Alcool «éthanol» (100 ; 90 ; 80 ) Toluène ou xylène 1. Préparation du formol 1/10 ème Formol concentré 35% Eau distillée 10 ml 90 ml 2. Table de Gay-Lussac pour la dilution de l éthanol Alcool à Alcool à diluer obtenir ,25 11,83 10,43 9,07 7, ,50 5,15 3,83 2,53 1, ,59 27,01 25,47 23,95 22, ,58 35,90 34,28 32,67 31,08 C est la quantité d eau (ml) à ajouter à 100 ml d alcool à diluer. Automate d'inclusion : Leica TP
20 Introduction ANNEXE 3 1. Préparation de l eau albuminée Albumine 1g Eau distillée 100 ml Glycérine 100ml Filtrer et ajouter de salicylate de soude (1g) a. Distributeur de la paraffine Leica b. Inclusion des coupes c. Collage des cassettes sur les moules d. Obtention de ruban de coupe e. Collage des coupes à l albumine sur plaque chauffante Protocole d inclusion, de coupe et de collage des coupes. 4
21 Introduction ANNEXE 4 1. Produits utilisés pour la coloration Hématoxyline-Eosine standard Alcool «éthanol» (100 ; 95 ; 75 ) Toluène ou xylène Hématoxyline de Harris Eosine Eau acétifiée Carbonate de lithium à saturation 2. Mode de préparation de l Hématoxyline de Harris (coloration des noyaux). Hématoxyline 5 g Ethanol absolu 50 ml Alun de potassium 100 g Oxyde rouge de mercure 2,5 g Eau distillée 1 litre Dissoudre l hématoxyline dans l éthanol absolu (100 ) ; Dissoudre l alun de potassium dans l eau distillée en chauffant légèrement et retirer du feu ; Mélanger les deux solutions, puis faire bouillir le mélange ; Retirer le mélange du feu et ajouter avec précaution par petites quantités l oxyde de mercure ; Chauffer de nouveau jusqu à ce que la solution acquière une couleur pourpre foncée ; Retirer immédiatement du feu et refroidir aussitôt dans un récipient rempli d eau ; Filtrer ; Ajouter avant chaque usage 2 à 4% d acide acétique glacial (100%) pour augmenter la précision de la coloration nucléaire. 5
22 Introduction 3. Mode de préparation de l éosine alcoolique 1% (coloration du cytoplasme) Eosine Alcool 90 1 g 100 ml 4. Mode de préparation du carbonate de lithium à saturation Carbonate de lithium Eau distillée 1,2 g 100 ml 5. Mode de préparation de l eau chlorhydrique (eau acétifiée) Acide chlorhydrique à 37% Eau distillée 1 ml 300 ml a. Automate de coloration - Leica AUTOSTAINER XL. b. Coloration c. Montage et collage des lames. Protocole de coloration hémalun-éosine. 6
23 Introduction Produit utilisés et mode de préparation des réactifs pour l immunohistochimie Toluène ou xylène Alcools (100 ; 90 ) Eau distillée Tampon PBS : prêt à l emplois ou fabriqué au laboratoire Eau oxygénée à 3% Panel d anticorps primaire Kit de révélation LSAB 2 HRP deux flacons, un pour l anticorps secondaire biotinylé, et le second pour le complexe streptavidine-biotine-peroxydase Chromogène AEC et DAB Kit HercepTest Dako Cytomation Milieu de montage aqueux spéciale immunohistochimie prêt à l emploi Hématoxyline de Mayer s fabriqué au laboratoire 1. Fixateur AFA (Alcool, Formol et acide acétique) Ethanol 100 Formol Acide acétique 60 ml 30 ml 10 ml 2. Adhésifs Pour une meilleur adhésion des coupes sur les lames, et suite à plusieurs essais, on a choisit la technique d Alun de Chrome-Gélatine (CrK (SO4)2, 12H2O) qui à donner les meilleurs résultats d adhésion : Dissoudre 3g de gélatine dans un litre d eau distillée à 60 C ; Mélange et chauffage jusqu à totale dissolution ; Ajouter 0,5g d alun de chrome ( sulfate de chrome et de potasium) ; Laisser chauffer pendant 30 minutes jusqu'à obtention de couleur verte ; Filtrer la préparation obtenue et maintenir à chaud ; Plonger les lames dans un bêcher contenant ¾ de la préparation ; 7
24 Introduction Egoutter les lames sur papier absorbant puis les sécher à l étuve. On peut conserver les lames gélatinées dans une boite fermée. 3. Tampon Solution phosphate Buffered Saline (PBS): NaCl KCl Na2HPO4 KH2PO4 20 g 0,5 g 4,0 g 0,5 g Nous avons utilisé au début des sachets contenant le PBS en poudre commercialisé par Dako Cytomation à dilué dans 500 ml d eau distillée, à ph 7.6. L eau oxygénée H2O2 Préparation d une eau oxygénée à 3% Pour celle de 30V on prend 7 ml pour 100 ml d eau distillée Nous disposons dans le laboratoire d une eau oxygénée de 10V, on prend 2.5 ml pour 100 ml d eau distillée. Solutions de restauration antigénique Tampon citrate ph6 Solution A : Citrate de sodium (C6 H5 Na3 O7 2H2O) 14,7g Eau distillée (QSP) Solution B : 500 ml Acide citrique monohydrate (C6H8O7 H2O) 10,5g Eau distillée (QSP) 500 ml Solution de travail : 41 ml de la solution A + 9 ml de la solution B et compléter jusqu à 500 ml par l eau distillée. TRS Target Rretrieval Solution 500 ml concentré x 10 On prend 25 ml de TRS dans 200 ml d eau distillée 8
25 Introduction Chromogène Les solution chromogène AEC Substrate-Chromogène ainsi que DAB, utilisées sont prêtes à l emplois, mais il est possible de les préparer à l abri de la lumière et en prenant toutes les précautions nécessaires lorsque l on manipule le produit carcinogène, DAB peut être sous forme de tablettes à dissoudre sinon flacon prêt à l emplois valable pour 150 tests, à raison de 15 ml par test, il est préférable d utiliser des chromogènes prêt à l emplois. Colorant Le colorant utilisé est l hématoxyline de Mayer s pour l IHC qui ne contient pas d alcool, spécialement adaptée à l AEC commercialisé sous forme de flacons prêts à l emplois. Préparation de l Hémalun de Mayer s : Hématoxyline 1 g Eau 1000 ml Dissoudre à chaud Refroidir Iodate de Na 0,2 g Alun de K 50 g Dissoudre Hydrate de Chloral 50 g Acide citrique 1 g Dissoudre Conserver bouché. Etape de la préparation des coupes incluses en paraffine Fixation Inclusion en paraffine Réalisation des coupes Séchage Réalisation de la coloration HE pour l étude histologique mammaire 9
26 Introduction Collage et séchage des lames Le collage se fait par chauffage de la lame sur une platine chauffante. 10 min sur une platine à 55 Égouttage de la lame (voir illustration) 10 min sur une platine à 65 Préparation des réactifs pour l immonohistochimie Préparation des anticorps Diluer le RE au 1/40 ème et le RP au 1/50 ème si on dispose d anticorps concentrés, si ces derniers sont prédilués on peut les utiliser directement. Chromogène DAB ou AEC 1ml du tampon de dilution (diluent) dans un tube calibré ajouter une goutte de DAB ou d AEC le réactif peut être utilisé immédiatement, stabilité 5 jours à 4 C Préparation du PBS Si le PBS est fourni sous forme de poudre conditionnée en sachets, diluer le contenu dans 1L d eau distillée, bien agiter. Préparation des réactifs à partir du kit HercepTest 1. Epitope retrieval solution : Diluer 1ml du flacon N 7 dans 10 ml d eau distillée, pour remplir le bac et faire en sorte que les lames soient entièrement trempées, on prépare 25 ml du flacon N 7 dans 250 ml d eau distillée, cette solution est préparée pour la restauration antigénique à la chaleur. 2. Tampon de lavage : Diluer 1ml du flacon N 8 dans 10 ml d eau distillée, pour remplir le bac et faire en sorte que les lames soient entièrement trempées, on prépare 25 ml du flacon N 8 dans 250 ml d eau distillée., ce ci est notre tampon de rinçage. 10
27 Introduction 3. Substrate-Chromogène Solution DAB Etape 1 : Transférer 1ml du flacon N 5 dans un tube à essai Etape 2 : Ajouter une goutte de chromogène DAB du flacon N 6, mélanger et appliquer. 11
28 Introduction Coloration cytoplasmique (éosine) Coloration nucléaire (hémalun) 1 cm Planche I : Etude histologique (standard : HE) d un carcinome canalaire infiltrant. Gr x
29 Introduction A B 0 C D Marquage nucléaire Coloration à l hémalun de Meyer s 1 cm 0,5 cm Planche II : Immunohistochimie des récepteurs à l œstrogène (RE) et progestérone (RP) : Fig. a et b : Fig. c et d : RE+/RP+, d une patiente atteinte d un carcinome mammaire infiltrant mixte. Gr x 100. RE-/RP+, d une patiente atteinte d un carcinome canalaire infiltrant GII. Gr. x
30 Introduction Marquage membranaire Coloration nucléaire à hémalun de Mayer s 1 cm Planche III: Immunohistochimie de l HER2 (marquage membranaire) d un carcinome canalaire infiltrant de grade III. Gr x
31 Introduction Marquage nucléaire Coloration à l hémalun de Meyer s 0,5 cm Planche IV : Etude immunohistochimique de la protéine p53 d un carcinome canalaire infiltrant. Gr x
32 Introduction Marquage cytoplasmique Coloration à l hémalun de Meyer s 1 cm 0,5 cm Planche V : Immunohistochimie de l actine Fig. a : Actine+, patiente atteinte d un Carcinome Canalaire Infiltrant, grade II. Gr x 40. Fig. b : Actine+, patiente atteinte d un Carcinome Canalaire Infiltrant, grade III. Gr x
33 Introduction a b c d Coloration à l hémalun de Meyer s a et d : Marquage cytoplasmique / c : Membranaire 1 cm 0,5 cm Planche VI : Immunohistochimie de la Vimentine, EMA et Cytokératine : Fig. a et b : Vim+, d une patiente atteinte d une tumeur phyllode, grade II. Gr x 40. Fig. c et d : EMA+/Cytk+, d une patiente atteinte d un Carcinome Canalaire Infiltrant grade II. Gr x
34 Introduction Introduction Le cancer du sein est le premier cancer de la femme, estimé à 1.05 million de nouveaux cas en l an 2000 en Europe (Parkin et al., 2003). En Afrique, le cancer du sein est relativement moins courant, estimé à nouveaux cas par an, soit 18% des cancers de la femme (Parkin et al., 2003). Le cancer du sein est une prolifération de cellules anormales qui aboutira à la formation d une masse ou tumeur maligne. Les cellules cancéreuses ont acquis une certaine indépendance face aux signaux extérieurs, beaucoup d études accusent l effet promoteur des hormones «œstrogènes et progestérones» dans le développement tumoral, ces hormones agissent par le biais des récepteurs nucléaires (Sigal-Zafran et al., 2004). Les cancers mammaires sont très certainement la localisation tumorale qui a fait l objet de la plus large exploration de l expression des Récepteurs Hormonaux, mais aussi de l HER2 «Human Epithelial Receptor» (exprimés dans 15 à 25% des cancers du sein selon le stade), dont l amplification génique conduit à leur surexpression à la surface de la cellule et, par conséquent, à une augmentation de la division cellulaire. Le diagnostic anatomopathologique des tumeurs a longtemps reposé sur la seule analyse morphologique des lésions en technique standard, l application il y a une vingtaine d années de l immunohistochimie dans l arsenal diagnostic, à rendu possible l étiquetage précis d un grand nombre de tumeurs malignes indifférenciées (Bailly, 1992). Les implications de l'immunohistochimie au pronostic des tumeurs et à la prédiction d'une réponse à la thérapeutique commencent à se développer, en particulier dans le cadre de la détection de récepteurs hormonaux et de la mise en évidence de la surexpression de HER2/neu dans les cancers du sein (Gerard et Torpora, 1995). L étude immunohistochimique des récepteurs hormonaux d une tumeur mammaire détermine son hormonosensibilité, il existe une grande disparité de réponse à l hormonothérapie selon que les tumeurs soient riches ou non en 18
35 Introduction récepteurs hormonaux, le taux de réponse ne dépasse pas 10% s ils sont absents, mais en cas de RH+, il s élève en relation linéaire avec le taux de récepteurs, allant jusqu à 80% de réponse. Les carcinomes qui surexpriment l HER2 sont de mauvais pronostic, cette surexpression est caractérisée par l absence des récepteurs hormonaux, qui eux par contre sont de bon pronostic. Les objectifs assignés à ce travail sont de doser les récepteurs hormonaux sur des préparations tissulaires de 39 carcinomes mammaires, inclus dans de la paraffine, et de rechercher une éventuelle surexpression de la protéine HER2 par la technique d immunohistochimie. Notre but consiste à révéler sur coupe histologique, par réaction antigène-anticorps, la présence de récepteurs antigéniques cellulaires intranucléaires, membranaires ou cytoplasmiques. Nous avons utilisé des marqueurs de révélation d antigènes dans la cellule mammaire, afin d étudier les différents types de marquage nucléaire (RE, RP, P53), membranaire (EMA, HER2), et cytoplasmique (vimentine, cytokératine et actine). Le degré d implications de l'immunohistochimie réside dans la prédiction d'une réponse à la thérapeutique hormonale en cas de récepteurs hormonaux positifs. Le dosage de l HER2 mesure le degré de la chimiorésistance des cancers mammaires, la surexpression de cette protéine est révélatrice de l agressivité de la tumeur. On peut aussi confirmer le diagnostic histologique par le biais de marqueurs qui détectent la surexpression de certaines particules spécifiques aux sarcomes ou aux carcinomes et établir le diagnostic différentiel entre les deux grâce à l immunohistochimie. Ceci nous a permis aussi l appréciation de différents types de marquages ; nucléaires (RH), membranaire (HER2, EMA), et cytoplasmique (Actine, Cytokératine, Vimentine), et l établissement de valeur seuil. 19
36 Chapitre I Description de la glande mammaire Du latin «sinus», pli, le sein est l appellation réservée dans l espèce humaine pour les deux mamelles de la femme, glandes mammaires caractéristiques de la classe des mammifères. Un réseau de canaux galactophores est présent à l état rudimentaire chez les individus des deux sexes, de l âge embryonnaire à l âge adulte, mais seules les femmes, sous l influence hormonale à la puberté, le long des cycles et pendant la grossesse et l allaitement, développent la partie glandulaire. Les seins sont atrophiés chez l individu mâle, sauf modification hormonale. Il contiennent les glandes lactogènes dont les sécrétions ont lieu essentiellement pendant la période de lactation de la mère après l accouchement, et qui débouchent par des canaux séparés au niveau du mamelon, l essentiel du corps du sein étant constitué de tissus adipeux. Les seins voient leur volume varier en fonction de différents paramètres tels que le cycle d ovulation, ou la grossesse. La limite de l aréole, sa pigmentation et son réseau glandulaire varient avec la grossesse et l allaitement (Arao et Debrux, 1979). 1. Anatomie de la glande mammaire Les tissus mammaires ne comprennent pas seulement le sein, mais aussi la partie du corps comprise entre la clavicule, l aisselle et la lame du sternum. Les muscles de la poitrine et de l épaule sont situés derrière les tissus mammaires. Chaque sein est constitué d un tissu graisseux plus ou moins important qui lui donne sa forme et dans lequel se trouve la glande mammaire (Arao et Debrux, 1979). Le tissu adipeux protége les canaux et les lobules. Le tiers du tissu mammaire se compose de graisse et de tissu conjonctif et les 2/3 se composent de canaux et de lobules. La glande mammaire est entourée par un fascia périphérique, l un superficiel (glande-peau), l autre profond (glande-muscle). Le premier est constitué d un tissu conjonctif très fin et très délicat, dont les coupes histologiques montrent qu ils s adaptent aux crêtes dermiques. Les ligaments de Cooper (fig. 1) (Goumont et al., 1993), faits de prolongements fibreux, constituent des indentations qui maintiennent une connexion étroite entre la face profonde du derme et la glande en y pénétrant au 20
37 Chapitre I Description de la glande mammaire niveau des saillies glandulaires : les crêtes fibro-glandulaires de Duret. La couche profonde du fascia mammaire est séparée du fascia du grand pectoral par un tissu lâche permettant la mobilisation de la glande sur le thorax et qui permet sa dissection. Une coupe parasagittale passant par le mamelon laisse entrevoir deux grands compartiments : l enveloppe cutanéo-graisseuse et le tissu conjonctivoglandulaire avec pour unité élémentaire le lobule mammaire qui s abouche sur un canal secondaire lobulaire (Goumont et al., 1993). Figure 1 : Coupe au niveau de la glande mammaire (Goumont et al., 1993). Sur le plan superficiel, le sein est recouvert de peau (Fascia superficialis) s étendant sans limite nette jusqu à la région mamelonaire, arrondie et pigmentée. Il n existe pas de plan de clivage entre la glande et la peau, ni de loge mammaire. En effet, le tissu est uni au derme par les ligaments de Cooper. Ces ligaments sont des amarres conjonctives et vasculo-nerveuses, suspendant la glande au plan cutané. Les rapports intimes entre le derme et la glande expliquent la difficulté à réaliser des mastectomies sous-cutanées totales (risque de dévascularisation en retirant l ensemble des crêtes). En périphérie, il n existe pas de ligne de réflexion nette entre le fascia pré et rétroglandulaire. Le tissu mammaire s amincit sur les côtés, progressivement et irrégulièrement. 21
38 Chapitre I Description de la glande mammaire Sur le Plan profond, le fascia rétromammaire est, contrairement au fascia prémammaire, bien individualisable et repose sur l aponévrose du muscle grand pectoral (Arao et Debrux, 1979). Le tissu cellulo-adipeux rétromammaire est une couche de tissu fibro-adipeux, encore appelée bourse séreuse rétromammaire de «Chassaignac», est développée en arrière du fascia rétromammaire, se continue en haut avec le fascia superficialis. Elle permet le glissement normal de la glande sur les plans musculaires sous-jacents, glissement qui disparaît en cas d envahissement des plans musculaires au cours des cancers du sein. Les tubulo-alvéoles de la glande mammaire au repos sont constituées de cellules disposées sur deux couches : sécrétrices, au contact de la lumière et myoépithéliales, au pourtour. L unité terminale ductulobulaire ou UTDL (Balynsky, 1979), est située à la fin des ramifications, après le galactophore de petit calibre, cette unité comprend le canalicule extra lobulaire et le canalicule intralobulaire). 22
39 Chapitre I Description de la glande mammaire Le mamelon comprend : La plaque aréolaire et Le mamelon proprement dit. Le mamelon est la partie centrale et surélevée de l aréole. Les canaux galactophores qui assurent l évacuation des sécrétions lactées y débouchent par des pores séparés (Arao et Debrux, 1979). Il y a différentes formes de mamelon ; normal, bref, et ombiliqué. La peau de l aréole a un aspect grenu car elle et parsemée de glandes cutanées et sébacées (Glande de Morgagni) qui s hypertrophient à la grossesse et prennent alors le nom de tubercule de Montgomery. L aréole est pourvue de fibres musculaires lisses, muscles sphinctériens péri-alvéolaires, qui contrôlent la fonction excrétrice du sein au moment de la lactation Vascularisation de la glande mammaire Le sein est richement vascularisé. Les parties non glandulaires sont constituées de tissu adipeux. La partie interne du sein est vascularisée par des branches profondes de l artère thoracique interne (Milerom et Martin, 1980). Les parties externes et inférieures reçoivent des branches de l artère thoracique externe, de l artère thoraco-acromiale et de l artère thoracique suprême. Le tissu cellulaire et la peau sont irrigués par le même dispositif artériel car la glande et la peau ont la même origine embryologique. Il existe un réseau anastomotique artériel très riche dans la glande mammaire (Milerom et Martin, 1980). L étude des veines est importante non seulement parce qu elles sont parallèles aux lymphatiques et parce que les métastases se font en suivant leur trajet. Trois groupes de veines profondes drainent la glande mammaire : les branches perforantes de la veine mammaire interne qui s abouche directement au réseau capillaire pulmonaire ; la veine axillaire naît de nombreuses veines en provenance de la face profonde du sein, ce trajet veineux à partir du sein conduit directement au réseau capillaire du poumon ; les veines intercostales, les plus importantes, communiquent avec les veines vertébrales et se jettent dans l azygos pour aboutir à la veine cave supérieur des poumons. 23
40 Chapitre I Description de la glande mammaire Au niveau du système lymphatique, le sein est divisé en 4 cadrans et 2 externes, 2 internes. Les cadrans externes sont drainés vers l artère thoracique externe, le creux axillaire (ganglion de Sorgius) et le ganglion sus-claviculaire. Les cadrans internes sont drainés sous le sternum par le ganglion intrathoracique puis le relais sus-claviculaire (fig. 2) (Ahren et Debrux, 1979). Figure 2 : Réseau lymphatique de la glande mammaire (Ahren et Debrux, 1977). 24
41 Chapitre I Description de la glande mammaire Selon le siège des ganglions axillaires, on distingue plusieurs chaînes : les ganglions mammaires externes : ils siégent au dessous du bord latéral du grand pectoral, au milieu du creux axillaire, suivant ainsi le cours de l artère thoracique latérale ; les ganglions mammaires internes : ils sont de petite taille entre 2 à 5 mm de diamètre. Ils suivent le trajet des vaisseaux mammaires internes, au sein d un tissu conjonctivo-graisseux (Balynsky, 1979). Les lymphatiques du sein doivent être divisés en lymphatiques cutanés drainant la lymphe de la peau mammaire et de la graisse sous-cutanée, et les lymphatiques de la glande elle-même (Ahren et Debrux, 1979). Les tissus mammaires baignent dans des liquides lymphatiques, qui permettent d éliminer les déchets, les cellules mortes et autres débris. Il y a environ 35 ganglions lymphatiques autour de chaque sein, dont la plupart sont situés dans le creux de l aisselle ou à proximité. Si un cancer se développe dans un sein, il s étend souvent aux ganglions car la lymphe peut contenir et faire circuler des débris mais aussi des cellules cancéreuses Attaches et limites Le sein est soutenu par la peau et un ligament suspenseur, la travée fibroglandulaire. Au niveau inférieur, le sillon sous-mammaire est formé par un épaississement de ces travées qui tire la peau en profondeur. La limite supérieure d implantation du sein se situe à la 2 ou 3 ème côte, sa limite inférieure entre la 6 ème ou la 7 ème côte (Arao et Debrux, 1979). 2. Histologie de la glande mammaire Le sein est une glande sudoripare modifiée qui assurent la production du lait. Située au-dessus des muscles grands pectoraux et grand dentelé, elle est reliée à ceux-ci par une couche de tissu conjonctif. Le système canalaire constitue la composante fonctionnelle de la glande mammaire (fig. 3) (Pujol et al., 2004). Le tissu fibro-adipeux entourant les canaux représente cependant la majeure partie du sein. Exception faite du court segment des canaux collecteurs qui s abouche à la peau au 25
42 Chapitre I Description de la glande mammaire niveau du mamelon et qui est bordé par un revêtement de type Malpighien, le système canalaire dans son ensemble est bordé par deux couches cellulaires : une couche interne de cellules épithéliales entourée par une couche externe discontinue de cellules myoépithéliales (fig. 4) (Barchielli et al., 1999). Ces deux couches cellulaires sont délimitées par une membrane basale, elle-même cernée en périphérie par quelques fibroblastes. Dans les canaux terminaux et les acini, les cellules épithéliales sont cubiques et les cellules myoépithéliales bien visibles, à cytoplasme clair (Milerom et Martin, 1980). A l intérieur de chaque glande mammaire, comprend de 15 à 20 lobes ou compartiments séparés par un tissu adipeux. Disposées en grappe, les alvéoles emmènent le lait (quand il est produit) dans une série de tubules secondaires. De là, le lait passe dans des canaux mammaires, près du mamelon, ces canaux s élargissent pour former des sinus lactifères, où le lait peut être entreposer, les sinus se continuent sous forme de canaux lactifères qui prennent fin au mamelon (Tortora et al., 1995). Les lobes et lobules ont une architecture schématiquement superposable à celle des autres glandes exocrines composées. On y trouve un système ramifié de canaux excréteurs terminés par des portions sécrétrices tubulo-alvéolaires. Chaque glande mammaire est constituée de lobes drainés par des canaux galactophores collecteurs «lactifères» s ouvrant individuellement à la peau au niveau du mamelon. Chaque lobe est lui-même constitué de lobules, chaque lobule étant constitué de tubulo-alvéoles correspondant à la partie sécrétrice de la glande. Les lobules sont entourés par du tissu conjonctif dense alors que le tissu conjonctif intralobulaire (tissu conjonctif palléal) est lâche (Ahren et Debrux, 1979). Les canaux galactophores excréteurs (ou canaux galactophores) sont d abord intralobulaires, puis interlobulaires (épithélium cubique avec présence de cellules myoépithéliales) et enfin inter lobaires à épithélium pavimenteux stratifié. 26
43 Chapitre I Description de la glande mammaire Figure 3 : Lobes et Lobule mammaires (Pujol et al., 2004). M A B Figure 4 : Coupe histologique pour identifier les cellules myoépithéliales (M) autour des alvéoles (A) et les vaisseaux sanguins (B) (Barchielli et al., 1999). 27
44 Chapitre I Description de la glande mammaire Le sein est composé de deux composantes : une composante adipeuse radiotransparente ; une composante fibroglandulaire radio-opaque. Le rapport entre le volume de la composante fibroglandualire et le volume de la composante graisseuse dépend de : l âge de la femme : l involution du sein commence à partir de l âge de 30 à 35 ans, cette involution est caractérisée par le remplacement progressif de la composante fibroglandulaire par du tissu adipeux ; en cas de surcharge pondérale, la composante adipeuse peut être accrue (Ahren et Debrux, 1979). 3. Involution et densité mammaire Le déclin des fonctions ovariennes à la ménopause, provoque une régression des structures de la glande mammaire ; les canaux galactophores sont maintenus, mais les alvéoles restantes ainsi que les lobules continuent de régresser avec l âge. (Berrie, 2001). L atrophie glandulaire du sein est la conséquence de l involution lobulaire avec atrophie de l épithélium, rétrécissement de la lumière canaliculaire, épaississement de la membrane basale et fibrose hyaline ou kystique, microscopique du tissu palléal. La densité des seins en mammographie est directement corrélée au pourcentage de la composante radio-opaque, fibro-glandulaire, et aux phénomènes liés au cycle hormonal menstruel : tels que les épisodes congestives, et la surcharge hydrique du parenchyme mammaire atteint ou non de dystrophie fibro-kystique (Rhodes et al., 2000). Ces phénomènes sont habituellement à l origine de la tension mammaire et de la mastodynie rencontrées au cours des cycles menstruels et chez certaines femmes sous traitement hormonal substitutif (THS). Le tableau 1 précise le type de densité en fonction de la description mammographique et sa prédominance selon l âge des patientes (Gerard et Torpora, 1995). 28
45 Chapitre I Description de la glande mammaire Densité des seins Les quatre types morphologiques Variations des taux des types mammographiques des seins selon Breast Imaging Reporting and Data morphologiques mammographiques des seins à 50 ans et 67 ans, calculés par System de l American College of Gairard et col (1993) dans une cohorte Radiology de femmes Description Type 50 ans 67 ans Le sein est presque entièrement graisseux. 1 14,5% 28% Il y a des opacités fibroglandulaires dispersées. 2 43% 54% Le tissu mammaire est dense et hétérogène. 3 38% 16% Le tissu mammaire est extrêmement dense. 4 5,6% 1,2% Tableau 1 : Classification de densité et variations en fonction de l âge (Gerard et Torpora, 1995). Le classement (très subjectif) des seins en quatre catégories d après le pourcentage des tissus denses : Catégorie I : moins de 10 % ; Catégorie II : de 10 à 49% ; Catégorie III : de 50 à 89% ; Catégorie IV : de égale ou supérieur à 90% (Ahren et Debrux, 1979). 4. Biologie descriptive de la glande mammaire 4.1. Fonctions physiologiques de la glande mammaire «l allaitement» L évolution des seins est le premier signe de puberté féminine avec un volume variable selon les femmes. La glande mammaire devient active en période d allaitement et produit le lait maternel, spécifique à l espèce humaine et adapté à 29
46 Chapitre I Description de la glande mammaire l alimentation du bébé pendant les premiers mois de la vie (Arao et Debrux, 1979). Le développement de cette glande dépend de trois facteurs interdépendants : l âge, la composition du tissu mammaire et l environnement hormonal. L organogenèse du sein est un phénomène tardif puisque l essentiel de la croissance mammaire se fait après la puberté et qu elle ne se termine qu au cours de la première grossesse menée à terme. Les fonctions essentielles des glandes mammaires sont la synthèse, la sécrétion et l éjection du lait : ces trois phénomènes constituent la lactation. La sécrétion du lait est due en grande partie à la prolactine, et dans une moindre mesure, à la progestérone et œstrogène. Les tissus mammaires subissent des changements au cours de la vie : les canaux galactophores sont prédominants chez les adolescentes, mais sont remplacés par de tissu adipeux chez les femmes plus âgées (Tortora et al., 1995). L ocytocine est une hormone libérée par le lobe postérieur de l hypophyse. Le rôle de cette hormone n est pas entièrement élucidé, mais concerne la mise en route du travail et la rétraction de l utérus à sa taille antérieure après l accouchement. Elle joue également un rôle important dans l induction de la sécrétion du lait par le sein au cours de l allaitement (c est-à-dire qu elle entraîne l éjection du lait du sein). La prolactine est libérée par le lobe antérieur de l hypophyse. Elle est étroitement liée au contrôle de la reproduction. Chez la femme, la prolactine stimule la sécrétion du lait maternel. Lorsqu elle est présente en grande quantité, elle inhibe également l ovulation et le cycle menstruel. Le sein de la femme est composé de 15 à 20 lobes convergeant vers le mamelon et contenant des grappes de glandes qui produisent le lait. Le lait de chaque grappe s écoule dans son propre conduit, le canal galactophore, et chaque conduit mène à un petit réservoir situé près du mamelon, avant de rejoindre celui-ci. Au bout du mamelon se trouvent donc 15 à 20 pores minuscules par lesquels s écoule le lait. Au cours de la grossesse, les tubulo-alvéoles de la glande mammaire se développent et sécrètent le colostrum. Pendant la première moitié de la grossesse, sous l influence des stéroïdes sexuels et tout particulièrement de la progestérone, les ramifications terminales du système canaliculaire prolifèrent et de très nombreux tubulo-alvéoles glandulaires se développent. Dès les premiers mois de la grossesse, sous l influence de la sécrétion de prolactine, les cellules glandulaires des tubuloalvéoles commencent à sécréter un produit riche en protéines et pauvre en lipides : le colostrum. 30
47 Chapitre I Description de la glande mammaire Après la ménopause, il se produit une involution progressive du système canaliculaire et des tubulo-alvéoles restants. Le tissu conjonctif devient plus dense et homogène, l épithélium s atrophie et une dilatation kystique des canaux persistants survient fréquemment (Trofani et Contesso, 1986). Le développement des seins est un des signes de la puberté chez la jeune fille. Ce développement s effectue grâce à l action de nombreuses hormones. Ce sont les œstrogènes, la progestérone et les hormones hypophysaires (hormone folliculostimulante ou FSH, hormone lutéinisante et prolactine). Pendant le cycle menstruel, la glande mammaire subit des modifications et notamment augmente de volume sous l effet des œstrogènes (2 semaines après le dernier jour des menstrues environ). Au moment de la ménopause, suite à une diminution de la fabrication hormonale (œstrogènes), le volume des seins diminue Régulation hormonale et cycle sexuel de la femme Les hormones sont des substance secrétées par des glandes endocrine libérées dans la circulation sanguine liées le plus souvent à une protéine qui régule leur actions, elles se fixent ensuite sur des récepteurs portés par les organes cibles, la production des hormones est elle-même stimulée ou freinée par un processus régulateur dit de rétrocontrôle. Les stéroïdes hormonaux sont des dérivés du cholestérol, secrétés par les ovaires ou les testicules, les stéroïdes ovariens sont les œstrogènes et progestérones et à un moindre degré les androgènes (hormones sexuelles mâles secrétées par les testicules et peu par les ovaires) (Gerard et Torpora, 1995). Toutes les hormones stéroïdes partagent la même structure à quatre noyaux, elles sont synthétisées sur le réticulum endoplasmique lisse. Toutefois, la forme de chaque hormone stéroïde diffère légèrement, cette légère différence dans les groupements permet une surprenante gamme de fonctions. On peut aussi classer les hormones en fonction de leur solubilité et selon l emplacement de leurs récepteurs, en trois grandes catégories : petites molécules lipophiles qui diffusent à travers une membrane plasmique pour atteindre des récepteurs intracellulaires ; molécules hydrophiles ; 31
48 Chapitre I Description de la glande mammaire molécules lipophiles qui se fixent à des récepteurs occupant la surface cellulaire (Barritt, 1992). La première catégorie correspond aux hormones liposolubles qui diffusent à travers la membrane plasmique et trouvent leur récepteur dans le cytosol ou dans le noyau. Le complexe récepteur-hormone s attache aux régions qui régissent la transcription de l ADN, pour moduler l expression de certains gènes, aux hormones de ce type appartiennent les stéroïdes, synthétisées à partir du cholestérol, elles possèdent un squelette chimique commun. Après avoir franchi la membrane plasmique, les stéroïdes s associent à leurs récepteurs protéiques intracellulaires pour former des complexes qui accélèrent ou freinent la transcription de gènes déterminés, en outre les complexes récepteurs-hormones sont capables de modifier sélectivement la stabilité de certains ARNm. L action des stéroïdes se prolonge pendant des heures ou des jours et influence souvent la croissance et la différenciation de tissus particuliers. Les particularités de ces hormones sont résumées dans le Tableau 2 (Smith et al., 1983). Le cycle menstruel et la menstruation sont sous la dépendance des hormones stéroïdes ovariennes, en effet la castration entraîne la disparition de toutes les manifestations du cycle. Les œstrogènes ce sont essentiellement le 17 bêta œstradiol, secrété par les cellules de la thèque interne du follicule ovarien puis en partie par le corps jaune, leur sécrétion, faible au début du cycle, augmente rapidement, avec un maximum avant l ovulation, puis décroît après l ovulation ; elle présente en phase lutéale un second maximum plus modéré, puis chute deux jours avant les menstrues, leur transport plasmatique se fait en partie sous forme libre et active, mais surtout sous forme liée à la binding globuline (Lopes et Pousset, 1989). La progestérone est sécrétée par le corps jaune ovarien, formé après l ovulation par vascularisation et lutéinisation des cellules de la granulosa, elle est absente en phase folliculaire, et sécrétée dans toute la deuxième partie du cycle, son taux s effondre en période prémenstruelle, son transport plasmatique est en partie libre et actif, en partie lié aux protéines. L activité des progestérones nécessite l imprégnation œstrogénique préalable, et aboutit aux modifications, permettant la nidation ovulatoire (Lopes et Pousset, 1989). 32
49 Chapitre I Description de la glande mammaire Caractéristiques Rétrocontrôle sur leur synthèse Mise en réserve de l hormone préformée Mécanisme de sécrétion Protéines plasmatiques de transport Survie dans le plasma Durée d action Récepteurs Stéroïdes oui Très réduite Diffusion à travers la membrane Oui Heures Heures à jours Cytosol ou noyau Commande de la transcription et de Mécanisme d action stabilité des ARNm par le complexe récepteur-hormone Tableau 2 : Propriétés notoires des hormones stéroïdes de mammifères (Smith et al., 1983). L hypothalamus contrôle la sécrétion des hormones gonadotropes hypophysaire par l intermédiaire d un facteur unique de régulation qui secrète une neuro-hormone, la GnRH (Gonadotrophin Releasing Hormone) (Gerard et Torpora, 1995). L hypophyse a un rôle de contrôle, la GnRH stimule la secrétions de deux hormones par les cellules endocrines gonadotropes de l adénohypophyse : la FSH (Folliculo Stimulating Hormone) et la LH (Luteinizing Hormone). FSH et LH sont véhiculées dans l ensemble de l organisme par la circulation sanguine. Elles stimulent les cellules endocrines de l ovaire. Ces cellules ovariennes secrètent deux types d hormones : les œstrogènes (dont l œstradiol), et la progestérone (Tortora et al., 1995). La prolactine est une hormone sécrétée par la glande hypophysaire située dans le cerveau. Après l accouchement, il y a sécrétion de prolactine qui va stimuler la production de lait au niveau des lobules mammaires, ce qui va entraîner la «montée de lait». En dehors de cette période, la prolactine n intervient pas dans la fonction mammaire. L éjection du lait dépend d une hormone l ocytocine libérée par la neurohypophyse (Tortora et al., 1995). 33
50 Chapitre I Description de la glande mammaire Ensemble, œstrogène et progestérone inhibent la sécrétion de FSH et de LH par l hypophyse de sorte qu aucun nouveau follicule ne se développe et, à fortiori, qu aucune ovulation ne se produise. Plus précisément, l œstrogène inhibe la sécrétion de FSH (ce qui fait qu un seul follicule se développe à la fois) tandis que la progestérone inhibe puissamment la sécrétion de LH, même celle qui aurait pu être induite par l œstrogène (ce qui empêche toute ovulation) (Lopes et Pousset, 1989). En l absence de fécondation, la production de progestérone et d œstrogène par le corps jaune s effondre finalement. L endomètre régresse en libérant le flux menstruel. La levée des inhibitions induit une nouvelle production de FSH par l hypophyse et un nouveau cycle commence (Lopes et Pousset, 1989). La concentration hormonale de l axe hypothalamo-hypophysaire au cours du cycle sexuel de la femme en absence de fécondation regroupe la cascade suivante : l hypothalamus commande la sécrétion par l hypophyse, des hormones FSH et LH qui seront détectées au niveau des ovaires ; la FSH commande le développement d un ovocyte au sein d un follicule encore immature de l ovaire ; le follicule produit de l œstrogène, une hormone qui induit le développement de l endomètre pour le préparer à l éventuelle nidation (implantation d un ovocyte fertilisé par un spermatozoïde) ; l œstrogène stimule une production accrue de LH par l hypophyse. L élévation importante du taux de LH dans le sang est appelée le pic LH. L ovocyte transite par les trompes de Faloppe vers l utérus. Toujours sous l influence de la LH, le follicule effondré se transforme en corps jaune sécrétant progestérone et œstrogène. Les taux élevés de progestérone et d œstrogène pendant la deuxième moitié du cycle (après l ovulation) maintiennent l endomètre dans un état de développement apte à recevoir l implantation de l ovocyte s il est fécondé. Ces hormones agissent en même temps comme une barrière s opposant à toute nouvelle fécondation, de sorte qu un seul ovocyte est en principe appelé à se développer à la fois (Lopes et Pousset, 1989). 34
51 Chapitre I Description de la glande mammaire La synthèse, libération et dégradation des hormones sont soumises à une régulation, par suite de leur puissante action. La libération et la destruction de certaines substances messagères sont ajustées de façon à exercer leur effet sans délai et très brièvement. Les organes endocriniens qui forment les hormones stéroïdiennes ne conservent guère d hormones mature, la libération de ces hormones dure plusieurs heures, sinon plusieurs jours, ces hormones à peine solubles dans l eau sont véhiculées dans le courant sanguin par des protéines porteuses : sous cette forme étroitement fixée, les hormones actives ne sont que très lentement détruites, les cellules ne répondent donc que progressivement aux hormones stéroïdes, mais subissent leur action pendant une bien longue période (de quelques heures à quelques jours) que ce n est le cas des effets dus aux hormones peptidiques (Berger, 2000) Contrôle hormonal de la croissance canaliculaire mammaire Les seins sont très sensibles aux variations hormonales, les œstrogènes d origine ovarienne entraînent une croissance des canaux. La progestérone également d origine ovarienne stimule le développement des acini. Pendant la puberté, les seins se développent sous l effet de ces hormones (fig. 5) (Nicholson et al., 2001). 35
52 Chapitre I Description de la glande mammaire Figure 5 : Niveau d action hormonale chez la femme (Nicholson et al., 2001) Au cours du cycle menstruel La phase proliférative (première moitié du cycle sous l effet des œstrogènes) est marquée par une multiplication des cellules épithéliales (augmentation des mitoses), une augmentation de la synthèse d ARN et de la production protéique, une réduction de la lumière des acini et un afflux de lymphocytes dans le tissu conjonctif (Vogel et al., 1992). La phase lutéale (seconde moitié du cycle sous l effet de la progestérone) est caractérisée par une dilatation de la lumière des acini centrée parfois sur un matériel de sécrétions intraluminales (différenciation des cellules épithéliales en cellules secrétoires), un épithélium quiescent, une vacuolisation des cellules myoépithéliales et un œdème (surcharge en eau) du tissu conjonctif (Longacre et Bartow, 1986). Ces modifications entraînent une modification du volume du sein qui apparaît généralement plus tendu voir sensible ou douloureux. 36
53 Chapitre I Description de la glande mammaire Pendant la grossesse La grossesse s accompagne d une importante sécrétion d œstrogène et de progestérone associée à celle de l hormone placentaire lactogène et de l hormone chorionique somatotrope. Dès le second trimestre de la grossesse, on observe une augmentation en nombre et en taille des acini (Battersby et Anderson, 1989) Pendant la lactation Après l accouchement, la disparition des effets inhibiteurs de l œstrogène et de la progestérone sur la prolactine, induit la lactation. Les acini sont distendus par un matériel de sécrétions à la fois dans les cellules et dans la lumière des unités ductulolobulaires. Une fois produit au niveau de ces unités, le lait est conduit au mamelon par les canaux galactophores. La production de lait cesse dans les 7 à 10 jours, s il n y a pas de stimulation par succion du mamelon. Cependant, il faut 3 à 4 mois au parenchyme mammaire pour retrouver son état de base (Peltier et Guinebretière, 1998) Ménopause La ménopause se caractérise par une raréfaction des acini suite à une chute des taux d œstrogène et de progestérone (Tavassoli, 1992). Les cellules épithéliales et myoépithéliales s atrophient alors que la membrane basale s épaissit. Le tissu conjonctif subit aussi une évolution avec altération des fibres élastiques et collagènes aboutissant à une ptose mammaire. Le sein de la femme ménopausée devient essentiellement constitué de tissu adipeux. Au cours de la vie fœtale : Au cours de la vie fœtale, et plus particulièrement lors du troisième trimestre de la grossesse, les œstrogènes et la progestérone produites par la mère, provoquent une canalisation de l épithélium mammaire, une différenciation du parenchyme mammaire et la formation des canaux galactophores, ainsi que le développement du réseau lobulo-alvéolaire. Après la naissance, la glande reste dans cet état rudimentaire ; À la puberté : Les premières modifications ovariennes apparaissent, avec la mise en place des cycles menstruels. La glande mammaire est alors soumise à une 37
54 Chapitre I Description de la glande mammaire alternance d exposition aux œstrogènes (1 ère moitié du cycle) et à la progestérone (2 ème moitié du cycle) ; Sur le plan expérimental, l administration pendant 14 jours d œstrogènes, de progestérones, de prolactine et d hormones de croissance provoque le développement canaliculaire de la glande mammaire de rate âgée de 26 à 28 jours et qui a été hypophysectomisée et castrée, la combinaison œstrogène, corticoïde, progestérone, prolactine, et hormones de croissances semble optimale pour induire le développement canaliculaire et un début de développement alvéolaire comparable à ceux observés au cours de la première moitié de la gestation (Milerom, 1980). In vitro, la même association assure le développement des canaux mammaires obtenus à partir de biopsies pratiquées chez la femme nullipare, dans ce dernier model la prolactine associé à l insuline a une action mitotique pendant 5 jours de culture (Delouis, 1980). L ensemble de ces résultats montre que la croissance canaliculaire dépend d une séquence hormonale comprenant des stéroïdes ovariens et de la prolactine associée à un corticoïde, dans cette séquence, le rôle de la prolactine est essentiel. L hormone de croissance semble avoir un effet additif favorable mais dont l amplitude est variable selon les espèces. Cette séquence hormonale contrôle aussi le développement lobulo-alveolaire qui survient au cours de la gestation (Milerom, 1980). 38
55 Chapitre I Description de la glande mammaire 5. Récepteurs hormonaux au niveau de la glande mammaire Les récepteurs stéroïdiens du sein sont des glycoprotéines situées dans la fraction cytosolique de la cellule épithéliale mammaire. Cette macromolécule de Da de poids moléculaire est en fait une molécule très malléable qui peut présenter différentes conformations spatiales, soit une forme native, généralement inactive soit une forme activée. Une cellule endocrine envoie un message sous la forme d une hormone qui va emprunter la circulation sanguine soit librement, soit liée à une protéine de transport. L hormone quitte la circulation pour atteindre la cellule cible, et se lie à un récepteur spécifique (Barritt, 1992). Les hormones stéroïdiennes pénètrent directement dans les cellules et exercent leur action grâce à des récepteurs spécifiques intracellulaires dans les tissus cibles, ces récepteurs ont une très grande affinité pour leurs hormones spécifiques (Tortora et al., 1995) étant hydrophobes et liposolubles elles sont transportées dans le sérum par l interaction avec des protéines spécifiques, le taux réduit de ces protéines en cas d obésité explique l excès de formes libre circulantes actives d œstrogènes. Ces hormones ont une affinité spécifique pour leurs récepteurs de l œstrogène ou de la progestérone et le complexe hormono-récepteur est capable d activer de façon spécifique le tissu mammaire en augmentant la multiplication cellulaire, mécanisme inducteur de la cancérogenèse. La biosynthèse des récepteurs hormonaux dépend d une régulation hormonale, ainsi l œstradiol stimule la synthèse de son propre récepteur cytosolique et celui de la progestérone inhibe la biosynthèse de son propre récepteur et la synthèse du récepteur de l œstradiol (Gerard et Torpora, 1995). Le récepteur activé modifie alors l expression génique, c est à dire qu il déclenche ou arrête l activité de gènes spécifiques de l ADN nucléaire. Une meilleure connaissance des bases biologiques du développement des cancers a permis de définir des cibles thérapeutiques, portant notamment sur les étapes de transduction d un signal de prolifération, de différenciation, d invasion ou de survie cellulaire. Les connaissances, ces dernières années en sciences fondamentales ont permis de mieux connaître les étapes de la transduction du signal depuis la fixation d un 39
56 Chapitre I Description de la glande mammaire ligand à son récepteur jusqu à la transcription de gènes impliqués dans la prolifération, la différenciation, l invasion et l angiogenèse cellulaire. Le passage d une cellule eucaryote de la phase quiescente (G0) à la phase de mitose (M), en réponse à des stimuli extérieurs, est un processus multi-étape. Il requiert la transduction de signaux divers (prolifération, migration, différenciation) et l activation de protéines intracellulaires. Ce processus finement régulé est altéré au sein des cellules néoplasiques, engendrant une prolifération, une migration et une différenciation cellulaires non contrôlées Récepteurs transmembranaires La communication inter et intracellulaire peut être schématiquement divisée en deux étapes : la fixation sur un récepteur transmembranaire d un signal extracellulaire, puis l activation de seconds messagers intracellulaires entraînant l activation de facteurs de transcription qui vont pouvoir agir directement sur la transcription de gènes impliqués dans les processus de prolifération, de migration et de différenciation cellulaires. Six familles de récepteurs à tyrosine kinase sont actuellement décrites se différenciant par leur ligand et leur structure chimique et sept récepteurs dit «orphelins» (Tronick et Aaronson, 1995) caractérisés par : un domaine extracellulaire, site de fixation du ligand (partie N terminale de la molécule) ; un domaine intracellulaire, site d ancrage dans la membrane cytoplasmique ; un domaine intracellulaire riche en résidu tyrosine, possédant une activité tyrosine kinase Récepteurs doués d activité de tyrosine kinase Les récepteurs doués d activité de tyrosine kinase (RTK) forment une vaste et grande famille de récepteurs cellulaires superficiels dont les ligands sont des hormones peptidiques ou protéiques solubles ou membranaires, comme l insuline ou le facteur de croissance épithélial. Quand un ligand s attache à ce type de récepteur, il en stimule l activité de tyrosine kinase, qui elle précipite une cascade de 40
57 Chapitre I Description de la glande mammaire transduction de signaux aptes à changer la physiologie de la cellule et/ou le profil d expression des gènes. Les voies empruntant les RTK jouent des rôles multiples, notamment en modulant la prolifération, et la différenciation des cellules, en les maintenant en vie et en ajustant leur métabolisme. Il a été découvert certains récepteurs à activité RTK en étudiant des cancers humains associés à des formes mutantes de récepteur de facteur de croissance qui donnent aux cellules l ordre de se diviser même en l absence de facteur de croissance, un de ces récepteurs mutants, codé par le locus neu, contribue à la prolifération anarchique de certains cancers du sein (Deshaies et al., 2005). Les Récepteurs transmembranaires de la famille HER (Humen Epithélial Receptor) représente une famille qui comprend quatre membres dénommés : R-EGF ou HER1, cerb2 ou HER2, cerb3 ou HER3 et cerb4 ou HER4 (Sedlacek, 2000) Récepteurs HER2 Le récepteur HER2 est aussi appelé erb-b2 en raison de sa similarité de séquence avec l oncogène viral v-erbb (virus de l érythroblastose aviaire). Ce récepteur de 185 kda est codé par le proto-oncogène neu (autre dénomination possible du récepteur : HER2/neu) (fig. 6) (Sedlacek, 2000). C est un récepteur orphelin puisque à ce jour, aucun ligand spécifique n a été identifié. Il a également la capacité de former des hétérodimères, de préférence avec HER1, à moindre fréquence avec HER3 et HER4. Son amplification génique conduit à sa surexpression à la surface de la cellule et, par conséquent, à une augmentation de la division cellulaire. Il est surexprimé dans 15 à 25% des cancers du sein selon le stade. Dans les tissus mammaires sains, on compte environ récepteurs HER2 par cellule. Dans les cancers du sein présentant une amplification du gène de HER2, on dénombre jusqu à 100 fois plus de récepteurs par cellule. Cette surexpression est associée à une augmentation de l agressivité de la tumeur, à la résistance de la tumeur aux traitements, à un risque augmenté de rechute et à une survie moindre (Ciardiello et Tortora, 2001). Par conséquent, HER2 est devenu une cible des thérapies antitumorales mammaires en raison de son rôle important dans le développement des cancers du sein. Les récepteurs de la famille HER peuvent être 41
58 Chapitre I Description de la glande mammaire tronqués dans leur partie extracellulaire, ce qui empêche la fixation des anticorps monoclonaux et ainsi leur action. La perte du domaine extracellulaire du récepteur tyrosine kinase ErbB2 et l expression d un récepteur tronqué en N-terminal sont corrélées à la présence de métastases ganglionnaires et sont des éléments pronostiques défavorables dans les cancers mammaires. a. Fonction physiologique Le mécanisme d action est des plus classiques. Le ligand se fixe à son récepteur, ce qui induit une dimérisation et une auto-activation des résidus tyrosine du domaine C terminal. Des molécules adaptatrices possédant un domaine d homologie Src (SH2 domaine) et un domaine de fixation à tyrosine sont à leur tour activées. Deux grandes voies de la transduction du signal sont privilégiées, la voie Ras/Raf/MAKK-MEK/ERK (Raf/mmitogen activated phosphoryled kinase kinase), et la voie des phospho-inositol/pi3kinase/akt (fig. 7) (Semenza, 1999), mais aussi les voies passant par la phospholipase C et la voie STATS (PAK-JNKK-JNK). Elles vont induire la phosphorylation de facteurs de transcription (Jun, Fos, myc, cycline D1) ainsi que la transcription de protéines impliquées dans les mécanismes de prolifération cellulaire, d angiogenèse, de migration, de différenciation cellulaire ou bien encore dans la survie cellulaire. Il est à noter que, en fonction de tel ou tel ligand, les récepteurs formeront des homodimères ou des hétérodimères (Ciardiello et Tortora, 2001). La protéine HER3 a perdu son activité tyrosine kinase et, à ce jour, aucun ligand spécifique de HER2 n est connu (Sedlacek, 2000). 42
59 Chapitre I Description de la glande mammaire Figure 6 : Les voies de signalisation cellulaire par la liaison du ligand à l HER2 (Sedlacek, 2000). 43
60 Chapitre I Description de la glande mammaire Figure 7 : Cascade de réponse induite par le stimuli externe et réponse physiologique qui en découle (Semenza, 1999). 44
61 Chapitre I Description de la glande mammaire b. Altération des récepteurs de la famille HER2 dans le cancer du sein Plusieurs mécanismes peuvent expliquer leur propriété oncogénique et leur implication dans le processus de cancérogenèse (Slichenmyer et Fry, 2001) : réarrangement du gène induisant la synthèse d une protéine oncogénique de fusion avec le site catalytique et le site de dimérisation/activation ; gain de fonction par une mutation ou une délétion du gène au niveau du site de régulation ; surexpression de la protéine par amplification du gène ; perte du mécanisme de régulation de l activité d auto-phosphorylation. Les anomalies décrites dans le cancer du sein sont des mutations ou des amplification géniques : HER1 (37%), HER2 (25 à 30%), HER3 (25 à 71%), HER4 (49 à 60%) (Starink et al., 1986). Dans le cancer du sein, HER1 et HER2 sont fréquemment co-exprimées (50% des cas) (Bacus et al., 1994). HER3 est surexprimée dans plus de 50% des cas du cancer du sein et elle est fréquemment co-exprimée avec HER2 laissant supposer qu elle joue un rôle prépondérant dans le processus de cancérogenèse (Leslie et Downes, 2002) R-EGF (HER1) et sa signalisation Le récepteur à l epidermal growth factor (REGF) est l un des quatre membres de la famille HER de récepteurs transmembranaires à activité tyrosine kinase : REGF ou HER1, HER2 ou C-erbB2, HER3 et HER4 (Thompson et Gill, 1885). C est une protéine d environ 1200 acides aminés possédant un domaine transmembranaire et une partie extracellulaire glycosylée qui fixe son ligand. Le domaine intracellulaire, caractérisé par une activité tyrosine kinase, est activé lorsque le ligand se fixe à son récepteur (Carpenter et Cohen, 1990). Ce récepteur activé catalyse le transfert d un groupement phosphate de l ATP vers la chaîne latérale d un résidu tyrosine, à la fois sur le récepteur lui-même et sur des protéines cellulaires spécifiques (Yarden et Ullrich, 1988). Ainsi, la liaison du ligand sur le REGF provoque la dimérisation du REGF, rendant les deux domaines intracellulaires capables de se phosphoryler mutuellement sur des résidus tyrosine. Il existe des phénomènes d hétérodimérisation entre le REGF et d autres membres de la famille HER. Les 45
62 Chapitre I Description de la glande mammaire ligands préférentiels du REGF sont l EGF et le TGFα. La phosphorylation des résidus tyrosine intracytoplasmiques déclenche des signaux de transduction intracellulaire, impliquant en particulier la voie des MAP-kinases, des phosphatidylinositol-3 kinases, et de STAT3 (voie AKT) (Yarden et Ullrich, 1988). L activation du REGF induit des modifications de la physiologie cellulaire avec, en particulier, une activation de la survie cellulaire et une inhibition de l apoptose par les voies d activation d AKT (Yarden et Sliwkoski, 2001). En thérapeutique inhiber les voies d activation du REGF a pour objectif de ralentir la division cellulaire et de restaurer en partie les capacités apoptotiques des cellules tumorales Libération de facteurs de croissance transformants Les facteurs de croissance transformants α et β (les TGF) sont des protéines secrétées par les cellules tumorales et capables de stimuler la multiplication de cellules normales, il existe des facteurs ou des hormones qui règlent la prolifération des cellules embryonnaires normales, mais que beaucoup de cellules tumorales expriment de façon aléatoire, comme elles le font d autres facteurs encore (Joly, 1994) Expression tumorale du REGF dans le cancer du sein Le cancer du sein est très certainement la localisation tumorale qui a fait l objet de la plus large exploration de l expression du REGF (Diéras et al., 2003). Ce phénomène a été déclenché par la publication initiale de Sainsbury et al.,1987 qui, il y a près de deux décennies, suggéraient un rôle pronostique très prometteur du REGF dans le cancer du sein. Cette valeur pronostique du REGF n a que très rarement été confirmée par la suite. Le débat sur la valeur pronostique du REGF dans le cancer du sein a été appuyé par une étude sur 780 patientes avec un suivi médian de 8 ans (Ferrero et al., 2001). Il ont utilisé un outil analytique réellement quantitatif : la mesure du nombre de récepteurs par technique biochimique de compétition de fixation du ligand (Scatchard). Sur ces bases, la concentration médiane du REGF dans la population étudiée était particulièrement basse (9 fmol/mg protéines) avec un écart allant du 46
63 Chapitre I Description de la glande mammaire non détectable à près de 800 fmol/mg protéines. Il n y avait pas de lien significatif entre l expression tumorale du REGF et les facteurs pronostiques reconnus tels que la taille, le grade histologique SBR et l envahissement ganglionnaire. En revanche, ils ont constaté une baisse constante et significative de l expression du REGF en fonction de l âge des patientes. Cette analyse a permis également de mettre en évidence une relation inversement significative entre le niveau d expression du récepteur à l œstradiol (RE) et celui du REGF. La comparaison REGF-cerbB2 (HER2) était attendue et a été menée par l équipe de Tsutsui (Tsutsui et al., 2003). Le marquage immunohistochimique des deux récepteurs pour une population de 670 patientes a conduit à l identification de quatre groupes : REGF- et HER2- pour 417 patientes, REGF+ et HER2- pour 136 patientes, REGF- et HER2+ pour 72 patientes et enfin REGF+ et HER2+ pour 45 patientes. Les auteurs notaient une valeur pronostique plus forte pour HER2 que pour REGF (Tsutsui et al., 2003). On peut raisonnablement considérer que l expression tumorale du REGF dans le cancer du sein se situe à un niveau mesurable mais relativement faible sans valeur pronostique reconnue. Le fait intéressant est la relation inverse entre REGF et récepteur aux estrogènes (RE) (Ferrero et al., 2001). L effet des œstrogènes est médié par les récepteurs aux œstrogènes (RE), qui sont des protéines nucléaires de 66 kda. Cependant les RE ne sont retrouvés que sur 6 à 7% des cellules épithéliales du sein normal, et plus particulièrement au niveau des lobules. L expression des RE au niveau des cellules épithéliales varie en fonction du cycle menstruel. L action des œstrogènes se fait donc à la fois de manière directe par l action sur les cellules épithéliales et indirecte par l action sur les cellules mésenchymateuses qui sécrètent des facteurs de croissance (EGF, TGF-α, IGF, FGF et TGF-β). L EGF et le TGF-α, agissent via le récepteur EGFR (Yarden et Ullrich, 1988) et sont des régulateurs de la prolifération et de la différenciation normale de l épithélium mammaire, en revanche, le TGF- β est un facteur inhibiteur de la croissance cellulaire. 47
64 Chapitre I Description de la glande mammaire Relation REGF et RE dans le cancer du sein Il existe au moins deux niveaux d interaction cellulaire à visibilité claire entre RE et REGF. Le premier se situe au niveau de la phosphorylation de RE médiée par la voie REGF (Bunone et al., 1996). Il est important de noter que cette phosphorylation active la fonction transcriptionnelle de RE indépendamment de son interaction avec l œstradiol, et ce même en présence du tamoxifène (Campbell et al., 2001) ; cela confère une propriété d hormonorésistance au RE phosphorylé via la voie REGF. Le second niveau d interaction concerne le lien entre RE et PI3K (Simoncini et al., 2000). En effet, non seulement PI3K phosphoryle et active RE mais REα est capable d interagir avec la sous-unité p85a de PI3K au niveau de la membrane cellulaire ; cette interaction RE-PI3K conduit à l activation de PI3K et à celle de la kinase AKT. La relation inversement significative antérieurement mise en évidence entre l expression tumorale du REGF et celle du RE peut être mise en rapport avec des données cliniques et précliniques qui montrent une moindre efficacité du tamoxifène dans les cancers du sein surexprimant REGF et HER2. De même, une résistance acquise à la déprivation ostrogénique est fréquemment associée à un accroissement d activité de la voie ERK1/2 MAP kinase (Santen et al., 2002). La famille des human epidermal growth factor receptors (HER) comprend quatre membres, HER1 (ou EGFR), HER2 (ou cerb2/neu), HER3 et HER4 comme il à été citer plus haut, impliqués principalement dans la prolifération de cellules normales mais aussi dans la croissance anormale de cellules de certains types de tumeurs humaines. Ces récepteurs HER, très impliqués dans le développement tumoral, sont les cibles idéales de thérapies anticancéreuses. Les anti-rtk sont soit des anticorps monoclonaux, soit des composés chimiques inhibiteurs de tyrosine kinase. Leur utilisation est fondée sur des critères diagnostiques renseignant le niveau d expression de leurs cibles. Comme il a été rapporté avec les anti-egfr (Tronick et Aaronson, 1995), ces thérapies peuvent être confrontées à des phénomènes de résistance, liés à des perturbations au niveau des voies de signalisation, du microenvironnement tumoral ou encore du système immunitaire. Ces voies de résistance peuvent être spécifiques d un type de récepteur ou communes à l ensemble des RTK. Deux grandes voies de transduction du signal 48
65 Chapitre I Description de la glande mammaire sont activées : la voie des MAP kinases et la voie de la PI3 kinase/akt. Ces deux voies de transduction du signal conduisent à l activation de protéines impliquées dans la prolifération cellulaire, l angiogenèse, la migration cellulaire, la différentiation cellulaire ou bien encore dans la survie cellulaire (Sedlacek, 2000) Récepteurs intracellulaire «stéroïdiens» Ce sont des glycoprotéines situées dans la fraction cytosolique de la cellule épithéliale mammaire, elles ont une affinité spécifique pour une hormone donnéeœstrogène ou progestérone- et le complexe hormono-récepteur est capable d activer de façon spécifique le tissu mammaire en augmentant la multiplication cellulaire, mécanisme même de la cancérogenèse. La biosynthèse des récepteurs hormonaux dépend d une régulation hormonale ainsi l œstradiol stimule la synthèse de son propre récepteur cytosolique et celui de la progestérone inhibe la biosynthèse de son propre récepteur et la synthèse du récepteur de l œstradiol. A l état non stimulé, les récepteurs sont liés a des protéines dites «de choc thermique» d un poids moléculaire de 90 KDa qui les entourent et préviennent leur interaction avec le site de liaison de l ADN, en présence de l hormone, la protéine de choc thermique est relarguée et le récepteur devient actif. Il se lie au site de réponse de l ADN et accélère la transcription de l ARNm grâce à sa fonction d activation (Joly, 1994). Les récepteurs intracytoplasmiques pénètrent dans le noyau après activation par les hormones, il possède plusieurs domaines d action notamment : le domaine de reconnaissance spécifique de l hormone ; le domaine de liaison avec l ADN. Les récepteurs nucléaires sont des récepteurs intracellulaires formant une large famille composée de plus de 150 protéines différentes. Ils sont présents dans de nombreuses espèces, y compris chez les invertébrés. Les récepteurs nucléaires fonctionnent comme des facteurs de transcription activés par la liaison de leur ligand. Ils possèdent de ce fait 2 domaines complémentaires : un domaine de liaison à l ADN permettant la reconnaissance de séquences d ADN spécifiques dénommées HRE, et un domaine de liaison au ligand. Les récepteurs activés se lient à l ADN sous forme de dimères. 49
66 Chapitre I Description de la glande mammaire Différents arguments épidémiologiques et expérimentaux suggèrent que les œstrogènes sont impliqués dans la cancérogenèse mammaire. En effet, une longue exposition aux œstrogènes endogènes (puberté précoce, ménopause tardive) augmente le risque de développer un cancer du sein (Begg et al., 1987). Cet argument épidémiologique est consolidé par des données expérimentales. Les études effectuées in vitro sur des lignées de cellules mammaires cancéreuses exprimant d une manière endogène le récepteur à l œstradiol (RE+) montrent que l œstradiol (E2) augmente la prolifération cellulaire (Chalbos et al., 1982). Cette prolifération pourrait être relayée par la stimulation de la transcription des gènes de facteurs de croissance (EGF ou insulin like growth factor II) (El-Tanani et Green, 1997) et l inactivation de la transcription de gènes induisant l apoptose (Vignon et al., 1992). D autres récepteurs peuvent contribuer à cette prolifération cellulaire, comme le récepteur à la progestérone (Nardulli et Katzenellenbogen, 1988). D un point de vue clinique, la présence du RE dans le cancer mammaire est liée à une meilleure différenciation tumorale : elle serait prédictive de la réponse au traitement antihormonal et aurait une valeur pronostique (Pichon et al., 1996). Des études expérimentales et cliniques montrent que la réponse à l hypoxie pourrait contribuer à la propagation tumorale, à la progression maligne et à la résistance au traitement dans ces tumeurs (Hockel et Vaupel, 2001). En effet, l hypoxie tumorale résulte d une mauvaise vascularisation tumorale compromettant les fonctions biologiques des cellules affectées. Elle stabilise le facteur HIF1α (hypoxia-inducible factor1α) et active la transcription de plusieurs gènes contrôlant le transport et le métabolisme du glucose, augmentant ainsi la survie des tumeurs sous les conditions d hypoxie (Semenza, 1999). De plus, HIF1α est considéré comme étant le centre inducteur de l activité angiogénique car il active la transcription du facteur de prolifération endothéliale, le facteur VEGF (Iyer et al., 1998). Bos et al., 2003 ont étudié le taux d expression et la localisation de HIF1α ainsi que l induction éventuelle de ses gènes cibles dans des cancers mammaires de différents stades et ont montré une augmentation du taux d HIF1α associée à une plus grande prolifération cellulaire et une élévation de l expression du RE et du VEGF (vascular endothelial growth factor) dans les tumeurs mammaires. 50
67 Chapitre I Description de la glande mammaire ERα, ERβ Découvert en 1958 par Elwood Jensen et cloné en 1986, le récepteur α des œstrogènes (ERα) est aujourd hui bien caractérisé. Beaucoup plus récemment, le récepteur β des œstrogènes (ERβ) a été identifié en Le ERα a été détecté principalement dans l ovaire, l utérus, l hypophyse, les testicules, l épididyme, le rein et la glande mammaire et dans plusieurs régions du cerveau. Le ERβ, quant à lui, se retrouve principalement dans la prostate, l ovaire, l utérus, le poumon, la rate et, tout comme l ERα, dans plusieurs régions du cerveau. Malgré de légères différences entre certains ligands, comme le 17α-œstradiol, qui se lie 5 fois plus fortement à l ERα que le ERβ, les deux formes du récepteur aux œstrogènes lient les mêmes ligands avec sensiblement la même efficacité. Les deux récepteurs ont une grande homologie d identité et les mêmes domaines sont présents sur les deux récepteurs (Bos et al., 2003) Récepteur à l œstradiol et voie de signalisation Il présente des caractéristiques structurales et des domaines fonctionnels communs aux récepteurs (Hall, 1994). L élément de réponse aux œstrogènes (ERE) est habituellement palindromique, formé de deux demi-sites inversés séparés par trois paires de bases (5 -GGTCAnnnTGACC-3 ) (Mangelsdorf et al., 1995). Les récepteurs nucléaires ont une structure en domaines commune avec deux régions hautement conservées : le domaine central de liaison à l ADN et le domaine C- terminal de liaison de l hormone (Klein-Hitpass et al., 1988). Dans le cas des récepteurs aux œstrogènes, l activation de la transcription des gènes se fait après stimulation hormonale par l E2 qui pénètre dans la cellule par diffusion passive et se lie à son récepteur spécifique. Le complexe hormone-récepteur se fixe à sa séquence spécifique, ERE (Chaplain et al., 1999). Le récepteur de l E2 (RE) peut aussi moduler l expression des gènes par interaction avec d autres facteurs transcriptionnels, ces effets transcriptionnels du RE expliquent probablement son implication dans le développement des cancers hormono-dépendants (Pratt et Toft, 2002). 51
68 Chapitre I Description de la glande mammaire En l absence d hormone, les récepteurs aux hormones stéroïdes existent sous forme d un complexe inactif composé de plusieurs protéines dont les protéines chaperonnes, telles que les protéines de choc thermique («heat shock protein» ou Hsp) (Dickson et al., 1986). Le rôle des Hsp et des autres protéines chaperonnes serait de maintenir le récepteur dans une conformation adéquate lui permettant de répondre rapidement à un signal hormonal. La liaison de l hormone au récepteur entraîne la dissociation de ce complexe et permet l activation du récepteur et sa liaison à l ADN (Pratt et Toft, 2002) Transconformation des récepteurs d œstrogènes La transconformation correspond à des modifications structurales du récepteur nucléaire aboutissant à son activation en tant que facteur transcriptionnel. Deux régions du récepteur sont particulièrement importantes pour ce processus : la région AF1 située en N-terminal et la région AF-2 située en C-terminal. Bien que les régions AF1 et AF2 puissent fonctionner de façon autonome, indépendamment l une de l autre, l interaction entre ces 2 régions est indispensable à une activité transcriptionnelle maximale des récepteurs nucléaires. (Deshaies et al., 2005). La région AF2 située dans l hélice H12 du domaine de liaison au ligand nécessite la liaison préalable du ligand pour être activée (Barchielli et al., 1999). Elle joue un rôle important dans l activité transcriptionnelle du récepteur nucléaire par sa capacité à interagir avec les cofacteurs (Pratt et Toft, 1997) Dimérisation du récepteur La majorité des récepteurs nucléaires se fixent à l ADN sous forme de dimères. De nombreux récepteurs nucléaires sont ainsi actifs sous forme homodimérique (exemple RE, RA, RP, RG). Certains récepteurs nucléaires forment des hétérodimères avec d autres récepteurs nucléaires (par exemple: HER1, HER2). Les hétérodimères peuvent intéresser deux isoformes différentes d un même récepteur (par exemple : le récepteur aux œstrogènes RE existe sous 2 isoformes différentes RE-alpha et RE-beta, qui peuvent former des dimères RE-alpha/RE-beta). Le dimère de récepteur se fixe sur une séquence spécifique de l ADN (HRE). La zone de dimérisation, hautement conservée, est située dans les régions E et C (Pratt et Toft, 2002). 52
69 Chapitre I Description de la glande mammaire La réponse transcriptionnelle est généralement une activation de la transcription des gènes cibles. Dans certains cas, une répression transcriptionnelle est observée. L activation des récepteurs nucléaires peut moduler la régulation de nombreuses protéines, cellulaires ou sécrétées. Ces protéines interviennent dans des fonctions cellulaires très variées telles que les fonctions différenciées de la cellule, la régulation de la prolifération cellulaire et l apoptose (Berger, 2000). 6. Récepteurs hormonaux en pathologie mammaire Depuis leur mise en évidence, les récepteurs cytosolique des œstrogènes (RE) puis ceux de la progestérone (RP) ont été très largement dosés dans le cancer du sein, malgré les difficulté techniques liés surtout à l hétérogénéité des tumeurs mammaires, et la remise en cause de leur localisation sub-cellulaire exacte, la mesure de RE et RP a fait la preuve de son double intérêt en clinique, pronostic et thérapeutiques, le contrôle hormonal de la glande mammaire normale ou pathologique ne se résume toutefois pas aux seuls récepteurs d œstrogènes et progestérones, la prolactine (RPL), seule ou en synergie avec d autres hormones, est par exemple indispensable au contrôle de la multiplication et de la différentiation de croissance notamment l Epidermal Growth Factor (EGF), sont également impliqués dans la multiplication cellulaires (Lefebbvre, 1985). 7. Etiologie hormonale du cancer du sein Les théories concernant l étiologie hormonale du cancer du sein sont fort nombreuses. Elles varient selon les auteurs. Toutefois, le fait que les œstrogènes puissent avoir un rôle carcinogène ou cocarcinogène ne semble plus guère discuté. Aussi importe-t il d évaluer ce risque en fonction des autres paramètres hormonaux pouvant être impliqués directement ou indirectement dans la promotion du cancer mammaire humain (Mauvais-Jarvis et D le, 1985). L étude éthiopathologique du cancer du sein implique la connaissance de la glande mammaire et des sécrétions hormonales qui l influencent (Mauriac et al., 2003). L origine des cancers du sein est manifestement multifactorielle : en effet ces cancers se développent dans un tissu dont la structure subit des variations cycliques et périodiques au cours des épisodes de la vie génito-obstetricale. Ces éléments sont 53
70 Chapitre I Description de la glande mammaire eux-mêmes sous la dépendance de multiples facteurs notamment hormonaux (Mauvais- Jarvis et D le, 1985). Il n y a pas d évidence en faveur du rôle «initiateur» des hormones sexuelles, lesquelles sont considérées plutôt comme des facteurs de promotion. Toutefois les hormones sexuelles pourraient avoir deux actions : celle de favoriser directement ou indirectement la synthèse de DNA et l activité mitotique des cellules initialement transformées par un agent carcinogène d initiation ; les hormones pourraient intervenir sur la durée de la période de latence qui s écoule entre l agression carcinogène et primaire et la tumeur patente Facteurs hormonaux chez la femme avant ménopause Qu ils soient endogènes ou exogènes, ils modifient le climat hormonal du tissu mammaire, et d éventuelle lésions bénignes préexistantes. Certaines pouvant être améliorées puisque celles-ci (prolactine, œstradiol, et progestérone) sont identiques chez l adolescentes ayant ou n ayant pas d antécédent familial de cancer du sein (Mauriac et al., 1986). Les œstrogènes seraient cancérogènes pour le sein plus en terme de durée d exposition que d intensité, il s agit là d ailleurs d une notion de cancérogenèse appliquée à tout les cancers, notamment en ce qui concerne les relations entre tabac et cancer bronchique (Mauvais- Jarvis et D le, 1985). La théorie de la fenêtre œstrogénique est basée sur les 5 postulats suivants : cancer du sein humain et induit par un carcinogène qui agit au niveau d une glande mammaire dite «susceptible» ; la stimulation œstrogénique non compensée par la progestérone constitue l état le plus favorable pour l induction du cancer mammaire ; il existe une longue période de latence entre l induction de la tumeur et son expression clinique ; la durée d exposition aux œstrogènes (fenêtre œstrogénique) détermine le risque de cancer mammaire ; la possibilité pour un cancer du sein d être induit par œstrogènes décroît avec l apparition de cycle ovulatoire, en particulier avec l établissement 54
71 Chapitre I Description de la glande mammaire d une première grossesse menée à terme (Mauvais- Jarvis et D le, 1985). Les œstrogènes endogènes existent sous trois formes, soit l œstradiol, l œstrone et l œstriol. Dans les tissus des mammifères, les œstrogènes exercent des effets biologiques essentiels à la manifestation d un grand nombre de processus physiologiques. La progestérone au niveau des cellules épithéliales des galactophores principaux, bloque le cycle des mitoses induites par les œstrogènes, mais au niveau des galactophores distaux en association avec les œstrogènes elle favorise la multiplication des canalicules. Les œstrogènes et la progestérone sont au 1 er plan comme en témoigne l augmentation de 15% du volume mammaire en fin de cycle avec une double composante d œdème et de prolifération épithéliale. La prolactine influence peu le développement du tissu mammaire au cours du cycle menstruel ou de la lactation, sa secrétions est parallèle à celle des œstrogènes et son rôle n est que lactogénique (Mauriac et al., 2003). Il semblerait que ce soit le déséquilibre entre œstrogènes et progestérones qui est surtout en cause du cancer du sein, de même un taux élevé d œstrogènes pourrait favoriser une augmentation de la secrétions de prolactine. L effet des œstrogènes est médié par leurs récepteurs (RE). L expression des RE au niveau des cellules épithéliales varie en fonction du cycle menstruel (Balynsky, 1979). L action des œstrogènes se fait donc à la fois de manière directe par l action sur les cellules épithéliales et indirecte par l action sur les cellules mésenchymateuses qui sécrètent des facteurs de croissance (EGF, TGF-α, IGF, FGF et TGF-β). L EGF et le TGF-α, agissent via le récepteur EGFR et sont des régulateurs de la prolifération et de la différenciation normale de l épithélium mammaire, en revanche, le TGF-β est un facteur inhibiteur de la croissance cellulaire (Day, 2001) Facteurs hormonaux chez la femme après ménopause Chez la femme non ménopausée, des œstrogènes sont produits dans les ovaires. Après la ménopause, les ovaires ne synthétisent plus d œstrogènes, mais le corps produit d autres hormones (androgènes) dans la corticosurrénale. Ces 55
72 Chapitre I Description de la glande mammaire hormones peuvent être transformées en œstrogènes sous l effet d une enzyme, l aromatase. Les hormones produites dans le tissu adipeux le sont grâce à cette aromatase, c est donc logique que le blocage de cette enzyme arrête la production de ces hormones après la ménopause. In vitro, la prolifération des cellules épithéliales est majorée par l œstradiol et diminuée par les antiœstrogènes ainsi que par la progestérone qui pourrait intervenir par une diminution des récepteurs aux œstrogènes et par une transformation de l œstradiol en œstrones, œstrogènes plus faibles. In vivo, l action antiproliférative de la progestérone est discutée du fait de la multiplication cellulaire maximale en fin de phase lutéale mais l application locale de progestérone naturelle est associée à une diminution de cette prolifération dans les études de Barrat et de Chang. La prolactine est retrouvée augmentée, cette augmentation pouvant être secondaire à l hyper œstrogénie et au stress (Mauvais- Jarvis et D le, 1985). 8. Rôle carcinogène des hormones sexuelles La survenue d un cancer résulte d une interaction entre des facteurs endogènes (l hôte) et exogènes (l environnement), en ce qui concerne ces derniers la carcinogenèse mammaire provoquée expérimentalement chez l animal démontre la complexité et le polymorphisme des agents en cause, qu ils soient de nature hormonale, génétique, clinique, physique ou virale. Les œstrogènes peuvent être générateurs de cancers chez l animal ou chez l homme. Les femmes castrées chirurgicalement ayant 35 ans ont un risque diminué des deux tiers par rapport aux femmes ménopausées entre 45 et 54 ans (Trichopoulos et al., 1972). Quoique les œstrogènes soient nécessaires à la formation d une tumeur mammaire, il est difficile de mettre en évidence une action directe de ce stéroïde sur la multiplication cellulaire dans les systèmes de culture. Afin d expliquer ce paradoxe, la suggestion que les œstrogènes ne sont pas en eux-mêmes des facteurs de croissance cellulaire a été posée, mais ils agissent en induisant la synthèse de facteurs de croissance. Certains de ces facteurs ont été décrits comme étant formés en 56
73 Chapitre I Description de la glande mammaire dehors du tissu mammaire on leur à donner le nom d œstromédine (Chalbos et Vignon, 1981). L œstriol (E3) aurait un rôle protecteur vis à vis du cancer du sein, le risque est inversement proportionnel aux taux d œstradiol, cela expliquerait le rôle protecteur de la première grossesse à terme, puisque durant le 3 ème trimestre d une gestation, l E3 sérique augmente de façon importante par rapport à l œstrone E1 et à E2 élevé pendant deux ans. De plus, la privation en œstrogènes comme paradoxalement leur prescription à doses thérapeutiques, peut entraîner une régression tumorale, ils agissent donc de façon différente selon le moment ils sont administrés, ce qui rend leur rôle difficile à cerner (Cole et Mac Mahon, 1969). Pour les œstrogènes exogènes, une première étude a suggéré que, chez les femmes porteuses d une mutation des gènes BRCA1 ou BRCA2, la contraception orale (CO) utilisée avant la première grossesse augmenterait le risque de cancer du sein (Ursin et al., 1997). Cette observation initiale portait sur un petit échantillon de patientes (n = 50). Une étude plus importante a porté sur des patientes ayant un risque familial élevé sans que des mutations aient été caractérisées. Les apparentées au premier degré (sœurs et filles) de patientes atteintes de cancer du sein qui avaient utilisé la CO avaient un risque plus élevé que les apparentées de second degré (petites-filles et nièces) (Grabrick et al., 2000), ainsi, le risque relatif de cancer du sein était de 3,3 pour les filles et les sœurs ayant utilisé une CO, est de 1,2, pour les nièces et les petites filles sous CO. Cette étude retrouvait aussi une augmentation du risque sous CO d autant plus importante que le nombre de cancers du sein dans les familles était élevé ou que la CO avait été prise avant 1975 (les contraceptifs étaient alors beaucoup plus dosés en œstrogènes). Très peu d études analysant l effet du traitement hormonal de la ménopause (THM) sur le risque familial de cancer du sein sont disponibles dans la littérature. Dans une méta-analyse, le THM ne semblait pas conférer d augmentation supplémentaire du risque familial, mais il ne s agissait pas de femmes présentant une mutation caractérisée (Lasset et Bonadona, 2001). Dans l étude de Rebbeck, portant sur une petite cohorte de femmes portant une mutation du gène BRCA1 qui ont subi 57
74 Chapitre I Description de la glande mammaire une ovariectomie prophylactique, le THM ne semblait pas augmenter le risque de cancer du sein après l intervention (Rebbeck et al., 1999). Les œstrogènes endogènes, font que les facteurs de la vie reproductive de la femme, tels que l âge de la puberté et de la ménopause, la parité, l âge de la première grossesse menée à terme, pourraient influencer le risque de cancer du sein dans les formes familiales. Dans certaines études, les femmes porteuses d une mutation de BRCA1 qui ont eu un enfant (en particulier avant 30 ans) ont plus de risque de développer un cancer du sein que les femmes nullipares (Jernstrom et al., 1999). Ainsi, Jernstrom rapporte qu une grossesse pourrait augmenter le risque de cancer du sein avant 40 ans chez les femmes génétiquement prédisposées, et que chaque grossesse successive augmente le risque de cancer du sein par rapport aux femmes nullipares. D autre part, Johannsson (Johannsson et al., 1998) trouve que le risque d avoir un cancer du sein associé à une grossesse (c est-à-dire au cours de la grossesse ou l année qui suit) est plus élevé en cas de mutation du gène BRCA1. Dans l étude de Rebbeck 2001, les femmes nullipares porteuses d une mutation des gènes BRCA1 ou 2, mais aussi celles qui avaient eu une première grossesse après 30 ans, semblaient avoir un risque de cancer du sein augmenté (Rebbeck et al., 2001). La multiplicité des facteurs confondants et l hétérogénéité des mutations étudiées sont peut-être en partie à l origine de ces discordances. Il serait donc prématuré de conseiller les femmes génétiquement prédisposées sur le risque lié à la grossesse. Une attitude de prudence consiste à mettre en place une surveillance mammaire pendant et au décours d une grossesse chez ces femmes. Alors qu un index de masse corporelle (IMC) élevé à l âge de 12 ans n est pas un facteur de risque indépendant de cancer du sein sporadique, un IMC élevé à l âge de 12 ans dont on connaît l association à un taux élevé d œstrogène circulant augmente d un facteur 4 le risque de cancer du sein chez les femmes ayant des antécédents familiaux évocateurs d une prédisposition génétique (Grabrick et al., 1999). La progestérone aide à l implantation de l embryon, soutient et épaissit l endomètre. En outre, la progestérone stimule le développement des glandes mammaires impliquées dans la production du lait. La 58
75 Chapitre I Description de la glande mammaire progestérone semble également jouer un rôle dans la suppression de la réponse immunologique de la mère aux antigènes du fœtus. La progestérone est produite par le corps jaune au stade précoce de la grossesse (Pujol et al., 1998). Vers la 7 ème semaine de grossesse, la progestérone est produite à la fois par le corps jaune et le placenta. Vers la 12 ème semaine, la sécrétion de la progestérone est entièrement prise en charge par le placenta. A la fin de la grossesse, la progestérone semble jouer un rôle dans l accouchement, le processus de la naissance. La progestérone provoque la croissance des lobules (acini) dans la seconde partie du cycle menstruel. L action anti-œstrogène de la progestérone est bien documentée, notamment son action sur la synthèse du récepteur de l œstradiol, laquelle a été démontrée dans le tissu mammaire humain l activité enzymatique du 17 β-hydroxystéroïde déshydrogénase qui converti l œstradiol en œstrone entraînant ainsi une diminution d activité biologique de l œstrogène dans le récepteur mammaire, en physiologie humaine, l existence d une fonction ovarienne cyclique de bonne qualité est donc nécessaire à la réalisation d une eutrophie mammaire adéquate en permettant le développement et l organisation de l arbre galactophore et de ses terminaisons acineuses ainsi que du tissu conjonctif et graisseux adjacent (Mauriac et al., 1986). 9. Autres hormones 9.1. Prolactine La différenciation adéquate et complète du système galactophore, en particulier de sa terminaison intralobulaire, implique l action successive et parfaitement coordonnée de l œstradiol, de la progestérone, puis de la prolactine (Mauriac et al., 1986). L œstradiol est une hormone initialement responsable du développement et de la différenciation de l épithélium galactophorique en augmentant l activité mitotique des cellules cylindriques et des couches cellulaires internes du galactophore. La progestérone pour sa part en synergie avec l œstradiol agit sur la partie terminale du galactophore en permettant sa différenciation en acinus, elle permet ainsi l organisation de la glande mammaire en un système sécrétoire, cette sécrétion ne devient elle même effective que lorsque la prolactine est sécrétée (Day, 2001). Une telle séquence est notamment observée en cas de grossesse, et plutôt cette grossesse surviendra, plus vite la différenciation cellulaire sera obtenue. 59
76 Chapitre I Description de la glande mammaire 9.2. Insuline, IGF-1 Le taux d incidence des cancers du sein, beaucoup plus élevé dans les pays riches, est à relier au mode de vie caractérisé par une faible activité physique, une alimentation riche en graisses totales et saturées, en hydrates de carbone raffinés et en protéines animales. Les études de cohortes ont montré une augmentation du risque de cancer du sein chez les femmes ménopausées qui présentent un profil endocrinien de type hyperandrogénique modéré. Ce profil est souvent associé à une hyperinsulinémie chronique, souvent elle-même induite par une obésité et une insulinorésistance associée. Cette hyperinsulinémie est liée à une diminution des taux plasmatiques des protéines de liaison et peut augmenter la biodisponibilité de l IGF-1 au niveau des tissus cibles. Comme l insuline, l IGF-1 inhibe la production hépatique des protéines de liaison des hormones sexuelles et stimule la production ovarienne de stéroïdes. De plus l IGF-1 peut stimuler directement le développement de tumeurs mammaires (Key, 2003). L ensemble de ces observations a conduit à l hypothèse d un risque accru de cancer du sein chez les femmes qui présentent les caractéristiques suivantes : une augmentation des taux plasmatiques d insuline à jeun, une augmentation des taux d IGF-1 pour des niveaux donnés des protéines de transport. L hyperinsulinémie et/ou l augmentation des taux plasmatiques d IGF-1 biodisponible, non lié aux protéines de transport, pourraient constituer le lien physiologique entre le mode de vie occidental, la suralimentation, le profil en hormone stéroïde de type hyperandrogène et l augmentation du risque de cancer du sein (Baulieu et al., 2003). Le tableau 3 résume les effets majeurs sur les tissus mammaires induits par les hormones, par leurs actions directes et indirectes (Gorins, 1978). 60
77 Chapitre I Description de la glande mammaire Hormone Action hormonale Croissance des galactophores ; Elévation de l activité mitotique ; Croissance du mamelon ; Œstrogènes Pigmentation de l aréole ; A forte doses : action sur les acini ; Augmentation de la vascularisation du stroma conjonctif et de la perméabilité capillaire. N agit qu en synergie avec les œstrogènes ; Bloque le cycle des mitoses épithéliales provoquées par les progestérone Hormones hypophysaires œstrogènes ; Développe les acini ; A forte doses seules : action variable sur les acini et même les galactophores. Indirecte Métabolisme hydrocarboné : insuline Ovaires : FSH et LH Surrénales : ACTH Thyroïde : TSH Directe Prolactine : développement des acini ; lactogenèse (les œstrogènes stimulent la sécrétion de la prolactine mais possède vis-à-vis d elle une action inhibitrice sur la glande mammaire). Tableau 3 : Action hormonale sur la glande mammaire (Gorins, 1978). 61
78 Chapitre II Pathologies et classification des lésions mammaires De nombreux médecins ont étudié au cours des siècles, le cancer du sein, Celse Aulus Cornelius, cent ans avant Jésus-Christ, fait dans son traité une description clinique du cancer du sein qui est une tumeur irrégulière avec une nette augmentation de la vascularisation veineuses, il distingue quatre étapes : une première étape précoce tumorale pure, une deuxième étape sans ulcération, une troisième étape avec ulcération, une quatrième étape avec un stade de diffusion. Le sein constitue un ensemble extrêmement complexe, encore imparfaitement classé, de nombreuses affections pourvues d étiquettes distinctes souvent mal délimitées, et les cas intermédiaires sont nombreux (Goumont et al., 1993). 1. Les maladies bénignes du sein Plusieurs maladies sont connues parmi elles : la mastalgie est une douleur aux seins qui est généralement bilatérale. Il semble que 70% des femmes souffriront de mastalgie au cours de leur vie. On distingue des douleurs mammaires cycliques, non cycliques ou musculo-squelettiques. Les femmes souffrant de mastalgie cyclique sévère sont souvent pré-ménopausées, nullipares ou primipare d âge précoce. La mastalgie non cyclique peut être associée à des lésions bénignes, comme des lésions fibrokystiques, les fibroadénomes et l ectasie canalaire. Dans aucun de ces cas, le sein n est sensible à la palpation. De nombreux facteurs peuvent influencer la mastalgie : le régime alimentaire, les taux de prolactine et la rétention d eau. Il y aurait deux causes principales à la douleur mammaire : l une hormonale (cyclique) et l autre inflammatoire (plutôt constante). La mastalgie n est généralement pas associée à des affections malignes. Cependant, un faible pourcentage peut être dû à un cancer du sein (Wheater et al., 1985) ; la maladie fibrokystique (MFK) se manifeste par la présence d une nodosité (petite masse) associée à des douleurs ou à une sensibilité des seins. Elle est le plus souvent responsable des masses au sein et des consultations pour une affection mammaire chez les femmes pré-ménopausées. La MFK affecte surtout les femmes de 30 à 55 ans. La MFK se déclare par un ou plusieurs kystes formés d une poche remplie de liquide, de consistance et de taille variables, mobile, lisse, 62
79 Chapitre II Pathologies et classification des lésions mammaires discrète qui peut être sensible et ferme à la palpation. Les causes probables de la MFK sont les facteurs hormonaux et alimentaires (notamment la caféine et les médicaments). Certains facteurs qui prédisposent à la MFK sont la nulliparité, des avortements spontanés, le fait de ne pas prendre de contraceptifs oraux, une ménopause tardive et un statut socio-économique élevé. La majorité des femmes atteintes de MFK ne courent pas un risque accru de cancer du sein. Néanmoins, il faut rester vigilante (Holland et al., 2000) ; Le fibroadénome est une lésion bénigne courante du sein. Il forme un nodule arrondi ou lobulé, unique ou multiple, discret, indolore, mobile et mesure généralement de 1 à 5 cm de diamètre. Il affecte en particulier les femmes de 20 à 30 ans. Contrairement aux tumeurs cancéreuses, les fibroadénomes se développent à partir d un lobule unique et non d une cellule unique. Ils résultent d une aberration du processus normal de développement des lobules. Il est rare que les fibroadénomes deviennent agressifs. Bien qu ils soient jugés bénins, la présence de tissu canalaire indique qu une dégénérescence maligne est possible ; l écoulement mammelonaire se manifeste par l apparition, à la surface du mamelon, de sécrétions d un ou de plusieurs galactophores (canaux mammaires). L écoulement mammelonaire n est pas rare. Il est signalé par environ 3 à 10% des femmes se plaignant de symptômes mammaires. C est une manifestation plus ou moins normale du sein, comme la majorité des écoulements bilatéraux causés par l ectasie canalaire (dilatation des canaux). Certains médicaments peuvent provoquer une galactorrhée (sécrétion spontanée résultant d une stimulation de la glande mammaire par une hormone, la prolactine). Un écoulement mammelonaire unicanalaire peut être associé à des mastopathies bénignes, dont le papillome intracanalaire, la maladie fibrokystique, la papillomatose et les infections sous-aréolaires. Il arrive parfois qu un écoulement mammelonaire constitue la manifestation initiale d un cancer du sein. L écoulement mammelonaire peut être associé à un cancer du sein ou à des lésions précancéreuses. Dans 4 à 12% des cas, l écoulement mammelonaire spontané, sanglant et unilatéral est associé à un cancer (Wheater et al., 1985) ; 63
80 Chapitre II Pathologies et classification des lésions mammaires les infections, inflammations et abcès, sont un état pathologique, liée à la présence de bactéries occasionnant des inflammations ou même des abcès (accumulation de pus). Les tumeurs bénignes sont bien limitées et leur croissance est purement locale. Les tumeurs malignes (cancer) tendent à infiltrer et détruire les tissus adjacents (envahissement). La dissémination des cellules néoplasiques malignes à distance du foyer initial (tumeur primitive), est une deuxième caractéristique des tumeurs malignes. L essaimage de ces cellules s effectue via les vaisseaux lymphatiques et/ou sanguins. Ces cellules à distance du foyer initial forme des foyers distincts qui croissent en tumeurs secondaires encore appelées métastases. En principe, le développement d une tumeur bénigne est souvent inoffensif alors que les tumeurs malignes peuvent entraîner le décès du patient en infiltrant et en détruisant certains organes vitaux (Wheater et al.,1985). 2. Les cancers mammaires Le cancer du sein est une prolifération de cellules anormales au niveau de la glande mammaire, prolifération qui aboutira à la formation d une masse ou tumeur maligne. Suivant que les cellules cancéreuses se développent dans les canaux ou dans les lobules, on parlera de cancers canalaires (le plus fréquent) ou de cancers lobulaires. Lorsque les cancers restent limités à l intérieur des canaux ou des lobules, on parle de cancers in situ. A ce stade, les cancers peuvent encore régresser spontanément dans un certain nombre de cas. Lorsque les cellules cancéreuses infiltrent les tissus autour des canaux ou des lobules, on parle de cancers infiltrants Le cancer in situ Des tumeurs non infiltrantes peuvent présenter des cellules d allures agressives et malignes (caractéristiques cytologiques de malignité) avec pléiomorphisme cellulaire et augmentation de l activité mitotique. Cette situation est souvent rencontrée dans les tissus épithéliaux, cellules de recouvrement des canaux galactophores et des acini. Ces tumeurs répondent à la définition de cancer in situ : cellules d allures malignes mais absence d envahissement des tissus voisins et 64
81 Chapitre II Pathologies et classification des lésions mammaires respect de la membrane basale, membrane délimitant la face externe de l épithélium des canaux galactophores et des acini (Peltier et Guinebretière, 1998). Lorsque les cellules cytologiquement malignes sont confinées aux canaux galactophores, on parle d épithélioma canalaire in situ encore appelé adénocarcinome intra-canalaire et lorsque les cellules malignes sont confinées aux lobules on parle d épithélioma lobulaire in situ ou d adénocarcinome intra-lobulaire. Le diagnostic des cancers in situ est important car ces tumeurs peuvent devenir infiltrantes (fig. 8) (Kopans, 1998), mais un traitement à un stade pré-invasif permet généralement une guérison définitive. Figure 8 : Passage d un Cancer Canalaire In Situ au stade d évolution infiltrant (Kopans, 1998) Carcinome Canalaire In Situ (CCIS) Le carcinome canalaire in situ (CCIS) se définit comme une prolifération de cellules épithéliales, cytologiquement malignes, confinées à l intérieur de l arbre galactophorique. Il se distingue du carcinome infiltrant par l absence d effraction de la membrane basale et d envahissement du conjonctif (fig. 9) (Wheater et al., 1985). La classification OMS 1981 du CCIS est fondée sur l architecture des lésions. On distingue 4 types architecturaux : massif, en comédons, papillaire et cribriforme. Cette classification s est révélée peu satisfaisante en raison de l absence de signification clinique de ces différents types architecturaux. Il est récemment apparu que les lésions constituées de cellules de grade nucléaire élevé étaient plus agressives. Bien qu il n y ait pas de consensus actuel sur la meilleure façon de classer 65
82 Chapitre II Pathologies et classification des lésions mammaires les CCIS. Le rapport des anatomopathologistes du groupe de travail est basé sur le grade nucléaire et dérive de celle décrite par Holland et al., (2000) : CCIS de haut grade nucléaire Il se compose de cellules dont les noyaux présentent d importantes atypies cytonucléaires. Les mitoses sont fréquentes. Le type architectural est variable. Il est souvent centré par des comédons de nécrose qui contiennent fréquemment des dépôts calciques amorphes. Les cellules bordant les espaces intercellulaires sont rarement polarisées CCIS de bas grade nucléaire Il est composé de cellules monomorphes, au noyau arrondi, souvent de petite taille, les mitoses sont peu nombreuses. La nécrose est rare. Le type architectural cribriforme (prolifération intracanalaire creusée par de petites cavités rondes glanduliformes) est le plus courant. Les cellules sont polarisées CCIS de grade intermédiaire Certains CCIS n entrent pas dans une des deux catégories précédentes. La morphologie des noyaux est intermédiaire, entre celle observée dans le CCIS de haut grade et celle observée dans le CCIS de bas grade. L architecture est variable (solide, cribriforme ou micropapillaire) Type mixte Certains CCIS associent plusieurs sous types histologiques. La lésion sera classée selon le grade nucléaire le plus élevé (Types histologiques des Tumeurs du Sein. Genève : OMS, 1981). Le type histologique des cancers est un élément important pour la conduite thérapeutique et le pronostic. Les tumeurs malignes du sein les plus fréquentes sont des adénocarcinomes développés à partir des canaux galactophores et des lobules. Ils représentent 98% des tumeurs malignes du sein. De nombreuses classifications ont été proposées, la classification de l OMS (1981) est le plus souvent utilisée basée sur l aspect histologique. 66
83 Chapitre II Pathologies et classification des lésions mammaires Carcinome Lobulaire In Situ (CLIS) Le carcinome lobulaire in situ est un carcinome intéressant les canalicules intralobulaires qui sont comblés et distendus par une prolifération de cellules peu jointives, sans envahissement du tissu conjonctif voisin (fig. 10) (Wheater et al., 1985). Les cellules sont en général régulières et de taille petite ou modérée, avec un cytoplasme faiblement coloré et un noyau rond ne présentant que peu ou pas de mitoses. Cette lésion est souvent une découverte microscopique fortuite dans un fragment de tissu mammaire retiré pour une autre raison. Les localisations multiples ou bilatérales sont fréquentes. Le carcinome lobulaire in situ peut être associé à un carcinome lobulaire ou canalaire infiltrant. Figure 9 : Carcinome canalaire in situ. Coloration HE. Gr X40 (Wheater et al., 1985). 67
84 Chapitre II Pathologies et classification des lésions mammaires Figure 10 : Carcinome lobulaire in situ coloration HE. Gr X10 (Wheater et al., 1985) Mode d extension des tumeurs malignes invasives l envahissement local est caractérisé par des cellules qui gagnent de proche en proche les tissus contigus par la voie la plus directe ou de moindre résistance ; l extension par les lymphatiques des cellules néoplasiques gagnent via les vaisseaux lymphatiques les ganglions régionaux, on parle alors d adénopathie (ganglion anormal) métastatique de la région axillaire, sus claviculaire ou mammaire interne ; l extension par les veines des cellules néoplasiques qui gagnent ainsi la circulation générale peuvent atteindre n importe quel organe mais sont souvent retenues par les capillaires du poumon où elles forment des métastases pulmonaires (fig. 11) (Peltier et Guinebretière, 1998). 68
85 Chapitre II Pathologies et classification des lésions mammaires Lorsque les cellules franchissent la membrane délimitant le canal ou le lobule, le cancer est dit «invasif» ou «infiltrant» comme il est clairement schématisé dans la figure 11 pour les canalaires et la figure 12 pour les lobulaires (Peltier et Guinebretière, 1998 ; Fournie, 2000). Les cellules cancéreuses peuvent alors passer dans les vaisseaux lymphatiques. Ces vaisseaux se dirigent vers les ganglions de l aisselle, qui constituent un obstacle à la dissémination de la tumeur. Figure 11 : Evolution d un carcinome canalaire et métastases (Peltier Guinebretière, 1998). 69
86 Chapitre II Pathologies et classification des lésions mammaires Figure 12 : Passage d un carcinome lobulaire in situ au stade d évolution de cancer invasif (Peltier et Guinebretière, 1998). 70
87 Chapitre II Pathologies et classification des lésions mammaires Carcinome Canalaire Infiltrant (CCI) Le type histologique du carcinome infiltrant a une valeur pronostique reconnue. C est la forme la plus fréquente des tumeurs malignes du sein. Ce groupe comprend les carcinomes infiltrants qui ne peuvent être classés dans une des variétés dites particulières. Les cellules tumorales se disposent généralement en îlots, en travées ou en formations glanduliformes. Carcinome canalaire infiltrant avec composante intracanalaire prédominante Il s agit d un carcinome essentiellement intracanalaire présentant des foyers d infiltration du tissu conjonctif. La classification de l OMS propose de réserver cette dénomination aux cas où la proportion de carcinome intra-canalaire est au moins 4 fois plus importante que celle de la composante infiltrante. Le carcinome microinvasif doit être séparé du CCI avec composante canalaire prédominante. Il est défini comme une tumeur constituée de façon prédominante par un CCIS mais dans lequel existe un ou plusieurs petits foyers infiltrants dont le diamètre n excède pas 1 mm. Cette définition étant très restrictive, les cas qui répondent à ces critères sont rares. La micro-invasion est le plus souvent associée au CCIS de haut grade nucléaire (RED, 1996) Carcinome Lobulaire Infiltrant (CLI) Le carcinome lobulaire infiltrant se compose de petites cellules régulières identiques à celles observées dans la forme lobulaire in situ. Classiquement les cellules sont dissociées les unes des autres, ou agencées en fines travées avec des aspects en file indienne ou en cible autour des galactophores non atteints. L identification de reliquats de carcinome lobulaire in situ aide au diagnostic. Carcinome mucineux Cette tumeur également nommée carcinome mucoïde ou colloïde, est un carcinome riche en mucus épithélial extracellulaire en quantité suffisante pour être visible macroscopiquement. Elle se caractérise par de petits îlots de cellules uniformes noyés dans une grande quantité de mucus extracellulaire. 71
88 Chapitre II Pathologies et classification des lésions mammaires Carcinome médullaire (à stroma lymphoïde) Ces tumeurs rares sont constituées de plages syncytiales de grandes cellules pléiomorphes (plages de cellules à limites cytoplasmiques indistinctes), à noyau vésiculeux et à nucléole proéminent. Le stroma souvent peu abondant contient toujours un grand nombre de cellules lymphoïdes. Les contours de la tumeur sont bien limités. Pour être classé en médullaire, l ensemble de la tumeur doit présenter ces caractéristiques. Malgré le faible degré de différenciation et le nombre élevé de mitoses, ces tumeurs paraissent avoir un pronostic plus favorable que celui des carcinomes canalaires infiltrants. Carcinome papillaire C est un carcinome rare dont l architecture infiltrante est surtout faite de structures papillaires. Il est de pronostic favorable. Carcinome tubuleux Les carcinomes tubuleux sont très bien différenciés. Les cellules sont régulières et disposées en tubules bien structurés, typiquement faits d une seule couche cellulaire et entourées d un abondant stroma fibreux. Le carcinome tubuleux est de pronostic favorable. Carcinome adénoïde kystique, mais aussi les Carcinomes sécrétants (juvénile), Carcinome apocrine, Carcinome métaplasique, et autres variétés (carcinome riche en lipides, carcinome à petites cellules, carcinome à cellules en bague à chaton, etc..). Ces variétés de carcinomes sont beaucoup plus rares et ont parfois des pronostics meilleurs que le CCI (carcinome adénoïde kystique et carcinome sécrétant) Maladie de Paget du mamelon C est une lésion dans laquelle de grandes cellules peu colorées apparaissent dans l épiderme du mamelon, essentiellement dans sa moitié profonde. Ces cellules contiennent de la mucine. La maladie de Paget du mamelon est presque invariablement associé à un carcinome intracanalaire et moins souvent à un 72
89 Chapitre II Pathologies et classification des lésions mammaires carcinome infiltrant. Il s agirait alors d une dissémination à l épiderme du mamelon du carcinome glandulaire sous-jacent (Milerom, 1980) Les tumeurs phyllode du sein Le terme de tumeurs phyllode (TP) est recommandé par l OMS en 1981, qui souligne le caractère commun à toutes ces lésions sans préciser le caractère bénin ou malin des structures, ni suggérer le potentiel évolutif. La TP est une tumeur bien circonscrite, présentant une structure foliaire, constitué de tissu conjonctif et d éléments épithéliaux analogues à ceux d un fibroadénome, mais caractérisé par une plus grande cellularité du tissu conjonctif. Il peut exister des foyers myxoïdes, adipeux, osseux, et choroïdiens. Il s agit en général d une grosse tumeur, mais la taille à elle seule n est pas un élément diagnostic (OMS, 1981). Il est utile de distinguer trois catégories : bénin, limite ou «Border-Line», Malin, en fonction des critères suivants : fréquence des mitose, caractères infiltrant en périphérie, atypies cellulaire et degré de cellularité. 3. Classifications des cancers mammaires 3.1. Classification des lésions pré-invasives et des carcinomes in situ Les pathologistes sont actuellement confrontés au spectre des lésions canalaires et lobulaires pré-invasives mammaires depuis la généralisation du dépistage mammographique. Les proliférations épithéliales intracanalaires sont actuellement classées en trois groupes : Hyperplasie Canalaire Simple (HCS) Les tumeurs les plus agressives pourraient avoir les HCS comme origine mais elles ne sont pas précurseurs direct de cancers invasifs, le risque relatif est de 1,5 à 2. Hyperplasie Canalaire Atypique (HCA) Elle constitue un facteur de risque relatif de 4 à 5, de 6 pour les femmes pré ménopausées et de 10 en cas d antécédent familial, 22% des femmes porteuses d HCA développeront un cancer invasif dans un délai de 8,3 ans (Pinder et Ellis, 2003). 73
90 Chapitre II Pathologies et classification des lésions mammaires Carcinome Canalair In Situ (CCIS) Il représente 15 à 20% des carcinomes mammaires, la mortalité due au CCIS est faible. La classification des CCIS dépend de l aspect architectural, cytonucléaire et la présence ou non de nécrose, le consensus privilégie une classification en trois grades : Grade I : population cellulaire dotée de noyaux monomorphes, à chromatine fine et sans nucléole ; Grade II : grade intermédiaire, présence de nécrose ; Grade III : le haut grade présentant un important pleiomorphisme nucléaire avec des nucléoles et des nécroses (Arnold et al., 2003). Une nouvelle entité est récemment introduite «Atypie Epithéliale Plane» (AEP) appelée aussi Métaplasie cylindrique atypique intégrée entre les HCS et HCA, les AEP surviennent surtout dans l arbre ductolobulaire. L aspect cellulaire des lésions pour le diagnostic est représenté dans le tableau 4 (Sigal-Zafrani et al., 2004). 74
91 Chapitre II Pathologies et classification des lésions mammaires Caractérisations histologiques Cellules Cohésion intercellulaire Expression de la E- cadherine Carcinome Canalaire in situ CCIS de bas grade : taille moyenne, bas grade nucléaire. CCIS de grade intermédiaire : taille moyenne, grade nucléaire intermédiaire. Généralement bonne, constante Néoplasie lobulaire in situ Forme classique : petites, arrondies avec un noyau finement granuleux, des nucléoles peu apparents et un rapport nucléo-cytoplasmique élevé Forme variante pléomorphe : grade nucléaire élevé. Absente Absente dans la majorité des cas. Si présente, faible. Architecture Variable Solide Lumières intra cytoplasmiques Extension pagétoïde dans les canaux inter lobulaire Rares Fréquente Généralement absente Souvent présente Nécrose Peu fréquente Habituellement absente Mitoses Peu fréquentes Peu fréquentes Mitoses anormales Rares Rares Tableau 4 : Classification prise en considération pour le diagnostic (Sigal-Zafrani et al., 2004) Classification de Tavassoli L OMS en 1981 recommandait la classification en trois grades selon l aspect nucléaire. Cependant elle introduit une nouvelle classification proposée par Tavassoli, cette classification réserve le terme de carcinome pour les lésions invasives et préfère pour les lésions pré-invasives, la dénomination de Ductal Intra-epithelial Néoplasia (DIN). Elle regroupe l HCA et le CCIS de bas grade et fait apparaître les atypies épithéliales planes (Tavassoli, 1992). 75
92 Chapitre II Pathologies et classification des lésions mammaires Les lésions lobulaires Elles sont regroupées sous le terme de «Néoplasie Lobulaire» (NL), il est reconnu que ces lésions sont un indicateur de risque de cancer invasif. Son incidence varie de 0,5 à 3,8 des biopsies, et touchent les femmes de 40 à 50 ans, ils surviennent environ 10 ans plutôt que les CCIS, les lésions lobulaires sont multifocales dans 50% des cas, et bilatérales dans 30% des cas. Histopathologiquement les NL sont définies par une prolifération cellulaire monomorphes siégeant dans les unités ductulobulaires terminales, on distingue : NL de type A : les cellules sont rondes et petites, le rapport nucléo-cytoplasmique est élevé, les noyaux sont ronds à chromatine homogène sans nucléole visible, les mitoses et nécroses sont rares. Il existe une perte de la cohésion cellulaire, la prolifération comble partiellement ou complètement les acini et peut les distendre. L architecture glandulaire est respectée ; NL de type B : les noyaux sont plus volumineux, et on a décrit des cellules en forme de bague à chaton ; NL en forme pléimorphique : caractérisée par des atypies cytonucléaires plus marquées, avec des noyaux très volumineux souvent nucléolés, associés à des mitoses et des nécroses (Hammond et al., 2003). La forme pléimorphique et en bague à chaton sont plus agressives et méritent d être mentionnées. Certains auteurs proposent de différencier entre HLA et CLIS, ces deux entités ont une définition histologique distincte et un risque de survenue du cancer invasif différent : CLIS : lorsque plus de la moitié des acini d une unité est comblée et distendue par des cellules néoplasiques, le diagnostic CLIS peut être porté ; HLA : si les acini sont en partie envahis, non ou peu distendus, avec une lumière encore visible, ou si moins de la moitié des acini sont envahis, le diagnostic HLA peut être porté. 76
93 Chapitre II Pathologies et classification des lésions mammaires Tavassoli et al ont proposé une classification LIN (Lobural Intra-Epithelial Neoplasia) divisée en trois grades : LIN 1 : correspond aux lésions HLA sans distension des acini ; LIN 2 : correspond aux lésions HLA avec distension des acini ou aux lésions CLIS ; LIN 3 : correspond à des entités particulières comme le type pleiomorphe, les lésions faites de cellules en bague à chaton et celles avec une nécrose. Pour Tavassoli, le risque de survenue de cancer invasif augmente avec le grade ainsi, LIN 3 sont les plus agressifs et souvent déjà associés à un carcinome infiltrant (Tavassoli et al., 2003) Classification selon le grade histologique (SBR = Scarff - Bloom et Richardson) Le rôle du grade histopronostic est maintenant largement admis pour les tumeurs carcinomateuses infiltrantes, le système le plus utilisé étant le grade de Scarff Bloom Richardson (SBR).La méthode du grading SBR consiste à évaluer 3 paramètres morphologiques avec des scores d Elston Ellis (tableau 5) : degré de différenciation (formation de tubules/cavités glandulaires) ; pléomorphisme nucléaire ; index mitotique. Un score allant de 1 à 3 est attribué à chacun de ces paramètres. Le grade SBR résulte de l addition de ces scores. Il est actuellement recommandé de ne pas limiter l évaluation du grade aux carcinomes canalaires infiltrants mais de l effectuer pour tous les sous types histologiques et cela pour 2 raisons principales : il est parfois difficile de déterminer le type de tumeur (canalaire ou autre) ; il peut y avoir des variations morphologiques importantes dans certains sous types histologiques (tableau 5). 77
94 Chapitre II Pathologies et classification des lésions mammaires Différentiation Tubulo-Glandulaire Pléomorphisme nucléaire Index mitotique (10 champs : G 40 X) Score 1 Score 2 Score 3 Moyennement différencié (10-75) Bien différencié plus de 75% de tumeurs) Noyaux petits, uniformes à contours réguliers. Noyaux plus grands que la normale. Nucléoles bien visibles. Faible ou absente (<10%) Pléomorphisme marqué (Noyaux vésiculeux, nucléole proéminent). < 10 mitoses plus de 22 mitoses Tableau 5 : Le grading histopronostic d Elston Ellis (Index de Nottingam). Les différents scores sont additionnés pour obtenir le grade histologique global : Grade I score 3 5 Grade II score 6 7 Grade III score Classification TNM internationale Cette classification permet de distinguer des formes : non Chirurgicales (33%) : formes métastatiques (M), inflammatoires (T4d), non métastatiques et non inflammatoires avec adénopathies homolatérale fixée (N2) (tableau 6). chirurgicales (70%) : T1, T2, T3, T4 avec N0 ou N1 et M0. La taille histologique est un facteur pronostic important surtout pour les tumeurs de moins de 1 cm dont le pronostic est excellent. Cependant quelque soit le statut ganglionnaire, la survie est corrélée à la taille tumorale (tableau 7) (Haagensen, 1971) Classification en stade Le stade d une maladie cancéreuse se définie par la présence ou non de ganglions malins et de métastases. La classification en stade permet de mieux définir une stratégie thérapeutique (fig. 13) (Hammond et al., 2003). 78
95 Chapitre II Pathologies et classification des lésions mammaires Tx : aucune information sur la tumeur ; T0 : absence de tumeur primitive ; Tis : cancer in-situ ; T1 : tumeur inférieure à 2 cm ; T2 : tumeur de 2 à 5 cm ; T : Tumeur primitive T3 : tumeur supérieure à 5 cm ; T4a : tumeur étendue à la paroi thoracique (quelle que soit sa taille) ; T4b : tumeur étendue à la peau (œdème, ulcération) ; T4c : T4a + T4b ; T4d : cancer inflammatoire. Nx : aucune information sur les adénopathies ; N0 : pas d adénopathies ; N : Adénopathies régionales N1 : adénopathie homolatérale mobile ; N2 : adénopathie homolatérale fixée ; N3 : adénopathie mammaire interne homolatérale Mx : aucune information sur les métastases ; M : Métastases M0 : pas de métastases ; M1 : métastases à distance (y compris adénopathie sus-claviculaire). Tableau 6 : Classification TNM des cancers mammaires. Taille de la tumeur (cm) Survie à 10 ans (en %) < 2 cm 75 2 à 3 cm 67 4 à 5 cm 46 > 6 cm 41 Tableau 7 : Relation entre la taille de la tumeur et la survie de 10 ans (Haagensen, 1971). 79
96 Chapitre II Pathologies et classification des lésions mammaires Les tumeurs mesurent 2 cm ou moins ; Aucune atteinte des ganglions Les tumeurs mesurent plus de 2 cm et 5 cm ou moins ; Les ganglions lymphatiques sont parfois touchés ; Le cancer s est propagé aux ganglions lymphatiques situés dans l aisselle. Le cancer du sein de stade III est le point de départ du cancer du sein avancé. Il se subdivise en cancers du sein de stade IIIa et stade IIIb. Cancer avancé, dont les cellules se sont propagées (métastasées) vers d autres régions de l organisme, le plus souvent aux poumons, au cerveau, aux os ou au foie. Figure 13 : Classification en stade du cancer du sein (Hammond et al., 2003). 80
97 Chapitre II Pathologies et classification des lésions mammaires 4. Mécanismes de déclenchement tumorale La cellule est régie par une multitude de gènes dont le rôle principal est de maintenir l intégrité du génome et de contrôler la prolifération. La mutation de certains de ces gènes entraîne une instabilité génétique menant à la dysfonction de la cellule et à sa transformation en cellule tumorale. Plusieurs facteurs peuvent être impliqués dans le passage d une cellule saine vers un état malin. On peut les regrouper en 6 catégories soit l activation de signaux de croissance et des oncogènes, l inhibition des signaux anti-prolifératifs, l inhibition de l apoptose, l immortalisation cellulaire, l activation de l angiogenèse et l invasion des tissus par les métastases (Hanahan et Weinberg, 2000). La première étape de cancérisation est une phase d initiation. Elle se caractérise par une accumulation de mutations qui ont pour conséquence une surexpression des facteurs pro-oncogéniques. Les cellules sont génétiquement anormales mais toujours contrôlées par l environnement cellulaire via les jonctions serrées (gap-junction). Lorsque les cellules entrent dans la seconde étape dite de promotion, elles acquièrent leur indépendance vis-à-vis des facteurs de croissance grâce aux protooncogènes, et perdent leur capacité de communication intercellulaire. Cette acquisition d indépendance peut se faire de plusieurs manières : soit la cellule est capable de synthétiser elle-même un certains nombre de facteurs, on parle alors de contrôle autocrine notamment avec une augmentation de la synthèse et une surexpression d «Insuline Growth Factor» (IGF), d «Epithelial Growth Factor» (EGF) ou encore TGF-α ; soit il y a une surexpression des récepteurs transducteurs de signaux comme par exemple c-erb B2, le récepteur de l EGF (Fedi et al., 2000). soit la cellule surexprime des facteurs de transcription, par exemple le prooncogène c-myc. Dans la cellule normale, il forme un dimère avec la protéine Max et induit la prolifération cellulaire. Ce stimulus est régulé dans les conditions physiologiques par le complexe Mad-Max. En cas de surexpression de c-myc, le complexe Myc-Max est favorisé au dépend de 81
98 Chapitre II Pathologies et classification des lésions mammaires Mad-Max ce qui entraîne une prolifération cellulaire non régulée (Turner, 2000a). Les mécanismes de cancérisation sont aussi provoqués par la perte d un certain nombre de contrôle sur la croissance cellulaire, avec notamment des pertes de fonctionnalité des anti-oncogènes Activation des signaux de croissance Les cellules normales dépendent de la présence de signaux de croissance pour passer du stade de quiescence à la prolifération. Ces signaux sont captés par les récepteurs transmembranaires et proviennent soit de facteurs de croissance, soit des composantes de la matrice extracellulaire, soit de molécules d interaction et d adhésion entre les cellules. Pour entrer dans un stade de prolifération, la cellule doit donc recevoir des signaux exogènes (Hanahan et Weinberg, 2000). Les cellules cancéreuses quant à elles ont acquis une certaine indépendance face aux signaux extérieurs. En effet, elles produisent leurs propres signaux de croissance pour lesquels elles sont sensibles créant ainsi une stimulation autocrine (Fedi et al., 2000). Il a d ailleurs été démontré que plusieurs oncogènes pouvaient imiter ces signaux, promouvant ainsi la prolifération cellulaire (Hanahan et Weinberg, 2000). Les cellules malignes peuvent agir également à deux autres niveaux pour acquérir une autonomie face aux signaux de croissance, soit au niveau des récepteurs liant ces signaux, soit sur le cheminement de ces signaux à l intérieur de la cellule. Tout gène cellulaire, appelé proto-oncogène (c-onc), susceptible de devenir, par suite d une modification qualitative ou quantitative, un gène transformant (fig. 14) (Hanahan et Weinberg, 2000), c est-à-dire un gène capable de conférer expérimentalement le phénotype cancéreux (transformation) à une cellule normale eucaryote (Turner, 2000a). L altération d un allèle est suffisante pour entraîner une activation anormale. Les oncogènes sont répartis en 6 grandes classes en fonction des oncoprotéines pour lesquels ils codent : 82
99 Chapitre II Pathologies et classification des lésions mammaires les facteurs de croissance (assurent une boucle de régulation autocrine), comme le proto-oncogènes codant pour les protéines de la famille FGF (fibroblast growth factor) ; les récepteurs transmembranaires de facteurs de croissance comme le proto-oncogène erb B qui code pour le récepteur à l EGF (epidermal growth factor) ; les G-protéines ou protéines membranaires liant le GTP, la molécule la plus étudiée est la protéine p21 ras (Rous avian sarcoma). Les oncogènes ras portent des mutations au niveau des aminoacides 12, 13 et 51, correspondant à la région liant le phosphore du site de liaison avec le nucléotide. L activité GTPase est perdue, et il existe une accumulation de la protéine p21 ras sous forme active liée au GTP ; les tyrosines protéine-kinases membranaires ; les protéine-kinases cytosoliques ; les protéines à activité nucléaire contrôlent la transcription de gènes cibles en interagissant avec l ADN comme le proto-oncogène erba codant pour le récepteur aux hormones thyroïdiennes, les proto-oncogènes fos, jun et c- myc (Turner, 2000b). Figure 14: Transformation de proto-oncogènes qui codent pour les protéines de cellules normales en oncogènes (Hanahan et Weinberg, 2000). 83
100 Chapitre II Pathologies et classification des lésions mammaires La version normale du gène (proto-oncogène) est mutée, donc celui-ci est suractivé par : la mutation ponctuelle aura lieu dans une séquence codante pour un proto-oncogène aboutissant à une modification fonctionnelle de l oncoprotéine. Les mutations faux-sens entraînant la substitution d un acide aminé par un autre, sont capables (Turner, 2000a) d activer des proto-oncogènes en oncogènes, en touchant par exemple un site catalytique ou en entraînant une activation substitutive de la protéine, telle une mutation faux-sens et activation de la famille ras aboutissant à un blocage en conformation active, liée au GTP ; les délétions, qui aboutissent le plus souvent à une perte de fonction, peuvent parfois entraîner une activation anormale si elles touchent une région régulatrice (Hill, 1997). L activation du proto-oncogène erb B qui code pour le récepteur à l EGF peut résulter de la délétion de la partie extra-membranaire et le domaine kinase intracytoplasmique est alors actif de façon constitutive ; Réarrangement structural, des altérations chromosomiques (translocations, inversions ) peuvent avoir pour conséquence moléculaire, la formation d un gène hybride généré par la fusion de régions codantes entraînant la synthèse de protéines chimériques non fonctionnelles (Hill, 1997). Codant pour une oncoprotéine : les protooncogènes, lors de translocations chromosomiques, peuvent être déconnectés de leur environnement moléculaire normal et placés sous le contrôle inapproprié d autres séquences à l origine d une modification de leur expression (Turner, 2000a) ; amplification génique correspond à une augmentation anormale du nombre de copies du gène dans la cellule, les copies surnuméraires se trouvant alors, soit sous forme intégrée dans un chromosome, soit sous forme de minichromosomes surnuméraires, les chromosomes doubleminute. Cette amplification entraîne généralement une augmentation du 84
101 Chapitre II Pathologies et classification des lésions mammaires niveau de l expression du gène : exemple : Les proto-oncogènes c-myc et N- myc sont souvent amplifiés dans les tumeurs solides. Le cancer résulte d un défaut de mort cellulaire des cellules transformées par inhibition de l apoptose. Lorsque l oncogène HER2/neu est surexprimé, (25% des cancers du sein) une résistance à l apoptose induite par le TNF est observée. Pour le cancer du sein, des mutations p53 sont observées dans 58% des cancers familiaux et 13% des cancers sporadiques. Le bcl-2 semble associé aux tumeurs «récepteurs hormonaux positifs», N1. Son expression est inversement corrélée à celle de p53 (Winter et Hickey, 2000). Son expression est corrélée au grade, à Ki67 (indice mitotique), et à l expression de REGF. Les gènes suppresseurs de tumeur sont aptes à inhiber la croissance cellulaire lorsqu ils sont introduits par transfection dans les cellules tumorales. Cette propriété s explique par la capacité de ces gènes à réguler négativement le cycle cellulaire et à induire l apoptose ou mort cellulaire programmée. Action cellulaire récessive, une altération des 2 allèles est nécessaire à l obtention d une perte d activité Contrôle du cycle cellulaire par les gènes suppresseurs de tumeur P53 Le cycle cellulaire eucaryote consiste en une succession de phases de synthèse de l ADN chromosomique (S) et de ségrégation des chromosomes (M) séparées par deux pauses, respectivement les phases pré-réplicatives (G1), entre M et S, et postréplicative (G2), entre S et M. Les transitions entre les phases G1/S et G2/M du cycle cellulaire sont sous le contrôle biochimique de la famille des protéines «cyclines». Les cyclines fonctionnent par fixation et activation des cyclines-dépendantes kinases (Cdk). Leur nom dérive du fait qu elles sont périodiquement synthétisées et détruites en synchronie avec le cycle cellulaire (Sherr, 1996). D autre part, la cellule contient des systèmes qui contrôlent l accomplissement correct des événements du cycle cellulaire. Lorsque de tels systèmes détectent une exposition de la cellule à des dommages ou à des signaux externes, ils déclenchent l inhibition des événements en aval. Les systèmes de surveillance ont été dénommés «points de contrôle» parce qu ils définissent les étapes où la progression peut être 85
102 Chapitre II Pathologies et classification des lésions mammaires arrêtée pendant le temps nécessaire pour contrôler que certaines conditions indispensables sont bien remplies (Williams et al., 1994) Mécanisme d action des anti-oncogènes Les anti-oncogènes agissent principalement en phase G1/S. Cette transition G1/S est sous la dépendance des facteurs de transcription de la famille E2F qui contrôlent l expression de gènes indispensables à la phase S de synthèse de l ADN. Les protéines de la famille E2F existent soit sous forme libre, soit sous forme inactive complexée à la protéine RB. L aptitude de la protéine RB à fixer les facteurs de transcription E2F dépend de son état de phosphorylation. En effet, lorsque la protéine RB est non phosphorylée, elle est active et peut fixer les facteurs E2F, il en résulte un blocage de la transition G1/S. Lorsque la protéine RB est phosphorylée, elle devient inactive et est incapable de fixer la protéine E2F qui, libérée, permet la transition G1/S (fig. 15) (Turner, 2000a). La phosphorylation de RB est elle-même sous la dépendance de complexes protéiques jouant le rôle de verrous moléculaires au niveau de la transition entre les différentes phases du cycle (Williams et al., 1994). Ces complexes sont composés d unités régulatrices, les cyclines, et d unités catalytiques, les kinases dépendantes de cyclines ou CDK (Cyclin Dependant Kinase). L association de ces deux unités constitue le complexe actif. 86
103 Chapitre II Pathologies et classification des lésions mammaires Figure 15 : Représentation schématique du rôle des protéines p53 et prb, codées par les anti-oncogènes p53 et Rb, dans la régulation de croissance des cellules normales du sein (Turner et al., 2000a). 87
104 Chapitre II Pathologies et classification des lésions mammaires Inhibition des signaux anti-prolifératifs Une autre façon pour la cellule cancéreuse d activer la prolifération est par l inactivation des facteurs suppresseurs de tumeur. Ces signaux anti-prolifératifs ont, entre autres, la fonction de maintenir les cellules en phase quiescente et l homéostasie dans les tissus. Ces signaux proviennent généralement soit de la cellule elle-même, soit des cellules environnantes ou de la matrice extracellulaire et sont transmis à la cellule par les récepteurs membranaires qui les transmettent à leur tour aux circuits intracellulaires. Il existe deux façons par lesquelles les signaux anti-prolifératifs peuvent empêcher la multiplication cellulaire. Tout d abord en maintenant la cellule en G0 dans un stade quiescent ou en forçant sa différenciation. La première méthode peut être réversible alors que la différenciation est permanente (Hanahan et Weinberg, 2000). L index apoptotique (AI) est corrélé à un grade élevé, à une aneuploïdie, à un index mitotique élevé, à une phase S élevée, à des récepteurs hormonaux négatifs, à une surexpression de p53 mutée. Cependant, l index apoptotique n est pas un facteur pronostic indépendant dans le cancer du sein. Les facteurs de croissance jouent un rôle prépondérant dans la prolifération des cellules endothéliales : VEGF : Il s agit d un puissant inducteur de l angiogenèse in vivo, son action est médiée par deux récepteurs endothéliaux de type Tyrosine Kinase. L expression du VEGF est médiée par l hypoxie ; FGF : Le bfgf stimule in vitro la prolifération des cellules endothéliales ; PDGF : stimule la sécrétion d agents mitogènes endothéliaux par les cellules stromales ; EGF/EGF-R : Il régit la boucle autocrine de la croissance endothéliale. Il facilite la sécrétion de VEGF par les cellules stromales ; Les facteurs de transcription dont une hyperexpression de protooncogènes c-jun et c-myc est également observée et est à l origine d une activation des cellules endothéliales. Une expression intratumorale endothéliale de c-ets-1 est à l origine de l activation des promoteurs de 88
105 Chapitre II Pathologies et classification des lésions mammaires protéases (upa, stromélysine1, collagénase I et IV). Cette expression est également impliquée dans la régulation d inhibiteurs de l angiogénèse Altérations des gènes suppresseurs de cancers Les altérations moléculaires à l origine de la perte de fonction des gènes suppresseurs dans les tumeurs solides sont variées. Il peut s agir de mutations ponctuelles, de délétions, d insertions, d anomalies de méthylation des promoteurs inhibant la transcription. La voie biologique contrôlant le cycle cellulaire au niveau de la transition G1/S et passant par les gènes suppresseurs p53, p16 et RB, est la voie la plus fréquemment altérée dans les cancers (Turner, 2000a) Contrôle génétique et rapport avec le cycle cellulaire (La famille bcl-2) Gène bcl-2 : Il s agit d un gène de résistance à l apoptose dans l espèce humaine, surexprimé dans 70% des cancers du sein ; Gènes bcl-x ; Bcl-xl code pour une protéine à activité anti-apoptotique ; Bcl-xs code pour une protéine tronquée pro-apoptotique ; Gène bax : code pour une protéine se complexant avec les protéines bcl-2 : Le complexe Bcl-2/bax est anti-apoptotique ; Le complexe Bax/bax est pro-apoptotique ; Le mode d action des protéines de la famille bcl-2 n est toujours pas connu précisément. D'autres contrôles génétiques du cycle cellulaire sont médiés par : protéine Fas/Apo-1 (récepteurs TNF, NGF) et famille ICE (cystéines protéases). 5. Aspects génétiques des cancers mammaires Le cancer résulte d une altération génétique, et présente un caractère de maladie génétique «au sens moléculaire du terme». Mais les altérations sont le plus souvent restreintes aux cellules tumorales, et le cancer est donc une maladie génétique somatique représentant un exemple de mosaïque (présence dans un même organisme de tissus génétiquement différents mais provenant du même zygote). 89
106 Chapitre II Pathologies et classification des lésions mammaires Le cancer n est le plus souvent pas une maladie génétique au sens «mendélien» du terme dans la mesure où celui-ci n est pas héréditaire. Dans les formes sporadiques, les anomalies impliquées dans la cancérogenèse sont restreintes aux cellules tumorales : elles sont dites somatiques. Les formes héréditaires de cancer de transmission autosomique dominante représentent 1 à 5% des cancers. Le cancer du sein présente une incidence élevée dans la population générale, il faut distinguer les formes héréditaires familiales et la survenue de concentrations familiales fortuites de cancer du sein. Les facteurs génétiques interviennent dans 5-10% des cancers du sein. Ils sont surtout responsables des cancers qui surviennent avant 40 ans. Le risque est plus important si le cancer s est déclaré chez une parente de premier degré (sœur, mère, fille) et il est d autant plus élevé que le cancer est apparu à un âge plus précoce. BRCA 1 et 2 ont été isolés et sont responsables de 3-5% des cancers du sein. Tous deux sont familiaux et sont associés à une apparition précoce du cancer du sein. Le gène BRCA 1 (anomalie sur le chromosome 17) est associé au cancer de l ovaire. Le gène BRCA 2 (anomalie sur le chromosome 13) est associé au cancer du sein de l Homme (Bénard et Guinebretiére 1999). Les tests de recherche de ces gènes ne sont pratiqués que chez les patientes suivantes : soit un minimum de trois antécédents familiaux de cancer du sein dont 1 avant 50 ans sur 1 ou 2 générations dans une même branche de la famille y compris du côté paternel, soit 1 antécédent familial avant 40 ans, soit un antécédent familial de cancer bilatéral dont 1 avant 50 ans Prédispositions héréditaires au cancer du sein : BRCA1 et BRCA2 Au cours de cette dernière décennie, la localisation puis l identification de deux gènes de prédisposition héréditaire au cancer du sein et de l ovaire, BRCA1 et BRCA2, ont constitué une avancée scientifique majeure dans la compréhension du cancer du sein familial (Hall et al., 1990). Parmi les facteurs de risque connus, et hormis l âge, une histoire familiale de cancer du sein constitue un facteur majeur, avec un risque relatif variable de 1,5 à 5,3 selon le nombre de sujets atteints, leur âge au diagnostic et le degré de parenté (Pharoah et al., 1997). 90
107 Chapitre II Pathologies et classification des lésions mammaires Ce risque s élève chez les sujets de moins de 50 ans. Si une majorité de cas de cancers du sein sont sporadiques, survenant en l absence de tout contexte familial, une concentration familiale est retrouvée dans environ 20 à 30% des cas (ASCO, 1998). L observation de certains clusters familiaux a suggéré depuis longtemps une composante héréditaire dans la survenue de ces tumeurs. Ainsi, le chirurgien Paul Broca dans son Traité des tumeurs de 1866 rapporte, dans une même généalogie, une dizaine de femmes atteintes d un cancer du sein sur plus de trois générations (Broca, 1866). Les premières études d épidémiologie génétique, par l intermédiaire des analyses de ségrégation ont apporté la preuve d une hérédité autosomique dominante, liée à la transmission d un gène majeur de fréquence allélique rare et de forte pénétrance (Williams et Anderson, 1984). Il a été estimé que 5 à 10% des cancers du sein survenaient dans un tel contexte (Claus et al., 1996). Les deux gènes de prédisposition, BRCA1 et BRCA2, ont été découvert en 1994, situés respectivement sur les chromosomes 17q21 et 13q12. Une méthode de clonage positionnel a permis par la suite leur identification (Miki et al., 1994). Être porteur d une mutation germinale de l un de ces gènes confère un risque cumulé élevé de développer un cancer du sein, estimé entre 60 et 85% à 70 ans pour une femme, auquel s associe un risque de cancer de l ovaire estimé entre 40 et 60% pour BRCA1 et 10 à 30% pour BRCA2 (Lasset et Bonadona, 2001). Les données issues d études de population : Peto et al., 1999 et l Anglian Breast Cancer Study Group (ABCSG, 2000) ont estimé la contribution des gènes BRCA1 et BRCA2 à partir de séries rétrospectives de cas de cancer du sein issus de registre de population et non sélectionnés sur leur histoire familiale. Les auteurs ont notamment étudié, parmi les apparentées au premier degré des cas index, la proportion de l excès de risque familial de cancer du sein attribuable aux deux gènes connus. Les estimations rapportées par les auteurs sont respectivement de 16% et 17%, après ajustement prenant en compte une sensibilité de détection des mutations inférieure à 100%. À partir des données d une étude française en population et prospective, il a été estimé un excès de risque familial à 21%. Ainsi, BRCA1 et BRCA2 ne permettent d expliquer qu une partie modeste des concentrations familiales de cancer du sein observées en population générale. 91
108 Chapitre II Pathologies et classification des lésions mammaires Le gène TSG101 a été trouvé dans près de 50% des cancers du sein. Il s agit d un gène normal qui serait suppresseur de tumeur mais qui aurait subi une mutation. Celle-ci lui aurait fait perdre sa propriété d empêcher les cellules précancéreuses de se transformer en cellules cancéreuses. Lors d une recherche menée entre 1976 et 1988 par des médecins de la Harvard School of Public Health auprès de femmes de 30 à 55 ans, les risques de souffrir du cancer du sein ont été quantifiés de la façon suivante : 7% quand la mère et les sœurs n ont jamais souffert de ce cancer ; 10% quand la mère en a déjà souffert ; 12,5% quand la mère en a souffert avant l âge de 50 ans; 13% quand une sœur en a souffert ; 17% quand la mère et une sœur en ont souffert (Harvard School of Public Health, 1988) Les altérations moléculaires constitutionnelles dans les cancers mammaires Trois gènes de prédisposition principaux sont décrits dans les cancers du sein familiaux : BRCA1 (chromosome 17) 50% des familles de «cancer du sein seul» ; 90% des familles de «cancers sein et ovaire» ; BRCA2 (chromosome 13) corrélation avec envahissement ganglionnaire ; Syndrome du «cancer du sein seul» et «cancers du sein et de l ovaire» ; Cancer du sein chez l homme. BRCA3 (chromosome 8) Familles de cancer du sein seul (Lasset et Bonadona, 2001). 92
109 Chapitre II Pathologies et classification des lésions mammaires 5.3. Les formes héréditaires de cancer du sein liées à BRCA1 et BRCA2 sont elles sensibles aux œstrogènes? Il existe un faisceau d arguments épidémiologiques et expérimentaux montrant que les formes héréditaires de cancer du sein, telles que celles impliquant une mutation des gènes BRCA1 et 2, pourraient être sensibles aux œstrogènes. Sur le plan biologique, de multiples interactions entre le gène BRCA1 et les œstrogènes ont été mises en évidence. Ainsi, l expression de BRCA1 peut être induite par les œstrogènes dans des modèles expérimentaux. Parallèlement, BRCA1 inhibe l activation transcriptionnelle par les œstrogènes de gènes cibles de la prolifération cellulaire. Le développement normal de la glande mammaire est sous le contrôle des hormones stéroïdes (Pujol et Maudelonde, 1997). Les études épidémiologiques récentes, qui ont analysé le risque de cancer du sein sous traitement hormonal de la ménopause (THM), confirment une augmentation significative du risque relatif chez les utilisatrices au long cours (Beral et al., 2003). Parallèlement, le traitement adjuvant du cancer du sein par anti-œstrogènes diminue l incidence des cancers du sein controlatéraux. Dans le cadre du NSABP (National Surgical Adjuvant Breast Project) (King et al., 2001), un essai de chimioprévention chez les femmes à risque de cancer du sein élevé, défini par les antécédents familiaux ou la présence de lésions mammaires bénignes, a montré une réduction d incidence dans le groupe traité par tamoxifène de près de 50% (Fisher et al., 1998) Œstrogéno-induction de BRCA1 L expression de BRCA1 dans le tissu mammaire est augmentée durant la puberté et la grossesse, au moment où les taux d œstrogènes sont élevés. L hypothèse d un lien entre œstrogènes et expression de BRCA1 est étayée par le fait que les œstrogènes et la progestérone stimulent l expression mammaire de BRCA1 chez des souris ovariectomisées (Bennett et al., 2000). De façon concordante, la déplétion en œstrogènes de lignées de cancer du sein RE+ réduit l expression de BRCA1, alors que le traitement par œstradiol augmente son expression (Seery et al., 1999). Notons cependant qu il n existe pas d élément de réponse fonctionnel aux œstrogènes (ERE, 93
110 Chapitre II Pathologies et classification des lésions mammaires séquence d ADN spécifique sur laquelle se fixe le complexe récepteur-œstrogène) sur le gène BRCA1 et que le mécanisme d induction paraît être indirect (Marks et al., 1997) Aspects biologiques de l implication de BRCA1 et 2 dans les cancers mammaires De nombreuses données expérimentales ont mis en évidence des interactions entre œstrogènes et expression des gènes BRCA1 et BRCA2 : induction de l expression de BRCA1 par l estradiol ; inhibition de la croissance et de la différenciation des galactophores par l estradiol chez des souris transgéniques mutées pour BRCA1 ; méthylation du promoteur de BRCA1 corrélée à la négativité des RE dans les cancers du sein sporadiques ; diminution de l expression de BRCA1 corrélée à la négativité des RE dans les cancers du sein sporadiques. Négativité des RE (Stoppa-Lyonnet et al., 2000). Par ailleurs, les œstrogènes induisent un phénotype distinct au niveau de la glande mammaire chez des souris hétérozygotes pour des mutations BRCA1 et BRCA2 (Bennett et al., 2000). Ainsi, les souris mutées ont un développement morphologique des canaux galactophores inhibé par l action des œstrogènes, à la différence des souris non mutées. Ces observations sont en accord avec l hypothèse que la perte du processus de réparation de l ADN dans des cellules mammaires ayant des mutations de BRCA1 ou de BRCA2 entraîne une inhibition de la croissance et de la différenciation œstrogéno-induites. En conclusion, BRCA1 et BRCA2 pourraient participer activement à la prolifération et à la différenciation induite par les œstrogènes, en particulier au cours des périodes d exposition hormonale importante REα et BRCA1 Les œstrogènes se fixent sur leurs récepteurs spécifiques, les REα et β, qui agissent comme des facteurs de transcription. Le complexe œstrogène-re se fixe sur la région promotrice de gènes cibles et en active la transcription. Dans les cancers 94
111 Chapitre II Pathologies et classification des lésions mammaires sporadiques, il semble qu il existe une relation entre l expression des ARN messagers de BRCA1 et du REα (Seery et al., 1999). En outre, la méthylation du promoteur de BRCA1 apparaît être corrélée à la perte d expression des RE et des récepteurs à la progestérone (RP) (Catteau et Morris, 2002). La plupart des cancers héréditaires ne seraient pas liés à la succession des événements hormonaux de la vie mais plutôt à la précocité de la puberté résultant possiblement d une sensibilité anormale de la glande mammaire aux hormones à cette période de la vie (Hamilton et Mack, 2003). Les formes sporadiques, au contraire, seraient plus liées à une exposition répétée et cumulée aux hormones durant la vie adulte BRCA1 et expression des RE : un lien paradoxal? Plusieurs hypothèses concernant la négativité des RE fréquemment retrouvée dans les cancers du sein liés à des mutations BRCA1 peuvent être évoquées. D une part, il est bien établi que les cellules épithéliales mammaires normales et cancéreuses régulent négativement l expression des RE sous l effet des œstrogènes (Pujol et al., 1998). Cette downregulation des RE pourrait aussi constituer un mécanisme de défense cellulaire visant à protéger la cellule vis-à-vis du stimulus œstrogénique prolifératif non contrôlé par la protéine BRCA1 altérée. L hypothèse d une régulation négative des RE sous l effet des œstrogènes peut être étayée par l observation d une négativité des RE observée uniquement en période d activité génitale (Vaziri et al., 2001). La perte d expression des RE dans les tumeurs mutées pour BRCA1 pourrait enfin correspondre à un événement moléculaire tardif de la progression tumorale. Cette perte d expression des RE serait alors elle-même facilitée par l instabilité génomique due à la perte de fonction de BRCA Hétérogénéité phénotypique des cancers mammaires Les cancers liés à des mutations de BRCA1 ou de BRCA2 présentent des caractéristiques tumorales sensiblement différentes de celles des tumeurs sporadiques. Ainsi les cancers BRCA1 présentent plus souvent un index mitotique élevé, et un grade SBR III (Lakhani et al., 1998). Une histologie de type médullaire est plus fréquemment retrouvée dans les formes BRCA1 (de l ordre de 10% des cas 95
112 Chapitre II Pathologies et classification des lésions mammaires BRCA1 versus 1% des cas sporadiques) (Eisinger et al., 1998). Les cancers BRCA2 sont également plus souvent de grades SBRII et III que les cancers sporadiques. Le pronostic des formes BRCA1 pourrait être par ailleurs plus réservé, bien que cette notion soit encore débattue (Stoppa-Lyonnet et al., 2000). Dans une analyse récente regroupant 10 études, la positivité des récepteurs aux œstrogènes (RE) était de 17% dans les tumeurs associées à une mutation de BRCA1 et de 63% dans les tumeurs liées à une mutation de BRCA2 (King et al., 2001). Plus de 70% des tumeurs du sein survenant chez des femmes porteuses d une mutation de BRCA1 n expriment pas les RE (Stoppa-Lyonnet et al., 2000). Rappelons que le taux de positivité des RE dans les cas sporadiques est de l ordre de 70% (Pujol et al., 1994). Cette expressivité tumorale moindre des RE dans les cancers du sein liés à BRCA1 par rapport aux cancers sporadiques serait surtout présente avant l âge de 50 ans (Vaziri et al., 2001). 96
113 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires 1. Epidémiologie du cancer du sein Le cancer du sein est un problème majeur de santé publique. Il constitue dans les pays occidentaux, l affection tumorale la plus fréquente de la femme. Parkin a estimé qu en 1980 le cancer du sein représentait 18% des cancers de la femme dans le monde. La même année, il était le cancer féminin le plus fréquent, suivi par le cancer du col de l utérus, du colon et rectum, de l estomac puis des poumons à égalité avec le cancer du corps utérin (tableau 8) (Parkin et al., 2003). Registre Taux standardisés chez la femme USA : Los Angeles (86-93) 88,6 France : Isère (86-93) 67,3 Algérie : Sidi Bel Abbés (97-98) 32,5 Japon : Osaka (86-93) 21,8 MALI : Bamako (86-93) 10,8 Espagne : Granada (86-93) 33,9 Tableau 8 : Taux d incidence standardisés des cancers du sein dans le monde pour habitants (Parkin et al., 2003) Epidémiologie descriptive mondiale L incidence des cancers du sein in situ a augmenté depuis une vingtaine d années dans les pays développés. Ils représentaient 1 à 5% des cancers du sein diagnostiqués en 1980, et actuellement, ils atteignent 10 à 20% de l ensemble des cancers en fonction des pays (Ernest et Barcley, 1996). L augmentation a été d abord observée au Etats-Unis à partir des années 1980, puis dans les pays européens à la fin des années L augmentation de l incidence est essentiellement due à l augmentation de la fréquence des CCIS (carcinome canalaire in situ), les CLIS (carcinome lobulaire in situ) ont aussi augmenté au cours du temps mais de façon plus modérée. L augmentation des CCIS au cours du temps est à mettre en relation avec le développement du dépistage par mammographie. Les modifications des facteurs de risque du cancer du sein au cours du temps, induisant une réelle augmentation de 97
114 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires l incidence ont pu jouer un rôle dans cette dynamique mais de façon plus modérée (Barchielli et al., 1999). Entre 1985 et 1995, ils ont estimé que 69% de l augmentation d incidence dans le monde des CIS (Cancer In Situ ; diagnostiqués entre 50 et 69 ans) pouvait être attribuée directement au dépistage mammographique Epidémiologie du cancer du sein en Europe Il existe une grande variabilité géographique, ce cancer est très fréquent dans le nord de l Europe et en Amérique du nord, sa fréquence est intermédiaire en Amérique du sud, et relativement faible en asie. Le rapport est de cinq environ entre les pays à forte et faible incidence comme il est clairement représenté dans le tableau 9 (Hill, 1997). L incidence augmente dans la plupart des pays, mais il est difficile de faire la part de ce qui est due au dépistage, la mortalité augmente aussi, sauf aux Etats-Unis, en France la mortalité par cancer du sein a régulièrement augmenté entre 1950 et 1980, mais elle est restée relativement stable depuis cette date, l augmentation observée avant 1980 était beaucoup plus importante chez les femmes âgées que chez les femmes jeunes, ainsi chez les femmes de moins de 45 ans la mortalité n a pas augmentée depuis plus de 20 ans (Rezvani, 1990). Le taux de survie d un cancer du sein tous stades confondus sont de l ordre de 70% à 5 ans et de 50% à 10 ans. Pour les patientes sans envahissement ganglionnaire et sans métastases lors du diagnostic initial, la survie à 5 ans est d environ 90% (Hill, 1997). Age (ans) > 65 Total France 14,8 138,4 210,4 73,8 Europe 19,3 156,5 224,5 83,1 Tableau 9 : Taux d incidence annuelle brute suivant l âge en France et en Europe pour habitants (Hill, 1997). 98
115 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires 1.3. Epidémiologie du cancer du sein en Afrique Le cancer du sein est le premier cancer de la femme, estimé à 1,05 million nouveaux cas ont été estimé en l an 2000, y compris 22% de cancers nouveau chez la femme. En Afrique, il est relativement moins courant, les nouveaux cas sont estimés à nouveaux cas soit 18% des cancers de la femme, au nord africain le cancer du sein est relativement plus courant que les cancers cervicaux à compter pour 27% des cancers comparé avec 15,7% du Sub-Sahara Africain (Parkin et al., 2003) Epidémiologie du cancer du sein en Algérie (données de la wilaya de Sidi Bel Abbés) Le cancer du sein est un cancer fréquent chez les femmes algériennes puisqu il représente 26,9% dans la wilaya d Oran pour l année 2001 (Registre du Cancer- Oran) et 32,5% dans la wilaya de Sidi Bel Abbés (Registre du Cancer SBA 1998), et 10,7% a Sétif (Registre du Cancer Setif, 1993). Le cancer du sein est un problème majeur de santé publique dans le monde, parce que c est le premier cancer de la femme ( nouveaux cas par an), et c est la première cause de mortalité par cancer chez les femmes de 35 à 55 ans (33,7 pour femmes). La répartition du cancer du sein par sexe à Sidi Bel Abbés (1998), compte 4 cas soit 3,2% chez les hommes et 122 cas soit 96,8% chez les femmes, avec prédominance des carcinomes canalaires infiltrants (55,6%). Quand à la répartition des cancers gynécologiques selon la localisation gynécologique à Sidi Bel Abbés (1998) compte 34% des cancers sont ceux du col, 9% de l utérus, 7% de l ovaire, et 50% du sein. A travers ces données, on remarque que le cancer du sein avec ses 50% a la plus grande part d incidence des cancers gynécologiques à Sidi Bel Abbés. L incidence annuelle des cancers du sein est croissante, situé en première place des cancers de la femme, dont la population à risque a un âge compris entre 40 et 49 ans, avec prédominance des carcinomes canalaires infiltrant (Registre des cancers SBA) Les facteurs de risques du cancer du sein Les facteurs génétiques sont responsables de 5 à 10% des cancers du sein. Il s agit en fait de la transmission héréditaire d une anomalie génétique impliquée dans 99
116 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires les processus de cancérisation, comme par exemple une forme altérée de gènes tels que BRCA1, BRCA2 ou p53. Un tel risque concerne les femmes ayant un parent proche (mère, sœur ou fille) atteint d une de ces anomalies (Chodosh et al., 1999). Les hormones endogènes sont très impliquées dans le développement de la glande mammaire et de ce fait jouent un rôle important en tant que facteurs de risque du cancer du sein. L apparition précoce des menstrues (avant 12 ans), une ménopause tardive (après 55 ans) et l absence de grossesse menée à terme avant 30 ans sont autant de facteurs favorisant l apparition d une tumeur mammaire. En revanche, une grossesse menée à terme avant 20 ans ainsi que l allaitement diminue considérablement les risques. Le risque élevé est en relation avec une surexposition aux œstrogènes endogènes (Davidson, 1994). Les variations d incidence existantes d un pays à l autre amènent à parler de risques environnementaux. Les hypothèses concernant le rôle d une alimentation trop riche en graisses animales comme facteur de risque n ont pas encore été démontrées à ce jour. En revanche, d autres facteurs environnementaux sont reconnus comme impliqués dans l apparition de cancers du sein. Notamment, on retrouve l exposition à de fortes radiations (cas des femmes de Nagasaki et Hirochima). Pour les personnes à risque, un certain nombre d éléments non modifiables multiplient d une manière importante - par rapport à la population générale - les risques pour une personne d être atteinte de ce cancer. On distingue différents types de facteurs de risque : L âge C est un facteur important, le cancer du sein est plus fréquent chez les personnes plus âgées. Pour le groupe d âge ans, le risque est de 0,5. En comparaison avec ce groupe d âge : ce risque est 2 fois plus élevé pour le groupe d âge ans, plus de 2,5 fois plus élevé pour les groupes d âge ans et ans et jusqu à près de 3 fois plus élevé pour le groupe d âge ans. Comme la plupart des cancers, le risque d avoir un cancer du sein augmente avec l âge. Pour ces raisons, des programmes de dépistage du cancer du sein ont été mis en place 100
117 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires pour les femmes à partir de 50 ans le plus souvent. Ainsi, à 40 ans, les probabilités sont de 1 sur 217 ; à 85 ans, elles sont de 1 sur 8. Le cancer du sein est rare avant 30 ans et son incidence augmente ensuite jusqu à l âge de 75 ans. 5% des cancers du sein surviennent après 40 ans : environ 17% entre 40 et 49 ans, 22% entre 50 et 59 ans, 22% entre 60 et 69 ans, 22% entre 70 et 79 et 12% au-delà de 80 ans (Statistiques canadiennes sur le cancer, 1998) Le sexe Bien que les hommes puissent développer un cancer du sein, cette maladie est 100 fois plus fréquente chez les femmes (Frouge, 1995), 1% chez les hommes algériens. Les maladies bénignes du sein avec atypies cellulaires chez Les femmes qui ont déjà souffert de cette affection sont plus susceptibles d être atteintes d un cancer (Tavassoli et al., 2003) Les femmes obèses Certaines études semblent démontrer une incidence élevée de cancer du sein avec un régime alimentaire riche en gras ou chez les personnes obèses. Chez la femme ménopausée, l obésité est associée à une augmentation du risque de cancer du sein. Par ailleurs, on sait que ce risque est plus important chez les femmes présentant des taux élevés d œstrogènes. Une nouvelle étude vient de montrer que ces hormones constituent la pierre angulaire de cette relation (Beauthier, 2003) L exposition à l hormone œstrogène endogène Il s agit de l œstrogène produit par l organisme. Chez les femmes préménopausées, l œstrogène est produit à 60% par les ovaires (sous forme d estradiol) et à 40% par les glandes surrénales (sous forme d estrone). Après la ménopause et l atrophie des ovaires, l œstrogène continue à être produit au niveau du tissu graisseux sous l action des glandes surrénales. Chez les femmes de ans atteintes de cancer du sein, elles ont des taux élevés d œstrogène. Le risque de cancer du sein augmente en fonction de la durée de stimulation œstrogénique du sein (fig. 16) (Pujol et al., 2004). 101
118 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Cela explique sa fréquence élevée en cas de ménarchie (début des premières règles) précoce, de ménopause tardive, de nulliparité (aucune grossesse), ou une grossesse tardive. Inversement, on note sa moindre fréquence chez les femmes qui ont subi une ovariectomie bilatérale (ablation des ovaires). En revanche, le nombre de grossesses et l allaitement prolongé pourraient diminuer le risque de développer un cancer du sein La pilule anticonceptionnelle Il existerait un très faible risque de cancer du sein en cas de début très précoce de la contraception ou de traitement prolongé de plus de ans (Frouge, 1995) L hormonothérapie post-ménopause Elle augmente le risque de cancer du sein chez les femmes qui la suivent ou qui l ont suivi pendant les 5 dernières années (fig. 17) (Pujol et al., 2004). Ce risque augmente de 2 pour pour les femmes qui ont suivi la HTR pendant 5 ans, et il augmente à 6 pour chez celles qui l ont suivi pendant 10 ans. Ce risque devient nul, 5 ans après la cessation de l HTR Les rayons-x et la mammographie Les appareillages modernes de mammographie ne délivrent que très peu de radiations comparativement à ce qui existait il y a ans. Toutefois, le risque de cancer du sein existe pour les femmes de moins de 30 ans en raison d une part de la susceptibilité glandulaire et d autre part de la plus grande quantité de radiation nécessaire pour imager leurs seins qui sont habituellement très denses à cet âge. Théoriquement, les mammographies répétées augmentent le risque de cancer du sein mais la proportion est nettement à l avantage des vies épargnées : soit un cancer du sein provoqué pour 1 million d examens contre 50 vies épargnées (Miki et al., 1994). 102
119 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Figure 16 : L origine hormonale de pathologie bénignes (Pujol et al., 2004)). 103
120 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Figure 17 : Facteurs favorisants l apparition d un cancer du sein (Pujol et al., 2004). 2. Dépistage précoce des cancers mammaires 2.1. Terminologie et principes généraux du dépistage Dépistage de la maladie et identification des personnes Il est important de distinguer le dépistage des cancers et l identification des personnes à risque, le terme de dépistage est réservé à la recherche de la maladie chez une personne ne présentant pas de signes cliniques. Dépistage des cancers : dépistage des lésions précancéreuses Selon la pathologie et son histoire naturelle, il existe une phase de tumeur bénigne précancéreuse. Dans ces situations, le même geste peut correspondre soit à du dépistage (mise en évidence des cancers), soit à de la prévention (mise en évidence de lésion précancéreuses). La découverte de lésions in situ pose des problèmes du point de vue de l évaluation de l action (Bernier, 2004). 104
121 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Efficacité du dépistage Le dépistage systématique du cancer du sein permet de dépister des lésions mammaires à un stade précoce comme en atteste l augmentation de fréquence des cancers in situ. Outre ces cancers in situ, les lésions infra-centimétriques sont également en augmentation et, aux États-Unis, on estime que lors de ces vingt dernières années, elles sont passées de 10% à 30% des cancers infiltrants du sein. Plusieurs facteurs concourent à l efficacité du dépistage que l on peut mesurer par différents indicateurs dont l augmentation moyenne d espérance de vie pour chaque personne-cible qui s y soumet (Pujol et al., 2004) Différents types de dépistages Le dépistage individuel Est demandé par le médecin généraliste ou spécialiste ou plus rarement sollicité par le sujet lui même en fonction de ses facteurs de risque propres tel que les cancers familiaux du sein, l autopalpation face au miroir. Le dépistage de masse S adresse à une population définie de plusieurs milliers d individus, une mammographie tout les six mois pour les femmes de plus de 50 ans et gratuitement mise à la disposition de ces sujets en France. Sur 100 femmes ayant effectué une première mammographie dans le cadre du programme de dépistage organisé, seules 46 femmes d entre elles ont effectué une seconde mammographie (Bernier, 2004). Les enjeux du dépistage précoce sont par conséquent importants pour les médecins qui effectuent des diagnostics à des stades plus précoces, et pour les patientes qui augmentent leurs chances de guérison (Bénard et Guinebretiére, 1999). 105
122 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires 2.3. Les recommandations actuelles pour le dépistage précoce du cancer du sein Sont les suivants : consultez le médecin immédiatement en cas : d une gêne persistant dans un ou les deux seins ; palpation d une masse mammaire ; palpation d un durcissement anormal du tissu mammaire ; modification de la couleur du sein ; rétraction cutanée du sein ; rétraction du mamelon ; apparition d un écoulement mammelonaire ; maladie de Paget (mamelon). Pour les femmes qui n ont aucun symptôme, il est conseillé : pour celles de plus de 20 ans, une autopalpation des seins (APS) par semaine ou par mois ; pour les femmes à partir de 50 ans, une mammographie, à répéter au minimum une fois tous les 2 ans. Il est maintenant reconnu que la réalisation régulière d une mammographie diminue la mortalité de 20 à 35% (Bernier, 2004). 3. Méthodes de diagnostic Grâce aux méthodes de diagnostic actuelles, le cancer mammaire peut être découvert à temps et à un stade précoce : 3.1. Mammographie Le sein grâce à sa situation et à sa plasticité se prête aisément à l examen radiographique. Cependant son faible contraste spontané : 0,86 pour la graisse, 0,96 pour le tissu fibreux, 1,13 pour la peau a longtemps constitué un obstacle difficile à surmonter. Les pionniers de la mammographie ont réussi grâce à des modifications de l appareillage de radiographie à obtenir de bonnes images illustrées des données de la clinique et plus rarement a révéler des lésions infra-cliniques (Le Treut et al., 1992). Dans la mammographie ou mastographie, les appareils utilisés sont les mammographes ; ils utilisent des doses faibles de rayons-x spécialement conçus pour visualiser la structure mammaire (Treilleux et Bremond, 2002). La mammographie 106
123 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires est la technique de dépistage la plus efficace pour déceler des tumeurs de moins de 1cm de diamètre (Tortora et al., 1995). Il existe actuellement deux types de mammographes : les mammographes conventionnels qui permettent l obtention des films radiologiques habituels ; les mammographes numériques qui utilisent un détecteur numérique permettant le traitement des images (zoom, modification de contraste, diagnostic assisté par ordinateur). D une façon générale, la lésion doit être décrite et classée en fonction de ses caractères les plus inquiétants. Les catégories sont les suivantes : catégorie 0 : un complément d imagerie est nécessaire : cette catégorie est réservée aux cas où la lecture des mammographies à été différée ; catégorie 1 : il n y a pas d anomalies visibles : ceci ne veut pas dire que le sein est normal ; catégorie 2 : les anomalies ont un aspect typiquement bénin : le risque d association à un cancer est insignifiant en pratique (Treilleux et Bremond, 2002). L image mammographique est le résultat d un ensemble de moyens mis en œuvre (techniques, chimiques, humain), qui tous interfèrent dans la formation de cette image et sur sa qualité. Les éléments caractérisant une image de qualité sont le bon contraste, la bonne définition et les bruits minimum. Les deux premiers éléments dépendent de l appareillage et de son fonctionnement, le troisième du couple écran/film (Goumont et al., 1993). Elle consiste à comprimer le sein puis l exposé à une faible dose de rayons X ; la compression est obtenue par une pelote de compression spécialement conçue pour ce type d exploration et réglée par une manipulatrice spécialisée pour qu elle soit indolore ou parfaitement tolérée par la patiente. Cette compression permet l étalement des tissus mammaires, ce qui facilite la visualisation des structures du sein et permet de réduire la dose de rayons-x délivrée. La dose de rayons-x qui est diffusée lors de la mammographie est inférieure 107
124 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires à celle auquelle on s expose si l on passe une journée en plein soleil. Ce rayonnement ne fait pas augmenter l incidence du cancer du sein (Peltier et Guinebretière, 1998). La mammographie permet de dépister une grande partie des affections du sein (anomalies bénignes ou malignes). Elle est réalisée : après la découverte d une tuméfaction ou anomalies des tissus mammaires ; systématiquement (sans anomalie visible ou palpable) : chez une femme ayant des antécédents personnels ou familiaux prédisposant au risque du cancer du sein ; chez toutes les femmes à partir de l âge 50 ans (Bourillon et al., 1998). L examen de dépistage comporte une mammographie de base (fig. 18) (Parent, 1995). Entre 50 et 74 ans, cet examen est réalisé dans le cadre du programme de dépistage. À l inverse, certains aspects considérés comme anormaux peuvent faire évoquer à tort une pathologie débutante. Dans ce cas, lorsqu il aura pris connaissance des clichés, le médecin apportera des explications et informera sur les explorations complémentaires qui pourront être réalisées afin de porter un diagnostic avec certitude (Trofani et Contesso, 1986) Echographie Le médecin peut décider de faire confirmer son premier diagnostic par une mammographie. L échographie est un examen complémentaire qui peut aider à localiser l anomalie pour faciliter un prélèvement ou reconnaître s il s agit d un kyste liquidien, mais elle ne peut jamais remplacer la mammographie (Peltier et Guinebretière, 1998). Seule, celle-ci, pratiquée régulièrement, permet de diagnostiquer la maladie à un stade suffisamment précoce pour que les soins soient légers et très efficaces (fig. 19) (Christoforov et al., 1998). C est un examen indolore et sans danger utilisant une sonde émettrice et réceptrice d ultrasons. L échographie produit des images par l intermédiaire d un appareil qui émet d abord une pulsation sonore à haute fréquences puis enregistre sur un moniteur (Tortora et al., 1995). 108
125 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Cliché de profil Cliché de face Figure 18 : Images mammographiques : clichés de face et de profil (Parent, 1995) Figure 19 : Image échographique d une patiente atteinte d un cancer du sein (Christoforov et al., 1998). 109
126 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires 3.3. Cytoponction L examen cytologique apporte un élément fondamental dans le diagnostic des lésions mammaires. En effet, l échographie se trouve limitée dans la caractérisation des lésions solides et parfois liquidiennes, dans de nombreuses situations (Goumont et al., 1993). La cytoponction se pratique avec une aiguille très fine, sans anesthésie, elle est quasiment indolore. Elle consiste à piquer plusieurs fois dans le nodule, pour étudier les cellules en différents endroits. Elle se pratique sur les nodules de plus d un centimètre de diamètre. Elle est parfois guidée par une échographie. Les micro-nodules (diamètre inférieur à 10 mm) sont beaucoup trop rarement cancéreux pour être cyto-ponctionnés (Guérin et al., 1998). En pathologie mammaire, la cytoponction est considérée comme un complément diagnostic initial pour des masses palpables pleines ou kystiques et, plus récemment pour des lésions mammaires non palpables, détectées sur mammographies. Le matériel cellulaire obtenu est examiné après coloration de type May-Grünwald-Giemsa (MGG) et/ou Papanicolaou. La technique est simple, rapide, peu onéreuse et présente peu de complications. La valeur de la cytoponction dépend de la qualité du prélèvement, de la préparation des lames et de l expérience du cytopathologiste. Selon les circonstances, la cytoponction d une lésion mammaire est réalisée par le clinicien, le radiologue ou le pathologiste. Dans tous les cas, certaines conditions techniques doivent être respectées afin d assurer une bonne préservation du matériel cellulaire et d atteindre le but du dépistage cytologique : intervenir chirurgicalement sur toutes les lésions malignes lors d une intervention chirurgicale. L examen se fait sous anesthésie locale et exige une asepsie rigoureuse, c est un soin stérile. On pratique une antisepsie de la peau, puis l opérateur immobilise la masse avec deux doigts, puis il pique et déplace l aiguille. Au retrait de l aiguille, les prélèvements sont fixés sur une lame et envoyé au laboratoire. Après la ponction, on doit assurer une compression de une à deux minutes. C est un examen simple, rapide et atraumatique (Guérin et al., 1998). Cet examen est indiqué lorsqu il s agit d une évacuation d un kyste et se renseigner sur les cellules évacuées. 110
127 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires 3.4. Immunohistochimie (IHC) La technique de détection in situ d un antigène (Ag) par immunohistochimie (IHC) est couramment utilisée sur coupes de tissus, à l aide d anticorps de reconnaissance spécifiques. Elles consistent à révéler sur coupe histologique, par réaction antigène-anticorps, la présence de récepteurs antigéniques cellulaires intranucléaires, membranaires ou cytoplasmiques. Le marqueur recherché ou l antigène (Ag) peut être intracellulaire ou membranaire ou extracellulaire, les anticorps utilisés sont soit polyclonaux, c est-àdire obtenu dans le sérum d un animal préalablement immunisé par l Ag (antisérum), soit monoclonaux par des techniques de fusion cellulaire (hybridome). Un anticorps ou immunoglobuline est une protéine complexe utilisée par le système immunitaire pour détecter et neutraliser les agents pathogènes comme les bactéries et les virus. Les anticorps sont sécrétés par des cellules dérivées des lymphocytes B, les plasmocytes, et reconnaissent des antigènes de manière spécifique (Berg et al., 2002). Formées de 4 chaînes polypeptidiques : 2 chaînes lourdes (H pour heavy,) et 2 chaînes légères (L pour light) qui sont reliées entre elles par un nombre variable de ponts disulfures assurant une flexibilité de la molécule. Ces chaînes forment une structure en Y et sont constituées de domaines globulaires de 110 acides aminés environ. Pour un anticorps donné, les deux chaînes lourdes sont identiques, de même pour les deux chaînes légères. Une immunoglobuline possède quatre domaines variables situés aux extrémités des deux «bras». L association entre un domaine variable porté par une chaîne lourde (VH) et le domaine variable adjacent porté par une chaîne légère (VL) constitue le site de reconnaissance (ou paratope) de l antigène. Ainsi, une molécule d immunoglobuline possède deux sites de liaison à l antigène, un au bout de chaque bras. Ces deux sites sont identiques, d où la possibilité de lier deux molécules d antigène par anticorps. À partir des années 1980, l arrivée des anticorps monoclonaux a contribué significativement à l essor de l immunohistochimie même si, pour certains antigènes, les anticorps polyclonaux restent d actualité (Janeway et Travers, 2001). Il n y a pas 111
128 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires eu, en anatomie pathologique, de technique plus révolutionnaire dans les 50 dernières années (Berg et al., 2002). Anticorps monoclonaux Sont des anticorps ne reconnaissant qu un seul type d épitope sur un antigène donné. Les anticorps monoclonaux sont par définition tous identiques et produits par un seul clone de plasmocyte. Les anticorps monoclonaux sont très largement utilisés en biologie et en médecine, à la fois comme outils de diagnostic et dans des buts thérapeutiques (Berg et al., 2002). Les cellules hybrides obtenues sont appelées hybridomes et, après sélection et multiplication dans un milieu de culture approprié, produisent des anticorps monoclonaux, très purs et en quantités importantes. Anticorps polyclonaux Sont un mélange d anticorps reconnaissant différents épitopes sur un antigène donné. Au cours de la réponse immunitaire, un organisme synthétise des anticorps dirigés contre plusieurs épitopes d un antigène : la réponse est dite polyclonale (Berg et al., 2002). Il existe différentes techniques plus ou moins complexes visant toutes à amplifier le signal. l anticorps primaire : qui reconnaît l antigène recherché, il peut être monoclonal ou polyclonal ; l anticorps secondaire : dirigé contre l anticorps primaire (ou plus exactement contre les immunoglobulines de l animal ayant produit l anticorps primaire) ; la visualisation d un complexe antigène-anticorps doit être réalisée in situ à l aide d un marqueur morphologique. Plusieurs méthodes sont possibles : radio-isotopique, fluorescence, métallique, enzymatique (fig. 20) (Kamoun, 1987). En anatomie pathologique, la méthode la plus appropriée pour révéler le complexe Ag/Ac sur coupes de tissus est la mise en évidence d une activité enzymatique, la plus communément utilisée est la peroxydase extraite du raifort (cruciféracée), car disponible en grande 112
129 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires quantité, stable, peu coûteuse et détectable par plusieurs chromogènes, elle est couplée de façon stable à des protéines (fig. 21) (Kamoun, 1987). Figure 20 : Anticorps primaire conjugué à l anticorps secondaire (Kamoun, 1987). Chromogène (donneur d électron) + H2O2 Peroxydase Produit coloré insoluble + H2O Figure 21 : Mode d action de la peroxydase (Kamoun, 1987). 113
130 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Les chromogènes les plus utilisés en immunohistoperoxydase, bien que carcinogènes, sont le 3-Amino-9-Ethyl-Carbazole (AEC) et la 3,3-Diaminobenzidine (DAB) (tableau 10) (Tijssen, 1985 ; Bailly, 1992). AEC Produit de réaction rouge facilitant l observation. Soluble dans les alcools et les solvants organiques. Les contre-colorants ne doivent pas contenir de l alcool. Le milieu de montage doit être aqueux. Peut perdre de son intensité coloration (diffusion dans le milieu de montage). DAB Précipité marron. Précipité insoluble. Tout contre-colorant peut être utilisé. Tout milieu de montage utilisé. Intensité de coloration pratiquement permanente. Tableau 10 : Caractéristiques des deux chromogènes de la peroxydase (Bailly, 1992). 114
131 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Dans l immunoperoxydase simple, on a : la directe : une seule étape et une seule espèce animale : l anticorps primaire est directement couplé à la peroxydase (Kamoun, 1987) ; Anticorps primaire conjugué + antigène marquage direct l indirecte : Deux étapes et deux espèces animales : l anticorps primaire est détecté par un second anticorps couplé à la peroxydase (Kamoun, 1987). AC secondaire conjugué + AC primaire + antigène marquage indirecte Dans les systèmes d amplification existant on distingue : Système PAP Trois étapes et trois espèces animales : un second anticorps sert de liaison entre l anticorps primaire et le complexe péroxydase-anti-peroxydase (Wilchek et Boyer, 1988). Système Biotine/Streptavidine Trois étapes et deux espèces animales : la caractéristique de ce système biotine (vitamine B1) streptavidine (avidine = protéine) est la haute affinité de la streptavidine pour la biotine. La streptavidine sert de pont entre le second anticorps biotinylé et plusieurs peroxydases biotinylées (Kamoun, 1987). Le principal avantage de ce système est l amplification considérable du signal sans augmenter le bruit de fond) (Tijssen, 1985). Il permet de plus une utilisation à de très faibles concentrations des réactifs et en particulier de l anticorps primaire du fait de la forte interaction existant entre la biotine et la streptavidine (Wilchek et Boyer, 1988). La biotinylation d un anticorps n altère pas ses propriétés de liaison à l antigène, l avidine est extraite du blanc d œuf, elle possède 4 sites de liaison à haute affinité pour la biotine, la streptavidine est une protéine isolée à partir d une bactérie Streptomyces avidini, elle a les mêmes propriétés de l avidine (4 sites de liaison à haute affinité pour la biotine) (Wilchek et Boyer, 1988). 115
132 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Apport de l immunohistochimie dans les cancers mammaires Un protocole immunohistochimique est une technique complexe composée de nombreuses étapes successives. Son résultat - le dépôt coloré obtenu -, dont la validité est contrôlée par des témoins, est influencé par des événements préalables à l acte immunohistochimique proprement dit, en particulier la fixation (Werner et al., 2000) et le temps de restauration antigénique (Mc Nicol et Richmond, 1998). Ces caractéristiques expliquent combien, il est difficile d assurer une reproductibilité parfaite du signal immunohistochimique (Bratthauer, 1999). L immunohistochimie (IHC) a pour objet la mise en évidence d antigènes in situ, sur préparations cellulaires ou tissulaires, à l aide d anticorps marqués. L IHC est maintenant utilisée en routine et s applique principalement à des prélèvements qui ont été fixés et inclus en paraffine. Il s agit d une technique d un très grand apport pour le diagnostic en oncologie : pour aider à classer une tumeur dans sa catégorie, pour identifier l origine d une métastase et, dans certains cas, pour aider à établir la malignité d une lésion. Les implications de l IHC au pronostic des tumeurs et à la prédiction d une réponse à la thérapeutique commencent à se développer, en particulier dans le cadre de la détection de récepteurs hormonaux et de la mise en évidence de la surexpression de HER2/neu dans les cancers du sein. Les résultats immunohistochimiques sont habituellement intégrés dans un ensemble de données histologiques, mais aussi cliniques et biologiques, pour permettre le diagnostic. Ainsi, le pathologiste écartera rarement une possibilité diagnostique sur la base d un marqueur absent si les autres paramètres cliniques et biologiques sont en faveur de ce diagnostic (Mc Nicol et Richmond, 1998). L absence d un marqueur peut être due à une particularité de la tumeur étudiée Immunohistochimie diagnostique L IHC trouve là ses principales applications. Elle est indiquée particulièrement lorsque l étude morphologique est limitée parce que : la tumeur est peu différenciée ; la tumeur est remaniée (nécrose) ; 116
133 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires le prélèvement est pauvre en cellules tumorales ou s accompagne d artefacts, notamment d écrasements cellulaires. L IHC peut être utilisée pour classer une tumeur dans une catégorie, soustyper une tumeur au sein d une catégorie et aider à établir la malignité d une lésion. Elle permet aussi l identification de cellules difficiles à visualiser ou à reconnaître formellement sur des colorations standard, ce qui peut être déterminant pour établir la malignité d une lésion. Les cellules visualisées par l immunomarquage peuvent être des cellules bénignes : cellules myoépithéliales au niveau du sein (Yaziji et al., 2000), dont l absence autour d amas épithéliaux suggère fortement la malignité de ces derniers. L immunomarquage peut aussi visualiser des cellules tumorales peu nombreuses, éparpillées ou en petits amas, par exemple au niveau d une zone de micro-invasion ou dans une maladie de Paget. Les cellules tumorales nécrosées, dont les noyaux ne sont plus colorés sur les colorations de routine, restent fréquemment détectables par certains anticorps de typages courants (Shin et al., 1998) Immunohistochimie pronostique et prédictive Les découvertes des 25 dernières années concernant les mécanismes de cancérogenèse et les gènes impliqués dans différentes étapes de la progression tumorale alimentent régulièrement la recherche clinique. De très nombreuses études se sont attachées à essayer de mettre en évidence le rôle pronostic ou prédictif de certains marqueurs biologiques ou génétiques en cancérologie (Hammond et al., 2003). Les facteurs étudiés appartiennent à différentes familles : les oncogènes, les gènes suppresseurs de tumeur, les marqueurs d instabilité microsatellitaire, les gènes codant pour les protéines du cycle cellulaire, les gènes d invasion et de potentiel métastatique, des marqueurs de sensibilité au traitement, des marqueurs d apoptose Différentes méthodes peuvent être utilisées pour les évaluer : les méthodes de biologie moléculaire sur broyats tissulaires (détection d amplification ou de mutations au niveau de l ADN, surexpression de l ARN ou des protéines), des techniques d hybridation in situ ou bien les techniques d IHC. Chaque technique 117
134 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires présente des avantages et des inconvénients. Rien que pour le cancer du sein, plus de 100 facteurs pronostiques différents ont été proposés (Allred et al., 1998). Cela a conduit à définir précisément les exigences que doit satisfaire un nouveau facteur pronostique ou prédictif (Hammond et al., 2003) : La dernière conférence de consensus du College of American Pathologists, en juin 1999, a fait le point sur les marqueurs pronostiques (et prédictifs) dans les tumeurs du sein. Pour les cancers du sein, l évaluation des récepteurs hormonaux par immunohistochimie a été classée dans la catégorie I. Ont été placés dans la catégorie II MiB-1 (Lehr et al., 1999) dont l évaluation ne peut être qu immunohistochimique, ainsi que HER2/neu (Ross et Fletcher, 1999) et p53 (Tsuda et Hirohashi, 1994) ces deux derniers paramètres pouvant être évalués par immunohistochimie ou par d autres méthodes. Plus de 15 années de travail ont été nécessaires pour que l évaluation immunohistochimique des récepteurs hormonaux dans les cancers du sein entre en routine et remplace les techniques biochimiques (Harvey et al., 1999). Les avantages de l IHC sont son caractère, rapide, simple et, par rapport à des techniques utilisant des broyats de tissus, la possibilité d un contrôle morphologique des zones positives, permettant de ne prendre en compte que le marquage du contingent invasif. À cela s ajoute la possibilité d évaluer du matériel fixé et inclus en paraffine et des échantillons de petite taille (biopsies, produit de cytoponction...) (Balaton, 1999). Même si les résultats de l IHC sont, aujourd hui encore, simplement semiquantitatifs, ils permettent de répondre parfaitement à la demande du clinicien, qui a essentiellement besoin de savoir si la tumeur mammaire de sa patiente contient ou non des récepteurs stéroïdiens en quantité significative. Les perspectives d amélioration pour l IHC des récepteurs hormonaux concernent l adoption d un seuil de positivité consensuel, la confection de témoins externes standardisés et l éventuelle mise en place d une évaluation complémentaire du statut des récepteurs bêta des œstrogènes. Le développement des mécanismes externes d assurance qualité doit être poursuivi. Ainsi, les données des programmes d évaluation externe de la performance technique montrent que, si 90% des participants sont capables de réaliser un immunomarquage correct d une tumeur 118
135 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires ayant une expression forte de récepteurs hormonaux, le pourcentage de marquages adéquats est aux environs de 50% lorsque la tumeur a une expression immunohistochimique faible en récepteurs (Rhodes et al., 2000). L anticorps monoclonal MiB1 reconnaît, sur coupe en paraffine, une protéine nucléaire non histone (Ki67) qui n est pas exprimée dans les cellules en G0 (Allred et al., 1998). Il s agit donc d un marqueur de prolifération tumorale qui permet de classer, en fonction du pourcentage de cellules marquées, les patientes en groupes de bon ou mauvais pronostic. Pour p53 (Ross et Fletcher, 1999), le problème est plus complexe : la détection par immunohistochimie est un reflet indirect d altérations du gène. La protéine anormale synthétisée par un gène muté a une durée de vie allongée et devient détectable par immunohistochimie car elle s accumule dans le noyau. Mais certaines mutations du gène entraînent un arrêt de synthèse de la protéine. Par ailleurs, une protéine fonctionnelle peut se trouver en excès et être détectée. Ainsi, l immunohistochimie est plutôt considérée comme une méthode de dépistage de mutations qui devraient par la suite être confirmées par techniques de séquençage, à partir de produits de PCR (Tsuda et Hirohashi, 1994). L apparition récente en oncologie d anticorps monoclonaux humanisés à usage thérapeutique a fourni un nouveau champ d applications à l IHC prédictive : la mise en évidence de cibles thérapeutiques. Ces cibles thérapeutiques sont la protéine ERBB2 dans les cancers du sein. ERBB2 est un oncogène qui est amplifié et surexprimé dans environ 20% des cancers du sein. Le produit de ce gène est la protéine ERBB2 qui est la cible de l Herceptine, un anticorps humanisé (Dowsett et al., 2003). Des études pilotes, concernant des patientes ayant des cancers du sein métastatiques, ont démontré que le taux de réponses cliniques à l Herceptine dépendait du niveau de surexpression de la protéine ERBB2 détecté par immunohistochimie (Di Leo et al., 2002). Si les applications de l IHC dans l établissement d un pronostic sont restreintes, cela vient plus du peu de poids statistique des paramètres biopathologiques par rapport aux paramètres cliniques que de la technique elle- 119
136 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires même. En revanche, l intérêt de l IHC dans la mise en évidence de cibles thérapeutiques comme les récepteurs hormonaux ou le produit de l oncogène HER2/neu est important. Une autre méthode d évaluation du statut ERBB2 concurrence actuellement l IHC : il s agit de l hybridation in situ (Fish) qui évalue le nombre de copies de gènes dans les cellules et détermine le niveau d amplification du gène ERBB2 (Mitchell et Press, 1999). L hybridation in situ est plus longue, bien plus chère, mais semble poser moins de problèmes de standardisation que l IHC (Tubbs et Stoler, 2000) L immunohistochimie en anatomie pathologique mammaire : Applications pratiques Le diagnostic anatomopathologique des tumeurs à longtemps reposait sur la seule analyse morphologique des lésions en technique standard, l application il y a une vingtaine d années de l IHC dans l arsenal diagnostique, à rendu possible l étiquetage précis d un grand nombre de tumeurs malignes indifférenciées (Bailly, 1992) Apport de l immunohistochimie dans le diagnostic différentiel L IHC peut apporter des informations complémentaires pour le diagnostic des proliférations intracanalaires. En effet plusieurs études récentes ont montré que la perte d expression par les cellules épithéliales canalaires de certains sous groupes de cytokératines est spécifique des lésions néoplasiques. Le profil immunohistochimique des lésions d hyperplasie canalaire atypique HCA et des carcinomes canalaire in situ CCIS est donc superposable et l analyse de ces cytokératines aide seulement à la distinction entre hyperplasie canalaire simple et lésions néoplasique intra-canalaire. A l autre extrémité du spectre des CCIS, l immunohistochimie peut aider à affirmer ou à infirmer l hypothèse d une microinvasion. Elle permet en effet d analyser l intégrité de la membrane basale des canaux ou des lobules à l aide d anticorps spécifiques de certains composants de cette membrane (collagène, laminine ), ou l intégrité de la couche myoépithéliale périphérique à l aide d anticorps spécifiques tel l actine-muscle-spécifique. 120
137 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires De plus lorsqu il existe des incertitudes diagnostiques entre des lésions de CCIS et des lésions néoplasiques lobulaires in situ, la démonstration de la protéine membranaire E-cadherine permet d apporter des arguments définitifs en faveur d une lésion d origine canalaire Les facteurs biologiques et moléculaires déterminés par l immunohistochimie a. Récepteurs hormonaux Les récepteurs d œstrogènes et de progestérones (RE, RP) sont le plus souvent recherchés par technique immunohistochimique sur des coupes histologiques de tumeurs fixées. La recherche des récepteurs hormonaux par IHC est utile lorsqu un prélèvement à l état frais n a pas été réalisé. C est le cas d une petite tumeur de découverte microscopique ou d une tumeur ancienne avec diffusion métastatique secondaire pouvant bénéficier d un traitement hormonal, la technique IHC permet de localiser précisément les récepteurs hormonaux dans les différents contingents cellulaire (malin infiltrant, malin in situ, bénin). Règles techniques La technique IHC est résumée dans l article «GEFPICS» (Groupe d Evaluation des Facteurs Pronostic par Immunohistochimie dans le Cancer du Sein), recommandations pour l évaluation IHC des récepteurs hormonaux sur coupes en paraffine dans les carcinomes mammaires. Il faut que le laboratoire utilisant la méthode IHC des récepteurs hormonaux (RH) participe à un programme d assurance qualité en IHC. Règles d interprétations Seul le marquage nucléaire est pris en considération, on apprécie la proportion de cellules infiltrantes positives par rapport à l ensemble des cellules carcinomateuses (positives et négatives), le résultat s exprime en pourcentage de cellules arrondi à la dizaine, et en intensité moyenne de marquage. Le seuil de 121
138 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires positivité pour les RE et les RP est fixé à 10% de cellules positives quelle que soit l intensité du marquage. Rédaction du compte rendu Exemple de fiche de réponse à inclure dans le compte rendu : la recherche de RH par immunohistochimie montre : récepteurs œstrogéniques : pourcentage et intensité de cellules marquées (exemple : 80%, intensité 3) ; récepteurs à la progestérone : pourcentage est intensité de cellules marquées (exemple : 40%, intensité 3) ; témoin interne : positif/négatif. La conclusion précise : présence ou absence de RE et/ou RP. En cas de très faible pourcentage de cellules tumorales positives (inférieur à 10%), on précisera dans le compte rendu que le seuil de positivité est fixé à 10% et l on conclura par absence du ou des RH (Sigal-Zafrani et al., 2004). La valeur prédictive de l IHC est très importante de la réponse à l hormonothérapie, on observe une réduction de 10% du taux de récidives métastatiques à 5 ans chez les patientes N-RE+ par rapport aux patientes N-RE-. On note une diminution de 20% des taux de rechutes métastatiques et de mortalité chez des patientes RE+ recevant une hormonothérapie adjuvante et un taux globale de réponse clinique de 60% chez des patientes RE+ avec diffusion métastatiques. Les taux de réponse clinique à la chimiothérapie seraient plus importants chez les patientes RE-, non ménopausées en situation adjuvante, et chez les patientes RE- en situation néoadjuvante. Quand à la valeur prédictive de réponse à l hormonothérapie des RP, on peut noter que le taux de réponse à l hormonothérapie des tumeurs RE+ RP+ est supérieur au taux de réponse des tumeurs RE+ RP-. b. L oncogène HER2 (HER2-neu ou c-erbb2 ou neu) La détermination du statut de HER2 dans le cancer du sein est devenue un enjeu important avec la mise au point du médicament Herceptin ciblant 122
139 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires spécifiquement les cellules surexprimant HER2. La technique IHC peut visualiser et quantifier la molécule cible sur une coupe de tissu. Règles techniques La sensibilité et la spécificité de détection de la surexpression d HER2 sont très variables en fonction du fixateur, du type du prétraitement, de l anticorps primaire, et de la méthode de révélation. Les résultats optimaux sont obtenus avec un prétraitement par la chaleur dans un tampon citrate dont le ph est égal à 6. Ceci, si on utilise pas le kit qui contient normalement un tampon prêt à l emploi après dilution. les deux anticorps les plus utilisés sont CB11 DA485, ces deux anticorps doivent être utilisés à des dilutions très importantes que celle du kit ; il faut utiliser une coupe de tumeur comportant des glandes bénignes, c est la négativité de ces glandes qui permettra de valider la réaction en cas de positivité du contingent tumoral ; Il faut disposer aussi d un témoin externe positif, par exemple un CCIS de haut grade de type comédocarcinome qui permettra de valider la réaction en cas de négativité de la tumeur (Gown, 1999). Règles d interprétations Seul le marquage membranaire cytoplasmique est pris en compte, il n existe pas de consensus sur la manière de répondre, les protocoles thérapeutiques se basent sur le score diagramme, pour l Herceptin, il n y a pas de seuil de positivité définie pour HER2 pour l instant, il est admis que la majorité des cellules tumorales infiltrantes doivent être positives avec une intensité de marquage modérée à forte, en règle générale, il y a une étroite corrélation entre le pourcentage de cellules marquées et l intensité de marquage (Press et al., 2002). HER2 et pronostic Vingt à 35% des carcinomes infiltrants surexprime HER2 par IHC. Des résultats très discordant ont été publiés sur la relation entre la surexpression d HER2 et le pronostic du cancer du sein. Chez les patientes N+, la majorité des études ont 123
140 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires montré en analyse univariée, une corrélation significative entre HER2 et la diminution de la survie sans récidive et de la survie globale. En analyses multivariées, HER2 est également fréquemment un facteur pronostic indépendant dans ce sous groupe, mais souvent de moindre importance par rapport aux facteurs pronostiques classiques, en particulier le grade histologique. Par contre chez les patientes N-, la majorité des études n ont pas montré qu HER2 avait une valeur pronostique significative (Sigal-Zafrani et al., 2004). HER2 et prédiction de la réponse à la chimiothérapie Chez les patientes ayant des tumeurs HER2 positives, les chimiothérapies adjuvantes seraient moins efficaces du fait d une chimiorésistance associée à la surexpression d HER2. c. La protéine p53 La p53 est une phosphoprotéine nucléaire qui agit en intégrant des signaux de stress cellulaire et en initiant l arrêt du cycle cellulaire ou apoptose. La protéine P53 mutée ne peut plus se lier à l ADN et est capable d inactiver la protéine P53 normale en formant des complexes avec celle-ci, l empêchant d interagir avec l ADN. Les demi-vies de P53 muté et des complexes P53 mutée-p53 normale sont augmentées, provoquant une accumulation dans le noyau des cellules tumorales et permettant leur détection par IHC. Au sein d une tumeur, la présence de rares cellules positives correspond plus à une accumulation physiologique de P53 normale en réponse à quelques stimuli divers, qu a une accumulation de P53 mutée (Gown, 1999). P53 et pronostic Que ce soit en situation néoadjuvante, adjuvante ou au stade métastatique, avec des chimiothérapies ou avec du tamoxifène, la détection IHC de P53 n a pas de valeur prédictive de réponse tumorale. Le bilan de la détection IHC de P53 ne permet pas son utilisation en routine à des fins pronostiques, les facteurs pronostiques classiques ont plus de poids pronostiques que la détection IHC de P53 (Sigal-Zafrani et al., 2004). 124
141 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires 4. Traitement du cancer du sein Quatre traitements peuvent être entrepris, parfois isolément, parfois en association : la chirurgie, la chimiothérapie, la radiothérapie, l hormonothérapie (Bourillon et al., 1998) Chirurgie La chirurgie radicale décrite par Halsted consiste à retirer en continuité la glande mammaire, les muscles pectoraux et les ganglions lymphatiques. Cette technique lourde et traumatisante a quasiment disparu au profit d une mammectomie moins large avec la conservation des muscles pectoraux et un curage axillaire (ganglionnaire) moins étendu. Pour les tumeurs de petites tailles, la mastectomie est remplacée par la tumorectomie associée à un curage axillaire et à de la radiothérapie (fig. 22) (Leroux, 2004). Le curage axillaire est à l heure actuelle facilité par la technique du ganglion sentinelle, qui permet de ne retirer que le premier ganglion de relais et non plus toute la chaîne. Cette méthode est dite de chirurgie conservatrice. Il existe des cancers du sein dits opérables d emblée. Pour les autres cas, la chirurgie est précédée d une cure de chimiothérapie ou d hormonothérapie, voire d une combinaison de ces différents traitements. Il peut s agir d une ablation de la tumeur (tumorectomie), associée à l examen histologique immédiat (dit extemporané), la femme étant toujours sous anesthésie générale, si l examen confirme la malignité le curage ganglionnaire axillaire est réalisé. Pour une tumeur volumineuse ou multiples, une ablation totale du sein (mastectomie radicale) est réalisée (Bourillon et al., 1998) relativement rare de nos jours, ou d une ablation partielle (mastectomie radicale modifiée, excision élargie). 125
142 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Figure 22 : Conduite chirurgicales après dépistage mammographique pour femmes ménopausées et femmes jeunes (Leroux, 2004). 126
143 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Curage axillaire Le curage axillaire consiste à enlever une partie des ganglions (10 environ) du creux de l aisselle au cours de l opération du sein. Ces ganglions sont ensuite examinés pour savoir s ils contiennent des cellules cancéreuses. On le pratique dans les cancers invasifs du sein dans le but de mettre en évidence des ganglions atteints. En effet, l atteinte des ganglions (présence de cellules tumorales) est toujours le facteur de risque le plus important concernant la gravité de la maladie, son risque de dissémination à distance (métastase du foie, poumon, os, cerveau, etc) et l indication de chimiothérapie qui en découle. Les conséquences sont d une part, l atteinte du drainage lymphatique du sein et du bras du côté opéré et d autre part, l augmentation de la sensibilité aux infections au niveau du bras. Le curage est assez mal toléré car il s agit d une incision proche d une articulation très mobile, le bras, dans une zone qui contient à la fois des nerfs très important qui sont préservés et des petits filets nerveux qui sont enlevés avec les ganglions, ce qui cause des douleurs Ganglion sentinelle Cette technique consiste à injecter un produit «marqueur» dans la tumeur avant l opération. Il s agit soit d une substance émettant un rayonnement, soit d un colorant bleu, soit de l association des deux. Ces produits parcourent le système lymphatique en quelques minutes et se concentrent dans le ou les premiers ganglions spécifiques qui drainent la tumeur, baptisés «ganglions sentinelles» Radiothérapie Pratiquée après une tumorectomie, consiste à irradier le sein et le pourtour de la zone retirée pour éviter les récidives locales. Le traitement comprend en générale de six à douze séances, à raison de une ou deux séances par semaine. Dans tout les cas la chirurgie est associée à une radiothérapie ou à une chimiothérapie Chimiothérapie Elle est utilisée lorsque la tumeur évolue rapidement chez la femme jeune ou lorsque des métastases ont été constatées. Le traitement s étend sur une période de deux à six mois. Au début des années cinquante sont apparue des drogues agissant à 127
144 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires différents niveaux de la division cellulaire à des doses susceptibles d affecter des cellules cancéreuses. Aujourd hui pour mieux cibler la tumeur, on associe plusieurs drogues aux propriétés complémentaires (polychimiothérapie), administrées à faible dose. La chimiothérapie a permis de prolonger la vie des malades (Bourillon et al., 1998). Ce qui rend les stratégies thérapeutiques imparfaitement adaptées à chaque cas de cancer du sein est l hétérogénéité clinique qui est mal appréhendée par les facteurs pronostiques histocliniques, ces facteurs dans les formes localisées sont : l âge, le statut ganglionnaire axillaire, la taille et le grade histologique de la tumeur ainsi que la présence de récepteurs hormonaux. La majorité des traitements actuels n ont pas d effet spécifique sur les cellules tumorales, entraînant une toxicité parfois dramatique (Lerebours et Lidereau, 2002). Les applications thérapeutiques directes de l analyse moléculaire du cancer du sein concernant l étude de l expression protéiques mesurée par l immunohistochimie (IHC) du récepteur de l œstradiol (RE) et de progestérone (RP) dans le cas des tumeurs invasives donne une corrélation positive entre leur présence et un état bien différencié, le pronostic des tumeurs exprimant RE et/ou RP est plus favorable en terme de survie (Goldhirsch et al., 2001). L expression de RE et RP est un facteur prédictif à l hormonothérapie dans le cancer du sein (Hayes et Thor, 2002). Il existe un rôle paradoxalement favorable de RE, dans la mesure où les œstrogènes stimulent la prolifération cellulaire via ce récepteur, ou encore du caractère de RE comme facteurs prédictif de réponse (The Chipping Forecast, 1999). L absence d expression conjointe de RE et RP est un facteur pronostic défavorable reconnu pour poser l indication d une chimiothérapie adjuvante dans le cancer du sein localisé sans envahissement ganglionnaire, le récepteur aux œstrogènes est la cible moléculaire de l hormonothérapie qui agit soit par arrêt de la sécrétion du ligand œstrogénique (castration en pré-ménopause et anti-aromatase en post-ménopausée), soit par interférence avec l interaction ligandrécepteurs (SERMs ou modulateur sélectif de RE) (The Chipping Forecast, 1999). 128
145 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires 4.4. Hormonothérapie En 1896, Georges Thomas Beatson publie pour la première fois l effet d une castration chez une femme porteuse de cancer du sein inopérable. En 1974 apparaissent les premières publications concernant le tamoxifène. Celui-ci se fixe sur les récepteurs d œstradiol dont il empêche l action sur ces récepteurs, il est le chef de fil d une nouvelle classe thérapeutique : les anti-œstrogènes. Sa bonne tolérance permettait son utilisation en adjuvant, les premiers essais en adjuvant ont été commencés dès 1975 et les premiers résultats ont été publiés au début des années Depuis cette date le tamoxifène a régné en maître sur l hormonothérapie (Ribeiro et Swindell, 1985). Les carcinomes mammaires se développent à partir des cellules épithéliales des galactophores. Les cellules tumorales gardent certaines caractéristiques des cellules initiales, notamment des récepteurs hormonaux, récepteurs d œstradiol (RE) et récepteurs de progestérone (RP), dont la présence les rend sensibles aux modifications du climat hormonal environnant. L hormonothérapie est basée sur cette sensibilité (Leugs et al., 1973). L arrivée des inhibiteurs de l aromatase (IA) met à notre disposition une arme supplémentaire pour l hormonothérapie du cancer du sein et modifient notre stratégie du traitement adjuvant comme de la prise en charge des cancers métastasés. L hormonothérapie chez la femme ménopausée contenant les IA en première ligne donne des taux de réponses plus importants que le tamoxifène avec une durée de réponse plus longue. La séquence des IA puis tamoxifène permet de retarder le recours à la chimiothérapie. Chez la femme non ménopausée, elle fait appel à l association tamoxifène et suppression ovarienne (SO) (Leugs et al., 1973). 129
146 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Hormonothérapie du cancer du sein métastatique Pour les femmes non ménopausées Le traitement hormonal du cancer du sein métastasé chez la femme jeune comprend la suppression ovarienne définitive, ou temporaire et le tamoxifène. La suppression ovarienne (SO) définitive par ovariectomie, décrite depuis 1886, a été longtemps appliqué aux femmes sans tenir compte des récepteurs hormonaux. Le taux de réponse est alors de 35% (Davidson, 1994). La suppression ovarienne temporaire utilise les analogues de LH-RH. Les taux de réponse sont comparables à ceux de la suppression définitive (par castration) : 35 à 45% (Bajetta et al., 1994). Les taux de réponses obtenues avec le tamoxifène sont du même ordre que ceux obtenus avec la suppression ovarienne (Ingel et al., 1986). L association d une SO au tamoxifène permet d annuler les effets de stimulation hypophysaire du tamoxifène et, dans le cas des analogues de LH-RH, de la supprimer. Par ailleurs, le tamoxifène peut compléter l effet de la SO en limitant l action de l œstradiol circulant résiduel. Chez la femme non ménopausée, des œstrogènes sont produits dans les ovaires. Après la ménopause, les ovaires ne synthétisent plus d œstrogènes, mais le corps produit d autres hormones (androgènes) dans la corticosurrénale. Ces hormones peuvent être transformées en œstrogènes sous l effet d une enzyme, l aromatase, les hormones produites dans le tissu adipeux le sont grâce a cette aromatase, c et donc logique que le blocage de cette enzyme arrête la production de ces hormones après la ménopause. a. Inhibiteurs de l aromatase (IA) Les IA n empêchent pas la synthèse ovarienne d œstradiol. Seuls, ils ne sont pas efficaces chez les femmes non ménopausées (Mauriac et al., 2003). Associés à la SO, ils pourraient diminuer le taux d œstradiol résiduel, en supprimant la synthèse périphérique d œstradiol. L association des deux pourrait entraîner des baisses d œstradiol plus importantes que la SO seule. Les œstrogènes sont des hormones essentielles pour le bon fonctionnement d un organisme féminin ou masculin. Leur production est principalement ovarienne chez la femme pré-ménopausée et surtout périphérique chez la femme ménopausée 130
147 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires et l homme. Leur action trophique est importante tant en physiologie qu en pathologie mammaire. Si le concept d antihormone a été découvert fortuitement, c est le fruit de nombreux travaux cliniques et fondamentaux qui a permis de développer le concept de thérapie ciblée puis de modulateur sélectif des récepteurs. Le rêve des thérapeutes est de moduler la structure de nouvelles drogues permettant d allier les avantages des œstrogènes à l absence de leurs effets délétères (Maudelonde et al., 2005). b. Œstrogènes et SERM En 1936, le concept d anti-œstrogène bloquant l action de l œstrogène dans le tissu mammaire pour prévenir le cancer du sein a été présenté pour la première fois par le professeur Antoine Lacassagne. Depuis ce temps, les anti-œstrogènes et les modulateurs sélectifs des récepteurs des œstrogènes (SERM) ont été développés et font maintenant partie des principales thérapies présentement utilisées pour combattre le cancer du sein. D autre part, le SERM apportant plus qu une simple protection contre le cancer du sein est de plus en plus considéré comme thérapie d avenir contre les effets non désirés de la ménopause (Christian et al., 2005). Les SERM («Selective Estrogen Receptor Modulator») ou modulateurs spécifiques des récepteurs aux œstrogènes (RE) sont des molécules ayant des effets œstrogéniques variables en fonction du tissu cible. Le tamoxifène, par exemple, est un antagoniste des RE au niveau du sein. Leurs indications médicales sont larges et comprennent : le traitement des cancers œstrogéno-dépendants ; le traitement substitutif de la ménopause. Les SERM peuvent moduler l action des récepteurs aux œstrogènes à plusieurs niveaux : du fait de leur affinité différente pour les RE ; en induisant, après liaison au RE, des modifications de conformation différentes du récepteur ; en modulant l activité transcriptionnelle des RE. 131
148 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Par ailleurs, un niveau de complexité supplémentaire est lié à l existence de 2 isoformes des récepteurs aux œstrogènes (isoformes RE-alpha et RE-beta) qui réagissent différemment vis-à-vis des SERM (fig. 23) (Christian et al., 2005). Les indications en cancérologie reposent sur leur activité antagoniste : effets recherchés est celui de l anti-prolifératif sur les cellules de cancer du sein. Figure 23: Structure biochimique des SERM (Christian et al., 2005). 132
149 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Les modulateurs sélectifs des récepteurs des œstrogènes sont des ligands des RE qui ont la capacité de bloquer l action des œstrogènes dans certains tissus alors qu ils imitent l action des œstrogènes dans d autres tissus. Katzenellenbogen et al., (1999) ont développé le concept de pharmacologie tripartite du récepteur des œstrogènes pour expliquer l action tissu-spécifique des œstrogènes ou d autres hormones sur les récepteurs nucléaires. Trois facteurs influencent l action sélective du récepteur : la nature et structure du ligand ; le type ou isoforme du récepteur avec lequel, le ligand forme un complexe ligand-récepteur ; l interaction du complexe avec une variété de composantes par lesquelles l action du complexe est liée à la régulation transcriptionelle. Ce dernier facteur semble être la composante critique de la modulation sélective du récepteur et comprend les sites de liaison et de modulation de l ADN ainsi qu une grande variété de coactivateurs et de corépresseurs. En utilisant la cristallographie, Brzozowski et al., ont démontré que la chaîne latérale du raloxifène était responsable de l effet anti-œstrogénique de la molécule. En présence d œstrogènes, l hélice 12 du domaine de liaison se replie au-dessus de la cavité où se retrouve le ligand et forme des liens entre les hélices 3, 5/6 et 11. En présence du raloxifène, l hélice 12 ne peut pas se replier au-dessus de la cavité car la chaîne latérale du raloxifène s y retrouve. L hélice 12 se replie donc dans une cavité entre l hélice 5 et la partie terminale carboxyle de l hélice 3. Le même changement de conformation a également été observé par Shiau et al., avec le 4- hydroxytamoxifène. Il y a une grande homologie entre les domaines de liaison des récepteurs nucléaires stéroïdiens et le même effet antagoniste du déplacement de l hélice 12 a été démontré dans le récepteur bêta des œstrogènes ainsi que pour le récepteur des hormones thyroïdiennes (TR), le récepteur de l acide rétinoïque trans (RAR), et le récepteur de l acide rétinoïque 9-cis (RXR). Ce mouvement de 130 de l hélice 12, qui s installe dans une nouvelle cavité, cache un résidu de lysine présent dans cette cavité qui est très important pour le recrutement de certains cofacteurs dépendants de l hormone (Christian et al., 2005). 133
150 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Une partie hydrophobe de l hélice 12 imitant un motif LXXLL forme un lien avec l AF2, empêchant la liaison du coactivateur p160. La capacité de liaison de l hormone ou du SERM provient principalement de l anneau A et des liens hydrogène et van der Waals qu il forme avec la cavité du ligand, et n est pas en cause dans l action agoniste ou antagoniste de la molécule (fig. 24) (Tanenbaum et al., 1998 ; Deshaies et al., 2005). Figure 24 : Action agoniste et antagoniste du SERM (Deshaies et al., 2005). c. Le tamoxifène et le raloxifène Le tamoxifène est le SERM le plus utilisé dans la prévention et le traitement des cancers œstrogéno-sensibles, découvert en 1962, avant la découverte du récepteur des œstrogènes, il est aujourd hui bien implanté en première ligne de traitement et prévention, et fait l objet de milliers de publications scientifiques. Se liant au RE avec un Kd de 2 mmol/l, soit 20 fois inférieur à celui du 17 β-estradiol, le tamoxifène inhibe la croissance de cellules MCF7 et de carcinomes du tissu mammaire. Il est clair maintenant que le tamoxifène diminue grandement le risque de cancer du sein chez la femme en pré- et postménopause. Le tamoxifène module 134
151 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires également le métabolisme des lipides en diminuant le cholestérol plasmatique et en augmentant les triglycérides. Il a aussi été démontré qu il a un effet agoniste en diminuant la prise alimentaire et en diminuant la perte de masse osseuse. Malheureusement, le tamoxifène augmente de 3 à 4 fois le risque de cancer de l endomètre. De plus, plusieurs cas de stéatose hépatique ont été répertoriés dans la littérature suite à un traitement avec le tamoxifène. Il y a également un taux assez élevé de développement de résistance au tamoxifène. Pour toutes ces raisons, il n est pas conseillé de traiter avec le tamoxifène pendant plus de 5 ans afin d éviter d augmenter considérablement le risque de cancer de l endomètre (Christian et al., 2005). Plus récemment, le raloxifène, SERM de 2 ème génération, a démontré des caractéristiques comparables au tamoxifène sans toutefois en avoir les effets négatifs. Se liant avec le récepteur des œstrogènes avec sensiblement la même affinité que l œstrogène, le raloxifène a une demi-vie beaucoup plus courte que le tamoxifène et doit donc être utilisé en plus grande quantité. Le raloxifène a un effet antiprolifératif sur les cellules MCF7 comparable au tamoxifène. Chez le rat, le raloxifène diminue la croissance des tumeurs cancéreuses induites par le DMBA, mais avec une moindre efficacité que le tamoxifène. Suite à des résultats non concluants contre la progression du cancer chez des femmes résistantes au tamoxifène, les études du raloxifène pour le traitement du cancer ne se sont pas concrétisées. Cependant, le raloxifène s est avéré efficace pour la prévention et la diminution du risque de cancer du sein et ce, sans augmenter les risques d endométriose. Le raloxifène démontre, comme le tamoxifène, une capacité à diminuer la cholestérolémie et à améliorer sensiblement le profil lipidique ainsi que les facteurs de risque de maladie cardiovasculaire (Christian et al., 2005). Le raloxifène est maintenant principalement utilisé pour ses propriétés bénéfiques contre l ostéoporose, démontrant une amélioration de 2% de la densité osseuse moyenne chez les femmes traitées, réduisant ainsi significativement le risque de fracture associé à la ménopause, comme l a bien démontré l étude MORE (Multiple Outcomes of Raloxifene Evaluation trial). Malgré l absence d effet sur la cognition, le raloxifène augmente légèrement les bouffées de chaleur. Finalement, le raloxifène est associé à 135
152 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires l augmentation sérieuse du risque de thrombo-embolie veineuse (Deshaies et al., 2005). De nouvelles études sont attendues dans un futur proche sur le raloxifène et le tamoxifène dans le but de connaître les effets à long terme (CORE ; Continuing Outcomes Relevant to Evista, suite de l étude MORE) du raloxifène sur les risques de fracture et de cancer du sein (RUTH; Raloxifene Use for The Heart ) ainsi que sur l efficacité à long terme comparée entre le raloxifène et le tamoxifène (STAR; Study of Tamoxifen and Raloxifene ) Hormonothérapie chez les femmes ménopausées Anti-œstrogènes Dans les cancers du sein métastatiques, le tamoxifène permet d obtenir une réponse objective chez 34% des patientes, avec une durée médiane de réponse de 24 mois. Le taux de réponse est corrélé à l âge et au site métastatique (Kaufmann et al., 2000). a. Inhibiteurs de l aromatase En première ligne, ils montrent une efficacité supérieure à celle du tamoxifène, avec des taux de réponse plus élevés et des durée de réponse plus longues. De plus leur tolérance est équivalente à celle du tamoxifène. b. Progestatifs Les progestatifs utilisés actuellement sont le mégestrol ou la médroxyprogestérone (MPA) (Kaufmann et al., 2000). Les taux de réponse obtenus sont comparables à ceux obtenus avec le tamoxifène. Ils ne sont utilisés qu en dernier recours d hormonothérapie (Mouridsen et al., 2003). Le tableau 11 résume la réduction relative de décès et de rechute en fonction de la conduite thérapeutique (Kaufmann et Hengartner, 2001). 136
153 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Réduction Réduction Traitements Population relative de relative de rechute décès castration sans chimiothérapie % 28% castration avec chimiothérapie % - 3% analogues de LH-RH ,3% 15,1% tamoxifène % 18% Tableau 11 : Réduction de rechute et de mortalité chez les femmes non ménopausées (Kaufmann et Hengartner, 2001). Les IA sont indiqués maintenant en hormonothérapie de première ligne dans les cancers du sein métastasés RE+. Le tamoxifène vient en seconde ligne (Mauriac et al., 2003). Dans le traitement adjuvant, l utilisation des IA est incontournable. Les cancers infracliniques dont la tumeur s accompagne d un envahissement ganglionnaire doivent être traités de manière identique à ceux dont la tumeur est palpable. En revanche, les tumeurs infracliniques sans envahissement ganglionnaire ont un pronostic, après traitement locorégional bien conduit, excellent avec une survie à cinq ans de plus de 90%. Il existe cependant probablement une différence entre les formes infiltrantes et non infiltrantes ; à 20 ans on observe 95% de survie pour les premières contre 83% pour les formes infiltrantes infra-centimétriques (Lopez et Smart, 1997). Ces cancers du sein ne nécessitent donc pas de traitement complémentaire, ni chimiothérapie, ni hormonothérapie en dehors de protocoles d étude (Goldhirsch et al., 1998). En effet, les bénéfices attendus dans de telles formes pourraient être inférieurs aux risques spécifiques du traitement. Cette question se pose pour la chimiothérapie mais également pour le tamoxifène, qui réduit le risque de cancer du sein controlatéral mais qui augmente le risque d accident thrombo-embolique, de cancer de l endomètre et peut-être de cancer colique. Le tableau 12 résume les différents paramètres et la conduite thérapeutique à tenir (Beral et al., 2003). 137
154 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires Eléments En faveur de L hormonothérapie La chimiothérapie Age > 75 ans < 70 ans Délai de rechute 3 ans < 3 ans Statut hormonal Ménopause Pré-ménopause Récepteurs hormonaux + - Réponse à une hormonothérapie antérieure + - Métastases hépatiques - + Métastases osseuses + +/- Tableau 12 : Cancer du sein métastatique : éléments aidant au choix du traitement général (Beral et al., 2003). Le compte-rendu anatomo-cyto-pathologique est un document de communication entre clinicien et pathologiste. Il comporte une description et une conclusion. La conclusion doit être claire et précise. Elle indiquera, par exemple, pour une tumeur : la dénomination précise proposée par une classification internationale, par exemple de l OMS ; le caractère bénin ou malin ; l histogénèse ; la différenciation du cancer ; pour certains cancers, le grade et/ou le stade dont les références seront citées ; d autres informations seront signalées selon le type de prélèvements : biopsie exérèse : taille de la tumeur, sa distance par rapport aux différentes limites de résection ; pièce opératoire : la conclusion doit apporter les éléments aidant à l évaluation du stade clinique : taille de la tumeur, extension locale, état des limites de résection, nombre de ganglions métastatiques ; 138
155 Chapitre III Epidémiologie, dépistage et traitement des cancers mammaires prélèvement cytopathologique : le compte-rendu doit signaler la cellularité du prélèvement. Si celle-ci est insuffisante ou de mauvaise qualité, aucune conclusion ne doit être donnée, en dehors de «prélèvement non significatif» sans valeur. Il faut éviter les termes de «prélèvement positif», et surtout «prélèvement négatif» qui peut signifier sans élément malin ou «sans élément significatif». Le compte-rendu cytologique a ses «limites» par rapport au compte-rendu histologique car il manque les arguments d architecture, les relations cellules épithéliales - tissu conjonctif, et donc le caractère in situ ou invasif d un carcinome (Allred et al., 1998). 139
156 Chapitre IV Matériel et Méthodes 1. Population étudiée Trente neuf échantillons provenant de patientes atteintes de cancer du sein, opérées et traitées au CHU de Sidi Bel Abbés, ont fait l objet de notre étude. Les patientes âgées entre 22 et 70 ans ont été recrutées entre Avril 2005, et Mai Nous avons travaillé sur des pièces de mastectomie, réceptionnées au service d anatomie pathologique du CHU de SBA. Les pièces opératoires sont examinées répertoriées et codifiées par les anatomopathologistes, des prélèvements sont effectués au niveau des zones suspectes de la pièce. 2. Examen macroscopique La pièce opératoire est pesée et mesurée avec une échelle centimétrique avant sa fixation au formol 10%. L'examen macroscopique doit notifier notamment la taille du ou des nodules tumoraux et la mesure précise entre le nodule et la limite d'exérèse la plus proche. Le nombre de prélèvements à effectuer pour l'étude histologique sera fonction non seulement de de la taille de la pièce opératoire, mais aussi de la taille et de la nature des lésions tumorales (sachant que T1 est une tumeur inférieur à 2 cm, T2 est une tumeur dont la taille est comprise entre 2 à 5 cm et T3, une tumeur dont la taille est supérieure à 5 cm (OMS, 1981)). En cas de carcinome intracanalaire, les prélèvements seront très nombreux, incluant si possible la tumeur dans sa totalité à la recherche de foyers infiltrants associés. En cas de tumeur infiltrante, plusieurs prélèvements seront effectués dans les zones suspectes. Lorsqu'il s'agit d'une mammectomie complémentaire d'une tumorectomie précédente, les prélèvements seront nombreux pour rechercher des lésions tumorales résiduelles dans le lit de la tumorectomie. Lors d un curage axillaire, la dissection doit être minutieuse afin d'isoler le plus grand nombre de ganglions lymphatiques. Tous les ganglions d'un curage axillaire font l'objet d'une étude histologique. Il est nécessaire d'examiner un minimum de dix ganglions lymphatiques pour considérer l'information pronostique fournie par l'étude histologique comme fiable. 140
157 Chapitre IV Matériel et Méthodes 3. Etude histologique et immunohistochimique Les échantillons prélevés ont été traités selon des protocoles histologiques et histochimiques communs. Les protocoles d inclusion et de coloration des tumeurs mammaires, sont représentés par les tableaux 13 et 14 (annexe 2) et comprennent les etapes suivantes : confection de coupes de 4 µm d épaisseur à l aide d un microtome (annexe 3) ; montage des coupes sur des lames albuminées et bien propres sur une platine chauffante (55 C) pendant 10 minutes ; coloration des coupes selon le protocole indiqué dans le tableau 14 (annexe 4) observation à l objectif 10 et 40, et prise de photo au grossissement x 40, à l aide d un microscope microscope hund WETZLAR relié à un appareil numérique type JVC (color video camera), au centre de recherche, laboratoire de biotoxicologie. Solutions Durée Fixation formol 3 à 4% + éosine 12 heures Déshydratation Alcool 80 Alcool 90 Alcool minutes 5 minutes 5 minutes Toluène 1 5 minutes Toluène 2 5 minutes Eclaircissement Toluène 3 5 minutes Toluène 4 5 minutes Paraffine chauffée à 57 C 2 heures Paraffinage Paraffine chauffée à 57 C 2 heures Inclusion proprement dite dans des moules métalliques Tableau 13 : Protocole d inclusion des prélèvements de cancer du sein. 141
158 Chapitre IV Matériel et Méthodes Déparaffinage et réhydratation Coloration Hémalun-éosine Déshydratation Réactifs Toluène 1 Toluène 2 Alcool 100 Alcool 95 Alcool 75 Eau courante Hématoxyline de Harris Eau courante Eau chlorhydrique Eau courante Carbonate de lithium Eau courante Alcool 95 Eosine Ethanol 95 Ethanol 100 Toluène 3 Toluène 4 Durée 2 minutes 2 minutes 2 minutes 2 minutes 2 minutes 10 minutes 5 minutes 10 minutes 10 secondes 5 minutes 10 secondes 5 minutes 2 minutes 01 minute 02 minutes 02 minutes 05 minutes 05 minutes Montage entre lame et lamelle dans de l Eukitt Tableau 14 : Protocole de coloration Hémalun-éosine. La prise en charge des prélèvements mammaires pour l immunohistochimie est identique à celle de la technique standard. Tout comme la technique de coloration histologique, la prise en charge macroscopique des pièces opératoires en pathologie mammaire pour l IHC doit elle aussi tenir compte du traitement conservateur qui est la fixation. Des renseignements cliniques et mammographiques précis, ainsi qu'une information sur le type d'exérèse chirurgicale réalisée sont nécessaires pour l'évaluation correcte de ces pièces opératoires, pour prélever des endroits les plus suspects. 142
159 Chapitre IV Matériel et Méthodes 3.1. Préparation des coupes incluses en paraffine pour l IHC Fixation Les fixateurs les plus couramment utilisés en immunohistochimie sont le formol tamponné, le liquide de Bouin et le liquide de Linnert (alcool formolé). Nous avons choisi des fragments de petite taille afin d assurer une bonne fixation dans un temps bref. Et nous avons opté pour le temps de fixation le plus bref, c est à dire inférieur à 24 heures selon le protocole d immunohistochimie (Shin et al., 1998). Nous avons obtenu une fixation optimale en 6 heures pour des fragments de petites tailles, avec une bonne conservation des structures morphologie du tissu, ainsi que de l épitope et le durcissement des pièces. La surfixation peut entraîner une réticulation du tissu mammaire pouvant gêner la diffusion des produits Inclusion en paraffine Pour une bonne conservation des antigènes, nous avons inclus les tissus dans de la paraffine à 58 C. Avant l inclusionnous avons déshydrater les prélèvements avant d être coulés dans un bain de paraffine, avec immersion dans des bains d alcool de concentrations croissante. Après l inclusion dans la paraffine les blocs sont refroidis. Avant de passer à la coupe, nous avons opté pour la gélatinisation des lames, dans des bains de gélatine préparée sur place (voir annexe) afin d éviter les décollements fréquents lors des traitements thermiques qui suivent Coupes au microtome couper des rubans au microtome, les coupes doivent être d environ 3 à 4 µm d épaisseur «coupes semi fines» ; récupération des rubans coupés sur des lames gélatinées dans un bain-marie ; les laisser sécher à l étuve 24 heures à 37 C ou 48 heures à température ambiante, à l abri de la poussière ; les lames peuvent être stockées à température ambiante. 143
160 Chapitre IV Matériel et Méthodes Séchage des lames Etape très importante pour l adhésion des coupes sur les lames : une nuit à 37 C (jusqu à 48 heures) ; après séchage, les lames peuvent être stockées à + 4 C si elles sont coupées d avance Déparaffinage et réhydratation Avant d entamer l immunomarquage, il est indispensable de déparaffiner les coupes et de les réhydrater : 03 bains de xylène de 10 minutes chacun ; 03 bains d alcool de concentration décroissante, de 3 minutes chacun ; 01 bain de tampon PBS de 5 minutes Démasquage antigénique Nous avons réalisé dans une solution à ph optimal (citrate à ph 6) dans un four micro-onde deux fois 5 minutes à 750 Watt. Avantages de la technique de démasquage des antigènes augmentation de l'exposition des épitopes antigéniques à la surface des tissus ; marquage fort et fiable ; réduit les faux négatifs sur tissus inclus en paraffine et fixés au formaldéhyde ; facile à utiliser. Parmi les paramètres importants de démasquage : durée de démasquage (deux fois 5 minutes dans un micro-onde, 40 minutes dans un bain-marie) ; température de démasquage (750 Watt dans un micro-onde, 90 C dans un bainmarie) ; nature et ph de la solution (citrate ph6, TRS ph7.5) ; plus la température est élevée, plus le démasquage est rapide, mais le décollement est fréquent au delà de 100 C. Le choix de la technique de démasquage doit être adaptée à chaque laboratoire utilisant la technique, il existe trois techniques de démasquage (tableau 15). 144
161 Chapitre IV Matériel et Méthodes Technique Mode opératoire Remarques deux fois 5 minutes ; Micro-onde 100 C Cocotte 120 C bain-marie 97 C refroidir 20 minutes sur paillasse ; réajuster le niveau entre 2 passages. 5 minutes sous pression ; refroidir 20 minutes sur paillasse. 20 à 40 minutes ; refroidir 20 minutes sur paillasse. Décollements Plus reproductible, décollements Très bonne reproductibilité absence de décollements Tableau 15 : Techniques de démasquage d antigènes Blocage des peroxydases endogènes L inhibition de l activité peroxydase endogène qui est présente dans certaines cellules (polynucléaire et monocytes) afin de révéler uniquement la peroxydase apportée et liée au complexe avidine-biotine et ce grâce à l eau oxygénée. Cette technique ne concerne que les techniques utilisant la peroxydase. Le blocage de la peroxydase endogène est un phénomène réversible. H2O2 à 3% pendant 5 minutes ; rinçage à l eau distillée ; rinçage au tampon PBS, deux fois 5 minutes. 145
162 Chapitre IV Matériel et Méthodes Application de l anticorps primaire Selon la tumeur recherchée et le type de tissu, on utilise l anticorps, l'anticorps primaire est déposé directement sur le tissu et reconnaît, s'il existe, le récepteur antigénique recherché. Il faut prendre soin de bien choisir l anticorps : mono ou polyclonal, prédilué ou concentré. Nous avons utiliser lors de notre pratique des anticorps prédilués afin de standardiser la technique, et des anticorps concentrés dilués à 2% (2µl pour 200µl de dilua) pour les 4 derniers cas. La durée d incubation : 40 à 60 minutes pour les anticorps à l HER2, EMA, P53 Jusqu à une nuit à 4 C pour les anticorps délicats des récepteurs RE/RP Révélation Nous avons utiliser le kit de révélation LSAB2-HRP, qui contient deux flacons, un flacon pour l anticorps secondaire biotinylé, on ajoute ensuite quelques gouttes du deuxième flacon contenant la stréptavidine couplée à un traceur. Le principe des kits LSAB c est que les anticorps secondaires sont multi-espèces. Révélation aux chromogènes La Diaminobenzidine (DAB) ou l'acide Ethynyl-Corbazole (AEC) révèle la réaction en brun et rouge respectivement suite à une précipitation avec la peroxydase. Contre coloration Une contre-coloration douce avec l'hématoxyline de Mayer s recolore le tissu et rend possible une détermination topographique du marquage, et l appréciation des cellules non marquées. Le colorant doit être très dilué, et la durée très courte (30 secondes environ). La coloration est stable et peut être analysée à tout moment, même plusieurs années après. De même, le bloc en paraffine archivé peut être recoupé et donne la possibilité de réactions complémentaires ultérieures. 146
163 Chapitre IV Matériel et Méthodes Montage et observation Le montage des lames sur lamelles se fait grâce à un milieu aqueux spécialement conçu pour la technique d immunohistochimie, le Faramount Mounting Medium, Aqueous, qui est conservé à 4 C. Lors de l observation on doit d abord balayer le prélèvement, en changent d objectif par ordre croissant pour apprécier l intensité du marquage et le nombre des cellules marquées. balayer tout le champ pour apprécier l ensemble, passage du plus petit grossissement (3,2), puis observer à l objectif 10 toutes les cellules marquées ; apprécier l endroit du marquage à l objectif 40, pour les récepteurs hormonaux, seul le marquage nucléaire (site spécifique du récepteur) d éléments carcinomateux invasifs a une valeur reconnue. Pour les autres marqueurs tel que l EMA et HER2, seul le marquage membranaire est pris en compte ; l analyse des marquages doit aboutir à déterminer la proportion des cellules marquées par rapport à l ensemble des cellules carcinomateuses dans le contingent invasif en éliminant les structures intra-canalaires (pourcentage arrondi à la dizaine) ; l intensité moyenne du marquage est appréciée sur une échelle qualitative de 0 à 3 (absente, faible, modérée, forte). Si plus de 10% des cellules sont marquées dans le champ de l observation, le résultat est positif, 10% est la valeur seuil. Nous avons par la suite réalisé des prises de photos au grossissement x 40 et x 100 à l aide du microscope hund WETZLAR relié à un appareil numérique type JVC (color video camera). La valeur seuil admise lors de notre travail est la valeur recommandée de 10% des cellules marquées. Ce seuil de 10% a été utilisé par plusieurs études avec corrélations cliniques ou comparaison avec les dosages biochimiques (valeur seuil de 10 fmol/mg de tissu). 147
164 Chapitre IV Matériel et Méthodes 3.2. Protocole de détection des récepteurs hormonaux sur tissus inclus en paraffine-lsab2 - Démasquage micro-onde et bain-marie Cette technique est basée sur l affinité de la biotine pour la streptavidine. La streptavidine présente 4 sites de liaisons à la biotine suivant une constante d affinité très élevée de M. Dans cette technique, un anticorps non couplé réagit avec l antigène du tissu. Un anticorps secondaire couplé à la biotine et dirigé contre l anticorps primaire est ajouté sur le tissu. La troisième étape consiste à ajouter une streptavidine directement couplée à l enzyme, d où le nom de la technique : LSAB (Labelled Strept Avidine Biotine). Préparation des anticorps Diluer le RE au 1/40 ème et le RP au 1/50 ème si on dispose d anticorps concentrés, si ces derniers sont prédilués on peut les utiliser directement. Le protocole des RP pour lequel, on à opté est le protocole utilisant le bain-marie avec une solution de restauration TRS, celle-ci doit être préchauffé avec la solution de démasquage à 98 C, pour celui des RE, on à utiliser le micro-onde et citrate comme solution de démasquage. Déparaffinage et réhydratation xylène 3 x 10 minutes alcool minutes alcool minutes alcool minutes rinçage à l eau distillée Démasquage antigénique à la chaleur Pour RE Les lames sont placées dans un portoir en verre, puis transférées dans un bac en plastique plongées dans une solution citrate à ph 6, le temps de démasquage est 148
165 Chapitre IV Matériel et Méthodes de deux fois 5 minutes, après chaque tour, on équilibre la solution pour éviter l évaporation, puis refroidissement sur paillasse pendant 20 minutes. Pour RP La solution de démasquage est préchaffée au bain-marie à 98 C, les lames sont ensuite placées dans la solution TRS, pendant 40 minutes. Puis refroidissement sur paillasse pendant 20 minutes. Rinçage à l eau distillée et lavage au PBS 5 minutes. Immunomarquage Blocage des peroxydases endogènes incubation avec l H2O2 pendant 10 minutes ; rinçage à l eau distillée ; rinçage au PBS pendant 5 minutes. Anticorps primaire incuber avec l anticorps primaire souris anti-récepteurs à l œstrogène humain prédilué clone 1D5 pendant 24 heures dans une chambre humide couverte ; incuber avec l anticorps primaire souris anti-récepteurs à la progestérone humain prédilué clone PgR 636 pendant 24 heures dans une chambre humide couverte. Il existe un kit commercialisé par DAKO pour la détection des récepteurs hormonaux, où l incubation de l anticorps primaire ne dure que 45 minutes avec un rinçage au PBS deux fois 5 minutes. Anticorps secondaire anticorps Multi-Link : incuber avec l anticorps secondaire biotinylé pendant 15 à 20 minutes ; rinçage au PBS. streptavidine-hrp : incuber avec la streptavidine pendant 15 à 20 minutes ; rinçage au PBS. 149
166 Chapitre IV Matériel et Méthodes Chromogène Nous avons utilisé l AEC pour la détection des récepteurs hormonaux, on applique l AEC et on laisse incuber le maximum de temps tout en contrôlant la formation du précipité sous le microscope ensuite rinçage à l eau distillée. Contre coloration et observation au microscope Nous avons utilisé l hématoxyline de Mayer s légère pendant 40 secondes, afin d éviter de masquer le marquage, ensuite montage des lames et observation au grossissement x 40 et x Protocole de détection de l HER2 sur tissus inclus en paraffine. Démasquage au bain-marie Nous avons utilisé le kit HercepTest pour le dosage immunohistochimique de la surexpression de la protéine HER2 dans le cancer du sein, ce kit contient un anticorps primaire de lapin qui se lie à cette protéine, et la réaction Ac-Ag est détectée grâce au réactif de visualisation fournie avec le kit. Protocole de marquage Etape 1 Après déparaffinage et réhydratation, on a procédé aux étapes suivantes : préchauffage de la solution de restauration à C au bain-marie, ensuite immerger les coupes déparaffinées dans le bac de solution pendant 40 minutes ; refroidissement pendant 20 minutes ; tremper les lames dans la solution de rinçage pendant 5 minutes. Etape 2 appliquer trois gouttes de la solution de blocage de la peroxydase, recouvrir et laisser 5 minutes ; rinçage à l eau distillée. Etape 3 : Anticorps primaire recouvrir l échantillon de trois gouttes de l anticorps primaire pendant 30 minutes ; 150
167 Chapitre IV Matériel et Méthodes rinçage au tampon de lavage. Etape 4 : Réactif de visualisation recouvrir l échantillon de trois gouttes de réactif de visualisation, laisser incuber pendant 30 minutes. Etape 5 : Substrate-Chromogène Solution DAB recouvrir l échantillon de trois gouttes de DAB pendant 10 minutes ; rinçage à l eau distillée. Etape 6 : Coloration de contraste immerger les lames dans un bain d hématoxyline de Mayer s pendant 2 à 5 minutes. Etape 7 : Montage on a utilisé un médium de montage permanent et aqueux. Lecture des lames L appréciation du marquage grâce au microscope ne prend en considération que les marquages membranaires, avec un seuil de positivité de 10% de cellules marquées, au grossissement x Protocole de détection de l Actnine, EMA, Cytokératine, Vimentine, P53 Le protocole adopté pour les autres anticorps est celui du bain-marie avec solution de restauration TRS, préchauffé à 98 C, le citrate a été utilisé pour les RE seulement, après plusieurs essais et comparaisons entre les deux solutions. Le protocole est le même pour les anticorps ; l Actnine, l EMA, la Cytokératine, la Vimentine, et la P53, la différence avec les récepteurs hormonaux se situe au niveau du temps d incubation (24heures pour les RH, et 60 minutes pour les anticorps sus cités), et le citrate pour les RE. Déparaffinage et réhydratation xylène 3 x 10 minutes alcool minutes 151
168 Chapitre IV Matériel et Méthodes alcool minutes alcool minutes rinçage à l eau distillée Démasquage antigénique à la chaleur La solution de démasquage est préchauffée au bain-marie à une température de 98 C, les lames sont ensuite placées dans la solution TRS pendant 40 minutes, puis refroidissement sur paillasse pendant 20 minutes. Un rinçage à l eau distillée et lavage au PBS pendant 5 minutes sont réalisés. Immunomarquage Blocage des peroxydases endogènes incubation avec l H2O2 pendant 10 minutes ; rinçage à l eau distillée ; rinçage au PBS pendant 5 minutes. Anticorps primaire Incuber avec l anticorps primaire dans une chambre humide couverte : l anticorps monoclonal de souris anti-humain clone 1A4 pour l actine ; l anticorps monoclonal de souris anti-humain clone AE1 pour la cytokératine ; l anticorps monoclonal de souris anti-humain clone E29 pour l EMA ; l anticorps monoclonal de souris anti-humain clone DO-7 pour la P53 ; l anticorps monoclonal de souris anti-humain clone V9 pour la vimentine ; la durée de l incubation est de 60 minutes dans une chambre humide couverte. Anticorps secondaire Anticorps Multi-Link : incuber avec l anticorps secondaire biotinylé pendant 15 à 20 minutes ; rinçage au PBS. streptavidine-hrp : incuber avec la streptavidine pendant 15 à 20 minutes. rinçage au PBS 152
169 Chapitre IV Matériel et Méthodes Chromogène On a utilisé l AEC pour la détection des récepteurs hormonaux, ainsi que pour les autres anticorps, on applique l AEC et on laisse incuber le maximum de temps tout en contrôlant la formation du précipité sous le microscope, ensuite un rinçage à l eau distillée est réalisée. Contre coloration On a utilisé l hématoxyline de Mayer s pendant 40 secondes, afin d éviter de masquer le marquage ensuite montage des lames et observation. L appréciation du marquage au microscope se fait en considérant les marquages membranaires pour EMA, cytoplasmiques pour cytokératine et l actine ainsi que la vimentine, pour la P53 c est un marquage nucléaire. A été admis le seuil de 10% de positivité pour tout types de marquage. 153
170 Chapitre V Résultats et Discussion Le diagnostic anatomopathologique des tumeurs a longtemps reposé sur la seule analyse morphologique des lésions en technique standard, l application il y a une vingtaine d années de l immunohistochimie dans l arsenal diagnostic, à rendu possible l étiquetage précis d un grand nombre de tumeurs malignes indifférenciées. 1. Résultats de l étude histologique L étude anatomopathologique et immunohistochimique des échantillons mammaires a concerné 39 femmes atteintes de cancer du sein. L âge des patientes recrutées pour notre étude est compris entre 22 et 70 ans, l âge moyen de survenue du cancer du sein chez ces femmes est de 38,5 ans, le pic de fréquence se situe entre 40 et 49 ans (fig. 25), 61% des femmes sont menopausées, et 39 % ne le sont pas (fig. 26). 154
171 Chapitre V Résultats et Discussion % des carcinomes 40% 35% 30% 25% 20% 15% 10% 5% 0% 8,33% 16,66% 38,88% 25% 8,33% 2,77% Tranches d'âge (ans) Figure 25 : Evaluation du taux des carcinomes en fonction de l âge (%). Femmes ménopausées Femmes non ménopausées Femmes non ménopausées 39% Femmes ménopausées 61% Figure 26 : Statut hormonal des 39 patientes. 155
172 Chapitre V Résultats et Discussion La taille de la tumeur a été prise en concidération chez les 39 cas de carcinomes mammaires qui ont été répartis en 3 groupes de taille : T1, T2 et T3 (sachant que T1 est une tumeur inférieur à 2 cm, T2 est une tumeur dont la taille est comprise entre 2 à 5 cm et T3, une tumeur dont la taille est supérieure à 5 cm (OMS, 1981)). 23,07% de notre échantillon a presenté une taille de type T1, dû probablement aux dépistages précoces qui permettent la découverte des tumeurs au début de leur déclenchement, la fréquence des tumeurs de taille T2 est de 28,21%, par contre la taille T3 est la plus fréquente (48,72%), avec souvent un état très évolué (fig. 27). En examinant la totalité de notre échantillon, nous avons noté 14 cas (soit 36%) sans envahissement ganglionnaire (N-) et 25 cas (soit 64%) avec envahissement ganglionnaire (N+) (fig. 28). 50% 48,72% T1 (< 2 cm) 5 cm > T2 > 2 cm Pourcentage 40% 30% 20% 10% 23,07% 28,21% T3 > 5 cm 0% T1 (< 2 cm) 5 cm > T2 > 2 cm T3 > 5 cm Taille de la tumeur Figure 27 : Répartition des carcinomes selon la taille de la tumeur (en cm). Absence de ganglions (N-) Présence de ganglions (N+) Absence de ganglions (N-) 36% Présence de ganglions (N+) 64% Figure 28 : Répartition des carcinomes selon l envahissement ganglionnaire 156
173 Chapitre V Résultats et Discussion La classification histopronostic selon Scarff Bloom Richardson (SBR) a revélé 61% cas à grade II, 17% de cas à grade I, et une fréquence intermédiaire de 22% pour les carcinomes de grade III (fig. 29). Le rôle du grade histopronostic est maintenant largement admis pour les tumeurs carcinomateuses infiltrantes. La méthode du grading SBR consiste à évaluer 3 paramètres morphologiques avec des scores. Notre série comporte des carcinomes infiltrant de grade différents, avec une composante de 61% de carcinomes canalaires infiltrant (CCI) (Planche I), 15% de types mixtes «canalaire et lobulaire à la fois» (CCL), 12% de tumeurs phyllode (conjonctif et épithéliale), et 12% de carcinomes lobulaire infiltrant (CLI) (fig. 30). Grade III 22% Grade I 17% Grade I Grade II Grade III Grade II 61% Figure 29 : Répartition des carcinomes selon le grade histopronostic de Scarff et Bloom Richardson (SBR) CCL 15% Phyllode 12% CCI CLI CCL Phyllode CLI 12% CCI 61% Figure 30 : Répartition des carcinomes selon le type histologique. 157
174 Chapitre V Résultats et Discussion Pour chaque type histologique, nous avons retenu les fréquences des grades histopronostiques représentées par les histogrammes suivants : Pour les carcinome canalaire infiltrant CCI On remarque une nette prédominance du grade II pour les carcinomes canalaires infiltrants (fig. 31). Pour les carcinome lobulaire infiltrant CLI Prédominance du grade II pour les carcinomes lobulaires infiltrants (fig. 32). Pour les carcinome canalaire et lobulaire infiltrant CCLI Prédominance du grade II pour les carcinomes canalaires et lobulaires infiltrants (fig. 33). Pour les tumeurs phyllode Fréquence égale des grades I et III avec une quasi-absence du grade II pour ce type de tumeur, contrairement aux autres types histologiques (fig. 34). 70% 61,62% 60% 50% % des CCI 40% 30% 16,16% 22,22% 20% 10% 0% Grade I Grade II Grade III Grade Figure 31 : Répartition selon le grade histopronosticque de SBR des carcinomes canalaires infiltrants. 158
Qu est-ce que le cancer du sein?
 Cancer du sein Qu est-ce que le cancer du sein? Laissez-nous vous expliquer. www.fondsanticancer.org www.esmo.org ESMO/FAC Patient Guide Series basés sur les recommandations de pratique clinique de ESMO
Cancer du sein Qu est-ce que le cancer du sein? Laissez-nous vous expliquer. www.fondsanticancer.org www.esmo.org ESMO/FAC Patient Guide Series basés sur les recommandations de pratique clinique de ESMO
Cancer du sein in situ
 traitements et soins octobre 2009 recommandations professionnelles Cancer du sein COLLECTION recommandations & référentiels Recommandations de prise en charge spécialisée Carcinome canalaire et carcinome
traitements et soins octobre 2009 recommandations professionnelles Cancer du sein COLLECTION recommandations & référentiels Recommandations de prise en charge spécialisée Carcinome canalaire et carcinome
Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic de cancer
 Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
TUMEURS DU BAS APPAREIL URINAIRE
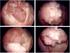 1 Plan de cours I - TUMEURS PRIMITIVES DE LA VESSIE c1 - Tumeurs papillaires non infiltrantes c2 - Tumeurs papillaires infiltrantes c3 - Carcinome in-situ en muqueuse plane D - Pronostic : II - TUMEURS
1 Plan de cours I - TUMEURS PRIMITIVES DE LA VESSIE c1 - Tumeurs papillaires non infiltrantes c2 - Tumeurs papillaires infiltrantes c3 - Carcinome in-situ en muqueuse plane D - Pronostic : II - TUMEURS
Dépistage et prévention du cancer du sein
 Actualisation du référentiel de pratiques de l examen périodique de santé Dépistage et prévention du cancer du sein Février 2015 État des connaissances sur le cancer du sein Structure anatomique et aspect
Actualisation du référentiel de pratiques de l examen périodique de santé Dépistage et prévention du cancer du sein Février 2015 État des connaissances sur le cancer du sein Structure anatomique et aspect
Dr E. CHEVRET UE2.1 2013-2014. Aperçu général sur l architecture et les fonctions cellulaires
 Aperçu général sur l architecture et les fonctions cellulaires I. Introduction II. Les microscopes 1. Le microscope optique 2. Le microscope à fluorescence 3. Le microscope confocal 4. Le microscope électronique
Aperçu général sur l architecture et les fonctions cellulaires I. Introduction II. Les microscopes 1. Le microscope optique 2. Le microscope à fluorescence 3. Le microscope confocal 4. Le microscope électronique
IRM du Cancer du Rectum
 IRM du Cancer du Rectum quels CHOIX TECHNIQUES pour quels OBJECTIFS THERAPEUTIQUES? Frank Boudghène, T. Andre, A. Stivalet, I. Frey, L. Paslaru, V. Ganthier, M. Tassart Hopital Tenon - Université Paris
IRM du Cancer du Rectum quels CHOIX TECHNIQUES pour quels OBJECTIFS THERAPEUTIQUES? Frank Boudghène, T. Andre, A. Stivalet, I. Frey, L. Paslaru, V. Ganthier, M. Tassart Hopital Tenon - Université Paris
Biomarqueurs en Cancérologie
 Biomarqueurs en Cancérologie Définition, détermination, usage Biomarqueurs et Cancer: définition Anomalie(s) quantitative(s) ou qualitative(s) Indicative(s) ou caractéristique(s) d un cancer ou de certaines
Biomarqueurs en Cancérologie Définition, détermination, usage Biomarqueurs et Cancer: définition Anomalie(s) quantitative(s) ou qualitative(s) Indicative(s) ou caractéristique(s) d un cancer ou de certaines
Recommandations 2005. Prise en charge des patients adultes atteints d un mélanome cutané MO
 Recommandations 2005 Prise en charge des patients adultes atteints d un mélanome cutané MO Recommandations pour la Pratique Clinique : Standards, Options et Recommandations 2005 pour la prise en charge
Recommandations 2005 Prise en charge des patients adultes atteints d un mélanome cutané MO Recommandations pour la Pratique Clinique : Standards, Options et Recommandations 2005 pour la prise en charge
Comprendre. le Cancer du sein. Mise à jour. Guide d information et de dialogue à l usage des personnes malades et de leurs proches
 Comprendre le Cancer du sein Mise à jour Guide d information et de dialogue à l usage des personnes malades et de leurs proches Ce guide s inscrit dans le cadre d un programme réalisé en partenariat avec
Comprendre le Cancer du sein Mise à jour Guide d information et de dialogue à l usage des personnes malades et de leurs proches Ce guide s inscrit dans le cadre d un programme réalisé en partenariat avec
Test d immunofluorescence (IF)
 Test d immunofluorescence (IF) 1.1 Prélèvement du cerveau et échantillonnage Avant toute manipulation, il est fondamental de s assurer que tout le personnel en contact avec un échantillon suspect soit
Test d immunofluorescence (IF) 1.1 Prélèvement du cerveau et échantillonnage Avant toute manipulation, il est fondamental de s assurer que tout le personnel en contact avec un échantillon suspect soit
Recherche Information - prévention - dépistage Actions pour les malades et leurs proches. Les cancers du sein
 Recherche Information - prévention - dépistage Actions pour les malades et leurs proches Les cancers du sein G R A N D P U B L I C Les cancers du sein Aujourd'hui, en France, comme dans de nombreux pays
Recherche Information - prévention - dépistage Actions pour les malades et leurs proches Les cancers du sein G R A N D P U B L I C Les cancers du sein Aujourd'hui, en France, comme dans de nombreux pays
Recommandations régionales Prise en charge des carcinomes cutanés
 Recommandations régionales Prise en charge des carcinomes cutanés - décembre 2009 - CARCINOMES BASOCELLULAIRES La chirurgie : traitement de référence et de 1 ère intention Classification clinique et histologique
Recommandations régionales Prise en charge des carcinomes cutanés - décembre 2009 - CARCINOMES BASOCELLULAIRES La chirurgie : traitement de référence et de 1 ère intention Classification clinique et histologique
Qu est-ce qu un sarcome?
 Qu est-ce qu un sarcome? Qu est-ce qu une tumeur? Une tumeur est une prolifération anormale de cellules. Les tumeurs ne devraient donc pas automatiquement être associées à un cancer. Certaines tumeurs
Qu est-ce qu un sarcome? Qu est-ce qu une tumeur? Une tumeur est une prolifération anormale de cellules. Les tumeurs ne devraient donc pas automatiquement être associées à un cancer. Certaines tumeurs
Les différents types de cancers et leurs stades. Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07
 Les différents types de cancers et leurs stades Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07 CARCINOGENESE multiple steps, accumulation d altd altérations continuum lésionnel
Les différents types de cancers et leurs stades Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07 CARCINOGENESE multiple steps, accumulation d altd altérations continuum lésionnel
Cancer du sein in situ
 traitements, soins et innovation OCTOBRE 2009 recommandations professionnelles Cancer du sein in situ COLLECTION recommandations & référentiels Recommandations de prise en charge spécialisée Carcinome
traitements, soins et innovation OCTOBRE 2009 recommandations professionnelles Cancer du sein in situ COLLECTION recommandations & référentiels Recommandations de prise en charge spécialisée Carcinome
DES de Pathologie AFIAP
 DES de athologie AFIA 21 novembre 2009 J. Audouin,, S. ain IMMUNOHISTOCHIMIE Introduction I - Différentes méthodes AC conjugués Enzyme - anti-enzyme : A, AAA rotéine conjuguée : avidine, streptavidine
DES de athologie AFIA 21 novembre 2009 J. Audouin,, S. ain IMMUNOHISTOCHIMIE Introduction I - Différentes méthodes AC conjugués Enzyme - anti-enzyme : A, AAA rotéine conjuguée : avidine, streptavidine
TECHNIQUES D AVENIR LASER DOPPLER IMAGING LASER DOPPLER IMAGING LASER DOPPLER IMAGING
 TECHNIQUES D AVENIR Jonathan LONDNER, Aurélie HAUTIER Centre Régional de Traitement des Grands Brûlés Service de chirurgie Plastique, Hôpital de la Conception, Marseille. DIAGNOSTIC DÉTERSION BOURGEONNEMENT
TECHNIQUES D AVENIR Jonathan LONDNER, Aurélie HAUTIER Centre Régional de Traitement des Grands Brûlés Service de chirurgie Plastique, Hôpital de la Conception, Marseille. DIAGNOSTIC DÉTERSION BOURGEONNEMENT
Le cliché thoracique
 Le cliché thoracique Date de création du document 2008-2009 Table des matières * Introduction... 1 1 Nomenclature radiologique... 1 2 Le cliché thoracique de face... 2 2. 1 Qualité du cliché... 1 2. 2
Le cliché thoracique Date de création du document 2008-2009 Table des matières * Introduction... 1 1 Nomenclature radiologique... 1 2 Le cliché thoracique de face... 2 2. 1 Qualité du cliché... 1 2. 2
ANTICORPS POLYCLONAUX ANTI IMMUNOGLOBULINES
 L OUTIL IDEAL POUR TOUTES LES DETECTIONS IMMUNOCHIMIQUES pour toutes les techniques immunodosages (EIA/ELISA) dot/ westernblot immunohistochimie immunocytochimie cytométrie en flux quel que soit le système
L OUTIL IDEAL POUR TOUTES LES DETECTIONS IMMUNOCHIMIQUES pour toutes les techniques immunodosages (EIA/ELISA) dot/ westernblot immunohistochimie immunocytochimie cytométrie en flux quel que soit le système
www.gbo.com/bioscience 1 Culture Cellulaire Microplaques 2 HTS- 3 Immunologie/ HLA 4 Microbiologie/ Bactériologie Containers 5 Tubes/ 6 Pipetage
 2 HTS 3 Immunologie / Immunologie Informations Techniques 3 I 2 ELISA 96 Puits 3 I 4 ELISA 96 Puits en Barrettes 3 I 6 en Barrettes de 8 Puits 3 I 7 en Barrettes de 12 Puits 3 I 8 en Barrettes de 16 Puits
2 HTS 3 Immunologie / Immunologie Informations Techniques 3 I 2 ELISA 96 Puits 3 I 4 ELISA 96 Puits en Barrettes 3 I 6 en Barrettes de 8 Puits 3 I 7 en Barrettes de 12 Puits 3 I 8 en Barrettes de 16 Puits
Sujets présentés par le Professeur Olivier CUSSENOT
 ANAMACaP Association Nationale des Malades du Cancer de la Prostate 17, bis Avenue Poincaré. 57400 SARREBOURG Sujets présentés par le Professeur Olivier CUSSENOT Place des nouvelles techniques d imagerie
ANAMACaP Association Nationale des Malades du Cancer de la Prostate 17, bis Avenue Poincaré. 57400 SARREBOURG Sujets présentés par le Professeur Olivier CUSSENOT Place des nouvelles techniques d imagerie
Les grands syndromes. Endoscopie trachéo-bronchique. Professeur D. ANTHOINE CHU de NANCY
 Les grands syndromes Endoscopie trachéo-bronchique Professeur D. ANTHOINE CHU de NANCY 1 Endoscopie souple avec pince et brosse (fibroscopie) 2 Endoscopie Arbre bronchique normal Bifurcation trachéobronchique
Les grands syndromes Endoscopie trachéo-bronchique Professeur D. ANTHOINE CHU de NANCY 1 Endoscopie souple avec pince et brosse (fibroscopie) 2 Endoscopie Arbre bronchique normal Bifurcation trachéobronchique
Quels sont les facteurs qui font augmenter les risques de cancer du rein?
 Qu est-ce que le cancer du rein? L adénocarcinome rénal est le type le plus fréquent de cancer du rein 1. Le rôle des reins consiste à filtrer le sang et à évacuer les déchets de l organisme dans l urine.
Qu est-ce que le cancer du rein? L adénocarcinome rénal est le type le plus fréquent de cancer du rein 1. Le rôle des reins consiste à filtrer le sang et à évacuer les déchets de l organisme dans l urine.
HMB-45 + Mart-1 (Melan A) + Tyrosinase (HMB-45+A103+T311)
 HMB-45 + Mart-1 (Melan A) + Tyrosinase Identification du Produit Réf. cat. Description 45318 IMPATH HMB-45&MART-1 RTU M (HMB-45&MelanA) Définitions Des Symboles P A E S DOC# DIS prêt à l emploi ascite
HMB-45 + Mart-1 (Melan A) + Tyrosinase Identification du Produit Réf. cat. Description 45318 IMPATH HMB-45&MART-1 RTU M (HMB-45&MelanA) Définitions Des Symboles P A E S DOC# DIS prêt à l emploi ascite
Pour l'instant, les connaissances actuelles ne permettent pas d'empêcher un cancer du sein de survenir.
 Dépistage Pour l'instant, les connaissances actuelles ne permettent pas d'empêcher un cancer du sein de survenir. Par contre, nous pouvons tenter de le dépister plus tôt afin d'avoir plus de chances de
Dépistage Pour l'instant, les connaissances actuelles ne permettent pas d'empêcher un cancer du sein de survenir. Par contre, nous pouvons tenter de le dépister plus tôt afin d'avoir plus de chances de
Actualités s cancérologiques : pneumologie
 Actualités s cancérologiques : pneumologie PLAN Incidence / facteurs de risque Anatomie Symptômes Types de tumeurs Diagnostic / extension Classification Traitement Pronostic Pneumologie : incidence Belgique
Actualités s cancérologiques : pneumologie PLAN Incidence / facteurs de risque Anatomie Symptômes Types de tumeurs Diagnostic / extension Classification Traitement Pronostic Pneumologie : incidence Belgique
GUIDE - AFFECTION LONGUE DURÉE. Tumeur maligne, affection maligne du tissu lymphatique ou hématopoïétique. Cancer du sein
 GUIDE - AFFECTION LONGUE DURÉE Tumeur maligne, affection maligne du tissu lymphatique ou hématopoïétique Cancer du sein Janvier 2010 Ce document s inscrit dans un double dispositif : La mise en œuvre de
GUIDE - AFFECTION LONGUE DURÉE Tumeur maligne, affection maligne du tissu lymphatique ou hématopoïétique Cancer du sein Janvier 2010 Ce document s inscrit dans un double dispositif : La mise en œuvre de
I - CLASSIFICATION DU DIABETE SUCRE
 I - CLASSIFICATION DU DIABETE SUCRE 1- Définition : Le diabète sucré se définit par une élévation anormale et chronique de la glycémie. Cette anomalie est commune à tous les types de diabète sucré, mais
I - CLASSIFICATION DU DIABETE SUCRE 1- Définition : Le diabète sucré se définit par une élévation anormale et chronique de la glycémie. Cette anomalie est commune à tous les types de diabète sucré, mais
Planches pour le Diagnostic microscopique du paludisme
 République Démocratique du Congo Ministère de la Santé Programme National de Lutte Contre le Paludisme Planches pour le Diagnostic microscopique du paludisme Ces planches visent à améliorer le diagnostic
République Démocratique du Congo Ministère de la Santé Programme National de Lutte Contre le Paludisme Planches pour le Diagnostic microscopique du paludisme Ces planches visent à améliorer le diagnostic
AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE
 AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE CONCOURS EXTERNE Session 2005 TRAVAUX PRATIQUES DE BIOCHIMIE PHYSIOLOGIE ALCOOL ET FOIE L éthanol, psychotrope puissant, est absorbé passivement dans l intestin
AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE CONCOURS EXTERNE Session 2005 TRAVAUX PRATIQUES DE BIOCHIMIE PHYSIOLOGIE ALCOOL ET FOIE L éthanol, psychotrope puissant, est absorbé passivement dans l intestin
Cancers de l hypopharynx
 Cancers de l hypopharynx A- GENERALITES 1) Epidémiologie Cancer fréquent et de pronostic grave du fait de son évolution insidieuse et de son caractère lymphophile. C est quasiment toujours un carcinome
Cancers de l hypopharynx A- GENERALITES 1) Epidémiologie Cancer fréquent et de pronostic grave du fait de son évolution insidieuse et de son caractère lymphophile. C est quasiment toujours un carcinome
Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA. Doctorant: Camelia MICU (DEMETRIAN)
 UNIVERSITÉ DE MÉDECINE ET PHARMACIE DE CRAIOVA FACULTÉ DE MÉDECINE CONTRIBUTIONS A L'ÉTUDE CLINIQUE ET MORPHOLOGIQUE DES CANCERS DU POUMON Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA Doctorant:
UNIVERSITÉ DE MÉDECINE ET PHARMACIE DE CRAIOVA FACULTÉ DE MÉDECINE CONTRIBUTIONS A L'ÉTUDE CLINIQUE ET MORPHOLOGIQUE DES CANCERS DU POUMON Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA Doctorant:
LASER DOPPLER. Cependant elle n est pas encore utilisée en routine mais reste du domaine de la recherche et de l évaluation.
 LASER DOPPLER INTRODUCTION La technique qui utilise l effet Doppler à partir d un faisceau laser est l une des seules qui permette d enregistrer en continu le reflet de la perfusion superficielle de tissus
LASER DOPPLER INTRODUCTION La technique qui utilise l effet Doppler à partir d un faisceau laser est l une des seules qui permette d enregistrer en continu le reflet de la perfusion superficielle de tissus
5.5.5 Exemple d un essai immunologique
 5.5.5 Exemple d un essai immunologique Test de grossesse Test en forme de bâtonnet destiné à mettre en évidence l'hormone spécifique de la grossesse, la gonadotrophine chorionique humaine (hcg), une glycoprotéine.
5.5.5 Exemple d un essai immunologique Test de grossesse Test en forme de bâtonnet destiné à mettre en évidence l'hormone spécifique de la grossesse, la gonadotrophine chorionique humaine (hcg), une glycoprotéine.
Le reflux gastro-oesophagien (280) Professeur Jacques FOURNET Avril 2003
 Pré-Requis : Corpus Médical Faculté de Médecine de Grenoble Le reflux gastro-oesophagien (280) Professeur Jacques FOURNET Avril 2003 Sécrétion acide et peptique de l estomac Motricité œsophagienne et gastrique
Pré-Requis : Corpus Médical Faculté de Médecine de Grenoble Le reflux gastro-oesophagien (280) Professeur Jacques FOURNET Avril 2003 Sécrétion acide et peptique de l estomac Motricité œsophagienne et gastrique
TUTORAT UE 5 2012-2013 Anatomie Correction Séance n 6 Semaine du 11/03/2013
 TUTORAT UE 5 2012-2013 Anatomie Correction Séance n 6 Semaine du 11/03/2013 Appareil respiratoire-organogénèse de l appareil digestif Cours du Pr. PRUDHOMME Séance préparée par Anissa BARAKAT, Caroline
TUTORAT UE 5 2012-2013 Anatomie Correction Séance n 6 Semaine du 11/03/2013 Appareil respiratoire-organogénèse de l appareil digestif Cours du Pr. PRUDHOMME Séance préparée par Anissa BARAKAT, Caroline
Rôle des acides biliaires dans la régulation de l homéostasie du glucose : implication de FXR dans la cellule bêta-pancréatique
 Rôle des acides biliaires dans la régulation de l homéostasie du glucose : implication de FXR dans la cellule bêta-pancréatique Tuteur : Anne Muhr-Tailleux cardiovasculaires et diabète (Equipe 1) Institut
Rôle des acides biliaires dans la régulation de l homéostasie du glucose : implication de FXR dans la cellule bêta-pancréatique Tuteur : Anne Muhr-Tailleux cardiovasculaires et diabète (Equipe 1) Institut
PLACE DE L IRM DANS LE BILAN D EXTENSION DU CANCER DU RECTUM. Professeur Paul LEGMANN Radiologie A - Cochin Paris
 PLACE DE L IRM DANS LE BILAN D EXTENSION DU CANCER DU RECTUM Professeur Paul LEGMANN Radiologie A - Cochin Paris Cancer du rectum France : 15000 décès/an : 1ère cause. Pronostic souvent réservé Métastases
PLACE DE L IRM DANS LE BILAN D EXTENSION DU CANCER DU RECTUM Professeur Paul LEGMANN Radiologie A - Cochin Paris Cancer du rectum France : 15000 décès/an : 1ère cause. Pronostic souvent réservé Métastases
Peut-on ne pas reprendre des marges «insuffisantes» en cas de Carcinome canalaire infiltrant
 Peut-on ne pas reprendre des marges «insuffisantes» en cas de Carcinome canalaire infiltrant Institut Cancérologie de l Ouest CHIRURGIE Dr. Isabelle Jaffré CAS CLINIQUE 1 36 ans 90B sans CI radiothérapie
Peut-on ne pas reprendre des marges «insuffisantes» en cas de Carcinome canalaire infiltrant Institut Cancérologie de l Ouest CHIRURGIE Dr. Isabelle Jaffré CAS CLINIQUE 1 36 ans 90B sans CI radiothérapie
UNE INTERVENTION CHIRURGICALE AU NIVEAU DU SEIN
 UNE INTERVENTION CHIRURGICALE AU NIVEAU DU SEIN Informations générales Pour vous, pour la vie Cette brochure vise à vous fournir des informations générales concernant l intervention chirurgicale que vous
UNE INTERVENTION CHIRURGICALE AU NIVEAU DU SEIN Informations générales Pour vous, pour la vie Cette brochure vise à vous fournir des informations générales concernant l intervention chirurgicale que vous
Cordarone et Thyroïde par François Boustani
 Physiologie de la thyroïde : l hormonosynthèse thyroïdienne se fait à partir de l iode essentiellement d origine digestive et de la thyroglobuline qui est une protéine synthétisée par la thyroïde à partir
Physiologie de la thyroïde : l hormonosynthèse thyroïdienne se fait à partir de l iode essentiellement d origine digestive et de la thyroglobuline qui est une protéine synthétisée par la thyroïde à partir
Leucémies de l enfant et de l adolescent
 Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Maladie de Hodgkin ou lymphome de Hodgkin
 Maladie de Hodgkin ou lymphome de Hodgkin Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca MALADIE DE HODGKIN Ce que vous devez savoir Même si vous entendez parler du
Maladie de Hodgkin ou lymphome de Hodgkin Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca MALADIE DE HODGKIN Ce que vous devez savoir Même si vous entendez parler du
RAPPORT DU CONTROLE DE MARCHE DES DISPOSITIFS MEDICAUX DE DIAGNOSTIC IN VITRO DE DOSAGE DE THYROGLOBULINE
 Direction de l'evaluation des Dispositifs Médicaux Département Surveillance du Marché Unité Evaluation et Contrôle du Marché - DIV RAPPORT DU CONTROLE DE MARCHE DES DISPOSITIFS MEDICAUX DE DIAGNOSTIC IN
Direction de l'evaluation des Dispositifs Médicaux Département Surveillance du Marché Unité Evaluation et Contrôle du Marché - DIV RAPPORT DU CONTROLE DE MARCHE DES DISPOSITIFS MEDICAUX DE DIAGNOSTIC IN
Moyens d étude de la peau
 Moyens d étude de la peau Dr. Yannick Le Corre yalecorre@chu-angers.fr Service de Dermatologie Vénéréologie Pr. L. Martin 2011-2012 CHU Angers UE Revêtement cutané Dermoscopie ou Dermatoscopie Examen de
Moyens d étude de la peau Dr. Yannick Le Corre yalecorre@chu-angers.fr Service de Dermatologie Vénéréologie Pr. L. Martin 2011-2012 CHU Angers UE Revêtement cutané Dermoscopie ou Dermatoscopie Examen de
A B C Eau Eau savonneuse Eau + détergent
 1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
Sein inflammatoire. Isabelle Leconte Cliniques universitaires St Luc
 Sein inflammatoire Isabelle Leconte Cliniques universitaires St Luc Sein inflammatoire 3 types Mastites infectieuses Mastites non infectieuses Cancer inflammatoire 2 situations cliniques Allaitement Hors
Sein inflammatoire Isabelle Leconte Cliniques universitaires St Luc Sein inflammatoire 3 types Mastites infectieuses Mastites non infectieuses Cancer inflammatoire 2 situations cliniques Allaitement Hors
De la chirurgie du nodule aux ganglions
 De la chirurgie du nodule aux ganglions Docteur Xavier CARRAT Institut Bergonié Clinique Saint Augustin Chirurgie des lésions bénignes de la thyroïde problématique opératoire «simple» avec indication portée
De la chirurgie du nodule aux ganglions Docteur Xavier CARRAT Institut Bergonié Clinique Saint Augustin Chirurgie des lésions bénignes de la thyroïde problématique opératoire «simple» avec indication portée
Quel apport de l imagerie dans les traitements anti-angiogéniques?
 Quel apport de l imagerie dans les traitements anti-angiogéniques? L Fournier, D Balvay, CA Cuénod Service de radiologie, Hôpital Européen Georges Pompidou Laboratoire de Recherche en Imagerie, Equipe
Quel apport de l imagerie dans les traitements anti-angiogéniques? L Fournier, D Balvay, CA Cuénod Service de radiologie, Hôpital Européen Georges Pompidou Laboratoire de Recherche en Imagerie, Equipe
Les tests de génétique moléculaire pour l accès aux thérapies ciblées en France en 2011
 Mesure 21 SOINS ET VIE DES MALADES Les tests de génétique moléculaire pour l accès aux thérapies ciblées en France en 2011 COLLECTION Rapports & synthèses POUR UN ACCÈS AUX THÉRAPIES CIBLÉES : - LES PLATEFORMES
Mesure 21 SOINS ET VIE DES MALADES Les tests de génétique moléculaire pour l accès aux thérapies ciblées en France en 2011 COLLECTION Rapports & synthèses POUR UN ACCÈS AUX THÉRAPIES CIBLÉES : - LES PLATEFORMES
Tumeurs cutanées épithéliales et mélaniques
 Examen National Classant Module transdisciplinaire 10 : Cancérologie, onco-hématologie Tumeurs cutanées épithéliales et mélaniques Mélanomes NOUVEAU P. SAIAG (Ambroise Paré, Boulogne Billancourt), J.-J.
Examen National Classant Module transdisciplinaire 10 : Cancérologie, onco-hématologie Tumeurs cutanées épithéliales et mélaniques Mélanomes NOUVEAU P. SAIAG (Ambroise Paré, Boulogne Billancourt), J.-J.
EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points)
 Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
ACIDES BASES. Chap.5 SPIESS
 ACIDES BASES «Je ne crois pas que l on me conteste que l acide n ait des pointes Il ne faut que le goûter pour tomber dans ce sentiment car il fait des picotements sur la langue.» Notion d activité et
ACIDES BASES «Je ne crois pas que l on me conteste que l acide n ait des pointes Il ne faut que le goûter pour tomber dans ce sentiment car il fait des picotements sur la langue.» Notion d activité et
KIT ELISA dosage immunologique anti-bsa REF : ELISA A RECEPTION DU COLIS : Vérifier la composition du colis indiquée ci-dessous en pages 1 et 2
 KIT ELISA dosage immunologique anti-bsa REF : ELISA : 0033 (0)169922672 : 0033 (0)169922674 : www.sordalab.com @ : sordalab@wanadoo.fr A RECEPTION DU COLIS : Vérifier la composition du colis indiquée ci-dessous
KIT ELISA dosage immunologique anti-bsa REF : ELISA : 0033 (0)169922672 : 0033 (0)169922674 : www.sordalab.com @ : sordalab@wanadoo.fr A RECEPTION DU COLIS : Vérifier la composition du colis indiquée ci-dessous
TECHNIQUES: Principes de la chromatographie
 TECHNIQUES: Principes de la chromatographie 1 Définition La chromatographie est une méthode physique de séparation basée sur les différentes affinités d un ou plusieurs composés à l égard de deux phases
TECHNIQUES: Principes de la chromatographie 1 Définition La chromatographie est une méthode physique de séparation basée sur les différentes affinités d un ou plusieurs composés à l égard de deux phases
EXERCICES : MECANISMES DE L IMMUNITE : pages 406 407 408 409 410
 EXERCICES : MECANISMES DE L IMMUNITE : pages 406 407 408 409 410 EXERCICE 1 PAGE 406 : EXPERIENCES A INTERPRETER Question : rôles respectifs du thymus et de la moelle osseuse dans la production des lymphocytes.
EXERCICES : MECANISMES DE L IMMUNITE : pages 406 407 408 409 410 EXERCICE 1 PAGE 406 : EXPERIENCES A INTERPRETER Question : rôles respectifs du thymus et de la moelle osseuse dans la production des lymphocytes.
L axe 5 du Cancéropole Nord Ouest
 L axe 5 du Cancéropole Nord Ouest Cancers, Individu id & Société L état des lieux d un pari Le Rapport Cordier 1 Biomarqueurs prédictifs 2 L axe 5 du Cancéropole Nord Ouest Cancers, Individu & Société
L axe 5 du Cancéropole Nord Ouest Cancers, Individu id & Société L état des lieux d un pari Le Rapport Cordier 1 Biomarqueurs prédictifs 2 L axe 5 du Cancéropole Nord Ouest Cancers, Individu & Société
A l Assistance Publique - Hôpitaux de Marseille, Octobre Rose est l occasion de mettre en valeur la filière de soins dédiée au cancer du sein.
 OCTOBRE ROSE 2013 La campagne Octobre Rose a pour but d inciter les femmes de 50 à 74 ans à participer au dépistage organisé du cancer du sein. Une femme sur trois ne se fait pas dépister ou pas de manière
OCTOBRE ROSE 2013 La campagne Octobre Rose a pour but d inciter les femmes de 50 à 74 ans à participer au dépistage organisé du cancer du sein. Une femme sur trois ne se fait pas dépister ou pas de manière
Lymphome non hodgkinien
 Lymphome non hodgkinien Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca LYMPHOME NON HODGKINIEN Ce que vous devez savoir Même si vous entendez parler du cancer presque
Lymphome non hodgkinien Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca LYMPHOME NON HODGKINIEN Ce que vous devez savoir Même si vous entendez parler du cancer presque
Pemetrexed, pionnier de la chimiothérapie histoguidée. Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var
 Pemetrexed, pionnier de la chimiothérapie histoguidée Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var SFPO Octobre 2009 EPIDEMIOLOGIE Incidence : 1.35 M par an dans le monde (12,4%) 28 000
Pemetrexed, pionnier de la chimiothérapie histoguidée Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var SFPO Octobre 2009 EPIDEMIOLOGIE Incidence : 1.35 M par an dans le monde (12,4%) 28 000
Cancer du sein. Du CA15-3 à la tomographie à émission de positons.
 Cancer du sein. Du CA15-3 à la tomographie à émission de positons. Un taux de récidive de 30% dans les dix premières années chez des patientes en rémission complète après un traitement curatif, requiert
Cancer du sein. Du CA15-3 à la tomographie à émission de positons. Un taux de récidive de 30% dans les dix premières années chez des patientes en rémission complète après un traitement curatif, requiert
UE2 CANCEROLOGIE Place de la Médecine Nucléaire
 UE2 CANCEROLOGIE Place de la Médecine Nucléaire Imagerie Imagerie de Gamma Caméra Tomographie d émission monophotoniqueou TEMP: radiopharmaceutiqueémetteurs de rayonnement Gamma Imagerie de Caméra TEP
UE2 CANCEROLOGIE Place de la Médecine Nucléaire Imagerie Imagerie de Gamma Caméra Tomographie d émission monophotoniqueou TEMP: radiopharmaceutiqueémetteurs de rayonnement Gamma Imagerie de Caméra TEP
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
Compte-rendu d examen anatomo-pathologique - hépatite chronique
 Compte-rendu d examen anatomo-pathologique - hépatite chronique À partir de la Vème année Médecine Générale et notamment pour les médecins anatomopathologues ANATOMIE PATHOLOGIQUE Hôpital du Bon Secours
Compte-rendu d examen anatomo-pathologique - hépatite chronique À partir de la Vème année Médecine Générale et notamment pour les médecins anatomopathologues ANATOMIE PATHOLOGIQUE Hôpital du Bon Secours
F JABNOUN, H BERMENT, R KHAYAT, M MOHALLEM, Y BARUKH, P CHEREL Institut Curie Hôpital René Huguenin, Saint Cloud JFR 2010
 F JABNOUN, H BERMENT, R KHAYAT, M MOHALLEM, Y BARUKH, P CHEREL Institut Curie Hôpital René Huguenin, Saint Cloud JFR 2010 Une anomalie ACR5 n est pas synonyme de malignité (VPP>95%) Quelle CAT après un
F JABNOUN, H BERMENT, R KHAYAT, M MOHALLEM, Y BARUKH, P CHEREL Institut Curie Hôpital René Huguenin, Saint Cloud JFR 2010 Une anomalie ACR5 n est pas synonyme de malignité (VPP>95%) Quelle CAT après un
33-Dosage des composés phénoliques
 33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
Les traitements du cancer invasif du col de l utérus
 JUIN 2011 Les traitements du cancer invasif du col de l utérus Nom du chapitre COLLECTION GUIDES PATIENTS LE COL DE L UTÉRUS LE CHOIX DES TRAITEMENTS LA CHIRURGIE LA RADIOTHÉRAPIE LA CHIMIOTHÉRAPIE LES
JUIN 2011 Les traitements du cancer invasif du col de l utérus Nom du chapitre COLLECTION GUIDES PATIENTS LE COL DE L UTÉRUS LE CHOIX DES TRAITEMENTS LA CHIRURGIE LA RADIOTHÉRAPIE LA CHIMIOTHÉRAPIE LES
d anatomo-pathologiste
 Le métierm d anatomo-pathologiste Paul P. de SAINT-MAUR Université Paris 6 -Hôpital Saint-Antoine Le 19 Novembre 2002 Le métier m d anatomopathologisted Qu est est-ce qu un un anatomo-pathologiste? Comment
Le métierm d anatomo-pathologiste Paul P. de SAINT-MAUR Université Paris 6 -Hôpital Saint-Antoine Le 19 Novembre 2002 Le métier m d anatomopathologisted Qu est est-ce qu un un anatomo-pathologiste? Comment
La fonction respiratoire
 La fonction respiratoire Introduction Fonction vitale : Au-delà de 3 min = atteintes graves Après 5 min = très altérés On parle de 3 phénomènes : Ventilation : respiration visible, échanges aériens intérieur
La fonction respiratoire Introduction Fonction vitale : Au-delà de 3 min = atteintes graves Après 5 min = très altérés On parle de 3 phénomènes : Ventilation : respiration visible, échanges aériens intérieur
DERMATOSES ECZEMATIFORMES LICHENOIDES ET ERYTHEMATO-SQUAMEUSES
 DERMATOSES ECZEMATIFORMES LICHENOIDES ET ERYTHEMATO-SQUAMEUSES I ECZEMA ET LESIONS ECZEMATIFORMES II LICHEN PLAN III LICHEN SCLERO-ATROPHIQUE IV MALADIE LUPIQUE V PSORIASIS VI AUTRES Parapsoriasis Kératodermies
DERMATOSES ECZEMATIFORMES LICHENOIDES ET ERYTHEMATO-SQUAMEUSES I ECZEMA ET LESIONS ECZEMATIFORMES II LICHEN PLAN III LICHEN SCLERO-ATROPHIQUE IV MALADIE LUPIQUE V PSORIASIS VI AUTRES Parapsoriasis Kératodermies
Dégénérescence maculaire liée à l âge
 Dégénérescence maculaire liée à l âge LUC-09-02/10-6087 - 1 - Dégénérescence maculaire liée à l âge Sommaire 1. Introduction 2. Qu est-ce que la dégénérescence maculaire liée à l âge? 3. Forme sèche et
Dégénérescence maculaire liée à l âge LUC-09-02/10-6087 - 1 - Dégénérescence maculaire liée à l âge Sommaire 1. Introduction 2. Qu est-ce que la dégénérescence maculaire liée à l âge? 3. Forme sèche et
Cytokines & Chimiokines
 Cytokines & Chimiokines I. (D après Förster, R. et al. (1999) Cell 99:23) Dans le but d étudier la régulation de la circulation des leucocytes dans l organisme, des souris déficientes pour le récepteur
Cytokines & Chimiokines I. (D après Förster, R. et al. (1999) Cell 99:23) Dans le but d étudier la régulation de la circulation des leucocytes dans l organisme, des souris déficientes pour le récepteur
La Dysplasie Ventriculaire Droite Arythmogène
 1 La Dysplasie Ventriculaire Droite Arythmogène Document rédigé par l équipe pluridisciplinaire du centre de référence pour les maladies cardiaques héréditaires (Paris), en collaboration avec des patients
1 La Dysplasie Ventriculaire Droite Arythmogène Document rédigé par l équipe pluridisciplinaire du centre de référence pour les maladies cardiaques héréditaires (Paris), en collaboration avec des patients
Les plateformes de génétique
 Thérapies ciblées : de l anatomopathologie th l à la biothérapie i Les plateformes de génétique moléculaire PO Schischmanoff UF Génétique moléculaire et oncogénétique CHU Avicenne ACP FHF 29 mars 2012
Thérapies ciblées : de l anatomopathologie th l à la biothérapie i Les plateformes de génétique moléculaire PO Schischmanoff UF Génétique moléculaire et oncogénétique CHU Avicenne ACP FHF 29 mars 2012
Focus. Assurances et tumeurs génitales des hommes jeunes. Unité de Recherche et Développement pour les Risques Aggravés.
 Unité de Recherche et Développement pour les Risques Aggravés Focus Juillet 2007 Assurances et tumeurs génitales des hommes jeunes Assurances et tumeurs génitales des hommes jeunes Conception et réalisation
Unité de Recherche et Développement pour les Risques Aggravés Focus Juillet 2007 Assurances et tumeurs génitales des hommes jeunes Assurances et tumeurs génitales des hommes jeunes Conception et réalisation
M2.6. 2012 Cancer du colon et du rectum. Coordination : Pr Hahnloser
 M2.6. 2012 Cancer du colon et du rectum Coordination : Pr Hahnloser Pathologie Dr. Maryse Fiche Cancers colo-rectaux Précurseurs : Images et figures : Robbins 8è Edition Objectifs d apprentissage : SCLO
M2.6. 2012 Cancer du colon et du rectum Coordination : Pr Hahnloser Pathologie Dr. Maryse Fiche Cancers colo-rectaux Précurseurs : Images et figures : Robbins 8è Edition Objectifs d apprentissage : SCLO
LE GRAND LIVRE Du. Pr Jean-Jacques Altman Dr Roxane Ducloux Dr Laurence Lévy-Dutel. Prévenir les complications. et surveiller la maladie
 Pr Jean-Jacques Altman Dr Roxane Ducloux Dr Laurence Lévy-Dutel LE GRAND LIVRE Du diabète Vivre avec le diabète à tout âge Traiter et surveiller la maladie Prévenir les complications, 2012 ISBN : 978-2-212-55509-7
Pr Jean-Jacques Altman Dr Roxane Ducloux Dr Laurence Lévy-Dutel LE GRAND LIVRE Du diabète Vivre avec le diabète à tout âge Traiter et surveiller la maladie Prévenir les complications, 2012 ISBN : 978-2-212-55509-7
Les traitements du cancer du rein
 MARS 2013 Les traitements du cancer du rein COLLECTION GUIDES PATIENTS LES REINS LE CHOIX DES TRAITEMENTS LA CHIRURGIE LES MÉDICAMENTS ANTICANCÉREUX LES PROFESSIONNELS LA VIE QUOTIDIENNE www.e-cancer.fr
MARS 2013 Les traitements du cancer du rein COLLECTION GUIDES PATIENTS LES REINS LE CHOIX DES TRAITEMENTS LA CHIRURGIE LES MÉDICAMENTS ANTICANCÉREUX LES PROFESSIONNELS LA VIE QUOTIDIENNE www.e-cancer.fr
Cellules procaryotes Service histologie Pr.k.mebarek
 Cellules procaryotes Service histologie Pr.k.mebarek I) Les cellules procaryotes II) Les cellules eucaryotes o 1) Caractéristiques générales des cellules eucaryotes o 2) Organisation des cellules eucaryotes
Cellules procaryotes Service histologie Pr.k.mebarek I) Les cellules procaryotes II) Les cellules eucaryotes o 1) Caractéristiques générales des cellules eucaryotes o 2) Organisation des cellules eucaryotes
Acides et bases. Acides et bases Page 1 sur 6
 Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
L eau dans le corps. Fig. 6 L eau dans le corps. Cerveau 85 % Dents 10 % Cœur 77 % Poumons 80 % Foie 73 % Reins 80 % Peau 71 % Muscles 73 %
 24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
Transgene accorde une option de licence exclusive pour le développement et la commercialisation de son produit d immunothérapie TG4010
 Parc d Innovation d Illkirch, France, le 10 mars 2010 Transgene accorde une option de licence exclusive pour le développement et la commercialisation de son produit d immunothérapie TG4010 Transgene (Euronext
Parc d Innovation d Illkirch, France, le 10 mars 2010 Transgene accorde une option de licence exclusive pour le développement et la commercialisation de son produit d immunothérapie TG4010 Transgene (Euronext
Activité 38 : Découvrir comment certains déchets issus de fonctionnement des organes sont éliminés de l organisme
 Activité 38 : Découvrir comment certains déchets issus de fonctionnement des organes sont éliminés de l organisme 1. EXTRAITS REFERENTIELS DU BO Partie du programme : Fonctionnement de l organisme et besoin
Activité 38 : Découvrir comment certains déchets issus de fonctionnement des organes sont éliminés de l organisme 1. EXTRAITS REFERENTIELS DU BO Partie du programme : Fonctionnement de l organisme et besoin
La lutte contre la tuberculose est régie par l arrêté royal du 17 octobre 2002.
 Le diagnostic de la tuberculose bovine La lutte contre la tuberculose est régie par l arrêté royal du 17 octobre 2002. 1. Tuberculination Dans la première phase d une infection de tuberculose bovine (Mycobacterium
Le diagnostic de la tuberculose bovine La lutte contre la tuberculose est régie par l arrêté royal du 17 octobre 2002. 1. Tuberculination Dans la première phase d une infection de tuberculose bovine (Mycobacterium
Information génétique
 chapitre 3 Information génétique et division cellulaire L étude de la division cellulaire est abordée pour découvrir comment est transmise et conservée l information génétique portée par les chromosomes.
chapitre 3 Information génétique et division cellulaire L étude de la division cellulaire est abordée pour découvrir comment est transmise et conservée l information génétique portée par les chromosomes.
Toxicité à long-terme d un herbicide Roundup et d un maïs modifié génétiquement pour tolérer le Roundup
 A l attention de toutes les personnes qui se méfient des jugements de valeur fussent-ils émis par des scientifiques- et qui préfèrent capter les informations à leur source pour s en faire une opinion personnelle.
A l attention de toutes les personnes qui se méfient des jugements de valeur fussent-ils émis par des scientifiques- et qui préfèrent capter les informations à leur source pour s en faire une opinion personnelle.
Défauts dan les sachets souples état date stérilisables en autoclave nouveau 31/05/2002 Caractérisation et classification
 chapitre page 7 Index CHAPITRE 7 CATÉGORIES DES DÉFAUTS 7.1 Abrasion 7.2 Cloque 7.3 Canal de fuite 7.4 Joint comprimé (ou séparation des couches dans la zone de scellage) 7.5 Joint contaminé 7.6 Joint
chapitre page 7 Index CHAPITRE 7 CATÉGORIES DES DÉFAUTS 7.1 Abrasion 7.2 Cloque 7.3 Canal de fuite 7.4 Joint comprimé (ou séparation des couches dans la zone de scellage) 7.5 Joint contaminé 7.6 Joint
ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER
 ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER Dr Michael Hummelsberger, Pr Jean-Gabriel Fuzibet, Service de Médecine Interne, Hôpital l Archet, CHU Nice 1. ANEMIE L étiologie de l anémie
ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER Dr Michael Hummelsberger, Pr Jean-Gabriel Fuzibet, Service de Médecine Interne, Hôpital l Archet, CHU Nice 1. ANEMIE L étiologie de l anémie
Exemple de cahier de laboratoire : cas du sujet 2014
 Exemple de cahier de laboratoire : cas du sujet 2014 Commentaires pour l'évaluation Contenu du cahier de laboratoire Problématique : Le glucose est un nutriment particulièrement important pour le sportif.
Exemple de cahier de laboratoire : cas du sujet 2014 Commentaires pour l'évaluation Contenu du cahier de laboratoire Problématique : Le glucose est un nutriment particulièrement important pour le sportif.
DON DE SANG. Label Don de Soi
 DON DE SANG Label Don de Soi 2015 SOMMAIRE Les différents types de dons p.3 Le don de sang total Le don de plasma Le don de plaquettes Le don de moelle osseuse Que soigne-t-on avec un don de sang? p.7
DON DE SANG Label Don de Soi 2015 SOMMAIRE Les différents types de dons p.3 Le don de sang total Le don de plasma Le don de plaquettes Le don de moelle osseuse Que soigne-t-on avec un don de sang? p.7
TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY)
 TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY) Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste Direction de l innovation scientifique et technologique Au Laboratoire
TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY) Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste Direction de l innovation scientifique et technologique Au Laboratoire
BIOPSIE de MOELLE OSSEUSE
 BIOPSIE de MOELLE OSSEUSE Le prélèvement de moelle osseuse? La moelle osseuse, tissu hématopoïétique situé dans la cavité centrale des os, peut être prélevée de deux façons : -par ponction sternale -par
BIOPSIE de MOELLE OSSEUSE Le prélèvement de moelle osseuse? La moelle osseuse, tissu hématopoïétique situé dans la cavité centrale des os, peut être prélevée de deux façons : -par ponction sternale -par
chronique La maladie rénale Un risque pour bon nombre de vos patients Document destiné aux professionnels de santé
 Document destiné aux professionnels de santé Agence relevant du ministère de la santé La maladie rénale chronique Un risque pour bon nombre de vos patients Clés pour la dépister et ralentir sa progression
Document destiné aux professionnels de santé Agence relevant du ministère de la santé La maladie rénale chronique Un risque pour bon nombre de vos patients Clés pour la dépister et ralentir sa progression
PROFIL DE POSTE PRATICIEN ANATOMIE ET CYTOLOGIE PATHOLOGIQUES
 ETABLISSEMENT CENTRE HOSPITALIER PUBLIC DU COTENTIN (CHPC) CHERBOURG (50) Deuxième établissement hospitalier de Basse-Normandie. SPECIALITE RECHERCHEE Anatomie et cytologie pathologiques (ACP). COMPETENCES
ETABLISSEMENT CENTRE HOSPITALIER PUBLIC DU COTENTIN (CHPC) CHERBOURG (50) Deuxième établissement hospitalier de Basse-Normandie. SPECIALITE RECHERCHEE Anatomie et cytologie pathologiques (ACP). COMPETENCES
Programme «maladie» - Partie II «Objectifs / Résultats» Objectif n 2 : développer la prévention
 Programme «maladie» - Partie II «Objectifs / Résultats» Objectif n 2 : développer la prévention Indicateur n 2-3 : Indicateurs sur le dépistage du cancer 1 er sous-indicateur : taux de participation au
Programme «maladie» - Partie II «Objectifs / Résultats» Objectif n 2 : développer la prévention Indicateur n 2-3 : Indicateurs sur le dépistage du cancer 1 er sous-indicateur : taux de participation au
des banques pour la recherche
 ADN, cellules, tissus... des banques pour la recherche FÉVRIER 2009 Les banques d échantillons de matériel biologique (tissus, cellules, ADN ), appelées biobanques, mettent à disposition des chercheurs
ADN, cellules, tissus... des banques pour la recherche FÉVRIER 2009 Les banques d échantillons de matériel biologique (tissus, cellules, ADN ), appelées biobanques, mettent à disposition des chercheurs
Chirurgie du cancer du sein
 Chirurgie du cancer du sein Chez le même éditeur ÉCHOGRAPHIE ET IMAGERIE PELVIENNE EN PRATIQUE GYNÉCOLOGIQUE, par Y. Ardaens, B. Guérin du Masgenêt, Ph. Coquel. Collection Imagerie médicale Précis, 2011,
Chirurgie du cancer du sein Chez le même éditeur ÉCHOGRAPHIE ET IMAGERIE PELVIENNE EN PRATIQUE GYNÉCOLOGIQUE, par Y. Ardaens, B. Guérin du Masgenêt, Ph. Coquel. Collection Imagerie médicale Précis, 2011,
