D autres présentations que les ampoules doivent être considérées pour l auto-administration par les patientes.
|
|
|
- Odette Chaput
- il y a 6 ans
- Total affichages :
Transcription
1 1. DÉNOMINATION DU MÉDICAMENT Luveris 75 UI poudre et solvant pour solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Un flacon contient 75 UI de lutropine alfa (hormone lutéinisante humaine recombinante, r-hlh). La lutropine alfa est produite dans des cellules ovariennes de hamster chinois (cellules CHO) génétiquement modifiées. Pour la liste complète des excipients, voir rubrique FORME PHARMACEUTIQUE Poudre et solvant pour solution injectable. Aspect de la poudre : pastille lyophilisée blanche Aspect du solvant : solution limpide incolore Le ph de la solution reconstituée est de 7,5 à 8,5. D autres présentations que les ampoules doivent être considérées pour l auto-administration par les patientes. 4. DONNÉES CLINIQUES 4.1 Indications thérapeutiques Luveris, en association avec une préparation à base d hormone folliculo-stimulante (FSH), est recommandé pour stimuler le développement folliculaire chez les femmes adultes qui présentent un déficit sévère en hormone lutéinisante (LH) et en FSH. Au cours des essais cliniques, ces patientes étaient définies par un taux plasmatique de LH endogène < 1,2 UI/l. 4.2 Posologie et mode d administration Tout traitement par Luveris doit être initié sous la surveillance d un médecin ayant l expérience du traitement des problèmes de fertilité. Posologie Chez les femmes présentant un déficit en LH et en FSH, l objectif du traitement par Luveris en association avec la FSH est de développer un seul follicule de Graaf mature, à partir duquel l ovule sera libéré après administration de choriogonadotropine humaine (hcg). Luveris devra être administré en injections quotidiennes, en même temps que la FSH. Ces patientes étant aménorrhéiques et présentant une faible sécrétion endogène d estrogènes, le traitement peut être débuté à tout moment du cycle. Luveris devra être administré en même temps que la follitropine alfa. Le traitement devra être adapté à la réponse individuelle de chaque patiente, celle-ci étant déterminée en mesurant la taille du follicule par échographie et la sécrétion estrogénique. Le traitement recommandé commence par 75 UI de lutropine alfa (soit un flacon de Luveris) par jour, avec 75 à 150 UI de FSH. 2
2 Des essais cliniques ont montré que Luveris augmentait la sensibilité ovarienne à la follitropine alfa. Si une augmentation de la dose de FSH est nécessaire, il est préférable d ajuster la dose à intervalles de 7 à 14 jours et par paliers de 37,5 UI à 75 UI. Il peut être justifié au cours d un cycle de prolonger la stimulation jusqu à 5 semaines. Quand une réponse optimale est obtenue, une injection unique de 250 microgrammes de r-hcg ou 5000 à UI d hcg devra être administrée 24 à 48 heures après les dernières injections de Luveris et de FSH. On recommandera alors à la patiente d avoir un rapport sexuel le jour même et le jour suivant l administration d hcg. Alternativement, une insémination intra-utérine (IIU) peut être pratiquée. Un soutien de phase lutéale peut être envisagé, étant donné que le manque de substances à activité lutéotrope (LH/hCG) après ovulation peut entraîner une insuffisance qualitative du corps jaune. Si une réponse excessive est obtenue, le traitement devra être arrêté et l hcg ne devra pas être administrée. Le traitement devra reprendre lors du cycle suivant, à une dose de FSH inférieure à celle du cycle abandonné. Populations particulières Population âgée Il n y a pas d indication justifiée pour l utilisation de Luveris dans la population âgée. La sécurité et l efficacité de Luveris chez les patientes âgées n ont pas été établies. Insuffisances rénale et hépatique La sécurité, l efficacité et la pharmacocinétique de Luveris chez les patientes atteintes d une insuffisance rénale ou hépatique n ont pas été établies. Population pédiatrique Il n y a pas d utilisation justifiée de Luveris dans la population pédiatrique. Mode d administration Luveris s administre par voie sous-cutanée. La première injection de Luveris doit être effectuée sous surveillance médicale directe. La poudre doit être reconstituée immédiatement avant l emploi avec le solvant fourni. L auto-administration de ce médicament ne doit être réalisée que par des patientes motivées, formées et pouvant disposer de conseils avisés. Pour les instructions concernant la reconstitution du médicament avant administration, voir la rubrique Contre-indications Luveris est contre-indiqué chez les patientes présentant : une hypersensibilité au principe actif ou à l un des excipients mentionnés à la rubrique 6.1 une tumeur hypothalamique ou hypophysaire une hypertrophie ou des kystes de l ovaire, non imputables à un syndrome des ovaires polykystiques et d étiologie inconnue des saignements gynécologiques d étiologie inconnue un carcinome ovarien, utérin ou mammaire Luveris ne doit pas être utilisé quand il existe des circonstances rendant une grossesse normale impossible, par exemple : insuffisance ovarienne primitive malformations des organes génitaux incompatibles avec une grossesse fibromes utérins incompatibles avec une grossesse 3
3 4.4 Mises en garde spéciales et précautions d emploi Avant d entreprendre le traitement, un bilan de la stérilité du couple est nécessaire ainsi que la recherche d éventuelles contre-indications à une grossesse. De plus, les patientes devront subir des examens portant sur l hypothyroïdie, l insuffisance corticosurrénalienne et l hyperprolactinémie pour lesquelles des traitements spécifiques seront prescrits. Porphyrie Chez les patientes atteintes de porphyrie ou ayant des antécédents familiaux de porphyrie, l utilisation de Luveris peut augmenter le risque d une crise aiguë. Une aggravation ou une première apparition de la maladie peut nécessiter l arrêt du traitement. Syndrome d hyperstimulation ovarienne (SHO) L hypertrophie des ovaires à un certain degré est un effet attendu suite à une stimulation ovarienne contrôlée. Celle-ci s observe plus fréquemment chez les femmes atteintes d un syndrome des ovaires polykystiques et régresse généralement sans aucun traitement. Par rapport à une hypertrophie des ovaires non compliquée, le SHO est une complication qui peut se manifester avec des degrés de sévérité croissants. Il comprend une hypertrophie marquée des ovaires, une concentration sérique élevée de stéroïdes sexuels, ainsi qu une augmentation de la perméabilité vasculaire pouvant entraîner une accumulation de liquide dans les cavités péritonéale, pleurale, et plus rarement péricardique. Un SHO d intensité légère peut inclure des douleurs abdominales, une gêne abdominale ainsi qu un ballonnement ou une hypertrophie des ovaires. Un SHO d intensité modérée peut en outre s accompagner de nausées, de vomissements, de la présence à l échographie d une ascite ou d une hypertrophie marquée des ovaires. Un SHO sévère inclut de plus des symptômes tels que : une hypertrophie sévère des ovaires, une prise de poids, une dyspnée ou une oligurie. Le bilan clinique peut mettre en évidence des signes cliniques tels qu une hypovolémie, une hémoconcentration, des déséquilibres électrolytiques, une ascite, un épanchement pleural ou un syndrome de détresse respiratoire aiguë. Très rarement, un SHO sévère peut s accompagner de complications comme une torsion des ovaires ou des accidents thromboemboliques, telles qu une embolie pulmonaire, un accident vasculaire cérébral ischémique ou un infarctus du myocarde. Les facteurs de risque de développement du SHO sont indépendamment le jeune âge, la maigreur, le syndrome des ovaires polykystiques, des doses plus élevées de gonadotrophines exogènes, des taux sériques d estradiol absolus élevés ou en augmentation rapide, ainsi que des antécédents de SHO, un grand nombre de follicules ovariens en développement et un grand nombre d ovocytes récupérés lors de cycles d assistance médicale à la procréation (AMP). Le respect des doses et des schémas d administration recommandés pour Luveris et pour la FSH peuvent permettre de réduire le risque d hyperstimulation ovarienne. Il est recommandé de surveiller les cycles de stimulation par examen échographique ainsi que par le dosage de l estradiol afin d identifier précocement les facteurs de risque. Certains résultats laissent supposer que l hcg joue un rôle clé dans le déclenchement d un SHO et que sa sévérité pourrait être plus élevée et sa durée plus longue en cas de grossesse. Par conséquent, en cas d hyperstimulation ovarienne, il est recommandé de ne pas administrer l hcg et de conseiller à la patiente de ne pas avoir de rapports sexuels ou d utiliser une contraception de type barrière pendant au moins 4 jours. Un SHO peut évoluer rapidement (en 24 heures) ou sur une période de plusieurs jours et devenir médicalement grave ; aussi les patientes devront être suivies pendant au moins 2 semaines après l administration d hcg. 4
4 En général, un SHO d intensité légère ou modérée disparaît spontanément. En cas de SHO sévère, il est recommandé d arrêter le traitement par gonadotrophines en cours, d hospitaliser la patiente et de débuter un traitement approprié. Torsion de l ovaire Une torsion de l ovaire a été rapportée après traitement par d autres gonadotrophines. Ceci peut être associé à d autres facteurs de risque comme un SHO, une grossesse, une chirurgie abdominale antérieure, des antécédents de torsion de l ovaire, un kyste ovarien antérieur ou actuel et un syndrome des ovaires polykystiques. Il est possible de limiter les dommages à l ovaire, causés par une réduction de l apport sanguin, par un diagnostic précoce et par une détorsion immédiate de l ovaire. Grossesse multiple Comparée à une conception naturelle, l incidence de grossesses et de naissances multiples est augmentée chez les patientes recevant un traitement inducteur de l ovulation. La majorité des grossesses multiples sont gémellaires. Une grossesse multiple, spécialement celle de haut rang, entraîne un risque élevé de complications pour la mère et les nouveau-nés. Afin de réduire le risque de grossesse multiple de haut rang, il est recommandé de surveiller attentivement la réponse ovarienne. Chez les patientes ayant recours à une assistance médicale à la procréation (AMP), le risque de grossesse multiple est principalement lié au nombre d embryons implantés dans l utérus, à leur qualité ainsi qu à l âge de la patiente. Fausse couche Le risque de fausse couche spontanée ou d avortement est plus élevé chez les patientes traitées dans le cadre d une stimulation de la croissance folliculaire par induction de l ovulation que dans le cas d une conception naturelle. Grossesse ectopique Les femmes ayant des antécédents de pathologie tubaire sont exposées à un risque de grossesse ectopique, que la grossesse ait été obtenue par conception spontanée ou au moyen d un traitement stimulant la fertilité. La prévalence des grossesses ectopiques après AMP est supérieure à celle de la population générale. Malformations congénitales La prévalence des malformations congénitales pourrait être légèrement plus élevée après AMP qu après conception spontanée. Ceci pourrait être dû à des facteurs parentaux (ex. âge de la mère, génétique), aux procédures d AMP et aux grossesses multiples. Accidents thromboemboliques Chez les femmes souffrant ou ayant récemment souffert d une maladie thromboembolique ou chez les femmes exposées aux facteurs de risque généralement reconnus d accidents thromboemboliques, tels que les antécédents personnels ou familiaux, une thrombophilie ou une obésité sévère (indice de masse corporelle > 30 kg/m 2 ), le traitement par gonadotrophines pourrait augmenter le risque d aggravation ou de survenue de tels accidents. Chez ces femmes, il est nécessaire de déterminer si les bénéfices de l administration de gonadotrophines sont supérieurs ou non aux risques éventuels. Il faut toutefois noter que la grossesse elle-même, ainsi que le SHO, sont également associés à un risque accru d accidents thromboemboliques. Tumeurs de l appareil génital Des tumeurs bénignes et malignes de l ovaire et d autres organes de la reproduction ont été rapportées chez des femmes ayant eu recours à plusieurs traitements contre l infertilité. Il n a pas encore été établi si le traitement par gonadotrophines augmente ou non le risque de ces tumeurs chez les femmes infertiles. 5
5 4.5 Interactions avec d autres médicaments et autres formes d interactions Aucune étude d interaction n a été réalisée. Luveris ne doit pas être mélangé dans une même seringue avec d autres médicaments, excepté avec la follitropine alfa. Des études ont montré que l administration simultanée de ces deux médicaments ne modifiait pas significativement l activité, la stabilité, les propriétés pharmacocinétiques ou pharmacodynamiques des substances actives. 4.6 Fertilité, grossesse et allaitement Grossesse Il n y a pas d indication pour l utilisation de Luveris pendant la grossesse. Les données disponibles sur un nombre limité de grossesses exposées n indiquent aucun effet indésirable des gonadotrophines sur la grossesse, le développement de l embryon ou du fœtus, l accouchement ou le développement postnatal après une stimulation ovarienne contrôlée. Aucun effet tératogène de Luveris n a été observé lors des études chez l animal. En cas d exposition pendant la grossesse, les données cliniques sont insuffisantes pour pouvoir exclure un effet tératogène de Luveris. Allaitement Luveris n est pas indiqué pendant l allaitement. Fertilité Luveris est indiqué pour la stimulation du développement folliculaire en association avec la FSH (voir rubrique 4.1). 4.7 Effets sur l aptitude à conduire des véhicules et à utiliser des machines Luveris n a aucun effet ou qu un effet négligeable sur l aptitude à conduire des véhicules et à utiliser des machines. 4.8 Effets indésirables Résumé du profil de sécurité Luveris est utilisé pour stimuler le développement folliculaire en association avec la follitropine alfa. Dans ce contexte, il est difficile d attribuer des effets indésirables à l une des substances en particulier. Lors d un essai clinique, des réactions au site d injection, d intensité légère et modérée (ecchymoses, douleur, rougeur, prurit ou tuméfaction) ont été rapportées respectivement dans 7,4 % et 0,9 % des injections. Aucune réaction d intensité sévère au site d injection n a été rapportée. Moins de 6 % des patientes traitées par Luveris ont présenté un syndrome d hyperstimulation ovarienne (SHO). Aucun SHO grave n a été rapporté (voir rubrique 4.4). Dans de rares cas, une torsion des annexes (complication de l hypertrophie des ovaires) et un hémopéritoine ont été associés au traitement par gonadotrophine ménopausique humaine. Bien que ces effets indésirables n aient pas été observés, il est possible qu ils puissent survenir également avec Luveris. Une grossesse ectopique peut également survenir, en particulier chez les femmes ayant des antécédents de pathologie tubaire. Liste des effets indésirables Les définitions suivantes s appliquent aux termes utilisés ci-après pour déterminer la fréquence des effets indésirables : très fréquent ( 1/10), fréquent ( 1/100, < 1/10), peu fréquent ( 1/1 000, < 1/100), rare ( 1/10 000, < 1/1 000), très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles). 6
6 Les effets indésirables suivants peuvent être observés après l administration de Luveris : Affections du système immunitaire Très rare : réactions d hypersensibilité légères à sévères y compris les réactions et chocs anaphylactiques. Affections du système nerveux Fréquent : maux de tête. Affections vasculaires Très rare : accident thromboembolique, généralement associé à un SHO sévère. Affections gastro-intestinales Fréquent : douleurs abdominales, gêne abdominale, nausées, vomissements, diarrhée. Affections des organes de reproduction et du sein Fréquent : SHO d intensité légère ou modérée (y compris la symptomatologie associée), kyste ovarien, douleurs mammaires, douleurs pelviennes. Troubles généraux et anomalies au site d administration Fréquent : réaction au site d injection (par ex. douleur, érythème, hématome, gonflement et/ou irritation au site d injection). Déclaration des effets indésirables suspectés La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration voir Annexe V. 4.9 Surdosage Les effets d un surdosage avec Luveris ne sont pas connus. Néanmoins, il existe un risque de survenue d un SHO, comme décrit à la rubrique 4.4. Des doses uniques allant jusqu à UI de lutropine alfa ont été administrées à des femmes volontaires saines sans effets indésirables graves et avec une bonne tolérance. Prise en charge Traitement symptomatique. 5. PROPRIÉTÉS PHARMACOLOGIQUES 5.1 Propriétés pharmacodynamiques Classe pharmacothérapeutique : hormones sexuelles et modulateurs de la fonction génitale, gonadotrophines, Code ATC : G03GA07 La lutropine alfa est une hormone lutéinisante humaine recombinante (r-hlh), une glycoprotéine composée de 2 sous-unités α et β liées de façon non covalente. L hormone lutéinisante (LH) se fixe aux cellules de la thèque (et de la granulosa) de l ovaire et aux cellules de Leydig du testicule, par l intermédiaire d un récepteur commun avec la choriogonadotropine humaine (hcg). Ce récepteur commun LH/CG appartient à la superfamille des récepteurs couplés aux protéines G ; en particulier, il comporte un large domaine extracellulaire. In vitro, l affinité de liaison de la hlh recombinante pour le récepteur LH/CG des cellules de Leydig tumorales (MA-10) est intermédiaire entre celle de l hcg et celle de la LH hypophysaire humaine, mais du même ordre de grandeur. 7
7 Au niveau ovarien, pendant la phase folliculaire, la LH stimule la sécrétion d androgènes par les cellules thécales ; ces androgènes servent de substrat à l aromatase, enzyme des cellules de la granulosa, pour la production d estradiol, nécessaire au développement folliculaire induit par la FSH. En milieu de cycle, le pic de LH déclenche la formation du corps jaune et l ovulation. Après l ovulation, la LH stimule la production de progestérone dans le corps jaune, en augmentant la transformation du cholestérol en prégnénolone. Dans le cadre de la stimulation du développement folliculaire chez les femmes anovulatoires présentant un déficit en LH et en FSH, l administration de lutropine alfa a essentiellement pour effet d augmenter la sécrétion d estradiol par les follicules, dont la croissance est stimulée par la FSH. Au cours des essais cliniques, les patientes étaient définies par un taux plasmatique de LH endogène < 1,2 UI/l (mesuré dans un seul laboratoire). Néanmoins, il faut tenir compte de l existence de variations inter-laboratoires pour le dosage de la LH. Dans ces essais, le taux d ovulation par cycle était de 70 à 75 %. 5.2 Propriétés pharmacocinétiques La pharmacocinétique de la lutropine alfa a été étudiée chez des femmes volontaires présentant une désensibilisation hypophysaire, à des doses allant de 75 UI à UI. Le profil pharmacocinétique de la lutropine alfa est analogue à celui de la LH extraite des urines humaines. Absorption Après administration sous-cutanée, la biodisponibilité absolue est d environ 60 %. Distribution Après administration intraveineuse, la lutropine alfa est distribuée rapidement avec une demi-vie initiale d environ 1 heure. Le volume de distribution à l état d équilibre est d environ 10 à 14 litres. Le temps de résidence moyen est d environ 5 heures. La pharmacocinétique de la lutropine alfa est linéaire, comme le montre l aire sous la courbe (ASC) qui reste directement proportionnelle à la dose administrée. La pharmacocinétique de la lutropine alfa est comparable après administration unique et répétée de Luveris et l accumulation de la lutropine alfa est minime. Il n y a pas d interaction pharmacocinétique avec la follitropine alfa en cas d administration simultanée des deux produits. Élimination Après administration sous-cutanée de Luveris, la lutropine alfa s élimine avec une demi-vie terminale d environ 10 à 12 heures. Après administration sous-cutanée, la demi-vie terminale est légèrement allongée. La clairance totale est d environ 2 litres par heure et moins de 5 % de la dose sont excrétés dans les urines. 5.3 Données de sécurité préclinique Les données non cliniques issues des études conventionnelles de pharmacologie de sécurité, toxicologie en administration répétée, génotoxicité et cancérogénèse n ont pas révélé de risque particulier pour l homme. La lutropine alfa a déclenché (ceci était prévisible de par la nature protéique hétérologue de cette hormone) une réponse immunitaire chez les animaux de laboratoire, après une période qui a réduit les taux plasmatiques mesurables de LH mais n a pas empêché totalement son action biologique. Aucun signe de toxicité liée au développement des anticorps anti-lutropine alfa n a été observé. L administration répétée de lutropine alfa à des rates et lapines gravides, à des doses égales et supérieures à 10 UI/kg/jour, a induit des perturbations de la reproduction, notamment une résorption des fœtus et une diminution de la prise de poids des mères. Toutefois, aucun effet tératogène imputable au médicament n a été observé chez ces deux modèles animaux. 8
8 D autres études ont démontré l absence de mutagénicité de la lutropine alfa. 6. DONNÉES PHARMACEUTIQUES 6.1 Liste des excipients Poudre : Saccharose Phosphate disodique dihydraté Phosphate monosodique monohydraté Polysorbate 20 Acide phosphorique concentré (pour ajustement du ph) Hydroxyde de sodium (pour ajustement du ph) L-méthionine Azote Solvant : Eau pour préparation injectable 6.2 Incompatibilités Ce médicament ne doit pas être administré mélangé dans une même injection avec d autres médicaments, à l exception de la follitropine alfa. 6.3 Durée de conservation 3 ans. 6.4 Précautions particulières de conservation À conserver à une température ne dépassant pas 25 C. À conserver dans l emballage extérieur d origine, à l abri de la lumière. 6.5 Nature et contenu de l emballage extérieur La poudre est conditionnée en flacons de 3 ml, en verre neutre incolore (type I). Les flacons sont fermés par un bouchon en bromobutyle, protégé par une bague d étanchéité en aluminium et un opercule amovible. Le solvant est conditionné en flacons de 2 ou 3 ml, en verre neutre incolore (type I), munis d un bouchon en caoutchouc téfloné, ou en ampoules de 2 ml, en verre neutre incolore (type I). Boîtes de 1, 3 ou 10 flacons, accompagnés du nombre correspondant de flacons ou d ampoules de solvant. Toutes les présentations peuvent ne pas être commercialisées. 6.6 Précautions particulières d élimination et manipulation Pour une utilisation immédiate et à usage unique après ouverture et reconstitution. La poudre doit être reconstituée avec le solvant, avant utilisation, en remuant doucement. La solution reconstituée ne doit pas être administrée si elle contient des particules ou si elle n est pas limpide. Luveris peut être mélangé avec la follitropine alfa et co-administré en une seule injection. Dans ce cas, Luveris doit d abord être reconstitué, puis utilisé pour reconstituer la poudre de follitropine alfa. 9
9 Afin d éviter l injection de volumes trop importants, 1 flacon de Luveris peut être reconstitué avec 1 ou 2 ampoule(s)/flacon(s) de follitropine alfa (37,5 UI, 75 UI ou 150 UI) dans 1 ml de solvant. Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur. 7. TITULAIRE DE L AUTORISATION DE MISE SUR LE MARCHÉ Merck Serono Europe Limited 56 Marsh Wall London E14 9TP Royaume-Uni 8. NUMÉRO(S) D AUTORISATION DE MISE SUR LE MARCHÉ EU/1/00/155/001 (1 flacon / 1 ampoule) EU/1/00/155/002 (3 flacons / 3 ampoules) EU/1/00/155/003 (10 flacons / 10 ampoules) EU/1/00/155/004 (1 flacon / 1 flacon) EU/1/00/155/005 (3 flacons / 3 flacons) EU/1/00/155/006 (10 flacons / 10 flacons) 9. DATE DE PREMIÈRE AUTORISATION/DE RENOUVELLEMENT DE L AUTORISATION Date de première autorisation : 29 novembre Date de dernier renouvellement : 30 novembre DATE DE MISE À JOUR DU TEXTE {MM/AAAA} Des informations détaillées sur ce médicament sont disponibles sur le site internet de l Agence européenne des médicaments 10
GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral intramusculaire
 ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
Exploration et Prise en charge d un couple infertile
 Exploration et Prise en charge d un couple infertile Florence LESOURD Pôle d Obstétrique, Gynécologie et Médecine de la Reproduction CHU Paule de Viguier - Toulouse DIU de Médecine de la Reproduction-Gynécologie
Exploration et Prise en charge d un couple infertile Florence LESOURD Pôle d Obstétrique, Gynécologie et Médecine de la Reproduction CHU Paule de Viguier - Toulouse DIU de Médecine de la Reproduction-Gynécologie
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION. 10 octobre 2001
 COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
NOTICE: INFORMATION DE L UTILISATEUR. Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain)
 NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
E04a - Héparines de bas poids moléculaire
 E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
PRISE EN CHARGE DES PRE ECLAMPSIES. Jérôme KOUTSOULIS. IADE DAR CHU Kremlin-Bicêtre. 94 Gérard CORSIA. PH DAR CHU Pitié-Salpétrière.
 PRISE EN CHARGE DES PRE ECLAMPSIES Jérôme KOUTSOULIS. IADE DAR CHU Kremlin-Bicêtre. 94 Gérard CORSIA. PH DAR CHU Pitié-Salpétrière. 75 Pas de conflits d intérêts. Définitions Pré éclampsie Définitions
PRISE EN CHARGE DES PRE ECLAMPSIES Jérôme KOUTSOULIS. IADE DAR CHU Kremlin-Bicêtre. 94 Gérard CORSIA. PH DAR CHU Pitié-Salpétrière. 75 Pas de conflits d intérêts. Définitions Pré éclampsie Définitions
Carte de soins et d urgence
 Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
Observation. Merci à l équipe de pharmaciens FormUtip iatro pour ce cas
 Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
COMMISSION DE LA TRANSPARENCE AVIS. 18 janvier 2006
 COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
E03 - Héparines non fractionnées (HNF)
 E03-1 E03 - Héparines non fractionnées (HNF) Les héparines sont des anticoagulants agissant par voie parentérale. 1. Modalités d u tilisation Mode d action : l héparine est un cofacteur de l antithrombine
E03-1 E03 - Héparines non fractionnées (HNF) Les héparines sont des anticoagulants agissant par voie parentérale. 1. Modalités d u tilisation Mode d action : l héparine est un cofacteur de l antithrombine
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Assurance Maladie Obligatoire Commission de la Transparence des médicaments. Avis 2 23 Octobre 2012
 Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 2 23 Octobre 2012 Titre I : Nom du médicament, DCI, forme pharmaceutique, dosage, présentation HUMIRA (DCI : Adalimumab
Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 2 23 Octobre 2012 Titre I : Nom du médicament, DCI, forme pharmaceutique, dosage, présentation HUMIRA (DCI : Adalimumab
Contraception après 40 ans
 Contraception après 40 ans Stratégies de choix des méthodes contraceptives chez la femme. Recommandations pour la pratique clinique Décembre 2004. ANAES/AFSSAPS Un vaste choix contraceptif Contraception
Contraception après 40 ans Stratégies de choix des méthodes contraceptives chez la femme. Recommandations pour la pratique clinique Décembre 2004. ANAES/AFSSAPS Un vaste choix contraceptif Contraception
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
HTA et grossesse. Dr M. Saidi-Oliver chef de clinique-assistant CHU de Nice
 HTA et grossesse Dr M. Saidi-Oliver chef de clinique-assistant CHU de Nice Définition HTA gravidique: Après 20 SA Systole> 140mmHg et/ou Diastole>90mmHg A 2 reprises séparées de plus de 6 heures Résolutive
HTA et grossesse Dr M. Saidi-Oliver chef de clinique-assistant CHU de Nice Définition HTA gravidique: Après 20 SA Systole> 140mmHg et/ou Diastole>90mmHg A 2 reprises séparées de plus de 6 heures Résolutive
e-santé du transplanté rénal : la télémédecine au service du greffé
 e-santé du transplanté rénal : la télémédecine au service du greffé Professeur Michèle Kessler CHU de Nancy et réseau Néphrolor L une des applications de la télémédecine est la télésurveillance à domicile,
e-santé du transplanté rénal : la télémédecine au service du greffé Professeur Michèle Kessler CHU de Nancy et réseau Néphrolor L une des applications de la télémédecine est la télésurveillance à domicile,
Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
 Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Par fiole: L - asparaginase 10.000 U.I. Pour les excipients, cfr section 6.1. 3.
Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Par fiole: L - asparaginase 10.000 U.I. Pour les excipients, cfr section 6.1. 3.
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE
 GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
Livret des nouveaux anticoagulants oraux. Ce qu il faut savoir pour bien gérer leur utilisation
 Livret des nouveaux anticoagulants oraux Ce qu il faut savoir pour bien gérer leur utilisation DONNÉES DU PATIENT Nom Adresse Tél MÉDECIN TRAITANT Nom Adresse Tél SPÉCIALISTE Nom Hôpital Tél MÉDICAMENT
Livret des nouveaux anticoagulants oraux Ce qu il faut savoir pour bien gérer leur utilisation DONNÉES DU PATIENT Nom Adresse Tél MÉDECIN TRAITANT Nom Adresse Tél SPÉCIALISTE Nom Hôpital Tél MÉDICAMENT
chronique La maladie rénale Un risque pour bon nombre de vos patients Document destiné aux professionnels de santé
 Document destiné aux professionnels de santé Agence relevant du ministère de la santé La maladie rénale chronique Un risque pour bon nombre de vos patients Clés pour la dépister et ralentir sa progression
Document destiné aux professionnels de santé Agence relevant du ministère de la santé La maladie rénale chronique Un risque pour bon nombre de vos patients Clés pour la dépister et ralentir sa progression
Les anticoagulants. PM Garcia Sam Hamati. sofomec 2008
 Les anticoagulants PM Garcia Sam Hamati sofomec 2008 1 Les anticoagulants sofomec 2008 point de vue HAS AVK = 13% des hospitalisations pour accidents iatrogènes 17 000 hospitalisations / an /France pas
Les anticoagulants PM Garcia Sam Hamati sofomec 2008 1 Les anticoagulants sofomec 2008 point de vue HAS AVK = 13% des hospitalisations pour accidents iatrogènes 17 000 hospitalisations / an /France pas
Maternité et activités sportives
 Maternité et activités sportives L obstétricien est de plus en plus souvent interrogé sur les avantages et les risques de maintenir ou de débuter une APS ou de loisir pendant la grossesse. Transformations
Maternité et activités sportives L obstétricien est de plus en plus souvent interrogé sur les avantages et les risques de maintenir ou de débuter une APS ou de loisir pendant la grossesse. Transformations
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
 ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 Ce médicament fait l objet d une surveillance supplémentaire qui permettra l identification rapide de nouvelles informations relatives à la sécurité. Les
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 Ce médicament fait l objet d une surveillance supplémentaire qui permettra l identification rapide de nouvelles informations relatives à la sécurité. Les
Plan. Introduction. Les Nouveaux Anticoagulants Oraux et le sujet âgé. Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or
 Plan Introduction Les Nouveaux Anticoagulants Oraux et le sujet âgé Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or Introduction NACO: une actualité brûlante! AVK: Plus forte incidence
Plan Introduction Les Nouveaux Anticoagulants Oraux et le sujet âgé Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or Introduction NACO: une actualité brûlante! AVK: Plus forte incidence
27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013
 27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013 Les Nouveaux Anticoagulants Oraux (NACO) dans la maladie thrombo embolique veineuse INTRODUCTION Thrombose veineuse
27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013 Les Nouveaux Anticoagulants Oraux (NACO) dans la maladie thrombo embolique veineuse INTRODUCTION Thrombose veineuse
Item 169 : Évaluation thérapeutique et niveau de preuve
 Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
Projet de grossesse : informations, messages de prévention, examens à proposer
 DOCUMENT D INFORMATION POUR LES PROFESSIONNELS Projet de grossesse : informations, messages de prévention, examens à proposer Septembre 2009 DÉFINITION ET OBJECTIF Dès lors qu ils expriment un projet de
DOCUMENT D INFORMATION POUR LES PROFESSIONNELS Projet de grossesse : informations, messages de prévention, examens à proposer Septembre 2009 DÉFINITION ET OBJECTIF Dès lors qu ils expriment un projet de
Traitement des calculs urinaires par fragmentation (Lithotripsie par ondes de choc extracorporelle)
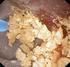 Traitement des calculs urinaires par fragmentation (Lithotripsie par ondes de choc extracorporelle) Le traitement des calculs urétéraux et rénaux a beaucoup changé depuis 1980 avec la venue d un appareil
Traitement des calculs urinaires par fragmentation (Lithotripsie par ondes de choc extracorporelle) Le traitement des calculs urétéraux et rénaux a beaucoup changé depuis 1980 avec la venue d un appareil
ASPECT ECHOGRAPHIQUE NORMAL DE LA CAVITE UTERINE APRES IVG. Dr D. Tasias Département de gynécologie, d'obstétrique et de stérilité
 Hôpitaux Universitaires de Genève ASPECT ECHOGRAPHIQUE NORMAL DE LA CAVITE UTERINE APRES IVG Dr D. Tasias Département de gynécologie, d'obstétrique et de stérilité Introduction (1) L IVG chirurgicale est
Hôpitaux Universitaires de Genève ASPECT ECHOGRAPHIQUE NORMAL DE LA CAVITE UTERINE APRES IVG Dr D. Tasias Département de gynécologie, d'obstétrique et de stérilité Introduction (1) L IVG chirurgicale est
Point d Information. Le PRAC a recommandé que le RCP soit modifié afin d inclure les informations suivantes:
 Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT. Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl par comprimé enrobé.
 RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1. Dé nomination du mé dicame nt Bisolax 5 mg comprimés enrobés. 2. Composition qualitative e t quantitative Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1. Dé nomination du mé dicame nt Bisolax 5 mg comprimés enrobés. 2. Composition qualitative e t quantitative Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl
LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B
 LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B Actualisation février 2009 Ce document est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service communication
LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B Actualisation février 2009 Ce document est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service communication
INTERET PRATIQUE DU MDRD AU CHU DE RENNES
 INTERET PRATIQUE DU MDRD AU CHU DE RENNES QU EST-CE QUE LE MDRD? Il s agit d une formule permettant d estimer le débit de filtration glomérulaire et donc la fonction rénale La formule est la suivante :
INTERET PRATIQUE DU MDRD AU CHU DE RENNES QU EST-CE QUE LE MDRD? Il s agit d une formule permettant d estimer le débit de filtration glomérulaire et donc la fonction rénale La formule est la suivante :
Fécondation in vitro avec don d ovocytes
 Fécondation in vitro avec don d ovocytes Ref. 155 / abril 2009 Service de Médecine de la Reproduction Gran Vía Carlos III 71-75 08028 Barcelona Tel. (+34) 93 227 47 00 Fax. (+34) 93 491 24 94 international@dexeus.com
Fécondation in vitro avec don d ovocytes Ref. 155 / abril 2009 Service de Médecine de la Reproduction Gran Vía Carlos III 71-75 08028 Barcelona Tel. (+34) 93 227 47 00 Fax. (+34) 93 491 24 94 international@dexeus.com
COMMISSION DE LA TRANSPARENCE AVIS. 10 mai 2006
 COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
COMMISSION DE LA TRANSPARENCE. Avis. 10 mars 2010
 COMMISSION DE LA TRANSPARENCE Avis 10 mars 2010 ARIXTRA 1,5 mg/0,3 ml, solution injectable en seringue pré-remplie - Boîte de 2 (CIP : 363 500-6) - Boîte de 7 (CIP : 363 501-2) - Boîte de 10 (CIP : 564
COMMISSION DE LA TRANSPARENCE Avis 10 mars 2010 ARIXTRA 1,5 mg/0,3 ml, solution injectable en seringue pré-remplie - Boîte de 2 (CIP : 363 500-6) - Boîte de 7 (CIP : 363 501-2) - Boîte de 10 (CIP : 564
Assurance Maladie Obligatoire Commission de la Transparence des médicaments. Avis 1 23 Octobre 2012
 Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 1 23 Octobre 2012 Titre I : Nom du médicament, DCI, Forme pharmaceutique, Dosage, Présentation - ARANESP 10 µg, Darbépoétine
Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 1 23 Octobre 2012 Titre I : Nom du médicament, DCI, Forme pharmaceutique, Dosage, Présentation - ARANESP 10 µg, Darbépoétine
QU EST-CE QUE LA PROPHYLAXIE?
 QU EST-CE QUE LA PROPHYLAXIE? TABLES DES MATIÈRES Publié par la Fédération mondiale de l hémophilie (FMH) Fédération mondiale de l hémophilie, 2014 La FMH encourage la traduction et la redistribution de
QU EST-CE QUE LA PROPHYLAXIE? TABLES DES MATIÈRES Publié par la Fédération mondiale de l hémophilie (FMH) Fédération mondiale de l hémophilie, 2014 La FMH encourage la traduction et la redistribution de
ÉVALUATION DE LA PERSONNE ATTEINTE D HYPERTENSION ARTÉRIELLE
 ÉVALUATION DE LA PERSONNE ATTEINTE D HYPERTENSION ARTÉRIELLE PRISE EN CHARGE SYSTÉMATISÉE DES PERSONNES ATTEINTES D HYPERTENSION ARTÉRIELLE SOCIÉTÉ QUÉBÉCOISE D HYPERTENSION ARTÉRIELLE 23 ÉVALUATION DE
ÉVALUATION DE LA PERSONNE ATTEINTE D HYPERTENSION ARTÉRIELLE PRISE EN CHARGE SYSTÉMATISÉE DES PERSONNES ATTEINTES D HYPERTENSION ARTÉRIELLE SOCIÉTÉ QUÉBÉCOISE D HYPERTENSION ARTÉRIELLE 23 ÉVALUATION DE
1 - Que faut-il retenir sur les anticoagulants oraux?
 La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
Point d information Avril 2012. Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir
 Point d information Avril 2012 Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir Le dabigatran (PRADAXA), inhibiteur direct de la thrombine,
Point d information Avril 2012 Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir Le dabigatran (PRADAXA), inhibiteur direct de la thrombine,
NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR. Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant
 B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
Les nouveaux anticoagulants oraux, FA et AVC. Docteur Thalie TRAISSAC Hôpital Saint André CAPCV 15 février 2014
 Les nouveaux anticoagulants oraux, FA et AVC Docteur Thalie TRAISSAC Hôpital Saint André CAPCV 15 février 2014 Un AVC toutes les 4 minutes 1 130 000 AVC par an en France 1 770 000 personnes ont été victimes
Les nouveaux anticoagulants oraux, FA et AVC Docteur Thalie TRAISSAC Hôpital Saint André CAPCV 15 février 2014 Un AVC toutes les 4 minutes 1 130 000 AVC par an en France 1 770 000 personnes ont été victimes
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
 ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 1. DÉNOMINATION DU MÉDICAMENT VÉTÉRINAIRE Equip WNV - émulsion injectable pour chevaux 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque dose de 1 ml contient:
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 1. DÉNOMINATION DU MÉDICAMENT VÉTÉRINAIRE Equip WNV - émulsion injectable pour chevaux 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque dose de 1 ml contient:
Fibrillation atriale chez le sujet âgé
 Dr Benoit Blanchard LE HAVRE Le 18 MARS 2014 Fibrillation atriale chez le sujet âgé Le plus fréquent des trouble du rythme cardiaque, 750,000 personnes atteintes de FA en France, 100,000 nouveaux cas chaque
Dr Benoit Blanchard LE HAVRE Le 18 MARS 2014 Fibrillation atriale chez le sujet âgé Le plus fréquent des trouble du rythme cardiaque, 750,000 personnes atteintes de FA en France, 100,000 nouveaux cas chaque
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT 2. COMPOSITION QUALITATIVE ET QUANTITATIVE 3. FORME PHARMACEUTIQUE 4. DONNEES CLINIQUES 4.1. Indications thérapeutiques 4.2.
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT 2. COMPOSITION QUALITATIVE ET QUANTITATIVE 3. FORME PHARMACEUTIQUE 4. DONNEES CLINIQUES 4.1. Indications thérapeutiques 4.2.
IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie
 1 sur 6 13/09/2010 16:58 Mis à jour : 23/02/2009 1. DENOMINATION DU MEDICAMENT IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
1 sur 6 13/09/2010 16:58 Mis à jour : 23/02/2009 1. DENOMINATION DU MEDICAMENT IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
ANNEXES AU REGLEMENT N 06/2010/CM/UEMOA
 UNION ECONOMIQUE ET MONETAIRE OUEST AFRICAINE ------------------------- La Commission ANNEXES AU REGLEMENT N 06/2010/CM/UEMOA LES ANNEXES AU REGLEMENT RELATIF AUX PROCEDURES D HOMOLOGATION DES PRODUITS
UNION ECONOMIQUE ET MONETAIRE OUEST AFRICAINE ------------------------- La Commission ANNEXES AU REGLEMENT N 06/2010/CM/UEMOA LES ANNEXES AU REGLEMENT RELATIF AUX PROCEDURES D HOMOLOGATION DES PRODUITS
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MEDICAMENT Osigraft 3,3 mg poudre pour suspension implantable 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque flacon contient 3,3
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MEDICAMENT Osigraft 3,3 mg poudre pour suspension implantable 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque flacon contient 3,3
La prise en charge de l AVC ischémique à l urgence
 La prise en charge de l AVC ischémique à l urgence Nathalie Bourdages, inf., B. Sc., conseillère en soins infirmiers, Direction des soins infirmiers et des regroupement clientèles, Centre hospitalier de
La prise en charge de l AVC ischémique à l urgence Nathalie Bourdages, inf., B. Sc., conseillère en soins infirmiers, Direction des soins infirmiers et des regroupement clientèles, Centre hospitalier de
RELPAX. hydrobromure d élétriptan
 RELPAX hydrobromure d élétriptan * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques * Conclusion * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques *
RELPAX hydrobromure d élétriptan * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques * Conclusion * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques *
B06 - CAT devant une ischémie aiguë des membres inférieurs
 B06-1 B06 - CAT devant une ischémie aiguë des membres inférieurs L ischémie aiguë est une interruption brutale du flux artériel au niveau d un membre entraînant une ischémie tissulaire. Elle constitue
B06-1 B06 - CAT devant une ischémie aiguë des membres inférieurs L ischémie aiguë est une interruption brutale du flux artériel au niveau d un membre entraînant une ischémie tissulaire. Elle constitue
COMMISSION DE LA TRANSPARENCE. Avis. 3 septembre 2008
 COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
Patient Diagnostics Tests Rapides Désir d Enfant
 Enceinte ou non? Patient Diagnostics Tests Rapides Désir d Enfant Les tests uniques en leur genre d aide à la planification familiale à utiliser chez soi Test d ovulation Test de grossesse précoce Test
Enceinte ou non? Patient Diagnostics Tests Rapides Désir d Enfant Les tests uniques en leur genre d aide à la planification familiale à utiliser chez soi Test d ovulation Test de grossesse précoce Test
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DÉNOMINATION DU MÉDICAMENT AVONEX 30 microgrammes poudre et solvant pour solution injectable 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque flacon
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DÉNOMINATION DU MÉDICAMENT AVONEX 30 microgrammes poudre et solvant pour solution injectable 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque flacon
Atelier N 2. Consultation de patientes porteuses d une maladie générale
 Atelier N 2 Consultation de patientes porteuses d une maladie générale Contre indica,ons à la grossesse Hypertension artérielle pulmonaire >30mmHg Maladie de Marfan (dilatation aortique>4 cm) Rétrécissement
Atelier N 2 Consultation de patientes porteuses d une maladie générale Contre indica,ons à la grossesse Hypertension artérielle pulmonaire >30mmHg Maladie de Marfan (dilatation aortique>4 cm) Rétrécissement
Nouveaux anticoagulants oraux : aspects pratiques
 Nouveaux anticoagulants oraux : aspects pratiques Christelle MARQUIE CHRU de Lille Clinique de Cardiologie L i l l e 2 Université du Droit et de la Santé Les NOAG: QCM 1. ont les mêmes indications que
Nouveaux anticoagulants oraux : aspects pratiques Christelle MARQUIE CHRU de Lille Clinique de Cardiologie L i l l e 2 Université du Droit et de la Santé Les NOAG: QCM 1. ont les mêmes indications que
Etablissement Français du Sang
 Etablissement Français du Sang LE LIEN ENTRE LA GÉNÉROSITÉ DES DONNEURS DE SANG ET LES BESOINS DES MALADES Document de préparation à l entretien médical préalable au don de sang Partie médicale La sécurité
Etablissement Français du Sang LE LIEN ENTRE LA GÉNÉROSITÉ DES DONNEURS DE SANG ET LES BESOINS DES MALADES Document de préparation à l entretien médical préalable au don de sang Partie médicale La sécurité
Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM)
 Hématologie biologique (Pr Marc Zandecki) Faculté de Médecine CHU 49000 Angers France Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM) 1. Structure et mode d'action
Hématologie biologique (Pr Marc Zandecki) Faculté de Médecine CHU 49000 Angers France Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM) 1. Structure et mode d'action
I - CLASSIFICATION DU DIABETE SUCRE
 I - CLASSIFICATION DU DIABETE SUCRE 1- Définition : Le diabète sucré se définit par une élévation anormale et chronique de la glycémie. Cette anomalie est commune à tous les types de diabète sucré, mais
I - CLASSIFICATION DU DIABETE SUCRE 1- Définition : Le diabète sucré se définit par une élévation anormale et chronique de la glycémie. Cette anomalie est commune à tous les types de diabète sucré, mais
19 thèmes dans 10 villes
 SATISFAIRE À VOS OBLIGATION DE DPC FACILEMENT GRÂCE AU CNGOF DPC réalisés par le CNGOF et financée par l Agrément CNGOF : 11 75 32 07 175 - FMC 100 098 Indemnité de 345 par jour et prise en charge hôtellerie
SATISFAIRE À VOS OBLIGATION DE DPC FACILEMENT GRÂCE AU CNGOF DPC réalisés par le CNGOF et financée par l Agrément CNGOF : 11 75 32 07 175 - FMC 100 098 Indemnité de 345 par jour et prise en charge hôtellerie
LASER DOPPLER. Cependant elle n est pas encore utilisée en routine mais reste du domaine de la recherche et de l évaluation.
 LASER DOPPLER INTRODUCTION La technique qui utilise l effet Doppler à partir d un faisceau laser est l une des seules qui permette d enregistrer en continu le reflet de la perfusion superficielle de tissus
LASER DOPPLER INTRODUCTION La technique qui utilise l effet Doppler à partir d un faisceau laser est l une des seules qui permette d enregistrer en continu le reflet de la perfusion superficielle de tissus
Thérapeutique anti-vhc et travail maritime. O. Farret HIA Bégin
 Thérapeutique anti-vhc et travail maritime O. Farret HIA Bégin Introduction «L hépatite C est une maladie le plus souvent mineure, mais potentiellement cancérigène, qu on peut ne pas traiter et surveiller
Thérapeutique anti-vhc et travail maritime O. Farret HIA Bégin Introduction «L hépatite C est une maladie le plus souvent mineure, mais potentiellement cancérigène, qu on peut ne pas traiter et surveiller
Pharmacologie des «nouveaux» anticoagulants oraux
 Pharmacologie des «nouveaux» anticoagulants oraux Apixaban, Dabigatran, Rivaroxaban Pr D. DEPLANQUE Département de Pharmacologie médicale EA 1046 et CIC 9301 INSERM-CHRU, Institut de Médecine Prédictive
Pharmacologie des «nouveaux» anticoagulants oraux Apixaban, Dabigatran, Rivaroxaban Pr D. DEPLANQUE Département de Pharmacologie médicale EA 1046 et CIC 9301 INSERM-CHRU, Institut de Médecine Prédictive
Unité d enseignement 4 : Perception/système nerveux/revêtement cutané
 Énoncés Unité d enseignement 4 : Perception/système nerveux/revêtement cutané N 109 Dermatoses faciales : acné, rosacée, dermatite séborrhéique Diagnostiquer l acné, la rosacée, la dermatite séborrhéique.
Énoncés Unité d enseignement 4 : Perception/système nerveux/revêtement cutané N 109 Dermatoses faciales : acné, rosacée, dermatite séborrhéique Diagnostiquer l acné, la rosacée, la dermatite séborrhéique.
F us u ses c ouc u he h s s po p nt n a t né n es J. L J. an sac CHU H T ou
 Fausses couches spontanées J Lansac CHU Tours Définition Avortement : expulsion produit de conception avant 22SA ou enfant
Fausses couches spontanées J Lansac CHU Tours Définition Avortement : expulsion produit de conception avant 22SA ou enfant
CONCOURS DE L INTERNAT EN PHARMACIE
 Ministère de l enseignement supérieur et de la recherche Ministère de la santé et des sports CONCOURS DE L INTERNAT EN PHARMACIE Valeurs biologiques usuelles Edition de Novembre 2009 (6 pages) Conseil
Ministère de l enseignement supérieur et de la recherche Ministère de la santé et des sports CONCOURS DE L INTERNAT EN PHARMACIE Valeurs biologiques usuelles Edition de Novembre 2009 (6 pages) Conseil
COMMISSION DE LA TRANSPARENCE AVIS. 19 octobre 2011
 COMMISSION DE LA TRANSPARENCE AVIS 19 octobre 2011 PEDIAVEN AP-HP G15, solution pour perfusion 1000 ml de solution en poche bi-compartiment, boîte de 4 (CIP: 419 999-0) PEDIAVEN AP-HP G20, solution pour
COMMISSION DE LA TRANSPARENCE AVIS 19 octobre 2011 PEDIAVEN AP-HP G15, solution pour perfusion 1000 ml de solution en poche bi-compartiment, boîte de 4 (CIP: 419 999-0) PEDIAVEN AP-HP G20, solution pour
Prise de position sur les biosimilaires. Résumé
 Prise de position sur les biosimilaires Résumé Les médicaments biotechnologiques, appelés également biomédicaments, occupent une place importante dans le traitement de maladies comme le cancer, la polyarthrite
Prise de position sur les biosimilaires Résumé Les médicaments biotechnologiques, appelés également biomédicaments, occupent une place importante dans le traitement de maladies comme le cancer, la polyarthrite
XARELTO (RIVAROXABAN) 2,5 MG - 15 MG - 20 MG, COMPRIMÉS PELLICULÉS GUIDE DE PRESCRIPTION
 Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament Xarelto 2,5 mg; 15 mg et 20 mg de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique
Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament Xarelto 2,5 mg; 15 mg et 20 mg de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique
CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE
 CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE BAXTER_CLINIMIX N9G15 E et N12G20E_Avis CT_14-02-2007.pdf BAXTER_CLINIMIX N9G15E N12G20E N14G30 N17G35_Avis CT_12-12-2001.pdf BAXTER_CLINIMIX changement
CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE BAXTER_CLINIMIX N9G15 E et N12G20E_Avis CT_14-02-2007.pdf BAXTER_CLINIMIX N9G15E N12G20E N14G30 N17G35_Avis CT_12-12-2001.pdf BAXTER_CLINIMIX changement
Conseils aux patients* Lutter activement. *pour les patients ayant subi une opération de remplacement de la hanche ou du genou
 Conseils aux patients* Lutter activement contre la thrombose *pour les patients ayant subi une opération de remplacement de la hanche ou du genou 2 Mentions légales Directeur de la publication : Bayer
Conseils aux patients* Lutter activement contre la thrombose *pour les patients ayant subi une opération de remplacement de la hanche ou du genou 2 Mentions légales Directeur de la publication : Bayer
Prise en charge de l embolie pulmonaire
 Prise en charge de l embolie pulmonaire Dr Serge Motte Liège 06.12.14 - Laack TA et Goyal DG, Emerg Med Clin N Am 2004; 961-983 2 PLAN Diagnostic Prise en charge: Phase aiguë: analyse de gravité Choix
Prise en charge de l embolie pulmonaire Dr Serge Motte Liège 06.12.14 - Laack TA et Goyal DG, Emerg Med Clin N Am 2004; 961-983 2 PLAN Diagnostic Prise en charge: Phase aiguë: analyse de gravité Choix
B08 - CAT devant une thrombose veineuse profonde des membres inférieurs
 B08-1 B08 - CAT devant une thrombose veineuse profonde des membres inférieurs 1. I n t r o d u c t i o n La thrombose veineuse profonde (TVP) des membres inférieurs est indissociable de sa complication
B08-1 B08 - CAT devant une thrombose veineuse profonde des membres inférieurs 1. I n t r o d u c t i o n La thrombose veineuse profonde (TVP) des membres inférieurs est indissociable de sa complication
5.5.5 Exemple d un essai immunologique
 5.5.5 Exemple d un essai immunologique Test de grossesse Test en forme de bâtonnet destiné à mettre en évidence l'hormone spécifique de la grossesse, la gonadotrophine chorionique humaine (hcg), une glycoprotéine.
5.5.5 Exemple d un essai immunologique Test de grossesse Test en forme de bâtonnet destiné à mettre en évidence l'hormone spécifique de la grossesse, la gonadotrophine chorionique humaine (hcg), une glycoprotéine.
Gyselle 20/30 SPIRIG HEALTHCARE
 Gyselle 20/30 SPIRIG HEALTHCARE OEMéd Qu est-ce que Gyselle 20/Gyselle 30 et quand doit-il être utilisé? Gyselle 20/Gyselle 30 est un médicament anticonceptionnel hormonal, appelé contraceptif oral ou
Gyselle 20/30 SPIRIG HEALTHCARE OEMéd Qu est-ce que Gyselle 20/Gyselle 30 et quand doit-il être utilisé? Gyselle 20/Gyselle 30 est un médicament anticonceptionnel hormonal, appelé contraceptif oral ou
L endométriose. souvent méconnue. Brochure d information destinée aux femmes atteintes et aux personnes
 L endométriose une maladie gynécologique évolutive, souvent méconnue Brochure d information destinée aux femmes atteintes et aux personnes intéressées Groupe d experts de l endométriose de la Société d
L endométriose une maladie gynécologique évolutive, souvent méconnue Brochure d information destinée aux femmes atteintes et aux personnes intéressées Groupe d experts de l endométriose de la Société d
Le traitement de l'insuffisance cardiaque chez le chien
 Folia veterinaria Le traitement de l'insuffisance cardiaque chez le chien Les principaux traitements à instaurer chez le chien insuffisant cardiaque sont passés en revue en insistant sur les critères de
Folia veterinaria Le traitement de l'insuffisance cardiaque chez le chien Les principaux traitements à instaurer chez le chien insuffisant cardiaque sont passés en revue en insistant sur les critères de
Migraine et céphalées de tension: diagnostic différentiel et enjeux thérapeutiques
 Migraine et céphalées de tension: diagnostic différentiel et enjeux thérapeutiques Dr Solène de Gaalon Service de neurologie- CHU Nantes Société française des migraines et céphalées Céphalées de tension
Migraine et céphalées de tension: diagnostic différentiel et enjeux thérapeutiques Dr Solène de Gaalon Service de neurologie- CHU Nantes Société française des migraines et céphalées Céphalées de tension
Pharmacovigilance des nouveaux anticoagulants oraux
 Pharmacovigilance des nouveaux anticoagulants oraux Dr A.Lillo-Le Louët, Centre Régional de Pharmacovigilance (CRPV) Paris-HEGP Avec avec Dr P.Lainé, CRPV - Angers Préambule Directeur du Centre Régional
Pharmacovigilance des nouveaux anticoagulants oraux Dr A.Lillo-Le Louët, Centre Régional de Pharmacovigilance (CRPV) Paris-HEGP Avec avec Dr P.Lainé, CRPV - Angers Préambule Directeur du Centre Régional
Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE. Hépatite chronique B
 Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE Hépatite chronique B Février 2015 Ce document est téléchargeable sur : www.has-sante.fr Haute Autorité de Santé Service des
Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE Hépatite chronique B Février 2015 Ce document est téléchargeable sur : www.has-sante.fr Haute Autorité de Santé Service des
ORDONNANCE COLLECTIVE
 ORDONNANCE COLLECTIVE Assurer le suivi des personnes recevant un Page 1 de 12 O.C. 6.5 Professionnels visés : Les infirmières qui possèdent la formation, les connaissances et les compétences nécessaires,
ORDONNANCE COLLECTIVE Assurer le suivi des personnes recevant un Page 1 de 12 O.C. 6.5 Professionnels visés : Les infirmières qui possèdent la formation, les connaissances et les compétences nécessaires,
Activité 38 : Découvrir comment certains déchets issus de fonctionnement des organes sont éliminés de l organisme
 Activité 38 : Découvrir comment certains déchets issus de fonctionnement des organes sont éliminés de l organisme 1. EXTRAITS REFERENTIELS DU BO Partie du programme : Fonctionnement de l organisme et besoin
Activité 38 : Découvrir comment certains déchets issus de fonctionnement des organes sont éliminés de l organisme 1. EXTRAITS REFERENTIELS DU BO Partie du programme : Fonctionnement de l organisme et besoin
Informations sur le rivaroxaban (Xarelto md ) et l apixaban (Eliquis md )
 Informations sur le rivaroxaban (Xarelto md ) et l apixaban (Eliquis md ) Préambule Ce document présente plusieurs informations utiles pour les prescripteurs afin de les aider lors de l utilisation du
Informations sur le rivaroxaban (Xarelto md ) et l apixaban (Eliquis md ) Préambule Ce document présente plusieurs informations utiles pour les prescripteurs afin de les aider lors de l utilisation du
EXEMPLE DE METHODOLOGIE POUR L ELABORATION D UN PROTOCOLE DOULEUR Marie AUBRY Infirmière référente douleur Hôpital TENON AP-HP Paris XX e SOMMAIRE
 EXEMPLE DE METHODOLOGIE POUR L ELABORATION D UN PROTOCOLE DOULEUR Marie AUBRY Infirmière référente douleur Hôpital TENON AP-HP Paris XX e SOMMAIRE Etape n 1 : Faire l état des lieux Identifier la situation
EXEMPLE DE METHODOLOGIE POUR L ELABORATION D UN PROTOCOLE DOULEUR Marie AUBRY Infirmière référente douleur Hôpital TENON AP-HP Paris XX e SOMMAIRE Etape n 1 : Faire l état des lieux Identifier la situation
Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS)
 Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS) Édition Conseil du médicament www.cdm.gouv.qc.ca Coordination Anne Fortin, pharmacienne Élaboration Conseil du médicament Fédération
Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS) Édition Conseil du médicament www.cdm.gouv.qc.ca Coordination Anne Fortin, pharmacienne Élaboration Conseil du médicament Fédération
French Version. Aciclovir Labatec 250 mg (For Intravenous Use Only) 02/2010. Product Information Leaflet for Aciclovir Labatec i.v.
 Product Information Leaflet for Aciclovir Labatec i.v. 250 mg French Version Aciclovir Labatec i.v. Composition Principe actif: Aciclovirum ut Acicloviri natricum (Praeparatio cryodesiccata). Excipients:
Product Information Leaflet for Aciclovir Labatec i.v. 250 mg French Version Aciclovir Labatec i.v. Composition Principe actif: Aciclovirum ut Acicloviri natricum (Praeparatio cryodesiccata). Excipients:
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine
 KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
Fiche Produit Profils Médicalisés PHMEV
 Guide méthodologique développé par l équipe de projets ci-dessous : Fiche Produit Profils Médicalisés PHMEV EQUIPE PROJET Chef de projet : Maryline CHARRA, Pharmacien Conseil Responsable de la mission
Guide méthodologique développé par l équipe de projets ci-dessous : Fiche Produit Profils Médicalisés PHMEV EQUIPE PROJET Chef de projet : Maryline CHARRA, Pharmacien Conseil Responsable de la mission
Etat des lieux et perspectives du don d'ovocytes en France
 Inspection générale des affaires sociales RM2011-024P Etat des lieux et perspectives du don d'ovocytes en France RAPPORT TOME I Établi par Dr Pierre ABALLEA Anne BURSTIN Jérôme GUEDJ Membres de l Inspection
Inspection générale des affaires sociales RM2011-024P Etat des lieux et perspectives du don d'ovocytes en France RAPPORT TOME I Établi par Dr Pierre ABALLEA Anne BURSTIN Jérôme GUEDJ Membres de l Inspection
Nouveaux anticoagulants oraux (NOAC)
 Nouveaux anticoagulants oraux (NOAC) Mécanisme d action Suivi biologique: comment et quand? A.Demulder IRIS-Lab 15/05/2013 1 Anticoagulants «traditionnels»: HNF Parentéral Suivi biologique avec ajustement
Nouveaux anticoagulants oraux (NOAC) Mécanisme d action Suivi biologique: comment et quand? A.Demulder IRIS-Lab 15/05/2013 1 Anticoagulants «traditionnels»: HNF Parentéral Suivi biologique avec ajustement
La Dysplasie Ventriculaire Droite Arythmogène
 1 La Dysplasie Ventriculaire Droite Arythmogène Document rédigé par l équipe pluridisciplinaire du centre de référence pour les maladies cardiaques héréditaires (Paris), en collaboration avec des patients
1 La Dysplasie Ventriculaire Droite Arythmogène Document rédigé par l équipe pluridisciplinaire du centre de référence pour les maladies cardiaques héréditaires (Paris), en collaboration avec des patients
Que sont les. inhibiteurs?
 Que sont les inhibiteurs? TABLE DES MATIÈRES Publié par la Fédération mondiale de l hémophilie (FMH) Fédération mondiale de l hémophilie, 2010 La FMH encourage la redistribution de ses publications à des
Que sont les inhibiteurs? TABLE DES MATIÈRES Publié par la Fédération mondiale de l hémophilie (FMH) Fédération mondiale de l hémophilie, 2010 La FMH encourage la redistribution de ses publications à des
Les nouveaux anticoagulants oraux sont arrivé! Faut il une surveillance biologique?
 Les nouveaux anticoagulants oraux sont arrivé! Faut il une surveillance biologique? Références : Pr Samama Journée de Biologie Praticienne Décembre 2011 I. Gouin-Thibault Journée de Biologie Clinique 2012
Les nouveaux anticoagulants oraux sont arrivé! Faut il une surveillance biologique? Références : Pr Samama Journée de Biologie Praticienne Décembre 2011 I. Gouin-Thibault Journée de Biologie Clinique 2012
Hémostase et Endocardite Surveillance des anticoagulants. Docteur Christine BOITEUX
 Hémostase et Endocardite Surveillance des anticoagulants Docteur Christine BOITEUX Théorie Endocardites et anticoagulation POUR Thromboses Emboles septiques CONTRE Favorise emboles septiques et diffusion
Hémostase et Endocardite Surveillance des anticoagulants Docteur Christine BOITEUX Théorie Endocardites et anticoagulation POUR Thromboses Emboles septiques CONTRE Favorise emboles septiques et diffusion
Mais pourquoi je ne suis pas enceinte?
 Mais pourquoi je ne suis pas? On a beau vouloir très fort un bébé, la nature ne nous obéit pas toujours au doigt et à l œil Ce qu il faut savoir pour être au top de sa fertilité et tomber plus facilement!...
Mais pourquoi je ne suis pas? On a beau vouloir très fort un bébé, la nature ne nous obéit pas toujours au doigt et à l œil Ce qu il faut savoir pour être au top de sa fertilité et tomber plus facilement!...
L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015
 L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015 Objectifs de la présentation Décrire l évolution clinique et la prise en charge d
L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015 Objectifs de la présentation Décrire l évolution clinique et la prise en charge d
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES :
 FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
Chapitre 1 : Introduction à la rééducation périnéale
 Chapitre 1 : Introduction à la rééducation périnéale 1. Historique. Kegel (1949). Bourcier (1970). 1985 : reconnaissance officielle d acte de MK. Développement de la MK périnéale : facteur éco/p sociale
Chapitre 1 : Introduction à la rééducation périnéale 1. Historique. Kegel (1949). Bourcier (1970). 1985 : reconnaissance officielle d acte de MK. Développement de la MK périnéale : facteur éco/p sociale
