French Version. Aciclovir Labatec 250 mg (For Intravenous Use Only) 02/2010. Product Information Leaflet for Aciclovir Labatec i.v.
|
|
|
- Coralie Flavie Viau
- il y a 8 ans
- Total affichages :
Transcription
1 Product Information Leaflet for Aciclovir Labatec i.v. 250 mg French Version Aciclovir Labatec i.v. Composition Principe actif: Aciclovirum ut Acicloviri natricum (Praeparatio cryodesiccata). Excipients: Aucun. Forme galénique et quantité de principe actif par unité Poudre pour solution pour perfusion. Flacon perforable à 250 mg d Aciclovir. Indications/Possibilités d emploi Infections dues à des virus Herpes simplex 1 et 2 Infections de la peau et des muqueuses, notamment primoinfection et récidives d herpès génital et d herpès labial; encéphalite à virus Herpes simplex; prévention des infections à virus Herpes simplex chez les patients immunodéprimés; Posologie/Mode d emploi Perfuser la dose nécessaire par voie intraveineuse, lentement, en l espace d une heure. Le traitement dure habituellement 5 jours, mais sa durée dépend essentiellement de l état du patient et du résultat du traitement. Le traitement de l encéphalite herpétique et des infections à herpes simplex du nouveau-né dure habituellement 10 jours. Adultes et enfants de plus de 12 ans Herpes simplex 5 mg/kg toutes les 8 heures. Zona 5 mg/kg toutes les 8 heures. Zona chez les patients immunodéprimés à fonction rénale normale 10 mg/kg toutes les 8 heures pendant 5 jours et plus. Encéphalite herpétique 10 mg/kg toutes les 8 heures pendant 10 jours. Prévention de l infection à CMV en cas de transplantation de moelle osseuse allogénique suppression des infections récidivantes à Herpes simplex (notamment herpès génital) chez les patients immunocompétents quand les autres traitements sont insuffisamment efficaces et que ces infections provoquent des troubles fréquents et prolongés; kératite à virus Herpes simplex; Herpes simplex du nouveau-né; pour les infections herpétiques graves (c est-à-dire les infections disséminées), l efficacité n a été étudiée que sur un petit nombre de patients et en outre l équivalence avec la vidarabine n est pas démontrée. Infections à virus herpétique varicelle-zona Zona (entreprendre le traitement aussi tôt que possible, c est-à-dire dans les 72 heures), chez les patients immunocompétents mais surtout chez les patients immunodéprimés, dans les formes disséminées et en cas de zona ophtalmique. Pour l instant, il n est pas parfaitement prouvé que le traitement a un effet favorable sur la névralgie post-zostérienne. Transplantation de moelle osseuse allogénique On utilise Aciclovir Labatec pour la prophylaxie des infections à CMV en cas de transplantation de moelle osseuse allogénique quand les patients sont séropositifs pour le CMV ou chez les patients séronégatifs mais dont le donneur est séropositif. Le traitement préventif commence 5 jours avant la transplantation et s achève le jour 30. Si on découvre ultérieurement du CMV dans le sang, il faut rapidement instaurer un traitement par une substance active contre le CMV (par exemple le ganciclovir). 500 mg/m² toutes les 8 heures. Durée: Commencer le traitement 5 jours avant la transplantation et le poursuivre pendant 30 jours après. Enfants âgés de 3 mois à 12 ans Herpes simplex 250 mg/m² toutes les 8 heures. Infection à virus varicelle-zona 250 mg/m² toutes les 8 heures. Varicelle chez les patients immunodéprimés à fonction rénale normale 500 mg/m² toutes les 8 heures. Encéphalite herpétique 500 mg/m² toutes les 8 heures pendant 10 jours. Transplantation de moelle osseuse allogénique (enfants >2 ans) GSASA - Questionnaire Page 1
2 500 mg/m² toutes les 8 heures, en commençant 5 jours avant la transplantation et en poursuivant jusqu à 30 jours après. Il ne faut pas utiliser de liquides biologiques ou colloïdaux (sang, solutions contenant des protéines). Les rares données disponibles permettent de supposer que les enfants de plus de 2 ans qui requièrent une transplantation de moelle osseuse doivent recevoir la même dose que les adultes pour la prévention de l infection à CMV. Nouveau-nés En cas d infection néonatale à Herpes simplex, il faut administrer Aciclovir Labatec à raison de 10 mg/kg toutes les 8 heures. Il faut ajuster la dose selon l âge, en tenant compte de la diminution de la clairance. Lors de la dilution, il faut respecter les règles suivantes: Pour les adultes, il faut ajouter la quantité nécessaire d Aciclovir à au moins 50 ml de liquide. On peut ajouter des doses de 250 à 500 mg dans 100 ml de soluté pour perfusion. Si la dose est plus forte, il faut préparer une deuxième perfusion ou augmenter le volume de liquide. Pour les enfants et nouveau-nés, chez lesquels la dose peut être égale ou inférieure à 100 mg, il faut ajouter 4 ml d Aciclovir dissous (100 mg d Aciclovir) à 20 ml de soluté pour perfusion. Patients âgés Chez le patient âgé, il faut tenir compte d une éventuelle insuffisance rénale et la posologie sera ajustée en conséquence (cf. «Posologie en cas d insuffisance rénale»). Veiller à assurer un apport liquidien suffisant. Posologie en cas d insuffisance rénale La prudence est de rigueur lors de l administration parentérale d Aciclovir chez les insuffisants rénaux. Veiller à assurer un apport liquidien suffisant. Les ajustements posologiques suivants sont recommandés: Clearance de la Posologie i.v. créatinine >50 ml Dose usuelle, toutes les 8 h (5 ou 10 mg/kg ou 500 mg/m²) ml/min Dose usuelle, toutes les 12 h ml/min Dose usuelle, toutes les 24 h 0 (anurie) 10 ml/min La moitié de la dose usuelle, toutes les 24 h Sous hémodialyse La moitié de la dose usuelle, toutes les 24 h et après la dialyse Préparation de la solution pour perfusion Comme les flacons perforables ne contiennent pas de conservateur, il faut respecter l asepsie lors de la reconstitution de la solution d Aciclovir Labatec et de la dilution par d autres solutions pour perfusion; ces manipulations doivent de préférence être effectuées immédiatement avant l emploi et il faut jeter toute solution reconstituée qui n a pas été utilisée. Reconstitution de la solution d Aciclovir Labatec Dissoudre la poudre lyophilisée d Aciclovir dans 10 ml d eau pour préparations injectables ou de solution de NaCl à 0,9%. 1 ml de la solution ainsi obtenue contient 25 mg d Aciclovir. Pour l administration, on peut soit perfuser cette solution à l aide d une pompe à perfusion en l espace d une heure (pas plus vite!) soit la diluer avec une solution pour perfusion. Dilution par d autres solutions pour perfusion A cet effet, on peut utiliser les solutions suivantes: soluté de NaCl à 0,45% ou 0,9%; soluté de NaCl à 0,18% + glucose à 4%; soluté de NaCl à 0,45% + glucose à 2,5%; soluté de Hartmann (soluté de lactate pour perfusion). Après l adjonction d Aciclovir Labatec, il faut bien agiter le soluté pour perfusion. Si la dilution est effectuée correctement, la concentration d Aciclovir ne dépasse pas 5 mg/ml (0,5%). Conservée à température ambiante (entre 15 et 25 C), la solution pour perfusion reste stable pendant 8 heures au maximum (stabilité physico-chimique). S il apparaît un trouble ou une cristallisation avant ou pendant la perfusion, il ne faut pas utiliser la solution pour perfusion. Contre-indications L usage d Aciclovir Labatec est contre-indiqué en cas d hypersensibilité connue à l Aciclovir et au valaciclovir. Mises en garde et précautions Utilisation en cas d insuffisance rénale et chez les patients âgés: l Aciclovir est éliminé par voie rénale, la posologie doit donc être réduite chez les patients insuffisants rénaux (cf. «Posologie/Mode d emploi»). La probabilité de troubles de la fonction rénale est majorée chez les patients âgés, une réduction posologique peut donc s avérer nécessaire dans ce groupe de patients. Aussi bien les insuffisants rénaux que les patients âgés sont exposés à un risque accru de troubles neurologiques; par conséquent, ils seront surveillés étroitement pour déceler les signes de ces effets indésirables. Dans les cas rapportés, les troubles étaient généralement réversibles après l arrêt du traitement (cf. «Effets indésirables»). S il faut perfuser des doses fortes d Aciclovir Labatec, par exemple en raison d une encéphalite herpétique, il faut surveiller la fonction rénale, surtout chez les patients déshydratés. Le ph de la solution d Aciclovir Labatec pour perfusion est d environ 11; il ne faut donc pas l ingérer. Etant donné que l herpès génital est une maladie sexuellement transmissible, il faut dire aux patientes et patients d éviter tout contact sexuel tant que des lésions visibles persistent. Interactions L Aciclovir est essentiellement excrété sous forme inchangée par voie rénale, par sécrétion tubulaire active. Les médicaments administrés en même temps et qui sont soumis au même mécanisme, peuvent provoquer une augmentation des taux plasmatiques d Aciclovir. Par ce mécanisme, le probénécide et la cimétidine provoquent une augmentation de l ASC de l Aciclovir et une diminution de sa clairance rénale. Cependant, du fait que la marge thérapeutique de l Aciclovir est large, aucun ajustement posologique n est nécessaire. Chez les patients qui reçoivent Aciclovir Labatec par voie intraveineuse, il faut être prudent lors de l administration concomitante de médicaments éliminés selon le même mécanisme, car les taux plasmatiques de l un ou des deux médicaments ou de leurs métabolites risquent d augmenter. Lors GSASA - Questionnaire Page 2
3 de l administration simultanée d Aciclovir et de mycophénolate mofétil, un immunosuppresseur utilisé lors des transplantations, on a constaté une augmentation de l ASC de l Aciclovir et du métabolite inactif du mycophénolate mofétil. Il faut également être prudent (et surveiller la fonction rénale) lorsque l Aciclovir Labatec est administré par voie intraveineuse en même temps que des médicaments qui influent sur d autres aspects de la fonction rénale (par exemple ciclosporine et tacrolimus). Grossesse/Allaitement Grossesse On a consigné, dans un registre des grossesses, les informations relatives aux enfants issus de femmes traitées par l Aciclovir (informations relevées chez des volontaires). On n a pas constaté d augmentation du nombre d anomalies congénitales et d anomalies spécifiques, comparativement à la population générale. Parmi 1082 naissances, on a observé 28 malformations qui n ont, semble-t-il, aucun caractère bien systématisé et aucune cause commune. Néanmoins, pendant la grossesse, le traitement intraveineux et oral n est indiqué qu en cas de nécessité impérieuse (voir aussi «Données précliniques»). Fertilité Pour l instant, il n existe pas d informations concernant l influence d Aciclovir Labatec intraveineux sur la fertilité féminine. Chez des hommes présentant un nombre normal de spermatozoïdes, l administration orale chronique d Aciclovir n a pas eu de retentissement cliniquement notable sur le nombre, la morphologie ou la motilité des spermatozoïdes. Réactions systémiques d hypersensibilité Très rarement: Anaphylaxie engageant le pronostic vital, fièvre, oedème de Quincke. Troubles psychiatriques et perturbations du système nerveux Très rarement: Céphalées, vertiges, agitation, confusion mentale, tremblement, ataxie, dysarthrie, hallucinations, symptômes psychotiques, convulsions, somnolence, encéphalopathie (y compris encéphalopathie toxique), coma. En dehors de très rares cas mortels, ces phénomènes ont le plus souvent été réversibles et ont généralement été observés chez les patients insuffisants rénaux ou présentant d autres facteurs prédisposant, p.ex. âge avancé sans insuffisance rénale préexistante. Pour le traitement, la dialyse a souvent été efficace. Vaisseaux Souvent: Phlébite. Appareil respiratoire Très rarement: Dyspnée. Appareil gastro-intestinal Souvent: Nausées, vomissements. Très rarement: Diarrhée, douleurs abdominales. Allaitement Foie et bile Après l administration orale de 200 mg 5 fois par jour, on a trouvé, dans le lait maternel, des concentrations d Aciclovir qui représentaient 0,6 à 4,1 fois le taux plasmatique. De telles concentrations exposeraient le nourrisson à une dose allant jusqu à 0,3 mg/kg par jour. Pour cette raison il ne faut pas allaiter pendant un traitement par Aciclovir Labatec. Souvent: Augmentation réversible du taux des enzymes hépatiques. Très rarement: Augmentation réversible du taux de bilirubine, ictère, hépatite. Effet sur l aptitude à la conduite et l utilisation de machines Aciclovir Labatec est généralement utilisé chez des patients hospitalisés. On n a pas mené d études concernant l effet d Aciclovir Labatec sur l aptitude à la conduite de véhicules ou à l utilisation de machines. Peau et tissu sous-cutané Souvent: Prurit, urticaire, éruption cutanée (y compris photosensibilisation). Très rarement: Alopécie diffuse. Reins et voies urinaires Compte tenu des effets secondaires d Aciclovir Labatec sur le système nerveux central, une perturbation de l aptitude à la conduite automobile et à l utilisation de machines ne peut pas être exclue. Effets indésirables Les effets indésirables observés sont classés de la façon suivante, en fonction de leur fréquence: Très souvent ( 1/10), souvent ( 1/100, <1/10), occasionnellement ( 1/1 000; <1/100), rarement ( 1/10 000, <1/1 000) et très rarement (<1/10 000). Sang et système lymphoïde Occasionnellement: Diminution des paramètres hématologiques (anémie, thrombopénie, leucopénie, neutropénie). Souvent: Augmentation de l urée et de la créatininémie. On suppose qu il existe une relation entre augmentation rapide de l urée et de la créatininémie, d une part, et les concentrations plasmatiques maximales ainsi que l état d hydratation du patient, d autre part (voir aussi «Surdosage»). Pour éviter ce phénomène, il ne faut pas injecter le médicament en bolus, mais en perfusion lente, en l espace d une heure. Très rarement: Perturbations de la fonction rénale, insuffisance rénale aiguë, douleurs rénales. Il faut veiller à assurer un apport liquidien suffisant. Une dégradation de la fonction rénale répond généralement rapidement à la réhydratation du patient et/ou à une réduction de la posologie ou à l arrêt du traitement. Cependant, exceptionnellement, il peut se développer une insuffisance rénale aiguë. GSASA - Questionnaire Page 3
4 Les douleurs rénales peuvent être associées à une insuffisance rénale. Troubles généraux et réactions au site d administration Très rarement: Fatigue, réactions inflammatoires locales. Après la perfusion accidentelle d Aciclovir Labatec dans le tissu extravasculaire, on a noté des réactions inflammatoires locales graves qui, dans quelques cas, ont conduit à une destruction de la peau. Surdosage Après des surdosages en Aciclovir administré par voie intraveineuse, on a constaté une augmentation du taux sérique de créatinine et de l urée, avec ensuite une insuffisance rénale. Après des surdosages, on a décrit des réactions neurologiques, y compris confusion mentale, hallucinations, états d agitation, crises convulsives et coma. Traitement: Il faut soigneusement surveiller les patients pour dépister les signes de toxicité. L hémodialyse améliore significativement l élimination de l Aciclovir à partir du sang si bien qu en cas de surdosage en Aciclovir, on peut envisager le recours à l hémodialyse comme possibilité de traitement. Propriétés/Effets Code ATC: J05AB01 Pharmacocinétique Absorption Chez l adulte, les concentrations plasmatiques moyennes à l état d équilibre après la perfusion de doses de 2,5 mg/kg, 5 mg/kg, 10 mg/kg et 15 mg/kg d Aciclovir, pendant une heure toutes les huit heures sont les suivantes: C max 5,1 µg/ml, 9,8 µg/ml, 20,7 µg/ml et 23,6 µg/ml et C min, mesurée 7 heures plus tard: 0,5 µg/ml, 0,7 µg/ml, 2,3 µg/ml et 2,0 µg/ml. Distribution Le taux de liaison aux protéines plasmatiques est relativement faible (de 9% à 33%) et il n y a pas lieu de craindre des interactions par supplantation. La concentration dans le liquide céphalorachidien atteint environ 50% du taux plasmatique et la concentration dans les vésicules des efflorescences cutanées herpétiques est à peu près égale à la concentration plasmatique. Le volume de distribution à l état d équilibre est en moyenne de 48 l/1,73 m² chez l adulte et de 28,8 l/1,73 m² chez le nouveau-né. L Aciclovir traverse le placenta et passe également dans le lait maternel. Les concentrations dans le lait maternel sont plus élevées que les concentrations enregistrées au même moment dans le plasma maternel (voir aussi «Grossesse/Allaitement»). La DE 50 moyenne est estimée à 0,1 µg/ml pour le HSV et 1 µg/ml pour le VZV. Métabolisme/Elimination Mécanisme d action L Aciclovir est une substance antivirale qui, in vitro et in vivo, exerce un effet inhibiteur sur les virus Herpes simplex (HSV) de type 1 et 2, et sur les virus varicelle-zona (VZV). En culture cellulaire, l activité antivirale de l Aciclovir est maximale contre le HSV 1; viennent ensuite, par ordre décroissant de l effet, le HSV 2 et le VZV. L effet inhibiteur de l Aciclovir sur le HSV 1, le HSV 2 et le VZV est très sélectif. Comme l Aciclovir n utilise pratiquement pas comme substrat la thymidine-kinase (TK) des cellules normales, non infectées, sa toxicité sur la cellule hôte est faible. Par contre, la TK codée par le HSV ou le VZV transforme l Aciclovir en monophosphate d Aciclovir, un analogue des nucléosides, lequel est transformé en diphosphate et finalement en triphosphate, sous l effet d enzymes cellulaires. Le triphosphate d Aciclovir interfère avec l ADN-polymérase virale et empêche la réplication de l ADN viral, de sorte qu après incorporation dans l ADN viral la chaîne est interrompue. Des utilisations prolongées et répétées d Aciclovir chez des patients gravement immunodéprimés peuvent faire apparaître des souches virales de sensibilité réduite, qui ne répondent plus au traitement par l Aciclovir. Le plus souvent, les isolats cliniques de sensibilité réduite présentent un déficit relatif en TK virale, mais on a aussi trouvé des souches avec modification de la TK virale ou de l ADN-polymérase virale. Des souches moins sensibles à l Aciclovir peuvent également se développer in vitro lors de l exposition d isolats de HSV à l Aciclovir. La relation entre la sensibilité des isolats d HSV déterminée in vitro et la réponse clinique au traitement par l Aciclovir n est pas claire. C est pourquoi, quand il existe des lésions actives, il est important d éviter tout contact susceptible de favoriser une transmission du virus. Le seul métabolite important de l Aciclovir est la 9- carboxyméthoxyméthyl-guanine, qui représente environ 10 à 15% de la quantité excrétée dans les urines. Après administration intraveineuse d Aciclovir, la demi-vie est d environ 2,9 heures chez l adulte. La majeure partie de l Aciclovir est excrétée sous forme inchangée par voie rénale. Comme la clairance rénale de l Aciclovir est nettement plus importante que la clairance de la créatinine, l excrétion rénale du médicament repose certainement non seulement sur une filtration glomérulaire, mais aussi sur une sécrétion tubulaire. L élimination extra-rénale est de 10% (Q 0 = 0,1) et la clairance corporelle totale de 260 ± 81 ml/min/1,73 m². Cinétique pour certains groupes de patients Chez des enfants de plus d un an, on a trouvé des valeurs de C max et de C min comparables à celles de l adulte, après l administration de doses de 250 mg/m² au lieu de 5 mg/kg et de 500 mg/m² au lieu de 10 mg/kg. Entre l âge de 1 an et l âge de 17 ans, la demi-vie moyenne est de 2,5 heures. Chez des nouveau-nés (0 3 mois) traités toutes les huit heures par une perfusion de 10 mg/kg administrée en l espace d une heure, on a trouvé une C max de 13,8 µg/ml et une C min de 2,3 µg/ml. La demi-vie était de 3,8 heures. En principe, la demi-vie t ½ dépend du degré de maturité des mécanismes régissant l excrétion rénale. Ce degré de maturité est lui-même fonction de l âge gestationnel, de l âge chronologique et du poids. Chez le nouveau-né à terme, la clairance corporelle totale est en moyenne d environ un tiers de celle des adultes. GSASA - Questionnaire Page 4
5 Chez les patients âgés, la clairance corporelle totale diminue en fonction de l âge, parallèlement à la diminution de la clairance de la créatinine, mais sans modification notable de la demi-vie. En cas d insuffisance rénale chronique, la demi-vie est de 19,5 heures; pendant une hémodialyse, elle est de 5,7 heures. Pendant la dialyse, le taux plasmatique d Aciclovir diminue d environ 60%. Comme l ont montré des études, ni les paramètres pharmacocinétiques de l Aciclovir ni ceux de la zidovudine ne se modifient quand ces deux médicaments sont utilisés en même temps chez des patients infectés par le VIH. Données précliniques Numéro d autorisation (Swissmedic). Présentation Aciclovir Labatec i.v. poudre pour solution pour perfusion à 250 mg : flacons perforables 5 [A]. Titulaire de l autorisation Labatec Pharma SA, 1217 Meyrin (Genève). Mutagénicité/Cancérogénicité Les tests de mutagénicité effectués à ce jour in vitro et sur des animaux ne montrent pas de risque génétique pour l être humain; l Aciclovir n est pas cancérogène. Mise à jour de l information Novembre 2009 Tératogénicité Utilisé par voie systémique chez des lapins, rats et souris dans des tests standard universellement admis, l Aciclovir n a eu aucun effet embryotoxique ou tératogène. Dans un test non standardisé effectué chez des rates, on a observé des malformations foetales, mais uniquement après l administration sous-cutanée de doses très fortes, toxiques pour la mère. La signification clinique de cette observation n est pas encore établie. Remarques particulières Incompatibilités Il faut utiliseraciclovir Labatec i.v. dans les solutés pour perfusion susmentionnés (voir «Préparation de la solution pour perfusion») et à la concentration indiquée. Il ne faut pas utiliser de liquides biologiques ou colloïdaux (sang, solutions contenant des protéines). Conservation Ce médicament ne doit être utilisé que jusqu à la date imprimée sur l emballage avec la mention «EXP». Remarques concernant le stockage Conserver les flacons perforables à température ambiante (15-25 C) et hors de portée des enfants. Etant donné que les flacons perforables ne contiennent pas de conservateur, il faut préparer la solution reconstituée d Aciclovir Labatec immédiatement avant l emploi. Toute solution reconstituée inutilisée doit être jetée. La solution diluée avec un autre soluté pour perfusion reste stable pendant 8 heures au maximum à température ambiante (15 25 C) (stabilité physico-chimique). GSASA - Questionnaire Page 5
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Le VIH et votre foie
 Le VIH et votre foie Le VIH et votre foie Que dois-je savoir au sujet de mon foie? Votre foie joue un rôle incroyablement important. Il filtre votre sang en éliminant les substances nocives (toxiques)
Le VIH et votre foie Le VIH et votre foie Que dois-je savoir au sujet de mon foie? Votre foie joue un rôle incroyablement important. Il filtre votre sang en éliminant les substances nocives (toxiques)
Suivi ambulatoire de l adulte transplanté rénal au-delà de 3 mois après transplantation
 SYNTHESE DES RECOMMANDATIONS PROFESSIONNELLES Suivi ambulatoire de l adulte transplanté rénal au-delà de 3 mois après transplantation Novembre 2007 OBJECTIF Assurer une qualité optimale du suivi et de
SYNTHESE DES RECOMMANDATIONS PROFESSIONNELLES Suivi ambulatoire de l adulte transplanté rénal au-delà de 3 mois après transplantation Novembre 2007 OBJECTIF Assurer une qualité optimale du suivi et de
COMMISSION DE LA TRANSPARENCE. Avis. 3 septembre 2008
 COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
Le traitement du paludisme d importation de l enfant est une urgence
 Le traitement du paludisme d importation de l enfant est une urgence Dominique GENDREL Necker-Enfants Malades Traiter en urgence en présence de trophozoïtes Plus de 80% des paludismes d importation en
Le traitement du paludisme d importation de l enfant est une urgence Dominique GENDREL Necker-Enfants Malades Traiter en urgence en présence de trophozoïtes Plus de 80% des paludismes d importation en
E04a - Héparines de bas poids moléculaire
 E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION. 10 octobre 2001
 COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
NOTICE: INFORMATION DE L UTILISATEUR. Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain)
 NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
HEPATITES VIRALES 22/09/09. Infectieux. Mme Daumas
 HEPATITES VIRALES 22/09/09 Mme Daumas Infectieux Introduction I. Hépatite aigu II. Hépatite chronique III. Les différents types d hépatites A. Hépatite A 1. Prévention de la transmission 2. Vaccination
HEPATITES VIRALES 22/09/09 Mme Daumas Infectieux Introduction I. Hépatite aigu II. Hépatite chronique III. Les différents types d hépatites A. Hépatite A 1. Prévention de la transmission 2. Vaccination
Professeur Diane GODIN-RIBUOT
 UE3-2 - Physiologie rénale Chapitre 5 : Mesure de la fonction rénale : la clairance rénale Professeur Diane GODIN-RIBUOT Année universitaire 2011/2012 Université Joseph Fourier de Grenoble - Tous droits
UE3-2 - Physiologie rénale Chapitre 5 : Mesure de la fonction rénale : la clairance rénale Professeur Diane GODIN-RIBUOT Année universitaire 2011/2012 Université Joseph Fourier de Grenoble - Tous droits
Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
 Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Par fiole: L - asparaginase 10.000 U.I. Pour les excipients, cfr section 6.1. 3.
Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Par fiole: L - asparaginase 10.000 U.I. Pour les excipients, cfr section 6.1. 3.
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT. Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl par comprimé enrobé.
 RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1. Dé nomination du mé dicame nt Bisolax 5 mg comprimés enrobés. 2. Composition qualitative e t quantitative Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1. Dé nomination du mé dicame nt Bisolax 5 mg comprimés enrobés. 2. Composition qualitative e t quantitative Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl
NOTICE : INFORMATION DE L UTILISATEUR. Delphi 0,1 % crème Acétonide de triamcinolone
 NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
Le don de moelle osseuse :
 DON DE MOELLE OSSEUSE Le don de moelle osseuse : se décider aujourd hui, s engager pour longtemps LA MOELLE OSSEUSE ET SA GREFFE La moelle osseuse C est le tissu mou dans le centre du corps des os qui
DON DE MOELLE OSSEUSE Le don de moelle osseuse : se décider aujourd hui, s engager pour longtemps LA MOELLE OSSEUSE ET SA GREFFE La moelle osseuse C est le tissu mou dans le centre du corps des os qui
Information professionnelle du Compendium Suisse des Médicaments. Aridol TRIMEDAL
 Aridol TRIMEDAL OEMéd Composition Principe actif: Mannitol. Excipients Gélules de 5, 10, 20 et 40 mg: Colorant: dioxyde de titane E 171. Gélules de 10, 20 et 40 mg: Colorant: oxyde de fer E 172. Forme
Aridol TRIMEDAL OEMéd Composition Principe actif: Mannitol. Excipients Gélules de 5, 10, 20 et 40 mg: Colorant: dioxyde de titane E 171. Gélules de 10, 20 et 40 mg: Colorant: oxyde de fer E 172. Forme
COMMISSION DE LA TRANSPARENCE AVIS. 10 mai 2006
 COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
NOTICE : INFORMATION DE L'UTILISATEUR. DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc
 NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
INTERET PRATIQUE DU MDRD AU CHU DE RENNES
 INTERET PRATIQUE DU MDRD AU CHU DE RENNES QU EST-CE QUE LE MDRD? Il s agit d une formule permettant d estimer le débit de filtration glomérulaire et donc la fonction rénale La formule est la suivante :
INTERET PRATIQUE DU MDRD AU CHU DE RENNES QU EST-CE QUE LE MDRD? Il s agit d une formule permettant d estimer le débit de filtration glomérulaire et donc la fonction rénale La formule est la suivante :
HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI. http://www.infectiologie.org.tn
 HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI LES MOYENS THERAPEUTIQUES Les interférons La ribavirine Les nouveaux produits INTERFERONS 1957: activité antivirale Interférence
HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI LES MOYENS THERAPEUTIQUES Les interférons La ribavirine Les nouveaux produits INTERFERONS 1957: activité antivirale Interférence
Bonne lecture!! et si vous souhaitez consulter le document de l AFEF dans son intégralité, c est ici
 Un résumé des recommandations éditées par l AFEF le 1 er juin 2015 Les recommandations de l AFEF vont plus loin que celles de l EASL. Le Pr Victor De Lédinghen, du CHU de Bordeaux, et secrétaire général
Un résumé des recommandations éditées par l AFEF le 1 er juin 2015 Les recommandations de l AFEF vont plus loin que celles de l EASL. Le Pr Victor De Lédinghen, du CHU de Bordeaux, et secrétaire général
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013
 NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
NOTICE : INFORMATIONS DU PATIENT. Keforal 500 mg comprimés pelliculés. Céfalexine monohydratée
 NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
Item 127 : Transplantation d'organes
 Item 127 : Transplantation d'organes Date de création du document 2008-2009 Table des matières * Introduction... 1 1 Allogreffe de moelle ou de cellules souches...1 2 Transplantation d'organes... 2 3 Diagnostic...3
Item 127 : Transplantation d'organes Date de création du document 2008-2009 Table des matières * Introduction... 1 1 Allogreffe de moelle ou de cellules souches...1 2 Transplantation d'organes... 2 3 Diagnostic...3
Carnet de suivi Lithium
 Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine
 KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES :
 FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
Protéger. son animal. la gamme FRONTLINE. grâce à la gamme. Contre les puces et les tiques. Efficace plusieurs semaines (1) Résistant à la pluie,
 la gamme Frontline Contre les puces et les tiques Efficace plusieurs semaines (1) Résistant à la pluie, aux bains et aux shampooings (2) Protéger son animal grâce à la gamme FRONTLINE La gamme FRONTLINE
la gamme Frontline Contre les puces et les tiques Efficace plusieurs semaines (1) Résistant à la pluie, aux bains et aux shampooings (2) Protéger son animal grâce à la gamme FRONTLINE La gamme FRONTLINE
PIL Décembre 2009. Autres composants: acide tartrique, macrogol 4000, macrogol 1000, macrogol 400, butylhydroxyanisol.
 Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Leucémies de l enfant et de l adolescent
 Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
chronique La maladie rénale Un risque pour bon nombre de vos patients Document destiné aux professionnels de santé
 Document destiné aux professionnels de santé Agence relevant du ministère de la santé La maladie rénale chronique Un risque pour bon nombre de vos patients Clés pour la dépister et ralentir sa progression
Document destiné aux professionnels de santé Agence relevant du ministère de la santé La maladie rénale chronique Un risque pour bon nombre de vos patients Clés pour la dépister et ralentir sa progression
GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral intramusculaire
 ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène
 NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
 ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 Ce médicament fait l objet d une surveillance supplémentaire qui permettra l identification rapide de nouvelles informations relatives à la sécurité. Les
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 Ce médicament fait l objet d une surveillance supplémentaire qui permettra l identification rapide de nouvelles informations relatives à la sécurité. Les
Infection à CMV et allogreffe de cellules souches hématopoïétiques : Expérience du Centre National de Greffe de Moelle Osseuse, Tunis.
 Infection à CMV et allogreffe de cellules souches hématopoïétiques : Expérience du Centre National de Greffe de Moelle Osseuse, Tunis. Tarek Ben Othman Congrès de la STPI, 24 avril 2009 Plan Introduction
Infection à CMV et allogreffe de cellules souches hématopoïétiques : Expérience du Centre National de Greffe de Moelle Osseuse, Tunis. Tarek Ben Othman Congrès de la STPI, 24 avril 2009 Plan Introduction
Indications de la césarienne programmée à terme
 Indications de la césarienne programmée à terme Janvier 2012 Quelles sont les indications de la césarienne programmée? Utérus cicatriciel Transmissions mère-enfant d infections maternelles Grossesse gémellaire
Indications de la césarienne programmée à terme Janvier 2012 Quelles sont les indications de la césarienne programmée? Utérus cicatriciel Transmissions mère-enfant d infections maternelles Grossesse gémellaire
L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE
 L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE NEUCHATEL, Suisse, 7 avril/prnewswire/ -- - LA LENALIDOMIDE est évaluée par l EMEA comme thérapie orale pour
L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE NEUCHATEL, Suisse, 7 avril/prnewswire/ -- - LA LENALIDOMIDE est évaluée par l EMEA comme thérapie orale pour
Principales causes de décès selon le groupe d âge. 0 24 25 44 45 64 65 84 85 et plus
 Module 2 Exercice 1: Cellules souches hématopoïétiques 1. Causes de décès en Suisse (2010) La figure suivante montre les causes de décès les plus fréquentes en Suisse en 2010, telles qu elles ont été relevées
Module 2 Exercice 1: Cellules souches hématopoïétiques 1. Causes de décès en Suisse (2010) La figure suivante montre les causes de décès les plus fréquentes en Suisse en 2010, telles qu elles ont été relevées
Bijsluiter FR versie Collier Propoxur Halsband B. NOTICE 1/5
 B. NOTICE 1/5 NOTICE COLLIER PROPOXUR HALSBAND pour chiens de petite taille et chats COLLIER PROPOXUR HALSBAND pour chiens de grande et moyenne taille 1. NOM ET ADRESSE DU TITULAIRE DE L AUTORISATION DE
B. NOTICE 1/5 NOTICE COLLIER PROPOXUR HALSBAND pour chiens de petite taille et chats COLLIER PROPOXUR HALSBAND pour chiens de grande et moyenne taille 1. NOM ET ADRESSE DU TITULAIRE DE L AUTORISATION DE
Observation. Merci à l équipe de pharmaciens FormUtip iatro pour ce cas
 Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
GUIDE PRATIQUE N 1 HERPES ASSOCIATION HERPES. Agissons contre l herpès
 GUIDE PRATIQUE N 1 HERPES ASSOCIATION HERPES Agissons contre l herpès L Herpès : une maladie très répandue En France, on estime qu environ 10 millions de personnes sont porteuses du virus de l herpès à
GUIDE PRATIQUE N 1 HERPES ASSOCIATION HERPES Agissons contre l herpès L Herpès : une maladie très répandue En France, on estime qu environ 10 millions de personnes sont porteuses du virus de l herpès à
Traitements de l hépatite B
 Traitements de l hépatite B S Matheron Service des maladies infectieuses et tropicales A Hôpital Bichat-Claude Bernard Virus de l hépatite B: histoire naturelle Contage Hépatite aigüe 70% asymptomatique
Traitements de l hépatite B S Matheron Service des maladies infectieuses et tropicales A Hôpital Bichat-Claude Bernard Virus de l hépatite B: histoire naturelle Contage Hépatite aigüe 70% asymptomatique
L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015
 L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015 Objectifs de la présentation Décrire l évolution clinique et la prise en charge d
L hépatite C pas compliqué! Véronique Lussier, M.D., F.R.C.P.C. Gastroentérologue Hôpital Honoré-Mercier 16 avril 2015 Objectifs de la présentation Décrire l évolution clinique et la prise en charge d
Pathologie VIH. Service maladies infectieuses Archet 1. Françoise ALEXIS, infirmière Monique BORGHI, infirmière 15 octobre 2013
 Pathologie VIH Service maladies infectieuses Archet 1 Françoise ALEXIS, infirmière Monique BORGHI, infirmière 15 octobre 2013 Les traitements antirétroviraux Sont classés en 5 familles selon leur mode
Pathologie VIH Service maladies infectieuses Archet 1 Françoise ALEXIS, infirmière Monique BORGHI, infirmière 15 octobre 2013 Les traitements antirétroviraux Sont classés en 5 familles selon leur mode
RELPAX. hydrobromure d élétriptan
 RELPAX hydrobromure d élétriptan * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques * Conclusion * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques *
RELPAX hydrobromure d élétriptan * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques * Conclusion * Pharmacocinétique * Toxicologie * Formulation galénique * Essais cliniques *
Notice publique PERDOLAN - PÉDIATRIE
 Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
NOTICE : INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés Bisacodyl
 NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
Carte de soins et d urgence
 Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
ACTUALITES THERAPEUTIQUES. Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012
 ACTUALITES THERAPEUTIQUES Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012 Traitement de fond Objectifs: Réduire le nombre de poussées Arrêter ou freiner la progression du handicap Les traitements disponibles
ACTUALITES THERAPEUTIQUES Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012 Traitement de fond Objectifs: Réduire le nombre de poussées Arrêter ou freiner la progression du handicap Les traitements disponibles
1 - Que faut-il retenir sur les anticoagulants oraux?
 La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR. Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant
 B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR. Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants. Acide acétylsalicylique
 NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
Traiter la goutte sans être débordé
 Fédération des médecins omnipraticiens du Québec Traiter la goutte sans être débordé Hélène Demers et Michel Lapierre Vous voulez traiter et prévenir la goutte? Lisez ce qui suit! Les différentes phases
Fédération des médecins omnipraticiens du Québec Traiter la goutte sans être débordé Hélène Demers et Michel Lapierre Vous voulez traiter et prévenir la goutte? Lisez ce qui suit! Les différentes phases
L eau dans le corps. Fig. 6 L eau dans le corps. Cerveau 85 % Dents 10 % Cœur 77 % Poumons 80 % Foie 73 % Reins 80 % Peau 71 % Muscles 73 %
 24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
24 L eau est le principal constituant du corps humain. La quantité moyenne d eau contenue dans un organisme adulte est de 65 %, ce qui correspond à environ 45 litres d eau pour une personne de 70 kilogrammes.
LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI
 LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI? LA MÉTHAMPHÉTAMINE est un produit stupéfiant illicite, synthétisé à partir de substances chimiques, également connu sous le nom de «crystal» ou «crystalmet», «ice»,
LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI? LA MÉTHAMPHÉTAMINE est un produit stupéfiant illicite, synthétisé à partir de substances chimiques, également connu sous le nom de «crystal» ou «crystalmet», «ice»,
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE
 GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
REHABILITATION DE LA FRICHE INDUSTRIELLE DE L ESTAQUE. Surveillance médico-professionnelle des entreprises intervenantes
 REHABILITATION DE LA FRICHE INDUSTRIELLE DE L ESTAQUE Surveillance médico-professionnelle des entreprises intervenantes Dr BAJON-THERY Dr COURJARET Dr SURET Dr DEWITTE Dr MICHOT Surveillance médico-professionnelle
REHABILITATION DE LA FRICHE INDUSTRIELLE DE L ESTAQUE Surveillance médico-professionnelle des entreprises intervenantes Dr BAJON-THERY Dr COURJARET Dr SURET Dr DEWITTE Dr MICHOT Surveillance médico-professionnelle
Atrovent HFA 20 mcg/bouffée solution pour inhalation en flacon pressurisé (bromure d'ipratropium)
 NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
En considérant que l effet anticoagulant du dabigatran débute dans les 2 heures suivant la prise du médicament :
 Informations sur le dabigatran (Pradaxa md ) Préambule : Ce document présente plusieurs informations utiles pour les prescripteurs afin de les aider lors de l utilisation du dabigatran (Pradaxa md ). L
Informations sur le dabigatran (Pradaxa md ) Préambule : Ce document présente plusieurs informations utiles pour les prescripteurs afin de les aider lors de l utilisation du dabigatran (Pradaxa md ). L
NOTICE: INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés. Bisacodyl
 NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
Don de moelle osseuse. pour. la vie. Agence relevant du ministère de la santé. Agence relevant du ministère de la santé
 Don de moelle osseuse Engagez-VOUS pour la vie 1 Pourquoi devenir veilleur de vie? Le don de moelle osseuse peut sauver des vies La greffe de moelle osseuse représente une chance importante de guérison
Don de moelle osseuse Engagez-VOUS pour la vie 1 Pourquoi devenir veilleur de vie? Le don de moelle osseuse peut sauver des vies La greffe de moelle osseuse représente une chance importante de guérison
Parasites externes du chat et du chien
 Parasites externes du chat et du chien Identification, prévention et traitement Les tiques Les tiques transmettent des maladies parfois mortelles. La prévention est la meilleure arme. 1 - Où les trouve-t-on?
Parasites externes du chat et du chien Identification, prévention et traitement Les tiques Les tiques transmettent des maladies parfois mortelles. La prévention est la meilleure arme. 1 - Où les trouve-t-on?
COMMISSION DE LA TRANSPARENCE. Avis. 23 mai 2007
 COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
NOTICE : INFORMATIONS DE L'UTILISATEUR. PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole
 NOTICE : INFORMATIONS DE L'UTILISATEUR PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole Veuillez lire attentivement l'intégralité de cette notice car elle contient des informations importantes
NOTICE : INFORMATIONS DE L'UTILISATEUR PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole Veuillez lire attentivement l'intégralité de cette notice car elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR. Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl)
 NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
HUMI-BLOCK - TOUPRET
 FICHE DE DONNEES DE SECURITE Révision antérieure : (Selon l annexe II du Règlement REACH de l UE 1907/2006) Mise à jour : 19 janvier 2010 Version : 1 HUMI-BLOCK - TOUPRET 1-IDENTIFICATION DU PRODUIT ET
FICHE DE DONNEES DE SECURITE Révision antérieure : (Selon l annexe II du Règlement REACH de l UE 1907/2006) Mise à jour : 19 janvier 2010 Version : 1 HUMI-BLOCK - TOUPRET 1-IDENTIFICATION DU PRODUIT ET
Mme BORGHI Monique Infirmière ETP Mme ALEXIS Françoise Hopital Archet I Infectiologie/Virologie Clinique
 Mme BORGHI Monique Infirmière ETP Mme ALEXIS Françoise Hopital Archet I Infectiologie/Virologie Clinique Une hépatite est une inflammation du foie causée soit par des substances toxiques (médicaments,
Mme BORGHI Monique Infirmière ETP Mme ALEXIS Françoise Hopital Archet I Infectiologie/Virologie Clinique Une hépatite est une inflammation du foie causée soit par des substances toxiques (médicaments,
Grossesse et rôle parental après une transplantation: Ce que vous devriez savoir
 Grossesse et rôle parental après une transplantation: Ce que vous devriez savoir Transplantation et grossesse La transplantation offre une seconde chance de vivre à bon nombre de personnes atteintes d
Grossesse et rôle parental après une transplantation: Ce que vous devriez savoir Transplantation et grossesse La transplantation offre une seconde chance de vivre à bon nombre de personnes atteintes d
www.dondemoelleosseuse.fr
 Agence relevant du ministère de la santé www.dondemoelleosseuse.fr 01 Pourquoi devenir Veilleur de Vie? Le don de moelle osseuse peut sauver des vies. Chaque année, des milliers de personnes - enfants
Agence relevant du ministère de la santé www.dondemoelleosseuse.fr 01 Pourquoi devenir Veilleur de Vie? Le don de moelle osseuse peut sauver des vies. Chaque année, des milliers de personnes - enfants
LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B
 LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B Actualisation février 2009 Ce document est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service communication
LISTE DES ACTES ET PRESTATIONS - AFFECTION DE LONGUE DURÉE HÉPATITE CHRONIQUE B Actualisation février 2009 Ce document est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service communication
Insuffisance rénale. Définition. o Insuffisance rénale aiguë
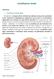 Insuffisance rénale Définition o Insuffisance rénale aiguë Se traduit par un brusque arrêt de la filtration des déchets du sang et de la production d urine. Associée à un déséquilibre de l organisme en
Insuffisance rénale Définition o Insuffisance rénale aiguë Se traduit par un brusque arrêt de la filtration des déchets du sang et de la production d urine. Associée à un déséquilibre de l organisme en
Le don de cellules souches. M.Lambermont Pascale Van Muylder
 Le don de cellules souches M.Lambermont Pascale Van Muylder 1 Pourquoi avons-nous recours à la greffe de CSH? Certaines maladies causent la destruction ou un fonctionnement anormal de la moelle osseuse.
Le don de cellules souches M.Lambermont Pascale Van Muylder 1 Pourquoi avons-nous recours à la greffe de CSH? Certaines maladies causent la destruction ou un fonctionnement anormal de la moelle osseuse.
Nouveaux anticoagulants oraux (NOAC)
 Nouveaux anticoagulants oraux (NOAC) Mécanisme d action Suivi biologique: comment et quand? A.Demulder IRIS-Lab 15/05/2013 1 Anticoagulants «traditionnels»: HNF Parentéral Suivi biologique avec ajustement
Nouveaux anticoagulants oraux (NOAC) Mécanisme d action Suivi biologique: comment et quand? A.Demulder IRIS-Lab 15/05/2013 1 Anticoagulants «traditionnels»: HNF Parentéral Suivi biologique avec ajustement
Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE. Hépatite chronique B
 Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE Hépatite chronique B Février 2015 Ce document est téléchargeable sur : www.has-sante.fr Haute Autorité de Santé Service des
Guide du parcours de soins Titre ACTES ET PRESTATIONS AFFECTION DE LONGUE DURÉE Hépatite chronique B Février 2015 Ce document est téléchargeable sur : www.has-sante.fr Haute Autorité de Santé Service des
Infection VIH et Grossesse Rédigée par : Laurichesse Hélène, C Jacomet
 Procédure qualité : «VIH et grossesse» Page 1 sur 6 CHU de Clermont-Ferrand Service de Gynécologie-obstétrique Pôle Gynécologie-Obstétrique biologie de la reproduction Procédure médicale Infection VIH
Procédure qualité : «VIH et grossesse» Page 1 sur 6 CHU de Clermont-Ferrand Service de Gynécologie-obstétrique Pôle Gynécologie-Obstétrique biologie de la reproduction Procédure médicale Infection VIH
Thérapeutique anti-vhc et travail maritime. O. Farret HIA Bégin
 Thérapeutique anti-vhc et travail maritime O. Farret HIA Bégin Introduction «L hépatite C est une maladie le plus souvent mineure, mais potentiellement cancérigène, qu on peut ne pas traiter et surveiller
Thérapeutique anti-vhc et travail maritime O. Farret HIA Bégin Introduction «L hépatite C est une maladie le plus souvent mineure, mais potentiellement cancérigène, qu on peut ne pas traiter et surveiller
NOTICE. ANSM - Mis à jour le : 25/03/2014. Dénomination du médicament. PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole
 NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
Itraconazole Sandoz 100 mg gélules Itraconazole
 Notice Itraconazole Sandoz 100 mg gélules Itraconazole Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire
Notice Itraconazole Sandoz 100 mg gélules Itraconazole Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire
Les triptans. quel casse-tête! Kim Messier et Michel Lapierre. Vous voulez prescrire des triptans? Lisez ce qui suit!
 Fédération des médecins omnipraticiens du Québec Les triptans quel casse-tête! Kim Messier et Michel Lapierre Vous voulez prescrire des triptans? Lisez ce qui suit! Les triptans, des agonistes sélectifs
Fédération des médecins omnipraticiens du Québec Les triptans quel casse-tête! Kim Messier et Michel Lapierre Vous voulez prescrire des triptans? Lisez ce qui suit! Les triptans, des agonistes sélectifs
NOTICE: INFORMATION DE L UTILISATEUR
 NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
Information à un nouveau donneur de cellules souches du sang
 Information à un nouveau donneur de cellules souches du sang Pour des raisons de simplification, les dénominations masculines s appliquent également aux femmes. La transplantation de cellules souches du
Information à un nouveau donneur de cellules souches du sang Pour des raisons de simplification, les dénominations masculines s appliquent également aux femmes. La transplantation de cellules souches du
Point d Information. Le PRAC a recommandé que le RCP soit modifié afin d inclure les informations suivantes:
 Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Point d information Avril 2012. Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir
 Point d information Avril 2012 Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir Le dabigatran (PRADAXA), inhibiteur direct de la thrombine,
Point d information Avril 2012 Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir Le dabigatran (PRADAXA), inhibiteur direct de la thrombine,
Stelara (ustekinumab)
 Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
Humira Solution pour injection dans un injecteur prérempli
 Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
Innovations thérapeutiques en transplantation
 Innovations thérapeutiques en transplantation 3èmes Assises de transplantation pulmonaire de la région Est Le 16 octobre 2010 Dr Armelle Schuller CHU Strasbourg Etat des lieux en transplantation : 2010
Innovations thérapeutiques en transplantation 3èmes Assises de transplantation pulmonaire de la région Est Le 16 octobre 2010 Dr Armelle Schuller CHU Strasbourg Etat des lieux en transplantation : 2010
DON DE SANG. Label Don de Soi
 DON DE SANG Label Don de Soi 2015 SOMMAIRE Les différents types de dons p.3 Le don de sang total Le don de plasma Le don de plaquettes Le don de moelle osseuse Que soigne-t-on avec un don de sang? p.7
DON DE SANG Label Don de Soi 2015 SOMMAIRE Les différents types de dons p.3 Le don de sang total Le don de plasma Le don de plaquettes Le don de moelle osseuse Que soigne-t-on avec un don de sang? p.7
LE SYNDROME DE BUDD CHIARI
 CENTRE DE REFERENCE DES MALADIES VASCULAIRES DU FOIE (C.R.M.V.F.) Hôpital Beaujon 100 bd du Général Leclerc 92110 Clichy Service d Hépatologie Pavillon Abrami (consultation) Pavillon Sergent (hospitalisation)
CENTRE DE REFERENCE DES MALADIES VASCULAIRES DU FOIE (C.R.M.V.F.) Hôpital Beaujon 100 bd du Général Leclerc 92110 Clichy Service d Hépatologie Pavillon Abrami (consultation) Pavillon Sergent (hospitalisation)
Anémie et maladie rénale chronique. Phases 1-4
 Anémie et maladie rénale chronique Phases 1-4 Initiative de qualité en matière d issue des maladies rénales de la National Kidney Foundation Saviez-vous que l initiative de qualité en matière d issue des
Anémie et maladie rénale chronique Phases 1-4 Initiative de qualité en matière d issue des maladies rénales de la National Kidney Foundation Saviez-vous que l initiative de qualité en matière d issue des
E03 - Héparines non fractionnées (HNF)
 E03-1 E03 - Héparines non fractionnées (HNF) Les héparines sont des anticoagulants agissant par voie parentérale. 1. Modalités d u tilisation Mode d action : l héparine est un cofacteur de l antithrombine
E03-1 E03 - Héparines non fractionnées (HNF) Les héparines sont des anticoagulants agissant par voie parentérale. 1. Modalités d u tilisation Mode d action : l héparine est un cofacteur de l antithrombine
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MÉDICAMENT Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Interféron
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MÉDICAMENT Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Interféron
IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie
 1 sur 6 13/09/2010 16:58 Mis à jour : 23/02/2009 1. DENOMINATION DU MEDICAMENT IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
1 sur 6 13/09/2010 16:58 Mis à jour : 23/02/2009 1. DENOMINATION DU MEDICAMENT IMIJECT 6 mg/0,5 ml, solution injectable pour voie sous-cutanée en seringue pré-remplie 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
XARELTO (RIVAROXABAN) 2,5 MG - 15 MG - 20 MG, COMPRIMÉS PELLICULÉS GUIDE DE PRESCRIPTION
 Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament Xarelto 2,5 mg; 15 mg et 20 mg de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique
Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament Xarelto 2,5 mg; 15 mg et 20 mg de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique
QUESTIONS FREQUEMMENT POSEES AUX EXPERTS DU SERVICE TELEPHONE VERT SIDA (800861061) ISTITUTO SUPERIORE DI SANITA
 QUESTIONS FREQUEMMENT POSEES AUX EXPERTS DU SERVICE TELEPHONE VERT SIDA (800861061) ISTITUTO SUPERIORE DI SANITA INFORMATIONS SUR LE TEST DE DEPISTAGE Q. Quels examens médicaux doit-on faire pour détecter
QUESTIONS FREQUEMMENT POSEES AUX EXPERTS DU SERVICE TELEPHONE VERT SIDA (800861061) ISTITUTO SUPERIORE DI SANITA INFORMATIONS SUR LE TEST DE DEPISTAGE Q. Quels examens médicaux doit-on faire pour détecter
La vaccination, une bonne protection
 Vaccin contre l hépatite A et l hépatite B La personne qui reçoit ce vaccin se protège contre l hépatite A, l hépatite B et leurs complications. L hépatite A et l hépatite B sont des infections du foie
Vaccin contre l hépatite A et l hépatite B La personne qui reçoit ce vaccin se protège contre l hépatite A, l hépatite B et leurs complications. L hépatite A et l hépatite B sont des infections du foie
Hépatite B. Le virus Structure et caractéristiques 07/02/2013
 Hépatite B Le virus Structure et caractéristiques o o o Famille des Hepadnaviridae Genre orthohepadnavirus Enveloppé, capside icosaédrique, 42 nm 1 Le virus Structure et caractéristiques En microscopie
Hépatite B Le virus Structure et caractéristiques o o o Famille des Hepadnaviridae Genre orthohepadnavirus Enveloppé, capside icosaédrique, 42 nm 1 Le virus Structure et caractéristiques En microscopie
1- Parmi les affirmations suivantes, quelles sont les réponses vraies :
 1- Parmi les affirmations suivantes, quelles sont les réponses vraies : a. Les troubles fonctionnels digestifs sont définis par les critères de Paris b. En France, le syndrome de l intestin irritable touche
1- Parmi les affirmations suivantes, quelles sont les réponses vraies : a. Les troubles fonctionnels digestifs sont définis par les critères de Paris b. En France, le syndrome de l intestin irritable touche
COMMISSION DE LA TRANSPARENCE AVIS. 18 janvier 2006
 COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
Mieux informé sur la maladie de reflux
 Information destinée aux patients Mieux informé sur la maladie de reflux Les médicaments à l arc-en-ciel Mise à jour de l'information: septembre 2013 «Maladie de reflux» Maladie de reflux La maladie de
Information destinée aux patients Mieux informé sur la maladie de reflux Les médicaments à l arc-en-ciel Mise à jour de l'information: septembre 2013 «Maladie de reflux» Maladie de reflux La maladie de
