En vue de l'obtention du. Présentée et soutenue par Alice BOULANGER Le 15 mai 2009
|
|
|
- Marianne Labbé
- il y a 10 ans
- Total affichages :
Transcription
1 THÈSE En vue de l'obtention du DOCTORAT DE L UNIVERSITÉ DE TOULOUSE Délivré par l'université Toulouse III - Paul Sabatier Discipline ou spécialité : Microbiologie Présentée et soutenue par Alice BOULANGER Le 15 mai 2009 Titre : Analyse d'un nouveau système CUT impliqué dans l'acquisition et l'utilisation du N-acétylglucosamine par Xanthomonas campestris pathovar campestris. JURY Jackie PLUMBRIDGE, Directeur de Recherche, CNRS, Paris, Rapporteur Christelle BRETON, Professeur, CERMAV, Grenoble, Rapporteur Charles MANCEAU, Ingénieur de Recherche, INRA, Angers, Rapporteur Valérie VERDIER, Directeur de Recherche, IRD, Montpellier, Examinateur Bernard MARTIN, Professeur de l Université Paul Sabatier, Toulouse, Examinateur Emmanuelle LAUBER? Charg2e de Recherche, CNRS, Toulouse, Co-Directeur de thèse Ecole doctorale : Sciences Ecologiques, Vétérinaires, Agronomiques et Bioingénieries Unité de recherche : Laboratoire des Interactions Plantes-Microorganismes Directeur de Thèse : Matthieu ARLAT
2 Doctorat de l Université de Toulouse délivré par l Université Toulouse III - Paul Sabatier U.F.R. Sciences de la Vie et de la Terre THÈSE Pour obtenir le grade de DOCTEUR DE L UNIVERSITÉ TOULOUSE III Discipline : Microbiologie «Microorganismes, du génome aux interactions avec l hôte» Présentée et soutenue par Alice BOULANGER Le 15 MAI 2009 à 14h00 Analyse d un nouveau système CUT impliqué dans l acquisition et l utilisation du N-acétylglucosamine par Xanthomonas campestris pathovar campestris. JURY Jackie PLUMBRIDGE, Directeur de Recherche, CNRS, Paris, Rapporteur Christelle BRETON, Professeur, CERMAV, Grenoble, Rapporteur Charles MANCEAU, Ingénieur de Recherche, INRA, Angers, Rapporteur Valérie VERDIER, Directeur de Recherche, IRD, Montpellier, Examinateur Bernard MARTIN, Professeur de l Université Paul Sabatier, Toulouse, Examinateur Emmanuelle LAUBER, Chargée de Recherche, CNRS, Toulouse, Co-Directeur de thèse Recherches effectuées au Laboratoire des Interactions Plantes-Microorganismes, UMR CNRS / INRA 2594 / , Chemin de Borde Rouge BP Castanet Tolosan cedex, France
3 REMERCIEMENTS Je souhaite remercier chacun des membres du jury d avoir accepté d examiner ce travail et d être venu assister à la soutenance de cette thèse. Merci à : Matthieu pour m avoir acceptée au sein de son équipe. Tu m as appris les bases de la phytopathologie et la patience (enfin pour la patience tu as essayé!!). Tu m as toujours laissé la possibilité de m exprimer. Merci également pour les blagues carambar et les sessions bizutages. Manue, la femme qui décroche plus vite que son ombre. Tu m as soutenue toutes ces années, merci pour toute l aide que tu m as apportée et tout ce que tu m as enseigné. J ai tenu le coup grâce à toi. Je te remercie également pour les bons moments passés ensemble, ta patience, les places de cinéma et le super fromage de chèvre. Martine et Claudine pour vous être occupées de moi comme de vraies mères. Martine, merci pour tous les coups de mains que tu n hésites pas à donner à tous moments et pour ta gentillesse. J ai beaucoup apprécié les discussions sur les péripéties du monde des microbiologistes toulousains. Claudine, merci pour tout le travail que tu effectues chaque jour et qui nous facilite grandement la vie que ce soit au sein du laboratoire ou de l équipe. Les décorations, le chocolat, le muguet et toutes les petites attentions dont tu nous gâtes tous rendent nos journées plus belles. Guitoune et Matcha avec qui j ai eu de nombreux fous rires. Vive le tableau des boulettes (bien que vous soyez des tricheurs), les batailles de glace (là aussi deux contre une c est de la triche!) et les discussions croustillantes (no comment). Guitoune, je conserve la boulette d or, et peut être qu un jour je te la remettrai. Il va falloir que tu t entraînes dur pour arriver à mon niveau et la mériter. Servane, ma morue. Nous avons passé de très bons moments en ta compagnie. Heureusement que tu étais là pour rendre les 1 er mai moins mortels. Les
4 «vendredi c est permis» m ont fait beaucoup de bien et tu m as ouvert la voie dans bien des domaines. Damien pour m avoir initié aux cultures de plantes et pour ses imitations inoubliables. Vincent avec qui je me suis beaucoup amusé pendant les manips. Laurent pour ton aide apportée lors de la préparation de ma soutenance. Pauline et Endrick qui sont la nouvelle génération de fous ayant envie de passer un doctorat. Je vous souhaite beaucoup de réussite et un avenir radieux. A tous les étudiants qui ont passé un moment avec nous et qui ont participé à la bonne humeur de l équipe. Alice, avec qui je partage de nombreux points communs. Je suis heureuse d avoir trouvé une nouvelle amie avec qui partager les joies et les difficultés de la vie. Tu m as aidé à passer les moments difficiles de fin de thèse et je t en remercie. Solène, Sandra, Lisa, Marie et Céline pour les soirées filles et votre amitié. J espère qu on aura l occasion de remettre ça rapidement. On va avoir encore pleins d heureux événements à fêter. A toutes les personnes qui animent la vie du labo, qui donnent de leur temps et de leur énergie pour faciliter le travail de chacun. Sans les amis et la famille, la vie serait trop dure. Je remercie ma maman qui me soutien et m encourage depuis toujours et à qui je dois tant. Sans toi tout ceci n aurait pas été possible. Merci à tous mes amis, à Anne, Candice, Nanou et Zarha. Vous avez toujours été là pour me soutenir et me remonter le moral et faire la fête quand j en avais besoin. Enfin, je remercie Jean-philippe qui partage ma vie. Merci pour tout le bonheur que tu m apportes chaque jour. Ce n est pas tous les jours facile de supporter les états d âme d une thèsarde en détresse mais tu as toujours su me redonner le sourire.
5 Le conte de la boulette Il était une fois, dans un laboratoire lointain, très lointain, une jolie thésarde prénommée Alice. Alice était en train de finir sa thèse, et avait donc eu beaucoup de bons résultats, seulement, on aurait dit que le destin l'avait frappé lors de sa naissance et la fit déesse de la boulette. Elle ne pouvait s'empêcher de commettre des boulettes, c'était inné, de temps à autres, ce qu'elle touchait se transformait en petites ou grosses conneries, si vous me passez l'expression mes vaillants lecteurs. Je vais donc vous conter l'histoire de la boulette du plasmide pvo. C'était un jour triste du mois de novembre de l'année 2008, et le valeureux guillaume était en train de faire des mutants pvo. Les fragments avaient déjà été amplifiés et séquencés. Il en était donc arrivé à la terrible étape de la ligation dans le plasmide pvo. Mais guillaume le bon s'était déjà affranchi de biens de ligation par le passé, et n'appréhendait aucunement cette étape. Seulement, il n'avait plus en sa possession de pvo. Il parti donc en quête de ce plasmide. Il réussi à en trouver auprès de la belle Alice, qui, remplie de générosité (j'en rajoute, c'est pour le conte), s'empressa de lui offrir un aliquot. Il lui demanda si le plasmide était vide et alice confirma avec célérité qu'il ne contenait effectivement pas de fragments en son sein. (C'est très important pour la suite de l'histoire). Guillaume le vaillant, accompagné de Martine la grande firent donc leurs ligations, sûr de ce plasmide, et passèrrent à l'étape de la digestion afin de vérifier si leurs fringants fragments étaient en place au sein de leur bien aimé plasmide (car j'avais fait une PCR de vérif avec oligos sur pvo et j'amplifiais un fragment de 300 environ donc c'était bon pour moi). Je vous laisse donc imaginer la stupeur de guillaume lorsqu'il vit que ses enzymes ne coupaient pas. Martine tenta donc de couper avec une enzyme, puis l'autre, avec une purif entre les deux,... Rien! Guillaume fît alors une PCR avec les oligos de construction, et, à sa grande surprise, ce fût du grand n'importe quoi! Il décida donc de retraverser toutes ses terribles étapes afin d'obtenir le grâle, un mutant pvo. Mais les semaines passèrent (2 quand même) et les ligations ne marchaient toujours pas. Guillaume le bienheureux ne comprenait pas jusqu'au jour où Martine, imaginant une quelconque baleine sous un gravillon, fit séquencer les pvo et vit que les séquences correspondaient au gène Guillaume le magnifique demanda alors à Alice si, par le plus grand des hasards, il y aurait pu y avoir quelque chose dans le plasmide. Et effectivement, Alice avait passé à Guillaume une miniprep de pvo avec un fragment dedans, tout en lui disant qu'il était vide. La malédiction avait encore frappée!! La déesse de la boulette avait accouchée de sa plus belle réalisation en trois ans de thèse. Guillaume digéra donc un autre pvo (sans rien dedans), fît les ligation, les transformation et eût beaucoup de bons et beaux transformants. Guy.
6 Liste des abréviations ABREVIATIONS ABC ADN ADNc AHL AMPc anhmurnac ARN Asn ATP Avr CASA CAZy CBP CC CDS CFU CHS CLP COS CRP CUT Da Dap DATDH DF DMSO dntp DO DSF DTT ECF EDTA EI EII EPS ET ETI Fru FUR GAG Gal GalNAc GlcNAc GMP GPI GRP ATP Binding Cassette Acide Deoxy-ribo-Nucléique ADN complémentaire N-acyl homoserine lactone Adénosine Monophosphate cyclique acide N-acétylmuramique anhydre Acide Ribo-Nucléique Asparagine Adenosine Triphosphate Avirulence Casamino Acid Carbohydrate Active Enzymes Chitin-Binding Protein Coiled-coil Coding DNA Sequence Colony Forming Unit Chitine Synthase camp receptor Like Protein ChitoOligoSaccharides camp Receptor Protein Carbohydrate Utilization containing TBDR Dalton acide Diaminopimélique 2,4-diacetamido-2,4,6-trideoxyhexose Diffusible Factor Diméthylsulfoxyde désoxyribonucléotides Tri-phosphate Densité Optique Diffusible Signal Factor Dithiothreitol Extracellular Cytoplasmic Function Acide éthylène-diamine-tétraacétique Enzyme I Enzyme II Exopolysaccharides Ethylène Effector-Triggered Immunity Fructose Ferric Uptake Regulator Glycosaminoglycane Galactose N-acétylgalactosamine N-acétylglucosamine Guanosine Monophosphate Glycophosphatidylinositol Glycine Rich Protein
7 Liste des abréviations HAMP Hop HPLC HPr HPRP HPt HR Hrc Hrp HSP IPTG ISR JA kb Kd kda KDG LAR Lpp LPS LRR LZ MAMP Man MIMP MCP MFS MS MurNAc NB / NBS NCBI NeuAc NLS NMR NO NRP OGT OMP ORF OTase PAGE PAMP PNPG pb PBP PCD PCR PEP PG Pgl PIP Host-Associated Molecular Pattern Hrp outer protein Chromatographie en phase liquide à haute performance Histidine containing protein HydroxyProline Rich protein Histidine Phosphotransférase Hypersensitive Response Hrp conserved Hypersensitive response and pathogenicity Heat-Shock Protein Isopropyl β-d-1-thiogalactopyranoside Induced Systemic Resistance Jasmonic Acid kilobase Constante de dissociation Kilodalton 2-keto-3-deoxygluconate Localized Acquired Resistance Lipoprotéines Lipopolysaccharides Leucine rich repeat Leucine zipper Microbes-Associated Molecular Pattern Mannose Microbes-Induced Molecular Pattern Methyl accepting Chemotaxis Protein Major Facilitator Superfamily Mass Spectrometry acide N-acétylmuramique Nucleotide Binding Site National Center for Biotechnology Information Acide Neuraminique Nuclear Localization Signal Nuclear Magnetic Resonance Nitric Oxyde NonRibosomal Peptide O-GlcNAc Transférase Outer Membrane Protein Open Reading Frame OligosaccharylTransférase polyacrylamide Gel Electrophoresis Pathogen Associated Molecular Pattern Paranitrophényl-β-D-galactoside paires de bases Penicillin-Binding Protein Programmed Cell Death Polymerase Chain Reaction phosphoénolpyruvate Peptidoglycane Protein glycosylation Plant Inducible Promoter
8 Liste des abréviations PME Pop PR PRP PRR PTI PTS pv. QS R RE RLK RLP rpm ROK ROS Rpf RT SA SAR SDS-PAGE Ser SNP sp. TBDT TCA TCT Thr TIR Trh T3SE T3SS UDP UV Xcc Xgal Xgluc Xop Xyl Pectine Méthyl Estérase Pseudomonas outer protein Pathogenesis-Related Proline Rich Protein Pattern Recognition Receptor PAMP-triggered immunity Phosphotransferase System pathovar Quorum Sensing Résistance Réticulum Endoplasmique Receptor-Like Kinase Receptor-Like Protein rotation per minute Repressor Open reading frame Kinase Reactive Oxygen Species Regulation of pathogenicity factors Reverse Transcription Salicylic Acid Systemic Acquired Resistance SulfateDodécylique Sodium- PolyAcrylamide Gel Electrophoresis Sérine Single Nucleotide Polymorphism Species TonB-Dependent Transporter TriCarboxylic Acid Trachéal CytoToxine Thréonine Toll / Interleukine1 Receptor domain Transcriptional regulator for hrp Type Three Secretion Effector Type Three Secretion System Uridine Diphosphate Ultra Violet Xanthomonas campestris pv. campestris 5-bromo-4-chloro-3-indolyl-beta-D-galactopyranoside 5-bromo-4-chloro-3-indolyl-beta-D-glucuronic acid Xanthomonas outer protein Xylose
9 Liste des figures Introduction générale Chapitre 1 LISTE DES FIGURES Figure 1 : Quelques exemples de Brassicacées cultivées et la plante modèle 8 Arabidopsis thaliana Figure 2 : Représentation schématique du cycle de vie de Xanthomonas campestris 9 pv. campestris (Xcc) lors d une interaction avec la plante hôte. Figure 3 : Symptômes de la nervure noire sur les feuilles de choux. 9 Chapitre 2 Figure 4 : Signalisation de la réponse basale et cibles de certains effecteurs de type III 11 connus Figure 5 : Représentation de la théorie Gène pour Gène de Flor (1971). 12 Figure 6 : Différentes classes de Protéines de Résistance. 13 Figure 7 : Le modèle en zig zag illustrant la production quantitative de l équipement 15 nécessaire à la défense immunitaire de la plante. Chapitre 3 Figure 8 : Représentation schématique de trois types de mobilité bactérienne. 17 Figure 9 : Modèle du système d acquisition du fer des bactéries Gram et de sa 19 régulation. Figure 10 : La paroi végétale. 20 Figure 11 : Représentation schématique de différents polymères de sucres composant 21 la paroi primaire végétale. Figure 12 : Modèle de fonctionnement d un locus CUT basé sur le locus sux de 24 Xanthomonas campestris pv. campestris. Figure 13 : La translocation de groupe par le système PTS, mode de transport actif de 24 carbohydrates à travers la membrane interne des bactéries à Gram négatif. Figure 14 : Représentation schématique du système Hrp. 25 Figure 15 : Modéles de régulation des gènes du système Hrp chez la bactérie 28 Ralstonia solanacearum et Xanthomonas. Figure 16 : Le xanthane, un exopolysaccharide produit par Xanthomonas campestris 29 pv. campestris. Figure 17 : Voie de synthèse de Xanthane chez Xanthomonas campestris pv. 29 campestris (Xcc). Figure 18 : Structures des molécules signales des deux systèmes de quorum sensing 30 de Xanthomonas campestris pv. campestris. Figure 19 : Modèle de la transduction du signal DSF chez Xanthomonas campestris 30 pv. campestris. Figure 20 : Représentation schématique du quorum sensing chez Xcc. 31 Figure 21 : Illustration des interactions entre Xanthomonas campestris pv. campestris 33 et une plante-hôte.
10 Etude de l acquisition et de l utilisation du GlcNAc Chapitre 2 Liste des figures Figure 22 : Le peptidoglycane 35 Figure 23 : Voie de biosynthèse du peptydoglycane (PG). 36 Figure 24 : Représentation schématique de l activité d enzymes clivant le 37 peptidoglycane. Figure 25 : Recyclage du peptidoglycane chez Escherichia coli. 38 Figure 26 : Représentation schématique des parois bactériennes. 39 Figure 27 : Structure du lipopolysaccharide (LPS) de E. coli O111:B4. 39 Figure 28 : Structure de la chitine. 40 Figure 29 : Structure schématique de glycosaminoglycanes (GAGs) et de 41 protéoglycanes. Figure 30 : Structure de l ancre GPI de l érythrocyte acétylcholinestérase humaine. 41 Figure 31 : Exemple d interactions impliquant des carbohydrates de surface. 42 Figure 32 : Relation dynamique entre phosphorylation et modification par le O- 44 GlcNAc d une protéine. Figure 33 : Structure du N-glycane précurseur greffé sur la protéine eucaryote en 45 cours de synthèse. Figure 34 : Représentation simplifiée des premières étapes de N-glycosylation dans le 45 réticulum endoplasmique (RE). Figure 35 : Structure des principaux N-glycanes rencontrés chez les mammifères. 45 Figure 36 : Structure des principaux N-glycanes rencontrés chez les plantes. 46 Figure 37 : Localisation majoritaire des différents types de N-glycanes dans la cellule 46 végétale. Figure 38 : Synthèse des différents types de N-glycanes dans le réticulum 46 endoplasmique (RE) et l appareil de Golgi des cellules végétales. Figure 39 : Exemples de sucres rares constituant les glycanes des glycoprotéines des 52 Archées et des bactéries. Figure 40 : Modèle de N- et O-glycosylation chez les archées et les bactéries. 53 Figure 41 : La N-glycosylation chez Campylobacter jejuni. 54 Chapitre 3 Figure 42 : Modèle de la voie de dégradation de la chitine chez Saccharophagus 56 degradans (anciennement nommé Microbulbifer degradans). Figure 43 : Représentation schématique du catabolisme du GlcNAc chez les bactéries. 59 Figure 44 : Séquences consensus reconnues par les régulateurs transcriptionnels 63 NagC, NagR et NagQ. Résultats Figure R1. Xanthomonas campestris pv. campestris (Xcc) utilizes N- acetylglucosamine and chitobiose as a carbon source. Figure R2. The Xanthomonas campestris pv. campestris N-acetylglucosamine CUT system and proposal model for N-glycans degradation
11 Liste des figures Figure R3. Glycoside hydrolases encoded by the Xanthomonas campestris pv. campestris glycan cluster are functional and controlled by NagR. Figure R4. Xanthomonas campestris pv. campestris Nag proteins are involved in the utilization of N-acetylglucosamine. Figure R5. Xanthomonas campestris pv. campestris NagK-II enzymes are involved in the phosphorylation of N-acetylglucosamine. Figure R6. Xanthomonas campestris pv. campestris naga mutants are sensitive to N- acetylglucosamine, in vitro. Figure R7. N-acetylglucosamine and N-acetylglucosamine-6P are the signalling molecules of NagR and NagQ respectively. Figure R8. Xanthomonas campestris pv. campestris naga and nagb-ii mutants are affected in pathogenicity. Figure R9. Xanthomonas campestris pv. campestris Nix glycoside hydrolases and the TonB-dependent transporter NixD play a central role in sensitivity to N- acetylglucosamine in planta. Figure R10. Schematic representation of the N-acetylglucosamine utilization pathway in Gram negative bacteria. Figure S1. Growth of Xanthomonas campestris pv. campestris wild-type strain in the presence of various carbon sources at 10 mm. Figure S2. Conservation of genes belonging to the N-acetylglucosamine (GlcNAc) utilization pathway among completely sequenced Xanthomonadaceae. Figure S3. Conservation of genes belonging to GlcNAc and glycan clusters in Xanthomonas campestris pv. campestris ATCC33913 and Novosphingobium aromaticivorans (Saro_DSM 12444). Figure S4. Location of mutations introduced in genes belonging to the Xanthomonas campestris pv. campestris N-acetylglucosamine utilization pathway and regions cloned in expression plasmids Discussion Figure D1. Représentation schématique du réseau de régulation du système GlcNAc de Xanthomonas campestris pv. campestris. Figure D2. Utilisation du phénotype du mutant ΔnagA pour suivre l expression d un gène in planta Matériel et Méthodes Figure M1. Principe de la construction des mutants par insertion du plasmide 116 pvo155. Figure M2. Délétion d un gène par la stratégie Cre/Lox. 117 Figure M3. Délétion d un gène par la stratégie SacB. 117 Figure M4. Carte génétique du plasmide pcz Figure M5. Index de la maladie développée par Xcc, après infection par «piercing» 119 de l écotype Sf-2 d A. thaliana ou de feuilles de choux Bartolo d après Meyer et al. (2005). Figure M6. Représentation schématique de la méthode de suivi de la croissance 120 bactérienne in planta.
12 Liste des tableaux LISTE DES TABLEAUX Interactions Plantes-Microorganismes Tableau 1. Liste des bactéries phytopathogènes dont le génome est entièrement séquencé et disponible, ainsi que les maladies provoquées par ces organismes. 4 Introduction générale Chapitre 1 Tableau 2. Caractéristiques générales et comparaison des 3 génomes de Xanthomonas campestris pv. campestris (Xcc) séquencés. 7 Chapitre 2 Tableau 3. Propriétés des différentes familles de protéines PR. 13 Chapitre 3 Tableau 4. Enzymes de dégradation de la paroi végétale de Xanthomonas campestris pv. campestris, source da Silva et al., (2002). Tableau 5. Effecteurs de type III connus chez la souche de Xanthomonas axonopodis pv. vesicatoria Etude de l acquisition et de l utilisation du GlcNAc chez Xcc Chapitre 2 Tableau 6. Enzymes impliquées dans le recyclage du peptidoglycane d Escherichia coli. Tableau 7. Diversité des O-glycanes de type mucine rencontrés chez l homme et leur localisation tissulaire Chapitre 3 Tableau 8. Occurrence et caractéristiques des gènes impliqués dans l utilisation de la chitine et du GlcNAc. 61 Résultats Table R1. Relative expression ratios of genes belonging to the N-acetylglucosamine utilization pathway. Table R2. [ 14 C]N-acetylglucosamine transport rates related to Xanthomonas campestris pv. campestris wild-type strain (Xcc568)
13 Liste des tableaux Table S1. Putative function of enzymes encoded by the Xanthomonas campestris pv. campestris glycan cluster. Table S2. Inhibition of [ 14 C] N-acetylglucosamine uptake by various carbohydrates in Xanthomonas campestris pv. campestris wild-type strain. Table S3. List of plasmids and Xanthomonas campestris pv. campestris strains used or generated in this study Matériel et Méthodes Tableau M1. Liste des réactifs et concentrations 115
14 Sommaire SOMMAIRE LES INTERACTIONS PLANTES-MICROORGANISMES... 4 INTRODUCTION GENERALE... 6 CHAPITRE 1. NOTRE MODÈLE D ÉTUDE, LA BACTÉRIE PHYTOPATHOGÈNE XANTHOMONAS CAMPESTRIS PV. CAMPESTRIS LE GENRE XANTHOMONAS LE GENOME DE XCC LES PLANTES HOTES DE XCC : LES BRASSICACEES LE CYCLE DE VIE DE XCC... 8 CHAPITRE 2. LES SYSTÈMES DE DÉFENSE DES PLANTES LA RECONNAISSANCE DU «NON SOI» ET L INDUCTION DE L IMMUNITE INNEE Les éliciteurs généraux et la réponse basale Les éliciteurs race spécifique Avr reconnus par les protéines de résistance R et la réponse hypersensible LA REPONSE SYSTEMIQUE ACQUISE LA COEVOLUTION PLANTES/PATHOGENES, UN VERITABLE PING PONG CHAPITRE 3. LES DÉTERMINANTS DU POUVOIR PATHOGÈNE BACTÉRIEN L ADHESION LA MOBILITE ET LE CHIMIOTACTISME LES SYSTEMES D ACQUISITION DU FER LA DEGRADATION DE LA PAROI VEGETALE ET L ACQUISITION DES SUCRES Composition de la paroi primaire La biodégradation de la paroi végétale par les bactéries A. Dégradation de la pectine B. Dégradation de la cellulose C. Dégradation de l hémicellulose D. Dégradation des protéines E. Le transport F. La régulation LE SYSTEME HRP ET SES EFFECTEURS La structure du T3SS Les effecteurs de type III (T3SE) Organisation et régulation des gènes du système Hrp LA PRODUCTION D EPS LE QUORUM SENSING LES PHYTOTOXINES ETUDE DE L ACQUISITION ET DE L UTILISATION DU N-ACETYLGLUCOSAMINE CHAPITRE 1. INTRODUCTION AU TRAVAIL DE THÈSE CHAPITRE 2. LE N-ACÉTYLGLUCOSAMINE DANS LE MONDE DU VIVANT
15 Sommaire 2.1 LE GlCNAC, UN ELEMENT DE STRUCTURE La paroi bactérienne A. Le peptidoglycane B. Le recyclage du peptidoglycane C. La paroi des bactéries à Gram D. La paroi des bactéries à Gram La chitine LE GlCNAC ET LES PROTEINES EUCARYOTES : LA GLYCOSYLATION Les protéines O-glycosylées A. Les O-glycanes de type mucine B. Les O-GlcNAc Les protéines N-glycosylées Rôles des O- et des N-glycanes LA GLYCOSYLATION CHEZ LES BACTERIES La O-glycosylation La N-glycosylation CHAPITRE 3. LE GlcNAc COMME SOURCE D ÉNERGIE LA DEGRADATION DE LA CHITINE LA DEGRADATION DES GLYCANES LE CATABOLISME DU GlCNAC Le transport du GlcNAc L étape de phosphorylation du GlcNAc La déacétylation du GlcNAc (par NagA) La déamination et l isomérisation La régulation CHAPITRE 4. LE GlcNAc ET LE POUVOIR PATHOGÈNE RESULTATS DISCUSSION GENERALE MATERIELS ET METHODES SOUCHES ET PLASMIDES MILIEUX ET RÉACTIFS BIOLOGIE MOLÉCULAIRE PREPARATION D ADN GENOMIQUE CONJUGAISON TRIPARENTALE CONSTRUCTION DE MUTANTS D INSERTION ET DE FUSIONS TRANSCRIPTIONNELLES CONSTRUCTION DES MUTANTS DE DELETION Par la méthode Cre/Lox Par la méthode «SacB» COMPLEMENTATION RT-PCR QUANTITATIVE (QRT-PCR) TEST DU POUVOIR PATHOGÈNE DES DIFFÉRENTS MUTANTS DE XCC INOCULATION PAR «PIERCING» SUR ARABIDOPSIS THALIANA SF2 ET CHOUX BARTOLO INOCULATION PAR INFILTRATION SUR POIVRON
16 Sommaire 4.3. CROISSANCE BACTERIENNE IN PLANTA SUR ARABIDOPSIS THALIANA SF2 (IGC ; INTERNAL GROWTH CURVE) TEST DE STABILITÉ DES INSERTIONS pvo IN PLANTA TESTS PHÉNOTYPIQUES TEST DU ROLE DU GlCNAC COMME SOURCE D AZOTE EFFET TOXIQUE DU GlCNAC ET DE LA PHASE STATIONNAIRE DE CROISSANCE SUR LA CROISSANCE DE MUTANTS DOSAGES D ACTIVITÉS ENZYMATIQUES DOSAGES DE L ACTIVITE β-glucuronidase AUTRES ACTIVITES ENZYMATIQUES TESTS DE TRANSPORT DE [ 14 C]GlcNAc TESTS DE PHOSPHORYLATION DU GlcNAc ANALYSES IN SILICO BIBLIOGRAPHIE
17 Tableau.1 Liste des bactéries phytopathogènes dont le génome est entièrement séquencé et disponible, ainsi que les maladies provoquées par ces organismes. D'après Groupe Espèce Maladie Gram - α-proteobactéries Gram - β-proteobactéries Gram - γ-proteobactéries Gram + Actinobactéries Taille du génome (MégaBases) Agrobacterium tumefaciens str. C58 galle du collet (crown gall) 5.67 Burkholderia cenocepacia AU 1054 pourriture aigre (sour skin) de l'oignon - pathogène sur patients atteints de fibrose kystique 7.25 Burkholderia cenocepacia HI2424 pourriture aigre (sour skin) de l'oignon - pathogène sur patients atteints de fibrose kystique 8.09 Burkholderia cenocepacia J2315 pourriture aigre (sour skin) de l'oignon - pathogène sur patients atteints de fibrose kystique 8.07 Burkholderia cenocepacia MC0-3 pourriture aigre (sour skin) de l'oignon - pathogène sur patients atteints de fibrose kystique 7,9 Ralstonia solanacearum GMI1000 flétrissement bactérien (bacterial wilt) 5.81 Erwinia carotovora subsp. atroseptica SCRI1043 pourriture molle (soft rot) et jambe noire (blackleg) de la pomme de terre 5.06 Pseudomonas aeruginosa PA7 pourriture molle (soft rot) 6,6 Pseudomonas aeruginosa PAO1 pourriture molle (soft rot) - pathogènes sur patients atteints de fibrose kystique 6.26 Pseudomonas aeruginosa UCBPP-PA14 pourriture molle (soft rot) - pathogènes sur patients atteints de fibrose kystique 6.53 Pseudomonas syringae pv. phaseolicola 1448A graisse à halo du haricot (halo blight of bean) 6.11 Pseudomonas syringae pv. syringae B728a graisse du haricot (brown spot) 6.09 Pseudomonas syringae pv. tomato str. DC3000 moucheture bactérienne (bacterial speck) de la tomate 6.54 Xanthomonas axonopodis pv. citri str. 306 chancre des agrumes (citrus canker) 5.27 Xanthomonas campestris pv. campestris str pourriture noire (black rot) des crucifères 5.15 Xanthomonas campestris pv. campestris str. ATCC pourriture noire (black rot) des crucifères 5.08 Xanthomonas campestris pv. campestris str. B100 pourriture noire (black rot) des crucifères 5.08 Xanthomonas axonopodis pv. vesicatoria str tache bactérienne (bacterial spot) de la tomate et du poivron 5.42 Xanthomonas oryzae pv. oryzae KACC10331 rouille des feuilles (bacterial blight) du riz 4.94 Xanthomonas oryzae pv. oryzae MAFF rouille des feuilles (bacterial blight) du riz 4.94 Xanthomonas oryzae pv. oryzae PXO99A rouille des feuilles (bacterial blight) du riz 5,24 Xylella fastidiosa 9a5c chlorose variégée des agrumes (citrus variegated chlorosis) 2.73 Xylella fastidiosa M12 chlorose variégée des agrumes (citrus variegated chlorosis) 2,48 Xylella fastidiosa M23 chlorose variégée des agrumes (citrus variegated chlorosis) 2,5 Xylella fastidiosa Temecula1 maladie de Pierce (Pierce's disease) du raisin 2.52 Clavibacter michiganensis subsp. sepedonicus pourriture annulaire (ring rot) de la pomme de terre 3.38 Leifsonia xyli subsp. xyli str. CTCB07 rabougrissement des repousses (ratoon stunting) de la canne à sucre 2.58 Streptomyces scabies gale commune (scab) de la pomme de terre 10.15
18 Les interactions plantes-micoorganismes 1 Les interactions Plantes-Microorganismes Au cours de sa vie, la plante va cohabiter et interagir avec de nombreux microorganismes tels que les virus, les mollicutes (mycoplasmes et spiroplasmes), les champignons, les bactéries et les nématodes. On peut définir trois types d interactions, les interactions de type symbiotique, de type saprophytique et les interactions de type pathogénique. Aujourd hui, le terme symbiose est souvent associé au mutualisme, défini par l association de deux organismes hétérospécifiques à bénéfice mutuel. Cependant, les interactions symbiotiques incluent le commensalisme (l association n est bénéfique que pour l un des deux partenaires, le second n est pas affectés par cette interaction), l amensalisme (un des acteurs inhibe le développement de l autre), et le parasitisme (l un des acteurs se développe au détriment de l autre). L organisme le plus grand est appelé hôte, alors que le plus petit est nommé symbiote ou symbionte. Les microorganismes saprophytes quant à eux, se nourrissent par absorption de matières organiques mortes, inertes ou en décomposition. Certaines bactéries ont développé une relation étroite avec la plante, leur permettant d échapper à la compétition avec d autres microorganismes. Ces bactéries vivent en saprophytes au niveau de la rhizosphère ou de la phyllosphère sans développer de relation mutualiste ou parasite avec la plante. Tout organisme parasite provoquant une maladie est dit pathogène. Le pouvoir pathogène d un organisme correspond à la capacité de cet organisme à développer une maladie sur son hôte, tandis que la virulence d un organisme correspond à une notion quantitative de l intensité du pouvoir pathogène. Un organisme pathogène peut avoir des souches plus ou moins virulentes. Pour induire une maladie, une bactérie pathogène doit être capable d adhérer, de coloniser et d envahir l hôte, de se multiplier et par conséquent d adapter son métabolisme à l environnement de l hôte, d échapper aux systèmes de défense de l hôte et de résister aux différents stress rencontrés et enfin de survivre entre deux cycles infectieux. Tous les éléments bactériens permettant la mise en place de ces différentes étapes sont définis comme facteurs de virulence. Il existe de nombreuses espèces de bactéries phytopathogènes (infectant les végétaux) regroupées majoritairement dans trois classes de protéobactéries, les α-, les β- et les γ-protéobactéries. Le génome de certaines de ces bactéries a été séquencé (Tableau 1). 4
19 Les interactions plantes-micoorganismes Dans certains cas, la distinction entre un organisme saprophyte, symbiotique ou pathogène n est pas toujours évidente. Certaines bactéries peuvent être saprophytes puis pathogènes au cours de différentes étapes de leur cycle de vie. La bactérie Burkholderia pseumallei, par exemple, est une bactérie saprophyte du sol également responsable de la mélioïdose, maladie humaine de l Asie du sud-est (Thaïlande, Myanmar, Singapour, Malaisie, Laos, Cambodge, Vietnam) (Kaestli et al., 2007). Dans l introduction générale, après une brève présentation de notre modèle d étude, je vous présenterai les systèmes de défenses mis en place par les plantes puis je vous parlerais des facteurs de virulence impliqués dans le développement de la maladie en prenant pour exemple notre modèle d étude. Dans une seconde partie, je développerai les différents aspects du rôle du N-acetylglucosamine (GlcNAc) dans le monde du vivant. Enfin, je discuterai les résultats obtenus au cours de ma thèse permettant la mise en évidence d un système particulier, dédié à l acquisition et à l utilisation du GlcNAc au cours de la vie in planta de Xcc. 5
20 INTRODUCTION GENERALE
21 Introduction générale 1 Chapitre 1. Notre modèle d étude, la bactérie phytopathogène Xanthomonas campestris pv. campestris L agriculture génère des conditions favorables au développement de maladies voire d épidémies par la culture d une même espèce de plante sur de grandes surfaces. Malgré les progrès effectués ces derniers siècles en pratiques phytosanitaires, le développement du commerce international, l accroissement des volumes de production et la politique de réduction de la diversité des espèces cultivées favorisent l émergence d épidémies. L élargissement de nos connaissances en phytopathologie est donc d une importance économique et écologique majeure afin d établir des plans de luttes durables et efficaces contre ces épidémies. Pour cela, des études approfondies des mécanismes de défense des plantes d une part et de mise en place de cycles infectieux d autre part, sont indispensables à une meilleure compréhension des interactions entre les plantes et leurs parasites. C est dans ce contexte que nous avons choisi d étudier les déterminants de l adaptation à son milieu et de la mise en place du pouvoir pathogène de la bactérie phytopathogène Xanthomonas campestris pv campestris (Xcc). La pourriture noire (black rot) ou autrement appelée nervure noire causée par Xcc est la maladie des Brassicacées (anciennement nommées Crucifères) la plus préjudiciable de par le monde (Williams, 1980). Toutes les Brassicacées maraîchères sont sensibles à cette maladie, sauf certains cultivars de radis et de chou frisé, qui sont moins facilement infectés Le genre Xanthomonas Les bactéries du genre Xanthomonas sont des bactéries à Gram négatif faisant partie de la classe des γ-protéobactéries. Ces bactéries sont aérobies strictes et ont pour particularité de produire des caroténoïdes appelés xanthomonadines qui pigmentent les colonies en jaune. D autre part Xcc est très étudiée pour sa capacité à produire un exopolysaccharide particulier, le xanthane qui donne un aspect mucoïde aux colonies (voir paragraphe 3.6), très utilisé comme agent épaississant dans les industries cosmétiques, agroalimentaires anisi que dans le bâtiment. 6
22 Tableau 2 : Caractéristiques générales et comparaison des 3 génomes de Xanthomonas campestris pv. campestris (Xcc ) séquencés. CDS, Coding DNA Sequences ; SNP, Single Length Polymorphism ; IS, Séquences d'insertion. (D'après Qian et al., 2005 ; Vorholter et al., 2008). Xcc 8004 Xcc ATCC33913 a Xcc B100 Caractéristiques générales Taille du génome (pb) Pourcentage en GC 64.94% 65.00% 65.00% Nombre total de séquences codantes (CDS) 4273 (87) b Nombre de CDS avec fonction assignée 2671 (1) b Nombre de CDS codant de putatives protéines conservées 1523 (27) b Nombre de CDS codant des protéines hypothétiques 79 (59) b Différences de séquences dans les CDS Nombre de gènes parfaitement identiques 3467 c 3408 Nombre de gènes identiques, de même taille, avec SNP c Nombre de gènes identiques avec insertions ou délétions c Nombre de gènes spécifiques de la souche Taille moyenne des CDS (pb) Nombre de séquences d'insertion (IS) a Données de da Silva et al. (2002) et GenBank (accession n AE008922). b Les nombres entre parenthèses indiquent le nombre de CDS possédant une protéine identique chez Xcc ATCC33913 mais non annotés par da Silva et al. (2002). c Traduit l'existence de duplications de CDSs.
23 Introduction générale Les membres du genre Xanthomonas infectent 124 espèces de plantes monocotylédones et 268 espèces de plantes dicotylédones (Leyns et al., 1984). Ce genre regroupait dans les années 90, plus de 170 espèces dont bon nombre sont des espèces phytopathogènes subdivisées en plus de 140 pathovars selon leurs plantes hôtes ( Des analyses d hybridation ADN-ADN (Vauterin et al., 1995) ont ensuite permis de reclasser ces bactéries, menant à la description de 20 espèces. L espèce Xanthomonas campestris comporte six pathovars : aberrans, armoraciae, barbareae, campestris, incanae et raphani, reclassés par la suite en trois pathovars, campestris, raphani, incanae par des analyses de pouvoir pathogène (Fargier and Manceau, 2007) Le génome de Xcc Le séquençage de trois souches de Xcc, la souche ATCC33913 séquencée au Brésil (da Silva et al., 2002), la souche 8004 séquencée en Chine (Qian et al., 2005) et la souche B100 séquencée en Allemagne à l université de Bielefeld (Vorholter et al., 2008), a facilité l étude des bases moléculaires de l interaction de la bactérie avec la plante. Les trois génomes sont dépourvus de plasmide, présentent un fort pourcentage en GC (65%) et sont riches en éléments transposables (Tableau 2). Le degré de conservation et la colinéarité entre les deux génomes des souches ATCC33913 et 8004 sont en général bien respectés, bien que plusieurs réarrangements aient été détectés entre les chromosomes de ces deux souches. Cependant, ces deux souches présentent de légères différences dans leur pouvoir pathogène sur différentes plantes. La souche ATCC33913 serait légèrement moins agressive sur certains cultivars de chou et de radis (Qian et al., 2005). La souche 8004 présente 92 séquences codantes putatives (CDS) supplémentaires par rapport à la souche ATCC33913, ainsi qu un nombre plus élevé de gènes «souche spécifiques» (108 contre 62). Des SNP (Single Nucleotide Polymorphism) sont observés dans 12% des CDS, et des réarrangements génomiques significatifs (translocations, inversions, insertions et délétions) différencient les deux souches (Qian et al., 2005). 7
24 A B C D E F Figure 1 : Quelques exemples de Brassicacées cultivées et la plante modèle Arabidopsis thaliana. A. Chou frisé ( B. Fleurs d Arabidopsis thaliana ( C. Chou rouge ( D. Choux-fleurs ( E. Choux raves ( F. Choux de Bruxelles (
25 1.3. Les plantes hôtes de Xcc : Les Brassicacées Introduction générale Xcc est capable d infecter de nombreuses Brassicacées telles que le chou-fleur, le brocoli, le rutabaga, le radis, le navet, le chou de Bruxelles, la moutarde, le canola, et de façon intéressante la plante modèle Arabidopsis thaliana dont le génome est séquencé (Bent et al., 1992; Lummerzheim et al., 1993; Meyer et al., 2005; Parker et al., 1993; Simpson and Johnson, 1990). Ceci facilite les études d interaction entre Xcc et son hôte. La famille des Brassicacées, anciennement Crucifères, consiste en une importante famille de plantes dicotylédones. Leurs fleurs sont composées de quatre pétales disposés en forme de croix. Elle comprend plus de 3000 espèces réparties en 350 genres. Ce sont principalement des plantes herbacées présentes dans le monde entier mais principalement localisées dans les régions tempérées de l hémisphère nord. Les Brassicacées colonisent presque tous les habitats : sables et rochers maritimes, bords de ruisseaux, pelouses, cultures, prairies de montagnes, etc. Parmi les plantes appartenant à cette famille, on trouve de nombreuses plantes cultivées pour la production d huile, la consommation humaine (choux, brocolis, navets ) et animale, ainsi que des plantes d ornement (Fig. 1). Une des caractéristiques intéressante des Brassicacées est la production de métabolites secondaires, les glycosinolates, qui ont un rôle dans la défense contre les insectes. Ces composés sont stockés dans la plante et libérés lors d une attaque de phytophages. Le glycosinolate est hydrolysé par la myrosinase en molécule toxique, l isothiocyanate. Ce dernier va être ingéré par les phytophages (Pfalz et al., 2007) Le cycle de vie de Xcc Xcc est une bactérie épiphyte vivant à la surface des feuilles. Lorsque les conditions environnementales sont favorables, correspondant à une température comprise entre 25 et 30 C et un taux d humidité élevé, elle va développer un cycle infectieux sur sa plante hôte. La première étape d infection de Xcc (Fig. 2) correspond à l entrée de la bactérie dans les tissus de la feuille. L entrée d une bactérie dans les tissus de la plante peut s effectuer grâce à des blessures, à l aide d insectes qui vont servir de vecteur ou encore par pénétration via des ouvertures naturelles. En effet, les bactéries de la phyllosphère ne peuvent avoir accès directement aux tissus internes des feuilles, ceux-ci étant protégés par la cuticule et l épiderme. Plusieurs structures naturelles vont pouvoir permettre l entrée de ces bactéries. Le 8
26 hydathode Vie épiphyte D A Infection Vaisseau du xylème B Colonisation Dissémination Transmission par les graines Vie saprophyte dans le sol C Développement des symptômes Mort de la plante Figure 2 : Représentation schématique du cycle de vie de Xanthomonas campestris pv. campestris (Xcc) lors d une interaction avec la plante hôte. Après une phase de vie épiphyte, Xcc va, dans certaines conditions, pénétrer à l intérieur des tissus végétaux par les hydathodes. La bactérie va ensuite pouvoir envahir les vaisseaux du xylème et induire les symptômes de la maladie. Enfin, la bactérie va survivre dans le sol et sur les débris végétaux après l infection. La dissémination des bactéries s effectue par le vent, la pluie, les insectes, mais aussi et surtout par le transport et l utilisation de graines contaminées. A. Vue en microscopie d un hydathode d Arabidopsis thaliana (Photo de Jacques Vasse, LIPM) B. Xcc exprimant le gène uida codant la glucuronidase, constitutivement (D après Hugouvieux et al., 1998). On voit ici les bactéries au niveau des hydathodes C. Xcc exprimant le gène de la luciférase (Lux) constitutivement (D après Meyer et al., 2005). Cette photo illustre la colonisation des vaisseaux du xylème par les bactéries. D. Gouttes de guttation présentes à la marge d une feuille d Arabidopsis thaliana. (D après Blanvillain 2007). Figure 3 : Symptômes de la nervure noire sur les feuilles de choux. Zones chlorotiques en forme de «V» produites par l infection du chou par la bactérie Xanthomonas campestris pv. campestris (Xcc)
27 Introduction générale site d entrée naturel de Xcc est un stomate aquifère localisé à la marge des feuilles, l hydatode (Hugouvieux et al., 1998). Les hydathodes sont localisés à l aboutissement des vaisseaux du xylème et sont impliqués dans les phénomènes de transpiration de la plante ou phénomène de guttation, lorsque la pression racinaire due à l humidité élevée est trop forte. Les bactéries vivant à la surface des feuilles vont se retrouver dans les gouttes de guttation est être absorbées en même temps que ces gouttes lorsque l humidité et donc la pression racinaire va diminuer. Xcc peut dans certains cas, entrer dans les tissus via des blessures ou par les stomates. Une fois localisée dans les vaisseaux du xylème, Xcc va pouvoir commencer la colonisation de la plante et provoquer l'apparition de lésions jaunes en forme de «V» devenant brunes et nécrosées au fil de leur progression vers la base des feuilles (Fig. 2 et 3). La production de xanthane et la croissance bactérienne vont boucher les vaisseaux entraînant le flétrissement et la nécrose des feuilles qui vont se dessécher complètement pour finir par tomber (Onsando, 1992; Williams, 1980). Xcc est capable de survivre pendant plusieurs années en saprophyte sur des débris végétaux et dans le sol, et se transmet à la graine lors de la production des semences. Les jeunes plants cultivés à partir de ces graines contaminées sont souvent infectés de façon systémique (Shaad et al., 1980; Shultz and Gabrielson, 1986). Les semences infectées et l eau de pluie sont la source majeure de dissémination de la bactérie. Pour éviter une épidémie, il faut sélectionner des semences saines, alterner les cultures avec des plantes qui ne sont pas des Brassicacées ou des écotypes résistants, travailler dans les champs seulement quand le feuillage est sec, éviter l arrosage par aspersion et irriguer au niveau des pieds et utiliser des pesticides pour éviter la dissémination via les insectes ( 9
28 Introduction générale 2 Chapitre 2. Les systèmes de défense des plantes En général, l infection d une plante par un pathogène reste une exception. Aux cours de leur coévolution, les plantes ont développé des stratégies élaborées leur permettant de se défendre efficacement contre les agents pathogènes. Il existe trois niveaux de défense de la plante. Tout d abord on trouve les barrières physiques : le microorganisme ne peut tout simplement pas entrer dans la plante. Cette fonction est assurée entre autres par les cires cuticulaires ou la paroi végétale. Si ces défenses ne suffisent pas, la plante peut détecter la présence de l agent pathogène afin d initier la mise en place de systèmes de défense locales et/ou systémiques. 2.1 La reconnaissance du «non soi» et l induction de l immunité innée La reconnaissance du microorganisme pathogène par la plante et l'induction des mécanismes de défense sont initiées par la perception de molécules appelées éliciteurs ou effecteurs. Les éliciteurs sont des signaux microbiens classiquement regroupés en deux catégories, les éliciteurs généraux qui provoquent des réactions sur tous les cultivars d une espèce végétale donnée et les éliciteurs race-spécifiques qui n ont d effet que sur des cultivars particuliers et qui sont codés par des gènes dits d avirulence. Ces systèmes de «chimioréception» permettent à la plante de percevoir la présence du «non soi» (Boller, 1995). La reconnaissance du pathogène via des récepteurs spécifiques va entraîner une reprogrammation génétique des cellules de l hôte et induire une réponse de défense généralement suffisante pour stopper la croissance du pathogène (Chisholm et al., 2006; Dangl and Jones, 2001; Nurnberger et al., 2004; Zipfel and Felix, 2005) Les éliciteurs généraux et la réponse basale Les éliciteurs généraux aussi appelés PAMPs pour «Pathogen-Associated Molecular Patterns» sont généralement des constituants stables et héréditaires, caractéristiques de l agent pathogène, souvent structuraux et de surface. On les appelle également MAMPs pour «Microbes-Associated Molecular Patterns». Ce terme comprend également les molécules 10
29 Effecteurs de type III flg22 elf18 Paroi cellulaire Système de sécrétion de type III FLS2 EFR BAK1 SERK Oxidase NADH Prf Fen AvrPtoB AvrPto ROS SGT1 HSP90 RAR1 AvrB AtMIN7 ETI Hop1 MAPKs PTI HopM1 Gènes induits par les PAMP GRP7 AvrBs3 PthA Gènes de sensibilité HopU1 Figure 4 : Signalisation de la réponse basale et cibles de certains effecteurs de type III connus. FLS2 et EFR sont des exemples de PRRs de surface. Le récepteur SERK est similaire à BAK1 et pourrait se dimériser avec les PRRs au moment de la stimulation par le ligand. Les protéines RAR1, GRP7, et AtMIN7 régulent les réponses de défense au niveau de la paroi végétale via des mécanismes inconnus. RAR1 réprime le dépôt de callose induit par flg22, alors que GRP7 induit le dépôt de callose lors de la reconnaissance des PAMPs. AtMIN7 pourrait jouer un rôle dans la voie ETI (ligne en pointillé). L effecteur AvrPto inhibe la transduction du signal par FLS2 et EFR pour bloquer la voie PTI. L effecteur HopAI1 inactive la signalisation MAP Kinase inhibant le voie PTI. HopU1 inhibe la voie PTI en modifiant la protéine GRP7. AvrB augmente l activité de RAR1 pour inhiber la voie PTI. L effecteur AvrPtoB induit l ubiquitination et la dégradation de la protéine Fen et empêche l initiation de la voie ETI via la protéine Prf (Protéine NBS-LRR). HopM1 déstabilise AtMIN7 pour inhiber les défenses au niveau de la paroi végétale. Les effecteurs de la famille AvrBs3/PthA se lient directement aux séquences promotrices des gènes de plantes et activent la transcription de certains gènes. Les effecteurs de type III sont en orange. PAMP, Pathogen-Associated Molecular Patterns ; ETI, effector-triggered immunity ; PTI, PAMP-triggered immunity ; NBS-LRR, Nucleotide Binding Site with Leucine Rich Repeat domain. (D après Zhou and Chai, 2008).
30 Introduction générale reconnues provenant de microorganismes non pathogènes. Cette notion de PAMPs est également valable chez les animaux, ces molécules vont alors induire les systèmes de défense de la réponse innée. Ces éliciteurs peuvent être de nature très variée. Il existe des PAMPs de natures peptidiques ou protéiques, comme les peptidoglycanes (Erbs et al., 2008), la flagelline (Felix et al., 1999; Sun et al., 2006) ou le facteur d élongation EF-Tu (Zipfel et al., 2006) qui peuvent être reconnus par la plante et induire les réponses de défense des plantes. La flagelline par exemple, est un puissant éliciteur. Un peptide de seulement 22 acides aminés (fgl22), situé au niveau N-terminal de la flagelline, peut être reconnu par le récepteur FLS2 et induire une réponse de défense chez Arabidopsis (Gomez-Gomez and Boller, 2002; Zipfel et al., 2004). On trouve également des PAMPs de nature oligosaccharidique ou lipidique comme les lipopolysaccharides (LPS) qui sont des constituants de la surface bactérienne. Les PAMPs peuvent aussi être produits à partir des constituants de la plante suite à une activité microbienne. On les appelle alors HAMPs pour «Host-Associated Molecular Patterns» (de Lorenzo, 2007) ou MIMPS pour «Microbe-Induced Molecular Patterns» (Bent and Mackey, 2007; Mackey and McFall, 2006). C est le cas des oligosaccharides provenant de la dégradation de la paroi végétale par les enzymes bactériennes (voir chapitre 3.4) comme les oligogalacturonates ou les glucanes (de Lorenzo, 2007). Les plantes reconnaissent ces substances avec une très grande sensibilité (Felix et al., 1999) [pour revue (Zipfel, 2008)]. Les récepteurs FLS2 reconnaissant la flagelline et EFR reconnaissant EF-Tu, sont des protéines transmembranaires possédant un domaine extracellulaire de type LRR (Leucine Rich Repeat) et un domaine intracellulaire de type Kinase. On appelle ce type de récepteurs aux PAMPs des RLK pour «Receptors-Like Kinase» ou PRR pour «Pattern Recognition Receptor». La reconnaissance des PAMPs par ces récepteurs induit l immunité basale équivalente à l immunité innée des mammifères (Nurnberger et al., 2004; Zipfel and Felix, 2005). Cette reconnaissance est nommée voie PTI pour PAMP-triggered immunity [(Chisholm et al., 2006) Fig. 4]. Au cours d un premier niveau de défense, la voie PTI va être induite via une cascade de signalisation de type MAP Kinase et une reprogrammation transcriptionnelle. Cette reprogrammation effectuée grâce à des facteurs de transcription de type WRKY, va mener à l induction de la production d espèces réactives de l oxygène (ROS) telles que les ions super oxydes (O - 2 ) et l H 2 O 2 (Delledonne et al., 2002; Torres et al., 2006) et d oxyde nitrique (NO). Elle ménera également à un flux rapide d ions à travers la membrane plasmique, une alcalinisation du milieu et un renforcement de la paroi par lignification et production de callose (polymère de D-glucose) ainsi qu une augmentation de la synthèse de protéines de parois riches en glycine (GRP), en 11
31 R Génotype de la plante hôte r Pathogène avirulent Plante non hôte Pathogène virulent Plante hôte Génotype du pathogène avr Avr Gène Avr Protéine Avr1 Protéine R1 Gène de résistance Résistance La plante et le pathogène sont incompatibles Plante hôte Pathogène virulent Maladie Gène de résistance Gène Avr Protéine Avr Maladie La plante et le pathogène sont compatibles Pathogène virulent Plante hôte Protéine R La plante et le pathogène sont compatibles Maladie La plante et le pathogène sont compatibles Figure 5 : Représentation de la théorie Gène pour Gène de Flor (1971). La reconnaissance d une protéine dite d avirulence de la bactérie par le produit d un gène de résistance de la plante mène à une interaction incompatible. On dit alors que la plante est non hôte et que la bactérie est avirulente. Lorsque l un des deux composants est absent, la relation devient compatible et la bactérie est capable de provoquer la maladie.
32 Introduction générale proline (PRP) ou en hydroxyproline (HPRP) et de subérine (Chisholm et al., 2006; Hardham et al., 2007; Maor and Shirasu, 2005). Cependant, ces mesures ne sont pas toujours suffisantes pour stopper la progression du pathogène, et d autres systèmes de résistance doivent être mis en place Les éliciteurs race spécifique Avr reconnus par les protéines de résistance R et la réponse hypersensible Le mécanisme moléculaire qui conduit à l'induction de la résistance est classiquement expliqué par le modèle de H.H. Flor appelé modèle "gène pour gène" (Flor, 1971) (Fig. 5). Pour que la plante soit résistante à un agent pathogène spécifique, une paire de gènes complémentaires de la plante (gène de résistance R) et de l'agent pathogène (gène d'avirulence avr) doit exister. L'interaction directe ou indirecte entre les produits de ces deux gènes conduit à la résistance. La plante est dite non hôte ou hôte résistant, l interaction est dite incompatible et le pathogène est avirulent. L'absence ou l'altération de l'un ou l'autre des gènes conduit au développement de la maladie. La plante devient alors hôte, l interaction compatible et le pathogène virulent (Fig. 5). La présence ou non de gènes de résistance correspondant au gène d avirulence va déterminer le spectre d hôte de l agent pathogène. Chez les bactéries phytopathogènes, de nombreux facteurs d'avirulence (plus de 40) ont majoritairement été isolés chez Pseudomonas syringae et Xanthomonas (Gopalan et al., 1996). Parmi ces gènes d avirulence, on trouve des gènes codant des effecteurs de type III qui sont des protéines transloquées par les bactéries dans la cellule eucaryote grâce à un système de sécrétion de type III (voir chapitre 3.5). Certains de ces effecteurs vont agir sur les voies de signalisation de défense pour les inhiber (Fig. 4). En effet, certains effecteurs de type III des bactéries vont pouvoir bloquer la voie PTI. Dans certains cas, ces effecteurs peuvent également trahir la présence du pathogène et induire d autres systèmes de défense. La plante va alors reconnaître ces effecteurs grâce à des protéines de résistance (Dangl and Jones, 2001; Van der Biezen and Jones, 1998) et initier la voie ETI (Effector-Triggered Immunity) qui correspond à une réponse PTI beaucoup plus forte et qui mène systématiquement à une mort cellulaire programmée (PCD, Programmed Cell Death ; ou apoptose) nommée réponse hypersensible (HR) (Fig. 4). La HR va permettre de confiner l agent pathogène dans la zone d infection (Lam et al., 2001). Elle a lieu dans les heures qui suivent l infection et peut être initiée par la reconnaissance de la plupart des microorganismes phytopathogènes. Les cellules qui meurent émettent alors des molécules 12
33 Tableau 3. Propriétés des différentes familles de protéines PR. (D'après Sels et al., 2008) Famille Membre type Taille typique (kda) Propriété Cible microbienne proposée Référence d'origine PR-1 Tobacco PR-1a 15 Antifongique Inconnue (Antoniw et al, 1980) PR-2 Tobacco PR-2 30 β-1,3-glucanase β-1,3-glucane (Antoniw et al, 1980) PR-3 Tobacco P, Q Chitinase (class I, II, IV, V, VI, Chitine (Van Loon, 1982) PR-4 Tobacco "R" Chitinase de classe I, II Chitine (Van Loon, 1982) PR-5 Tobacco S 25 "Thaumatin-like" Membrane (Van Loon, 1982) PR-6 Tomato Inhibitor I 8 Inhibiteur de protéase a (Green et Ryan, 1972) PR-7 Tomato P69 75 Endoprotéase a (Vera et al, 1988) PR-8 Cucumber chitinase 28 Chitinase de classe III Chitine (Métraux et al, 1988) PR-9 Tobacco "lignin-forming" 35 Péroxidase a (Lagrimini et al, 1987) PR-10 Parsley "PR1" 17 Ribonuclease-like a (Somssich et al, 1986) PR-11 Tobacco "class V" 40 Chitinase de class I Chitine (Melchers et al, 1994) PR-12 Radish Rs-AFP3 5 Défensine Membrane (Terras et al, 1995) PR-13 Arabidopsis THI2.1 5 Thionine Membrane (Epple et al, 1995) PR-14 Barley LTP4 9 Protéine de transfer de lipides Membrane (Garcia-Olmedo et al, 1995) PR-15 Barley OxOa (germin) 20 Oxalate oxidase a (Zhang et al, 1995) PR-16 Barley OxOLP 20 Oxalate oxidase-like a (Wei et al, 1998) PR-17 Tabac PRp27 27 Inconnue a (Okushima et al, 2000) Le tableau a été adapté de a Pas d'activité antimicrobienne identifiée in vitro
34 RLP RLK PGIP LRR LRR LRR Apoplaste Membrane plasmique TD TD TD Cytoplasme CC CC TIR NB NB LRR Domain e kinase NBS-LRR (RRS1-R) LRR TIR Xa27 NB NBS-LRR LRR NLS WRKY Noyau Figure 6 : Différentes classes de Protéines de Résistance. Les protéines de résistance (R) sont classées selon la structure de leurs domaines. Les deux classes les plus importantes comprennent les protéines NBS-LRR (autrement nommées NB- LRR ou NLRs) et les protéines de résistance extracellulaires LRR (elrr). Les protéines de la classe des NB-LRR peuvent avoir des domaines «coiled-coil» ou «Tollinterleukin-1 receptor» au niveau des acides aminés terminaux. La protéine RRS1-R, par exemple, est un nouveau membre de la classe NB-LRR contenant un signal de localisation nucléaire en C-terminal et un domaine ayant des homologies avec les facteurs de transcription WRKY. Les protéines elrrs ont été réparties en trois sous-classes selon leurs domaines, les RLPs possédant un domaine extracellulaire LRR et un domaine transmembranaire, les RLKs possédant en plus un domaine kinase cytoplasmique et les PGIPs possédant un domaine LRR localisé dans la paroi végétale. Une nouvelle protéine R, Xa27 possédant une similarité de séquence avec des protéines de fonction inconnue et n ayant aucun homologue autre que chez le riz, a été identifiée. NB ou NBS, Nucleotide Binding Site ; LRR, Leucine Rich Repeat ; TIR, Toll-interleukin-1 receptor ; CC, Coiled-Coil ; NLS, Nuclear Localization Signal ; RLP, Receptor-Like Proteins ; RLK, Receptor-Like Kinase ; PGIP, Polygalacturonase Inhibiting Protein. (D après Chisholm et al., 2006)
35 Introduction générale servant de signaux d alerte, perçus par les cellules voisines. Ces cellules vont alors mettre en place des mécanismes de défense consistant essentiellement en la production de molécules antimicrobiennes (flavonoïdes, coumarines, phytoalexines, anthocyanines) (Dangl and Jones, 2001) ou de ROS et à la mise en place de barrières physiques (callose, lignification, bourrelets cicatriciels) (Klarzynski and Fritig, 2001). Le trafic vésiculaire est activé sans doute pour augmenter la sécrétion de molécules antimicrobiennes et de composants permettant l épaississement de la paroi (Bestwick et al., 1995; Brown IR et al., 1995; Keshavarzi et al., 2004). Un grand nombre de gènes va être induit dont des gènes codant des protéines PR (Pathogenesis Related) stables qui sont normalement exprimées à un taux non détectable mais qui s accumulent dans les tissus lors d une infection. Les protéines PR ont généralement une activité antimicrobienne, comme des chitinases qui vont dégrader les parois des champignons ou des protéases (Tableau 3). Des gènes de biosynthèse de l éthylène (ET) ou de l acide salicylique (SA) peuvent aussi être induits. Cette réponse des cellules voisines du site de HR correspond à la Réponse Locale Acquise ou LAR. Ces cellules seraient à l origine de signaux transmis au reste de la plante pour induire une réponse de défense généralisée. Plusieurs classes de protéines de résistance sont aujourd hui décrites comme étant à l origine de cette réponse (Fig. 6). Les protéines kinases intracellulaires, comme la protéine Pto chez la tomate confère une résistance à P. syringae pv. tomato (Martin et al., 1993). Les protéines NBS-LRR ou encore appelées, NB ou NLRs (NBS pour «Nucleotide Binding Site et LRR pour «Leucine Rich Repeat) représentent la famille la plus importante de protéine de résistance chez les végétaux avec au moins 200 représentants. Le domaine LRR faciliterait l interaction entre la protéine R et d autres protéines de la voie de signalisation chez Arabidopsis. On trouve également les protéines TIR-NBS-LRR ayant un domaine TIR pour «Toll and Interleukine Receptor» impliqué dans la signalisation, les protéines LZ-NBS-LRR avec un domaine «Leucine Zipper» qui faciliterait la dimérisation des protéines, les protéines CC-NB-LRR qui possèdent un domaine Coiled-Coil (CC). La protéine RRS1-R (Resistance to Ralstonia solanacearum 1-R) d Arabidopsis thaliana est un nouveau membre de la sousclasse TIR-NBS-LRR, qui présente deux domaines supplémentaires, un domaine NLS (Nuclear Localization Signal) ainsi qu un domaine homologue aux facteurs de transcription WRKY (Deslandes et al., 2002; Deslandes et al., 2003). Il existe également des protéines de résistance extracellulaires ayant un domaine LRR (elrr). Certaines de ces protéines possèdent un domaine transmembranaire et définissent la classe des RLP (Receptor-Like Proteins). Les membres d une sous classe de RLP, les RLK (Receptor-Like Kinases), 13
36 Introduction générale possèdent un domaine kinase intracellulaire supplémentaire et sont homologues aux PRR impliqués dans la reconnaissance des PAMPs. La reconnaissance des effecteurs peut s effectuer selon deux modèles : le modèle récepteur-ligand où la protéine Avr va être directement reconnue par la protéine R (Keen, 1990) et le modèle de «garde» où la protéine R va reconnaître la modification effectuée sur la cible de la protéine Avr (de Wit, 2002). 2.2 La réponse systémique acquise La résistance localisée peut donc être suivie par la mise en place d une Résistance dite Systémique Acquise (SAR) qui consiste en la mise en place de systèmes de défense à long terme et à distance contre une large gamme de microorganismes. La SAR permettra une meilleure résistance de la plante lors d une seconde agression (Durrant and Dong, 2004). Elle est caractérisée par l'activation d'un certain nombre de gènes codant des protéines à activité antibiotiques comme des dérivés de la voie des phenylpropanoïdes et des protéines PR. L induction des systèmes de défense résulte d un réseau complexe de régulation impliquant des médiateurs comme l acide salicylique (SA), le jasmonate (JA), l éthylène (ET) et d autres hormones comme l acide abscissique. Plusieurs signaux pourraient être impliqués dans l induction de la SAR. Tout d abord, le SA dont le taux augmente dans les tissus proches de l infection puis dans tous les tissus serait le signal majeur pour une réponse systémique (Gaffney et al., 1993; Malamy et al., 1990). Cependant le SA ne serait pas le signal mobile de la SAR. Ce rôle serait attribué à une protéine lipidique apoplastique (Maldonado et al., 2002). L ET pourrait également être impliqué dans la signalisation de la SAR (Verberne et al., 2003). La transduction du message via le SA nécessite la protéine NPR1 (Non-expressor of Pathogenesis-Related genes 1) aussi connue sous le nom de NIM1 (Non-inducible IMmunity 1). NPR1 est une protéine régulatrice qui va activer l expression des gènes PR sans se fixer à l ADN (Pieterse and Van Loon, 2004). NPR1 est également impliquée dans la signalisation de la Résistance Systémique Induite (ISR) activée lors de la colonisation des racines par certaines espèces de rhizobactéries non-pathogènes (Pieterse et al., 2002). 14
37 Haut PTI ETS ETI ETS ETI Seuil pour la HR Amplitude de la défense 1 Effecteurs du 3 pathogène Effecteurs du pathogène 2 Avr-R 4 5 Avr-R Seuil pour une résistance efficace Bas PAMPs Figure 7 : Le modèle en zig zag illustrant la production quantitative de l équipement nécessaire à la défense immunitaire de la plante. (1), la plante détecte les PAMPs grâce aux PRRs et induit la voie PTI. (2), le pathogène va délivrer une batterie d effecteurs qui va bloquer la voie PTI ou permettre la nutrition et la dispersion du pathogène résultant en une sensibilité nommée ETS (effectortriggered susceptibility). (3), un effecteur va être reconnu par une protéine de résistance (NB-LRR) activant la voie ETI et permettant la mise en place de la HR. (4), les pathogènes ayant perdu l effecteur rouge et/ou ayant éventuellement un nouvel effecteur (bleu) permettant de bloquer la voie ETI sont sélectionnés. (5), L évolution va alors sélectionner des plantes ayant un nouvel allèle codant une protéine de résistance capable de reconnaître un des nouveaux effecteurs acquis par le pathogène induisant la voie ETI. L amplitude de la résistance est proportionnelle à [PTI ETS+ETI]. ETS, effector-triggered susceptibility ; ETI, effector-triggered immunity ; PTI, PAMP-triggered immunity ; PAMP, Pathogen-Associated Molecular Patterns ; PRR, pattern recognition receptors ; NB, Nucleotide Binding Site ; LRR, Leucine Rich Repeat ; HR, hypersensitive response. (D après Jones and Dangl, 2006)
38 Introduction générale 2.3 La coévolution plantes/pathogènes, un véritable ping pong L interaction entre les plantes et leurs pathogènes est une guerre de l innovation sans fin. Les pathogènes mettent au point des systèmes d attaque leur permettant de se développer alors que la plante va développer des systèmes de contre-attaque. L avantage obtenu par l un ou l autre des protagonistes ne dure jamais longtemps. Ainsi, les PAMPs vont être reconnus par les PRRs induisant la voie PTI et empêchant la colonisation. Les pathogènes vont alors déployer des effecteurs qui vont interférer dans la voie PTI et permettre la virulence. Les effecteurs vont être reconnus par les protéines de résistance et la voie ETI va être induite menant à une HR. Certains pathogènes vont posséder des effecteurs leur permettant de détourner cette voie ETI. Il faudra alors de nouvelles protéines de résistance pour empêcher la dissémination du pathogène (Jones and Dangl, 2006) (Fig. 7). 15
39 Introduction générale 3 Chapitre 3. Les déterminants du pouvoir pathogène bactérien Nous venons de voir que les plantes possèdent tout un arsenal de systèmes leur permettant de limiter le développement de maladies. De leur côté, les agents pathogènes possèdent de nombreux facteurs de virulence leur permettant d infecter et de se développer dans la plante. Les principaux déterminants du pouvoir pathogène bactériens sont décrits dans ce chapitre, en prenant pour exemple, quand cela est posible, les facteurs de virulence identifiés chez les Xanthomonadaceaes. 3.1 L adhésion Une fois la bactérie pathogène entrée dans les tissus de l hôte (via des ouvertures naturelles, des vecteurs ou des blessures), elle va pouvoir se fixer aux cellules pour établir un centre d infection à partir duquel elle va se disséminer. Cette étape d adhérence implique des molécules bactériennes de surface appelées adhésines. Ces molécules vont reconnaître des récepteurs spécifiques des cellules de l hôte tels que des glycolipides ou des protéoglycanes (Rostand and Esko, 1997). L adhésion peut se faire à l aide de pili ou fimbriae (Craig et al., 2004), des protéines spécialisées non fibrillaires ou de la couche mucoïde. Des gènes codant des pili de type IV, qui sont des homopolymères de piline (protéine de KDa), sont présents chez les bactéries phytopathogènes Pseudomonas syringae (Roine et al., 1998), X. campestris pv. vesicatoria (aujourd hui classé dans l espèce X. axonopodis) (Ojanen-Reuhs et al., 1997), X.oryzae pv. oryzae (Lim et al., 2008) ou encore Ralstonia solanacearum (Kang et al., 2002). Chez X. campestris pv. hyacinthi ainsi que chez P. syringae pv. phaseolicola par exemple, le pilus de type IV est impliqué dans l attachement aux stomates des feuilles de la plante hôte (Romantschuk and Bamford, 1986; van Doorn et al., 1994). Les génomes de Xylella fastidiosa (Simpson et al., 2000) et de R. solanacearum (Salanoubat et al., 2002) possèdent quant à eux des gènes codant de nombreuses adhésines potentielles. On trouve plus particulièrement 14 homologues de l hémagglutinine (FHA) de Bordetella pertussis chez la bactérie R. solanacearum. 16
40 A B C 1 Polymérisation Pilus 2 Attachement 3 Dépolymérisation Twitching Swarming Swimming Figure 8 : Représentation schématique de trois types de mobilité bactérienne. A. Mobilité par par «twitching» via le pilus de type IV. Ce processus peut être divisé en trois étapes : (1) la polymérisation du pilus, (2) l attachement du pilus à la surface de migration, (3) la dépolymérisation du pilus entrainant la tractation de la bactérie. B. Mobilité par «swarming» via la rotation de plusieurs flagelles latéraux. C. Mobilité par «swimming» grâce à la rotation d un flagelle polaire.
41 Introduction générale Chez Dickeya dadantii et X. oryzae pv. oryzae les adhésines non fibrillaire HecA et XadA sont impliquées dans la virulence (Ray et al., 2002; Rojas et al., 2002). Il est intéressant de noter que Xcc possède un orthologue du gène xada mais sa fonction dans l adhésion et la virulence n a pas été encore démontrée. 3.2 La mobilité et le chimiotactisme Il existe plusieurs types de mobilité. La mobilité par «twiching» réalisée grâce aux pili de type IV (Craig and Li, 2008; Kaiser, 2007). La mobilité par «swarming» (nage en surface) et «swimming» (nage dans un liquide) sont réalisées généralement par le flagelle, long appendice protéique flexible et motorisé [(Fig. 8), revue sur le flagelle (Chevance and Hughes, 2008)]. Le filament flagellaire est composé d une succession de flagelline, protéine pouvant être reconnue par la plante est induire les systèmes de défense (Chapitre 2). La bactérie Mixococcus xanthus possède une machinerie de sécrétion de gels visqueux la propulsant vers l avant (Wolgemuth et al., 2002). Les bactéries mobiles peuvent être attirées par des substances nutritives comme les sucres, les acides aminés, l oxygène, ou être repoussées par des substances nuisibles. On appelle ce phénomène le chimiotactisme. Les bactéries vont diriger leur mouvement en fonction d un gradient chimique. En effet, la rotation du flagelle est directement reliée au système de chimiotactisme. Le mécanisme moléculaire du chimiotactisme est complexe. Il implique des changements conformationnels des protéines par méthylation ou phosphorylation. La transduction du signal a été largement étudiée chez Escherichia. coli mais beaucoup moins chez les autres espèces bactériennes. Les substances attractives et répulsives sont détectées grâce à un système de phospho-relais à deux composants. Des chimiorécepteurs (MCP, Methyl accepting Chemotaxis Proteins) de nature protéique vont transmettre le signal à d autres composants du système, les chimiosenseurs. Des études ont démontré que les systèmes de chimiotactisme sont également impliqués dans la régulation de la mobilité via les pili de type IV (Bhaya et al., 2001; Sun et al., 2000; Whitchurch et al., 2004). Le chimiotactisme peut être important pour la formation de biofilm et pour la mise en place du pouvoir pathogène. Par exemple, chez la bactérie phytopathogène R. solanacearum responsable du flétrissement bactérien de la tomate, il existe un système d aérotaxie et 17
42 Introduction générale d énergie taxie permettant à la bactérie de se diriger vers les racines de tomate. Des mutants dans ces systèmes sont retardés dans le développement de la maladie (Yao and Allen, 2007). L annotation des génomes de Xanthomonas séquencés a montré la présence de 26 gènes conservés chez les souches de Xcc qui pourraient être impliqués dans l assemblage du pilus de type IV permettant la mobilité par «twitching» et l adhésion aux cellules eucaryotes. Xcc possède également des gènes de biosynthèse du flagelle et des chémorécepteurs organisés en quatre groupes répartis sur 150 kb. Un de ces groupes possède plusieurs copies quasiidentiques et répétées en tandem du gène tsr codant des chimiorécepteurs de type MCP. Ce genre de répétition est peu courant chez les bactéries et laisse penser que le chimiotactisme est un processus important dans la vie de Xcc (da Silva et al., 2002). Les études menées par Shen et Ronald (Shen and Ronald, 2002) suggèrent que le chimiotactisme vers les gouttes de guttation faciliterait l accès au site d infection avant la pénétration. 3.3 Les systèmes d acquisition du fer Le fer est un cofacteur essentiel à de nombreuses enzymes et par conséquant, participe à de nombreuses voies métaboliques que ce soit chez les procaryotes ou les eucaryotes. Le couple redox Fe 2+ /Fe 3+ permet de catalyser un large spectre de réactions d oxydoréduction et de transfert d électrons. La capture du fer est restreinte à deux formes du fer, le fer ferreux Fe 2+ et le fer ferrique Fe 3+. Dans l environnement, le Fe 3+ libre assimilable dans le milieu n est disponible qu à l état de traces (10 9 à M). Les organismes vivants ont donc dû mettre en place des systèmes efficaces d acquisition du fer. Ceci est d autant plus vrai lors de relations hôte-pathogène au cours desquelles les deux partenaires sont en compétition pour cette acquisition. Les bactéries ont développé un système de capture du fer impliquant des molécules appelées sidérophores capables de complexer le fer ferrique avec une très grande affinité, des systèmes de transport spécifiques dits TonB-dépendants qui vont transporter les complexes fer/sidérophores dans la cellule et un système de régulation capable de percevoir le taux de fer intracellulaire via la protéine Fur (Braun and Killmann, 1999). Les sidérophores sont nécessaires à la virulence de nombreux pathogènes (Ratledge and Dover, 2000). Par exemple, la production des sidérophores chrysobactine et achromobactine est essentielle pour la mise en place de l infection par Dickeya dadantii (anciennement nommée Erwinia chrysanthemi) (Expert, 2005; Franza et al., 2005). De plus, de nombreux pathogènes animaux 18
43 A Complexe Fersidérophore Complexes fer /siderophore B TBDT Transporteur ABC ExbD E ExbB TonB ExbD E ExbB TonB Antisigma Fe 2+ Fur - Fe 2+ σ ECF ARN Polymérase Fur box Gènes impliqués dans l acquisition du fer et son stockage Figure 9 : Modèle du système d acquisition du fer des bactéries Gram et de sa régulation. Le complexe Fe 3+ -sidérophore est reconnu par le transporteur de la membrane externe, ici un TBDT (TonB-Dependent Transporter). Suivant le cas, le TBDT aura une fonction de transport et/ou une fonction de signalisation. Le transport et la transmission du signal dépendent de l énergie provenant du complexe TonB ExbB ExbD. A. Le complexe Fe 3+ -sidérophore est transporté vers le périplasme par le TBDT puis vers le cytoplasme via le transporteur de type ABC. Quand le niveau intracellulaire en fer est élevé le répresseur Fur complexé au fer va réprimer la transcription des gènes impliqués dans l acquisition du fer. B. Le signal de fixation du complexe Fe 3+ -sidérophore au TBDT va être transmis de l extension N-terminale du TBDT vers le facteur anti-sigma qui va libérer un facteur sigma de type ECF permettant la transcription des gènes. (D après Schalk et al., 2004 et Blanvillain, 2007)
44 Introduction générale ont développé la capacité de reconnaître directement les hèmes de leur hôte tel que l hémoglobine (Wagegg and Braun, 1981; Wandersman and Delepelaire, 2004). Le transport des complexes fer/sidérophores s effectue de façon active grâce à des transporteurs de la membrane externe. L énergie requise pour ce transport provient de la force protomotrice transférée au transporteur par le complexe TonB-ExbB-ExbD localisé dans la membrane plasmique [Fig.9, (Schalk et al., 2004)]. Le transporteur de la membrane externe est alors appelé TBDT pour «TonB-Dependent Transporter». Ces transporteurs sont capables de faire passer des molécules supérieures à 600 Da à travers la membrane externe. Xcc possède un complexe TonB/ExbB/ExbD1 essentiel à l acquisition du fer. De façon atypique, cette bactérie possède un second gène exbd codant une protéine ExbD2 non essentielle pour l acquisition du fer et incapable de substituer ExbD1 (Wiggerich et al., 1997). De plus, il a été montré que ces quatre gènes sont nécessaires à la production d une HR sur le poivron nonhôte, mais que seuls les gènes tonb, exbb et exbd1 sont indispensables à la virulence sur plante Hôte (Wiggerich and Puhler, 2000). Chez Xcc, les TBDTs sont sur-représentés. En effet, 72 gènes codant des TBDTs potentiels ont été identifiés dans son génome dont seulement neuf seraient impliqués dans l acquisition du fer et sont régulés par la protéine Fur (Blanvillain et al., 2007). Une fois dans le périplasme, le complexe fer/sidérophore est pris en charge par un transporteur de type ABC, et le fer sera libéré sous forme Fe 2+ dans le cytoplasme. Les gènes impliqués dans l acquisition et le stockage du fer sont finement régulés en fonction du taux de fer intracellulaire disponible. Cette régulation est assurée par le répresseur Fur capable de lier le Fe 2+ cytoplasmique. En présence de fer, la protéine Fur complexée au Fe 2+ va se fixer sur un opérateur en amont des gènes d acquisition et de stockage du fer et empêcher leur transcription (Escolar et al., 1999; Hantke, 2001). Chez D. dadantii, la protéine Fur régule non seulement les gènes d acquisition et de stockage du fer mais également les gènes codant pour des pectates lyases impliquées dans la virulence qui permettent la dégradation des parois végétales (Franza et al., 2005). Dans certains cas, il existe un second niveau de régulation où le signal de fixation du complexe fer/sidérophore au TBDT est transmis via une extension N-terminale de ce TBDT au facteur anti-sigma localisé dans la membrane plasmique. Ce dernier va alors libérer le facteur sigma nécessaire à la transcription des gènes d acquisition du fer (Schalk et al., 2004) (Fig. 9). Chez la bactérie R. solanacearum par exemple, l interaction entre la bactérie et la cellule végétale est perçue par le TBDT PrhA qui va, après changement conformationnel, transduire le signal à un couple sigma/anti-sigma PrhI/PrhR et entraîner, via une cascade de 19
45 A Paroi secondaire Paroi primaire Lamelle moyenne B Lamelle moyenne Paroi primaire Pectines Microfibres de cellulose Membrane plasmique Hémicelluloses Protéines solubles Figure 10 : La paroi végétale. A. Représentation schématique de la paroi de cellules du sclérenchyme. La paroi végétale est généralement constituée de trois éléments se formant successivement au cours de la différentiation cellulaire : la lamelle moyenne, la paroi primaire, et les trois couches de la paroi secondaire. Image provenant du site B. Représentation schématique de la structure de la paroi primaire. Elle consiste en un réseau complexe de fibres de cellulose, de pectine, d hémicellulose et de protéines solubles. Image provenant du site thumbs/5/53/plant_cell_wall-diagram.svg.png
46 Introduction générale régulation, la transcription des gènes hrp codant le système de sécrétion de type III nécessaire au développement de la maladie (Marenda et al., 1998). 3.4 La dégradation de la paroi végétale et l acquisition des sucres Une fois dans les tissus de la plante, les bactéries pathogènes vont dégrader la paroi des cellules végétales. Cette dégradation entraînera une libération de nutriments qui seront utilisés comme source de carbone et d énergie par les bactéries, mais permettra également une dissémination des agents pathogènes dans les tissus. La paroi cellulaire des végétaux est généralement constituée de trois structures juxtaposées : la lamelle moyenne (riche en substances pectiques), la paroi primaire et la paroi secondaire (Fig. 10). Les cellules peu différenciées ou en cours de croissance présentent surtout une paroi primaire tandis que les cellules différenciées possèdent une paroi primaire et une paroi secondaire rigide. La paroi primaire se présente comme un réseau lâche de microfibrilles de cellulose, englobées dans une matrice amorphe fortement hydratée de pectines et d hémicelluloses. La paroi secondaire, quant à elle, est une structure inextensible et faiblement hydrophobe, constituée de cellulose et de lignines, présentant trois couches successives conférant une grande résistance à la paroi Composition de la paroi primaire Structurellement, la paroi primaire se compose de cellulose, d hémicellulose et de substances pectiques (ou pectines) (Cosgrove, 2005; Lerouxel et al., 2006). La callose est le premier polysaccharide produit lors de la formation de la paroi (Fig. 11A) (Verma, 2001). Cette molécule est constituée de D-glucopyrannoses reliés entre eux par des liaisons osidiques β-1,3. Elle est rapidement remplacée par la cellulose, un β-1,4-glucane qui constitue la trame principale de la paroi primaire. Cet assemblage polysaccharidique est constitué d un motif de base dénommé cellobiose constitué de deux α-d-glucopyrannoses reliés par une liaison osidique β-1,4 (Fig. 11B). Les molécules de cellulose peuvent s organiser en filaments appelés microfibrilles réunies par une matrice d hémicellulose et de pectine (Fig. 10). L hémicellulose peut être composée de différents polyosides tels que les glucomannanes, qui sont des polymères constitués de D-glucopyrannose et de D-mannopyrannose, les 20
47 A B C HO HO HO O O OH O OH HO OH HO HO HO O OH HO O OH OH O OH Callose Cellobiose Xyloglucane D Pectine Rhamnogalacturonane de type I Arabinane Polygalacturonane Rhamnogalacturonane de type II Arabinogalactane Galactane Acide Acide Fucopyrannose galacturonique Fucopyrannose galacturonique KDO KDO DHA DHA L-AceA D-Api AceA D-Api Acétylation Acétylation Méthylation Méthylation Galactopyrannose Arabinopyrannose Arabinofuranose Rhamnopyrannose Acide acérique Xylopyrannose Glucopyrannose Figure 11 : Représentation schématique de différents polymères de sucres composant la paroi primaire végétale. A. Callose constituée de D-glucopyrannoses reliés entre eux par des liaisons osidiques β-1,3. B. Cellobiose constituée de deux α-d-glucopyrannoses reliés par une liaison osidique β -1,4. C est l unité de base de la cellulose. C. Exemple de xyloglucane, constituant de l hémicellulose. D. Représentation schématique des polymères constituant la pectine. KDO, acide 2- céto-3-déoxy-d-manno-octulosonique ; DHA, acide 3-déoxy-D-lyxo-2- heptulosarique ; D-Api, D-Apiose.
48 Introduction générale xyloglucanes (hémicelluloses majeurs des parois primaires de dicotylédones) dont le squelette se compose de β-d-glucopyrannoses (Fig. 11C) et les xylanes dont le squelette est composé d unités de β-d-xylopyrannose. Parmi les hémicelluloses, citons également les β-glucanes mixtes, polymères de β-d-glucopyrannose et les mannanes, structures linéaires de D- mannopyrannose. Les substances pectiques quant à elles sont des polymères complexes, présents en abondance dans la lamelle moyenne et la paroi primaire. La pectine est composée majoritairement d acide D-galacturonique. On trouve trois types de polymères composant la pectine, les polygalacturonanes et les rhamnogalacturonanes de types I et II. Les rhamnogalacturonanes ont une structure complexe avec de nombreuses ramifications (Fig. 11D). De nombreuses glycoprotéines comme les extensines sont présentes dans les parois. Peu solubles et difficiles à extraire, leur rôle exact n est pas clairement connu. Suivant leur composition en acides aminés, il est possible de distinguer les HRGPs (Hydroxyprolin Rich GlycoProteins, fortement O-glycosylées) parmis lesquelles on distingue les GRP (Glycin Rich Proteins, non glycosylées), les PRP (Prolin Rich Proteins, faiblement glycosylées) et les AGPs (arabinogalactan-proteins). La paroi végétale contient également des protéines riches en glycine (GRPs) (Mousavi and Hotta, 2005). Enfin la paroi primaire contient des acides phénoliques (acide férulique, acide para coumarique) liés de façon covalente (liaisons ester) aux polymères d hémicellulose chez les monocotylédones et aux substances pectiques chez les dicotylédones. Ils sont impliqués dans la formation de ponts inter-chaînes ou associés avec la lignine La biodégradation de la paroi végétale par les bactéries Pour être assimilable, la paroi doit être digérée en sous unités plus petites par les bactéries. Xcc possède un répertoire important d enzymes de dégradation de la paroi végétale (Tableau 4) impliquées dans la dégradation de la pectine, de la cellulose (cellulases, cellobiosidases et β-glucosidases) et de l hémicellulose (xylanases, xylosidases, arabinosidases). Ce «CAZyome» ou glycobiome (enzymes répertoriées dans la base de donnée CAZy, important représente une capacité d utilisation des ressources importante, facilite sa progression dans les tissus et lui confère un avantage non négligeable dans la compétition entre les bactéries pour la nutrition. 21
49 Tableau 4. Enzymes de dégradation de la paroi végétale de Xanthomonas campestris pv. campestris, source da Silva et al., (2002). (D après Meyer, 2005). Enzymes de dégradation de la paroi végétale chez Xcc Activité enzymatique Nombre Nom Numéro de l'orf Enzymes Pectinolytiques 9 Enzymes Cellulolytiques 18 Enzymes Hémicellulolytiques 13 Nombre total = 40 Polygalacturonases (PG) Pectates lyases (PL) Pectine méthylestérases (PME) Rhamnogalaturonane acétylestérase Rhamnogalaturonases (3 ORF tronquées) Cellulases Cellobiosidases Beta-glucosidases Xylanases Xylosidases/arabinosidases XCC2266 XCC3459 XCC0122 XCC0644 XCC0645 XCC2815 XCC0121 XCC2265 XCC0154 XCC3377 XCC3378 XCC3379 XCC0026 XCC0027 XCC0028 XCC1752 XCC2387 XCC3380 XCC3381 XCC3521 XCC3535 XCC3160 XCC3534 XCC1090 XCC1250 XCC1775 XCC2892 XCC4106 XCC1404 XCC3814 XCC0144 XCC0857 XCC3038 XCC4115 XCC4118 XCC0149 XCC1178 XCC1755 XCC2398 XCC3975 XCC4064 XCC4105 XCC4122 Nom du gène pgla peh-1 pel pel pelb egl egl egl egl2 cels engxca bglx bglx celd nixi bgls bglx xynb xynb xyna xynb xylb xyls xsa xynb xylb xsa
50 Introduction générale A. Dégradation de la pectine Il y a quatre familles principales d enzymes impliquées dans la dégradation de la pectine : les polygalacturonases, les pectates lyases, les pectines lyases et les pectine méthylestérases (PME) (Tableau 4). Les PME vont déestérifier les pectines facilitant ainsi les actions des polygalacturonases et des pectate lyases. Les PME favorisent ainsi la macération des tissus chez D. dadantii (Shevchik and Hugouvieux-Cotte-Pattat, 1997). Le génome de Xcc possède deux gènes codant des pectine méthylestérases, deux gènes codant des polygalacturonases pghaxc et pghbxc dont l expression est régulée par les régulateurs majeurs du système Hrp (Cf paragraphe 3.5), HrpG et HrpX ainsi que par le répresseur catabolique CLP, un homologue au répresseur de l AMP cyclique d E. coli. Ces polygalacturonases sont sécrétées via le système de sécrétion de type II (Wang et al., 2008). Xcc possède également quatre gènes codant des pectate lyases, mais ne semble pas posséder de pectine lyases. Les pectine méthylestérases vont faciliter la macération des tissus alors que les polygalacturonases vont être impliquées dans la formation de gels pectiques altérant la conduction de sève et permettant à la bactérie de collecter des nutriments d origine végétale (Prade et al., 1999). B. Dégradation de la cellulose Les cellulases peuvent être de deux types, les endo-β1,4-glucanases (Eng) et les cellobiohydrolases (Exg). Deux endoglucanases ont été décrites dans la souche 8004 de Xcc. L une d entre elles est codée par le gène engxca et a été caractérisée par Gough et ses collaborateurs (Gough et al., 1990). La seconde est codée par le gène engxcb (Schroter et al., 2001). La protéine EngXCB fait partie d une famille de protéines possédant une séquence signal suggérant une sécrétion via le système de sécrétion de type II. La délétion des gènes engxca et engxcb entraîne une diminution d un facteur cinq de l activité cellulolytique (Schroter et al., 2001). C. Dégradation de l hémicellulose Il existe dans le génome de Xcc, 5 gènes codant pour des xylanases potentielles qui vont cliver le xylane, polymère abondant dans les vaisseaux du xylème, dont certains sont conservés chez X. oryzae pv. oryzae (Ray et al., 2000). Les xylanases, arabinosidases et 22
51 Introduction générale xylosidases pourraient avoir un rôle dans l acquisition de sucres fournissant de l énergie à la bactérie. D. Dégradation des protéines Xcc possède également un très large protéasome avec 278 peptidases potentielles appartenant à de nombreuses familles (Base de donnée MEROPS : Un métalloprotéase à zinc par exemple, a été décrite chez Xcc. Elle interviendrait dans la dégradation de glycoprotéines riches en proline (PRP) ou en hydroxyproline (HRGP) localisées dans la matrice extracellulaire. Ces protéines sont majoritairement O-glycosylées (Kieliszewski and Shpak, 2001). Les PRPs et HRGPs pourraient avoir un rôle dans la défense des plantes par agglutination et immobilisation des bactéries. La capacité de Xcc à dégrader ces protéines pourrait altérer les réponses de défense des plantes (Dow et al., 1998). Xcc produit également une endo-β1,4-mannanase impliquée dans la virulence (Dow et al., 2003). Cette protéine serait impliquée dans la dissolution d agrégats bactériens permettant le relargage de bactéries planctoniques et la dissémination de Xcc dans les tissus. E. Le transport Comme il est mentionné dans le Chapitre 2 de l introduction générale, une fois les polymères de la paroi partiellement dégradés, le produit de cette dégradation peut être reconnu par la plante comme des MIMPs et induire les systèmes de défense. Il est donc dans l intérêt de la bactérie d avoir des systèmes efficaces de transport des produits de dégradation. Le transport à travers la membrane externe peut faire intervenir des transporteurs passif de type porine (Nikaido, 2003) ou actifs de type TBDT (Cf paragraphe 3.3) (Blanvillain et al., 2007; Eisenbeis et al., 2008; Neugebauer et al., 2005; Schauer et al., 2008). Il a été montré que ces TBDTs pouvaient être impliqués dans le transport actif d autes molécules que les complexes fer-sidérophores, comme la vitamine B12 (Gudmundsdottir et al., 1989), le nickel (Schauer et al., 2007), ou des carbohydrates végétaux avec une très forte affinité (Blanvillain et al., 2007; Eisenbeis et al., 2008; Lohmiller et al., 2008; Neugebauer et al., 2005). Une étude approfondie de l acquisition du saccharose chez Xcc a montré que ce sucre est transporté via un TBDT et que les gènes impliqués dans son utilisation et son transport sont regroupés en locus fonctionnel nommé CUT locus (Carbohydrate Utilization loci containing 23
52 Transport actif Saccharose Transport passif Extérieur SuxA Porine? Membrane externe ExbD2? ExbD1? ExbB TonB SuxC Membrane interne SuxR SuxB Cytoplasme suxr suxc suxa suxb XCC3356 XCC3357 XCC3358 XCC3359 Régulateur Transporteur Transporteur TonB-dépendant Saccharose hydrolase WT sux Virulence/Adaptation WT sux Figure 12 : Modèle de fonctionnement d un locus CUT basé sur le locus sux de Xanthomonas campestris pv. campestris. Le saccharose va traverser la membrane externe de façon active via le TBDT SuxA ou de façon passive via une porine. Il est ensuite transporté du périplasme vers le cytoplasme par le transporteur de la membrane interne SuxC. Une fois dans le cytoplasme, le saccharose pourrait interagir avec le répresseur SuxR (permettant alors l induction des gènes sux) et servir de substrat à la saccharose hydrolase SuxB. La double flèche représente la balance entre l implication potentielle des loci CUT dans l adaptation métabolique et le contrôle de la virulence. (D après Blanvillain et al., 2007) (i) Structure 1 système PTS du mannitol MI EIIABC C B A Réaction 4 Réaction 3 Réaction 2 (ii) Structure 2 (iii) Structure 3 système PTS du glucose système PTS du mannose S Réaction 5 SP S P Réaction 1 P S S P S S S HPr B A C EI EI PEP EIIBC EIIA C B A D HPr EI EI EIICD EIIAB S Pyruvate P Figure 13 : La translocation de groupe par le système PTS, mode de transport actif de carbohydrates à travers la membrane interne des bactéries à Gram négatif. Cette figure illustre les 3 structures différentes de l enzyme EII et leur exemple représentatif chez Escherichia coli. La figure schématise également le mécanisme du transport, qui procède par une succession de 5 réactions chimiques au cours desquelles le groupe phosphore du phosphoenolpyruvate (PEP) est transféré au carbohydrate via des intermédiaires phosphorylés de EI (Enzyme I), HPr (Histidine containing Protein), EIIA (Enzyme IIA) et EIIB (Enzyme IIB). MI, Membrane Interne. (D après Postma et al., 1993 ; Blanvillain, 2007).
53 Introduction générale TBDTs). Ce CUT locus est composé d un régulateur transcriptionel, d un transporteur de la membrane interne, d une enzyme de dégradation du saccharose et d un TBDT (Blanvillain et al., 2007) (Fig. 12). D autres loci de ce type pourraient être impliqués dans l utilisation et l acquisition de divers produits issus de la dégradation de la paroi végétale (Blanvillain et al., 2007). Pour le passage de la membrane interne, de nombreuses bactéries utilisent des systèmes PTS («Sugar PhosphoTransférase Sytem») qui vont transporter et phosphoryler leur substrat de façon simultanée, en utilisant du phosphoénolpyruvate (PEP) comme donneur de phosphate. Ce sont des systèmes complexes comprenant 3 entités catalytiques essentielles nommées enzyme I (EI), enzyme II (EII) et Hpr (Heat-stable, histidine-phosphorylatable protein). La fixation du substrat à la perméase membranaire EII (fixation de très forte affinité) entraîne le transfert du groupe phosphate du PEP au carbohydrate, via des intermédiaires phosphorylés de EI, HPr, EIIA et EIIB [Fig. 13, (Postma et al., 1993)]. C est EII qui est responsable de la spécificité du système à un ou plusieurs sucres. Ce système peut également jouer un rôle dans la régulation transcriptionnelle et d autres ramifications du métabolisme (Saier and Reizer, 1994). Xcc possède un système PTS spécifique du glucose et un système spécifique du fructose (da Silva et al., 2002; de Crecy-Lagard et al., 1995). F. La régulation Chez Xcc, la synthèse d exoenzymes est finement régulée via le quorum sensing (détaillé plus loin), le métabolisme (CLP) (He et al., 2007) et des régulateurs tels que RsmA (Chao et al., 2008) ou le système à deux composant RavS/RavR (He et al., 2009). CLP est un homologue de CRP (AMP cylcic receptor protein) sensible au taux d AMP cyclique dans la bactérie et impliqué dans la répression catabolique. RsmA est une protéine de liaison à l ARN fonctionnant comme un régulateur post-transcriptionnel de nombreux processus cellulaires bactériens. Chez D. dadantii, KdgR est connu pour réguler l expression des enzymes pectinolytiques à des stades infectieux précis (Hugouvieux-Cotte-Pattat et al., 1996). Des travaux ont montré que in vitro, la fixation de KdgR à son opérateur est régulée par la présence du produit de dégradation de la pectine, le 2-keto-3-deoxygluconate (KDG) (Thomson et al., 1999). Il existe deux gènes kdgr (XCC4042 et XCC0373 incomplet) chez Xcc qui pourraient avoir le même type de fonction. 24
54 Translocon Cytosol Membrane plasmique Cellule végétale pilus Hrp Paroi végétale Corps basal Membrane externe Periplasme Membrane interne cytoplasme Bactérie Effecteturs de type III Figure 14 : Représentation schématique du système Hrp. Le système Hrp est composé de trois éléments principaux, le corps basal faisant le lien entre le cytoplasme et la membrane externe, le pilus Hrp permettant de traverser la paroi végétale, et le translocon formant un pore à travers la membrane plasmique de la cellule végétale. Ce système va permettre le passage de protéines bactériennes nommées effecteurs de type III du cytoplasme bactérien au cytosol de la cellule hôte.
55 Introduction générale 3.5 Le système Hrp et ses effecteurs Le système de sécrétion de type III ou T3SS (Type Three Secretion System) est utilisé dans deux structures majeures, le flagelle et l injectisome. Ici nous ne parlerons que du système correspondant à l injectisome. Le T3SS est présent chez de nombreux pathogènes animaux tels que Salmonella, Yersinia, E. coli et pathogènes végétaux tels que les bactéries des groupes Pseudomonas, Xanthomonas, Erwinia, Ralstonia, ou Pantoea (Cornelis, 2006). Il est nécessaire au développement de la maladie sur les plantes hôtes. Le T3SS est capable d injecter des facteurs de virulence (effecteurs de type III, T3SE) directement dans le cytosol de la cellule de l hôte. Il est activé dans certains cas, par le contact avec la cellule hôte et dépend de la voie générale de sécrétion «Sec». Un mutant dans l un des composants de ce système devient en général non pathogène et incapable d induire la HR sur une plante nonhôte ou hôte résistante. Ce système est donc également appelé système Hrp pour «hypersensitive response and pathogenicity» La structure du T3SS Le système Hrp est codé par des gènes hrp et hrc (Hypersensitive response and conserved). Les protéines Hrc sont les protéines qui forment le corps basal du T3SS et sont très conservées. Les protéines Hrp sont quant à elles secrétées par le T3SS. Le cluster hrp de Xcc s étend sur 21.7 Kb et comprend 21 gènes. Il contient 9 gènes hrc. Le corps basal se prolonge par un pilus extracellulaire creux reliant la bactérie et la cellule hôte, appelé pilus Hrp (Fig. 14). Il est composé d une protéine, la piline, comme HrpA chez P. syringae (Guttman et al., 2006), HrpY chez R. solanacearum (Van Gijsegem et al., 2000) ou encore HrpE chez X. axonopodis pv. vesicatoria (Weber and Koebnik, 2005, 2006). Son diamètre mesure environ 6 à 8 nm chez P. syringae pv. tomato (Roine et al., 1997) et il peut atteindre plusieurs µm de long chez les bactéries phytopathogènes leur permettant de traverser la paroi végétale et d atteindre la membrane plasmique. Enfin le pilus Hrp est terminé par un translocon formant un pore dans la membrane plasmique végétale permettant le passage des effecteurs de type III du pilus vers le cytosole de la cellule eucaryote. Chez X. axonopodis pv. vesicatoria, HrpF serait un composant du translocon (Buttner et al., 2002), ainsi que l harpine HrpZ chez P. syringae (Guttman et al., 2006; Weber and Koebnik, 2005) qui serait une protéine importante pour l induction des systèmes de défense de la plante. HrpF 25
56 Introduction générale montre des similarités avec les protéines HrpK de P.s syringae, NolX de Rhizobium, et PopF1/PopF2 de R. solanacearum (Alfano and Collmer, 2004; Meyer et al., 2006) Les effecteurs de type III (T3SE) Parmi les protéines transitant par les T3SS on distingue deux grands groupes de protéines, les protéines «helper» et les protéines effectrices. Les protéines «helper» vont faciliter la translocation des effecteurs. Parmis ces protéines on trouve les harpines par exemple, qui seraient impliquées dans la formation de pores dans la membrane plasmique de l hôte (HrpZ de P. syringae pv. phaseicola et PopA de R. solanacearum) (Lee et al., 2001; Racape et al., 2005) et pourraient faciliter l accès des effecteurs de type III au cytoplasme de l hôte. Il existe d autres protéines sécrétées et non transloquées telles que HrpW, HopAK1 et HopAJ1 chez P. syringae (Chang et al., 2005). HrpW et HopAK1 possèdent un domaine pectate lyase. HopAJ1 possède des homologies avec les transglycosylases (Guttman et al., 2002). Ces protéines pourraient donc être impliquées dans une dégradation localisée de la paroi végétale, permettant l accès du T3SS à la membrane plasmique. Les protéines effectrices ou effecteurs de type III (T3SE) sont des protéines qui vont être transférées dans la cellule de l hôte grâce au T3SS et qui vont interférer dans certaines fonctions de la cellule eucaryote. Nombre de ces effecteurs sont impliqués dans l altération de la réponse basale de l hôte mais peuvent également altérer la voie de signalisation hormonale de la plante, interférer dans la HR et dans la résistance non hôte [pour revue (Grant et al., 2006; Zhou and Chai, 2008)], et ce grâce à différentes fonctions et des domaines ayant des caractéristiques de protéines eucaryotes. Les effecteurs les mieux étudiés sont désignés comme des protéines d avirulence «Avr» car elles sont détectées par les plantes non-hôtes et induisent un phénotype d avirulence (voir chapitre 2) (Keen, 1990; Staskawicz et al., 1984). Cependant, de nombreux T3SE ont été identifiés grâce à leur capacité à transiter par le T3SS. Ces effecteurs ont été nommés Hop pour «Hrp outer protein» chez Pseudomonas (Alfano and Collmer, 1997), Xop pour «Xanthomonas outer protein» chez Xanthomonas (Noel et al., 2001) ou Pop pour «Pseudomonas outer protein» chez Ralstonia (qui faisait partie du groupe Pseudomonas à l époque de cette identification) (Arlat et al., 1994). Un grand nombre d effecteurs de type III a été caractérisé chez X. axonopodis pv. vesicatoria, comme la protéine XopD, étudiée récemment, qui retarde la dégénérescence des tissus de tomate infectée par Xav en interférant avec la transcription des gènes de la plante 26
57 Tableau 5. Effecteurs de type III connus chez la souche de Xanthomonas axonopodis pv. vesicatoria. (Daprès Gürlebeck et al., 2006) Nom du gène Fonctions et homologies prédites Dépendant de HrpG a GC% b Présence d'un homologue c Xac Xcc Xoo Pst Rs Eca avrbs1 fonction inconnue Références Ronald and Staskawicz (1988) ; Escolar et al. (2001) avrbs2 glycérophosphoryl-diester phosphodiesterase potentielle nd Swords et al. (1996) avrrxv cystéine protéase potentielle, famille YopJ/AvrRxv (+) + Whalen et al. (1993) ; Ciesiolka et al. (1999) xopb homologue à HopD1 (P. syringae pv. tomato ) Noël et al. (2001) xopc fonction inconnue (+) Noël et al. (2003) xopd cystéine protéase SUMO; famille C Noël et al. (2002) ; Hotson et al. (2003) xopf1 fonction inconnue nd (+) (+) + Roden et al. (2004) xopf2 fonction inconnue nd (+) (+) + Roden et al. (2004) xopj cystéine protéase potentielle, famille YopJ/AvrRxv (+) + Roden et al. (2004) xopn fonction inconnue nd Roden et al. (2004) xopo Homologue à HopK1 et AvrRps4 (P. syringae nd Roden et al. (2004) xopp fonction inconnue nd Roden et al. (2004) xopq protéine de la famille HopQ1-1, inosine-uridine nucléoside N - ribohydrolase potentielle nd Roden et al. (2004) xopx fonction inconnue nd Metz et al. (2005) ecf Facteur de chlorose précoce, homologue à HopAE1 (P. syringae pv. syringae ) Morales et al., (2005) a : co-régulation avec le système de sécrétion de type III dépendante de HrpG et HrpX (nd, non determiné). b : contenu en GC de la région codante. c : Homologie déterminée grâce aux algorithmes BLAST. (+) Homologie partielle ou homologue tronqué dans le génome correspondant (Xac : X. axonopodis pv. citri ; Xcc : X. campestris pv. campestris ; Xoo : X. oryzae pv. oryzae ; Pst : P. syringae pv. tomato ; Rs : R. solanacearum ; Eca : E. carotovora subsp. atroseptica ).
58 Introduction générale hôte (Kim et al., 2008), XopE1 et XopE2 qui sont des protéines ayant pour cible la membrane plasmique de la cellule hôte (Thieme et al., 2007), AvrXv3 qui élicite la résistance chez la tomate de lignée Hawaii 7981 (Balaji et al., 2007), AvrBS3 qui est responsable de l induction de la HR chez les cultivars de poivron non-hôtes (Bonas et al., 1989; Gurlebeck et al., 2006), et encore bien d autres dont certains sont répertoriés dans le Tableau 5. Certains de ces effecteurs sont conservés chez d autres espèces de Xanthomonas alors que d autres sont spécifiques à l espèce et même au pathovar étudié. Un nombre moins important d effecteurs spécifiques a été caractérisé chez Xcc. La protéine XopXccN, homologue à XopN de X. axonopodis pv. vesicatoria, a notamment été récemment étudiée. Elle joue un rôle dans la virulence de Xcc et son expression est régulée par HrpG et HrpX (Jiang et al., 2008). La protéine AvrAc, possédant un domaine LRR, est responsable de l avirulence de Xcc sur Arabidopsis thaliana d écotype col-0 et pourrait agir spécifiquement au niveau des vaisseaux du xylème (Xu et al., 2008). De nombreux effecteurs restent à identifier et à étudier. Plusieurs critères peuvent permettre l identification d effecteurs potentiels, comme la présence d une PIP-box (Plant Inducible Promoteur-box de séquence consensus TTCGC-N 15 -TTCGC) en amont du gène, l homologie avec d autres effecteurs connus, un profil d expression similaire à d autres effecteurs connus, ou encore la présence de domaines homologues à des domaines de protéines eucaryotes. L étude de ces effecteurs mènera à une meilleure compréhension de la mise en place du pouvoir pathogène par la bactérie et des critères de spécificité d hôte. La collection d effecteurs d une bactérie détermine sa compatibilité avec la plante et par conséquent le profil de croissance et de développement des symptômes Organisation et régulation des gènes du système Hrp Les gènes hrp et hrc codant le T3SS sont généralement regroupés en cluster Hrp ou en îlot de pathogénicité (Dobrindt et al., 2004). Cependant des gènes codant des effecteurs de type III peuvent être dispersés sur le chromosome ou les plasmides et sont généralement associés au gène codant leur protéine chaperonne (Arnold et al., 2003). Les signaux induisant l expression de ces gènes proviennent de facteurs environnementaux ou de la cellule hôte (Arlat et al., 1992; Rahme et al., 1992; Schulte and Bonas, 1992; Wei et al., 1992; Xiao et al., 1992). La régulation des gènes du système Hrp peut être divisée en deux catégories : la régulation chez Erwinia spp., Pantoea stewartii, et Pseudomonas syringae (groupe I) et la régulation chez les Xanthomonas et Ralstonia solanacearum (groupe II) (Alfano and Collmer, 1997). 27
59 Paroi cellulaire de la plante Paroi cellulaire de la plante O.M. extension N-Terminal 1 PrhA O.M. 1 PrhA? I.M. Anti-σ PrhR 2 PrhI 3 σ ECF I.M.? PrhJ Trh 4 4 HrpG HrpG 6 5 PhcA 6 HrpB HrpX 7 7 INDUCTION de la transcription des gènes hrp Figure 15 : Modèles de régulation des gènes du système Hrp chez les bactéries Ralstonia solanacearum (à gauche) et Xanthomonas (à droite). 1, PrhA est localisé dans la membrane externe et perçoit le «signal plante» pour le transférer à l anti-sigma PrhR. 3, PrhR active PrhI. 4, PrhI active la transcription de prhj. 5, PrhJ active la transcription de hrpg (cette transcription est activée par Trh chez Xanthomonas oryzae). 6, PhcA réprime l expression du gène hrpg probablement au niveau post-transcriptionnel. 7, HrpG active la transcription de hrpb chez Ralstonia solanacearum et de hrpx chez Xanthomonas spp.. 8, HrpX et HrpB reconnaissent les «PIP/hrpII-box» des promoteurs des gènes hrp et activent leur transcription. Les composés dans la partie grisée sont recquis pour l activation des gènes hrp en milieu inducteur et en présence de la plante. Les composés dans la partie non grisée sont les gènes spécifiques à R. solanacearum recquis pour l induction des gènes hrp dans la plante. (D après Tang et al, 2006)
60 Introduction générale La régulation du groupe I fait intervenir deux facteurs sigma (HrpL et RpoN), un système à deux composants (HrpS/HrpR ou GacS/GacA). Les protéines HrpS et HrpR vont former un hétérodimère permettant l induction de la transcription de hrpl via RpoN, et un système de régulation de la stabilité de l ARN hrpl (système RsmAB) et de la protéine HrpR (protéase Lon) (Tang et al., 2006). La régulation du groupe II met en œuvre un activateur de type AraC, la protéine HrpB chez R. solanacearum et HrpX chez Xanthomonas. Les gènes hrpb et hrpx sont sous le contrôle du régulateur HrpG. Chez R. solanacearum, hrpg est transcrit par un facteur sigma de type ECF, PrhI. En absence d un signal transmis par le TBDT PrhA, ce facteur sigma est retenu par un facteur anti-sigma membranaire PrhR (Fig.15). Chez Xoo le régulateur Trh (Transcriptional regulator for hrp) appartenant à la famille des régulateurs GntR, induit l expression de hrpg (Tsuge et al., 2006). Le régulateur HrpX régule l expression des gènes hrp et des effecteurs de type III en se fixant sur un motif de type PIP-box. Chez X. oryzae pv. oryzicola, un gène annoté prha codant un TBDT conventionnel non homologue au TBDT PrhA inducteur de R. solanacearum, est impliqué dans l établissement de la HR sur tabac et la virulence. De plus, le régulateur global RsmA est impliqué dans de nombreux processus cellulaires de Xcc tels que la HR sur poivrons ECW10R non-hôte, la mobilité, la production d amylase, d endoglucanase, l induction des gènes hrp et des effecteurs de type III (Chao et al., 2008). 3.6 La production d EPS De nombreuses bactéries sont capables de synthétiser des polymères de sucres qui seront ensuite sécrétés dans le milieu extracellulaire. Ces EPS resteront associés à la cellule sous forme de capsule ou d une couche plus fluide. Durant la phase de vie saprophyte ou épiphyte, ils protègent les bactéries de la dessiccation et des UV, réduisent le contact avec des macromolécules hydrophobes ou chargées et permettent une meilleure adhésion aux surfaces. La synthèse d EPS peut être contrôlée par le quorum sensing ou d autres signaux environnementaux. De nombreuses bactéries phytopathogènes comme R. solanacearum, Pantoea stewartii, et X. campestris, produisent des EPS favorisant la virulence, la colonisation, l adhésion et la survie. Le xanthane, EPS produit par Xcc, est un polymère acide composé de sous-unités pentasaccharidiques formant un squelette de cellulose avec des chaînes latérales composées 28
61 A B C 0,5 µm 0,5 µm Figure 16 : Le xanthane, un exopolysaccharide produit par Xanthomonas campestris pv. campestris. A. Colonies de Xanthomonas campestris pv. campestris cultivées sur milieu riche. L aspect mucoïde est dû à la production d exopolysaccharide (EPS) et la couleur jaune à la production d un pigment, la xanthomonadine. B. Bactéries enchassées dans leur matrice exopolysaccharidique (Photos de microscopie électronique de Jacques Vasse, LIPM). C. Unité structurelle du xanthane (D après Becker et al., 1998). Le xanthane est un polymère acide constitué d une unité pentasaccharidique répétée formant un squelette de cellulose avec des chaînes latérales composées d acide mannose(β- 1,4)glucuronique(β-1,2)mannose liées en β-1,3 au squelette. Les résidus mannose peuvent être acétylés ou pyruvylés (Jansson et al., 1975).
62 -Pyr -Ac -Ac -Pyr GumB -Ac -Ac -Ac -Ac -Pyr OM -PyrGumB OM -Ac -Ac -Pyr -Ac -Pyr -Ac -Ac -Ac -Pyr Périplasme GumD P P GumM P P P P GumH P P GumK P P GumF GumG P GumL P GumI P P GumJ -Ac -Ac -Ac -Ac -Pyr GumE Polymérase? -Ac GumC UDP-Glucuronate IM Cytoplasme UDP-Mannose UDP-Glucose NAD + NADH + H + Glucose Glucose-1-P UTP UDPG PP PPi UDPG deh XanB GTP PPi Glucose-6-P Fructose-6-P Mannose-6-P Mannose-1-P XanA PGI XanB XanA P P Polyprenol-diP GK ADP ATP Figure 17 : Voie de synthèse de Xanthane chez Xanthomonas campestris pv. campestris (Xcc). Ac, acétyl ; Pyr, pyruvyl ; PPi, pyrophosphate ; GK, glucokinase ; PGI, phosphoglucose isomérase ; UDPG-PP, UDP-glucose pyrophosphorylase ; UDPG-deH, UDP-glucose déshydrogénase. La liste des enzymes et des gènes impliqués dans cette biosynthèse n est pas exhaustive. (D après Becker et al., 1998; Vorhölter et al., 2008).
63 Introduction générale de mannose(β-1,4)acide glucuronique(β-1,2)mannose liées en β-1,3 au résidu [(Jansson et al., 1975), Fig. 16]. Deux loci sont impliqués dans la biosynthèse d EPS chez Xcc : une région de 35,3 Kb et le groupe de gènes gum (Capage et al., 1987; Hotte et al., 1990; Vanderslice et al., 1990 ; Vorholter et al., 2008). Le groupe de gènes gum est composé de 12 gènes (gumb à gumm, Fig. 17). Il est responsable de l assemblage séquentiel et de la polymérisation des unités pentasaccharidiques, ainsi que du largage du polymère dans le milieu (Ielpi et al., 1993). Certains gènes comme xana et xanb, localisés dans la région de 35.3 kb, sont responsables de la biosynthèse des sucres précurseurs. Ces protéines sont impliquées dans la synthèse des EPS et des lipopolysaccharides (LPS) (Koplin et al., 1992). De plus, les produits des gènes rpf, clp et pigb sont impliqués dans la régulation de la production d EPS (voir paragraphe 4.4.7). Enfin six nouveaux gènes (XCC3741 à XCC3747 dans la souche ATCC33913 et XC_3811 à XC_3816 dans la souche 8004) sont impliqués dans la production d EPS et dans la virulence (Lu et al., 2007). Les EPS jouent un rôle important durant l infection. Pour preuve, un mutant altéré dans la production de xanthane montre une virulence réduite in planta (Katzen et al., 1998; Newman et al., 1994). Le xanthane permet d augmenter la virulence des bactéries en supprimant la formation de callose par la plante hôte (Yun et al., 2006), et en masquant les bactéries afin d empêcher leur reconnaissance par les systèmes de défense de l hôte (Alvarez, 2000). Les EPS sont également impliqués dans la formation de biofilm protégeant Xcc de la dessiccation, des UV et de composés antimicrobiens lors de la phase de vie épiphyte (Denny, 1995). Le xanthane n est pas requis pour l attachement de Xcc aux surfaces, mais dans la formation d agrégats (Crossman and Dow, 2004). Chez Xcc le passage de la forme non mobile virulente vers la forme mobile avirulente est concomitant avec l arrêt de production d EPS (Kamoun and Kado, 1990). Le xanthane est également très important en industrie et en biotechnologie. Il est non toxique et ne cause aucune irritation au niveau des yeux et de la peau (Kennedy and Bradshaw, 1984). La gomme xanthane est très stable et résistante à la température, au ph et à l action d enzymes de dégradation (Leela and Sharma, 2000). Grâce à ces propriétés, elle est utilisée dans les industries alimentaires, pharmaceutiques, cosmétiques, et textiles. De plus, la forte viscosité et la solubilité de ce polymère dans l eau permet également son utilisation dans l industrie pétrolière pour une meilleure récupération du pétrole (Garcia-Ochoa et al., 2000). 29
64 A O H CH 3 C C C CH 3 B O OH O H H butyrolactone O acide cis-11-methyl-2- dodecenoique Figure 18 : Structures des molécules signales des deux systèmes de quorum sensing de Xanthomonas campestris pv. campestris. A. Facteur diffusible (DF), d après Chun et al., B. Facteur signal diffusible (DSF), d après He and Zhang, Faible densité cellulaire Forte densité cellulaire OM IM ME MI Précurseur DSF RpfB? OM IM ME MI RpfF RpfB? Biosynthèse de DSF RpfF RpfG Virulence et adaptation P P RpfC P P RpfG Virulence et adaptation RpfC Figure 19 : Modèle de la transduction du signal DSF chez Xanthomonas campestris pv. campestris. Les protéines RpfB et RpfF sont impliquées dans la synthèse du DSF. A faible concentration cellulaire, le senseur RpfC forme un complexe avec RpfF, la protéine de synthèse du DSF, limitant ainsi la synthèse de DSF. Les flèches en pointillés représentent le taux basal de signalisation. A forte concentration cellulaire, DSF interagit avec RpfC et induit un changement conformationnel de RpfC suivi d une autophosphorylation menant au relargage de RpfF et au phosphorelais du senseur vers le régulateur RpfG. Il y a alors augmentation de la synthèse de DSF et génération d un signal fort d induction du régulon DSF.?, précurseur inconnu ; ME, membrane externe ; MI, membrane interne ; DSF, facteur signal diffusible. (D après He and Zhang, 2008)
65 Introduction générale 3.7 Le quorum sensing Le quorum sensing est un système qui permet à une bactérie de percevoir la densité bactérienne (le nombre de ses congénères présents). Il repose sur la capacité des bactéries à communiquer entre elles en utilisant des signaux moléculaires appelés auto-inducteurs. Le quorum sensing requiert une croissance dans un environnement confiné où la densité de la population augmente et la concentration de l'auto-inducteur va pouvoir dépasser un seuil critique qui sera alors perçu par les bactéries qui le produisent, entraînant l induction de fonctions cellulaires spécifiques. Les fonctions régulées par quorum-sensing sont très diverses. Elles incluent le pouvoir pathogène chez E. carotovora par exemple (Loh et al., 2002), le transfert conjugatif de plasmides chez Agrobacterium (Oger and Farrand, 2002) ou chez différents Rhizobium (McAnulla et al., 2007), la production d'antibiotiques ou d'antifongiques, l'apparition de la compétence, ou la mise en place de flagelles, la synthèse d EPS, la formation de biofilm, la production d enzymes de dégradation, de sidérophores ou de pigment, la bioluminescence chez Vibrio fisheri et la réponse aux stress (Von Bodman et al., 2003). Cette communication inter bactéries contribue à la synchronisation de l'expression de gènes particuliers au sein d'une population bactérienne et participe à l adaptation à la disponibilité en nutriments, la compétition contre d autres microorganismes ou encore la mise en place de l infection par les bactéries pathogènes qui doivent coordonner l expression des facteurs de virulence pour échapper au système immunitaire de l hôte (Gonzalez and Keshavan, 2006). Parmi les auto-inducteurs identifiés, les N-acyl homoserine lactone (AHLs) sont les mieux étudiés [pour revue (Dong et al., 2007; Williams, 2007)]. Il existe cependant d autres types de signaux tels que les quinolones et les dipeptides cycliques connus chez P. aeruginosa (Holden et al., 1999; Pesci et al., 1999), deux molécules de bas poids moléculaire chez X. campestris [voir Chapitre 4 (Poplawsky et al., 1998)], et un dérivé d acide gras chez R. solanacearum (Flavier et al., 1997). Xcc possèdent deux systèmes de quorum sensing, jouant un rôle dans la synthèse d EPS et la régulation de l expression de facteurs de virulence comme la synthèse d exoenzymes, la formation de biofilm, l acquisition du fer ou la survie lors de la vie épiphyte (Fig. 20). Le premier système de quorum sensing implique un facteur diffusible (DF), codé par le gène pigb, qui joue un rôle important dans la régulation de la production de xanthomonadine (Poplawsky and Chun, 1997, 1998). D après des analyses MS, le DF aurait une structure de butyrolactone (Fig. 18) (Chun et al., 1997). Ceci doit être vérifié par 30
66 Signal hôte Signaux environnementaux DSF DF P Protéines GGDEF EAL HD-GYP RpfC RpfG P P P RpfF Biosynthèse de DSF di-gmp cyclique 2 GMPs Clp Biofilm Zur FhrR Capture de fer Cycle TCA Respiration aérobie Résistance aux drogues Détoxification Enzymes extracellulaires Synthèse d EPS Protéines du métabolisme Protéines membranaires Gènes du flagelle Système Hrp Protéines ribosomiques Pigment Synthèse d EPS Figure 20 : Représentation schématique du quorum sensing chez Xcc. Le quorum sensing est impliqué dans la régulation de nombreux processus cellulaire chez Xcc. Il implique un système de phosphorelais à deux composant RpfC/RpfG, un métabolite secondaire, le di-gmp et de nombreux régulateurs transcriptionel. Seules les protéines possédant le domaine métabolique du di-gmp cyclique (GGDEF, EAL, et HD-GYP) peuvent moduler le taux de di-gmp cyclique et agir sur le régulon DSF via les régulateurs CLP, Fhr et Zur. CLP est un homologue de la protéine CRP (camp receptor protein) d E. coli impliquée dans la répression catabolique, FhrR est un homologue du répresseur Fur impliqué dans la régulation de l acquisition du fer et Zur est initialement impliqué dans la régulation de l acquisition du zinc. Les flèches pleines représentent une interaction protéine-protéine ou une modulation directe du signal ; les flèches en pointillé montrent une voie de régulation potentielle. (D après He and Zhang, 2008)
67 Introduction générale résonance magnétique nucléaire (NMR) ou par synthèse chimique. Le gène XCC4014 de la souche ATCC33913 codant une protéine similaire à une déoxygénase pteridine dépendante est nécessaire à la production du signal DF (Poplawsky et al., 2005). Le second système de quorum sensing implique la production d un facteur signal diffusible (DSF) (Barber et al., 1997), qui est caractérisé comme étant un acide cis-11-methyl-2-dodecanoique (Fig. 18) (Wang et al., 2004). Le groupe de gènes rpfabcdefghi (pour «regulation of pathogenicity factors») est indirectement impliqué dans la production d EPS et d enzymes extracellulaires (Tang et al., 1991). Parmi ce groupe, l opéron rpfghc code un système à deux composants impliqué dans la transduction du signal DSF (Fig 19). RpfC est une protéine hybride avec un domaine de type senseur à kinase et un domaine de type régulateur de réponse et un domaine de type histidine phosphotransférase (HPt) (Slater et al., 2000; Tang et al., 1991). RpfH est homologue au domaine senseur transmembranaire de RpfC et pourrait stabiliser RpfC dans la membrane (Slater et al., 2000). Le régulateur de réponse RpfG possède un domaine d entrée typique couplé à un domaine hydrolase (HD-GYP) homologue aux phosphodiestérases impliquées dans la signalisation du diguanylate cyclique. Par conséquent, RpfG pourrait contrôler la synthèse d EPS et d exoenzymes de façon indirecte en modifiant le taux de di- GMP cyclique (par action sur la synthèse et le recyclage de ce composé) (Crossman and Dow, 2004 ; Dow et al., 2006; Fouhy et al., 2006; Ryan et al., 2006a; Ryan et al., 2006b; Ryan et al., 2007). De plus une mutation dans rpfg ou rpfc diminue l expression du répresseur catabolique CLP. Ce dernier pourrait donc avoir un rôle important dans la voie DSF (He et al., 2007). A côté de cet opéron on trouve les gènes rpfb et rpff qui sont impliqués dans la synthèse du DSF. Une mutation dans rpff réduit la production d EPS et d enzymes extracellulaires (Barber et al., 1997; He et al., 2006; Tang et al., 1991). RpfF possède des similarités de séquence avec une enoyl-coa hydratase et RpfB est une CoA ligase agissant sur les acides gras à longues chaînes (Barber et al., 1997). L action de rpff est réprimée par RpfC (Crossman and Dow, 2004). Le régulon DSF de Xcc contient 165 gènes distribués sur tout le génome (He et al., 2006). Parmi eux, plus de 80% sont activés via le DSF et 20% sont réprimés. Le produit des gènes de ce régulon est réparti en douze groupes fonctionnels (Fig. 20) : (1) les enzymes extracellulaires, (2) la synthèse et la sécrétion de lipopolysaccharides et d EPS, (3) la résistance aux drogues et la détoxification, (4) la biosynthèse du flagelle, la mobilité et le chimiotactisme, (5) la HR et le système Hrp, (6) l acquisition du fer, (7) le métabolisme des protéines, (8) le cycle de l acide tricarboxylique (TCA), (9) la respiration aérobie, (10) les régulateurs de transcription, (11) les composés de la membrane et les transporteurs et (12) le 31
68 Introduction générale métabolisme des acides gras et autres (He et al., 2006). La voie DSF aurait également un rôle important dans la régulation de la formation de biofilm (Crossman and Dow, 2004). L implication de la voie DSF dans toutes ces fonctions suggère que le quorum sensing n est pas seulement essentiel dans la virulence de Xcc mais également le maintien de ses compétences écologiques. DF et DSF sont des signaux distincts tant par leur différence d activité biologique que par leur mobilité chromatographique, leur structure biochimique et leurs gènes de biosynthèse (Barber et al., 1997; Poplawsky et al., 2005; Poplawsky et al., 1998; Wang et al., 2004). Le fait que la production d EPS soit influencée par ces deux molécules signales laisse penser que les deux systèmes de quorum sensing de Xcc pourraient interagir l un avec l autre au niveau de certaines jonctions de régulation. L utilisation de deux systèmes de quorum sensing permet une plasticité de réponse à différents signaux environnementaux. 3.8 Les phytotoxines De nombreuses bactéries pathogènes chez les animaux ainsi que les champignons produisent des toxines nocives pour leur hôte. Cependant il semble que ce phénomène soit moins courant ou moins documenté chez les bactéries phytopathogènes (Hogenhout and Loria, 2008; Strobel, 1977, 1982). Les phytotoxines bactériennes les plus connues sont celles produites par P. syringae, comme la coronatine qui mime l action du jasmonate et induit la chlorose des tissus de la plante ainsi que l ouverture des stomates (Melotto et al., 2008), et qui est corégulée avec les gènes hrp ; la syringomycine et la syringopeptine qui forment des pores dans la membrane plasmique des cellules végétales et induisent une fuite d électrolytes ; la tabtoxine et la phaseolotoxine qui sont de bons agents antimicrobiens et antifongiques (Bender et al., 1999). E. carotovora possède un gène codant un peptide non ribosomique (NRP) similaire à celui codant la syringomycine de P. syringae et un cluster de gènes similaire au cluster cfa de Pseudomonas, codant les gènes de synthèse de la coronatine (Bell et al., 2004). Certaines espèces de Xanthomonas produisent des phytotoxines. X. albilineans par exemple, produit l albicidine, qui bloque la réplication chez une large gamme de bactéries à Gram positif et négatif et dans les plastes des cellules de la canne à sucre (Birch and Patil, 1985; Birch and Patil, 1987). L albicidine joue un rôle important dans l invasion systémique 32
69 Figure 21 : Illustration des interactions entre Xanthomonas campestris pv. campestris et une plante-hôte. EPS, Exopolysaccharides ; FAAH, Fatty Acid Hydroxylase ; hrp, hypersensitive response and pathogenicity genes ; LPS, Lipopolysaccharides ; ROS, Reactive Oxygen Species ; R-protein, Resistance protein ; Xps, Xanthomonas protein secretion. (Extrait de Qian et al., 2005).
70 Introduction générale et le développement des symptômes sur la canne à sucre (Zhang and Birch, 1997; Zhang et al., 1999). De plus, des gènes syr similaires aux gènes de synthèse de la syringomycine de P. syringae sont présents chez X. axonopodis pv. citri (Etchegaray et al., 2004). Les processus impliqués dans la mise en place du pouvoir pathogène de Xcc sont récapitulés dans la figure
71 ETUDE DE L ACQUISITION ET DE L UTILISATION DU N-ACETYLGLUCOSAMINE
72 Etude de l acquisition et de l utilisation du N-acétylglucosamine 4 Chapitre 1. Introduction au travail de thèse Les bactéries phytopathogènes possèdent des facultés adaptatives qui leur permettent non seulement d'infecter les plantes hôtes mais aussi de survivre dans l'environnement entre deux cycles infectieux. Ces propriétés adaptatives reposent sur la perception de signaux spécifiques et sur la mise en place de programmes génétiques finement régulés. L'étude et la caractérisation des mécanismes contrôlant le déclenchement de ces programmes de régulation devrait nous permettre de mieux comprendre le cycle de vie des pathogènes. Une étude menée par Ashby en 2004 sur 105 espèces bactériennes a montré une relation entre le nombre de gènes codant des régulateurs de réponse et la complexité du mode de vie de la bactérie (Ashby, 2004). Afin d étudier l interaction de Xcc avec sa plante hôte, l équipe s intéresse à tous les mécanismes permettant à Xcc de s adapter à son milieu, notamment lors du processus d infection. Pour cela, une étude systématique in silico des gènes régulateurs et récepteurs de la souche ATCC33913 de Xcc a été débutée dans l équipe avant mon arrivée. Cette étude a permis d identifier 524 gènes codant des protéines intervenant potentiellement dans la perception et la régulation de signaux, soit 12 % des protéines potentielles de Xcc. Parmi ces gènes on trouve 162 gènes codant des récepteurs potentiels et 362 gènes codant des régulateurs potentiels. Dans le cadre de ma thèse, j ai débuté une étude par mutagenèse systématique des régulateurs de transcription de la famille LacI de Xcc via l insertion d un vecteur suicide. Au cours de la caractérisation de la virulence de ces différents mutants, j ai identifié un mutant incapable de développer les symptômes de la maladie sur une plante hôte. Ce mutant possède une insertion polaire dans le répresseur de type LacI codé par le gène XCC3412. Ce répresseur est localisé au sein d un cluster de gènes potentiellement impliqués dans l acquisition et l utilisation du N-acétylglucosamine (GlcNAc ou NAG). Nous avons donc poursuivi l étude de ce locus, de son implication dans l adaptation de Xcc à la plante et dans la mise en place du pouvoir pathogène. Avant de vous décrire le travail réalisé au cours de ma thèse, je me propose de décrire quelques rôles du GlcNAc dans le monde du vivant et notamment son utilisation chez les bactéries. 34
73 A 4 c HO 6 CH 2 OH 5 c OH c OH O 2 c c 3 O c 1 HN CH 3 B OH CH 2 OH O OH O NHCOCH 3 GlcNAc O MurNAc O H N L-Ala O O NHCOCH 3 O OH O N H Glu O H N O D-Ala N H O O OH meso-dap OH C NH 2 MurNAc A MurNAc GlcNAc G D A A GlcNAc MurNAc G D GlcNAc A MurNAc A GlcNAc G D MurNAc A A GlcNAc MurNAc G D A GlcNAc A A G MurNAc G D D MurNAc A A A G D A A G D A MurNAc A G D A Figure 22 : Le peptidoglycane. A. Molécule de β-d-n-acétylglucosamine (GlcNAc ou NAG) B. Structure de la muréine, monomère de peptidoglycane. Le Peptidoglycane (PG) est composé d unités N-acétylglucosamine (GlcNAc) et d unités acide N- acétylmuramique (MurNAc) reliées par des liaisons β-1,4. Le MurNAc est lié à une chaîne peptidique composée d alanine (Ala ou A), d acide glutamique (Glu ou G) et d acide diaminopimélique (Dap ou D) chez les bactéries Gram -. C. Les Chaînes de peptidoglycanes sont reliées entre elles par des ponts transpeptidiques (lignes rouges) reliant le Dap au dernier résidus Ala de la chaîne suivante. (D après Cloud-Hansen et al., 2006)
74 Etude de l acquisition et de l utilisation du N-acétylglucosamine 5 Chapitre 2. Le N-acétylglucosamine dans le monde du vivant Le N-acétylglucosamine (GlcNAc) (Fig. 22A) est un sucre aminé ayant un rôle important dans de nombreux processus cellulaires de la bactérie jusqu à l homme. Il peut faire partie d éléments structuraux des organismes, être impliqué dans la modification postraductionnelle des protéines via la glycosylation ou être utilisé comme source d énergie par le métabolisme. Il peut également être un composant de molécules signales comme c est le cas pour les facteurs Nod produits par des bactéries symbiotiques. Dans ce chapitre, je détaillerai le rôle du GlcNAc comme élément de structure et de modification protéique. 5.1 Le GlcNAc, un élément de structure La paroi bactérienne En 1884, Christian Gram montre, grâce à la coloration qui porte son nom, que les bactéries se divisent en deux groupes : les bactéries de coloration de Gram positives (ou Gram +, de couleur violette) et les bactéries de coloration de Gram négatives (ou Gram -, qui sont de couleur rose). Cette différence de coloration à permis de définir deux types de parois (Gram + et Gram - ) qui possèdent une structure commune formant un réseau autour de la membrane plasmique, le peptidoglycane (PG) (Fig. 22B et 22C). A. Le peptidoglycane Le PG est responsable de la forme et de la taille spécifique de la bactérie et permet l ancrage de nombreuses protéines (Dramsi et al., 2008). Il a pour rôle de préserver l intégrité cellulaire de la bactérie. Une mutation dans un gène de biosynthèse du PG ou sa dégradation mène à une lyse cellulaire. Comme son nom l'indique, le monomère de PG est constitué d'une partie glucidique avec une alternance de GlcNAc et d acide N-acétylmuramique (MurNAc) reliés par des liaisons osidiques β-1,4 et d'une partie peptidique composée de quatre acides aminés (Fig. 22B). Le groupement D-lactoyl du résidu MurNAc est relié à la chaîne peptidique composée le plus souvent par du L-Ala-γ-D-Glu-meso-Dap (ou L-Lys)-D-Ala-D- 35
75 A A D GlcNAc Peptidoglycane A G MurNAc A A A D GlcNAc A G D GlcNAc G P P P A MurNAc P P 3 A MurNAc P P Périplasme C 55 -PP? UppP C 55 -P Polymérases (PBPs) MraY MurG Lipide I 2 Lipide II Membrane UppS P P P A G D A UDP MurNAc UM P P P MurNAc UDP GlcNAc P UDP P MurNAc Cytoplasme A A A A D A G D A G GlcNAc A A Fru-6-P Gln GlmS Glu-6-P D-glutamine GlmM Glu-1-P 1 GlcNAc-1-P UDP UDP GlmU GlmU MurA GlcNAc A G D A A UDP MurNAc MurNAc GlcNAc MurF A G D A D-Ala-D-Ala UDP MurB UDP MurNAc MurE Dap A G D MurC UDP UDP A MurNAc MurNAc MurD Acetyl-CoA UDP PEP NADPH L-Alanine A G G D C 55 -PP : undecaprenyl pyrophosphate C 55 -P : undecaprenyl phosphate Gln : Glutamine PEP : PhosphoEnolPyruvate Dap : d acide Acide diaminopimélique Fru-6-P Glu-6-P Glu-1-P UDP GlcNAc Fructose-6-P Glucosamine-6-P Glucosamine-1-P UDP-GlcNAc enolpyruvate Figure 23 : Voie de biosynthèse du peptydoglycane (PG). La voie de biosynthèse du PG peut être divisée en trois grandes étapes. (1) La synthèse des précurseurs (UDP-GlcNAc et UDP-MurNAc-pentapeptide, zone grisée). (2) Le transfert des précurseurs au transporteur lipidique (ou lipide donneur) et le passage vers le périplasme. (3) Le transfert du monomère à la chaîne de peptidoglycane en cours de synthèse. (D après Barreteau et al., 2008; Bouhss et al., 2008)
76 Etude de l acquisition et de l utilisation du N-acétylglucosamine Ala (Fig. 22) (Vollmer et al., 2008a). Le dernier résidu D-Alanine est perdu au cours de la formation du PG. Le réseau de PG est constitué de polymères de PG. Ces polymères appelés muréines, sont reliés entre eux par des liaisons transpeptidiques (Vollmer et al., 2008a). Il semblerait que toutes les bactéries partagent les mêmes étapes de synthèse du PG qui sont au nombre de trois (Fig. 23) [pour revues (Barreteau et al., 2008; Bouhss et al., 2008)] : (1) les précurseurs UDP-MurNAc-pentapeptide et UDP-GlcNAc sont synthétisés dans le cytoplasme. La synthèse de l UDP-GlcNAc est différente entre les procaryotes et les eucaryotes. Chez les bactéries, une seule enzyme, GlmU, permet le passage du glucosamine- 1-phosphate à l UDP-GlcNAc alors que l action de deux enzymes est nécessaire à cette transformation chez les eucaryotes (Barreteau et al., 2008). (2) Après avoir été transférés sur un transporteur lipidique (undecaprenyl pyrophosphate), le monomère de PG est transloqué sur la face externe de la membrane plasmique. (3) Le disaccharide-peptide est attaché au polymère de PG en cours de synthèse par un transfert glycosidique et une réaction de transpeptidation. Bien que ces étapes de synthèse soient conservées, il existe un certain degré de variation possible au niveau de la composition de la chaîne peptidique et/ou au niveau du pont peptidique. De plus, des modifications secondaires au niveau du polymère de PG comme la N-deacétylation, la O-acétylation et la N-glycolylation sont fréquemment observées dans les PG matures (Vollmer et al., 2008a), notamment chez les bactéries pathogènes. Ces modifications pourraient limiter l effet des antibiotiques (notamment des β-lactamines comme la pénicilline ayant pour cible le PG) et des lysozymes (enzymes présente dans les larmes, la salive..., capables d'hydrolyser les liaisons osidiques du PG). Elles pourraient également empêcher la reconnaissance du PG par les systèmes de défense de l hôte. En effet, le PG est un MAMPs (voir introduction générale Chapitre 2) fréquemment reconnu au cours des interactions entre bactéries et mammifères (Cloud-Hansen et al., 2006) ainsi qu au cours des interactions avec les plantes. Il a été montré récemment que des fragments de PG d A. tumefaciens et de X. campestris induisent les réponses de défenses basales chez Arabidopsis thaliana (Erbs et al., 2008). B. Le recyclage du peptidoglycane Les bactéries sont généralement capables de fragmenter, d importer et de réutiliser tous les éléments constituant le PG (pour revue (Park and Uehara, 2008)). E. coli par exemple 36
77 Peptidoglycane γ-d-mesodapendopeptidase Glucosaminidase D,D-endopeptidase Amidase N-acetylmuramyl-L-alanine Muramidase ou Transglycosylase lytique N-acétylglucosamine Acide N-acétylmuramique Acide N-acétyl-anhydromuramique D,D-carboxypeptidase Alanine D-glutamate ou iso-glutamine Acide diaminopimélique (Dap) Figure 24 : Représentation schématique de l activité d enzymes clivant le peptidoglycane. Les ciseaux représentent les sites de coupure. Ceci n est pas une représentation exhaustive des activités enzymatiques clivant le PG. On trouve les trois grandes classes d enzymes de dégradation du PG décrites chez Escherichia coli, les endopeptidases (en rouge), les amidases (en bleu) et les glucosaminidases. (en orange). (Daprès Boneca, 2005) Tableau 6. Enzymes impliquées dans le recyclage du peptidoglycane d Escherichia coli. (D après Park et Uehara, 2008) Gènes Activité Localisation Référence(s) ampg GlcNAc-anhMurNAc perméase Membrane intene (Cheng and Park, 2002) ; (Jacobs et al., 1994) ampd anhmurnac-l-ala amidase Cytoplasme (Holtje et al., 1994) ; (Jacobs et al., 1994) mpl (yjfg ) UDP-MurNAc:L-Ala--D-Glu-Dap ligase Cytoplasme (Herve et al., 2007) ; (Mengin-Lecreulx et al., 1996) ldca (f304 gene) LD-Carboxypeptidase Cytoplasme (Templin et al., 1999) ; (Ursinus et al., 1992) mpaa (ycji ) γ-d-glu-dap amidase Cytoplasme (Uehara and Park, 2003) ycjg L-Ala-D/L-Glu épimérase Cytoplasme (Schmidt et al., 2001) nagz (ycfo ) β-n -Acetylglucosaminidase Cytoplasme (Cheng et al., 2000) nagk (ycfx ) GlcNAc kinase Cytoplasme (Uehara and Park, 2004) anmk (ydhh ) anhmurnac kinase Cytoplasme (Uehara et al., 2005) murq (yfeu ) MurNAc-6-P éthèrase Cytoplasme (Jaeger et al., 2005) ; (Uehara et al., 2006) amid (ybjr ) anhmurnac-l-ala amidase Membrane externe (Uehara and Park, 2007) mppa protéine de liaison au peptide muréique Périplasme (Park et al., 1998)
78 Etude de l acquisition et de l utilisation du N-acétylglucosamine recycle environs 45 % de son PG à chaque génération (Goodell, 1985). Dans un premier temps, E. coli va dégrader le réseau de PG à l aide de trois classes d enzymes capables de couper les liaisons du PG (Fig. 24). La classe 1 regroupe les endopeptidases comme les PBP4 (penicillin-binding protein 4), PBP7, et MepA qui clivent le pont transpeptidique entre deux polymères de PG. La classe 2 comprend trois MurNAc-L-Ala amidases AmiA, AmiB et AmiC. Ces trois enzymes sont localisées dans le périplasme et participent à la séparation cellulaire au cours de la division. Elles clivent la liaison entre le peptide et le MurNAc du PG intacte (Heidrich et al., 2001; Priyadarshini et al., 2007). Une quatrième amidase, AmiD, présente dans la membrane externe, a été récemment identifiée (Uehara and Park, 2007). Les amidases vont larguer des tri-, tetra- et pentapeptides qui vont diffuser en dehors de la cellule ou entrer dans le cytoplasme via le système MppA-OppBCDF. MppA est une protéine périplasmique qui est requise dans la capture des muro-tripeptides (Park et al., 1998), tandis que OppBCDF sont des composants d un transporteur d oligopeptides ATP-dependant (Pearce et al., 1992). Il semblerait que MppA transporte le tripeptide vers les Opp membranaires pour le transport vers le cytoplasme. Enfin, la classe 3 regroupe les glucosaminidases et les transglycosylases lytiques. Les transglycosylases lytiques vont cliver le polymère de PG entre le carbone 1 du MurNAc et le carbone 4 du GlcNAc et former du MurNAc anhydre (anhmurnac) (Holtje et al., 1975). La transglycosylase principale, responsable du recyclage du PG est SltY, une enzyme soluble du périplasme. Le recyclage du PG débute donc par l action des tranglycosylases et des endopeptidases, menant à la production de monomères de muropeptides anhydres (GlcNAcanhMurNAc-peptides) (Glauner, 1988). Neuf enzymes, une perméase et une protéine de liaison périplasmique ont été identifiées chez E. coli comme nécessaires au recyclage des produits de dégradation de ces muropeptides anhydres (Tableau 6, Fig. 25). Ces molécules vont être spécifiquement prises en charge par la perméase AmpG (Fig. 25) et être transportés vers le cytoplasme (Jacobs et al., 1994). Cette perméase localisée dans la membrane interne est essentielle au recyclage du PG. Elle appartient à la super famille des major facilitator (MFS) et est capable de transporter d assez larges molécules (Park and Uehara, 2008), grâce à l énergie protomotrice (Cheng and Park, 2002). Cette perméase transporte spécifiquement le disaccharide GlcNAc-anhMurNAc lié ou non au peptide (Park and Uehara, 2008). D autre part, le transporteur de la membrane interne MurP est impliqué dans le transport d acide N- acétylmuramique-6p et d acide N-acétylmuramique anhydre. 37
79 Membrane externe Dégradation du peptidoglycane (Endopeptidases, Amidases, Glucosaminidases, transglycosylases) peptidoglycane Membrane interne Lipide I Synthèse Lipide II MurP AmpG MppA Opp UDP-MurNAc MraY MurG D-lactate GlcNAc-anhMurNAc L-Ala GlcNAc-6-P MurNAc-6-P L-Ala D-Glu MurQ AnmK D-Glu meso-dap NagK ATP,Mg meso-dap D-Ala GlcNAc anhmurnac D-Ala D-Ala NagZ MurF GlcNAc-anhMurNAc AmpD D-Ala D-Ala UDP-MurNAc L-Ala LdcA Mpl D-Glu D-Ala L-Ala D-Glu UDP-MurNAc meso-dap meso-dap Synthèse MpaA meso-dap L-Ala D-Glu YcjG L-Ala L-Glu cytoplasme L-Ala PepD + L-Glu Figure 25 : Recyclage du peptidoglycane chez Escherichia coli. Le peptidolycane (PG) est dégradé par des enzymes périplasmiques dont la principale est la transglycosylase SltY. Les produits de dégradation sont ensuite importés dans le cytoplasme par les transporteurs AmpG, MurP, MppA/OppBCDF. Le peptide une fois relargué via AmpD sera soit découpé en acides aminés libres soit greffé à l UDP-MurNAc via la ligase Mpl pour intégrer la voie de biosynthèse du PG. Le disaccharide GlcNAc-anhMurNAc va être transformé en GlcNAc-6-P qui sera utilisé soit pour la synthèse de nouvelles molécules de peptidoglycane soit pour produire de l énergie par la voie de la glycolyse. MurNAc, Acide N-acétylmuramique ; anh, anhydre ; GlcNAc, N-acétylglucosamine ; Ala, Alanine ; Glu, Glutamine ; meso-dap, Acide meso-diaminopimélique. (Daprès Park and Uehara, 2008)
80 Etude de l acquisition et de l utilisation du N-acétylglucosamine Ce recyclage va générer des molécules qui seront soit utilisées pour la synthèse de nouveaux polymères de PG, soit comme source d énergie. Une fois dans le cytoplasme (Fig. 25), la carboxypeptidase LdcA va cliver la D-Ala du tetrapeptide pour former un MurNActripeptide (Templin et al., 1999). AmpD, une anhydro-n-acétylmuramyl-l-ala amidase qui va cliver le muropeptide anhydre au niveau de la liaison anhmurnac-l-ala produisant un peptide et un disaccharide (Jacobs et al., 1995). AmpD va cliver les anhmurnac-tripeptides mais pas les UDP-MurNAc-pentapeptides nécessaires à la synthèse du PG. Le peptide L-Alaγ-D-Glu-meso-Dap peut être directement réutilisé pour la synthèse de PG (Goodell, 1985). Ce tripeptide va être utilisé par la ligase Mpl pour former de l'udp-murnac-tripeptide, un intermédiaire classique de la synthèse du PG. Il existe cependant une seconde voie où l amidase MpaA et l épimérase du L-Ala-D/L-Glu (YcjG) vont libérer les acides aminés du peptide sous forme simple pour les réutiliser. En parallèle, le disaccharide GlcNAc-anhMurNAc est également recyclé. Une β-nacétylglucosaminidase, NagZ chez E. coli, va libérer le GlcNAc du disaccharide. Le GlcNAc et le MurNAc ainsi obtenus vont tous deux être convertis en GlcNAc-6-phosphate qui sera soit utilisé pour former de l UDP-GlcNAc soit utilisé dans la voie de la glycolyse (ceci sera décrit en détail ultérieurement). Comme nous l avons vu dans l introduction générale, le muropeptide peut être potentiellement reconnus par les systèmes de défense de l hôte au cours du processus d infection. Il est donc d autant plus important pour les bactéries pathogènes de posséder un système efficace d import des produits de dégradation du PG afin d éviter que ces molécules ne soient reconnues par l hôte (Boneca, 2005; Chaput and Boneca, 2007; Cloud-Hansen et al., 2006). D autre part il a été montré que les fragments de PG provenant de ce recyclage sont des facteurs de virulence chez certaines bactéries. Par exemple, le muro-tétrapeptide de Bordetella pertusis, autrement appelé TCT (Trachéal CytoToxine), est responsable de la destruction de cellules épithéliales ciliées du système respiratoire (Goldman et al., 1982). Un mutant ampd chez R. solanacearum altéré dans le recyclage du PG, n est plus capable de développer le flétrissement bactérien de la tomate. Cependant, les mécanismes impliqués dans cette absence de virulence ne sont pas connus (Park, 1995). Une mutation d une transglycosylase d E. amylovora diminue la virulence de la bactérie (Zhao et al., 2005). La croissance du mutant in planta est comparable à la souche sauvage au cours des deux premiers jours puis diminue légèrement par la suite. 38
81 A Acides téichoïques Acides lipotéichoïques Peptidoglycane Paroi Espace Périplasmique Membrane plasmique Protéine intrinsèque Phospholipides B Porine Protéine intrinsèque LPS polysaccharide Lipide A Lipoprotéine de Braun Peptidoglycane Membrane externe Périplasme Membrane plasmique Protéine intrinsèque Phospholipides Figure 26 : Représentation schématique des parois bactériennes. A. Paroi de bactéries à Gram positif. B. Paroi de bactéries à Gram négatif. Images : observation au microscope optique de colorations de Gram de bactéries Gram - et Gram +. Source :
82 Gal Gal NGa Gal NGa Gal NGa NAG n = 4-40 Antigène O NGa NAG Glc NAG + H 3 N Gal Glc Hep O- Hep O O O P P O O O - KDO O O O - P O O HO O O HO O Gal NH O O O Hep OH P O O - KDO O O KDO O P O O - + NH 3 O HO O O O- O O O - O NH P P OO O O OH O O Partie centrale, Oligosaccharide conservé Extérieur de la cellule Intérieur de la cellule Lipide A Figure 27 : Structure du lipopolysaccharide (LPS) de E. coli O111:B4. Hep : L-glycerol-D-manno-heptose ; Gal : galactose ; Glc : glucose ; KDO : acide 2- céto-3-déoxyoctonique ; NGa : N-acétyl-galactosamine ; NAG : N-acétylglucosamine. (D après Magalhães et al., 2007)
83 Etude de l acquisition et de l utilisation du N-acétylglucosamine Enfin les fragments de PG peuvent servir de molécule signale indiquant à la bactérie la présence d antibiotique de type β-lactame produit par d autres microorganismes (Hanson and Sanders, 1999). Ce signal est généré par l action de l antibiotique lui-même. Les fragments sont transportés dans le cytoplasme via AmpG et l augmentation de la concentration de ces fragments va mener à l induction de la β-lactamases, AmpC (Hanson and Sanders, 1999). C. La paroi des bactéries à Gram + La paroi des bactéries Gram + (Fig. 26A) possède un réseau de PG épais constitué d empilements réguliers de strates de muréine. Cette paroi renferme également des polymères linéaires d'acides téichoïques (polymère à base de ribitol et glycérol phosphate) liés au PG (Neuhaus and Baddiley, 2003). Certains sont ancrés directement dans la membrane plasmique par l'intermédiaire d'une partie lipidique et portent le nom d'acides lipotéichoïques. D. La paroi des bactéries à Gram - La paroi des bactéries Gram - (Fig. 26B) montre une structure différente de la paroi des Gram +. Elle est constituée d une membrane externe apparentée à la membrane plasmique. Les deux membranes vont délimiter un espace appelé périplasme. On trouve dans ce périplasme un réseau de PG très limité se résumant à une ou deux couches de muréine reliées à la membrane externe par des protéines spécialisées, les lipoprotéines de Braun connues aussi sous le nom de muréine lipoprotéine ou Lpp (Braun and Rehn, 1969; Braun, 1975). La couche externe de la membrane externe est majoritairement constituée de lipopolysaccharides (LPS) (Fig. 27). Celui-ci est formé d une région hydrophobe, le lipide A, inséré dans le feuillet lipidique membranaire. Chez E. coli, le lipide A est composé d un disaccharide de β-1,6. D- glucosamine phosphorylé lié à des acides gras hydroxylés et non-hydroxylés (6 chaînes d acides gras sont liées au disaccharide chez E. coli). Les chaînes d acides aminés vont être greffées sur des résidus GlcNAc par les enzymes LpxA et LpxD (Dixon and Darveau, 2005). Sur l une des molécules de glucosamine, une séquence linéaire de polysaccharides (Antigène O, dont la composition varie selon la bactérie étudiée) est branchée via un dimère de sucre rare à sept carbones, le KDO (core du LPS). Le lipide A est une endotoxine jouant un rôle important dans la physiopathologie du choc septique et qui est responsable de la mise en place de la fièvre au cours de certaines maladies. L antigène O va être potentiellement reconnu par les anticorps des mammifères et servir au sérotypage des bactéries. Le LPS a plusieurs rôles 39
84 CH 2 OH OH O O CH 2 OH OH O O CH 2 OH OH O OH HO NH COCH 3 NH COCH 3 n NH COCH 3 N-acétylglucosamine Figure 28 : Structure de la chitine.
85 Etude de l acquisition et de l utilisation du N-acétylglucosamine dans l interaction de la bactérie avec la plante. Il permet une faible perméabilité de la membrane bactérienne la protégeant ainsi des substances antibactériennes produites par l hôte. Inversement, le LPS comme le PG est un MAMPs induisant les systèmes de défense des plantes (Newman et al., 2007) La chitine La chitine est le deuxième composé du vivant le plus représenté à la surface de la Terre, après la cellulose. C est un homoglycane, de structure linéaire composé de sous unités de GlcNAc liées entre elles par des ponts glycosidiques β-1,4 (Fig. 28). Le réseau de chitine peut avoir une configuration antiparallèle (α) ou parallèle (β). Elle est l un des principaux composants de l exosquelette des insectes et autres arthropodes (crustacés, arachnides, etc.). Chez les champignons, la chitine est un constituant essentiel de la paroi latérale qui entoure et protège les cellules fongiques vis à vis de l'environnement. On trouve de la chitine dans les algues vertes, les mollusques, les protozoaires, le zooplancton, etc. La chitine représente donc une des plus abondantes sources organiques de carbone. Ce composé est généralement bien supporté par les tissus biologiques et est donc utilisé en cosmétique ou dans le traitement des brûlures. En chirurgie, il est utilisé pour la fabrication de fils chirurgicaux en raison de sa résistance et de sa flexibilité. La chitine est également utilisée pour filtrer les eaux usées, car elle forme des chaînes ionisables qui permettent de fixer les éléments organiques en suspension (Muzzarelli, 1997; Shigemasa and Minami, 1996). Le polymère de chitine d'origine biologique est synthétisé par une activité enzymatique appelée chitine synthase (CHS). Les Arthropodes sont les premiers producteurs de chitine dans les systèmes aquatiques où la production de chitine est estimée à environs tonnes métriques par an (Keyhani and Roseman, 1999). Malgré cela, la chitine n est présente que sous forme de trace dans les sédiments marins. La dégradation de la chitine est donc une étape clé du cycle des nutriments dans l environnement (Gooday, 1990; Poulicek et al., 1998), à laquelle les microorganismes participent en tant que premiers agents de dégradation. 40
86 Acide hyaluronique Ser 4S 4S 4S Chondroitine sulfate (CS) Ser 4S 4S 4S 2S 2S Dermatane sulfate (DS) 6S 2S NS 2S NS3S Héparane sulfate (HS) Ser Corps de la protéine xylose Acide glucuronique GalNAc Galactose Acide iduronique GlcNAc Membrane cellulaire Figure 29 : Structure schématique de glycosaminoglycanes (GAGs) et de protéoglycanes. Il existe deux types principaux de GAGs: les GAGs non sulfatés (acide hyaluronique) et les GAGs sulfatés (héparane sulfate, chondroitine sulfate, dermatane sulfate et kératine sulfate). A l exception de l acide hyaluronique, les GAGs sont généralement liés de façon covalente à une protéine (au niveau d une sérine) formant un protéoglycane. (D après Souza-Fernandes et al., 2006) Lien phosphoéthanolamine + H 3 N O O P O - HO HO O HO HO O O P O HO O - O O O HO HO H N O HO O + NH 3 O O O P O O - O OH O H 3 N + O HO HO Protéine Glycane O O O P O - HO O O OC 18 H 37 O C 15 H 31 C 21 H 35 Queue phospholipidique Figure 30 : Structure de l ancre GPI de l érythrocyte acétylcholinestérase humaine. L ancre GPI peut être divisée en trois domaines : le lien phosphoéthanolamine (en rouge), le glycane conservé (en noire) et la queue phospholipidique (en bleu). Les appendices en bleu sont variables (y compris la queue lipidique). (D après Paulick and Bertozzi., 2008) O
87 Etude de l acquisition et de l utilisation du N-acétylglucosamine 5.2 Le GlcNAc et les protéines eucaryotes : la glycosylation La glycosylation consiste en une modification post-traductionnelle des protéines via le branchement de polymères de sucres plus ou moins complexes au niveau d acides aminés spécifiques. Ce type de modification post-traductionnelle est le plus répandu dans le vivant ainsi que l un des plus complexes. Il est estimé que la moitié des protéines de mammifères sont glycosylées (Apweiler et al., 1999). Ces modifications ont un rôle très important dans de nombreux processus cellulaires. Elles peuvent être impliquées dans la conformation de la protéine, la régulation de l activité de la protéine, sa stabilité, la transduction de signaux, la reconnaissance de molécules par des récepteurs, etc. (Reiko et al., 2005). Cinq catégories de glycoconjugés basées sur le type de branchement de l oligosaccharide sont décrites. On trouve des protéines O-glycosylées, des protéines N- glycosylées, des glycosaminoglycanes, des protéines ancrées via un groupement glycophosphatidylinositol (GPI) et des glycolipides. Les glycosaminoglycanes (GAGs) sont des polymères saccharidiques pouvant contenir du galactose, galactosamine, N-acétylgalactosamine-4-sulphate, acide glucuuronique, acide iduronique, et GlcNAc. Ils sont généralement reliés à la protéine au niveau d un résidu sérine ou thréonine et dont la séquence varie dans la composition en sucre, l acétylation et la N- et O-sulfatation. Il existe deux types principaux de GAGs définies en fonction de leur état de sulfatation. On trouve les GAGs non-sulfatés comme l acide hyaluronique et les GAGs sulfatés comme l héparane sulfate (contient du GlcNAc), la chondroitine sulfate, le dermatane sulfate et le kératan sulfate (Fig. 29) (Scott, 1992). Les GAGs peuvent avoir une taille comprise entre 1 et unités disaccharidiques. Plusieurs GAGs peuvent être liés à une même protéine formant un protéoglycane. Les groupements GPIs (Paulick and Bertozzi, 2008) sont des structures greffées au niveau C-terminal de nombreuses protéines eucaryotes. Cette modification permet l attachement de la protéine à la surface externe de la membrane cellulaire. Ces protéines jouent un rôle important dans la transduction de signaux, la maladie du prion, la réponse immunitaire et la pathologie du trypanosome. Leur structure peut se décomposer en trois parties comme présenté sur la figure 30. Les glycolipides sont des dérivés glycosylés importants des lipides de la membrane cellulaire souvent associés à des récepteurs membranaires et sont présent au niveau des 41
88 Figure 31 : Exemple d interactions impliquant des carbohydrates de surface. (a) Interaction entre cellules, (b) avec un anticorps, (c) avec un virus, (d) avec une bactérie et (e) avec une hormone ou une toxine. (D après Saxon and Bertozzi., 2001)
89 Etude de l acquisition et de l utilisation du N-acétylglucosamine radeaux lipidiques. Ce sont également des composants de récepteurs qui peuvent être impliqués dans le système immunitaire. Enfin, la dernière catégorie correspond à la O- et la N-glycosylation qui sont d'une grande importance dans la signalisation et la reconnaissance cellulaire. Ces deux types de glycosylation seront détaillés dans la suite de ce chapitre. Le phénomène de glycosylation est aujourd hui largement étudié de par le monde notamment pour son importance en médecine et en pharmacologie. Les cellules cancéreuses par exemple, sécrètent des protéines glycosylées particulières qui peuvent servir de marqueurs de la maladie et ainsi permettre d établir un diagnostic. La plupart des récepteurs permettant les interactions avec les lymphocytes (cellules du système immunitaire des mammifères) sont glycosylés (Rudd et al., 1999). La glycosylation des protéines de surfaces forme la première couche extracellulaire des cellules eucaryotes permettant d adhérer aux autres cellules, d être reconnue par les anticorps, les virus et les bactéries ou de reconnaître d autres cellules, des hormones, des toxines (Fig. 31) (Dwek, 1996; Varki, 1993). Aujourd hui, de nouvelles techniques telles que la HPLC (Chromatographie en phase liquide à haute performance) et la spectrométrie de masse permettent de séquencer directement les oligosaccharides libérés par les protéines au sein de gels SDS-PAGE. Ces techniques vont permettre une étude de la glycosylation dans tous les domaines où elle est impliquée. Etant donné le rôle de la glycosylation dans de nombreux processus cellulaires, il n est pas surprenant de trouver des glycosylations anormales impliquées dans certaines maladies comme le cancer (Dennis et al., 1999). L étude du suivi et du contrôle des processus de glycosylation permettra la synthèse de molécules thérapeutiques, chez les plantes par exemple (Bardor et al., 2006) Les protéines O-glycosylées La O-glycosylation est initiée par l attachement d un sucre à un résidu sérine ou thréonine d une protéine. Elle produit une très grande variété de structures chimiques. Chaque sucre possède trois ou quatre sites de liaison potentiels à un autre sucre en configuration α ou β, permettant de former plusieurs branches. Pour la plupart des O-glycosylations, la séquence consensus pour l attachement du premier sucre n est pas encore connue. Il existe plusieurs 42
90 Tableau 7. Diversité des O-glycanes de type mucine rencontrés chez l homme et leur localisation tissulaire. (D après Wopereis et al., 2006) Structure Tissu humain 1 Gal β-1,3 GalNAc La plupart des cellules et des protéines sécrétées 2 Gal β-1,3 (GlcNAc β-1,6) GalNAc Toutes les cellules sanguines 3 GlcNAc β-1,3 GalNAc Colon et salive 4 GlcNAc β-1,3 (GlcNAc β-1,6) GalNAc Cellules sécrétant des mucines 5 GalNAc α-1,3 GalNAc Meconium 6 GlcNAc β-1,6 GalNAc Tissu ovarien 7 GlcNAc α-1,6 GalNAc Non précisé 8 Gal α-1,3 GalNAc Bronche
91 Etude de l acquisition et de l utilisation du N-acétylglucosamine types de O-glycanes (classés selon le premier sucre lié à la protéine) dont deux majeures, les O-glycanes de type mucine et les O-GlcNAc. A. Les O-glycanes de type mucine Les O-glycanes de type mucine consistent en une O-glycosylation reliée à la protéine par du N-acétylgalactosamine (GalNAc). Huit structures différentes de O-glycanes de type mucine peuvent êtres définies selon le second sucre rencontré et le type de liaison à ce sucre (Tableau 7). Le squelette du glycane peut être ensuite modifié, par exemple par l ajout d unités GlcNAc. Ce type de modification est également rencontré chez les N-glycanes (Cf paragraphe 1.2.2). Plusieurs sucres peuvent être présents à l extrémité non réduite du glycane : de l acide neuramique, du fucose, du GlcNAc et du GalNAc (Nacétylgalactosamine). Ces sucres peuvent être modifiés en position 6 et/ou 3 par sulfatation (Van den Steen et al., 1998). L acide neuramique peut être également modifié aux positions 4, 7, 8 et 9 par des groupements O-acétyl ester (Varki, 1992). Toutes ces modifications mènent à la production de plusieurs centaines d O-glycanes de type mucine différents. La voie de biosynthèse des O-glycanes de type mucine est localisée dans l appareil de Golgi. La O-glycosylation débute après le repliement et l oligomérisation des protéines soit dans le RE tardif, soit dans un compartiment de l appareil de Golgi [pour revue, (Wopereis et al., 2006)] par le transfert de GalNAc via une N-acétylgalactosaminyl transférase. La biosynthèse des glycanes peut être divisée en trois grandes étapes. Premièrement, les sucres sont synthétisés dans le cytosol. Deuxièmement, ces sucres sont transportés dans le RE ou l appareil de Golgi. Enfin troisièmement, des glycosyltransférases spécifiques vont attacher ces sucres à la protéine ou à un glycane en cours de synthèse dans le RE ou le Golgi. Plusieurs étapes dans la synthèse de sucres requièrent de l ATP. Par conséquent, l état métabolique de la cellule influence le taux de glycosylation. B. Les O-GlcNAc Ce type d O-glycosylation consiste en une simple liaison d un résidu GlcNAc à la protéine, au niveau d une sérine ou d une thréonine donnant un O-GlcNAc. A ce jour, aucune séquence consensus n a put être impliquée dans le ciblage de cette O-glycosylation. On retrouve cette modification généralement sur les protéines nucléaires et cytosoliques mais 43
92 A Protéine native OGT O-GlcNAcase Kinase Phosphatase G Protéine glycosylée P B Protéine native Phosphoprotéine P G Glycophosphoprotéine OGT O-GlcNAcase Phosphatase Kinase G Protéine glycosylée Figure 32 : Relation dynamique entre phosphorylation et modification par le O- GlcNAc d une protéine. A. Il existe une compétition entre le O-GlcNAc et le O-phosphate pour la liaison au site de modification d une même protéine. Selon le type de modification trouvé la stabilité et l activité de la protéine diffèrent. B. Pour certaines protéines, le O-GlcNAc et le O-phosphate peuvent être greffés à coté l un de l autre influençant réciproquement la fonction ou le recyclage de la protéine. (D après Hart et al., 2007)
93 Etude de l acquisition et de l utilisation du N-acétylglucosamine également sur les protéines mitochondriales, et des protéines associées à la membrane (Zachara and Hart, 2006). La liaison de O-GlcNAc est une modification conservée au cours de l évolution (présente chez tous les métazoaires étudiés à ce jour) permettant de réguler l activité de ces protéines (Love and Hanover, 2005). Cette modification post-traductionnelle est analogue aux modifications des protéines par phosphorylation et est impliquée dans de nombreux processus tels que le cycle cellulaire, la signalisation via l insuline ou le protéasome (Zachara and Hart, 2004a). En effet ce processus de glycosylation via un résidu GlcNAc est un processus réversible catalysé par une β-n-acétylglucosaminyl transférase (O-GlcNAc transférases ou OGTs) et une β-n-acétylglucosaminidase (O-GlcNAcases) respectivement (Hurtado-Guerrero et al., 2008; Lubas et al., 1997; Wells and Hart, 2003), la machinerie de glycosylation décrite précédemment n étant pas impliquée (Love et al., 2003; Wells and Hart, 2003). La O-GlcNAc transférase et la O-GlcNAcase agissent de concert avec les kinases et les phosphatases générant différentes isoformes de protéines (Fig. 32). Ces isoformes diffèrent dans leurs propriétés comme leur capacité d interaction avec d autres protéines, leur stabilité et leur activité enzymatique. Par conséquent le branchement d O-GlcNAc joue un rôle important dans la régulation des voies de signalisation des cellules des plantes et des mammifères. L ajout d O-GlcNAc est en partie dépendant du taux d UDP-GlcNAc disponible provenant de la voie de biosynthèse des hexosamines. Or le taux d UDP-GlcNAc est également un signal cellulaire de disponibilité en nutriment (glucose et glucosamine). L altération du métabolisme d O-GlcNAc peut avoir lieu au cours de maladies humaines telles que des désordres neurodégénératifs, le diabète, et le cancer. Des études statistiques de la localisation d O-glycanes de type mucine et d O-GlcNAc ont permis de développer un algorithme permettant de prédire le site de fixation à la protéine de ces deux types de glycosylations disponible sur Internet (serveur de prédiction NetOglyc 3.1, (Julenius et al., 2005) Les protéines N-glycosylées Les N-glycanes sont des chaînes complexes et variées de sucres transférées en un seul bloc (contrairement à ce qui est observé pour les O-glycanes) à la protéine. Ce transfert s effectue au niveau d un résidu asparagine localisé dans une séquence consensus Asn-X- 44
94 Man Man α (1,2) α (1,2) Man Man α (1,6) α (1,3) Man α (1,6) β (1,4) β (1,4) Man NAG NAG Asn Protéine Glu Glu Glu α (1,2) α (1,3) α (1,3) α (1,2) Man Man Man α (1,2) α (1,3) Figure 33 : Structure du N-glycane précurseur greffé sur la protéine eucaryote en cours de synthèse. Le glycane précurseur est composé de deux unités N-acétylglucosamine (NAG), de neuf unités Mannose (Man) et de trois unités Glucose (Glu). La région grisée représente la structure minimale commune à tous les N-glycanes. (D après Ruddock and Molinari, 2006) Cnx ( ) Protéine naissante GI GII ERp57 Protéine Mal/Non conformée Protéine native GII (ER α-manni) Protéine native Export Voie de sécrétion Retranslocation Dégradation cytosolique RE Protéine Mal conformée Figure 34 : Représentation simplifiée des premières étapes de N-glycosylation dans le réticulum endoplasmique (RE). Ces étapes sont communes chez les animaux et les végétaux. Le N-glycane précurseur est greffé à la protéine en cours de synthèse. Les deux résidus glucose terminaux sont relargués grâce à l action des glycanases GI et GII. Le glycane est alors reconnu par le système de protéines chaperonnes (Cnx) comprenant la calnexine et la calreticuline. Ce système va ensuite interagir avec la protéine ERp57, une oxidoréductase qui va participer à la maturation de la protéine. La plupart des protéines sont relarguées sous forme native vers l appareil de Golgi où la maturation de la protéine va se poursuivre. Les protéines mal conformées vont être redirigées vers le cytosol pour être dégradées. Le code couleur correspond à ceux de la figure 33. (D après Ruddock and Molinari, 2006)
95 Man Man NAG Man Man NAG NAG NAG NAG NAG α (1,3) Man Man α (1,6) β (1,2) Man α (1,3) Man α (1,6) β (1,2) Man Man β (1,2) Man β (1,2) Man β (1,2) Man β (1,2) Man α (1,3) Man α (1,6) α (1,3) Man α (1,6) α (1,3) Man α (1,6) α (1,3) Man α (1,6) α (1,3) Man α (1,6) β (1,4) β (1,4) β (1,4) β (1,4) β (1,4) NAG NAG NAG NAG NAG β (1,4) β (1,4) β (1,4) β (1,4) β (1,4) NAG NAG NAG NAG NAG α (1,6) Fuc Asn Asn Asn Asn Asn Protéine Protéine Protéine Protéine Protéine Riche en Mannose Hybride Complexe Figure 35 : Structure des principaux N-glycanes rencontrés chez les mammifères. Les N-glycanes vont être modifiés dans le Golgi générant des glycanes de type riche en mannose, hybride et complexe. Les flèches verticales indiquent la localisation de modifications supplémentaires au cours de la diversification. Tous les sites ne seront pas modifiés sur un seul glycane. NAG, N-acétylglucosamine ; Man, Mannose ; Glu, Glucose ; Fuc, Fucose. (D après Berninsone, 2006)
96 Etude de l acquisition et de l utilisation du N-acétylglucosamine Ser/Thr, où X peut être n importe quel acide aminé excepté la proline. Cependant, tous les sites correspondant à ce consensus ne sont pas N-glycosylés. Comme pour la biosynthèse des O-glycanes (excepté les O-GlcNAc), la synthèse des N-glycanes s effectue dans le RE et l appareil de Golgi au cours de la voie de sécrétion et d adressage des protéines. Un oligosaccharide précurseur est greffé à la protéine dans le RE puis va éventuellement subir plusieurs modifications une fois la protéine localisée dans l appareil de Golgi. Tous les N-glycanes présentent une structure minimale commune, constituée d une unité chitobiose (dimère de GlcNAc), d un résidu β-mannose relié au chitobiose et de deux résidus α-mannose liés au résidu β-mannose en position 3 et 6 (Man 3 - GlcNac 2 ) (zone grisée sur la Fig. 33) (Kornfeld and Kornfeld, 1985). Les types de N-glycanes existant chez les mammifères et les plantes ainsi que certaines étapes de la voie de biosynthèse des N-glycanes diffèrent. Chez les mammifères, la N-glycosylation est catalysée par une oligosaccharyl transférase associée au complexe de translocation des protéines dans le RE. Cette enzyme va transférer un oligosaccharide glucose 3 -Man 9 -GlcNAc 2 (Fig. 33) pré-assemblé du donneur lipidique dolichol pyrophosphate situé dans la membrane du RE au polypeptide en cours de synthèse. Cette étape est impliquée dans le contrôle du bon repliement des protéines. En effet, les N-glycanes facilitent le repliement des protéines et permettent un recrutement efficace des lectines chaperonnes (Fig. 34). De plus, des glycanases présentes dans le RE sont capables d ôter les résidus glucoses ou mannoses des N-glycanes, menant à un adressage de la protéine soit vers le système de sécrétion soit vers le protéasome (pour revue (Molinari, 2007; Ruddock and Molinari, 2006) (Fig. 34). Une fois dans l appareil de Golgi, des résidus mannose vont être enlevés. Le N-glycane sera alors constitué de Man 5 -GlcNAc 2 et va servir de substrat à de nombreuses glycosidases et glycosyltransférases qui vont le modifier. La plupart de ces enzymes localisées dans le Golgi possèdent une courte région cytoplasmique N-terminale, un domaine transmembranaire et un large domaine catalytique (Saint-Jore- Dupas et al., 2006). L action de ces enzymes va aboutir à la production d un large répertoire de N-glycanes. Trois types majeurs de N-glycanes sont produits chez les mammifères, Les N- glycanes de type riche en mannose, de type complexes ou de type hybrides (Fig. 35). Les N- glycanes de type hybride correspondent à une combinaison entre le type riche en mannose et le type complexe (Fig. 35). Les N-glycanes de type complexe peuvent posséder un résidu fucose relié au premier résidu GlcNAc. D autres sucres peuvent être ajoutés à cette structure, notamment des résidus galactose, de l acide sialique et de l acide neuraminique (Fig. 35). La 45
97 Epitope de Lewis Man Man Man α (1,2) α (1,2) α (1,2) Gal Gal β (1,3) β (1,3) Man Man Man α (1,4) Fuc NAG α (1,4) NAG Fuc a NAG Man Man α (1,2) α (1,3) Man Man α (1,6) Man Man β (1,2) Man β (1,2) Man β (1,2) α (1,3) Man Man α (1,6) α (1,3) α (1,6) Man β (1,4) α (1,3) α (1,6) Man Xyl β (1,2) β (1,4) α (1,3) α (1,6) Man Xyl β (1,2) β (1,4) α (1,3) α (1,6) Man Xyl β (1,2) β (1,4) NAG NAG NAG NAG β (1,4) β (1,4) β (1,4) β (1,4) NAG NAG Fuc α (1,3) NAG Fuc α (1,3) NAG Fuc α (1,3) Asn Asn Asn Asn Protéine Protéine Protéine Protéine Riche en mannose Paucimannosidique Complexe Hybride Figure 36 : Structure des principaux N-glycanes rencontrés chez les plantes. Les unités saccharidiques représentées par des zones hachées sont facultatives. La zone grisée représente les modifications apportées au glycane de type complexe menant à la formation d un épitope de Lewis a. NAG, N-acétylglucosamine ; Man, Mannose ; Glu, Glucose ; Fuc, Fucose ; Xyl, Xylose ; Gal, Galactose. (D après Lerouge et al., 1998) Paroi et membrane plasmique N Réticulum Endoplasmique Vacuole Glycane de type Paucimannosidique Appareil de Golgi N-glycane de type riche en mannose Compartiment Extracellulaire (incluant la paroi cellulaire) N-glycanes de type complexe et à épitope de Lewis Figure 37 : Localisation majoritaire des différents types de N-glycanes dans la cellule végétale. La majorité des glycanes de type paucimannosidique sont présents sur les protéines de la vacuole et des graines alors que les glycanes de types complexes sont généralement associés aux glycoprotéines extracellulaires. Le code couleur correspond à celui de la figure 36. (D après Lerouge et al., 1998)
98 RE Asn Glucosidase I et II + ER-mannosidase? Asn α-man I Appareil de Golgi Asn GNT I Asn β(1,2)-xylt + α(1,3)-fuct Asn α-man II GNT II Asn Glycane de type hybride β(1,2)-xylt + α(1,3)-fuct Asn β(1,3)-galt + α(1,4)-fuct Glycanes de type complexe Asn Figure 38 : Synthèse des différents types de N-glycanes dans le réticulum endoplasmique (RE) et l appareil de Golgi des cellules végétales. α-man I, α-mannosidase I ; α-man II, α-mannosidase II ; GNT I, N- acétylglucosaminyltransférase I ; GNT II, N-acétylglucosaminyltransférase II ; β(1,2)-xylt, β(1,2)-xylosyltransférase ; α(1,3)-fuct, α(1,3)-fucosyltransférase ; β(1,3)-galt, β(1,3)- galactosyltransférase ; α(1,4)-fuct, α(1,4)-fucosyltransférase. Le code couleur correspond à ceux de la figure 36. (D après Lerouge et al., 1998)
99 Etude de l acquisition et de l utilisation du N-acétylglucosamine majorité des glycoprotéines sécrétées ou localisées à la surface cellulaire possèdent des glycanes de type complexe. Chez les plantes, les étapes de synthèse des N-glycanes dans le RE sont identiques à celles présentes chez les mammifères. Ce sont les étapes de modification effectuées dans l appareil de Golgi qui vont être différentes. Quatre classes de N-glycanes ont été définies chez les plantes avec les glycanes de types complexe, riche en mannose et hybride, mais également des glycanes de type paucimannosidique qui correspondent à des N-glycanes de type complexe dépourvus d unités GlcNAc terminales (Fig. 36) (Lerouge et al., 1998; Wilson, 2002). Les trois premières classes présentent des spécificités par rapport aux glycanes présents chez les mammifères. En effet, les N-glycanes de type riche en mannose ont une structure de base contenant 5 à 9 résidus mannoses. Les N-glycanes de type complexe et hybride végétaux sont caractérisés par la présence de résidus α-1,3-fucose liés au premier résidu GlcNAc et/ou de résidus β-1,2-xylose liés un résidu β-mannose (Figs. 36, 37 et 38). Il est important de noter qu à ce jour, le xylose ne semble pas entrer dans la composition des N- glycanes des mammifères. De plus, aucun résidu d acide neuraminique n a été identifié chez les plantes à ce jour. Ces différences entre plantes et mammifères représentent une barrière pour la synthèse chez les végétaux de protéines glycosylées de mammifères à visée thérapeutique. Certains N-glycanes des type complexe animaux ou végétaux peuvent posséder des résidus fucose ou galactose supplémentaires liés aux unités GlcNAc terminales (Fitchette- Laine et al., 1997; Melo et al., 1997). Ces sucres vont définir l antigène de Lewis dont seule la forme a (Galβ-1,3(Fucα-1,4)GlcNAc) a été retrouvée chez les végétaux à ce jour (Fig. 36). En ce qui concerne la localisation cellulaire de ces différents N-glycanes chez les plantes, il a été montré que la plupart des glycoprotéines extracellulaires ou localisées au niveau de la paroi végétale présentent une N-glycosylation de type complexe (Fig. 36 et 37). Bien que trouvés sur des glycoprotéines extracellulaires et vacuolaires, les N-glycanes de type riche en mannose sont le plus souvent associés aux protéines localisées dans le RE (Fig. 37). Les décorations de type paucimannosidique sont, quant à elles, retrouvées principalement sur les glycoprotéines localisées dans la vacuole et dans les graines (Fig 37). Les enzymes impliquées dans la N-glycosylation chez les plantes ont été identifiées et caractérisées (Fig. 38) à l aide de plusieurs approches telles que la production de mutants altérés dans la voie de synthèse des N-glycanes (Rayon et al., 1999; Strasser et al., 2004; Strasser et al., 2005; Strasser et al., 2006; Strasser et al., 2007; von Schaewen et al., 1993) et une immunolocalisation des produits des glycosyltransférases (Fitchette et al., 1999; Fitchette-laine et al., 1994; Laine et al., 1991). Le mutant cgl d Arabidopsis ne possède plus 46
100 Etude de l acquisition et de l utilisation du N-acétylglucosamine la N-acétylglucosaminyl transférase I (GNT I) et est incapable de synthétiser des N-glycanes de type complexe (Strasser et al., 2005; von Schaewen et al., 1993). Un mutant mur1 d Arabidopsis incapable de synthétiser du L-fucose dans les feuilles a été utilisé pour caractériser les N-glycanes de plantes (Bonin et al., 1997; Rayon et al., 1999; Reiter et al., 1993). L immunolocalisation a permis de montrer une compartimentation des étapes de modification des N-glycanes au niveau de l appareil de Golgi comme cela a été précédemment montré chez les mammifères (Roth et al., 1988). Chez les plantes, le β-1,2- xylose est ajouté aux N-glycanes le plus souvent au niveau de la région médiane de l appareil de Golgi, alors que l α-1,3-fucosylation à lieu surtout du coté trans-golgi (citernes les plus éloignées du RE (Fitchette-laine et al., 1994; Zhang and Staehelin, 1992)). De plus, la biosynthèse des antennes de Lewis est un événement tardif dans l appareil de Golgi localisé du coté trans-golgi et dans le réseau trans-golgi (Fitchette et al., 1999). Etant données les modifications possibles effectuées par les glycosidases et les glycosyl transférases, on trouve une large hétérogénéité de glycosylation chez les plantes et les mammifères. Cette hétérogénéité est présente à trois niveaux : au niveau du nombre de N- glycanes présents sur une protéine, au niveau des modifications des différents N-glycanes d une même protéine et au niveau du type de N-glycanes pouvant se fixer sur le même site de glycosylation de la protéine. En résumé, une même protéine peut porter un ou plusieurs N- glycanes de structures différentes à des sites différents et un même site de glycosylation peut être glycosylé par des N-glycanes de types différents (Costa et al., 1997; Melo et al., 1997; Oxley and Bacic, 1995; Rayon et al., 1996; Sturm, 1991; Takahashi et al., 1990). Par exemple, la phaseoline (une protéine de réserve trouvée dans les graines de haricots) diglycosylée possède deux N-glycanes de type riche en mannose branchés sur les asparagines 252 et 341, alors que la phaseoline monoglycosylée possède un N-glycane de type paucimannosidique au niveau de l asparagine 252 (Sturm et al., 1987) Rôles des O- et des N-glycanes Les O- et les N-glycanes sont impliqués dans plusieurs processus cellulaires. La glycosylation influe sur la propriété hydrophile des protéines. Les mucines par exemple, sont des protéines de mammifères qui sont fortement glycosylées par des O-glycanes de type mucine et qui sont présentes au niveau de la face externe du tube digestif, du tractus respiratoire ou du système génital. Ces protéines portent un ensemble de glycanes sialylés 47
101 Etude de l acquisition et de l utilisation du N-acétylglucosamine formant des régions chargées négativement et donnant aux mucines la capacité de capter une grande quantité d eau et de former un mucus. Les glycanes sont impliqués dans la mise en place de la structure de la protéine, dans la stabilité de la protéine et dans l interaction avec d autres protéines. Les N-glycanes sont des appendices hydrophiles qui s étendent sur 30 Å autour du squelette de la protéine. Ils vont faciliter le repliement de la protéine en augmentant la solubilité de la chaînes peptidique en cours de synthèse et en recrutant les lectines chaperonnes (Imperiali and Rickert, 1995; Molinari, 2007; Ruddock and Molinari, 2006; Wormald and Dwek, 1999). En effet, les sucres de ces glycanes sont reconnus par les lectines qui vont être impliquées dans l adressage des glycoprotéines vers le système de sécrétion ou le protéasome. Dans les cellules animales, la phosphorylation de N-glycanes de type riche en mannose va être reconnue par des récepteurs membranaires et ces glycoprotéines vont être adressées au lysosome (Sly and Fischer, 1982). Chez les plantes, par contre, la N-glycosylation ne semble pas avoir de rôle particulier dans l adressage des protéines vers la vacuole (Bollini et al., 1985; Lerouge et al., 1998; Voelker et al., 1989). Des effets de la glycosylation sur l augmentation ou la diminution de l activité de certaines protéines ont été également décrits. Par exemple, une glycosylation de type mucine sur l interleukine 5 diminue sont activité (Kodama et al., 1993), alors qu elle va augmenter l activité enzymatique de la lactase phosphorisine hydrolase humaine (Naim and Lentze, 1992). La concanavaline A, une lectine trouvée dans les graines de haricots, est synthétisée sous forme de prolectine inactive N-glycosylée, la pro-cona. L inhibition de cette glycosylation réduit la solubilité de la lectine et affecte sont transport du RE vers la vacuole (Faye and Chrispeels, 1987). De plus, la pro-cona peut être activée par une déglycosylation in vitro (Sheldon and Bowles, 1992). Dans ce cas, la N-glycosylation de la protéine est importante à la fois pour son adressage et pour son activité. Pour un grand nombre de molécules, notamment les hormones et les cytokinines, il a été démontré que la glycosylation contribue à l activité spécifique de ces molécules. En général, la glycosylation diminue cette activité spécifique. Même si dans la plupart des cas l effet de la glycosylation ou de la déglycosylation de ces molécules n est pas spectaculaire, ces petites différences peuvent être amplifiées lors d une cascade de signalisation comme c est le cas pour la voie de signalisation via les cytokinines (Opdenakker et al., 1993; Opdenakker et al., 1995). L activité des enzymes capables de déglycosyler les protéines est donc importante pour la régulation de nombreux processus cellulaires. 48
102 Etude de l acquisition et de l utilisation du N-acétylglucosamine La glycosylation peut également avoir un rôle dans l interaction récepteur ligand. Par exemple, la O-glycosylation du récepteur à la neurotrophine joue un rôle dans la reconnaissance du ligand et peut-être aussi dans la transduction du signal (Chapman et al., 1996; Van den Steen et al., 1998). La glycosylation du ligand peut également être importante pour la liaison au récepteur. PSGL-1 (P-selectin glycoprotein ligand-1) par exemple possède plusieurs O-glycanes dont certains ont une structure reconnue par la P-selectine (Van den Steen et al., 1998). La protéine elrr de résistance de la tomate Cf-9, impliquée dans la reconnaissance de peptides d avirulence (voir introduction générale, chapitre 2), est une protéine N-glycosylée. L altération de chacun des 22 sites potentiels de glycosylation du domaine extracellulaire de Cf-9 montre que la plupart de ces sites contribuent à l activité de la protéine (van der Hoorn et al., 2005). La glycosylation est une caractéristique conservée chez d autres protéines elrr (van der Hoorn et al., 2005). D autre part, les glycanes peuvent avoir un rôle dans la reconnaissance immunologique. Les glycanes sont des structures reconnues par les anticorps et les anticorps sont eux même glycosylés. Les N-glycanes végétaux par exemple sont reconnus par les anticorps IgE impliqués dans les allergies alimentaires et aux pollens (Aalberse et al., 1981; Batanero et al., 1996; Faye and Chispeels, 1988; van Ree and Aalberse, 1993). La glycosylation joue donc un rôle dans l interaction entre l hôte et le pathogène via l activitée de ces récepteurs. La glycosylation par les O-GlcNAc semble quant à elle avoir un rôle important dans une grande variété de voies de signalisation comme la régulation de la transcription, la dégradation des protéines via le protéasome, l apoptose, l insuline (Hanover, 2001; Hart et al., 2007; McClain et al., 2002; Vosseller et al., 2002; Wells et al., 2001), le cycle cellulaire et les stress cellulaires (pour revue voir (Hart et al., 2007; Slawson et al., 2006; Van den Steen et al., 1998; Zachara and Hart, 2006). De plus, il a été récemment montré que les O-GlcNAc modulent de façon indirecte la mobilité des neutrophiles (Kneass and Marchase, 2005). Environ un quart des protéines O-GlcNAcétylées sont impliquées dans la transcription ou la traduction. En effet, chez les eucaryotes, l ajout de O-GlcNAc est impliqué dans la régulation de l expression des gènes par modification des propriétés de nombreuses protéines intervenant dans la régulation de la transcription telles que la ARN polymérase II, des facteurs de transcription, des protéines associées à la chromatine, des protéines impliquées dans la traduction, etc (Comer and Hart, 1999; Love and Hanover, 2005; Zachara and Hart, 2006). L ajout d O-GlcNAc peut aussi bien réprimer ou induire la transcription des gènes selon le promoteur impliqué et les autres protéines associées à cette régulation. D autre part, de 49
103 Etude de l acquisition et de l utilisation du N-acétylglucosamine nombreuses protéines intervenant dans la régulation de la formation du cytosquelette portent des groupements de type O-GlcNAc, en particulier celles impliquées dans la construction de ponts d actines et dans la régulation de l assemblage des microtubules (Zachara and Hart, 2006). Dans les neurones, les sites d attachement de O-GlcNAc sur la synapsine I (Cole and Hart, 1999) pourraient être impliqués dans la modulation de l interaction de la synapsine I avec le cytosquelette. L O-GlcNAcétylation joue aussi un rôle comme régulateur de croissance et de prolifération. La délétion de l OGT (O-GlcNAc transférase) dans des fibroblastes d embryons de souris mène à un retard de croissance, à une augmentation du taux de l inhibiteur de cycline p27 et à la mort cellulaire (O'Donnell et al., 2004). La O- GlcNAcétylation est également directement impliquée dans la signalisation hormonale (acide gibberellique) de la croissance chez les plantes où les gènes spy et sec (secret agent) codent tous deux pour des OGTs (Hartweck et al., 2006). Contrairement à ce qui existe chez les plantes qui possèdent plusieurs OGTs, les mammifères et les insectes ne semblent posséder qu un seul gène codant une OGT (Kreppel et al., 1997; Lubas et al., 1997). Plusieurs études ont montré que la O-GlcNAcétylation des protéines peut directement ou indirectement réguler leur dégradation (Han and Kudlow, 1997). Des analyses protéomiques ont démontré que de nombreuses protéines du centre catalytique et de régulation du protéasome 26S sont modifiées par des O-GlcNAc (Sumegi et al., 2003) chez la drosophile. Enfin, on trouve également des groupements O-GlcNAc de façon abondante sur les protéines ayant un rôle dans la réponse aux stress. Chez les mammifères, une des premières réponses au stress consiste en une augmentation rapide et globale de la O-GlcNAcétylation de nombreuses protéines (Zachara and Hart, 2004b). Le taux d O-GlcNAcétylation redevient normal au bout de 24 à 48 heures après induction. Si l on diminue artificiellement le taux d OGT et/ou de O-GlcNAc, les cellules seront moins tolérantes aux stress alors qu une augmentation du taux de O-GlcNAc aura l effet inverse (Zachara and Hart, 2004b, 2006). L O-GlcNAc module la tolérance aux stress en partie en altérant le taux de protéines de réponse aux stress thermique HSPs (heat-shock proteins). De plus, le O-GlcNAc pourrait protéger les cellules par d autres processus tels que la stabilisation des protéines ou l inhibition de l agrégation des protéines par recrutement de la protéine chaperonne HSP70 (Guinez et al., 2004). En résumé, la glycosylation augmente la stabilité des protéines, leur résistance à la chaleur, leur propriété hydrophile et leur résistance aux protéases en les recouvrant un peu à la 50
104 Etude de l acquisition et de l utilisation du N-acétylglucosamine façon d une ombrelle. Elle est également impliquée dans l immunité, la signalisation via des récepteurs, les interactions protéines-protéines, la modulation de l activité de certaines enzymes et de molécules signales, et l expression de protéines. Un glycane particulier peut être impliqué dans plusieurs fonctions à différents endroits et différents moments au sein d un même organisme (Varki, 1993). Il existe chez les animaux et les plantes, des glycanes libres non fixés à une protéine. Deux types d enzymes de déglycosylation cytosoliques peuvent générer des glycanes libres : les endo-β-n-acétylglucosaminidases (ENGase) qui coupent entre les deux unités GlcNAc du N-glycane et les peptides N-glycanase (PNGase) qui libèrent les N-glycanes des glycoprotéines en clivant la liaison entre le premier résidu GlcNAc et le résidu asparagine (Suzuki et al., 2002a). Il est intéressant de noter que la plante modèle Arabidopsis thaliana possède deux orthologues distincts des ENGases. Ces deux enzymes n ont apparemment pas de séquence signal et seraient par conséquent localisées dans le cytosol (Suzuki et al., 2002b). Après leur rétro-transport dans le cytosol et avant leur dégradation par le protéasome, les glycoprotéines sont déglycosylées par une N-glycanase cytosolique (Chantret and Moore, 2008; Suzuki, 2007). Cette déglycosylation génère de nombreux N-glycanes de type riche en mannose dans le cytosol. Le traitement des chaînes de N-glycanes dans le RE ainsi que dans l appareil de Golgi a fait l objet de nombreuses études. Il a été montré que durant la N- glycosylation des proteins dans le RE, une quantité significative d oligosaccharides libres est formée (Moore, 1999). Lors de cette formation, ces glycanes libres sont transportés vers le cytosol (Chantret and Moore, 2008). Ce transport est important pour la cellule car il entre en compétition avec le transport des glycoprotéines vers la voie de dégradation. D après leurs structures (Priem et al., 1993), les N-glycanes libres chez les plantes pourraient provenir de la dégradation des glycolipides ou des glycoprotéines dans le cytosol. Plusieurs études ont montré un rôle de ces N-glycanes libres dans le métabolisme des plantes. Par exemple, les N- glycanes libres stimulent le mûrissement des tomates (Priem and Gross, 1992), sont présents très tôt au cours du développement des graines (Kimura and Matsuo, 2000) et pourraient influencer leur croissance (Priem et al., 1990). Nous venons de voir que la glycosylation, bien que très variable de par sa nature, est un événement très conservé et essentiel à la vie des cellules eucaryotes. Ces modifications ont longtemps été considérées comme absentes chez les bactéries. Cependant, il a été montré récemment que les bactéries sont capables de modifier leurs protéines par glycosylation bien qu elles soient dépourvues de RE et d appareil de Golgi. 51
105 A H 3 C O AcHN HO AcHN OH Di-N-diacétylbacillosamise (Bac) B HO H 3 C O HO AcHN OH N-acétylfucosamise C OH OH H 3 C O COO cahn H HO cahn Acide pseudaminique (Pse) D OH H 3 C H 2 N H 2 N HO O OH Acide légionaminique COO H E H 3 C HO H H HO OH H NH H COO H O O NAc OH F HO H AcN COO H H H H O NAc H OH Acide 2,3-diacétamidodideoxy-glucuronique H H H Acide 6-Thr-2-acétamido-2-deoxymannuronique G H 3 C O C HN CH 3 O HO NH C O H 3 C Serin e 2,4-diacétamido-2,4,6-tridéoxyhexose (DATDH) lié à une sérine Figure 39 : Exemples de sucres rares constituant les glycanes des glycoprotéines des Archées et des bactéries. (D après Abu-Qarn et al., 2008)
106 Etude de l acquisition et de l utilisation du N-acétylglucosamine 5.3 La glycosylation chez les bactéries Il est clair aujourd hui que les Archées et les bactéries sont capables de glycosyler leurs protéines. Les premières glycoprotéines non eucaryotes ont été découvertes dans la couche S d une Archée halophile, Halobacterium salinarium, par Mescher et Trominger en 1976 (Mescher and Strominger, 1976). Aujourd hui, un grand panel de glycoprotéines procaryotes a été identifié (Spiro, 2002). Les bactéries sont capables de modifier leurs protéines par des O- et des N-glycanes possédant, en plus des sucres présents chez les eucaryotes, des sucres rares servant à lier le glycane à la protéine. Jusqu à présent, la glycosylation chez les procaryotes n a pas été étudiée de manière très active. Il semble cependant, qu elle occupe une place importante chez certaines bactéries. Par ailleurs, il apparaît une très grande diversité dans la composition de ces glycanes bactériens. Bien que dans les exemples décrits à ce jour, le GlcNAc n entre pas directement dans la composition de ces glycanes, cette molécule est utilisée comme un précurseur important. Il m a donc semblé important de ne pas négliger cette voie potentielle d utilisation du GlcNAc et donc de détailler les connaissances acquises quant aux voies de glycosylation bactérienne dans ce chapitre La O-glycosylation La O-glycosylation bactérienne apparaît comme ayant une plus grande diversité de composition et de structure que celle rencontrée chez les cellules eucaryotes. Les pili de bactéries pathogènes comme Neisseria meningitidis (Stimson et al., 1995) et Neisseria gonorrhoeae (Hegge et al., 2004) contiennent des protéines O-glycosylées par des sucres particuliers (Fig. 39). Il a été proposé que le trisaccharide β-d-galp(1,4)-α-d-galp(1,3)- DATDH (Galp, ; DATDH, 2,4-diacetamido-2,4,6-trideoxyhexose), composant un O-glycane trouvé chez N. meningitidis (Stimson et al., 1995), pourrait être important pour échapper au système immunitaire de l hôte et augmenter la solubilité de la piline (Marceau et al., 1998; Power et al., 2003). Les pili de type IV de P. aeruginosa contiennent des glycoprotéines analogues, où le O-glycane est relié à la protéine par l acide pseudaminique (Pse, Fig. 39C), un sucre à neuf carbones ressemblant à l acide sialique (Castric et al., 2001). Les flagelles de bactéries Gram négatives pathogènes comme Campylobacter jejuni (Thibault et al., 2001) et Helicobacter pylori (Schirm et al., 2003) possèdent également des liaisons de type O à des 52
107 A C. jejuni Périplasme Mb Cytoplasme UDP- + PglFED Und-P UMP + PglK Und-PP- Und-PP- Und-PP- PglA + UDP- PglC + UDP- PglI PglIHJ + + UDP- UDP- Und-PP- PglB B H. volcanii Milieu extérieue Mb Cytoplasme Dol-P? AglG AglFI AglE AglD? Dol-P- Dol-P- Dol-P- Dol-P- Dol-P- Dol-P- AglB C N. gonorrhoeae Périplasme Mb Cytoplasme GlcNAc Und-P PglBCD PglA PglE UDP- UDP- UDP- UMP + Und-PP- Und-PP- Und-PP- Und-PP- PglF PglO Bac / DATDH GalNAc Glc Hex HexUA 190 Da Figure 40 : Modèle de N- et O-glycosylation chez les archées et les bactéries. A. N-glycosylation chez Campylobacter jejuni. B. N-glycosylation des glycoprotéines de la couche S chez Haloferax volcanii. C. O-glycosylation de la piline de Neisseria gonorrhoeae Bac, di-n-acétylbacillosamine ; DATDH, Gal-β3-Gal-α3-2,4-diacétamido-2,4,6-tridéoxyhexose ; Dol-P, dolichyl phosphate ; GalNAc, N-acétylgalactosamine ; Glc, glucose ; GlcNAc, N- acétylglucosamine ; Hex, hexose ; HexUA, acid hexuronique ; Mb, membrane ; UMP, uridine monophosphate ; Und-PP, undécaprényl-pyrophosphate ; 190 Da, saccharide de 190 Dalton non caractérisé. (D après Abu-Qarn et al., 2008)
108 Etude de l acquisition et de l utilisation du N-acétylglucosamine sucres analogues à l acide pseudaminique et à l acide sialique. De plus, une liaison de type O d α-arabinofuranoside à une thréonine a été identifiée sur la piline de type IV de P. aeruginosa (Voisin et al., 2007). La glycosylation de la piline et de la flagelline est souvent importante pour l assemblage correct des filaments, pour la mobilité, pour la colonisation et par conséquent pour la virulence. La souche C. jejuni NCTC11168 possède un cluster de glycosylation flagellaire contenant approximativement 50 gènes dont des gènes codant des protéines de structure FlaA et FlaB, protéines qui sont elles-mêmes glycosylées (Schirm et al., 2004). L annotation du locus suggère qu à peu près la moitié de ces gènes pourraient être impliqués dans la biosynthèse de glycanes. On y trouve de multiples orthologues de gènes de biosynthèse de l acide sialique mais aucune glycosyltransférase n a été caractérisée dans ce locus (Szymanski and Wren, 2005). Chez les cellules eucaryotes, la O-glycosylation s effectue par l ajout séquentiel de sucres reliés à un nucléotide (généralement de l UDP) directement au niveau d une thréonine ou d une sérine de la protéine (Cf paragraphe 1.2). Ce type de mécanisme est utilisé pour la O-glycosylation de flagellines de nombreuses espèces bactériennes (Logan, 2006). Cependant, le mécanisme de O-glycosylation semble différent pour certaines protéines procaryotes, où la O-glycosylation s effectue via des mécanismes analogues à ceux rencontrés pour la N-glycosylation, c'est-à-dire par le transfert en bloc du glycane pré-synthétisé sur un lipide donneur, à la protéine acceptrice via une oligosaccharyltransférase (OTase) comme c est le cas chez la bactérie N. gonorhoeae (Fig. 40B). Chez P. aeruginosa 1244 et N. meningitidis MC58 O, l oligosaccharide est également transféré en bloc par les OTases PilO et PglL respectivement, à partir d un donneur undecaprenol-pyrophosphate (Und-PP) (Castric, 1995; Comer et al., 2002; Faridmoayer et al., 2007). PilO et PglL vont agir dans le périplasme et ont une spécificité de glycanes assez large. L activité de PilO est tout de même réduite à des oligosaccharides courts alors que PglL est capable de transférer divers oligo- et polysaccharides. Malgré leur faible similarité de séquence, PilO et PglL appartiennent à une nouvelle famille de «O-OTase» capable de transférer des oligosaccharides à partir de lipides donneurs (Faridmoayer et al., 2007). La O-glycosylation de ces protéines bactériennes a un rôle important dans l interaction avec l hôte et dans l assemblage de complexes protéiques. Il a été récemment montré que la glycosylation de la flagelline est nécessaire pour la formation du filament et donc pour la mobilité de Campylobacter (Goon et al., 2003; Logan et al., 2002). Les glycanes sont des structures qui vont être potentiellement reconnues par les systèmes de défense de l hôte. Les pathogènes peuvent échapper au système immunitaire grâce à deux mécanismes communs de 53
109 A OH HO HO GalNAc O AcH N α1,4 O OH HO HO HO HO GalNAc O AcH N O Glc α1,4 O OH O AcH HO N β1,3 OH GalNAc GalNAc GalNAc α1,4 O OH HO O AcH N α1,4 O OH HO α1,3 O NHA AcH N c O Me O AcH N Bac β1,n NH Asn NH GlcGalNAc 5 Bacβ1,N-Asn O O B gne wfab pglh pgli pglj pglb pgla pglc pgld wfaj pgle pglf pglg Glycosyltransférase Oligosaccharyl transférase Biosynthèse du bacillosamine Figure 41 : La N-glycosylation chez Campylobacter jejuni. A. Heptasaccharide aprés transfert sur la protéine cible au cours des N-glycosylations chez Campylobacter jejuni. (Bac = bacillosamine ; GalNAc = N-acétylgalactosamine ; Asn = asparagine ; Glc = glucose) B. Cluster pgl de Campylobacter jejuni. (D après Weerapana and Imperiali, 2006)
110 Etude de l acquisition et de l utilisation du N-acétylglucosamine variation génétique : la variation de phase (Wisniewski-Dye and Vial, 2008), ou un polymorphisme des gènes du locus de glycosylation menant à un changement de la composition de la voie de biosynthèse (Szymanski and Wren, 2005). La voie de glycosylation de la piline de type IV de Neisseria utilise les deux mécanismes de variation. La variation dans le gène pgle par exemple, permet au résidu terminal β1-4gal de subir une variation de phase convertissant une structure trisaccharidique en une structure disaccharidique (Power and Jennings, 2003). Les loci pgl de N. meningitidis et de N. gonorrhoeae montrent un polymorphisme avec des fusions de gènes, des délétions et des insertions (Kahler et al., 2001). P. aeruginosa montre également un polymorphisme de séquences et de gènes dans l îlot de glycosylation (Arora et al., 2004). Le locus de glycosylation flagellaire de Campylobacter possède des gènes codant de nombreuses enzymes impliquées dans la biosynthèse de carbohydrates complexes et variables et des gènes possédant des variations de phases. Des gènes similaires à ceux de ce locus sont présents chez les espèces Helicobacter, Aeromonas, Clostridium, Caulobacter et Methanococcus, mais pas chez les entérobactéries (Szymanski and Wren, 2005). La capacité de générer des formes variées de flagelline glycosylée suggère l existence d un mécanisme permettant une variation antigénique de la flagelline et donc une évasion du système immunitaire de l hôte. Takeuchi et al. ont caractérisé un îlot de glycosylation qui permet une glycosylation variable de la flagelline selon le pathovar, affectant ainsi la reconnaissance du flagelle par l hôte et donc la spécificité d hôte (Takeuchi et al., 2003). De plus, la spécificité d hôte de bactéries symbiotiques est dépendante de la variabilité des décorations de sucres trouvées sur leurs lipochitooligosaccharides (facteurs Nod) (Schultze and Kondorosi, 1996) La N-glycosylation Le premier système de N-glycosylation bactérien a été découvert chez C. jejuni (Szymanski et al., 1999; Szymanski et al., 2003; Szymanski and Wren, 2005), responsable de gastroentérite. Le transfert de ce système chez E. coli a permis de construire de nombreux mutants permettant la caractérisation de la voie de glycosylation (Alaimo et al., 2006; Feldman et al., 2005; Wacker et al., 2002; Wacker et al., 2006). C est le seul système de N- glycosylation bactérien bien caractérisé à ce jour. La machinerie nécessaire à cette glycosylation est codée par un locus de 12 gènes nommé locus pgl pour «protein glycosylation» (Linton et al., 2005) (Fig 41). Les gènes pgla à pglg, ont une homologie avec les gènes codant les enzymes de biosynthèse des LPS et des polysaccharides de la capsule 54
111 Etude de l acquisition et de l utilisation du N-acétylglucosamine (CPS) mais une mutation dans l un de ces gènes n altère pas cette synthèse (Weerapana and Imperiali, 2006). Les enzymes de ce locus synthétisent un heptasaccharide présenté sur la figure 41A (Young et al., 2002) Le locus pgl code entre autre 5 glycosyltransférases potentielles (PglA, PglC, PglH, PglI, et PglJ) et une oligosaccharyl transférase PglB (Fig. 41B) responsable du transfert en bloc du glycane du lipide vers l asparagine de la protéine, de façon similaire à ce qui se passe chez les cellules eucaryotes (Kelly et al., 2006; Linton et al., 2005) (Fig 40A). Chez C. jejuni la séquence protéique reconnue pour ce transfert est D/E-Z- N-X-S/T où Z et X peuvent correspondre à n importe quel acide aminé excepté la proline (Kowarik et al., 2006), la séquence optimale correspondant à DQNAT (Chen et al., 2007). Le locus pgl code également pour trois enzymes impliquées dans la synthèse de sucres : une UDP-GlcNAc C-6 déhydratase, PglF (Creuzenet, 2004) ; une C-4 aminotransférase, PglE (Schoenhofen et al., 2006; Vijayakumar et al., 2006) et une N-acétyltransférase, PglD (Olivier et al., 2006) (Fig. 41B). Ces enzymes vont transformer l UDP-GlcNAc en UDP-di-Nacétylbacillosamine. Trente huit glycoprotéines pouvant être N-glycosylées ont été identifiées chez C. jejuni (Young et al., 2002) et la plupart de ces protéines sont annotées pour être localisées dans le périplasme suggérant que le système de N-glycosylation est spécifique des protéines périplasmiques. La mutation des gènes du locus pgl entraîne une forte diminution de l immunoréactivité de nombreuses protéines de C. jejuni suggérant un rôle des N-glycanes dans la reconnaissance par l hôte. Il a été également montré que les N-glycanes jouent un rôle important dans l assemblage de complexes protéiques chez C. jejuni. VirB10 par exemple, est une protéine N-glycosylée présente dans le système de sécrétion de type IV de cette bactérie. Lorsque VirB10 est déglycosylée, la compétence de la bactérie est diminuée à cause d un défaut d assemblage des protéines (Larsen et al., 2004). Un homologue de la protéine VirB10 a été trouvé chez Wolinella succinogenes, qui est la seule autre bactérie connue pour avoir un système homologue au système pgl. De façon surprenante, les voies de O-glycosylation et de N-glycosylation bactériennes se ressemblent, ce qui n est pas le cas chez les cellules eucaryotes. Les gènes du cluster pgl de N. meningitidis responsables de la O-glycosylation montrent une homologie significative avec les gènes du cluster pgl de C. jejuni impliqués dans la N-glycosylation. 55
112 chitine ChiA ChiC ChiB CbpA COS Porine TBDT? Membrane externe GlcNAc CdxA COS Périplasme HexA, HexB Chitobiose?? Membrane interne GlcNAc HexC Chitobiose cytoplasme Figure 42 : Modèle de la voie de dégradation de la chitine chez Saccharophagus degradans (anciennement nommée Microbulbifer degradans). La chitine est dépolymérisée en chitooligosaccharides (COS) par les chitinases sécrétées ChiA, ChiB et ChiC. CbpA jouerait le rôle d ancre entre le polymère et la bactérie. Les chitooligosaccharides sont ensuite transportés dans le périplasme et dégradés en GlcNAc et en chitobiose par la chitodextrinase CdxA. Le chitobiose peut être converti en GlcNAc par les N-acétylglucosaminidases périplasmiques HexA et HexB. Le GlcNAc et le chitobiose sont transportés vers le cytoplasme. Le chitobiose cytoplasmique peut être dégradé en GlcNAc par la N-acétylglucosaminidase cytoplasmique HexC. (D après Howard et al., 2003)
113 Etude de l acquisition et de l utilisation du N-acétylglucosamine 6 Chapitre 3. Le GlcNAc comme source d énergie Le GlcNAc est une source de carbone et d azote. Ainsi de nombreuses bactéries sont capables d utiliser ce sucre comme source d énergie et ont développé des systèmes d acquisition du GlcNAc provenant du recyclage du PG (paragraphe ) ou de la dégradation de matériel exogène tel que la chitine. Comme nous l avons vu précédemment, on trouve du GlcNAc dans le peptidoglycane, la chitine et les glycanes. Nous avons déjà parlé de l implication du GlcNAc dans le cycle du peptidoglycane. Nous allons donc nous intéresser maintenant aux systèmes bactériens impliqués dans la dégradation de la chitine, la dégradation des unités N-glycanes et dans le catabolisme du GlcNAc. L utilisation de sources exogènes de GlcNAc comme source d énergie est conservée chez de nombreuses bactéries. 6.1 La dégradation de la chitine Nous avons vu que la chitine est un polymère très abondant dans l environnement, notamment dans les milieux aquatiques, et est une source importante de carbone et d azote sous forme de GlcNAc. Alors que la capacité à métaboliser le GlcNAc est un processus très conservé, la capacité à dégrader la chitine est limitée à un certain nombre de groupes bactériens chez les Protéobactéries, les Bactéroïdes, les Actinobactéries, et les Firmicutes (Cottrell et al., 2000). Le processus complet de dégradation de la chitine a fait l objet d une revue (Keyhani and Roseman, 1999) qui montre l existence de quatre grandes étapes dans cette voie de dégradation : la détection de la présence de chitine qui va conduire à l induction de l expression de gènes impliqués dans l attachement aux molécules de chitine, la dégradation enzymatique, et enfin, la capture et l utilisation des produits de dégradation. Ces étapes nécessitent l action de nombreuses protéines dont des chitinases (Chi, E.C ), des protéines de fixations à la chitine non-catalytiques (CBP pour Chitin-Binding Proteins), des chitodextrinases (CdxA) et enfin des N-acétylglucosaminidases périplasmiques (Hex) et cytoplasmiques (chitobiases et N-acétylhexosaminidases) (Fig. 42) (Keyhani and Roseman, 1996a, b; Techkarnjanaruk and Goodman, 1999). 56
114 Etude de l acquisition et de l utilisation du N-acétylglucosamine Chez Vibrio furnissii et V. cholerae, des oligomères de GlcNAc sont perçus comme le signal majeur indiquant aux bactéries la présence de chitine (Li and Roseman, 2004) et conduisant à l induction de gènes du catabolisme de la chitine. L adhésion à la chitine peut faire intervenir des protéines de surfaces spécifiques comme ChiRP chez V. cholerae (Kirn et al., 2005; Meibom et al., 2004) ou des processus non spécifiques via des interactions hydrophobes ou ioniques. Cette adhésion mène à la formation de biofilms contenant une population bactérienne hétérogène et variable. La dégradation de la chitine a été largement étudiée chez les bactéries aquatiques cultivables comme les espèces d Alteromonas (Orikoshi et al., 2005), Salinivibrio costicola (Aunpad and Panbangred, 2003), Saccharophagus degradans (anciennement nommée Microbulbifer degradans) (Howard et al., 2003), Vibrio alginolyticus (Suginta, 2007), V. cholerae (Kirn et al., 2005; Li and Roseman, 2004; Meibom et al., 2004), V. harveyi (Svitil et al., 1997) et V. furnissii (Bassler et al., 1991; Li and Roseman, 2004). Chez ces bactéries, les chitinases et les β-glucosaminidases vont dégrader de façon séquentielle le polymère de chitine en molécules plus petites et plus solubles (Keyhani and Roseman, 1999). Chez les Alteromonas, quatre chitinases ont été identifiées (ChiA, ChiB, ChiC et ChiD) et sont sécrétées en présence de chitine. ChiA semble jouer un rôle prépondérant dans la dégradation de la chitine (Orikoshi et al., 2005). Chez les bactéries du genre Vibrio, les chito-oligosaccharides traversent la membrane externe via des porines spécifiques (ou chitoporines) de la famille OmpC codées par le gène chip (Keyhani et al., 2000; Meibom et al., 2004). D après les analyses bioinformatiques menées par Yang et ses collaborateurs en 2006 sur de nombreuses bactéries, deux autres types de transporteurs de la membrane externe pourraient être impliqués dans le transport de ces oligosaccharides, une porine de la famille des OprD et des transporteurs de type TBDT. Les porines de la famille des OprD sont connues pour être impliquées dans le transport de nombreux nutriments chez P. aeruginosa (Tamber et al., 2006). Comme nous l avons vu précédemment, les TBDTs sont des transporteurs actifs laissant passer de larges molécules comme des carbohydrates complexes [pour revue (Schauer et al., 2008)]. Des études de profils d expression de mutants chez V. cholerae et de souches cultivées avec des polymères de deux à six unités de GlcNAc ont permis l identification de gènes régulés par ces molécules (Meibom et al., 2004). Le senseur ChiS régule l expression des gènes de dégradation des polymères de GlcNAc dont l opéron de dégradation de la chitobiose (GlcNAc 2 ), deux chitinases extracellulaires, une chitoporine et le pilus ChiRP. Chez cette bactérie, le GlcNAc coordonne l expression des gènes impliqués dans la chimiotaxie, l adhésion, le transport et l assimilation du GlcNAc. La plupart des gènes codant des 57
115 Etude de l acquisition et de l utilisation du N-acétylglucosamine chitinases, des CBP, des chitodextrinases, et des β-n-acétylglucosaminidases périplasmiques semblent corégulés avec les gènes de la voie du catabolisme du GlcNAc (décrite plus loin). Les dernières étapes de la dégradation de la chitine mènent à la libération de chitobiose ou de GlcNAc dans le périplasme. Ces molécules vont être métabolisées et entrer soit dans la voie de la glycolyse, soit dans la voie de biosynthèse des constituants de la paroi bactérienne. 6.2 La dégradation des glycanes Certaines bactéries ont développé des systèmes de dégradation des groupements glycanes des protéines de l hôte. Certains streptocoques pathogènes par exemple, sont des organismes fermenteurs ayant une activité glycosidique impliquée dans la nutrition in vivo, par dégradation des groupements glycanes des glycoprotéines de l hôte (Beighton et al., 1994). Streptococcus oralis est capable d utiliser l AGP (α 1 -acid glycoprotein) du sérum humain comme source de carbone in vitro (Byers et al., 1999). L AGP est une protéine hautement glycosylée possédant cinq types de N-glycanes complexes syalilés (Fournet et al., 1978; Hermentin et al., 1992; Yoshima et al., 1981) dont certains possède des épitopes de Lewis (De Graaf et al., 1993; Van der Linden et al., 1994; Van Dijk, 1995). Des études ont montré que la production de sialidase et de N-acétyl-β-D-glucosaminidase chez S. oralis mène au clivage de l acide neuraminique (NeuAc), et du GlcNAc des glycoprotéines du sérum et que ces deux sucres aminés permettent la croissance de la bactérie (Homer et al., 1995; Homer et al., 1996). S. pneumoniae possède des glycosidases sécrétées ou associées à la surface cellulaire qui vont modifier les glycoconjugués présents chez l hôte (Berry et al., 1994; Berry et al., 1996; Camara et al., 1994; Clarke et al., 1995; Muramatsu et al., 2001; Umemoto et al., 1977; Zahner and Hakenbeck, 2000). Cette bactérie est capable de déglycosyler les molécules de défense de l hôte via l activité séquentielle de neuraminidases (NanA et NanB), d une β-galactosidase (BgaA), et d une N-acétylglucosaminidase (StrH), qui vont cliver le NeuAc, le galactose et le GlcNAc présents à l extrémité des glycanes (King et al., 2006). De plus le génome des pneumocoques code des transporteurs et des enzymes du catabolisme de ces sucres qui seront utilisés pour la fermentation in vivo. S. pneumoniae est donc capable d utiliser les sucres libérés lors de la déglycosylation des glycoprotéines du sérum humain pour sa croissance (Burnaugh et al., 2008). De plus, S. pneumoniae est capable d utiliser la glycoprotéine mucine comme source de nutriments. La croissance en présence de cette protéine augmente la transcription du gène nana, gène indispensable à cette croissance 58
116 Dégradation de la chitine Dégradation d unités glycanes GlcNAc Périplasme MI Cytoplasme Système PTS NagE Perméase NagP Transporteur ABC? NagK-I / NagK-II GlcNAc-6-P NagA NagB / NagB-II GlcN-6-P Fru-6-P GlmS GlmM GlcNAc Recyclage du peptidoglycane glycolyse GlcN-1-P GlmU GlcNAc-1-P GlmU UDP-GlcNAc Biosynthèse de peptidoglycane Figure 43 : Représentation schématique du catabolisme du GlcNAc chez les bactéries. Le GlcNAc localisé dans le périplasme va être transporté dans le cytoplasme soit par un système de type PTS qui va phosphoryler le GlcNAc de façon simultanée au transport, soit par un autre type de transporteur tel que les perméases ou les transporteus de type ABC par exemple. Dans ces derniers cas, le GlcNAc sera phosphorylé via une N- acétylglucosamine kinase NagK-I ou NagK-II. Le GlcNAc-6-P sera ensuite déacétylé par l enzyme NagA en glucosamine-6-p qui sera déaminé et isomérisé en fructose-6-p par NagB ou NagB-II. Le fructose-6-p pourra alors être utilisé dans la voie de la glycolyse. D autre part, le fructose-6-p et le glucosamine-6-p peuvent également être utilisés dans la voie de biosyntèse du peptidoglycane (en bleu). GlcNAc, N-acétylglucosamine ; GlcN, glucosamine ; Fru, fructose ; MI, membrane interne.
117 Etude de l acquisition et de l utilisation du N-acétylglucosamine (Yesilkaya et al., 2008). On note la présence d activité sialate O-acétylesterase et d enzymes impliquées dans la dégradation des glycoprotéines dans les extraits cellulaires de pneumocoques. Une activité endo-n-acétyl-β-d-glucosaminidase (ENGase) a été détectée chez Enterococcus faecalis, un pathogène nosocomial, lui permettant d utiliser la RNaseB comme substrat pour sa croissance (Roberts et al., 2000). Cette enzyme hydrolyse les liaisons entre un résidu GlcNAc est un autre sucre. Trois types d ENGases peuvent être définis. Les ENGases agissant sur la muréine, celles agissant sur la chitine et celles agissant sur les glycanes. L activité ENGase décrite chez E. faecalis libère les glycanes de types riche en mannose de leur protéine et appartient donc à la troisième catégorie d ENGase. Le glycane une fois libéré va subir d autres étapes de dégradation libérant des monosaccharides utilisés pour la croissance. Une étude de la distribution de l activité ENGase chez les entérocoques et de la capacité de ces bactéries à pousser avec la RNaseB comme substrat a montré que 10 des 18 espèces d Enterococcus isolées à partir de mammifères possèdent cette activité et que ces 10 espèces sont capables d utiliser les glycanes libérés pour croître (Roberts et al., 2001). Les glycanes représentent donc également une source de carbone pour certaines bactéries pathogènes de l homme et cette déglycosylation est très certainement impliquée dans le développement de maladies. 6.3 Le catabolisme du GlcNAc Le GlcNAc peut être à la fois une source de carbone et d azote pour les bactéries. Il permet une croissance d E. coli comparable a celle observée en présence de glucose (Plumbridge and Kolb, 1993; White, 1968). De nombreuses espèces bactériennes possèdent une voie de catabolisme du GlcNAc conservée. Cette voie mène à la transformation du GlcNAc en fructose-6-phosphate (Fru-6-P) par trois étapes cytoplasmiques successives (Fig. 43) : une phosphorylation, une déacétylation et une déamination-isomérisation. Le Fru-6-P va ensuite pouvoir entrer dans la voie de la glycolyse. Les enzymes permettant ces réactions biochimiques sont très conservées et les gènes codant ces enzymes sont souvent organisés en opéron comme c est le cas chez E. coli (Barnhart et al., 2006). 59
118 6.3.1 Le transport du GlcNAc Etude de l acquisition et de l utilisation du N-acétylglucosamine Il a été récemment montré que le GlcNAc libre pouvait traverser la membrane externe de Caulobacter crescentus via un TBDT (Eisenbeis et al., 2008). Pour le passage du périplasme vers le cytoplasme, il existe plusieurs types de transporteurs utilisés selon la bactérie étudiée (Yang et al., 2006). Chez E. coli par exemple, le GlcNAc est pris en charge par un système de transport de type PTS (PhosphoTransferase System) ayant une haute affinité pour le GlcNAc et par un autre système PTS ayant une affinité plus forte pour le mannose (ManXYZ) (Postma and Lengeler, 1985; Postma et al., 1993). Le GlcNAc va être reconnu par la perméase membranaire EII du système PTS spécifique au GlcNAc, NagE, puis va être transporté vers le cytoplasme et phosphorylé simultanément en GlcNAc-6-P (Rogers et al., 1988). Le gène nage est conservé chez les Entérobactéries et les Vibrions ainsi que chez certaines α et β protéobactéries (Yang et al., 2006). La bactérie Gram + Streptomyces olivaceoviridis semble quant à elle utiliser un système de type ABC (ATP-Binding Cassette) pour le transport du GlcNAc à travers la membrane plasmique (Xiao et al., 2002). Les transporteurs ABC couplent directement l'énergie issue de l hydrolyse d'atp au transport des molécules. On trouve des gènes codant des systèmes de type ABC regroupés avec des gènes impliqués dans l utilisation du GlcNAc chez Silicibacter spp et les Rhizobactéries (e.g. mll4771 mll4779 chez Mesorhizobium loti). Enfin, le transport du GlcNAc dans les bactéries n ayant pas d homologues au système Nag-PTS ou au système ABC, pourrait s effectuer à l aide de transporteurs MFS (major facilitator superfamily) comme la perméase NagP identifiée chez Shewanella oneidensis, les Alteromonas et les Xanthomonas (Yang et al., 2006). Le gène nagp est localisé dans la même région chromosomique que les autres gènes nag. NagP possède 12 segments transmembranaires prédits et est homologue à la perméase du fucose FucP (environ 25% d identité) d E. coli. La protéine Ngt1 ayant des similarités avec les transporteurs MFS permet le transport de GlcNAc chez le champignon pathogène Candida albicans (Alvarez and Konopka, 2007). Une autre protéine présente notamment chez S. oneidensis ou X. axonopodis, NagX, ayant 11 segments transmembranaires potentiels, pourrait également transporter du GlcNAc ou des produits de dégradation de la chitine (Yang et al., 2006) L étape de phosphorylation du GlcNAc Nous avons vu que le GlcNAc pouvait être phosphorylé au cours du transport par le système PTS. Cependant, les bactéries ne disposant pas de système de ce type doivent 60
119 Tableau 8. Occurrence et caractéristiques des gènes impliqués dans l utilisation de la chitine et du GlcNAc. La présence des gènes codant les protéines impliquées dans l acquisition et l utilisation de la chitine et du GlcNAc est représentée par les blocs colorés. La couleur des blocs correspond aux trois régulons identifiés. Vert, régulon NagC (comme chez E. coli); jaune, régulon NagR (comme chez S. oneidensis ), et bleu, régulon NagQ (α- et β-protéobacteries). Les gènes n appartenant à priori pas à l un de ces régulons sont représenté en par les blocs gris. PTS, phosphoénolpyruvate-carbohydrate phosphotransférase system ; GlcNAc, N -acétylglucosamine ; CBP, chitin-binding protein ; CdxA, chitodextrinase ; Hex, β-n -acétylglucosaminidase ; TBDT, TonB dependent Transporter. (D après Yang et al., 2006) Groupe taxonomique et Organismes (nombre totale de génomes / espèces ayant une voie de catabolisme du GlcNAc) Alteromonadales (11/15) Shewanella oneidensis MR-1 S. putrefaciens CN-32 S. amazonis SB2B Shewanella sp. PV-4 Shewanella baltica OS155 S. denitrificans OS-217 Shewanella sp. ANA-3 Shewanella frigidimarina Saccharophagus degradans Colwellia psychrerythraea Xanthomonadales (5/5) Xanthomonas (Xoo, Xcv, Xac) Xylella fastidiosa Stenotrophomonas maltophilia Enterobacteriales (11/12) Escherichia coli Serratia marcescens Erwinia carotovora Photorhabdus luminescens Yersinia pestis Pasteurellales (1/6) Pasteurella multicoda Vibrionales (5/5) Vibrio cholerea Photobacterium profundus Psuedomonadales (2/5) Pseudomonas aeruginosa β-proteobacteria (9/24) Chromobacterium violaceum Burkholderia pseudomallei α-proteobacteria (14/42) Brucella melitensis Mesorhizobium loti Gluconobacter oxydans caulobacter crescentus catabolisme du GlcNAc Transport du GlcNAc NagK NagB Membrane Interne Membrane externe NagA I II I II PTS ABC NagP NagX TBDT Porine Régulateurs NagC NagQ NagR Dégradation de la chitine Hex CdxA Chitinases CBP
120 Etude de l acquisition et de l utilisation du N-acétylglucosamine posséder une kinase spécifique du GlcNAc pour former du GlcNAc-6-P. En 2006, Yang et ses collaborateurs, dans leur étude bioinformatique des systèmes de catabolisme du GlcNAc chez de nombreuses espèces bactériennes, ont identifié une GlcNAc kinase potentielle chez S. oneidensis appelée NagK-I et ont montré que cette kinase est bien fonctionelle. Cette enzyme possède un motif ressemblant au motif de liaison à l ATP des kinases de sucres (domaine PFAM PF01869) et est similaire à une GlcNAc kinase de mammifère (Hinderlich et al., 2000). Le gène codant cette enzyme est conservé chez les Alteromonas et quelques α protéobactéries (Tableau 8). Une enzyme non orthologue, NagK-II appartenant à la famille des glucoses kinases (domaine PFAM PF02685) a été identifié chez les espèces de Xanthomonas (Yang et al., 2006) La déacétylation du GlcNAc (par NagA) Le GlcNAc-6-P est déacétylé en glucosamine-6-p (Glu-6-P) par la déacétylase NagA (E.C ) (Jones-Mortimer and Kornberg, 1980; Plumbridge, 1989; Rogers et al., 1988; White, 1968). Cette étape est une étape clé du catabolisme du GlcNAc et du recyclage du peptidoglycane (Uehara and Park, 2002, 2003, 2004; Uehara et al., 2005; Uehara et al., 2006; White and Pasternak, 1967). NagA fait partie de la super famille des amidohydrolases (AHS) (Seibert and Raushel, 2005) ; elle est active sous forme tétramérique et requiert la présence d ions divalents pour fonctionner (Ferreira et al., 2006). Plus de 300 homologues à la protéine NagA d E. coli K12 ont été identifiés dans la base de données NCBI (National Center for Biotechnology Information). Cette enzyme est conservée dans un groupe phylogénétique très large allant des bactéries aux mammifères (Hall et al., 2007). Chez E. coli, l accumulation de GlcNAc-6-P cytoplasmique dans un mutant naga est toxique et entraîne une inhibition de la croissance bactérienne (Bernheim and Dobrogosz, 1970; White, 1968). De plus, le GlcNAc-6- P est une molécule signal importante pour la régulation de certains processus cellulaires tels que la production de fibres curli (Barnhart et al., 2006), la répression catabolique (Goldenbaum et al., 1970) et la régulation de l expression des gènes impliqués dans la catabolisme du chitobiose et du GlcNAc (Plumbridge and Pellegrini, 2004) La déamination et l isomérisation Au cours de la dernière étape, le Glu-6-P subit une déamination et une isomérisation de façon simultanée pour être transformé en fructose-6-p (Fru-6-P). Cette étape est catalysée 61
121 Etude de l acquisition et de l utilisation du N-acétylglucosamine par l enzyme NagB qui est une Glu-6-phosphate déaminase (EC ) appartenant à la famille des aldose ketose isomérases. Cette enzyme est un hexamère composé de sous unités identiques et qui montre une activation allostérique par le GlcNAc-6-P (Altamirano et al., 1995). NagB a été identifié dans de nombreuses espèces animales, fongiques et bactériennes. Cependant le gène nagb ne possède pas d orthologue chez S. oneidensis et de nombreuses autres protéobactéries (Yang et al., 2006). Par contre, une Glu-6-P déaminase alternative appelé NagB-II a été identifiée chez ces bactéries, sur la base de la localisation chromosomique de leur gène (groupé avec les autres gènes du catabolisme du GlcNAc) et caractérisée chez S. oneidensis (Yang et al., 2006). La réaction catalysée par NagB ou NagB-II est la dernière étape de la voie d utilisation du GlcNAc, pouvant diverger vers la voie de biosynthèse des nucléotides liés à un sucre aminé et donc vers la voie de biosynthèse du peptidoglycane (Fig 43). NagB-II appartient à la famille des isomérases de sucres et est similaire au domaine C-terminal de la Glu-6-P synthase GlmS d E. coli qui est l enzyme qui catalyse la biosynthèse de Glu-6-P à partir de Fru-6-P au cours de la biosynthèse de la muréine bactérienne. NagB est capable de faire la réaction inverse, c est à dire de catalyser la synthèse de sucres aminés selon l équilibre de la réaction (Alvarez-Anorve et al., 2005; Calcagno et al., 1984; Vogler and Lengeler, 1989) alors que GlmS est NagB-II ne semblent pouvoir effectuer la réaction que dans un sens. La balance entre la synthèse de Glu-6-P et sa dégradation en Fru-6-P est finement régulée chez E. coli par le régulateur transcriptionnel NagC (Plumbridge, 1995; Plumbridge et al., 1993). L expression du gène glms est régulée par la présence de GlcNAc ou de glucosamine. Cette expression est inhibée lorsque les gènes du locus nag sont activés (Plumbridge, 1995) La régulation Le GlcNAc étant une molécule importante pour la vie de la bactérie et le GlcNAc-6-P étant impliqué dans plusieurs voies de signalisations, la régulation de l expression des gènes d acquisition et d utilisation du GlcNAc (incluant les gènes de dégradation de la chitine et de transport des produits de cette dégradation) est complexe. Elle fait intervenir de nombreux régulateurs et des boucles de rétrocontrôle. Selon la bactérie étudiée, l expression des gènes impliqués dans l acquisition et le catabolisme du GlcNAc peut être régulée par trois régulateurs principaux, NagC, NagR et NagQ. En général, chaque bactérie ne possède qu un de ces trois régulateurs (Yang et al., 2006). On peut alors classer les bactéries selon le 62
122 A Séquence consensus reconnue par NagC B Séquence consensus reconnue par NagC Séquence consensus reconnue par NagR Séquence consensus reconnue par NagQ Figure 44 : Séquences consensus reconnues par les régulateurs transcriptionnels NagC, NagR et NagQ. A. Séquence consensus reconnue par NagC proposée par El Qaidi and Plumbridge, B. Séquences consensus reconnues par NagC, NagR et NagQ proposées par Yang et al., 2006.
123 Etude de l acquisition et de l utilisation du N-acétylglucosamine régulateur utilisé. Les entérobactéries vont généralement posséder le régulateur NagC alors que les Alteromonas utiliseraient plutôt le régulateur NagR. La plupart des Pseudomonas, des α- et des β-protéobactéries vont quant à elles utiliser un régulateur de type NagQ. A ce jour, seules les Xanthomonas possèdent à la fois un gène codant un régulateur NagR et un gène codant un régulateur NagQ. Des analyses bioinformatiques ont permis d identifier les boites de régulation potentielles de chacun de ces régulateurs [Fig 44, (Yang et al., 2006)]. Récemment, le site de fixation de NagC a été clairement défini par des expériences de digestion à la Dnase I (footprint) (El Qaidi and Plumbridge, 2008). NagC est un régulateur appartenant à la famille ROK (Repressor, Open reading frame, Kinase) possédant un site de liaison à l ADN en N-terminal et un domaine comparable au domaine kinase de sucres en C-terminal (Titgemeyer et al., 1994). La molécule activatrice reconnue par NagC est le GlcNAc-6-P. Ce régulateur possède un régulon assez large comprenant majoritairement trois types de gènes chez E. coli. On trouve dans ce régulon, les gènes de l opéron nag, nage-bacd impliqués dans le transport et le catabolisme du GlcNAc (Plumbridge and Pellegrini, 2004; Plumbridge, 1991) ; les gènes impliqués dans le transport et l utilisation des de la chitobiose, l opéron chbbacrfg (Plumbridge and Pellegrini, 2004); les gènes de l opéron glmus (Plumbridge, 1995) impliqués dans la biosynthèse des peptidoglycanes et les gènes de l opéron manxyz (Plumbridge, 1991) qui codent pour le second transporteur PTS du glucosamine chez E. coli (Curtis and Epstein, 1975; Jones- Mortimer and Kornberg, 1980). Les gènes nag, chb et man sont réprimés par NagC alors que les gènes glm sont eux activés par NagC. NagC est également impliqué dans l activation de l expression de la recombinase FimB intervenant dans l activation de l expression de l opéron de synthèse des fimbriae de type I (Sohanpal et al., 2004; Sohanpal et al., 2007). Chez les espèces de Vibrio, le régulon NagC comprendrait également les gènes impliqués dans la chimiotaxie, la dégradation et l acquisition de la chitine (Yang et al., 2006) (Meibom et al., 2004). NagR appartient à la famille des répresseurs transcriptionels LacI [pour revue (Lewis, 2005)]. Le site de liaison à l ADN de NagR identifié par Yang et ses collaborateurs est caractéristique des opérateurs de type LacI (Gelfand and Laikova, 2003). Chez Shewanella et Colwellia, le régulon potentiel de NagR contient des enzymes impliquées dans la dégradation de la chitine, les enzymes du catabolisme du GlcNAc, des transporteurs de type TBDT, des hydrolases de sucres, ainsi que des sulfatases potentiellement impliquées dans la désulfatation de polysaccharides de GlcNAc sulfaté. La présence d une boite NagR en amont du gène nagr 63
124 Etude de l acquisition et de l utilisation du N-acétylglucosamine chez Shewanella et Colwellia suggère une autorégulation de son expression (Yang et al., 2006). Enfin, NagQ est un répresseur de la famille des GntR localisé dans le cluster des gènes nag chez les α, β et certaines γ protéobactéries (Yang et al., 2006). Le motif potentiel de liaison à l ADN de NagQ correspond à deux ou trois répétitions imparfaites du motif TGGTATT séparées par 4 paires de bases (Fig. 44). Ce type d opérateur est caractéristique des GntR (Rigali et al., 2002). Le régulon potentiel de NagQ comporte les gènes nag et quelques gènes de dégradation de la chitine chez Chromobacterium violaceum, Caulobacter crescentus, et les espèces Burkholderia. 64
125 Etude de l acquisition et de l utilisation du N-acétylglucosamine 7 Chapitre 4. Le GlcNAc et le pouvoir pathogène Nous venons de voir que des bactéries sont capables de dégrader la chitine et les unités glycanes des protéines. Pour certaines bactéries, cette dégradation fait partie intégrante de leur pouvoir pathogène et peut être considéré comme un facteur de virulence important. La carapace des crustacés, par exemple, est parfois attaquée par des microorganismes. Cette maladie est appelée «shell disease syndrom» car elle n est pas le fait d un seul agent microbien mais d une population diverse qui va dégrader la chitine composant la cuticule de l hôte [pour revue voir (Vogan et al., 2008)]. Cette maladie affecte de nombreuses espèces de crustacés sauvages ou cultivés et est caractérisée par des lésions noires à la surface de l exosquelette. De nombreuses études ont tenté d identifier les microorganismes responsables de cette maladie. Des variétés de Pseudomonas, Vibrios et d Aeromonas cultivables sont associées aux lésions affectant le crabe bleu, Callinectes sapidus (Noga et al., 2000). D autre part, on sait aujourd hui que l interaction de V. cholerae avec la chitine joue un rôle important dans le développement d épidémies de choléra (pour revue (Pruzzo et al., 2008). L association de cette bactérie avec le zooplancton et leurs œufs dispersés dans l eau s'est avérée être un facteur clé dans le développement saisonnier et géographique d'épidémies de choléra et de pandémies (Lipp et al., 2002). Un biofilm sur un copépode peut contenir 10 4 cellules de V. cholerae, or la dose clinique pour l infection est de 10 3 cellules. L association de ces bactéries avec la chitine pourrait les protéger contre les acides gastriques rencontrés au cours du transit stomacal (Nalin et al., 1979). De plus, il a été récemment montré que les ligands produits par V. cholerae impliqués dans la colonisation des intestins (TCP et MSHA) (Attridge et al., 1996; Finn et al., 1987; Herrington et al., 1988; Kirn et al., 2000; Tacket et al., 1998; Thelin and Taylor, 1996), sont également impliqués dans la fixation à la chitine et la formation de biofilms (Finn et al., 1987; Kaper et al., 1995; Reguera and Kolter, 2005; Tacket et al., 1998). Une protéine de 53 kda impliquée dans l attachement de V. cholerae aux particules de chitine des copépodes (Tarsi and Pruzzo, 1999), permet également l attachement de la bactérie à des cultures de cellules épithéliales (Zampini et al., 2005). Cette interaction se fait via une liaison au GlcNAc présent sur les glycanes et les lipides de l épithélium intestinal. Des expériences ont montré que l adhésion de V. cholerae aux cellules de l intestin de lapin est inhibée par l ajout de GlcNAc (Datta-Roy et al., 1989; Sasmal et al., 1992). La dégradation des glycanes est également un facteur de virulence important pour de nombreuses bactéries pathogènes. La production de sialidase est un facteur de virulence 65
126 Etude de l acquisition et de l utilisation du N-acétylglucosamine produit par de nombreux pathogènes de mammifères tels que V. cholerae, S. pneumoniae, Salmonella typhimurium et Bacillus fragilis (Corfield, 1992; Godoy et al., 1993). Un des rôles de cette enzyme, mise a part la libération de sucres utilisés pour le métabolisme, serait d endommager les tissus et d altérer la fonction des glycoprotéines de l hôte (Corfield, 1992). Des études in vivo montrent que des mutants de B. fragilis incapables de produire la sialidase prolifèrent moins bien chez le rat (Godoy et al., 1993). Les glycosylations ayant de nombreux rôles dans la stabilité protéique, la signalisation cellulaire et l activité enzymatique, il n est sans doute pas anodin que les bactéries pathogènes ciblent et dégradent ces modifications protéiques. Le GlcNAc est lui-même important pour la virulence de certaines bactéries. La présence de GlcNAc induit la production de composants importants pour la colonisation de l hôte comme les fimbriae permettant l adhésion aux cellules hôtes (Sohanpal et al., 2004), les gènes codant les systèmes de pompes antidrogues (Hirakawa et al., 2006) et la production de curli impliqués dans la formation de biofilms (Barnhart et al., 2006). La présence de GlcNAc entraîne un changement morphologique chez le champignon pathogène Candida albicans qui va passer d une forme ronde et globulaire à une croissance sous forme d hyphe (cellules allongées et fines). Cette transition morphologique serait un facteur de virulence important pour le développement de la maladie (Singh et al., 2001; Sudbery et al., 2004; Whiteway and Oberholzer, 2004). Enfin, chez S. thyphimurium, un mutant du gène naga est moins phagocyté par les macrophages (Gahring et al., 1990) et n est plus cytotoxique (Lindgren et al., 1996). Tous ces exemples montrent que l acquisition et l utilisation du GlcNAc a non seulement un rôle important dans le métabolisme et la synthèse de la paroi bactérienne, mais également dans le pouvoir pathogène de nombreux microorganismes ce qui en fait des cibles potentielles pour des traitements thérapeutiques. Il est important de noter que, contrairement aux études menées sur les pathogènes animaux, à ma connaissance, aucune analyse n a été effectuée sur le rôle du GlcNAc dans la virulence de bactéries phytopathogènes. 66
127 RESULTATS
128 Résultats Xcc possède un locus impliqué dans l acquisition et l utilisation du GlcNAc. Ce locus comprend un transporteur de la membrane interne de la famille MFS (NagP), deux enzymes impliqués dans le catabolisme du GlcNAc (NagA et NagB-II) et deux régulateurs transcriptionels (NagQ et NagR). De plus, la séquence consensus reconnue par NagR est présente en amont de quatre gènes codant des TBDTs (XCC0531, XCC2887, XCC3045 et XCC3408) et de deux gènes codant des N-acétylglucosamines kinases potentielles (NagK-IIA, NagKII-B) (Yang et al., 2006). Les TBDTs codés par les gènes XCC3046 et XCC2944 se trouvant en avale de deux gènes ayant une boîte de régulation NagR potentielle, pourraient également faire partie du régulon NagR. Nous avons mené une étude sur le rôle de chacun de ces acteurs dans l acquisition et l utilisation de GlcNAc, dans l adaptation de Xcc à la plante et dans la mise en place du pouvoir pathogène. Nous avons pu montrer que Xcc rencontre et utilise du GlcNAc lorsqu il est inoculé dans les vaisseaux du xylème et que ce GlcNAc provient de la plante. Nous avons également montré qu un locus comprenant des gènes codant des enzymes de dégradation de carbohydrates pouvant être impliquées dans la dégradation de glycanes de glycoprotéines, est impliqué dans la libération de GlcNAc in planta. L ensemble de ces travaux est regroupé dans un aricle récemment soumis pour publication et présenté ci-après. 67
129 Résultats N-acetylglucosamine: an unexpected substrate exploited by the plant pathogen Xanthomonas campestris pv. campestris during infection Alice Boulanger 1, Guillaume Déjean 1, Martine Lautier 1,2, Marie Glories 1, Matthieu Arlat 1,2 and Emmanuelle Lauber *1. 1 Laboratoire des Interactions Plantes Micro-organismes (LIPM), UMR CNRS-INRA 2594/441, F Castanet-Tolosan, France. 2 Université de Toulouse, UPS, 118 Route de Narbonne, F Toulouse, France. Running title: The GlcNAc utilization pathway of Xanthomonas * To whom correspondence should be addressed: Laboratoire des Interactions Plantes Microorganismes (LIPM), UMR CNRS-INRA 2594/441, F Castanet-Tolosan, France. Phone: (+33) Fax: (+33) [email protected] 68
130 Résultats Abstract Xanthomonas campestris pv. campestris (Xcc), the causal agent of black rot disease of Brassicaceae, is known for its ability to exploit plant compounds. This aptitude is correlated with the presence of specific CUT systems (Carbohydrate Utilization systems containing TonB-dependent transporters) devoted to the scavenging of plant carbohydrates. In this study, we identified a new Xcc CUT system involved in the exploitation of N-acetylglucosamine (GlcNAc) from plant origin. This GlcNAc CUT system, which is under the control of NagR and NagQ regulatory genes, can be divided into an upper pathway involved in the external generation and uptake through the outer membrane of GlcNAc-containing carbohydrates and a lower pathway corresponding to the uptake through the inner membrane and catabolism of GlcNAc. We show that this system is used during the infection of host plants. Indeed, a naga mutant, affected in GlcNAc catabolism and sensitive to this compound, is unable to grow in planta and to induce disease symptoms. This phenotype is reversed when mutations in the upper pathway are introduced in naga mutants, thus underlying the importance of the upper pathway in the generation of GlcNAc in planta. Based on glycoside hydrolase activities belonging to the upper pathway, we propose that glycans from glycoproteins might be the source of GlcNAc for Xcc during infection. Our comparative study shows that the Xcc CUT system is specifically conserved in phytopathogenic Xanthomonadaceae suggesting that the abiltity to exploit GlcNAc probably through the degradation of glycans of plant origin is a common feature of this bacterial family. Although GlcNAc is an important nutrient source for chitinolytic bacteria, the exploitation of this molecule by phytopathogenic bacteria was never suspected. Therefore, this work broadens the source of GlcNAc metabolized by bacteria and sheds new light on metabolic capabilities of plant pathogenic bacteria. 69
131 Résultats Author summary N-acetylglucosamine (GlcNAc) is an amino sugar that carries out important roles in a broad range of cells from bacteria to plants and animals. Most marine bacteria and insect pathogens have developed sophisticated mechanisms for the catabolism of the second most abundant biopolymer in nature, chitin, which is a GlcNAc homopolymer. However, whether non-chitinolytic bacteria find GlcNAc in their environment and what is the natural source of this molecule remain obscure. The data presented here suggest that the plant pathogenic bacterium Xanthomonas campestris pv. campestris (Xcc) encounters and exploits GlcNAc of plant origin during infection. Characterization of the Xcc GlcNAc utilization pathway and its complex regulatory network led to the identification of specific traits as compared to other bacteria and most notably the source of GlcNAc, i.e. glycans from plant glycosylated proteins. An outer membrane transporter and glycoside hydrolases belonging to the Xcc GlcNAc utilization pathway were shown to play a direct role in the generation of GlcNAc in planta. 70
132 Résultats Introduction N-acetylglucosamine (GlcNAc) is an amino sugar that carries out important roles in a broad range of cells from bacteria to humans. In bacteria, this amino sugar is utilized for the synthesis of cell surface structures such as the peptidoglycan [1], lipopolysaccharide in Gramnegative bacteria [2] and lipoteichoic acid in Gram-positive bacteria [3]. A polysaccharide containing β-1,6-linked GlcNAc which plays an important role in biofilm formation in Escherichia coli and Staphylococcus epidermidis [4-6], also promotes transmission of Yersinia pestis to the mammalian host [7] and impacts S. epidermidis colonization, virulence and host immune evasion [8,9]. In Caulobacter crescentus, GlcNAc polymers are important components of the holdfast structure [10,11] which is required for the permanent attachment of cells to their substrate [12]. In addition to these functions, GlcNAc also plays an important role in supplying carbon and energy to a variety of organisms including bacteria, by entering into the glycolytic pathway after being converted into fructose-6p [13,14]. Chitin, a homopolymer of β-1,4-linked GlcNAc, is the main component of cell walls of fungi as well as of cuticles and exoskeletons of worms, arthropods, mollusks and crustaceans [15]. Microorganisms have developed sophisticated mechanisms for the catabolism of this polymer, which is degraded by specific hydrolases [16]. Resultant monoand disaccharides are taken up through specific transporters [17,18]. Therefore, this polymer constitutes a natural source of GlcNAc for chitinolytic bacteria such as marine bacteria [19] and insect pathogens [20]. Although some specificities have been identified [21], the GlcNAc catabolic pathway, which is well characterized in E. coli [22-24], is conserved in both chitinolytic and non-chitinolytic bacteria [21,25,26]. This suggests that chitin is not the unique source of GlcNAc for bacteria. Another source derives from peptidoglycan recycling. For example, in E. coli, about 50% of this cell wall murein is broken down each generation [27,28]. Glycans from glycosylated proteins may also contain GlcNAc. Indeed, all N-linked glycans, which are attached to an asparagine residue, possess an invariant pentasaccharidic core, that contains two GlcNAc residues, and complex- and hybrid-type N-glycans contain additional GlcNAc residues [29]. Furthermore, O-linked glycans such as those present in mucins and typically linked via N-acetylgalactosamine to either a serine or a threonine residue, may possess additional GlcNAc residues [30,31]. Animal pathogens such as Enteroccocus faecalis, Streptococcus pneumoniae or S. oralis, are able to degrade glycan units to sustain growth [32-34]. In a comparative study of bacterial GlcNAc utilization pathways and regulatory networks, Yang and co-workers identified conserved and distinct features in chitinolytic and 71
133 Résultats non-chitinolytic bacteria including phytopathogenic Xanthomonas [21]. Xanthomonas campestris pv. campestris (Xcc), the causal agent of black rot disease of Brassicaceae, is known to encode extracellular enzymes which contribute to the pathogenicity of the bacterium by providing nutrients through degradation of plant cell walls, thus facilitating its spreading in plant tissues [35,36]. This remarkable feature likely reflects the presence of specific genetic programs devoted to the exploitation of nutrients present in the plant habitat. Indeed, a previous study showed the existence of specific CUT loci (Carbohydrate Utilization loci containing TonB dependent transporters) involved in the acquisition and utilization of plant carbohydrates [37]. These loci are characterized by the presence of genes coding for regulators, degradative enzymes, inner membrane transporters and outer membrane TonBdependent transporters (TBDTs). Interestingly, the putative GlcNAc utilization pathway identified in Xanthomonas strains by Yang and co-workers might represent a GlcNAc CUT system. This prompted us to further investigate this system and to determine whether it could play a role during plant infection. Results presented in this paper clearly reveal that Xcc encounters and utilizes GlcNAccontaining carbohydrates in planta during the infection process. A TBDT and glycoside hydrolases seem to play a direct role in the generation of GlcNAc in planta. Based on enzymatic activities of these glycoside hydrolases, we propose that glycans from plant glycosylated proteins could be the source of GlcNAc for this bacterium. We have characterized the regulatory network and the GlcNAc utilization pathway that we have separated into an upper pathway, i.e. generation of GlcNAc-containing carbohydrates and uptake through the outer membrane, and a lower pathway, i.e. uptake through the inner membrane and catabolism of GlcNAc to fructose-6p. Altogether, our results establish the existence of a GlcNAc CUT system in Xcc. 72
134 1,5 1,3 no addition GlcNAc (0.1%) Chitobiose (0.1%) Chitine (0.1%) 1,1 OD600 0,9 0,7 0,5 0,3 0, Time (h) Figure R1. Xanthomonas campestris pv. campestris (Xcc) utilizes N-acetylglucosamine and chitobiose as a carbon source. Xcc wild-type strain was cultivated in minimal medium containing 0.1% N-acetylglucosamine (GlcNAc), chitobiose or chitin. 2 1, , ,4 1.4 OD600 1, no addition Gluconate Glutamate Glycérol Glucosamine Maltose GlcNAc Xylose Glucose Sucrose 0, , , , Time (h) Figure S1. Growth of Xanthomonas campestris pv. campestris wild-type strain in the presence of various carbon sources at 10 mm. After an overnight growth in complete MOKA medium, cells were harvested, washed and resuspended in minimal medium. Indicated carbohydrates were added at a final concentration of 10 mm. GlcNAc: N-acetylglucosamine.
135 Résultats Results GlcNAc is a carbon and nitrogen source for Xcc We compared the growth rate of Xcc strain ATCC33913 in minimal medium supplemented with various carbon sources, such as glutamate, glucosamine, maltose, xylose, sucrose or glucose and also GlcNAc, chitobiose or chitin. After sucrose and glucose, GlcNAc was one of the best carbon sources for Xcc and its supplementation led to a similar growth rate as xylose (Figure S1) and chitobiose (Figure R1). In the presence of chitin, slight growth was observed (Figure R1), probably due to the presence of low amounts of free GlcNAc or chitobiose molecules. This result suggests that Xcc strain ATCC33913 is not able to efficiently degrade chitin. Therefore, contrary to most marine chitinolytic bacteria such as Vibrios [19], chitin is probably not the main GlcNAc source for Xcc during its life cycle. GlcNAc was also a nitrogen source for Xcc, since this bacterium could grow in nitrogen depleted minimal medium in presence of GlcNAc, whereas no growth was observed in the presence of glucose (data not shown). Description of Xcc genes belonging to the GlcNAc utilization pathway In proteobacteria, the expression of GlcNAc-specific genes is controlled by specific transcriptional regulators: NagC, mainly in enterobacteria and Vibrionales, NagR in Alteromonadales and Xanthomonadales and NagQ mainly in α- and β-proteobacteria and several γ-proteobacteria [21]. Interestingly, Xanthomonas strains are the only bacteria having two of these regulators, NagR and NagQ [21]. In Xylella, with completely sequenced genomes, only nagr is present while nagq is partially deleted suggesting gene loss during the evolution of this genus (Figure S2B). As described by Yang and co-workers [21], in Xcc one putative binding motif specific for NagQ (named NagQ-box) is localized upstream the nagq gene (XCC3414, Figure R2A). This gene is followed by genes coding for the proposed inner membrane transporter NagP (XCC3413), the regulator NagR (XCC3412), the GlcN-6P deaminase NagB-II (XCC3411) and the GlcNAc-6P deacetylase NagA (XCC3410). As these genes are clustered in the genome and proposed to be involved in the same function, i.e. GlcNAc catabolism, we named the Xcc locus from XCC3414 to XCC3410 the GlcNAc cluster. NagR-boxes (Figure R2A) are localized upstream of genes coding for two glucokinase-like proteins, NagK-II (XCC2886 and XCC2943) as well as upstream of genes coding for TBDTs (XCC0531, XCC2887, XCC3045 and XCC3408) [21]. These four TBDTs and the TBDT encoded by XCC2944 localized downstream of XCC2943 have been proposed to be involved in the uptake of GlcNAc through 73
136 A GlcNAc cluster TBDT nixa deacetylase naga regulator nagr regulator nagq TBDT naxa cytochrome P450 hydroxylase kinase nagk-iib ATP dep. RNA helicase trna nucleotidyl transferase nisin resistance nagb-ii nagp deaminase MFS transporter naxb TBDT nixc TBDT TBDT nixb hyp kinase nagk-iia α-lfucosidase nixe β-hexosaminidase nixg β-glucosidase nixi α-1,2 mannosidase nixk TTSS putative effector xopd hyp nixd TBDT nixf endo-β-n-acetyl glucosaminidase nixh β-mannosidase nixj hyp nixl β-galactosidase glycan cluster B XCC2888: NixE Fuc α(1,4) XCC2914 Gal β(1,3) NAG β(1,2) Man α(1,6) XCC2888: NixE Fuc α(1,3) XCC2895: NixL XCC2890: NixG Man β(1,4) NAG β(1,4) NAG (Asn) Protein Gal XCC2888: NixE β(1,3) NAG β(1,2) α(1,4) Fuc Man α(1,3) Xyl β(1,2) XCC2891: NixH XCC2889: NixF Figure R2. The Xanthomonas campestris pv. campestris N-acetylglucosamine CUT system and proposal model for N-glycans degradation. A. Genomic context of genes belonging to the GlcNAc utilization pathway. NagR-boxes are represented by black circles and the NagQ-box is represented by a red circle. Grey colour indicates a gene coding for a hypothetical protein and white colour indicates genes that do not belong to the GlcNAc CUT system. B. Proposed cleavage sites by enzymes encoded by the Xcc glycan cluster on a complex-type N-glycan with Lewisa epitopes. Residues conserved in all N-glycans are represented in black, residues found in all complex-type N-glycans are represented in dark grey and residues specific to complex-type N-glycans with Lewisa epitopes are represented in light grey. Cleavage sites proposed in the KEGG pathway database ( are depicted by plain arrows, whereas the cleavage site proposed in the present study is depicted by a dashed arrow. Asn: asparagine; Fuc: fucose; CUT system: Carbohydrate Utilization system containing TBDTs; Gal: galactose; hyp: hypothetical protein; Man: mannose; NAG: N-acetylglucosamine; nax: N-acetylglucosamine-associated in Xanthomonas; nix: N-acetylglucosamine-induced in Xanthomonas; TBDT: TonB-dependent transporter; TTSS: type three secretion system; Xyl: xylose.
137 Table S1. Putative function of enzymes encoded by the Xanthomonas campestris pv. campestris glycan cluster. XCC2888: nixe XCC2889: nixf XCC2890: nixg genome annotation a alpha-l-fucosidase, FucA1 conserved hypothetical protein beta-hexosaminidase, NahA GH family GH-29 GH-18 GH-20 alpha-l-fucosidase (EC ) chitinase (EC ) beta-hexosaminidase (EC ) endo-beta-n-acetylglucosaminidase (EC ) lacto-n-biosidase (EC ) Known activities of the GH family xylanase inhibitor beta-1,6-n-acetylglucosaminidase (EC ) concanavalin B narbonin Proposed EC number nd nd nd Other protein in the Xcc genome belonging to the same GH family XCC1251 (GH-29) Proposed activity and EC number alpha-l-fucosidase (EC ) beta-hexosaminidase (EC ) Other protein(s) with the same proposed function XCC1251 (PF01120; PF00754; TAT) XCC1283 (GH-3; NagZ) Domains (InterProScan Sequence Search) d PF01120; SM00812 PF00704; SM00636 PF00728 Reannotation e no no no Signal peptide cleavage position f XCC2891: nixh XCC2892: nixi XCC2893: nixj genome annotation a beta-mannosidase glucan 1,4-beta-glucosidase conserved hypothetical protein GH family GH-2 GH-3 beta-galactosidase (EC ) beta-glucosidase (EC ) beta-mannosidase (EC ) xylan 1,4-beta-xylosidase (EC ) beta-glucuronidase (EC ) beta-n-acetylhexosaminidase (EC ) Known activities of the GH family mannosylglycoprotein endo-betamannosidase (EC ) glucan 1,3-beta-glucosidase (EC ) exo-beta-glucosaminidase (EC ) glucan 1,4-beta-glucosidase (EC ) exo-1,3-1,4-glucanase (EC ) alpha-l-arabinofuranosidase (EC ) Proposed EC number nd nd nd Other protein in the Xcc genome belonging to the same GH family XCC1256 (EC ); XCC4116 (EC ); XCC3162 (GH-2) XCC1090 (GH-3; TAT); XCC1250 (GH-3); XCC1283 (GH-3); XCC1404 (GH-3); XCC1775 (GH-3) ; XCC3814 (GH-3); XCC4106 (GH-3) Proposed activity and EC number beta-mannosidase (EC ) Other protein(s) with the same proposed function Domains (InterProScan Sequence Search) d PF02836; PF02837; PF00703 PF00933; PF01915; PF07691 PF06824; TIGR01409 Reannotation e no no no Signal peptide cleavage position f XCC2894: nixk XCC2895: nixl XCC2914 genome annotation a conserved hypothetical protein beta-galactosidase, bga asparaginase, AspG GH family GH-92 GH-35 alpha-1,2-mannosidase (EC ) beta-galactosidase (EC ) Known activities of the GH family exo-beta-glucosaminidase (EC ) Proposed EC number nd EC Other protein in the Xcc genome belonging to the XCC1081 (GH-92); XCC3342 (GH-92); same GH family XCC4221 (GH-92) XCC1754 (GH-35); XCC2404 (GH-35) CAZy database b Proposed activity and EC number beta-galactosidase (EC ) asparaginase (EC ) Other protein(s) with the same proposed function XCC1256 (GH-2); XCC4116 (GH-2) KEGG pathwa y databa se c KE GG path way data CAZy database b KEGG pathway CAZy database b database c Domains (InterProScan Sequence Search) d PF07971; TIGR01409 PF01301 PF01112 Reannotation e no no 38 aa extension Signal peptide cleavage position f
138 Résultats the outer membrane [21]. We were not able to detect other NagR- or NagQ-boxes in the Xcc genome, matching the consensus motif described by Yang and co-workers [21], but we identified another TBDT gene (XCC3046) downstream of the XCC3045 TBDT gene, which might thus belong to the same operon. Furthermore, downstream of the XCC2887 TBDT gene and in the same orientation, we identified genes coding for several carbohydrate degradative enzymes (XCC2888 to XCC2895, Figure R2A) that might belong to the NagR regulon. All these genes, localized downstream NagR- or NagQ-boxes are proposed to belong to a GlcNAc utilization pathway. N-glycans: a proposed substrate for degradative enzymes belonging to the GlcNAc utilization pathway The putative function of the carbohydrate degradative enzymes encoded by XCC2888 to XCC2895 was examined by using the KEGG pathway database ( and the Carbohydrate-Active enzyme database (CAZy, This analysis confirmed that XCC2888 codes for a α- L-fucosidase, XCC2890 for a β-hexosaminidase, XCC2891 for a β-mannosidase, and XCC2895 for a β-galactosidase (Table S1). Over-expression of the latter protein in Xcc Xc17 strain leads to an increase in β-galactosidase activity [38]. All these enzymes, including the asparaginase encoded by XCC2914, were proposed in the KEGG pathway database to cleave glycosidic bonds found in N-glycans of N-glycoproteins. Furthermore, XCC2889 codes for a protein of the glycoside hydrolase GH-18 family, which includes chitinase (EC ) and endo-β-n-acetylglucosaminidase (EC ). This gene was annotated as chia in the Xcc genome strain B100 [39]. However, as shown above, Xcc strain ATCC33913 seems not to be able to use this polymer as a carbon source (see Figure R1). Therefore, and according to the putative function proposed by the KEGG pathway database for the other genes of the locus, we propose that this enzyme could be involved in the endohydrolysis of the N,N'- diacetylchitobiosyl units found in all N-glycans (Figure R2B). Finally, XCC2894 codes for an α-1,2-mannosidase (GH-29; EC ), which could cleave α-1,2 glycosidic bonds between two mannose residues found in high mannose-type N-glycans (data not shown), XCC2892 codes for a protein belonging to the glycoside hydrolase GH-3 family including β-glucosidase (EC ) and XCC2893, codes for a hypothetical protein. The role of the two latter proteins in the degradation of N-glycans could not be attributed. All these proteins from XCC2888 to XCC2895 possess a signal peptide (Table S1) as determined by using the SignalP server [40], suggesting that they are all translocated through the inner membrane to 74
139 Table R1. Relative expression ratios of genes belonging to the N -acetylglucosamine utilization pathway a WT GlcNAc ΔnagQ MME ΔnagR MME vs vs vs WT MME WT MME WT MME Gene ID Gene name Ratio (+/- SD) Ratio (+/- SD) Ratio (+/- SD) XCC3414 nagq 17.5 (1.4) nd 0.5 (0.04) XCC3413 nagp 7.5 (0.3) 2.7 (0.6) 0.8 (0.1) XCC3412 nagr 7 (0.7) 6.1 (1.7) nd XCC3411 nagb-ii 18 (1.9) 3.1 (0.2) 0.9 (0.1) XCC3410 naga 8.9 (1.4) 9.9 (0.3) 0.4 (0.28) XCC (0.3) nd nd XCC3408 nixa 15.6 (0.7) 0.3 (0.03) 7.8 (1.2) XCC0531 nixb 6 (0.4) 0.8 (0.03) 1.1 (0.5) XCC3045 naxa 0.4 (0.1) 0.8 (0.1) 0.3 (0.03) XCC3046 b naxb 0.25 (0.06) nd nd XCC2943 nagk-iib 115 (0.5) 1.7 (0.7) c 27 (7) c XCC2944 nixc 8.2 (0.1) 0.5 (0.06) 40 (14) XCC2886 b nagk-iia 2.8 (1) 0.9 (0.02) 4.9 (1) XCC2887 nixd 107 (12) 0.9 (0.6) 48 (15) XCC2888 nixe 62.3 (3.6) 0.7 (0.2) 31 (2) XCC2889 nixf 88.3 (12.7) 0.7 (0.01) 24 (2) XCC2890 nixg 33.1 (3.8) 1 (0.4) 2.8 (1.3) XCC2891 nixh 4 (0.2) 0.9 (0.1) 2.1 (0.2) XCC2893 nixj 17.5 (2.5) 0.6 (0.3) 0.9 (0.2) XCC2894 nixk 6.7 (0.1) 0.6 (0.2) 1.6 (0.3) XCC2895 nixl 8.5 (0.6) 0.7 (0.3) 1.8 (0.7) XCC2914 aspg 1 (0.01) 1.3 (0.5) 0.9 (0.3) nd: not determined; SD: standard deviation; WT: wild-type; GlcNAc: N -acetylglucosamine; nix : N - acetylglucosamine-induced in X anthomonas ; nax : N -acetylglucosamine-associated in X anthomonas. a From real-time quantitative reverse-transcriptase polymerase chain reaction perfomed in at least three independent experiments. Calculation of relative expression includes normalization against the 16S rrna endogenous control gene. b From β-glucuronidase assays performed in at least three independent experiments using pvo155 insertion mutants leading to transcriptional fusion with the promotorless uida gene. Insertions were made in the wild-type strain and for XCC2886, in the ΔnagR, and ΔnagQ deleted strains. c qrt-pcr expression values were obtained from nagr and nagq pvo155 insertion mutants instead of deletion mutants.
140 Résultats the periplasm or to the extracellular medium. XCC2895 is probably not secreted as no β- galactosidase activity is detected in the culture supernantent [38]. Although most of the enzymes encoded by this cluster are proposed by the KEGG pathway database to be involved in the degradation of N-glycan units, we cannot exclude a role in the degradation of other glycans. Therefore, the cluster from XCC2888 to XCC2895 was named the glycan cluster and was proposed to be involved in the de-glycosylation of glycosylated substrates such as glycoproteins or glycolipids, and especially N-glycoproteins. This hypothesis is strengthened by the presence of XCC2914 in the vicinity of the glycan cluster which codes for a putative asparaginase, an enzyme involved in the cleavage of N- glycoproteins between the asparagine residue of the protein and the first GlcNAc of the N- glycan. The identification of the glycan cluster suggests that in Xcc, glycans and especially N- glycans could be a source of GlcNAc. Therefore, we propose that Xcc possesses a GlcNAc pathway which encompasses degradation of glycan units, transport through outer and inner membranes and GlcNAc catabolism in the cytoplasm. To confirm this hypothesis, we tested whether these genes belonged to the NagR/NagQ regulon and whether their expression was influenced by GlcNAc. GlcNAc pathway genes are induced by GlcNAc The expression profile of genes which were hypothesized to belong to the GlcNAc pathway in the absence or in the presence of GlcNAc was monitored by quantitative real-time reverse transcriptase polymerase chain reaction experiments (qrt-pcr) in a wild-type background, or by β-glucuronidase expression assays using pvo155 insertion mutants. Except for TBDTs encoded by XCC3045 and XCC3046 genes, the nisin resistance gene XCC3409 and the asparaginase encoded by XCC2914, all the genes belonging to the GlcNAc utilization pathway, including genes belonging to the glycan cluster, were clearly induced in the presence of GlcNAc (Table R1). This result confirmed the connection between GlcNAc and nag genes as well as the glycan cluster. Based on these results, we proposed to name TBDT genes that are induced by GlcNAc and genes belonging to the glycan cluster, nix genes for N-acetylglucosamine-induced in Xanthomonas. The TBDT genes XCC3045 and XCC3046, which are not induced but rather slightly repressed by GlcNAc although they possess a NagR-box, were named nax genes for N-acetylglucosamine-associated in Xanthomonas (see Figure 2A). Both nix and nax genes are proposed to define an upper GlcNAc utilization pathway, including degradation of complex molecules and their uptake 75
141 Résultats through the outer membrane, whereas nag genes appear to belong to a lower GlcNAc utilization pathway, including transport of GlcNAc through the inner membrane and its catabolism (see Figure R10). One of the gene showing the highest induction level by GlcNAc (i.e. nixd) was mutated by insertion of the suicide plasmid pvo155 leading to transcriptional fusion with the promoterless uida reporter gene. β-glucuronidase expression assays showed that induction in the presence of GlcNAc was detected at concentrations ranging from 5 µm to 10 mm, maximal induction being observed at 50 µm (data not shown). Furthermore, induction was also observed with glucosamine (GlcN) but with a lower magnitude and at higher concentrations of GlcN. No induction was observed below 250 µm GlcN (data not shown). Similar results were previously observed for E. coli nag genes [41]. NagQ and NagR are GlcNAc pathway specific regulators To understand the precise role of NagQ and NagR regulators in the expression of genes belonging to the Xcc GlcNAc utilization pathway, we examined the expression of each gene in the wild-type background as compared to nagq or nagr mutant backgrounds. We constructed insertion and deletion mutants of these two regulators but we mainly used deletion mutants to avoid polar effects since these genes might belong to an operon (from XCC3414 to XCC3410, see Figure R2A). All genes belonging to the GlcNAc cluster and localized downstream the NagQ-box were clearly induced in the nagq mutant (Table R1), suggesting that NagQ is a repressor and revealing the functionality of the NagQ-box. It is worth noting that NagQ represses the expression of the nagr regulatory gene. This latter regulator, which belongs to the LacI repressor family, was found to repress most of the genes located downstream of a NagR-box, including the TBDT gene nixd and degradative enzyme genes from nixe to nixh (Table R1), thus confirming the relationship between the glycan cluster and the GlcNAc cluster. Therefore, most of the NagR-boxes seem to be functional and NagR mainly regulates the expression of genes involved in the upper pathway plus genes potentially involved in GlcNAc phosphorylation, i.e. nagk-ii genes. Surprisingly, nixb, nixj, nixk and nixl genes seem not to be controlled by NagR in these experiments, although they are induced in the presence of GlcNAc (Table R1). However, as presented below, the β-galactosidase activity encoded by nixl was higher in the ΔnagR background as compared to that observed in the wild-type background, suggesting that the expression of nixl is repressed by NagR. These contradictory 76
142 Figure R3. Glycoside hydrolases encoded by the Xanthomonas campestris pv. campestris glycan cluster are functional and controlled by NagR. Enzymatic activities were checked using specific 4-nitrophenyl glycosides: A. 4-Nitrophenyl b-d-mannopyranoside, substrate for b-mannosidase activity, related to NixH. B. 4-Nitrophenyl b-d-galactopyranoside, substrate for b-galactosidase activity, related to NixL. C. 4-Nitrophenyl a-l-fucopyranoside, specific for a-l-fucosidase activity, related to NixE. D. 4-Nitrophenyl N-acetyl-b-D-glucosaminide, specific for b-hexosaminidase activity, related to NixF and/or NixG. E. 4-Nitrophenyl a-d-mannopyranoside, specific for a-mannosidase activity, related to NixK.
143 Résultats results could be due to the instability of the polycistronic mrna encompassing the entire glycan cluster and the TBDT gene nixd as compared to the stability of the proteins. Nix enzymatic activities are controlled by NagR Enzymatic activities of several proteins encoded by the glycan cluster were analyzed as described in Materials and Methods, by using 4-nitrophenyl glycosides synthetic substrates. In all cases, the enzymatic activity predicted in the glycan cluster was detected and was enhanced in the ΔnagR mutant as compared to the wild-type strain (Figure R3). Thus, all these activities appear to be under the control of NagR. In the strain deleted for the entire glycan cluster (ΔnixE-nixL), β-mannosidase and β- galactosidase activities, corresponding to NixH and NixL respectively, were drastically reduced (Figure R3A and RB). This result suggests that these two enzymatic activities are mainly encoded by nixh and nixl belonging to the glycan cluster. This was confirmed by studying ΔnixH (Figure R3A) and ΔnixL (Figure R3B) mutants. The residual β-galactosidase activity observed could be due to other β-galactosidases encoded in the Xcc genome such as XCC1256 or XCC4116 as proposed in the KEGG pathway and in the CAZy databases (see Table S1) or to XCC1754, a β-galactosidase recently identified in the Xcc strain Xc17 [42]. Induction of the α-l-fucosidase and α-mannosidase activities observed in the nagr background was lost when the glycan cluster was deleted (ΔnixE-nixL nagr::pvo strain, see Figure R3C and E), thus suggesting that these NagR-dependent activities are due to enzymes encoded by the glycan cluster. The α-l-fucosidase NagR-dependent activity was due to NixE, as no induction was observed in the ΔnixE nagr::pvo double mutant (Figure R3C). The basal α-l-fucosidase activity observed could be due to XCC1251, a protein belonging to the same GH family (see Table S1). Similarly, the basal α-mannosidase activity observed is probably due to XCC1081, XCC3342 and/or XCC4221 (see Table S1). The 4-Nitrophenyl N-acetyl-β-D-glucosaminide glycoconjugate is a putative substrate for both the β-hexosaminidase encoded by nixg and the endo-β-n-acetylglucosaminidase encoded by nixf. Hydrolysis of this substrate was significantly reduced in the ΔnixE-nixL mutant as compared to the wild-type strain (Figure R3D), suggesting that part of the activity observed in the wild-type strain is due to the glycan cluster. In the ΔnagR strain, degradation of the glycoconjugate was enhanced. However, in the nagr mutant background, this enhancement was more pronounced and not reduced when the glycan cluster was deleted (ΔnixE-nixL nagr::pvo double mutant). This result suggests that this NagR-dependent 77
144 Table R2. [ 14 C]N -acetylglucosamine transport rates related to Xanthomonas campestris pv. campestris wild-type strain (Xcc 568). Xcc strain Genotype Function Time (min) b % Transport mean (+/- SD) Xcc 568 a (6) XP124 ΔnagP inner membrane (0.4) transporter XP153 ΔnagP pc-nagp (4) Xcc 568 a (16) XP059 nixa ::pvo TBDT (1) XP010 nixb ::pvo TBDT (10) XP041 nixc ::pvo TBDT (47) XP040 nixd ::pvo TBDT (5) XP044 naxa ::pvo TBDT (21) XP108 XCC0320 ::pvo putative porin (9) XP109 XCC0359 ::pvo putative porin (12) XP110 XCC1529 ::pvo porin O (8) XP111 XCC2373 ::pvo putative porin (3) XP112 XCC2589 ::pvo porin O (12) XP113 XCC3241 ::pvo porin (4) XP114 XCC3347 ::pvo porin O (12) XP115 XCC3353 ::pvo porin O (9) a Xcc 568: wild type strain. b Time after [ 14 C]N -acetylglucosamine addition.
145 Résultats activity is not encoded by the glycan cluster. Therefore it seems that the NagR-regulon could be broader. A putative β-hexosaminidase candidate could be NagZ encoded by XCC1283 as proposed in the KEGG pathway database (see Table S1). In E. coli, this β-nacetylglucosaminidase hydrolyzes β-1,4 glycosidic bounds between GlcNAc and anhydro-nacetylmuramic acid during the recycling of cell wall muropeptides [43]. An insertion mutant in nagz displayed a similar enzymatic activity as the wild-type strain (Figure R3D). Thus, this protein seems not to be involved in the degradation of the substrate tested. All these experiments confirm the linkage between NagR and consequently GlcNAc and glycoside hydrolase activities such as β-mannosidase, β-galactosidase, β-hexosaminidase, α-l-fucosidase and α-mannosidase. Furthermore, proteins encoded by the Xcc glycan cluster seem to play a central role in generating these enzymatic activities. Therefore, these results reinforce the hypothesis that complex glycans which contain various glycosidic bonds could be substrates for enzymes encoded by the glycan cluster. Complete degradation of GlcNAc-containing glycan units should lead to the generation of free GlcNAc that should be transported through the outer membrane of the bacterium. Free GlcNAc passively diffuses through the outer membrane In Xcc, at least six TBDTs belong to the GlcNAc utilization pathway. To analyze the involvement of these active transporters in the uptake of free GlcNAc, we compared the uptake rate of [ 14 C]GlcNAc obtained for the Xcc wild-type strain and for insertion mutants in each of nix and nax TBDT genes. Except for the nixa mutant, which showed a slightly but significant reduced uptake level (90% of the value obtained for the wild-type strain), none of the tested TBDT mutants was significantly affected in the uptake of GlcNAc (Table R2). Bacterial growth of strains carrying mutations in the nix and nax TBDT genes in the presence of free GlcNAc at 10 mm was similar to the growth rate obtained for the wild-type strain (data not shown), confirming that none of these TBDTs is required for the utilization of free GlcNAc in liquid cultures. Concentration-dependent GlcNAc transport experiments showed kinetic values with a slow rate ranging between 5 and 50 µm GlcNAc, defining a K d value of µm (data not shown), which reflects passive diffusion rather than an active uptake. Indeed, this K d value is in a similar range to the K d value obtained for the E. coli LamB maltoporin with maltodextrins having a degree of polymerization from 4 (K d = 300 µm) to 6 (K d = 75 µm) [44]. Furthermore, this K d value is more than 100-fold higher than the estimated K d value observed 78
146 OD , , , , ,5 WT (-NA (-GlcNAc) G) WT (+NAG) (+GlcNAc) ΔnagP DnagP (+GlcNAc) (+NAG) ΔnagK-IIAB DnagK-II (+NAG) (+GlcNAc) ΔnagQ-nagA D (+NAG) (+GlcNAc) ΔnagB-II DnagB-II (+GlcNAc) (+NAG) ΔnagA DnagA (+GlcNAc) (+NAG) Figure R4. Xanthomonas campestris pv. campestris Nag proteins are involved in the utilization of N-acetylglucosamine. Bacterial strains were cultivated in minimal medium containing 10 mm of N- acetylglucosamine (GlcNAc) , , , , Time (h) Carbohydrate Concentration (µm) % of control mean (+/- SD) Control No addition 100 (5) N -acetylglucosamine (5) 5 97 (1) (1) (2) N -acetylglucosamine-6p (5) (2) (4) (4) Glucosamine (6) 5 93 (3) (3) (0) Chitobiose (6) 5 74 (5) (1) (4) Glucose (3) 5 97 (4) (3) (5) Galactose (7) 5 99 (3) (5) (5) Mannose (4) 5 98 (2) (1) (5) Fructose (5) 5 97 (4) (3) (4) Xylose (6) (2) (5) (11) Sucrose (5) (1) (5) (7) Table S2. Inhibition of [ 14 C] N- acetylglucosamine uptake by various carbohydrates in Xanthomonas campestris pv. campestris wild-type strain. Cells were harvested after an incubation of 1 hour. Standard deviations (SD) were calculated from three independent experiments.
147 Résultats for transport of GlcNAc through the TBDT CC0446 in Caulobacter crescentus [45]. Thus, in Xcc, free GlcNAc uptake through the outer membrane seems to occur by passive diffusion, mediated partially by the NixA TBDT and probably via porins. Therefore, in a second set of experiments, we analyzed the involvement of Xcc porins in the transport of this molecule. We indentified 8 putative porins in the Xcc genome. Insertion mutants were obtained for all of the corresponding genes and none of these mutants was affected in GlcNAc uptake (Table R2). Furthermore, none of these genes was induced in the presence of GlcNAc, as compared to other carbon sources (data not shown). All these results suggest that in Xcc, none of the outer membrane transporters tested seem to play a major role in free GlcNAc uptake. However, TBDTs and porins might also have redundant functions. NagP is the unique GlcNAc inner membrane transporter NagP belongs to the non-phosphorylating major facilitator family inner membrane transport system (MFS). The ΔnagP strain is impaired in growth on GlcNAc (Figure R4), suggesting that this transporter could be involved in the uptake of GlcNAc through the inner membrane. To confirm this hypothesis, we performed uptake experiments using [ 14 C]GlcNAc. The uptake rate of radiolabelled GlcNAc obtained for the ΔnagP strain reached only 1.2% of the value obtained for the wild-type strain (Table R2), showing that GlcNAc translocation in this mutant strain is severely impaired. In the complemented strain, when NagP was supplied in trans on a constitutive expression plasmid, GlcNAc transport capacity of the mutant strain was restored (Table R2), confirming that NagP is involved in GlcNAc transport through the inner membrane. To our knowledge, this is the first documented report of bacterial GlcNAc uptake through a MFS transport system. Competition experiments of [ 14 C]GlcNAc uptake in the presence of variable amounts of unlabelled GlcNAc or other carbohydrates (Table S2) showed that GlcNAc, glucosamine and chitobiose, inhibit GlcNAc uptake to a similar degree. This result suggests that NagP can also transport these GlcNAc-related molecules. However, inhibition of GlcNAc uptake by chitobiose could either be due to the chitobiose molecule itself or to its degradation product, i.e. GlcNAc. Interestingly, in E. coli, GlcNAc, glucosamine and chitobiose are transported through the inner membrane by three different transporters belonging to the phosphotransferase system (PTS), NagE [46], ManXYZ [47] and ChbABC [48] respectively. However, in this bacterium, GlcNAc is also taken by the ManXYZ PTS system and GlcN can also be taken up by the glucose-specific transporter encoded by ptsg [47]. 79
148 Figure R5. Xanthomonas campestris pv. campestris NagK-II enzymes are involved in the phosphorylation of N-acetylglucosamine. A. Growth curves of mutant strains cultivated in minimal medium supplemented (+) or not (-) with N-acetylglucosamine (GlcNAc). WT: wild-type strain. B. In vitro GlcNAc kinase assay using cell-free extracts based on the NAD+/NADH ratio (see Materials and Methods). The activity obtained in a medium depleted in ATP was subtracted. Strains were cultured in minimal medium supplemented with 10 mm GlcNAc to induce the expression of nagk-ii genes. Error bars represent the standard deviation obtained from 4 independent experiments.
149 Résultats NagK-IIA is the major GlcNAc kinase In E. coli, GlcNAc phosphorylation occurs concomitantly to its uptake through the PTS transporter system. On the contrary, the Xcc NagP inner membrane transporter is a nonphosphorylating transport system. Therefore, in this bacterium, phosphorylation might be the first cytoplasmic step of GlcNAc catabolism. Xcc encodes three proteins belonging to the glucokinase family: XCC2137, XCC2886 and XCC2943. Recently, it was demonstrated that the ortholog of XCC2137 in Xcc strain 8004 (XC1976) is responsible for the phosphorylation of glucose [49]. Based on genome context evidence [21] and regarding the finding that they belong to the NagR regulon (present work), we examined whether the two proteins XCC2886 (named NagK-IIA) and XCC2943 (named NagK-IIB, Figure R2A) are involved in GlcNAc utilization and whether they could be GlcNAc kinases. The double mutant ΔnagK-IIAB was clearly affected in bacterial growth on GlcNAc (Figure R4 and Figure R5A). The single mutant ΔnagK-IIA was also affected but to a lesser extent (Figure R5A). Finally, the single mutant ΔnagK-IIB was found to have a growth rate similar to that of the wild-type strain (Figure R5A), suggesting that this protein is not required for GlcNAc utilization in Xcc. However, growth of the double mutant ΔnagK-IIAB on GlcNAc was restored when either nagk-iia or nagk-iib were over-expressed in trans from an expression plasmid (data not shown). These results suggest that NagK-IIA plays a major role in GlcNAc utilization, but NagK-IIB, which is not essential, also participates in the catabolism of this molecule. In a second set of experiments, GlcNAc kinase activity from wild-type and mutants cell-free extracts was measured by a kinase enzyme-linked assay, based on the NAD + /NADH ratio (see Materials and Methods). In the ΔnagK-IIAB strain, GlcNAc kinase activity was reduced to about 41% of the activity obtained for the wild-type strain (Figure R5B). The high remaining GlcNAc kinase activity observed for the double mutant could be due to the presence of residual ADP or pyruvate in crude extracts used in these experiments. GlcNAc kinase activity was restored when either nagk-iia or nagk-iib were supplied in trans on an expression plasmid, suggesting that both of these proteins are involved in GlcNAc phosphorylation. The activity obtained for both single mutants was not significantly different than the activity obtained for the wild-type strain. In both cases, complementation with the corresponding gene cloned on an expression plasmid led to an activity corresponding to more than 160% of the value obtained for the wild-type strain. This enhanced activity could be due to an over-expression of the GlcNAc kinase from the complementing plasmid. 80
150 Figure S2. Conservation of genes belonging to the N-acetylglucosamine (GlcNAc) utilization pathway among completely sequenced Xanthomonadaceae. Homologous genes are marked by matching colors. A. Conservation of the glycan cluster. B. Conservation of the GlcNAc cluster. C. Conservation of the region surrounding the nagk-iib gene.
151 A , , , ,2 Glucose (-) Glucose (+) Xylose (-) Xylose (+) Gluconate (-) Gluconate (+) B OD , , , , , ,2 10 µm 50 µm 250 µm 10 µm 50 µm 250 µm D Bacterial density [log (cfu/ml)] 9, , , , , , , , , ,8 7.8 WT Wild-type DnagA ΔnagA naga::pvo OD ,8 GlcNAc 0.6 0, , , Time (h) C Time (h) E Bacterial density [Log (cfu/ml)] Time (h) 10, , , , , ,0 8.0 WT Wild-type DnagA ΔnagA ampg::pvo DnagA ΔnagA ampg::pvo 7, Time (h) Figure R6. Xanthomonas campestris pv. campestris naga mutants are sensitive to N- acetylglucosamine, in vitro. A. Effect of the addition of N-acetylglucosamine (GlcNAc) on growth of the DnagA mutant cultivated in minimal medium containing various carbon sources at 20 mm. After 4h of growth, media were supplemented (+) or not (-) with N-acetylglucosamine at 10 mm. B. Effect of different concentrations of N-acetylglucosamine on growth of the DnagA (plain lines) and naga::pvo (dashed lines) mutants. Cells were grown in minimal medium containing indicated concentrations of GlcNAc. C. Effect of secondary mutations on GlcNAc sensitivity of the naga::pvo mutant. Strains were streaked on a minimal medium plate containing 10 mm of N-acetylglucosamine. 1: wild-type strain; 2: naga::pvo; 3: DnagP; 4:DnagP/nagA::pVO; 5: DnagK-IIAB; 6: DnagK-IIAB/nagA::pVO. A picture was taken after 48 hours of growth. D. In vitro bacterial density of naga deletion (DnagA) and insertion (naga::pvo) mutants during growth in minimal medium. Each data point represents the mean and the standard deviation calculated from two independent experiments. E. In vitro bacterial density of the naga deletion mutant (DnagA), an insertion mutant in ampg (ampg::pvo) and a double mutant DnagA ampg::pvo, during growth in minimal medium. Each data point represents the mean and the standard deviation calculated from two independent experiments.
152 Résultats These results suggest that NagK-IIA is the major GlcNAc kinase in Xcc, whereas NagK-IIB is also a GlcNAc kinase but seems to play a minor role in GlcNAc utilization during bacterial growth in liquid cultures containing free GlcNAc. Almost all sequenced Xanthomonas strains encode these two proteins. However, in X. oryzae pv. oryzae, the ortholog of XCC2943 contains several frame shifts suggesting that the encoded protein is not functional. Furthermore, this gene is absent in Xylella strains (Figure S2C). These observations suggest that this gene has been lost during the evolution of Xylella and X. oryzae pv. oryzae. naga and nagb-ii mutants are sensitive to GlcNAc The two next steps in GlcNAc catabolism involve the NagA deacetylase which catalyses the conversion of GlcNAc-6P into GlcN-6P and the NagB-II deaminase which is responsible for deamination and isomerization of GlcN-6P to fructose-6p (see Figure R10). These two enzymatic activities have been already characterized in Shewanella oneidensis strain MR-1 [21]. Furthermore, NagA and NagB-II are well conserved in Xcc (51% identity, 66% similarity and 46% identity, 60% similarity respectively with the corresponding S. oneidensis genes). Therefore, in this study, we did not study enzymatic activities of Xcc NagA and NagB-II, but focused on the characterization of Xcc mutants in these genes. A Xcc ATCC33913 strain mutated in the naga gene exhibited a rapid inhibition of growth when GlcNAc was added to the medium (Figures R4 and R6A). Such a phenomenon, previously observed in E. coli [50,51], has been proposed to be due to the accumulation of GlcNAc-6P, thus leading to pentose starvation, resulting in cessation of growth [52]. Contrary to what was observed in E. coli [52], this amino sugar sensitivity was still observed when gluconate or xylose was added to the medium (Figure R6A). However, Xcc seems to be less sensitive to GlcNAc than E. coli, as complete inhibition of Xcc growth was observed at 1 mm (data not shown), whereas 12.5 µm is sufficient for E. coli [52]. Intriguingly, the naga insertion mutant seemed to be less sensitive to GlcNAc than the ΔnagA deletion mutant, since significant differences in inhibition of growth between these two strains were observed for concentrations ranging from 10 µm to 250 µm of GlcNAc (Figure R6B). As naga is the last gene of the operon, this difference is not due to a polar effect in the expression of a downstream gene. Due to the location of the pvo155 insertion, a small peptide (corresponding to the N-terminal 78 aa) could be synthesized in the naga::pvo insertion mutant, that could have an effect on GlcNAc sensitivity. 81
153 Résultats As observed for the ΔnagA strain, the ΔnagB-II mutant also exhibited sensitivity when grown on GlcNAc, but to a lesser extent. Indeed, no sensitivity was observed below 10 µm (data not shown) and at 10 mm, a very slow growth was still observed (Figure R4). Differences in sensitivity observed for the nagb-ii mutant as compared to the naga mutant could be due to the gradual assimilation of GlcN-6P in the cell, thus limiting its accumulation, as previously proposed for E. coli [52]. In complemented strains, bacterial growth was restored. However, to observe complete complementation of the ΔnagB-II strain, induction of the expression of the corresponding gene by the addition of isopropyl-beta-thio-galactoside (IPTG) was required (data not shown). In the Xcc naga mutant background, when the inner membrane transporter was absent (ΔnagP naga::pvo double mutant) or when the two GlcNAc kinases were mutated (ΔnagK- IIAB naga::pvo triple mutant), sensitivity to GlcNAc was abolished (Figure R6C), showing that this phenotype requires entry and phosphorylation of GlcNAc in the bacterial cell. These results confirm that Xcc is able to utilize free GlcNAc as a carbon and nitrogen source. However, questions remain about the origin of GlcNAc exploited by Xcc, whether this compound is used by the bacterium during the interaction with plants and if so, what is the signalling molecule responsible for the induction of the system? As described above, Xcc codes for two GlcNAc regulators, NagR and NagQ. Do they respond to the same molecule? NagR and NagQ have distinct signalling molecules Metabolic operons controlled by repressors require a signalling molecule to relieve the repression. In E. coli, expression of nag genes is under the control of NagC [41], and GlcNAc-6P was shown to be the signalling molecule of this repressor [51]. In this bacterium, accumulation of GlcNAc-6P in a naga mutant is correlated with derepression of the nag regulon [51]. In Xcc, two regulators are involved in the regulation of genes belonging to the GlcNAc pathway (see above). To identify the intracellular signalling molecules of NagR and NagQ, we checked the expression levels of GlcNAc utilization pathway genes by qrt-pcr, in mutants altered in two consecutive steps of this pathway, i.e. GlcNAc phosphorylation and GlcNAc-6P deacetylation. In the ΔnagK-IIAB double mutant, GlcNAc is not phosphorylated and is therefore expected to accumulate when cells are cultured on this carbon source. In this mutant, all the NagR-regulated genes, including all the nix genes that belong to the upper pathway, were still 82
154 A B Relative expression level (x100) (-) (+) WT mme WT nag WT (-) (+) (-) (+) (-) (+) (-) (+) WT ΔnagK-IIAB WT ΔnagK-IIAB C (-) (+) (-) (+) (-) (+) WT ΔnagK-IIAB ΔnagA Figure R7. N-acetylglucosamine and N-acetylglucosamine-6P are the signalling molecules of NagR and NagQ respectively. A. Expression of nixc, a NagR-regulated gene. Similar profiles were obtained for nixb and nixd. B. Expression of nixf, a NagR-regulated gene. Similar profiles were obtained for nixa, nixe, nixg, nixh, nixj, nixk and nixl. C. Expression of nagp, a NagQ-regulated gene. Similar profiles were obtained for nagq, nagr and nagb-ii and for naga in wild-type and DnagK-IIAB backgrounds. From real-time quantitative RT-PCR (qrt-pcr) performed in at least three independent experiments on RNA extracted from the wild-type strain (WT), nagk-iiab or naga deleted strains cultivated in minimal medium supplemented (+) or not (-) with N-acetylglucosamine (GlcNAc) at 10 mm. Calculation of relative expression includes normalization against the endogenous control gene 16S RNA.
155 Résultats highly induced in the presence of GlcNAc as compared to the expression obtained for the wild-type strain cultivated in minimal medium without GlcNAc (see Figure R7A and RB for representative examples of the two expression profiles obtained). Thus, even in the absence of GlcNAc kinases, repression caused by NagR was still relieved by the addition of GlcNAc in the medium, suggesting that the signalling molecule specific to NagR, is present in the ΔnagK-IIAB double mutant strain, and could therefore be GlcNAc. On the other hand, genes belonging to the GlcNAc cluster showed a different expression profile. Indeed, in the ΔnagK-IIAB double mutant, none of these genes were derepressed in the presence of GlcNAc, as compared to the wild-type strain (Figure R7C). Thus, it seems that the signalling molecule specific to NagQ is not produced in the absence of GlcNAc kinases, suggesting that it is generated later in the GlcNAc pathway. In the naga deleted strain, the GlcNAc pathway is blocked after GlcNAc phosphorylation thus provoking GlcNAc-6P accumulation. When this strain was cultivated on GlcNAc, all the NagQ-regulated genes were induced as compared to the wild-type strain cultivated in minimal medium (Figure R7C). Thus, in this context, the signalling molecule specific to NagQ is still produced and could therefore be GlcNAc-6P. Altogether, these results suggest that in Xcc, NagR and NagQ have distinct signalling molecules belonging to the same metabolic pathway that is GlcNAc and GlcNAc-6P respectively. Generation of signalling molecules during peptidoglycan recycling NagR-regulated genes in the ΔnagK-IIAB background and NagQ-regulated genes in the ΔnagA background are induced irrespective to the presence or absence of GlcNAc in the medium (see Figure R7). This high expression level despite the absence of GlcNAc in the medium could be due to the liberation and accumulation of GlcNAc and GlcNAc-6P respectively during peptidoglycan recycling. Indeed, in E. coli and probably in other Gram negative bacteria, almost 50 % of the peptidoglycan, which contains a large fraction of GlcNAc, is broken down and recycled at each generation [27,28] and in this bacterium, NagA was confirmed to play a role in murein recycling [53]. To confirm this hypothesis, we analyzed the survival of naga mutants grown in minimal medium without GlcNAc. During the first hours of growth, ΔnagA and wild-type strains showed a similar growth (Figure R6D). At the entry into the stationary phase, the ΔnagA strain displayed a complete inhibition of growth as compared to the wild-type strain, whereas the naga::pvo strain exhibited a similar growth to that of the wild-type strain (Figure R6D). 83
156 A ,5 Disease index 2, , dpi 5 dpi 6 dpi 7 dpi , ,5 1 0, ,5 0 WT Wild-type DnagA ΔnagA DnagA ΔnagA pcnaga pc-naga DnagB-II ΔnagB-II DnagB-II ΔnagB-II pcnagb-ii pc-nagb-ii 0 WT Wild-type naga::pvo naga::pvo DnagP ΔnagP DnagP ΔnagP naga::pvo naga::pvo DnagK-IIAB DnagK-IIAB ΔnagK-IIAB ΔnagK-IIAB naga::pvo naga::pvo DnagA ΔnagA AmpG::pVO ampg::pvo DnagA ΔnagA AmpG::pVO ampg::pvo Bacterial strain B Wild-type C 8 ΔnagA Wild-type ΔnagA ΔnagA/ pc-naga Bacterial density [log (cfu/cm2)] WT Wild-type D3410 ΔnagA D3410 ΔnagA/ p3410 pc-naga Days post inoculation (dpi) Figure R8. Xanthomonas campestris pv. campestris naga and nagb-ii mutants are affected in pathogenicity. A. Disease index after inoculation on Arabidopsis thaliana ecotype Sf-2. Disease symptoms were scored 4 to 7 days after inoculation. Each leaf was individually scored as: no symptom=0; weak chlorosis surrounding the wound sites=1; V-shaped chlorosis=2; necrosis=3; leaf death=4. The represented average disease scores and the standard deviations were calculated from the values of four plants with four inoculated leaves per plant. B. Symptoms observed on Bartolo cabbage (upper and middle panels) and on Arabidopsis thaliana ecotype Sf-2 (lower panels). C. Internal growth curves (IGC) after inoculation on Arabidopsis thaliana ecotype Sf-2.
157 Résultats In E. coli, peptidoglycan degradation products, i.e. anhydro-muropeptides, are transported across the inner membrane into the cytoplasm via AmpG permease [28,54]. A protein showing homology to this inner membrane transporter is encoded by the Xcc genome and named AmpG (XCC3845; 34 % identity, 52 % similarity with the E. coli AmpG permease). Interestingly, bacterial growth of the Xcc ΔnagA ampg::pvo double mutant in minimal medium without GlcNAc was comparable to the growth observed for the wild-type strain (Figure R6E). Therefore, when ampg is mutated, deletion of naga gene did not lead to inhibition of growth at the entry into the stationary phase. This result suggests that inhibition of growth observed for the Xcc ΔnagA strain at the entry into the stationary phase is due to GlcNAc sensitivity during peptidoglycan recycling via the AmpG permease. The difference in growth rate observed at the entry into the stationary phase for the naga deletion and insertion mutants (see above, Figure R6D) could be due to the lesser GlcNAc sensitivity observed for the naga::pvo strain as compared to the ΔnagA strain grown at low GlcNAc concentrations (see above, Figure R6B). naga and nagb-ii mutants are altered in pathogenicity To determine the importance of the Xcc GlcNAc pathway during the infection process, pathogenicity tests were performed with mutants in various genes belonging to this pathway on susceptible plants such as Arabidopsis thaliana ecotype Sf-2 or Bartolo cabbage. Deletion of the entire GlcNAc cluster and mutations in nix or nax genes did not significantly affect disease development (data not shown). However, we observed a significant delay in symptom development with the nagb-ii deleted strain (Figure R8A), and no symptom was observed with the naga mutants after inoculation either by piercing of the central vein (Figure R8A and R8B) or by infiltration of the leaf parenchyma (data not shown). In Xcc strain 8004, it has already been reported that a naga mutant displays a reduced virulence [55]. Finally, none of the mutants were affected in hypersensitive response (HR) on the resistant pepper cultivar ECW-10R (data not shown). The absence of symptoms observed for the ΔnagA mutant on susceptible plants was due to a deficiency in bacterial growth in planta, as population of the strain rapidly decreased and, after 7 days, the level of population obtained for the ΔnagA mutant was 2 to 3 orders of magnitude lower than that of the wild-type strain (Figure R8C). Similar results were obtained for the naga::pvo insertion mutant, but the level of population obtained was only 1 order of magnitude lower than the population reached by the wild-type strain (data not shown). In the ΔnagA/pC-nagA complemented strain, both bacterial growth and disease development were 84
158 Résultats restored, confirming that the phenotype of the mutant is correlated with the absence of the NagA protein (Figure R8). As mentioned above, the ΔnagB-II mutant is clearly delayed in symptom development (see Figure R8A). A similar delay was still observed when nagb-ii was supplied in trans on an expression plasmid (ΔnagB-II/pC-nagB-II, Figure R8A). This absence of complementation observed in planta could be due to the expression level of the protein, since to obtain complete complementation in vitro, IPTG must be added to the medium (data not shown). Absence of symptoms for the naga mutants is due to GlcNAc from plant As mentioned above, absence of symptoms for naga mutants is due to a deficiency in bacterial growth. In the naga::pvo background, when the NagP inner membrane transporter was absent (ΔnagP naga::pvo double mutant) or when the two GlcNAc kinases were mutated (ΔnagK-IIAB naga::pvo triple mutant), disease was restored (Figure R8A). These results clearly show the linkage between the absence of symptoms for this naga mutant and GlcNAc entry into the cytoplasm of the bacterium and its phosphorylation. Therefore, the absence of symptoms for the naga mutants probably reflects sensitivity to GlcNAc encountered during the infection process. For the ΔnagA ampg::pvo mutant, no symptoms were observed (Figure R8A). Therefore, the GlcNAc sensitivity observed for this strain was probably not due to the recycling of GlcNAc-containing muropeptides. Furthermore, as mentioned above, the naga::pvo insertion mutant seems not to be sensitive to GlcNAc generated by the bacterium during its growth. Therefore, GlcNAc sensitivity observed in planta for the naga::pvo and the ΔnagA ampg::pvo strains is probably due to GlcNAc generated from the plant. Since the naga::pvo mutant is not sensitive to bacterial-derived GlcNAc, further studies were performed with this mutant. The upper pathway is responsible for the release of GlcNAc in planta To investigate the role of the glycan cluster in the generation of GlcNAc during the infection process, we tested the GlcNAc sensitivity of a naga::pvo mutant in a ΔnixE-nixL background in planta. Interestingly, when the glycan cluster was deleted, symptom development was restored (Figure R9A), suggesting that in planta, sensitivity to GlcNAc was greatly reduced in the ΔnixE-nixL naga::pvo strain as compared to the naga::pvo mutant. Symptoms observed for the ΔnixE-nixL naga::pvo strain were not due to an indirect effect of 85
159 A 3 2, dpi B 2 3 Disease index 2 1, dpi 6 dpi 7 dpi 1 4 0, Wild-type naga::pvo ΔnixE naga::pvo ΔnixH naga::pvo ΔnixL naga::pvo ΔnixE-nixL naga::pvo WT naga::pvo Dni xe naga::pvo Dni xh naga::pvo Dni xl naga::pvo Dni xe-ni xl naga::pvo 6 5 Disease index 2, , dpi 5dpi 6dpi 7dpi , WT naga::pvo Dni xd Dni xd naga::pvo Dni xd D0127- Wild-type naga::pvo ΔnixD ΔnixD naga::pvo Bacterial strain Dni xd D0127- ΔnixD 0128::ni xd Δ ::nixD ΔnixD 0128::ni xd Δ naga::pvo ::nixd naga::pvo 6 5 Figure R9. Xanthomonas campestris pv. campestris Nix glycoside hydrolases and the TonB-dependent transporter NixD play a central role in sensitivity to N- acetylglucosamine in planta. A. Pathogenicity tests were performed on Arabidopsis thaliana Sf-2 plants. Disease symptoms were scored 4 to 7 days after inoculation. Each leaf was individually scored as: no symptom=0; weak chlorosis surrounding the wound sites=1; V-shaped chlorosis=2; necrosis=3; leaf death=4. The represented average disease scores and the standard deviations were calculated from the values of four plants with four inoculated leaves per plant. B. Growth on minimal medium (MME) plates supplemented with 10 mm glucose (upper panel) or 10 mm N-acetylglucosamine (lower panel). 1: wild-type strain; 2: naga::pvo; 3: DnixD; 4: DnixD naga::pvo; 5: DnixE-nixL; 6: DnixE-nixL naga::pvo. Pictures were taken after 48 hours of growth at 28 C.
160 Résultats the ΔnixE-nixL deletion on the expression of upstream genes (i.e. nixd and nagk-iia) as verified by qrt-pcr (data not shown). It is worth noting that the ΔnixE-nixL naga::pvo strain is still sensitive to free GlcNAc in vitro as no growth was observed on GlcNAccontaining plates (Figure R9B). This result suggests that GlcNAc sensitivity observed in planta is not due to free GlcNAc present in plant tissues but rather to GlcNAc generated from complex carbohydrates containing this molecule which did not provoke sensitivity unless they were degraded by enzymes encoded by the glycan cluster. Interestingly, we observed a slight delay in symptom development for the ΔnixE-nixL naga::pvo strain as compared to the wild-type strain (Figure R9A). This could be due to the generation of very low amounts of GlcNAc by other glycoside hydrolases encoded by Xcc (see above). Sensitivity to GlcNAc of the naga mutant was not reduced when genes of the glycan cluster were deleted individually. Indeed, the disease indices obtained for ΔnixE naga::pvo, ΔnixH naga::pvo or ΔnixL naga::pvo double mutants were comparable to those obtained for the naga::pvo strain (Figure R9A). It is worth noting that for all these mutants, GlcNAc could still be generated from complex-type N-glycans (see Figure R2B), thus explaining that these mutants are sensitive to GlcNAc in planta. Deletion of the TBDT gene nixd had a drastic effect on GlcNAc sensitivity of the naga mutant. Indeed, the ΔnixD naga::pvo double mutant induced symptoms comparable to those obtained for the wild-type strain (Figure R9A). This mutant was still sensitive to GlcNAc in vitro (Figure R9B), thus suggesting that the deletion introduced in the nixd gene did not affect both the uptake of free GlcNAc and its phosphorylation. Furthermore, these results suggest that NixD play a central role in the uptake of GlcNAc-containing carbohydrates. Deletion of nixd did not affect the expression of downstream genes as both β- mannosidase and β-galactosidase activities were similar in the wild-type strain and in the ΔnixD mutant (data not shown). When nixd was supplied in trans by using an expression plasmid (ΔnixD naga::pvo pc-nixd strain), no complementation was obtained as symptoms observed on plants were similar to those observed for the ΔnixD naga::pvo strain (data not shown). This absence of complementation was due to the rapid loss of the plasmid. Indeed, in this context, the loss of the plasmid is submitted to positive selection and after 5 days, resistance carried by the plasmid was lost by 99% of bacteria recovered from the infected tissues (data not shown). Therefore, we constructed a ΔnixD naga::pvo strain carrying the nixd gene integrated into Xcc chromosome under the control of the Ptac promoter by 86
161 Résultats replacing two transposase genes XCC0127 and XCC0128 (see Material and Methods). Deletion of these two transposase genes did not affect bacterial growth in liquid media, symptom development as well as sensitivity to GlcNAc of the naga::pvo Δ strain both in vitro and in vivo (data not shown). The complemented strain ΔnixD naga::pvo Δ ::nixD strain was severely impaired in disease development (Figure R9A), therefore confirming the involvement of the NixD TBDT in GlcNAc sensitivity of a naga mutant in planta, and probably in the uptake of specific GlcNAc-containing complex carbohydrates. 87
162 GlcNAc utilization upper pathway Chitinolytic bacteria Chitin (GlcNAc polymer) Chitinase CBP Chito-oligosaccharides? TBDTs Porins Fuc Gal NAG Gal NAG Fuc GlcNAc Porins Man Man Xanthomonas? Man Xyl? NAG? Fuc NAG protein (Asn) Protein N-glycans Nix GDE GlcNAc-containing oligosaccharides Nix/Nax TBDTs Plant glycosylated substrates Plant cell CW Chito-oligosaccharides CdxA Hex GlcNAc Nix GDE GlcNAc-containing oligosaccharides PTS ABC MFS MFS XCC3413 (NagP) GlcNAc GlcNAc utilization lower pathway NagK* GlcNAc-6P NagA XCC2886 (NagK-IIA) XCC2943 (NagK-IIB) XCC3410 (NagA) GlcN-6P NagB* XCC3411 (NagB-II) Fructose-6P Bacterial cell IM PP PG OM Figure R10. Schematic representation of the N-acetylglucosamine utilization pathway in Gram negative bacteria. N-acetylglucosamine (GlcNAc) utilization upper pathways, i.e. GlcNAc generation by the degradation of chitin (left part, adapted from [21]) or N-glycans (right part, from this work) are represented in dark green, whereas GlcNAc utilization lower pathways (i.e. GlcNAc catabolism) are represented in red. Enzymatic reactions are designated by solid arrows whereas dotted arrows indicate transport. ABC: ATP-binding cassette transporter; CBP: chitin-binding protein; Cdx: chitodextrinase; CW: plant cell wall; GDE: glycan degrading enzymes; Hex: hexosaminidase; IM: inner membrane; MFS: major facilitator transporter; Nax: N-acetylglucosamine-associated in Xanthomonas; Nix: N- acetylglucosamine-induced in Xanthomonas; OM: outer membrane; PG: peptidoglycan; PP: periplasm; PTS: PEP-dependent phosphotransferase transporter; TBDT: TonB-dependent transporter.
163 Résultats Discussion Many bacteria living in changing environments, including phytopathogenic bacteria, display an extensive repertoire of enzymes belonging to different metabolic pathways allowing the exploitation of numerous substrates. The ability to exploit various substrates has hampered pathologists in their study on the influence of a particular metabolic pathway in bacterial development during the interaction with the host. Indeed, mutations in one specific metabolic pathway very often have no visible effect on pathogenicity, due to the utilization of other substrates. In the present study, we took advantage of the sensitivity to GlcNAc of a mutant in the GlcNAc deacetylase gene naga to demonstrate that Xcc consumes this molecule during the infection process although the importance of the capacity to consume this molecule in virulence could not be inferred in our pathogenicity tests. In chitinolytic bacteria such as Vibrio or Shewanella species, utilization of GlcNAc encompasses i) an upper pathway consisting in the degradation of chitin, uptake through the outer membrane of chito-oligosaccharides which are further degraded in GlcNAc into the periplasm and ii) a lower pathway which includes uptake through the inner membrane and catabolism of GlcNAc to fructose-6p into the cytoplasm [21]. Results obtained in this study suggest that although it shares similarities with chitinolytic bacteria, the Xcc GlcNAc utilization pathway displays specificities (Figure R10), the most notable one concerning the origin of GlcNAc in planta which is proposed to be generated from glycans of glycosylated compounds. Another specificity comes from the complexity of the regulatory network with several degrees of interconnections between the regulatory pathways under the control of NagR and NagQ repressors. Complexity of the Xcc GlcNAc regulatory network Our regulatory study on GlcNAc-regulated genes showed that both repressors are functional. Several degrees of complexity in the Xcc GlcNAc regulatory network were identified: i) Genes belonging to the GlcNAc pathway are under the control of a specific GlcNAc regulator. Upper pathway genes involved in the generation and transport through the outer membrane of GlcNAc-containing carbohydrates and their further degradation leading to the production of free GlcNAc are regulated by NagR. On the other hand, most of genes belonging to the lower pathway involved in the uptake of free GlcNAc through the inner membrane and its catabolism, are under the control of NagQ. An exception was observed in this clear division. Indeed, the two GlcNAc kinase genes nagk-iia and nagk-iib that belong 88
164 Résultats to the lower pathway are both regulated by NagR. It is worth noting that GlcNAc kinases belonging to the NagK-II family [21] were experimentally validated for the first time in this work. ii) GlcNAc is proposed to be the NagR signalling molecule, whereas its phosphorylation product, i.e. GlcNAc-6P, is proposed to be the NagQ signalling molecule. iii) NagQ represses its own expression as well as the expression of NagR. Therefore, the presence of high amounts of GlcNAc-6P will lead to the induction of the expression of both repressors, thus limiting the generation and entry of free GlcNAc into the cytoplasm of the cell. This second level of regulation is important for the dynamic equilibrium between generation of GlcNAc and GlcNAc-6P consumption. Indeed, since GlcNAc-6P is toxic for Xcc, it is essential for the bacterium not to accumulate this compound in the cell. It is important to note here that in S. oneidensis as well as in E. coli, GlcNAc-6P was shown to be responsible for the allosteric activation of NagB-II and NagB respectively [14,21]. iv) Finally, entry of the NagR signalling molecule is regulated by NagQ, and production of the NagQ signalling molecule is regulated by NagR. This additional level of regulation increases the complexity of the GlcNAc regulatory network in Xcc, but also its sensitivity and its fitness. In the chitinolytic bacterium Vibrio cholerae, regulation of the expression of upper pathway genes, mainly involved in chitin degradation, is controlled by ChiS, a twocomponent hybrid sensor/kinase of the ArcB-type [25,56], whereas the NagC regulon has been proposed to include genes involved in GlcNAc catabolism as well as genes involved in chitin sensing and degradation that are not controlled by ChiS [21,25]. Thus, in this bacterium, upper pathway genes could be divided into two classes: i) genes regulated by ChiS and ii) genes co-ordinately regulated with lower pathway genes by NagC. In E. coli, upper pathway genes involved in chitobiose uptake and metabolism are regulated by a specific regulator ChbR, as well as by NagC which also regulates the expression of lower pathway genes [51,57]. Therefore, it seems that the regulation of the expression of lower pathway genes is similar in all bacteria cited above and depends on the perception of GlcNAc-6P by specific repressors (NagQ in Xcc and NagC in Vibrio and E. coli). On the other hand, regulation of the expression of upper pathway genes significantly differs in these bacteria by the nature of regulators. However, in all these cases including Xcc, regulation of the expression of upper and lower pathway genes is interconnected. 89
165 Résultats Xcc encounters plant-derived GlcNAc during infection In E. coli, mutations in naga lead to the accumulation of GlcNAc-6P which is toxic for the bacterium. Therefore, E. coli naga mutants display amino sugar sensitivity when cultured in the presence of GlcNAc [52]. Although specificities were observed as compared to E. coli, Xcc naga insertion and deletion mutants were shown to be sensitive to GlcNAc in vitro. No symptoms were observed on both A. thaliana and Bartolo cabbage when Xcc naga mutants are inoculated and we show that this absence of symptoms is due to GlcNAc sensitivity. Furthermore, the phenotype observed for the naga insertion mutant was not due to GlcNAc recycled from bacteria. Therefore, amino sugar sensitivity observed for this naga mutant in planta suggested that Xcc encountered GlcNAc derived from the plant during the infection. Plant glycosylated compounds: a proposed source of GlcNAc for Xanthomonas Xcc produces an extensive repertoire of glycoside hydrolases, lyases and esterases [58] that target linkages present in plant cell wall polysaccharides such as cellulose, mannan, xylan, galacturonan and pectin, thus generating molecules that enter in the central metabolism of this bacterium. Furthermore, bacteria of the genus Xanthomonas and especially X. axonopodis pv. manihotis, produce exoglycosidases which selectively removed specific sugar residues [59]. However, to our knowledge, GlcNAc was never considered as a putative substrate that could be encountered or generated by Xcc during infection of host plants. This amino sugar, assembled in β-1,4 linkages, composes chitin, one of the most abundant polysaccharide in nature after cellulose. Chitin is found throughout all kingdoms and is the main component of the cell walls of fungi and of the exoskeletons of crustaceans, but it is absent from plants. Glycoside hydrolases encoded by XCC2888 to XCC2895 were identified in this paper to be part of the GlcNAc regulon via NagR. Furthermore, these enzymes were proposed in the KEGG pathway database to degrade N-glycans from N-glycosylated proteins. We confirmed that genes of this cluster are functional and code for their predicted enzymatic activities, although in some cases, additional activities seem to be encoded by genes located elsewhere in the chromosome. The nature of the molecules degraded by these enzymes can be very diverse, but their combination and the KEGG database prediction strongly suggest that glycans and in particular the glycan moieties of plant glycoproteins could be targeted by this cluster. Although further investigations are required to identify the exact substrate of these enzymes and their precise role, this cluster was named the glycan cluster. Pathogenicity tests conducted with naga mutants, which are sensitive to GlcNAc and non pathogenic, 90
166 Figure S3. Conservation of genes belonging to GlcNAc and glycan clusters in Xanthomonas campestris pv. campestris ATCC33913 and Novosphingobium aromaticivorans (Saro_DSM 12444). Homologous genes are marcked by matching colors. White color indicates non conserved genes. For conserved genes, percentages of identity and similarity to the corresponding Xanthomonas campestris pv. campestris (XCC_ATCC33913) gene are indicated beneath.
167 Résultats confirm the involvement of this cluster in the generation of GlcNAc during plant infection. Indeed, naga mutants carrying a deletion of the glycan cluster recovered the ability to produce disease symptoms and thus specifically lost their GlcNAc sensitivity in planta. Therefore, we propose that in Xcc, the GlcNAc upper pathway is involved in plant glycans degradation (Figure R10), thus confirming the existence of functional upper and lower pathways, the latter one being involved in the catabolism of GlcNAc generated by the upper pathway. Conservation of the GlcNAc utilization pathway The glycan and the GlcNAc clusters are both conserved in all Xanthomonas and Xylella strains sequenced so far (Figure S2). Due to its restricted life cycle and its genome reduction, Xylella is considered as a minimal Xanthomonas model pathogen [60,61]. Therefore, the conservation of the glycan and GlcNAc clusters in this genus may reveal an important role for the GlcNAc pathway during the interaction with plants. The upper glycan pathway was only partially detected in Novosphingobium aromaticivorans [37] (Figure S3), a ubiquitous bacterium isolated from a wide range of environmental sites. In this bacterium, nixe, nixf, and nixl are absent, therefore suggesting a difference in substrate specificity as compared to Xanthomonadaceae (see Figure R2). It is interesting to note that in N. aromaticivorans the partial glycan cluster is contiguous to the cluster involved in GlcNAc catabolism. Altogether, these data reinforce the hypothesis that the entire glycan cluster is specific of Xanthomonadaceae. Moreover, comparative studies carried out with the genomes of two strains of Stenotrophomonas maltophilia (K279a and R551-3) which belong to the Xanthomonadaceae family and is not pathogenic on plants, are also informative. Indeed, although the GlcNAc lower pathway is partially conserved in both S. maltophilia strains, the glycan cluster is absent except nixg which was proposed to code for a β-n-acetyl-hexosaminidase [62]. These data confirm that the glycan cluster is specific to phytopathogenic Xanthomonadaceae. Interestingly, in S. maltophilia strains a nixg ortholog is located downstream the orthologs of nixd and nagk-iia (data not shown). Furthermore, in both S. maltophilia strains, the GlcNAc cluster lacks the nagq regulatory gene whereas nagr is conserved in both strains. A NagRbox was found in the promoter of chia [21], a gene coding for a chitinase which may play a role in the biocontrol activity of S. maltophilia strain 34S1 [63]. These results suggest the existence of an upper pathway in S. maltophilia probably involved in chitin utilization, thus showing that the upper pathway reflects the niche exploited by these bacteria. 91
168 Résultats NixD is involved in the uptake of GlcNAc-containing carbohydrates Compared to the huge amount of cell wall polysaccharides, N-glycans represent only a minor proportion of sugar polymers in plants [64]. Therefore, to exploit these molecules, bacteria must be able to recognize and transport them with high specificity and high affinity. Recently, we have defined a new type of systems named CUT loci/systems (Carbohydrate Utilization loci/systems containing TBDT) involved in the scavenging of scarce nutrients [37]. The Xcc glycan cluster was identified as a putative partial CUT locus [37]. Based on results obtained in this paper, this cluster is now proposed to be part of a more complex GlcNAc CUT system involved in the scavenging of GlcNAc-containing carbohydrates and in the catabolism of free GlcNAc thus generated. In Gram negative bacteria, active transport of carbohydrates through the outer membrane via TBDTs is a relatively recent concept [37,45,65-67]. In Xcc, the SuxA TBDT was demonstrated to be responsible for the uptake of sucrose at low concentrations [37]. Furthermore, specific TBDTs were proposed to be involved in the transport of pectin, xylan and maltodextrin degradation products [37]. In C. crescentus, the MalA TBDT was demonstrated to be involved in the active uptake of maltodextrins [66], whereas recently, the TBDT encoded by CC0446 was shown to be the only outer membrane transporter for GlcNAc [45]. In Xcc, 6 TBDTs belong to the GlcNAc CUT system, 2 of which (NixA and NixB) do not possess a canonical C-terminal membrane anchoring domain [37]. Although TBDTs were identified in the Xcc GlcNAc CUT system, free GlcNAc is not actively transported thus suggesting that these TBDTs are not involved in the active transport of this molecule. However, in the naga insertion mutant background, symptoms were restored when the TBDT gene nixd was deleted. Therefore, when this TBDT is absent, GlcNAc sensitivity of the naga mutant is lost, suggesting that NixD TBDT is responsible for the entry of GlcNAc-containing carbohydrates generated in planta during the infection. The role of the other TBDTs belonging to the GlcNAc CUT system remains elusive. Do they participate in the passive uptake of free GlcNAc or, during the infection, in the uptake of glycan degradation products that do not contain GlcNAc? Furthermore, a role in the transport of GlcNAc-containing carbohydrates during another step of the bacterial life cycle cannot be excluded. Finally, we cannot rule out an involvement in the uptake of peptidoglycan degradation products released during bacterial growth as well as during cell lysis. Recently, muropeptides from Gram-positive and Gram-negative phytopathogens, including those from Xcc strain 8004, were shown to elicit plant innate immunity [68,69]. 92
169 Résultats Therefore, these molecules represent new Microbe-Associated Molecular Pattern (MAMPs) in plant-bacterial interactions, and efficient uptake by active and specific transporters could be a strategy for the bacterium to limit the elicitation of plant defences. Degradation of glycans: just for feeding? If the glycan cluster is really involved in the degradation of glycans, what role does play this process in Xcc? The first and obvious answer is that it provides nutriments which are necessary for bacterial growth during the infection. Although N-glycans are widely distributed, these compounds represent only a small fraction of carbohydrates found in plants. However, a recent proteomic study performed on A. thaliana stems revealed that most of N- glycosylated proteins are predicted to have signal peptides allowing secretion to the cell wall or plasma membrane [70] and could therefore be accessible to Xcc during the infection process. In the human pathogen Streptococcus pneumoniae, monosaccharides released during the sequential degradation of complex-type N-glycans from human glycoconjugates, are used as a source of fermentable carbon [33]. Although the oligosaccharide moiety could be the nutrient source, glycan degradative enzymes could also contribute to the accessibility of the peptide part of the glycoprotein to bacterial proteases resulting in an optimized nutrient supply. Indeed, glycoproteins become more sensitive to proteases after de-glycosylation of N- linked oligosaccharides [71]. Such a role could also be proposed for Xcc GlcNAc utilization pathway, one possibility being the access to amino-acids as nutriments. Another possibility is that glycoprotein degradation might lead to a weakening of plant cell wall. Finally, this cluster could have an impact in signalization by activating or inactivating the function of proteins from the host. Indeed, in eukaryotes, glycosylation occurs concomitantly to the translation and plays a crucial role in the proper folding of the protein and intracellular trafficking related to cell surface expression [72]. Glycosylations also regulate many physiological and pathological events, including cell growth [73], cell migration and cancer progression [74,75], differentiation [76], plant cell wall synthesis [77,78], and host-pathogen interactions [79]. Further investigations are now being undertaken to answer these questions. 93
170 ΔnagQ-nagA ΔnagB-II ΔnagQ nixb::pvo ΔnagA ΔnagP ΔnagR ΔnagK-IIB 0531 nixa::pvo naga::pvo nagr::pvo nagq::pvo nixc::pvo nixb nixa Nisine resistance naga nagb-ii nagr nagp nagq nagk-iib nixc pc-naga pc-nagp pc-nagk-iib naxa::pvo naxb::pvo pc-nagb-ii naxa naxb ΔnixD-nixL ΔnixE-nixL ΔnixD ΔnagK-IIA ΔnixE ΔnixH ΔnixL nagk-iia::pvo nixd::pvo nagk-iia nixd nixe nixf nixg nixh nixi nixj nixk nixl pc-nagk-iia pc-nixd Figure S4. Location of mutations introduced in genes belonging to the Xanthomonas campestris pv. campestris N-acetylglucosamine utilization pathway and regions cloned in expression plasmids. Mutations are indicated above the maps: arrowheads indicated pvo155 insertions and deleted sequences are represented by horizontal dashed bars. Regions cloned in plasmids are indicated below the maps: horizontal thick bars indicate sequences used for plasmid constructions.
171 Résultats Materials and Methods Bacterial strains, plasmids and growth conditions The Xanthomonas campestris pv. campestris (Xcc) strains and plasmids used in this study are listed in Table S3. Xcc cells were grown at 30 C in MOKA [37] or KADO [80] rich media, or in MME minimal medium [81]. Minimal medium depleted in natrium contained only K 2 HPO g/l and KH 2 PO g/l. E. coli cells were grown on Luria-Bertani medium at 37 C. For solid media, agar was added to 1.5 % (W/V) final concentration. Antibiotics were used at the following concentrations for Xcc: rifampicin: 50 µg/ml; kanamycin: 50 µg/ml; tetracycline: 5 µg/ml; pimaricin: 30 µg/ml. Antibiotics were used at the following concentrations for E. coli: ampicillin: 50 µg/ml; kanamycin: 50 µg/ml; tetracycline: 10 µg/ml. Construction of Xanthomonas campestris pv. campestris mutants Insertion mutants were constructed using the suicide plasmid pvo155 [82]. A bp internal fragment for each ORF was amplified by PCR. Oligonucleotide primers used for PCR amplifications will be provided upon request. Locations of insertions are indicated in Table S3 and most are represented in Figure S4. Deletion mutants were constructed using the cre-lox system adapted from Marx and colleagues [83,84], or by using the sacb system [85]. Deleted regions are indicated in Table S3 and most are represented in Figure S4. Plasmid constructions DNA manipulations followed the procedures described by Sambrook and associates [86]. For complementation studies, the XCC3410, XCC3411, XCC3413, XCC2886, XCC2943 and XCC2887 genes (naga, nagb-ii, nagp, nagk-iia, nagk-iib and nixd respectively, see Figure S4 and Table S3) were amplified by PCR using appropriate primers (Oligonucleotide primers used for PCR amplification will be provided upon request). PCR products were cloned into pcz917, a derivative of pfaj1700 [87] containing a 2094 bp fragment of psc150 [88] with the laci gene, a Ptac promoter and a T7 terminator. Plasmids were introduced into E. coli by electroporation and into Xanthomonas strains by triparental conjugation, as described by Turner et al. [89]. 94
172 Résultats Complementation by chromosomal insertion XCC2887 gene (nixd) was amplified by PCR using appropriate primers and cloned into the MCS of the pcz1034 plasmid (see Table S3). The plasmid obtained was introduced in Xcc by triparental conjugation and deletion of the XCC0127 to XCC0128 region combined to the insertion of XCC2887 under the control of the Ptac promoter and the T7 terminator was achieved by using the sacb protocol [85]. Expression studies For β-glucuronidase assays performed as previously described [90], bacterial cultures in the appropriate medium were harvested after 6 hours incubation. For Quantitative RT-PCR (qrt-pcr), a 6 hour bacterial culture in the appropriate medium was harvested at an OD 600 = 0.4 to 0.6. RNA was extracted using the RNeasy Mini Kit (QIAGEN). Two µg of RNA was treated with RNase-free DNase I (Sigma) for 30 min at 37 C. After DNase inactivation (10 min at 75 C), RNAs were reverse-transcribed by Superscript II (Invitrogen) using random hexamers (Biolabs) for 10 min at room temperature followed by 1 h at 42 C. Quantitative-PCR amplification was performed on a Light Cycler (Roche): 10 min 95 C, 1 cycle; 5 sec 95 C, 10 sec 65 C; 20 sec 72 C; 40 to 50 cycles. Experiments were carried out in three independent biological experiments. Oligonucleotide primers used for quantitative-pcr amplifications will be provided upon request. As a control for real-time PCR, we used the 16S rrna as previously described [37,91]. Amplification conditions were: 10 min 95 C, 1 cycle; 5 sec 95 C; 10 sec 70 C; 20 sec 72 C; 40 to 50 cycles. Pathogenicity tests Hypersensitive response (HR) assays were conducted by infiltration of the leaf parenchyma of Pepper ECW10R plants as previously described [81]. Pathogenicity tests were conducted on Arabidopsis thaliana Sf-2 ecotype as previously described [92] using a bacterial inoculum density of OD 600 =0.05. Each strain was tested on sets of four 4-weeks old plants with 4 leaves per plant. At least two independent experiments were performed. Disease development was scored at days 3 to 7 post-inoculation using a disease index ranging from 0 (no symptom), to 4 (leaf death). Similarly, Bartolo cabbage leaves of 6-week old plants were inoculated by piercing the central vein three times with a needle that had been dipped in a bacterial suspension (OD 600 =0.2). Disease development was scored at days 3 to 7 post-inoculation using a disease index ranging from 0 (no symptom), to 4 (necrosis encompassing inoculated sites). 95
173 Résultats Growth curves In vitro growth curves were realized by turbidimetry measurement at OD 600 or by enumeration of bacterial colonies (CFU, Colony Formation Units). To determine in planta bacterial population we performed Internal Growth Curves (IGC). Twenty plants were inoculated and symptoms were scored as described above. Each strain was tested in at least two independent experiments. Three inoculated leaf discs per plants were sampled using a cork borer (diameter, 0.65 cm; surface area, 0.33 cm 2 ) at days 0, 1, 3 and 7 after inoculation. Three discs were collected at the inoculation site. Samples were collected from three plants per time point and ground with beads in 500 µl sterile MME. The homogenates were serially diluted and 5 µl drops were spotted three times for each dilution (10-1 to 10-6 ) with a multichannel pipette on well-dried plates supplemented with rifampicin and pimaricin. Plates were incubated at 30 C for 24h. Colonies were enumerated in spots containing 1 to 30 colonies. Bacterial densities in leaves were calculated and were given in log CFU/cm 2. [ 14 C]GlcNAc transport experiments Transport experiments of radiolabelled GlcNAc (PerkinElmer, specific activity of 2.04 GBq/mmol) were performed as previously described [37]. Briefly, cells were precultured in MOKA medium. After centrifugation and adjustment to an OD 600 of 1 in MME, 150 µl of bacteria were added to 75 µl [ 14 C]GlcNAc (0.5 µm final in MME) and after various incubation times, were collected by filtration, washed with 10 ml water, dried and the radioactivity was determined in a liquid scintillation counter. For competition experiments, unlabelled sugars were added to [ 14 C]GlcNAc at a final concentration ranging from 0.5 to 100 µm. The concentration-dependent initial GlcNAc transport was determined using the rapid dilution method as previously described [37,66]. Cells were incubated for 15 sec in presence of 0.1, 0.25, 0.5, 1, 2.5, 5, 10, 25 and 50 µm [ 14 C] GlcNAc and 0.2 ml samples were diluted into 5 ml MME supplemented with 0.1 mm GlcNAc. Cells were collected by filtration, washed with 10 ml MME supplemented with 1 mm GlcNAc, dried and the radioactivity was determined. Enzymatic activities using nitrophenyl glycosides The 4-Nitrophenyl α-l-fucopyranoside (substrate for α-fucosidase), 4-Nitrophenyl α-dmannopyranoside (substrate for α-mannosidase), 4-Nitrophenyl β-d-galactopyranoside (substrate for β-d-galactosidase), 4-Nitrophenyl β-d-mannopyranoside (substrate for β- 96
174 Résultats mannosidase) and 4-Nitrophenyl N-acetyl-β-D-glucopyranoside (substrate for β- hexosaminidase or β-n-acetylglucosaminidase) were obtained from sigma-aldrich. All substrates were diluted in water except for 4-Nitrophenyl α-l-fucopyranoside which was diluted in DMSO. Strains were precultured overnight in MOKA medium and further incubated in minimal medium for 6 hours. For β-hexosaminidase/β-n-acetylglucosaminidase activities, 400 µl of culture were added to 400µl of citrate buffer 200 mm ph 5.5 and to 40 µl of BSA 100 mg/ml. After 15 min at 37 C, 200 µl of substrate (4 mg/ml) were added. The reaction was stopped by the addition of 400 µl of K 2 CO 3 1 M when the coloration turned to yellow and OD 420 and OD 550 were measured. For all other activities, tests were performed in phosphate buffer containing Na 2 HPO 4 60 mm, NaH 2 PO 4 40 mm, KCl 10 mm, MgSO 4 1 mm and BSA 1 mg/ml, with substrates at 10 mg/ml. Na 2 CO 3 1 M was added to stop the reaction. Samples were incubated at 37 C for β- galactosidase and α-fucosidase activities, 34 C for β-mannosidase and 30 C for α- mannosidase. Activities were presented as miller units. GlcNAc phosphorylation assays GlcNAc kinase activity assays were performed using an enzyme-linked assay based on the NAD + /NADH ratio adapted from [93]. Fifty ml of an overnight culture in minimal medium supplemented with GlcNAc 10 mm were centrifuged and resuspended in 2 ml of resuspension buffer (0.05 mm Tris HCl ph 8, 13.3 mm MgCl 2, 0.1 mm EDTA, 1 mm DTT). Cells were disrupted with a French press and 100 µl of cell-free extracts were added to 900µl of reaction buffer (0.1 M Tris HCl ph 7.5, 10 mm MgCl 2, 1 mm PEP, 4 mm ATP, 0.2 mm NADH, 10 mm GlcNAc, 4 U Lactate dehydrogenase, 4 U pyruvate kinase) previously incubated for 5 min at 37 C. OD 340 was immediately measured each 10 sec for 5 min at 37 C. The decrease in OD 340 corresponded to the production of NAD + from NADH and is indirectly correlated to the GlcNAc phosphorylation into GlcNAc-6P. Enzymatic activities were given as nmol NAD + formed per min per mg of proteins. Protein concentrations of cell lysates were measured by using the Bradford assay (BioRad). 97
175 Résultats Acknowledgments We are grateful to Laurent Noël for valuable discussion and Frans J. de Bruijn for critical review of the manuscript. 98
176 Résultats References 1. Rogers HJ, Perkins HR, Ward JB (1980) Microbial Cell Walls and Membranes; Hall Ca, editor. London, UK. 2. Dixon DR, Darveau RP (2005) Lipopolysaccharide heterogeneity: innate host responses to bacterial modification of lipid a structure. J Dent Res 84: Coley J, Duckworth M, Baddiley J (1972) The occurrence of lipoteichoic acids in the membranes of gram-positive bacteria. J Gen Microbiol 73: Agladze K, Wang X, Romeo T (2005) Spatial periodicity of Escherichia coli K-12 biofilm microstructure initiates during a reversible, polar attachment phase of development and requires the polysaccharide adhesin PGA. J Bacteriol 187: Mack D, Riedewald J, Rohde H, Magnus T, Feucht HH, et al. (1999) Essential functional role of the polysaccharide intercellular adhesin of Staphylococcus epidermidis in hemagglutination. Infect Immun 67: Darby C (2008) Uniquely insidious: Yersinia pestis biofilms. Trends Microbiol 16: Hinnebusch BJ, Erickson DL (2008) Yersinia pestis biofilm in the flea vector and its role in the transmission of plague. Curr Top Microbiol Immunol 322: Vuong C, Kocianova S, Yao Y, Carmody AB, Otto M (2004) Increased colonization of indwelling medical devices by quorum-sensing mutants of Staphylococcus epidermidis in vivo. J Infect Dis 190: Vuong C, Voyich JM, Fischer ER, Braughton KR, Whitney AR, et al. (2004) Polysaccharide intercellular adhesin (PIA) protects Staphylococcus epidermidis against major components of the human innate immune system. Cell Microbiol 6: Li G, Smith CS, Brun YV, Tang JX (2005) The elastic properties of the Caulobacter crescentus adhesive holdfast are dependent on oligomers of N-acetylglucosamine. J Bacteriol 187: Tsang PH, Li G, Brun YV, Freund LB, Tang JX (2006) Adhesion of single bacterial cells in the micronewton range. Proc Natl Acad Sci U S A 103: Bodenmiller D, Toh E, Brun YV (2004) Development of surface adhesion in Caulobacter crescentus. J Bacteriol 186: Alvarez-Anorve LI, Calcagno ML, Plumbridge J (2005) Why does Escherichia coli grow more slowly on glucosamine than on N-acetylglucosamine? Effects of enzyme levels 99
177 Résultats and allosteric activation of GlcN6P deaminase (NagB) on growth rates. J Bacteriol 187: Calcagno M, Campos PJ, Mulliert G, Suastegui J (1984) Purification, molecular and kinetic properties of glucosamine-6-phosphate isomerase (deaminase) from Escherichia coli. Biochim Biophys Acta 787: Gooday GW (1990) The ecology of chitin degradation. In: Marshall KC, editor. Advances in microbial ecology. New York: Plenum Press. pp Warren RA (1996) Microbial hydrolysis of polysaccharides. Annu Rev Microbiol 50: Keyhani NO, Roseman S (1997) Wild-type Escherichia coli grows on the chitin disaccharide, N,N'-diacetylchitobiose, by expressing the cel operon. Proc Natl Acad Sci U S A 94: Toratani T, Shoji T, Ikehara T, Suzuki K, Watanabe T (2008) The importance of chitobiase and N-acetylglucosamine (GlcNAc) uptake in N,N'-diacetylchitobiose [(GlcNAc)2] utilization by Serratia marcescens 2,170. Microbiology 154: Keyhani NO, Roseman S (1999) Physiological aspects of chitin catabolism in marine bacteria. Biochim Biophys Acta 1473: Grimont PA, Grimont F (1978) The genus Serratia. Annu Rev Microbiol 32: Yang C, Rodionov DA, Li X, Laikova ON, Gelfand MS, et al. (2006) Comparative genomics and experimental characterization of N-acetylglucosamine utilization pathway of Shewanella oneidensis. J Biol Chem 281: Plumbridge JA (1989) Sequence of the nagbacd operon in Escherichia coli K12 and pattern of transcription within the nag regulon. Mol Microbiol 3: Plumbridge JA, Cochet O, Souza JM, Altamirano MM, Calcagno ML, et al. (1993) Coordinated regulation of amino sugar-synthesizing and -degrading enzymes in Escherichia coli K-12. J Bacteriol 175: Plumbridge J, Vimr E (1999) Convergent pathways for utilization of the amino sugars N- acetylglucosamine, N-acetylmannosamine, and N-acetylneuraminic acid by Escherichia coli. J Bacteriol 181: Meibom KL, Li XB, Nielsen AT, Wu CY, Roseman S, et al. (2004) The Vibrio cholerae chitin utilization program. Proc Natl Acad Sci U S A 101: Peri KG, Goldie H, Waygood EB (1990) Cloning and characterization of the N- acetylglucosamine operon of Escherichia coli. Biochem Cell Biol 68: Goodell EW (1985) Recycling of murein by Escherichia coli. J Bacteriol 163:
178 Résultats 28. Jacobs C, Huang LJ, Bartowsky E, Normark S, Park JT (1994) Bacterial cell wall recycling provides cytosolic muropeptides as effectors for beta-lactamase induction. Embo J 13: Lerouge P, Cabanes-Macheteau M, Rayon C, Fischette-Laine AC, Gomord V, et al. (1998) N-glycoprotein biosynthesis in plants: recent developments and future trends. Plant Mol Biol 38: Van den Steen P, Rudd PM, Dwek RA, Opdenakker G (1998) Concepts and principles of O-linked glycosylation. Crit Rev Biochem Mol Biol 33: Wopereis S, Lefeber DJ, Morava E, Wevers RA (2006) Mechanisms in protein O-glycan biosynthesis and clinical and molecular aspects of protein O-glycan biosynthesis defects: a review. Clin Chem 52: Roberts G, Tarelli E, Homer KA, Philpott-Howard J, Beighton D (2000) Production of an endo-beta-n-acetylglucosaminidase activity mediates growth of Enterococcus faecalis on a high-mannose-type glycoprotein. J Bacteriol 182: Burnaugh AM, Frantz LJ, King SJ (2008) Growth of Streptococcus pneumoniae on human glycoconjugates is dependent upon the sequential activity of bacterial exoglycosidases. J Bacteriol 190: Byers HL, Tarelli E, Homer KA, Beighton D (1999) Sequential deglycosylation and utilization of the N-linked, complex-type glycans of human alpha1-acid glycoprotein mediates growth of Streptococcus oralis. Glycobiology 9: Onsando J (1992) Black rot of crucifers. Diseases of Vegetables and Oil Seed Crops 2: Dow JM, Daniels MJ (1994) Pathogenicity determinants and global regulation of pathogenicity of Xanthomonas campestris pv. campestris. Curr Top Microbiol Immunol 192: Blanvillain S, Meyer D, Boulanger A, Lautier M, Guynet C, et al. (2007) Plant carbohydrate scavenging through TonB-dependent receptors: a feature shared by phytopathogenic and aquatic bacteria. PLoS ONE 2: e Yang TC, Hu RM, Hsiao YM, Weng SF, Tseng YH (2003) Molecular genetic analyses of potential beta-galactosidase genes in Xanthomonas campestris. J Mol Microbiol Biotechnol 6: Vorholter FJ, Schneiker S, Goesmann A, Krause L, Bekel T, et al. (2008) The genome of Xanthomonas campestris pv. campestris B100 and its use for the reconstruction of metabolic pathways involved in xanthan biosynthesis. J Biotechnol 134:
179 Résultats 40. Bendtsen JD, Nielsen H, von Heijne G, Brunak S (2004) Improved prediction of signal peptides: SignalP 3.0. J Mol Biol 340: Vogler AP, Lengeler JW (1989) Analysis of the nag regulon from Escherichia coli K12 and Klebsiella pneumoniae and of its regulation. Mol Gen Genet 219: Yang TC, Hu RM, Weng SF, Tseng YH (2007) Identification of a hypothetical protein of plant pathogenic Xanthomonas campestris as a novel beta-galactosidase. J Mol Microbiol Biotechnol 13: Cheng Q, Li H, Merdek K, Park JT (2000) Molecular characterization of the beta-nacetylglucosaminidase of Escherichia coli and its role in cell wall recycling. J Bacteriol 182: Freundlieb S, Ehmann U, Boos W (1988) Facilitated diffusion of p-nitrophenyl-alpha-dmaltohexaoside through the outer membrane of Escherichia coli. Characterization of LamB as a specific and saturable channel for maltooligosaccharides. J Biol Chem 263: Eisenbeis S, Lohmiller S, Valdebenito M, Leicht S, Braun V (2008) NagA-dependent uptake of N-acetyl-glucosamine and N-acetyl-chitin oligosaccharides across the outer membrane of Caulobacter crescentus. J Bacteriol 190: Lengeler JW, Jahreis K, Wehmeier UF (1994) Enzymes II of the phospho enol pyruvatedependent phosphotransferase systems: their structure and function in carbohydrate transport. Biochim Biophys Acta 1188: Jones-Mortimer MC, Kornberg HL (1980) Amino-sugar transport systems of Escherichia coli K12. J Gen Microbiol 117: Keyhani NO, Wang LX, Lee YC, Roseman S (2000) The chitin disaccharide, N,N'- diacetylchitobiose, is catabolized by Escherichia coli and is transported/phosphorylated by the phosphoenolpyruvate:glycose phosphotransferase system. J Biol Chem 275: Lu GT, Yang ZJ, Peng FY, Tan YN, Tang YQ, et al. (2007) The role of glucose kinase in carbohydrate utilization and extracellular polysaccharide production in Xanthomonas campestris pathovar campestris. Microbiology 153: White RJ (1968) Control of amino sugar metabolism in Escherichia coli and isolation of mutants unable to degrade amino sugars. Biochem J 106: Plumbridge JA (1991) Repression and induction of the nag regulon of Escherichia coli K- 12: the roles of nagc and naga in maintenance of the uninduced state. Mol Microbiol 5:
180 Résultats 52. Bernheim NJ, Dobrogosz WJ (1970) Amino sugar sensitivity in Escherichia coli mutants unable to grow on N-acetylglucosamine. J Bacteriol 101: Park JT (2001) Identification of a dedicated recycling pathway for anhydro-nacetylmuramic acid and N-acetylglucosamine derived from Escherichia coli cell wall murein. J Bacteriol 183: Cheng Q, Park JT (2002) Substrate specificity of the AmpG permease required for recycling of cell wall anhydro-muropeptides. J Bacteriol 184: Qian W, Jia Y, Ren SX, He YQ, Feng JX, et al. (2005) Comparative and functional genomic analyses of the pathogenicity of phytopathogen Xanthomonas campestris pv. campestris. Genome Res 15: Li X, Roseman S (2004) The chitinolytic cascade in Vibrios is regulated by chitin oligosaccharides and a two-component chitin catabolic sensor/kinase. Proc Natl Acad Sci U S A 101: Plumbridge J, Pellegrini O (2004) Expression of the chitobiose operon of Escherichia coli is regulated by three transcription factors: NagC, ChbR and CAP. Mol Microbiol 52: da Silva ACR, Ferro JA, Reinach FC, Farah CS, Furlan LR, et al. (2002) Comparison of the genomes of two Xanthomonas pathogens with differing host specificities. Nature 417: Wong-Madden ST, Landry D (1995) Purification and characterization of novel glycosidases from the bacterial genus Xanthomonas. Glycobiology 5: Puhler A, Arlat M, Becker A, Gottfert M, Morrissey JP, et al. (2004) What can bacterial genome research teach us about bacteria-plant interactions? Curr Opin Plant Biol 7: Dow JM, Daniels MJ (2000) Xylella genomics and bacterial pathogenicity to plants. Yeast 17: Crossman LC, Gould VC, Dow JM, Vernikos GS, Okazaki A, et al. (2008) The complete genome, comparative and functional analysis of Stenotrophomonas maltophilia reveals an organism heavily shielded by drug resistance determinants. Genome Biol 9: R Kobayashi DY, Reedy RM, Bick J, Oudemans PV (2002) Characterization of a chitinase gene from Stenotrophomonas maltophilia strain 34S1 and its involvement in biological control. Appl Environ Microbiol 68:
181 Résultats 64. Seveno M, Cabrera G, Triguero A, Burel C, Leprince J, et al. (2008) Plant N-glycan profiling of minute amounts of material. Anal Biochem 379: Schauer K, Rodionov DA, de Reuse H (2008) New substrates for TonB-dependent transport: do we only see the 'tip of the iceberg'? Trends Biochem Sci 33: Neugebauer H, Herrmann C, Kammer W, Schwarz G, Nordheim A, et al. (2005) ExbBDdependent transport of maltodextrins through the novel MalA protein across the outer membrane of Caulobacter crescentus. J Bacteriol 187: Koebnik R (2005) TonB-dependent trans-envelope signalling: the exception or the rule? Trends Microbiol 13: Gust AA, Biswas R, Lenz HD, Rauhut T, Ranf S, et al. (2007) Bacteria-derived peptidoglycans constitute pathogen-associated molecular patterns triggering innate immunity in Arabidopsis. J Biol Chem 282: Erbs G, Silipo A, Aslam S, De Castro C, Liparoti V, et al. (2008) Peptidoglycan and muropeptides from pathogens Agrobacterium and Xanthomonas elicit plant innate immunity: structure and activity. Chem Biol 15: Minic Z, Jamet E, Negroni L, Arsene der Garabedian P, Zivy M, et al. (2007) A subproteome of Arabidopsis thaliana mature stems trapped on Concanavalin A is enriched in cell wall glycoside hydrolases. J Exp Bot 58: Berger S, Menudier A, Julien R, Karamanos Y (1995) Do de-n-glycosylation enzymes have an important role in plant cells? Biochimie 77: Lanctot PM, Leclerc PC, Clement M, Auger-Messier M, Escher E, et al. (2005) Importance of N-glycosylation positioning for cell-surface expression, targeting, affinity and quality control of the human AT1 receptor. Biochem J 390: Zhao H, Sun L, Wang L, Xu Z, Zhou F, et al. (2008) N-glycosylation at Asn residues 554 and 566 of E-cadherin affects cell cycle progression through extracellular signalregulated protein kinase signaling pathway. Acta Biochim Biophys Sin (Shanghai) 40: Dennis JW, Granovsky M, Warren CE (1999) Glycoprotein glycosylation and cancer progression. Biochim Biophys Acta 1473: Zhao YY, Takahashi M, Gu JG, Miyoshi E, Matsumoto A, et al. (2008) Functional roles of N-glycans in cell signaling and cell adhesion in cancer. Cancer Sci 99: Boisson M, Gomord V, Audran C, Berger N, Dubreucq B, et al. (2001) Arabidopsis glucosidase I mutants reveal a critical role of N-glycan trimming in seed development. Embo J 20:
182 Résultats 77. Lukowitz W, Nickle TC, Meinke DW, Last RL, Conklin PL, et al. (2001) Arabidopsis cyt1 mutants are deficient in a mannose-1-phosphate guanylyltransferase and point to a requirement of N-linked glycosylation for cellulose biosynthesis. Proc Natl Acad Sci U S A 98: Gillmor CS, Poindexter P, Lorieau J, Palcic MM, Somerville C (2002) Alpha-glucosidase I is required for cellulose biosynthesis and morphogenesis in Arabidopsis. J Cell Biol 156: Fumagalli O, Tall BD, Schipper C, Oelschlaeger TA (1997) N-glycosylated proteins are involved in efficient internalization of Klebsiella pneumoniae by cultured human epithelial cells. Infect Immun 65: Arlat M, Van Gijsegem F, Huet JC, Pernollet JC, Boucher CA (1994) PopA1, a protein which induces a hypersensitivity-like response on specific Petunia genotypes, is secreted via the Hrp pathway of Pseudomonas solanacearum. Embo J 13: Arlat M, Gough CL, Barber CE, Boucher C, Daniels MJ (1991) Xanthomonas campestris contains a cluster of hrp genes related to the larger hrp cluster of Pseudomonas solanacearum. Mol Plant Microbe Interact 4: Oke V, Long SR (1999) Bacterial genes induced within the nodule during the Rhizobiumlegume symbiosis. Mol Microbiol 32: Marx CJ, Lidstrom ME (2002) Broad-host-range cre-lox system for antibiotic marker recycling in gram-negative bacteria. Biotechniques 33: Angot A, Peeters N, Lechner E, Vailleau F, Baud C, et al. (2006) Ralstonia solanacearum requires F-box-like domain-containing type III effectors to promote disease on several host plants. Proc Natl Acad Sci U S A 103: Schafer A, Tauch A, Jager W, Kalinowski J, Thierbach G, et al. (1994) Small mobilizable multi-purpose cloning vectors derived from the Escherichia coli plasmids pk18 and pk19: selection of defined deletions in the chromosome of Corynebacterium glutamicum. Gene 145: Sambrook J, Fritsch EF, Maniatis T (1989) Molecular cloning: a laboratory manual; Laboratory CSH, editor. NY. 87. Dombrecht B, Vanderleyden J, Michiels J (2001) Stable RK2-derived cloning vectors for the analysis of gene expression and gene function in gram-negative bacteria. Mol Plant Microbe Interact 14:
183 Résultats 88. Cunnac S (2004) Identification à l'échelle génomique des effecteurs dépendant du système de sécrétion de type III de la bactérie phytopathogène Ralstonia solanacearum. Toulouse: Université Toulouse III Paul Sabatier. 184 p. 89. Turner P, Barber CE, Daniels MJ (1985) Evidence for clustered pathogenicity genes in Xanthomonas campestris pv. campestris. Mol Gen Genet 199: Jefferson RA, Kavanagh TA, Bevan MW (1987) GUS fusions: beta-glucuronidase as a sensitive and versatile gene fusion marker in higher plants. Embo J 6: Morales CQ, Posada J, Macneale E, Franklin D, Rivas I, et al. (2005) Functional analysis of the early chlorosis factor gene. Mol Plant Microbe Interact 18: Meyer D, Lauber E, Roby D, Arlat M, Kroj T (2005) Optimization of pathogenicity assays to study the Arabidopsis thaliana-xanthomonas campestris pv. campestris pathosystem. Molecular Plant Pathology 6: Gonzali S, Pistelli L, De Bellis L, Alpi A (2001) Characterization of two Arabidopsis thaliana fructokinases. Plant Sci 160:
184 DISCUSSION GENERALE
185 Discussion Historiquement, l étude du catabolisme bactérien de carbohydrates complexes a contribué à la compréhension de la physiologie bactérienne. Cependant, ces systèmes de catabolisme ont été longtemps sous-estimés quant à leur rôle potentiel dans la virulence de bactéries pathogènes. En effet, on définit généralement un facteur de virulence comme une molécule causant directement des dommages à l hôte et produite seulement par les bactéries pathogènes (Wassenaar and Gaastra, 2001). Or, les gènes participant aux processus physiologiques de base sont généralement présents chez les bactéries pathogènes et non pathogènes, excluant ainsi la possibilité d une participation de ces gènes dans la virulence. Les processus physiologiques centraux permettant à la bactérie de proliférer dans l hôte sont pourtant essentiels au pouvoir pathogène (Smith, 2007). De récentes investigations ont permis de suggérer que le catabolisme de carbohydrates peut avoir un rôle bien plus important que ce que l on imaginait, dans le pouvoir pathogène de bactéries pathogènes d animaux (Hava and Camilli, 2002; Moyrand et al., 2007) ou de plantes (Berger et al., 2007; Blanvillain et al., 2007) et qu il aurait évolué lors des interactions avec l hôte. Xcc est une bactérie capable d utiliser, de façon très efficace, la plupart des nutriments à sa portée lors de son cycle de vie et notamment lors de l infection d une plante hôte. Pour celà, la bactérie possède des systèmes d acquisition et d utilisation de carbohydrates végétaux impliquant : (i) Une large gamme d enzymes de dégradation de polymères de sucres composant notamment la paroi végétale. (ii) Des systèmes de transport actifs et très efficaces tels que les TBDTs (Schauer et al., 2008) (iii) Un réseau de régulation permettant d activer l expression de ces différents acteurs au moment adéquat. Dans certains cas, les gènes codant les enzymes de dégradation d un substrat, les transporteurs des produits de dégradation de ce substrat et les régulateurs transcriptionnels sont regroupés sur le génome en loci fonctionnels nommés CUT loci (Carbohydrate Utilization loci containing TBDTs). En 2007, des travaux menés dans notre équipe ont permis de montrer d une part, le rôle d un tel locus dans l acquisition et l utilisation du saccharose par Xcc et d autre part, l importance de ce locus pour la virulence de la bactérie (Blanvillain et al., 2007). De plus, des oligosaccharines, comme les oligogalacturonides, sont bien connues pour provoquer l induction des systèmes de défense de la plante et pour influencer la croissance de 107
186 Discussion la plante (Albersheim et al., 1983; Fry et al., 1993; Priem et al., 1994). Les produits de dégradation des glycanes générés par la bactérie pourrait être perçus par la plante comme des MIMPs et induire les réponses de défense de celle-ci. Il serait donc important pour la bactérie d internaliser rapidement ces produits de dégradation. Le rôle des TBDTs appartenant aux systèmes CUT dans l internalisation de ces produits de dégradation pourrait donc être double : pour l exploitation des rares nutriments présents mais aussi pour limiter la reconnaissance par la plante de molécules signales générées par la bactérie. Le réseau métabolique d une bactérie est complexe et regroupe de nombreuses voies de catabolisme de carbohydrates qui s entrecroisent. C est pour cette raison qu il est difficile d observer un phénotype lorsque l on court-circuite une seule voie de catabolisme. Nous avons tiré partie de la sensibilité d un mutant naga de Xcc au GlcNAc pour montrer l importance d un cluster de gènes dans la génération et l acquisition de GlcNAc in planta au cours de l infection. Un nouveau système CUT impliqué dans l acquisition et l utilisation du GlcNAc à été défini chez Xcc et a pu être divisé en deux voies. La voie amont est impliquée dans la génération de GlcNAc in planta au cours de l infection et dans le transport de carbohydrates à travers la membrane externe de la bactérie. Nous avons montré notamment qu un TBDT et un cluster de gènes codant des hydrolases glycolytiques jouent un rôle dans cette libération de GlcNAc in planta et que la plupart de ces enzymes sont fonctionnelles in vitro. La voie aval est impliquée dans le transport du GlcNAc à travers la membrane interne de la bactérie, le catabolisme du GlcNAc et la régulation transcriptionnelle de l expression des gènes du système. Nous avonc montré qu un seul transporteur de type MFS (NagP) permet le transport du GlcNAc du périplasme vers le cytoplasme et que deux GlcNAc kinases sont impliquées dans la phosphorylation du GlcNAc. C est la première fois que l implication d un transporteur de type MFS dans le transport de GlcNAc chez une bactérie est prouvé. D autre part, nous avons caractérisé le réseau de régulation du système GlcNAc. C est la première fois qu une étude montre qu une bactérie phytopathogène utilise du GlcNAc provenant de sa plante hôte. Afin de ne pas être redondante avec la discussion du papier, je vais axer principalement cette discussion sur les perspectives de ce travail. 108
187 Discussion D où provient le GlcNAc généré in planta? Lorsque l on inocule la bactérie par piercing au niveau de la feuille de la plante hôte, les premiers éléments rencontrés par Xcc sont la sève de xylème et la paroi des cellules végétales. Le transport de sève de xylème se fait via des vaisseaux composés de cellules mortes et creuses. En plus des sels inorganiques, des nutriments organiques tels que des acides aminés, des sucres, des acides organiques ainsi que des protéines sont transportés via les vaisseaux du xylème des racines vers les parties aériennes (Schurr and Schulze, 1995). Bien que ces protéines puissent avoir un rôle important, seule une petite fraction d entre-elles ont été identifiée. Une étude de la composition en protéine de la sève de xylème de Brassica napus a permis d identifier de nombreuses protéines parmi lesquelles on trouve des peroxydases et des chitinases, des protéines PR de défense, des protéines riches en glycine, des protéinases, des hydrolases et des lectines (Kehr et al., 2005). A ma connaissance, aucun polymère de la paroi végétale décrit à ce jour ne contient du GlcNAc. Cependant, la paroi contient de nombreuses protéines telles que les glycoprotéines riches en hydroxyproline (HRGPs) parmi lesquelles on trouve : les extensines, les protéines riches en proline (PRPs), les protéines arabinogalactane (AGPs) (Wu et al., 2001). La paroi végétale contient également des protéines riches en glycine (GRPs) (Mousavi and Hotta, 2005). L identification d un cluster de gènes codant des enzymes dont l expression est régulée par la présence de GlcNAc et qui, selon la base de données KEGG, seraient capables de couper les liaisons entre les résidus de sucres composant les N-glycanes, nous laisse penser que les unités glycanes des glycoprotéines végétales pourraient être le substrat de ce CUT système. Des approches complémentaires pourraient permettre d identifier l origine végétale du GlcNAc. Une approche sans a priori consiste tout d abord à tester la sensibilité d un mutant naga de Xcc lorsqu il est cultivé dans de la sève de xylème ou des extraits de paroi végétale préparés à partir d hypocotyle d Arabidopsis (Feiz et al., 2006). Si le mutant naga montre un retard de croissance en présence de sève de xylème et ou d extraits de paroi végétale, alors nous pourrons tenter d isoler la ou les molécule(s) contenant du GlcNAc par des expériences de purifications successives, notamment en purifiant les protéines par colonnes d affinité, puis les protéines glycosilées jusqu à la purification de protéines portant des glycanes. 109
188 Discussion Une approche avec a priori cette fois pourrait permettre de montrer l activité de déglycosylation des enzymes du locus glycane identifié au cours de cette thèse. La déglycosylation de protéines commerciales glycosylées, telles que la RNaseB et la peroxydase isolée du raifort, ou de protéines pariétales purifiées (Jamet et al., 2008), pourra être suivie par électrophorèse sur gel de polyacrylamide après coculture en présence de Xcc. L élimination des unités glycanes sera corrélée avec une diminution de la taille de la protéine. La déglycosylation potentielle pourra également être suivie in vitro, en présence des enzymes du locus glycane purifiées, par la technique de MALDI-TOF (Roberts et al., 2000; Roberts et al., 2001). Ceci devrait nous permettre de caractériser le rôle de chacune des enzymes du locus glycane. De plus, de nombreux mutants d Arabidopsis thaliana altérés dans la synthèse de N- glycanes sont disponibles (Hartweck et al., 2006; Lerouxel et al., 2005; Strasser et al., 2004; Strasser et al., 2005; Strasser et al., 2006; Strasser et al., 2007; von Schaewen et al., 1993). Des tests de sensibilité au GlcNAc du mutant naga in planta, ainsi que des mesures de la virulence pourront être réalisés sur ces différents mutants de plante. Pour quelles raisons Xcc dégraderait les unités glycanes des glycoprotéines végétales au cours de l infection? Une des premières raisons pour laquelle Xcc dégraderait les unités N-glycanes pourrait être l utilisation des molécules résultant de cette dégradation pour l apport d énergie. En effet il a été montré récemment que certains pathogènes animaux tels que S. pneumoniae, ou E. faecalis sont capables de dégrader des unités N-glycanes et d utiliser les produits de cette dégradation pour leur croissance (cf paragraphe 2.3 du chapitre «Le GlcNAc comme source d énergie») (Burnaugh et al., 2008; Roberts et al., 2000; Roberts et al., 2001). De plus, nous savons que les unités glycanes peuvent avoir pour rôle de protéger les protéines qu ils décorent contre les protéases (Berger et al., 1995). Xcc possédant un large répertoire de protéases (CAZy, la déglycosylation des protéines par les enzymes du cluster glycane pourrait faciliter l accès de ces protéases à la partie peptidique de ces glycoprotéines. Il serait intéressant de voir s il existe un lien entre le système d acquisition et d utilisation du GlcNAc de Xcc et les protéases. Le GlcNAc et les régulateurs NagR et NagQ jouent-ils un rôle dans l expression de gènes codant des protéases? Nous avons vu précédemment que la glycosylation eucaryote peut avoir de nombreux rôles tels que participer au repliement des protéines en cours de synthèse et dans le trafic 110
189 Discussion cellulaire des protéines de surfaces (Lanctot et al., 2005). De nombreux récepteurs de surface sont glycosylés, cette modification agissant de façon variable sur la reconnaissance du ligand et sur la transduction du signal (Ho et al., 1999; Servant et al., 1996; van der Hoorn et al., 2005; Yan et al., 2008). La glycosylation régule également de nombreux processus physiologiques et pathologiques comme la croissance cellulaire (Zhao et al., 2008), la migration des cellules et la progression des cancers (Dennis et al., 1999; Zhao et al., 2008), la différentiation cellulaire (Boisson et al., 2001), la synthèse de la paroi des cellules végétales (Gillmor et al., 2002; Lukowitz et al., 2001), et l interaction hôte pathogène (Fumagalli et al., 1997). Par conséquent, la deuxième fonction possible de la dégradation des glycanes durant l infection pourrait être de moduler (activer ou inactiver) la fonction des protéines de l hôte. Nous avons vu précédemment que de nombreux récepteurs elrr impliqués dans la reconnaissance de l hôte sont glycosylés (van der Hoorn et al., 2005). Cette glycosylation est importante pour leur fonction. Nous pouvons imaginer que la déglycosylation de tels récepteurs par la bactérie pourrait être une stratégie intéressante pour limiter l induction des systèmes de défenses de la plante. Chez les plantes, des N-glycanes libres jouent un rôle dans la différentiation, la croissance et la maturation (Priem et al., 1990) ainsi que dans la germination et la maturation des fruits (Priem and Gross, 1992). Ces N-glycanes libres sont donc considérés comme des oligosaccharines qui sont des oligosaccharides complexes ayant une activité biologique et à faible concentration, un rôle potentiel dans la signalisation inter-cellulaire (Albersheim et al., 1983; Fry et al., 1993; Priem et al., 1994). Ce sont les endo-β-n-acétylglucosaminidases (ENGase, EC ) qui coupent la liaison glycosydique β-1,4 reliant les deux unités GlcNAc du N-glycane et les asparaginases (PNGase, EC ) qui clivent la liaison entre le premier résidu GlcNAc et le résidu asparagine (Suzuki et al., 2002a), qui libèrent les N-glycanes des glycoprotéines. Xcc possède deux protéines appartenant à la famille des ENGases, FlgJ (GH73, codé par le gène XCC1944) et NixF (GH18, codé par le gène XCC2889 appartenant au cluster glycane du système d acquisition et d utilisation du GlcNAc, Figure R2 du papier). Chez S. typhymurium, FlgJ est connue pour jouer un rôle crucial dans la formation du flagelle. En effet, cette muraminidase est responsable de la dégradation localisée de la couche de peptidoglycane, permettant ainsi la pénétration de la tige du flagelle (Nambu et al., 1999). 111
190 Dégradation d unités glycanes de glycoprotéines végétales? Produits de dégradation ME Périplasme MI GlcNAc Perméase NagP Cytoplasme Recyclage du peptidoglycane GlcNAc nagk-iib 2943 TBDT 2944 TBDT 0531 NagK-I / NagK-II GlcNAc-6-P TBDT 3408 resistance àla Nisine 3409 NagR NagQ Locus GlcNAc naga 3410 nagb-ii 3411 nagr 3412 nagp 3413 nagq 3414 déacétylase déaminase répresseur LacI perméase régulateur GntR NagA Glu-6-P NagB / NagB-II Fru-6-P Glycosyle hydrolases nagk-iia TBDT Locus Glycane Figure D1. Représentation schématique du réseau de régulation du système GlcNAc de Xanthomonas campestris pv. campestris. Le système GlcNAc comprend deux régulateurs, un régulateur de la famille des GntR, NagQ et un régulateur de la famille LacI, NagR. Chacun de ces régulateur pourrait se complexer avec une molécule signale différente réprimant leur activité : le GlcNAc pour NagR et le GlcNAc-6-P pour NagQ. La boîte de fixation à l ADN de NagQ identifiée est représentée par un point rouge, celles de NagR par des points noirs en amont des gènes régulés. ME, Membrane externe ; MI, membrane interne ; GlcNAc, N-acétylglucosamine ; Glu, glucose ; Fru, fructose ; TBDT, TonB Dependent Transporter.
191 Discussion Bien que la fonction de la protéine NixF reste à confirmer, nous proposons que cette protéine serait responsable du clivage de la liaison entre les deux unités GlcNAc formant la structure de base du N-glycane et donc de la libération de l unité N-glycane. La libération des N-glycanes par l activité ENGase bactérienne pourrait modifier le signal de développement de la plante infectée. Le système CUT GlcNAc a-t-il un rôle lors d une autre étape du cycle de vie de Xcc que l infection? Nous avons montré que du GlcNAc est généré et utilisé par Xcc au cours de l infection. Il serait intéressant d étudier le rôle potentiel du système CUT GlcNAc au cours d une autre étape du cycle de vie de Xcc comme la vie épiphyte, la vie saprophyte ou encore la transmission à la génération suivante de la plante hôte. Il serait donc intéressant de tester la capacité de mutants de ce système à survivre et/ou à se développer sur les parties aériennes des plantes hôtes ainsi que sur des débris végétaux. D autre part, la capacité de ces mutants à se transmettre de graines à graines pourrait également être mesurée (Darsonval et al., 2008). Un système de régulation complexe : Nous avons montré que le système CUT GlcNAc possède deux régulateurs transcriptionnels, NagQ qui fait partie de la famille des GntR et qui est responsable de la répression des gènes du locus GlcNAc et NagR appartenant à la famille des LacI et qui réprime l expression des autres gènes du système CUT, gènes responsables de la génération de GlcNAc, de son transport à travers la membrane externe et de la phosphorylation du GlcNAc en GlcNAc-6P. La complexité du réseau de régulation de ce système est due à plusieurs points. Tout d abord, par le fait que NagQ réprime l expression de NagR (Fig. D1). Lorsque les gènes impliqués dans le catabolisme du GlcNAc (excepté nagk-iia et nagk-iib) sont activés, la production du répresseur NagR augmente, entraînant la répression des gènes de la voie amont. D autre part, ces deux régulateurs auraient chacun une molécule signale différente, le GlcNAc pour NagR et le GlcNAc-6P pour NagQ. Par conséquent, la dérépression du locus GlcNAc par la présence de GlcNAc-6P entraîne une augmentation de la production de NagR et donc une diminution de la synthèse de cette molécule signale, l expression des GlcNAc kinases étant réprimée. De plus, l entrée de la molécule signale de NagR, le GlcNAc, dans la cellule dépend du transporteur NagP dont l expression est régulée indirectement par NagQ. 112
192 Xcc ΔnagA XCC0127 XCC0128 orit + sacb nagb-ii nagp nagr nagq ΔnagA Km R oriv pk18mobsacb-x Séquence en avale du gène XCC0128 Séquence en amont du gène XCC0127 naga Promoteur X àtester Promoteur X àtester naga Xcc ΔnagA ΔXCC0127-XCC0128::PromXnagA Recombinaison homologue dans la souche Xcc ΔnagA nagb-ii nagp nagr nagq ΔnagA 3409 Inoculation de la souche dans la plante hôte de Xcc Le promoteur X s exprime in planta, le gène naga est exprimé et complémente la délétion naga Le promoteur X ne s exprime pas in planta, le gène naga n est pas exprimé, pas de complémentation la délétion naga Symptômes Pas de Symptômes Figure D2. Utilisation du phénotype du mutant ΔnagA pour suivre l expression d un gène in planta.
193 Discussion Cette complexité de régulation permet à la bactérie une régulation très fine du système et, en présence de GlcNAc, d avoir un certain équilibre entre la production de molécules signales éventuellement toxique pour la bactérie et la production d enzymes impliquées dans le catabolisme de ces molécules. Nous n avons pas été en mesure d identifier d autres boites NagR et NagQ dans le génome de Xcc que celles identifiées par Yang et ses collaborateurs (2006). Cependant, les résultats obtenus lors des tests enzymatiques, notamment les résultats du test d activité N- acétylglucosaminidase nous montrent qu il existe au moins une autre enzyme non identifiée régulée par NagR. Il est donc important de tester l étendue des régulons NagR et NagQ par des tests de puces à ADN sur génome complet. Pour cela, il sera nécessaire de comparer l expression des gènes dans un mutant nagr ou nagq avec l expression des gènes dans la souche sauvage ou surexprimant le régulateur muté. D autre part, il sera intéressant de comparer l expression des gènes d une souche sauvage cultivée en présence ou non de GlcNAc afin d avoir une vision plus globale des gènes régulés par la présence de cette molécule et de voir si plusieurs voies sont régulées par cette molécule (El Qaidi et al., 2009; Plumbridge and Pellegrini, 2004). Il serait également intéressant de tester l implication éventuelle de régulateurs globaux comme CLP (répression catabolique), RpfC/RpfG (régulateurs à deux composants du quorum sensing), HrpG/HrpX (régulateurs du système Hrp) Le mutant naga, un nouvel outil génétique? L absence de développement de symptômes sur plante du mutant naga pourrait devenir un outil très intéressant d une part pour l étude du système CUT GlcNAc et d autre part pour l étude de l expression de gènes de Xcc in planta. En ce qui concerne le système CUT GlcNAc, il serait intéressant de créer une banque de mutants aléatoires dans le mutant naga et de rechercher les suppresseurs du phénotype naga, afin de déterminer s il existe d autres gènes impliqués dans la génération de GlcNAc in planta au cours de l infection. Plus largement, le phénotype naga pourrait permettre de tester l expression in planta d une large gamme de promoteurs. En effet il suffit de cloner les promoteurs à tester en amont du gène sauvage naga et de transférer le tout sur le chromosome de la souche mutante naga. Si le promoteur testé s exprime in planta, il y aura alors transcription du gène naga sauvage, complémentation de la mutation naga et donc développement de symptômes sur la plante (Fig. D2). 113
194 Discussion Le travail réalisé au cours de cette thèse a donc permis de débuter l étude des mécanismes permettant la génération et l utilisation du GlcNAc d origine végétale au cours de l infection par Xcc. Il ouvre de nouvelles perspectives quant à l étude de la capacité de cette bactérie à dégrader les unités glycanes des glycoprotéines végétaeles et le rôle de cette dégradation dans l adaptation de la bactérie au milieu plante. Il permet également le développement d un outil permettant de suivre l expression de gènes in planta et notamment dans les vaisseaux du xylème. 114
195 MATERIELS ET METHODES
196 Tableau M1. Liste des réactifs et concentrations Abréviation Antibiotique Concentration de la Solution stock Amp Ampicilline 50 mg/ml 50 µg/ml Cm Chloramphénicole 10 mg/ml Kan Kanamycine 10 mg/ml 50 µg/ml Rif Rifampicine 10 mg/ml 50 µg/ml Spec Spectinomycine 10 mg/ml 40 µg/ml Tet Tétracycline 5 mg/ml Pim Pimaricine 30 mg/ml 30 µg/ml Xgal 5-bromo-4-chloro-3-indolyl-beta-D-galactopyranoside 20 mg/ml 40 µg/ml Xgluc 5-bromo-4-chloro-3-indolyl-beta-D-glucuronic acid 25 mg/ml 125 µg/ml IPTG Isopropyl β-d-1-thiogalactopyranoside 100 mm 200 µm Concentration finale utilisée 100 µg/ml pour E. coli 10 µg/ml pour Xcc 10 µg/ml pour E. coli 5 µg/ml pour Xcc
197 Matériel et Méthodes 1 Souches et plasmides Toutes les souches de Xanthomonas campestris pv. campestris (Xcc) utilisées dérivent de la souche Xcc LMG568 ATCC Les souches d Escherichia coli utilisées dérivent de la souche TG1. Les souches et les plasmides sont répertoriés dans le tableau S3 du papier. 2 Milieux et réactifs Les cellules d E. coli sont cultivées dans un milieu Luria Bertani (LB, commandé chez Invitrogen), à 37 C en aérobiose, à agitation constante pour les cultures en milieu liquide (Miller, 1992). Xcc est cultivée à 30 C en aérobiose, à agitation constante en milieu riche MOKA (Yeast extract, Difco, à 0,4 % ; Casamino acid à 0,8 % ; K 2 HPO 4 à 0,2 % ; MgSO 4-7H 2 O à 0,03%), (Blanvillain et al., 2007) ou en milieu minimum MME (K 2 HPO 4 à 1,05 %, KH 2 PO 4 à 0,45 %, (NH 4 ) 2 SO 4 à 0,1 %, MgSO 4-7 H 2 O 1 mm, Casamino acid à 0,15 % ) (Arlat et al., 1991). Lorsque c est nécéssaire, du saccharose à 10 g/l est ajouté au milieu riche. Pour les milieux gélosés, 1.5% d agar est ajouté. L ampicilline (Amp, préparé dans de l eau), la kanamycine (Kan, préparée dans l eau), le chloramphénicol (Cm, préparé dans de l éthanol), la rifampicine (Rif, préparée dans du méthanol), la tétracycline (Tet, préparée dans de l éthanol à 50%), la spectinomycine (préparée dans l eau), la pimaricine (préparé dans de l eau), le Xgal (préparé dans du diméthylformamide), le Xgluc (préparé dans du diméthylformamide) et L IPTG (préparé dans l eau) sont ajoutés aux milieux aux concentrations répertoriée dans le tableau M1. Les solutions stock dexgal et Xgluc doivent être conservées à l obscurité. 3 Biologie moléculaire 3.1. Préparation d ADN génomique 1.5 ml de préculture est centrifugé 1 min rpm. Le surnageant est éliminé par retournement du tube et le culot repris dans la goutte de surnageant restante. Les cellules sont lysées par ajout de 200 μl de tampon de lyse (Tris-acétate ph mm, Sodium Acétate 20mM, EDTA 1mM, SDS 1%) et 60 μl de NaCl à 5 M. Les échantillons sont ensuite incubés 115
198 Xcc gène-x 1 PCR Bléo R 2 Clonage pvo155-x orit Km R Amp R Xcc WT PCR-X uida 3 Recombinaison homologue Mutant Xcc-X::pVO155 Figure M1. Principe de la construction des mutants par insertion du plasmide pvo155. (Oke and Long, 1999) 1. Une portion du gène cible X est amplifiée par PCR à l aide d oligonucléotides spécifiques portant à leurs extrémités 5 les sites de restriction nécessaires au clonage dans le vecteur pvo Le fragment PCR obtenu est cloné dans le vecteur pvo155 en amont du gène rapporteur uida codant la β-glucuronidase. 3. Ce nouveau plasmide est d abord transformé dans une souche d E. coli puis, après vérification de la séquence, il est transféré dans la souche de Xanthomonas à muter par conjugaison triparentale. L événement de recombinaison homologue par simple «crossing over» entre le produit PCR X et le gène X de la souche sauvage LMG568 de Xcc sera sélectionné par criblage des souches résistantes à la kanamycine. Le site d insertion du vecteur est vérifié par PCR à l aide d un oligonucléotide spécifique de gène et un oligonucléotide spécifique du vecteur. L insertion du vecteur pvo155 dans le gène cible mène à la mutation de ce gène et à la création d une fusion transcriptionnelle entre le promoteur de ce gène et le gène rapporteur uida. OriT, Origine de réplication ; Bléo R, gène de résistance à la bléomycine ; Km R, gène de résistance à la kanamycine ; Amp R, gène de résistance à l ampicilline.
199 Matériel et Méthodes 1 min à température ambiante puis centrifugés 20 min à rpm à 4 C. 1 volume de phénol/chloroforme est ajouté au surnageant et mélangé par inversion. Une nouvelle étape de centrifugation est réalisée 15 min à rpm à 4 C. 2 volumes d éthanol absolu froid sont ajoutés au surnageant, le tout est mélangé par inversion puis centrifugé 20 min à 4 C. Le culot est lavé avec de l éthanol à 70%, centrifugé 5 min et séché au speed vac avant d être repris dans 100 μl TE 10/1 ph7 (Tris 10 mm, EDTA 1 mm) Conjugaison triparentale Xcc n étant pas facilement transformable, les transferts d ADN sont réalisés par conjugaison. Une préculture des souches est réalisée en milieu MOKA saccharose avec ou sans 2 % glycérol. 30 μl de préculture des souches Xcc LMG568 Rif R (Souche receveuse), E. coli portant le vecteur à transférer (Souche donneuse) et E. coli prk2073 [Souche «helper» permettant la conjugaison (Vargas et al., 1999)] sont mélangés puis déposés sur un filtre de nitrate de cellulose stérile de pores de 0.45µm (Sartorius) préalablement déposé sur une boite de milieu complet sans antibiotique. Après une nuit d incubation à 30 C, les filtres sont repris dans 2 (pour une construction de mutant) ou 10 ml (pour un simple transfert de vecteur) d eau stérile. 100 µl de l échantillon ainsi que le culot sont étalés sur des boites de milieux riches contenant les antibiotiques appropriés Construction de mutants d insertion et de fusions transcriptionnelles Les mutants d insertion ont été construits à l aide du vecteur suicide pvo155 (Oke and Long, 1999). Des fragments de 300 à 500 pb, internes au gène cible, ont été amplifiés par PCR et clonjés dans le plasmide pvo155. L insertion du vecteur suicide pvo155 dans le gène cible, réalisée par recombinaison homologue, mène à la création d une fusion transcriptionnelle entre le promoteur du gène cible et le gène rapporteur uida codant la glucuronidase du vecteur pvo155 (Figure M1). 116
200 Gène X 1 PCR WT Amont Aval 2 Clonage loxp pcm184 loxp kanamycin 3 Recombinaison homologue Recombinase Cre loxp loxp kanamycin ΔGène X :: kan pcre Tet R 4 Recombinaison par la recombinase Cre loxp 5 PCR ΔGène X Figure M2. Délétion d un gène par la stratégie Cre/Lox. (Marx and Lidstrom, 2002) 1: une portion amont et aval du gène cible X est amplifiée par PCR à l aide d oligonucléotides spécifiques portant à leurs extrémités les sites de restriction nécessaires au clonage dans le vecteur pcm Les fragments PCR obtenus sont clonés dans le vecteur pcm184 de part et d autre des sites loxp. 3. Ce nouveau plasmide est d abord transformé dans une souche d E. coli puis, après vérification de la séquence, il est transféré dans la souche de Xcc à muter par conjugaison triparentale. Le double événement de recombinaison entre les fragment amont et aval du gène X porté par le vecteur et sur le chromosome de la souche sauvage LMG568 de Xcc sera sélectionné par criblage des souches résistantes à la kanamycine. Ce double événement de recombinaison mène au remplacement du gène cible par la cassette «loxp-kanamycineloxp». 4. Le vecteur pcre est transféré dans la nouvelle souche par conjugaison triparentale. Ce vecteur porte un gène cre codant la recombinase Cre capable de reconnaître les sites loxp et d effectuer un événement de recombinaison entre ces deux sites, ceci menant à la perte du gène de résistance à la kanamycine. Cet événement est sélectionné par criblage des souches résistantes à la tétracycline et sensibles à la kanamycine. 5. La délétion du gène est vérifiée par PCR à l aide d un oligonucléotide s hybridant en amont du gène X et un oligonucléotide s hybridant en aval du gène X. Après plusieurs cultures de la souche ΔGène X sans pression de sélection, la perte du vecteur pcre est sélectionnée par criblage des souches sensibles à la tétracycline. Tet R, gène de résistance à la tétracycline ; Kan, kanamycine.
201 Gène X 1 PCR Amont orit sacb Aval 2 Clonage Km R pk18mobsacb-x oriv Recombinaison homologue 1 3 lacz Gène X Gene X 50% 50% 4 Recombinaison homologue 2 Xcc WT Gène X sacb Km R orit pk18mobsacb-x oriv lacz Xcc ΔGène X 5 PCR + + sacb Km R orit pk18 mobsacb-gène X lacz oriv Figure M3. Délétion d un gène par la stratégie SacB. (Schafer et al., 1994) 1. Une portion amont et aval du gène cible X est amplifiée par PCR à l aide d oligonucléotides spécifiques portant à leurs extrémités les sites de restriction nécessaires au clonage dans le vecteur pk18mobsacb. 2. Les fragments PCR obtenus sont clonés dans le vecteur à l intérieur du gène lacz. 3. Ce nouveau plasmide est d abord transformé dans une souche d E. coli puis, après vérification de la séquence, il est transféré dans la souche de Xanthomonas à muter par conjugaison triparentale. L insertion du vecteur sur le chromosome de la souche sauvage LMG568 de Xcc sera sélectionné par criblage des souches résistantes à la kanamycine et sensibles au saccharose (due à la présence du gène sacb). 4. L excision du vecteur sera ensuite sélectionné par criblage des souches sensibles à la kanamycine et résistantes au saccharose. 5. Dans 50 % des cas, cette excision mènera à la restauration d un génotype sauvage et dans 50 % des cas elle mènera à la délétion du gène cible. La délétion du gène est vérifiée par PCR à l aide d un oligonucléotide s hybridant en amont du gène X et un oligonucléotide s hybridant en aval du gène X. Km R, gène de résistance à la kanamycine.
202 Matériel et Méthodes 3.4. Construction des mutants de délétion Par la méthode Cre/Lox Des régions d environs 500 pb en amont et en aval du gène cible sont amplifiées par PCR (Figure M2) puis clonées dans le vecteur suicide pcm184 de part et d autre des sites loxp et du gène de résistance à la kanamycine (Marx and Lidstrom, 2002). Le vecteur est alors transféré par conjugaison triparentale dans la souche à muter. Le double événement de recombinaison menant au remplacement du gène cible par la cassette loxp-kanamycine-loxp est sélectionné sur milieux riche contenant de la kanamycine. Le vecteur pcre portant le gène codant la recombinase Cre et le gène de résistance à la tétracycline est à son tour transféré dans cette nouvelle souche. Les clones possédant ce vecteur sont sélectionnés sur un milieu riche contenant de la tétracycline. La recombinase Cre va reconnaître les deux sites loxp et permettre un événement de recombinaison entre ces deux sites, menant à la perte du gène codant la résistance à la kanamycine. La souche mutée est cultivée pendant plusieurs jours en milieu riche sans antibiotique afin de promouvoir la perte du vecteur Cre. Sans pression de sélection, un plasmide n est pas stable dans une souche de Xcc. On obtient au final, une souche ayant perdu le gène cible, et possédant un site loxp à la place, sensible à la kanamycine et à la téracycline. Attention, le site loxp crée un ATG avec le site de multiclonage, il est donc nécessaire d ajouter un ou plusieurs codons de terminaison de la traduction dans la partie 5 du produit PCR aval Par la méthode «SacB» Le site loxp laissé par la technique Cre/Lox peut poser des problèmes lorsque l on veut déléter plusieurs gènes. Il peut y avoir un risque de réarrangement chromosomique par recombinaison entre les différents sites loxp laissés lors des délétions par cette technique. Dans certains cas nous avons donc utilisé la méthode de délétion «SacB» qui ne laisse que la présence d un site de restriction. Les mêmes régions amont et aval du gène cible sont amplifiées puis clonées dans le vecteur pk18mobsacb (Figure M3). Ce vecteur porte le gène de résistance à la kanamycine et le gène sacb qui confère aux bactéries Gram - et certaines bactéries Gram + une sensibilité au saccharose (Schafer et al., 1994). Après transfert du vecteur dans la souche à muter, l intégration du vecteur dans le chromosome est sélectionnée sur milieu MOKA contenant de la kanamycine. Les clones kanamycine résistants sont repiqués sur MOKA rifampicine saccharose 10%. Les bactéries capables de pousser sur 117
203 Kan ptaq-smc-t7 Figure M4. Carte génétique du plasmide pcz1034. Kan: gène de résistance à la kanamycine aval 128: 700 paires de bases localisées juste en aval du gène XCC0128. amont 127: 700 paires de bases localisées juste en amont du gène XCC0127. ptaq: promoteur inductible à l IPTG. SMC: Sites Multiples de Clonage. T7: Terminateur de transcription T7
204 Matériel et Méthodes saccharose ont perdu le plasmide après un deuxième événement de recombinaison. On sélectionne donc les bactéries saccharose résistantes et qui sont également kanamycine sensible. Après cet évènement de recombinaison, environ 50 % des clones auront perdu le gène cible et 50 % seront redevenus sauvages. Il faut donc tester une dizaine de clones par PCR pour vérifier la perte du gène Complémentation La complémentation est réalisée par l apport en trans d un vecteur portant une copie sauvage du gène muté sous le contrôle d un promoteur inductible à l IPTG, Ptac et portant un gène de résistance à la tétracycline. Cependant, en absence d une pression de sélection, Xcc a tendance à perdre rapidement les vecteurs que nous lui avons transférés. Il est donc difficile de tester l effet d une complémentation génétique sur le développement des symptômes de la maladie sur plante. Pour cette raison, une deuxième technique de complémentation a été développée. La complémentation est alors réalisée par insertion d une copie du gène muté directement sur le chromosome en remplacement de deux gènes (XCC0127 et XCC0128) codant des transposases d origine sans doute virale. Pour cela le vecteur pk18mobsacb, utilisé à l origine pour la construction de mutants de délétion par la technique «SacB», a été transformé. Le gène lacz et le site multiple de clonage de pk18mobsacb ont été remplacés par une séquence de 700 pb de la région en amont de XCC0127 et une séquence de 700 pb de la région en aval de XCC0128 encadrant un promoteur Ptac, un site multiple de clonage et un terminateur de transcription T7 (Figure M4). Une fois la copie sauvage du gène muté clonée dans ce vecteur, le tout est transféré dans la souche à complémenter par conjugaison triparentale. Le double événement de recombinaison menant à l insertion du gène sur le chromosome est sélectionné comme décrit dans la technique «SacB» (voir ci-dessus) RT-PCR Quantitative (qrt-pcr) Les cellules sont cultivées dans le milieu approprié pendant 6 heures jusqu à l obtention d une DO 600 comprise entre 0,4 et 0,6. Les ARNs sont extraits à l aide du kit RNeasy Mini (QIAGEN). 2 µg d ARN sont traités avec la DNase I RNase-free (GE-Healthcare) pendant 30 min à 37 C. Après l inactivation de la DNase (10 min à 75 C), les ARNs sont incubés en présence d oligonucléotides de séquence aléatoire (Random hexamers, Biolabs), pendant
205 Arabidopsis thaliana Choux Bartolo Figure M5. Index de la maladie développée par Xanthomonas campestris pv. campestris, après infection par «piercing» de l écotype Sf-2 d A. thaliana ou de feuilles de choux Bartolo d après Meyer et al. (2005). Le développement des symptômes est noté de 0 à 4 (nombre en bas à gauche des photos). Pour A. thaliana : 0, pas de symptôme ; 1, légère chlorose autour du site d inoculation ; 2, chlorose étendue en forme de «V» ; 3, nécrose de la feuille ; 4, feuille tombée (non montré). Pour le chou : 0, pas de symptôme ; 1, légère chlorose autour du site d inoculation ; 2, chlorose étendue en forme de «V» confinée entre les deux premières nervures ; 2.5, chlorose en forme de «V»; 3,; 3.5, nécrose de la feuille confinée entre les deux premières nervures avec une chlorose dépassant les deux premières nervures ; 4, nécrose de la feuille dépassant les deux premières nervures.
206 Matériel et Méthodes min à 70 C afin de les dénaturer puis pendant 30 secondes à 4 C pour éviter leur renaturation. Après ajout de 2.5 µl de dntp 10 mm, 5 µl de DTT 0.1 M, 10 µl de tampon 5X (fourni avec la superscript II), 1µl de RNasin (Promega) et 1 µl de Superscript II (Invitrogen) les oligonucléotides sont hybridés 10 min à température ambiante, la polymérisation de l ADN est réalisée pendant 1 h à 42 C puis la réaction est stoppée par une incubation à 95 C pendant 2 min. Les tests de PCR quantitative sont effectués sur le Light Cycler de Roche à partir de 1µl d une dilution au 1/20 ème des ADNc mélangés à 6 µl d eau, 1µl d oligonucléotides spécifiques du gène dont on souhaite étudier l expression et 2 µl de mix enzymatique (Roche). Le cycle d amplification est le suivant : 10 min 95 C, 1 cycle ; 5 sec 95 C, 10 sec 65 C, 20 sec 72 C, 40 à 50 cycles. Trois répétitions indépendantes au moins sont réalisées, ainsi que des contrôles négatifs avec les ARNs non rétro-transcrits et l eau. La normalisation des expériences de qrt-pcr a été effectuée sur l ARN ribosomique 16S comme décrit par (Morales et al., 2005). L amplification de 72 pb de l ARNr 16S par les oligonucléotides amont (5 -TGACGGTACCCAAAGAATAAGCA-3 ) et aval (5 - ACGCTTGCACCCTTCGTATTA-3 ) a été effectuée grâce au cycle suivant : 10 min 95 C, 1 cycle ; 5 sec 95 C, 10 sec 70 C, 20 sec 72 C, 40 à 50 cycles. 4 Test du pouvoir pathogène des différents mutants de Xcc 4.1. Inoculation par «piercing» sur Arabidopsis thaliana SF2 et choux Bartolo Les expériences d inoculation sont menées comme décrit dans Meyer et al, (2005). En résumé, une aiguille est trempée dans une solution bactérienne dont la DO 600 est de 0.05 pour les arabette et de 0,2 pour les choux. Les feuilles sont ensuite percées avec cette aiguille en trois points au niveau de la nervure centrale (Figure M5). Pour les arabettes (Plantules agées d un mois), on inocule 4 plantes par souche et 4 feuilles par plante. Dans le cas des choux, on inocule la deuxième paire de feuille de plantes agées de 6 semaines environs. Les arabettes inoculées sont incubées dans une chambre de culture, ayant une température ambiante de 22 C, un taux d humidité d environ 60%, 9 h de jours et 15 h de nuit. Les choux inoculés sont incubés en mini serres dans une salle de culture ayant une température de jour de 27 C, une température de nuit de 25 C, 14h de jour et 10 h de nuit. L apparition des symptômes est 119
207 P 1 2 D Figure M6. Représentation schématique de la méthode de suivi de la croissance bactérienne in planta. 1. Les feuilles sont percées au niveau de la nervure centrale, en deux trous, situés à la pointe de la feuille disques foliaires par plante sont prélevés au site d inoculation (site «proximal», P) et à l opposé de la feuille (au site «distal», D) à l emporte pièce (diamètre, 0.65 cm, aire, 0.33 cm2). Ces disques sont ensuite broyés dans 500µl d H 2 O au broyeur à bille. 3. Les échantillons sont ensuite dilués de 10-1 à10-6 en plaque puis 5 µl de chaque dilution sont déposés sur des grandes boites carrées de milieu gélosée (contenant les antibiotiques de sélection) en 3 répétitions. Les microcolonies sont comptées au niveau de chaque spot.
208 Matériel et Méthodes observée à 3, 4, 5, 6, et 7 jours après l inoculation. Les indices de la maladie sont représentés figure 4M Inoculation par infiltration sur poivron Les feuilles de poivrons sont très légèrement entaillées à l aide de la pointe d une aiguille sur la face inférieure des feuilles. Une solution bactérienne d une DO 600 de 0,2 est infiltrée dans les tissus de la feuille à l aide d une seringue. L apparition ou non d une HR (Hypersensitive Response) est observée après 24 heures d incubation en salle de culture à 25 C, 14 h de jour et 10 h de nuit Croissance bactérienne in planta sur Arabidopsis thaliana SF2 (IGC ; Internal Growth Curve) 20 plantes par souches sont inoculées à la même DO 600 que celle utilisée pour les tests de pouvoir pathogène. Les feuilles sont percées au niveau de la nervure centrale, en deux trous, situés à la pointe de la feuille. L annotation des symptômes se fait comme cela a été décrit précédemment. Chaque souche est testée par au moins deux expériences indépendantes. Pour mesurer la croissance bactérienne in planta, 3 disques foliaires par plante sont prélevés au site d inoculation (site «proximal») et à l opposé de la feuille (au site «distal») à l emporte pièce (diamètre : 0,65 cm, aire : 0,33 cm 2 ). Les prélèvements se font sur 3 plantes différentes par point, à t0, 1, 3 et 7 jours après inoculation. 500µl d H 2 O sont ajoutés par tube ainsi que quelques billes de verre de 2 mm de diamètre. Les échantillons sont broyés à l aide d un broyeur Quiagen avec une fréquence de 30mvt/s pendant 2 fois 30 secondes. Les échantillons sont ensuite dilués de 10-1 à 10-6 en plaque puis 5 µl de chaque dilution sont déposés sur des grandes boites carrées de MOKA contenant de la rifampicine et de la pimaricine à 30µg/ml (antifongique) en 3 répétitions. (Figure M6) Les microcolonies sont comptées à l intérieure de chaque spot. Le nombre de CFU par cm 2 est déterminé par la formule suivante : 120
209 Matériel et Méthodes Log (CFU / cm 2 ) = log [(nb de colos * dilution retenue pour le comptage * (Volume d eau pour le broyage / Volume du spot déposé)) / (nombre de disques foliaires * surface d un disque foliaire)] 5 Test de stabilité des insertions pvo in planta 7 jours après l inoculation, la stabilité des insertions pvo des mutants (résistants à la kanamycine) est testée. Pour cela, on broie, à l aide de billes en verre de 2 mm de diamètre, une feuille inoculée par souche testée dans 500 µl d eau stérile. 50 µl des dilutions 10-3 (pour les mutants ne développant pas de symptômes sur plante) 10-4 et 10-5 (pour les autres) sont étalées sur milieu MOKA contenant de la rifampicine et de la pimaricine. Une centaine de clones par souches sont repiqués sur boites MOKA rifampicine et sur boites MOKA rifampicine et Kanamycine pour tester leur résistance à la Kanamycine. 6 Tests phénotypiques 6.1. Test du rôle du GlcNAc comme source d azote La souche sauvage de Xcc est cultivée en milieu minimum MME dépourvu d azote (K 2 HPO 4 à 1,05 %, KH 2 PO 4 à 0,45 %, MgSO 4-7 H 2 O 1 mm) avec ou sans ajout de GlcNAc 10 mm ou de Glucose 10 mm. La croissance est suivie par mesure de la turbidimétrie à 600nm Effet toxique du GlcNAc et de la phase stationnaire de croissance sur la croissance de mutants Les souches sont cultivées en milieu riche MOKA puis ensemencées dans le milieu approprié à une DO 600 de 0,1. A t0, 10h, 24h, 48h, 72h et 96h, la DO 600 est mesurée et les cultures sont diluées d un facteur 10 4 et 10 6 dans 5 ml d eau stérile. Les dilutions sont ensuite étalées sur des boites MOKA contenant de la rifampicine à l aide de l ensemenceur en spiral d Interscience. Après deux jours d incubation à 30 C, les colonies sont comptées et la densité bactérienne initiale est calculée. 121
210 Matériel et Méthodes Pour l effet du GlcNAc les souches sont cultivées en milieu minimum ou riche avec du GlcNAc à différentes concentrations et la croissance bactérienne est suivie par mesure de la DO Dosages d activités enzymatiques Différentes activités enzymatiques sont testées en mesurant l hydrolyse de substrats de synthèse tels que les 4-nitrophény-glycosides. Après 6 h d incubation dans le milieu approprié, la DO 600 des cultures est mesurée. L activité spécifique est exprimée en unités arbitraires, calculée selon la même formule que pour l activité β-galactosidase. Activité Spécifique = (DO 415-1,75* DO 550 )/(DO 600 *0.001*V en ml*t en min) 7.1. Dosages de l activité β-glucuronidase Solutions : Tampon GEB : Na 2 HPO 4 50 mm, ph 7 NaH 2 PO 4 50 mm, ph 7 EDTA 10 mm, ph 8 Triton 1 X Na lauryl sarcosine 0.1 % β-mercaptoéthanol mm PNPG (4-nitrophenyl-β glucuronide) mg/ml Dosages : 600 μl (volume V) de culture sont centrifugés, le culot est repris dans 600 μl de tampon GEB et vortexé pendant 10 secondes. Les tubes sont incubés 15 minutes à 37 C. 60 μl de PNPG est ajouté et les tubes sont incubés à 37 C pendant la durée nécessaire à l apparition d une coloration jaune (temps t, 1 h maximum). 250 μl de Na 2 CO 3 1 M est ajouté pour stopper la réaction, les tubes sont ensuite centrifugés 5 à 15 minutes à rpm. La DO 415 et la DO 550 sont mesurées au spectrophotomètre. 122
211 Matériel et Méthodes 7.2. Autres activités enzymatiques Activés testées : β-mannosidase, substrat : 4-Nitrophenyl β-d-mannopyranoside ; α- mannosidase, substrat : 4-Nitrophenyl α-d-mannopyranoside ; N-acétyl-β-glucosaminidase, substrat : 4-Nitrophenyl N-acétyl-β-D-glucosaminide ; β-galactosidase, substrat : 4- Nitrophenyl β-d-galactopyranoside ; α-l-fucosidase, substrat : 4-Nitrophenyl α-lfucopyranoside. Pour mesurer l activité N-acétyl-β-glucosaminidase, 400 µl de culture est mélangé à 400µl de tampon citrate 200mM ph 5.5 et à 40 µl de BSA à 100 mg/ml. Après 15 minutes d incubation à 37 C, 200 µl de substrat à 4 mg/ml est ajouté. Les tubes sont incubés à 37 C pendant la durée nécessaire à l apparition d une coloration jaune (temps t, 1 h maximum). 400 µl de K 2 CO 3 1 M est ajouté pour stopper la réaction, les tubes sont ensuite centrifugés 5 à 15 minutes à rpm. La DO 415 et la DO 550 sont mesurées. Pour les autres activités enzymatiques, les dosages sont réalisés dans du tampon phosphate ph7 (Na 2 HPO 4 60 mm, NaH 2 PO 4 40 mm, KCl 10 mm, MgSO 4 1 mm et BSA 1 mg/ml), et 200 µl de substrat à une concentration de 10 mg/ml est ajouté au mélange réactionnel. Les échantillons sont incubés à 37 C pour les tests d activité β-galactosidase et L-Fucosidase, 34 C pour les tests d activité β-mannosidase et 30 C pour les tests d activité α-mannosidase. La réaction est stoppée par l ajout de 400 µl de Na 2 CO 3 1 M et les DO 415 et DO 550 sont mesurées. Tous les substrats sont dilués dans l eau mis à part le 4-Nitrophenyl α-lfucopyranoside qui est repris dans du DMSO. Le 4-Nitrophenyl α-l-fucopyranoside, 4-Nitrophenyl α-d-mannopyranoside, 4-Nitrophenyl β-d-galactopyranoside, 4-Nitrophenyl β-d-mannopyranoside et le 4-Nitrophenyl N-acétyl-β- D-glucosaminide viennent de chez Sigma-aldrich. 8 Tests de transport de [ 14 C]GlcNAc Les cellules sont cultivées une nuit en milieu riche MOKA puis centrifugées (attention, les bactéries ne doivent pas être préalablement étalées sur des boites contenant le sucre testé). Le surnageant est éliminé et les culots sont resuspendus en milieu minimum MME à une DO 600 ajustée à µl de cellules sont mélangées à 75 µl de [ 14 C]GlcNAc (concentration finale de 0,5 µm) (Blanvillain et al., 2007). Après un temps d incubation variable à 28 C, les cellules 123
212 Matériel et Méthodes sont collectées par filtration sur des filtres de nitrate de cellulose, lavées avec 10 ml d eau, séchées pendant 20 minutes sur papier watmann à l'étuve préchauffée à 45 puis et incubées 1 heure dans 3,8 ml de liquide à scintillation. Le taux de radioactivité présent sur les filtres est mesuré à l aide d un compteur à scintillation. Pour les tests de compétition, les sucres non radiomarqués sont ajoutés au [ 14 C]GlcNAc à une concentration finale allant de 0,5 à 500 µm. Le Kd du transport est déterminé par mesure du transport initial (sur des temps très cours) en présence de différentes concentrations de GlcNAc (Blanvillain et al., 2007; Neugebauer et al., 2005). Les cellules sont incubées 15 sec en présence de 0.1, 0.25, 0.5, 1, 2.5, 5, 10, 25 et 50 µm [ 14 C] GlcNAc et 0,2 ml d échantillons sont dilués dans 5 ml d eau contenant 0,1 mm de GlcNAc. Les cellules sont ensuite collectées, lavées, séchées et la radioactivité est mesurée comme décrit préalablement. Formule : DPM/60= 1Bq Navogadro= 6,023E+23 Nombre de molécules transporté par cellules =[DPM/60x Navogadro]/[Activité Spécifique du sucre marqué x DO600 x nombre de bactéries x Vol déposé sur filtre x Facteur de dilution] 9 Tests de phosphorylation du GlcNAc Les tests d activité kinase sont réalisés par une mesure d activité enzymatique liée au ratio NAD + /NADH (Gonzali et al., 2001). Réaction : GlcNAc + ATP PEP + ADP Pyruvate + NADH NagK-II Pyruvate kinase Lactate déshydrogénase GlcNAc-6-P + ADP pyruvate + ATP lactate + NAD+ Une gamme étalon de dosage protéique par la technique de Bradford [10 µl d échantillon dans 990 µl de réactif de Bradford (Biorad), incubé 5 min à température ambiante, mesure de la DO 595 ] est réalisée avec des quantités de BSA allant de 0,05 µg à 1 mg. Une seconde gamme étalon de dosage de NADH est réalisée en mesurant l absorbance de concentrations de NADH allant de 0,1 µm à 1M à 340 nm. 124
213 Matériel et Méthodes 50 ml d une culture de Xcc en milieu minimum MME contenant du GlcNAc 10 mm sont centrifugés 20 minutes à 4000 rpm. Le culot bactérien obtenu est repris dans 2 ml de tampon de resuspension (0,05 mm Tris HCl ph8, 13,3 mm MgCl 2, 0,1 mm EDTA, 1 mm DTT). A partir de ce moment, les échantillons sont gardés dans la glace. Les cellules sont lysées par deux passages à la presse de French. Les échantillons sont ensuite centrifugés 2 min à vitesse maximum et le surnageant est transvasé dans un tube propre. 100 µl de ce lysat cellulaire est mélange à 900µl de tampon de réaction (0,1 M Tris HCl ph 7,5, 10 mm MgCl 2, 1 mm PEP, 4 mm ATP, 0,2 mm NADH, 10 mm GlcNAc, 4 U Lactate déshydrogénase, 4 U pyruvate kinase) incubé préalablement 5 min à 37 C. LA DO 340 est mesurée immédiatement puis toutes les 10 sec pendant 5 min (le blanc est réalisé avec un mélange réactionnel ne contenant pas l ATP et le NADH). La diminution de DO correspond à la consommation de NADH en NAD + et est directement corrélée à la phosphorylation du GlcNAc en GlcNAc-6-P. La quantité de protéines présente dans chacun des échantillons est mesurée par la technique de Bradford. L activité kinase est donnée en nmol de NAD + formé par min par mg de protéines. Formule: Activité= (NADH consommé (nmol))/(temps (min)* quantité protéines (mg)) 10 Analyses in silico La présence de séquences signales responsables du passage de la membrane interne à été déterminée grâce au serveur SignalP 3.0 (Bendtsen et al., 2004) avec les paramètres par défaut pour les bactéries a Gram négatif. 125
214 BIBLIOGRAPHIE
215 Bibliographie Aalberse, R.C., Koshte, V., and Clemens, J.G. (1981) Immunoglobulin E antibodies that crossreact with vegetable foods, pollen, and Hymenoptera venom. J Allergy Clin Immunol 68: Abu-Qarn, M., Eichler, J., and Sharon, N. (2008) Not just for Eukarya anymore: protein glycosylation in Bacteria and Archaea. Curr Opin Struct Biol 18: Alaimo, C., Catrein, I., Morf, L., Marolda, C.L., Callewaert, N., Valvano, M.A., Feldman, M.F., and Aebi, M. (2006) Two distinct but interchangeable mechanisms for flipping of lipid-linked oligosaccharides. Embo J 25: Albersheim, P., Darvill, A.G., McNeil, M., Valent, B., Sharp, J.K., Nothnagel, E.A., Davis, K.R., Yamazaki, N., Gollin, D.J., York, W.S., Dudman, W.F., Darvill, J.E., and Dell, A. (1983) Oligosaccharins, naturally occuring carbohydrates with biological regulatory functions. In Structure and Function of Plant Genomes. O Ciferri, L.D. (ed). New York: Plenum, pp Alfano, J.R., and Collmer, A. (1997) The type III (Hrp) secretion pathway of plant pathogenic bacteria: trafficking harpins, Avr proteins, and death. J Bacteriol 179: Alfano, J.R., and Collmer, A. (2004) Type III secretion system effector proteins: double agents in bacterial disease and plant defense. Annu Rev Phytopathol 42: Altamirano, M.M., Plumbridge, J.A., Horjales, E., and Calcagno, M.L. (1995) Asymmetric allosteric activation of Escherichia coli glucosamine-6-phosphate deaminase produced by replacements of Tyr 121. Biochemistry 34: Alvarez, A.M. (2000) Black rot of crucifers. In Mechanisms of Resistance to Plant Diseases: Alvarez, F.J., and Konopka, J.B. (2007) Identification of an N-acetylglucosamine transporter that mediates hyphal induction in Candida albicans. Mol Biol Cell 18: Alvarez-Anorve, L.I., Calcagno, M.L., and Plumbridge, J. (2005) Why does Escherichia coli grow more slowly on glucosamine than on N-acetylglucosamine? Effects of enzyme levels and allosteric activation of GlcN6P deaminase (NagB) on growth rates. J Bacteriol 187: Antoniw, J.F., Ritter, C.E., Pierpoint, W.S., and Van Loon, L.C. (1980) Comparison of three pathogenesis-related proteins from plants of two cultivars of tobacco infected with TMV. J Gen Virol 47: Apweiler, R., Hermjakob, H., and Sharon, N. (1999) On the frequency of protein glycosylation, as deduced from analysis of the SWISS-PROT database. Biochim Biophys Acta 1473: 4-8. Arlat, M., Gough, C.L., Barber, C.E., Boucher, C., and Daniels, M.J. (1991) Xanthomonas campestris contains a cluster of hrp genes related to the larger hrp cluster of Pseudomonas solanacearum. Mol Plant Microbe Interact 4: Arlat, M., Gough, C.L., Zischek, C., Barberis, P.A., Trigalet, A., and Boucher, C.A. (1992) Transcriptional organization and expression of the large hrp gene cluster of Pseudomonas solanacearum. Mol Plant Microbe Interact 5: Arlat, M., Van Gijsegem, F., Huet, J.C., Pernollet, J.C., and Boucher, C.A. (1994) PopA1, a protein which induces a hypersensitivity-like response on specific Petunia genotypes, is secreted via the Hrp pathway of Pseudomonas solanacearum. Embo J 13: Arnold, D.L., Pitman, A., and Jackson, R.W. (2003) Pathogenicity and other genomic islands in plant pathogenic bacteria. MoL Plant Pathol. 4: Arora, S.K., Wolfgang, M.C., Lory, S., and Ramphal, R. (2004) Sequence polymorphism in the glycosylation island and flagellins of Pseudomonas aeruginosa. J. Bacteriol. 186:
216 Bibliographie Ashby, M.K. (2004) Survey of the number of two-component response regulator genes in the complete and annotated genome sequences of prokaryotes. FEMS Microbiol Lett 231: Attridge, S.R., Manning, P.A., Holmgren, J., and Jonson, G. (1996) Relative significance of mannose-sensitive hemagglutinin and toxin-coregulated pili in colonization of infant mice by Vibrio cholerae El Tor. Infect Immun 64: Aunpad, R., and Panbangred, W. (2003) Cloning and characterization of the constitutively expressed chitinase C gene from a marine bacterium, Salinivibrio costicola strain 5SM-1. J Biosci Bioeng 96: Balaji, V., Gibly, A., Debbie, P., and Sessa, G. (2007) Transcriptional analysis of the tomato resistance response triggered by recognition of the Xanthomonas type III effector AvrXv3. Funct Integr Genomics 7: Barber, C.E., Tang, J.L., Feng, J.X., Pan, M.Q., Wilson, T.J., Slater, H., Dow, J.M., Williams, P., and Daniels, M.J. (1997) A novel regulatory system required for pathogenicity of Xanthomonas campestris is mediated by a small diffusible signal molecule. Mol Microbiol 24: Bardor, M., Cabrera, G., Rudd, P.M., Dwek, R.A., Cremata, J.A., and Lerouge, P. (2006) Analytical strategies to investigate plant N-glycan profiles in the context of plant-made pharmaceuticals. Curr Opin Struct Biol 16: Barnhart, M.M., Lynem, J., and Chapman, M.R. (2006) GlcNAc-6P levels modulate the expression of Curli fibers by Escherichia coli. J Bacteriol 188: Barreteau, H., Kovac, A., Boniface, A., Sova, M., Gobec, S., and Blanot, D. (2008) Cytoplasmic steps of peptidoglycan biosynthesis. FEMS Microbiol Rev 32: Bassler, B.L., Yu, C., Lee, Y.C., and Roseman, S. (1991) Chitin utilization by marine bacteria. Degradation and catabolism of chitin oligosaccharides by Vibrio furnissii. J Biol Chem 266: Batanero, E., Villalba, M., Monsalve, R.I., and Rodriguez, R. (1996) Cross-reactivity between the major allergen from olive pollen and unrelated glycoproteins: evidence of an epitope in the glycan moiety of the allergen. J Allergy Clin Immunol 97: Becker, A., Katzen, F., Puhler, A., and Ielpi, L. (1998) Xanthan gum biosynthesis and application: a biochemical/genetic perspective. Appl Microbiol Biotechnol 50: Beighton, D., Carr, A.D., and Oppenheim, B.A. (1994) Identification of viridans streptococci associated with bacteraemia in neutropenic cancer patients. J Med Microbiol 40: Bell, K.S., Sebaihia, M., Pritchard, L., Holden, M.T., Hyman, L.J., Holeva, M.C., Thomson, N.R., Bentley, S.D., Churcher, L.J., Mungall, K., Atkin, R., Bason, N., Brooks, K., Chillingworth, T., Clark, K., Doggett, J., Fraser, A., Hance, Z., Hauser, H., Jagels, K., Moule, S., Norbertczak, H., Ormond, D., Price, C., Quail, M.A., Sanders, M., Walker, D., Whitehead, S., Salmond, G.P., Birch, P.R., Parkhill, J., and Toth, I.K. (2004) Genome sequence of the enterobacterial phytopathogen Erwinia carotovora subsp. atroseptica and characterization of virulence factors. Proc Natl Acad Sci U S A 101: Bender, C.L., Alarcon-Chaidez, F., and Gross, D.C. (1999) Pseudomonas syringae phytotoxins: mode of action, regulation, and biosynthesis by peptide and polyketide synthetases. Microbiol Mol Biol Rev 63: Bendtsen, J.D., Nielsen, H., von Heijne, G., and Brunak, S. (2004) Improved prediction of signal peptides: SignalP 3.0. J Mol Biol 340: Bent, A.F., Innes, R.W., Ecker, J.R., and Staskawicz, B.J. (1992) Disease development in ethylene-insensitive Arabidopsis thaliana infected with virulent and avirulent Pseudomonas and Xanthomonas pathogens. Mol Plant Microbe Interact 5:
217 Bibliographie Bent, A.F., and Mackey, D. (2007) Elicitors, effectors, and R genes: the new paradigm and a lifetime supply of questions. Annu Rev Phytopathol 45: Berger, S., Menudier, A., Julien, R., and Karamanos, Y. (1995) Do de-n-glycosylation enzymes have an important role in plant cells? Biochimie 77: Berger, S., Sinha, A.K., and Roitsch, T. (2007) Plant physiology meets phytopathology: plant primary metabolism and plant-pathogen interactions. J Exp Bot 58: Bernheim, N.J., and Dobrogosz, W.J. (1970) Amino sugar sensitivity in Escherichia coli mutants unable to grow on N-acetylglucosamine. J Bacteriol 101: Berninsone, P.M. (2006) Carbohydrates and glycosylation. WormBook: Berry, A.M., Lock, R.A., Thomas, S.M., Rajan, D.P., Hansman, D., and Paton, J.C. (1994) Cloning and nucleotide sequence of the Streptococcus pneumoniae hyaluronidase gene and purification of the enzyme from recombinant Escherichia coli. Infect Immun 62: Berry, A.M., Lock, R.A., and Paton, J.C. (1996) Cloning and characterization of nanb, a second Streptococcus pneumoniae neuraminidase gene, and purification of the NanB enzyme from recombinant Escherichia coli. J Bacteriol 178: Bestwick, C.S., Bennett, M.H., and Mansfield, J.W. (1995) Hrp Mutant of Pseudomonas syringae pv phaseolicola Induces Cell Wall Alterations but Not Membrane Damage Leading to the Hypersensitive Reaction in Lettuce. Plant Physiol 108: Bhaya, D., Takahashi, A., and Grossman, A.R. (2001) Light regulation of type IV pilusdependent motility by chemosensor-like elements in Synechocystis PCC6803. Proc Natl Acad Sci U S A 98: Birch, R.G., and Patil, S.S. (1985) Preliminary characterization of an antibiotic produced by Xanthomonas albilineans which inhibits DNA synthesis in Escherichia coli. J Gen Microbiol 131: Birch, R.G., and Patil, S.S. (1987) Evidence that an albicidin-like phytotoxin induces chlorosis in sugarcane leaf scald disease by blocking plastid DNAreplication. Physiol Mol Plant Pathol 30. Blanvillain, S. (2007) Etude des récepteurs TonB-dépendants et d'un nouvel effecteur de type III de la bactérie phytopathogène Xanthomonas campestris pv. campestris. Thèse. Blanvillain, S., Meyer, D., Boulanger, A., Lautier, M., Guynet, C., Denance, N., Vasse, J., Lauber, E., and Arlat, M. (2007) Plant carbohydrate scavenging through tonbdependent receptors: a feature shared by phytopathogenic and aquatic bacteria. PLoS ONE 2: e224. Boisson, M., Gomord, V., Audran, C., Berger, N., Dubreucq, B., Granier, F., Lerouge, P., Faye, L., Caboche, M., and Lepiniec, L. (2001) Arabidopsis glucosidase I mutants reveal a critical role of N-glycan trimming in seed development. Embo J 20: Boller, T. (1995) Chemoperception of microbila signals in plant cells. Annu Rev Plant Physiol Plant Mol Biol 46: Bollini, R., Ceriotti, A., Daminati, M.G., and Vitale, A. (1985) Glycosylation is not needed for the intracellular transport of phytohemagglutinin in developping Phaseolus vulgaris cotyledons and for the maintenance of its biological activities. Physiol Plant 65: Bonas, U., Stall, R.E., and Staskawicz, B. (1989) Genetic and structural characterization of the avirulence gene avrbs3 from Xanthomonas campestris pv. vesicatoria. Mol Gen Genet 218: Boneca, I.G. (2005) The role of peptidoglycan in pathogenesis. Curr Opin Microbiol 8: Bonin, C.P., Potter, I., Vanzin, G.F., and Reiter, W.D. (1997) The MUR1 gene of Arabidopsis thaliana encodes an isoform of GDP-D-mannose-4,6-dehydratase, catalyzing the first 128
218 Bibliographie step in the de novo synthesis of GDP-L-fucose. Proc Natl Acad Sci U S A 94: Bouhss, A., Trunkfield, A.E., Bugg, T.D., and Mengin-Lecreulx, D. (2008) The biosynthesis of peptidoglycan lipid-linked intermediates. FEMS Microbiol Rev 32: Braun, V., and Rehn, K. (1969) Chemical characterization, spatial distribution and function of a lipoprotein (murein-lipoprotein) of the E. coli cell wall. The specific effect of trypsin on the membrane structure. Eur J Biochem 10: Braun, V. (1975) Covalent lipoprotein from the outer membrane of Escherichia coli. Biochim Biophys Acta 415: Braun, V., and Killmann, H. (1999) Bacterial solutions to the iron-supply problem. Trends Biochem Sci 24: Brown IR, Mansfield JW, and U, B. (1995) hrp genes in Xanthomonas campestris pv. vesicatoria determine ability to suppress papilla deposition in pepper mesophyll cells. Mol Plant Microbe Interact 8. Burnaugh, A.M., Frantz, L.J., and King, S.J. (2008) Growth of Streptococcus pneumoniae on human glycoconjugates is dependent upon the sequential activity of bacterial exoglycosidases. J Bacteriol 190: Buttner, D., Nennstiel, D., Klusener, B., and Bonas, U. (2002) Functional analysis of HrpF, a putative type III translocon protein from Xanthomonas campestris pv. vesicatoria. J Bacteriol 184: Byers, H.L., Tarelli, E., Homer, K.A., and Beighton, D. (1999) Sequential deglycosylation and utilization of the N-linked, complex-type glycans of human alpha1-acid glycoprotein mediates growth of Streptococcus oralis. Glycobiology 9: Calcagno, M., Campos, P.J., Mulliert, G., and Suastegui, J. (1984) Purification, molecular and kinetic properties of glucosamine-6-phosphate isomerase (deaminase) from Escherichia coli. Biochim Biophys Acta 787: Camara, M., Boulnois, G.J., Andrew, P.W., and Mitchell, T.J. (1994) A neuraminidase from Streptococcus pneumoniae has the features of a surface protein. Infect Immun 62: Capage, M.A., Doherty, D.H., Betlach, M.R., and Vanderslice, R.W. (1987) Recombinant- DNA mediated production of xanthan gum. International patent WO87/ Castric, P. (1995) pilo, a gene required for glycosylation of Pseudomonas aeruginosa 1244 pilin. Microbiology 141 ( Pt 5): Castric, P., Cassels, F.J., and Carlson, R.W. (2001) Structural characterization of the Pseudomonas aeruginosa 1244 pilin glycan. J Biol Chem 276: Chang, J.H., Urbach, J.M., Law, T.F., Arnold, L.W., Hu, A., Gombar, S., Grant, S.R., Ausubel, F.M., and Dangl, J.L. (2005) A high-throughput, near-saturating screen for type III effector genes from Pseudomonas syringae. Proc Natl Acad Sci U S A 102: Chantret, I., and Moore, S.E. (2008) Free oligosaccharide regulation during mammalian protein N-glycosylation. Glycobiology 18: Chao, N.X., Wei, K., Chen, Q., Meng, Q.L., Tang, D.J., He, Y.Q., Lu, G.T., Jiang, B.L., Liang, X.X., Feng, J.X., Chen, B., and Tang, J.L. (2008) The rsma-like gene rsma(xcc) of Xanthomonas campestris pv. campestris is involved in the control of various cellular processes, including pathogenesis. Mol Plant Microbe Interact 21: Chapman, B.S., Eckart, M.R., Kaufman, S.E., and Lapointe, G.R. (1996) O-linked oligosaccharide on the 75-kDa neurotrophin receptor. J Neurochem 66: Chaput, C., and Boneca, I.G. (2007) Peptidoglycan detection by mammals and flies. Microbes Infect 9:
219 Bibliographie Chen, M.M., Glover, K.J., and Imperiali, B. (2007) From peptide to protein: comparative analysis of the substrate specificity of N-linked glycosylation in C. jejuni. Biochemistry 46: Cheng, Q., Li, H., Merdek, K., and Park, J.T. (2000) Molecular characterization of the beta-nacetylglucosaminidase of Escherichia coli and its role in cell wall recycling. J Bacteriol 182: Cheng, Q., and Park, J.T. (2002) Substrate specificity of the AmpG permease required for recycling of cell wall anhydro-muropeptides. J Bacteriol 184: Chevance, F.F., and Hughes, K.T. (2008) Coordinating assembly of a bacterial macromolecular machine. Nat Rev Microbiol 6: Chisholm, S.T., Coaker, G., Day, B., and Staskawicz, B.J. (2006) Host-microbe interactions: shaping the evolution of the plant immune response. Cell 124: Chun, W., Cui, J., and Poplawsky, A. (1997) Purification, characterization and biological role of a pheromone produced by Xanthomonas campestris pv. campestris. Physiological and Molecular Plant Pathology 51: Ciesiolka, L.D., Hwin, T., Gearlds, J.D., Minsavage, G.V., Saenz, R., Bravo, M., Handley, V., Conover, S.M., Zhang, H., Caporgno, J., Phengrasamy, N.B., Toms, A.O., Stall, R.E., and Whalen, M.C. (1999) Regulation of expression of avirulence gene avrrxv and identification of a family of host interaction factors by sequence analysis of avrbst. Mol Plant Microbe Interact 12: Clarke, V.A., Platt, N., and Butters, T.D. (1995) Cloning and expression of the beta-nacetylglucosaminidase gene from Streptococcus pneumoniae. Generation of truncated enzymes with modified a glycon specificity. J Biol Chem 270: Cloud-Hansen, K.A., Peterson, S.B., Stabb, E.V., Goldman, W.E., McFall-Ngai, M.J., and Handelsman, J. (2006) Breaching the great wall: peptidoglycan and microbial interactions. Nat Rev Microbiol 4: Cole, R.N., and Hart, G.W. (1999) Glycosylation sites flank phosphorylation sites on synapsin I: O-linked N-acetylglucosamine residues are localized within domains mediating synapsin I interactions. J Neurochem 73: Comer, F.I., and Hart, G.W. (1999) O-GlcNAc and the control of gene expression. Biochim Biophys Acta 1473: Comer, J.E., Marshall, M.A., Blanch, V.J., Deal, C.D., and Castric, P. (2002) Identification of the Pseudomonas aeruginosa 1244 pilin glycosylation site. Infect Immun 70: Corfield, T. (1992) Bacterial sialidases--roles in pathogenicity and nutrition. Glycobiology 2: Cornelis, G.R. (2006) The type III secretion injectisome. Nat Rev Microbiol 4: Cosgrove, D.J. (2005) Growth of the plant cell wall. Nat Rev Mol Cell Biol 6: Costa, J., Ashford, D.A., Nimtz, M., Bento, I., Frazao, C., Esteves, C.L., Faro, C.J., Kervinen, J., Pires, E., Verissimo, P., Wlodawer, A., and Carrondo, M.A. (1997) The glycosylation of the aspartic proteinases from barley (Hordeum vulgare L.) and cardoon (Cynara cardunculus L.). Eur J Biochem 243: Cottrell, M.T., Wood, D.N., Yu, L., and Kirchman, D.L. (2000) Selected chitinase genes in cultured and uncultured marine bacteria in the alpha- and gamma-subclasses of the proteobacteria. Appl Environ Microbiol 66: Craig, L., Pique, M.E., and Tainer, J.A. (2004) Type IV pilus structure and bacterial pathogenicity. Nat Rev Microbiol 2: Craig, L., and Li, J. (2008) Type IV pili: paradoxes in form and function. Curr Opin Struct Biol 18: Creuzenet, C. (2004) Characterization of CJ1293, a new UDP-GlcNAc C6 dehydratase from Campylobacter jejuni. FEBS Lett 559:
220 Bibliographie Crossman, L., and Dow, J.M. (2004) Biofilm formation and dispersal in Xanthomonas campestris. Microbes Infect 6: Curtis, S.J., and Epstein, W. (1975) Phosphorylation of D-glucose in Escherichia coli mutants defective in glucosephosphotransferase, mannosephosphotransferase, and glucokinase. J Bacteriol 122: da Silva, A.C., Ferro, J.A., Reinach, F.C., Farah, C.S., Furlan, L.R., Quaggio, R.B., Monteiro- Vitorello, C.B., Van Sluys, M.A., Almeida, N.F., Alves, L.M., do Amaral, A.M., Bertolini, M.C., Camargo, L.E., Camarotte, G., Cannavan, F., Cardozo, J., Chambergo, F., Ciapina, L.P., Cicarelli, R.M., Coutinho, L.L., Cursino-Santos, J.R., El-Dorry, H., Faria, J.B., Ferreira, A.J., Ferreira, R.C., Ferro, M.I., Formighieri, E.F., Franco, M.C., Greggio, C.C., Gruber, A., Katsuyama, A.M., Kishi, L.T., Leite, R.P., Lemos, E.G., Lemos, M.V., Locali, E.C., Machado, M.A., Madeira, A.M., Martinez- Rossi, N.M., Martins, E.C., Meidanis, J., Menck, C.F., Miyaki, C.Y., Moon, D.H., Moreira, L.M., Novo, M.T., Okura, V.K., Oliveira, M.C., Oliveira, V.R., Pereira, H.A., Rossi, A., Sena, J.A., Silva, C., de Souza, R.F., Spinola, L.A., Takita, M.A., Tamura, R.E., Teixeira, E.C., Tezza, R.I., Trindade dos Santos, M., Truffi, D., Tsai, S.M., White, F.F., Setubal, J.C., and Kitajima, J.P. (2002) Comparison of the genomes of two Xanthomonas pathogens with differing host specificities. Nature 417: Dangl, J.L., and Jones, J.D. (2001) Plant pathogens and integrated defence responses to infection. Nature 411: Darsonval, A., Darrasse, A., Meyer, D., Demarty, M., Durand, K., Bureau, C., Manceau, C., and Jacques, M.A. (2008) The Type III secretion system of Xanthomonas fuscans subsp. fuscans is involved in the phyllosphere colonization process and in transmission to seeds of susceptible beans. Appl Environ Microbiol 74: Datta-Roy, K., Dasgupta, C., and Ghose, A.C. (1989) Hemagglutination and intestinal adherence properties of clinical and environmental isolates of non-o1 Vibrio cholerae. Appl Environ Microbiol 55: de Crecy-Lagard, V., Binet, M., and Danchin, A. (1995) Fructose phosphotransferase system of Xanthomonas campestris pv. campestris: characterization of the frub gene. Microbiology 141 ( Pt 9): De Graaf, T.W., Van der Stelt, M.E., Anbergen, M.G., and van Dijk, W. (1993) Inflammation-induced expression of sialyl Lewis X-containing glycan structures on alpha 1-acid glycoprotein (orosomucoid) in human sera. J Exp Med 177: de Lorenzo, G. (2007) Oligogalacturonide signalling: sensing a breach in wall. XIII International Congress on Molecular Plant-Microbe Interaction (MPMI), Sorrento, Italy. de Wit, P.J. (2002) Plant biology: on guard. Nature 416: Delledonne, M., Murgia, I., Ederle, D., Sbicego, P.F., Biondani, A., and Polverari, A.L., C. (2002) Reactive oxygen intermediates modulate nitric oxyde signaling in the plant hypersensitive disease-resistance response. Plant Physiology Biochemistry 40: Dennis, J.W., Granovsky, M., and Warren, C.E. (1999) Glycoprotein glycosylation and cancer progression. Biochim Biophys Acta 1473: Denny, T.P. (1995) Involvement of bacterial polysaccharides in plant pathogenesis. Annu Rev Phytopathol 33: Deslandes, L., Olivier, J., Theulieres, F., Hirsch, J., Feng, D.X., Bittner-Eddy, P., Beynon, J., and Marco, Y. (2002) Resistance to Ralstonia solanacearum in Arabidopsis thaliana is conferred by the recessive RRS1-R gene, a member of a novel family of resistance genes. Proc Natl Acad Sci U S A 99: Deslandes, L., Olivier, J., Peeters, N., Feng, D.X., Khounlotham, M., Boucher, C., Somssich, I., Genin, S., and Marco, Y. (2003) Physical interaction between RRS1-R, a protein 131
221 Bibliographie conferring resistance to bacterial wilt, and PopP2, a type III effector targeted to the plant nucleus. Proc Natl Acad Sci U S A 100: Dixon, D.R., and Darveau, R.P. (2005) Lipopolysaccharide heterogeneity: innate host responses to bacterial modification of lipid a structure. J Dent Res 84: Dobrindt, U., Hochhut, B., Hentschel, U., and Hacker, J. (2004) Genomic islands in pathogenic and environmental microorganisms. Nat Rev Microbiol 2: Dong, Y.H., Wang, L.Y., and Zhang, L.H. (2007) Quorum-quenching microbial infections: mechanisms and implications. Philos Trans R Soc Lond B Biol Sci 362: Dow, J.M., Davies, H.A., and Daniels, M.J. (1998) A metalloprotease from Xanthomonas campestris that specifically degrades proline/hydroxyproline-rich glycoproteins of the plant extracellular matrix. Mol Plant Microbe Interact 11: Dow, J.M., Crossman, L., Findlay, K., He, Y.Q., Feng, J.X., and Tang, J.L. (2003) Biofilm dispersal in Xanthomonas campestris is controlled by cell-cell signaling and is required for full virulence to plants. Proc Natl Acad Sci U S A 100: Dow, J.M., Fouhy, Y., Lucey, J.F., and Ryan, R.P. (2006) The HD-GYP domain, cyclic di- GMP signaling, and bacterial virulence to plants. Mol Plant Microbe Interact 19: Dramsi, S., Magnet, S., Davison, S., and Arthur, M. (2008) Covalent attachment of proteins to peptidoglycan. FEMS Microbiol Rev 32: Durrant, W.E., and Dong, X. (2004) Systemic acquired resistance. Annu Rev Phytopathol 42: Dwek, R.A. (1996) Glycobiology: Toward Understanding the Function of Sugars. Chem Rev 96: Eisenbeis, S., Lohmiller, S., Valdebenito, M., Leicht, S., and Braun, V. (2008) NagAdependent uptake of N-acetyl-glucosamine and N-acetyl-chitin oligosaccharides across the outer membrane of Caulobacter crescentus. J Bacteriol 190: El Qaidi, S., and Plumbridge, J. (2008) Switching control of expression of ptsg from the Mlc regulon to the NagC regulon. J Bacteriol 190: El Qaidi, S., Allemand, F., Oberto, J., and Plumbridge, J. (2009) Repression of galp, the galactose transporter in Escherichia coli, requires the specific regulator of N- acetylglucosamine metabolism. Mol Microbiol 71: Epple, P., Apel, K., and Bohlmann, H. (1995) An Arabidopsis thaliana thionin gene is inducible via a signal transduction pathway different from that for pathogenesisrelated proteins. Plant Physiol 109: Erbs, G., Silipo, A., Aslam, S., De Castro, C., Liparoti, V., Flagiello, A., Pucci, P., Lanzetta, R., Parrilli, M., Molinaro, A., Newman, M.A., and Cooper, R.M. (2008) Peptidoglycan and muropeptides from pathogens Agrobacterium and Xanthomonas elicit plant innate immunity: structure and activity. Chem Biol 15: Escolar, L., Perez-Martin, J., and de Lorenzo, V. (1999) Opening the iron box: transcriptional metalloregulation by the Fur protein. J Bacteriol 181: Escolar, L., van den Ackerveken, G., Rossier, O., Pieplow, S., and U., B. (2001) Type III secretion and in planta recognition of the Xanthomonas avirulence proteins AvrBs1 and AvrBsT. MoL Plant Pathol. 2: Etchegaray, A., Silva-Stenico, M.E., Moon, D.H., and Tsai, S.M. (2004) In silico analysis of nonribosomal peptide synthetases of Xanthomonas axonopodis pv. citri: identification of putative siderophore and lipopeptide biosynthetic genes. Microbiol Res 159: Expert, D. (2005) Genetic regulation of iron in Erwinia chrysanthemi as pertains to bacterial virulence. Barton LL, Abadia J (eds) Iron nutrition in plants and rhizospheric microorganisms.:
222 Bibliographie Fargier, E., and Manceau, C. (2007) Pathogenicity assays restrict the species Xanthomonas campestris into three pathovars and reveal nine races within X. campestris pv. campestris. Plant Pathology 56: Faridmoayer, A., Fentabil, M.A., Mills, D.C., Klassen, J.S., and Feldman, M.F. (2007) Functional characterization of bacterial oligosaccharyltransferases involved in O- linked protein glycosylation. J Bacteriol 189: Faye, L., and Chrispeels, M.J. (1987) Transport and processing of the glycosylated precursor of concanavalin A in jack-bean. Planta 170: Faye, L., and Chispeels, M.J. (1988) Common antigenic determinants in the glycoproteins of plants, molluscs and insects. Glycoconjugate J 5: Feiz, L., Irshad, M., Pont-Lezica, R.F., Canut, H., and Jamet, E. (2006) Evaluation of cell wall preparations for proteomics: a new procedure for purifying cell walls from Arabidopsis hypocotyls. Plant Methods 2: 10. Feldman, M.F., Wacker, M., Hernandez, M., Hitchen, P.G., Marolda, C.L., Kowarik, M., Morris, H.R., Dell, A., Valvano, M.A., and Aebi, M. (2005) Engineering N-linked protein glycosylation with diverse O antigen lipopolysaccharide structures in Escherichia coli. Proc Natl Acad Sci U S A 102: Felix, G., Duran, J.D., Volko, S., and Boller, T. (1999) Plants have a sensitive perception system for the most conserved domain of bacterial flagellin. Plant J 18: Ferreira, F.M., Mendoza-Hernandez, G., Castaneda-Bueno, M., Aparicio, R., Fischer, H., Calcagno, M.L., and Oliva, G. (2006) Structural analysis of N-acetylglucosamine-6- phosphate deacetylase apoenzyme from Escherichia coli. J Mol Biol 359: Finn, T.M., Reiser, J., Germanier, R., and Cryz, S.J., Jr. (1987) Cell-associated hemagglutinin-deficient mutant of Vibrio cholerae. Infect Immun 55: Fitchette, A.C., Cabanes-Macheteau, M., Marvin, L., Martin, B., Satiat-Jeunemaitre, B., Gomord, V., Crooks, K., Lerouge, P., Faye, L., and Hawes, C. (1999) Biosynthesis and immunolocalization of Lewis a-containing N-glycans in the plant cell. Plant Physiol 121: Fitchette-laine, A.C., Gomord, V., Chekkafi, A., and Faye, L. (1994) Distribution of xylosylation and fucosylation in the plant Golgi apparatus. Plant J. 5: Fitchette-Laine, A.C., Gomord, V., Cabanes, M., Michalski, J.C., Saint Macary, M., Foucher, B., Cavelier, B., Hawes, C., Lerouge, P., and Faye, L. (1997) N-glycans harboring the Lewis a epitope are expressed at the surface of plant cells. Plant J 12: Flavier, A.B., Clough, S.J., Schell, M.A., and Denny, T.P. (1997) Identification of 3- hydroxypalmitic acid methyl ester as a novel autoregulator controlling virulence in Ralstonia solanacearum. Mol Microbiol 26: Flor, H.H. (1971) Current status of the gene-for-gene concept. Annu Rev Microbiol 9: Fouhy, Y., Lucey, J.F., Ryan, R.P., and Dow, J.M. (2006) Cell-cell signaling, cyclic di-gmp turnover and regulation of virulence in Xanthomonas campestris. Res Microbiol 157: Fournet, B., Montreuil, J., Strecker, G., Dorland, L., Haverkamp, J., Vliegenthart, F.G., Binette, J.P., and Schmid, K. (1978) Determination of the primary structures of 16 asialo-carbohydrate units derived from human plasma alpha 1-acid glycoprotein by 360-MHZ 1H NMR spectroscopy and permethylation analysis. Biochemistry 17: Franza, T., Mahe, B., and Expert, D. (2005) Erwinia chrysanthemi requires a second iron transport route dependent of the siderophore achromobactin for extracellular growth and plant infection. Mol Microbiol 55: Fry, S.C., Aldington, S., Hetherington, P.R., and Aitken, J. (1993) Oligosaccharides as signals and substrates in the plant cell wall. Plant Physiol 103:
223 Bibliographie Fumagalli, O., Tall, B.D., Schipper, C., and Oelschlaeger, T.A. (1997) N-glycosylated proteins are involved in efficient internalization of Klebsiella pneumoniae by cultured human epithelial cells. Infect Immun 65: Gaffney, T., Friedrich, L., Vernooij, B., Negrotto, D., Nye, G., Uknes, S., Ward, E., Kessmann, H., and Ryals, J. (1993) Requirement of Salicylic Acid for the Induction of Systemic Acquired Resistance. Science 261: Gahring, L.C., Heffron, F., Finlay, B.B., and Falkow, S. (1990) Invasion and replication of Salmonella typhimurium in animal cells. Infect Immun 58: Garcia-Ochoa, F., Santos, V.E., Casas, J.A., and Gomez, E. (2000) Xanthan gum: production, recovery, and properties. Biotechnol Adv 18: Garcia-Olmedo, F., Molina, A., Segura, A., and Moreno, M. (1995) The defensive role of nonspecific lipid-transfer proteins in plants. Trends Microbiol 3: Gelfand, M.S., and Laikova, O.N. (2003) in Frontiers in Computational Genomics. Koonin, E. V., and Galperin, M. Y., eds, Caister Academic Press, Wymondham, UK: Gillmor, C.S., Poindexter, P., Lorieau, J., Palcic, M.M., and Somerville, C. (2002) Alphaglucosidase I is required for cellulose biosynthesis and morphogenesis in Arabidopsis. J Cell Biol 156: Glauner, B. (1988) Separation and quantification of muropeptides with high-performance liquid chromatography. Anal Biochem 172: Godoy, V.G., Dallas, M.M., Russo, T.A., and Malamy, M.H. (1993) A role for Bacteroides fragilis neuraminidase in bacterial growth in two model systems. Infect Immun 61: Goldenbaum, P.E., Broman, R.L., and Dobrogosz, W.J. (1970) Cyclic 3',5'-adenosine monophosphate and N-acetylglucosamine-6-phosphate as regulatory signals in catabolite repression of the lac operon in Escherichia coli. J Bacteriol 103: Goldman, W.E., Klapper, D.G., and Baseman, J.B. (1982) Detection, isolation, and analysis of a released Bordetella pertussis product toxic to cultured tracheal cells. Infect Immun 36: Gomez-Gomez, L., and Boller, T. (2002) Flagellin perception: a paradigm for innate immunity. Trends Plant Sci 7: Gonzalez, J.E., and Keshavan, N.D. (2006) Messing with bacterial quorum sensing. Microbiol Mol Biol Rev 70: Gonzali, S., Pistelli, L., De Bellis, L., and Alpi, A. (2001) Characterization of two Arabidopsis thaliana fructokinases. Plant Sci 160: Gooday, G.W. (1990) The ecology of chitin degradation. Adv. Microb. Ecol. 11: Goodell, E.W. (1985) Recycling of murein by Escherichia coli. J Bacteriol 163: Goon, S., Kelly, J.F., Logan, S.M., Ewing, C.P., and Guerry, P. (2003) Pseudaminic acid, the major modification on Campylobacter flagellin, is synthesized via the Cj1293 gene. Mol Microbiol 50: Gopalan, S., Bauer, D.W., Alfano, J.R., Loniello, A.O., He, S.Y., and Collmer, A. (1996) Expression of the Pseudomonas syringae avirulence protein AvrB in plant cells alleviates its dependence on the hypersensitive response and pathogenicity (Hrp) secretion system in eliciting genotype-specific hypersensitive cell death. Plant Cell 8: Gough, C.L., Dow, J.M., Keen, J., Henrissat, B., and Daniels, M.J. (1990) Nucleotide sequence of the engxca gene encoding the major endoglucanase of Xanthomonas campestris pv. campestris. Gene 89: Grant, S.R., Fisher, E.J., Chang, J.H., Mole, B.M., and Dangl, J.L. (2006) Subterfuge and manipulation: type III effector proteins of phytopathogenic bacteria. Annu Rev Microbiol 60:
224 Bibliographie Green, T.R., and Ryan, C.A. (1972) Wound-Induced Proteinase Inhibitor in Plant Leaves: A Possible Defense Mechanism against Insects. Science 175: Gudmundsdottir, A., Bell, P.E., Lundrigan, M.D., Bradbeer, C., and Kadner, R.J. (1989) Point mutations in a conserved region (TonB box) of Escherichia coli outer membrane protein BtuB affect vitamin B12 transport. J Bacteriol 171: Guinez, C., Lemoine, J., Michalski, J.C., and Lefebvre, T. (2004) 70-kDa-heat shock protein presents an adjustable lectinic activity towards O-linked N-acetylglucosamine. Biochem Biophys Res Commun 319: Gurlebeck, D., Thieme, F., and Bonas, U. (2006) Type III effector proteins from the plant pathogen Xanthomonas and their role in the interaction with the host plant. J Plant Physiol 163: Guttman, D.S., Vinatzer, B.A., Sarkar, S.F., Ranall, M.V., Kettler, G., and Greenberg, J.T. (2002) A functional screen for the type III (Hrp) secretome of the plant pathogen Pseudomonas syringae. Science 295: Guttman, D.S., Gropp, S.J., Morgan, R.L., and Wang, P.W. (2006) Diversifying selection drives the evolution of the type III secretion system pilus of Pseudomonas syringae. Mol Biol Evol 23: Hall, R.S., Brown, S., Fedorov, A.A., Fedorov, E.V., Xu, C., Babbitt, P.C., Almo, S.C., and Raushel, F.M. (2007) Structural diversity within the mononuclear and binuclear active sites of N-acetyl-D-glucosamine-6-phosphate deacetylase. Biochemistry 46: Han, I., and Kudlow, J.E. (1997) Reduced O glycosylation of Sp1 is associated with increased proteasome susceptibility. Mol Cell Biol 17: Hanover, J.A. (2001) Glycan-dependent signaling: O-linked N-acetylglucosamine. Faseb J 15: Hanson, N.D., and Sanders, C.C. (1999) Regulation of inducible AmpC beta-lactamase expression among Enterobacteriaceae. Curr Pharm Des 5: Hantke, K. (2001) Iron and metal regulation in bacteria. Curr Opin Microbiol 4: Hardham, A.R., Jones, D.A., and Takemoto, D. (2007) Cytoskeleton and cell wall function in penetration resistance. Curr Opin Plant Biol 10: Hart, G.W., Housley, M.P., and Slawson, C. (2007) Cycling of O-linked beta-nacetylglucosamine on nucleocytoplasmic proteins. Nature 446: Hartweck, L.M., Genger, R.K., Grey, W.M., and Olszewski, N.E. (2006) SECRET AGENT and SPINDLY have overlapping roles in the development of Arabidopsis thaliana L. Heyn. J Exp Bot 57: Hava, D.L., and Camilli, A. (2002) Large-scale identification of serotype 4 Streptococcus pneumoniae virulence factors. Mol Microbiol 45: He, Y.W., Xu, M., Lin, K., Ng, Y.J., Wen, C.M., Wang, L.H., Liu, Z.D., Zhang, H.B., Dong, Y.H., Dow, J.M., and Zhang, L.H. (2006) Genome scale analysis of diffusible signal factor regulon in Xanthomonas campestris pv. campestris: identification of novel cellcell communication-dependent genes and functions. Mol Microbiol 59: He, Y.W., Ng, A.Y., Xu, M., Lin, K., Wang, L.H., Dong, Y.H., and Zhang, L.H. (2007) Xanthomonas campestris cell-cell communication involves a putative nucleotide receptor protein Clp and a hierarchical signalling network. Mol Microbiol 64: He, Y.W., and Zhang, L.H. (2008) Quorum sensing and virulence regulation in Xanthomonas campestris. FEMS Microbiol Rev 32: He, Y.W., Boon, C., Zhou, L., and Zhang, L.H. (2009) Co-regulation of Xanthomonas campestris virulence by quorum sensing and a novel two-component regulatory system RavS/RavR. Mol Microbiol. 135
225 Bibliographie Hegge, F.T., Hitchen, P.G., Aas, F.E., Kristiansen, H., Lovold, C., Egge-Jacobsen, W., Panico, M., Leong, W.Y., Bull, V., Virji, M., Morris, H.R., Dell, A., and Koomey, M. (2004) Unique modifications with phosphocholine and phosphoethanolamine define alternate antigenic forms of Neisseria gonorrhoeae type IV pili. Proc Natl Acad Sci U S A 101: Heidrich, C., Templin, M.F., Ursinus, A., Merdanovic, M., Berger, J., Schwarz, H., de Pedro, M.A., and Holtje, J.V. (2001) Involvement of N-acetylmuramyl-L-alanine amidases in cell separation and antibiotic-induced autolysis of Escherichia coli. Mol Microbiol 41: Hermentin, P., Witzel, R., Doenges, R., Bauer, R., Haupt, H., Patel, T., Parekh, R.B., and Brazel, D. (1992) The mapping by high-ph anion-exchange chromatography with pulsed amperometric detection and capillary electrophoresis of the carbohydrate moieties of human plasma alpha 1-acid glycoprotein. Anal Biochem 206: Herrington, D.A., Hall, R.H., Losonsky, G., Mekalanos, J.J., Taylor, R.K., and Levine, M.M. (1988) Toxin, toxin-coregulated pili, and the toxr regulon are essential for Vibrio cholerae pathogenesis in humans. J Exp Med 168: Herve, M., Boniface, A., Gobec, S., Blanot, D., and Mengin-Lecreulx, D. (2007) Biochemical characterization and physiological properties of Escherichia coli UDP-Nacetylmuramate:L-alanyl-gamma-D-glutamyl-meso-diaminopimelate ligase. J Bacteriol 189: Hinderlich, S., Berger, M., Schwarzkopf, M., Effertz, K., and Reutter, W. (2000) Molecular cloning and characterization of murine and human N-acetylglucosamine kinase. Eur J Biochem 267: Hirakawa, H., Inazumi, Y., Senda, Y., Kobayashi, A., Hirata, T., Nishino, K., and Yamaguchi, A. (2006) N-acetyl-d-glucosamine induces the expression of multidrug exporter genes, mdtef, via catabolite activation in Escherichia coli. J Bacteriol 188: Ho, H.H., Gilbert, M.T., Nussenzveig, D.R., and Gershengorn, M.C. (1999) Glycosylation is important for binding to human calcitonin receptors. Biochemistry 38: Hogenhout, S.A., and Loria, R. (2008) Virulence mechanisms of Gram-positive plant pathogenic bacteria. Curr Opin Plant Biol 11: Holden, M.T., Ram Chhabra, S., de Nys, R., Stead, P., Bainton, N.J., Hill, P.J., Manefield, M., Kumar, N., Labatte, M., England, D., Rice, S., Givskov, M., Salmond, G.P., Stewart, G.S., Bycroft, B.W., Kjelleberg, S., and Williams, P. (1999) Quorum-sensing cross talk: isolation and chemical characterization of cyclic dipeptides from Pseudomonas aeruginosa and other gram-negative bacteria. Mol Microbiol 33: Holtje, J.V., Mirelman, D., Sharon, N., and Schwarz, U. (1975) Novel type of murein transglycosylase in Escherichia coli. J Bacteriol 124: Holtje, J.V., Kopp, U., Ursinus, A., and Wiedemann, B. (1994) The negative regulator of beta-lactamase induction AmpD is a N-acetyl-anhydromuramyl-L-alanine amidase. FEMS Microbiol Lett 122: Homer, K.A., Foxall, P., Nicholson, J., hilpott-howard, J., and Beighton, D. (1995) Utilization of glycoprotein-derived N-acetylsugars by Streptococcus oralis. J. Dent. Res. 74: 506. Homer, K.A., Kelley, S., Hawkes, J., Beighton, D., and Grootveld, M.C. (1996) Metabolism of glycoprotein-derived sialic acid and N-acetylglucosamine by Streptococcus oralis. Microbiology 142 ( Pt 5): Hotson, A., Chosed, R., Shu, H., Orth, K., and Mudgett, M.B. (2003) Xanthomonas type III effector XopD targets SUMO-conjugated proteins in planta. Mol Microbiol 50:
226 Bibliographie Hotte, B., Rath-Arnold, I., Puhler, A., and Simon, R. (1990) Cloning and analysis of a kilobase DNA region involved in exopolysaccharide production by Xanthomonas campestris pv. campestris. J Bacteriol 172: Howard, M.B., Ekborg, N.A., Taylor, L.E., Weiner, R.M., and Hutcheson, S.W. (2003) Genomic analysis and initial characterization of the chitinolytic system of Microbulbifer degradans strain J Bacteriol 185: Hugouvieux, V., Barber, C.E., and Daniels, M.J. (1998) Entry of Xanthomonas campestris pv. campestris into hydathodes of Arabidopsis thaliana leaves: a system for studying early infection events in bacterial pathogenesis. Mol Plant Microbe Interact 11: Hugouvieux-Cotte-Pattat, N., Condemine, G., Nasser, W., and Reverchon, S. (1996) Regulation of pectinolysis in Erwinia chrysanthemi. Annu Rev Microbiol 50: Hurtado-Guerrero, R., Dorfmueller, H.C., and van Aalten, D.M. (2008) Molecular mechanisms of O-GlcNAcylation. Curr Opin Struct Biol. Ielpi, L., Couso, R.O., and Dankert, M.A. (1993) Sequential assembly and polymerization of the polyprenol-linked pentasaccharide repeating unit of the xanthan polysaccharide in Xanthomonas campestris. J Bacteriol 175: Imperiali, B., and Rickert, K.W. (1995) Conformational implications of asparagine-linked glycosylation. Proc Natl Acad Sci U S A 92: Jacobs, C., Huang, L.J., Bartowsky, E., Normark, S., and Park, J.T. (1994) Bacterial cell wall recycling provides cytosolic muropeptides as effectors for beta-lactamase induction. Embo J 13: Jacobs, C., Joris, B., Jamin, M., Klarsov, K., Van Beeumen, J., Mengin-Lecreulx, D., van Heijenoort, J., Park, J.T., Normark, S., and Frere, J.M. (1995) AmpD, essential for both beta-lactamase regulation and cell wall recycling, is a novel cytosolic N- acetylmuramyl-l-alanine amidase. Mol Microbiol 15: Jaeger, T., Arsic, M., and Mayer, C. (2005) Scission of the lactyl ether bond of N- acetylmuramic acid by Escherichia coli "etherase". J Biol Chem 280: Jamet, E., Boudart, G., Borderies, G., Charmont, S., Lafitte, C., Rossignol, M., Canut, H., and Pont-Lezica, R. (2008) Isolation of plant cell wall proteins. Methods Mol Biol 425: Jansson, P.-E., Keene, L., Lindberg, B.S.o.t.e.-., Car-, c.p.f.x.c., and 275±282, b.r. (1975) Structure of the extracellular polysaccharide from Xanthomonas campestris. Carbohydrates Res 45: Jiang, B.L., He, Y.Q., Cen, W.J., Wei, H.Y., Jiang, G.F., Jiang, W., Hang, X.H., Feng, J.X., Lu, G.T., Tang, D.J., and Tang, J.L. (2008) The type III secretion effector XopXccN of Xanthomonas campestris pv. campestris is required for full virulence. Res Microbiol 159: Jones, J.D., and Dangl, J.L. (2006) The plant immune system. Nature 444: Jones-Mortimer, M.C., and Kornberg, H.L. (1980) Amino-sugar transport systems of Escherichia coli K12. J Gen Microbiol 117: Julenius, K., Molgaard, A., Gupta, R., and Brunak, S. (2005) Prediction, conservation analysis, and structural characterization of mammalian mucin-type O-glycosylation sites. Glycobiology 15: Kaestli, M., Mayo, M., Harrington, G., Watt, F., Hill, J., Gal, D., and Currie, B.J. (2007) Sensitive and specific molecular detection of Burkholderia pseudomallei, the causative agent of melioidosis, in the soil of tropical northern Australia. Appl Environ Microbiol 73: Kahler, C.M., Martin, L.E., Tzeng, Y.L., Miller, Y.K., Sharkey, K., Stephens, D.S., and Davies, J.K. (2001) Polymorphisms in pilin glycosylation Locus of Neisseria meningitidis expressing class II pili. Infect Immun 69:
227 Bibliographie Kaiser, D. (2007) Bacterial swarming: a re-examination of cell-movement patterns. Curr Biol 17: R Kamoun, S., and Kado, C.I. (1990) Phenotypic Switching Affecting Chemotaxis, Xanthan Production, and Virulence in Xanthomonas campestris. Appl Environ Microbiol 56: Kang, Y., Liu, H., Genin, S., Schell, M.A., and Denny, T.P. (2002) Ralstonia solanacearum requires type 4 pili to adhere to multiple surfaces and for natural transformation and virulence. Mol Microbiol 46: Kaper, J.B., Morris, J.G., Jr., and Levine, M.M. (1995) Cholera. Clin Microbiol Rev 8: Katzen, F., Ferreiro, D.U., Oddo, C.G., Ielmini, M.V., Becker, A., Puhler, A., and Ielpi, L. (1998) Xanthomonas campestris pv. campestris gum mutants: effects on xanthan biosynthesis and plant virulence. J Bacteriol 180: Keen, N.T. (1990) Gene-for-gene complementarity in plant-pathogen interactions. Annu Rev Genet 24: Kehr, J., Buhtz, A., and Giavalisco, P. (2005) Analysis of xylem sap proteins from Brassica napus. BMC Plant Biol 5: 11. Kelly, J., Jarrell, H., Millar, L., Tessier, L., Fiori, L.M., Lau, P.C., Allan, B., and Szymanski, C.M. (2006) Biosynthesis of the N-linked glycan in Campylobacter jejuni and addition onto protein through block transfer. J Bacteriol 188: Kennedy, J., and Bradshaw, I. (1984) Production, properties and applications of xanthan. Prog Ind Microbiol 19: Keshavarzi, M., Soylu, S., Brown, I., Bonas, U., Nicole, M., Rossiter, J., and Mansfield, J. (2004) Basal defenses induced in pepper by lipopolysaccharides are suppressed by Xanthomonas campestris pv. vesicatoria. Mol Plant Microbe Interact 17: Keyhani, N.O., and Roseman, S. (1996a) The chitin catabolic cascade in the marine bacterium Vibrio furnissii. Molecular cloning, isolation, and characterization of a periplasmic beta-n-acetylglucosaminidase. J Biol Chem 271: Keyhani, N.O., and Roseman, S. (1996b) The chitin catabolic cascade in the marine bacterium Vibrio furnissii. Molecular cloning, isolation, and characterization of a periplasmic chitodextrinase. J Biol Chem 271: Keyhani, N.O., and Roseman, S. (1999) Physiological aspects of chitin catabolism in marine bacteria. Biochim Biophys Acta 1473: Keyhani, N.O., Li, X.B., and Roseman, S. (2000) Chitin catabolism in the marine bacterium Vibrio furnissii. Identification and molecular cloning of a chitoporin. J Biol Chem 275: Kieliszewski, M.J., and Shpak, E. (2001) Synthetic genes for the elucidation of glycosylation codes for arabinogalactan-proteins and other hydroxyproline-rich glycoproteins. Cell Mol Life Sci 58: Kim, J.G., Taylor, K.W., Hotson, A., Keegan, M., Schmelz, E.A., and Mudgett, M.B. (2008) XopD SUMO protease affects host transcription, promotes pathogen growth, and delays symptom development in xanthomonas-infected tomato leaves. Plant Cell 20: Kimura, Y., and Matsuo, S. (2000) Free N-glycans already occur at an early stage of seed development. J Biochem 127: King, S.J., Hippe, K.R., and Weiser, J.N. (2006) Deglycosylation of human glycoconjugates by the sequential activities of exoglycosidases expressed by Streptococcus pneumoniae. Mol Microbiol 59: Kirn, T.J., Lafferty, M.J., Sandoe, C.M., and Taylor, R.K. (2000) Delineation of pilin domains required for bacterial association into microcolonies and intestinal colonization by Vibrio cholerae. Mol Microbiol 35:
228 Bibliographie Kirn, T.J., Jude, B.A., and Taylor, R.K. (2005) A colonization factor links Vibrio cholerae environmental survival and human infection. Nature 438: Klarzynski, O., and Fritig, B. (2001) Stimulation of plant natural defenses. C R Acad Sci III 324: Kneass, Z.T., and Marchase, R.B. (2005) Protein O-GlcNAc modulates motility-associated signaling intermediates in neutrophils. J Biol Chem 280: Kodama, S., Tsujimoto, M., Tsuruoka, N., Sugo, T., Endo, T., and Kobata, A. (1993) Role of sugar chains in the in-vitro activity of recombinant human interleukin 5. Eur J Biochem 211: Koplin, R., Arnold, W., Hotte, B., Simon, R., Wang, G., and Puhler, A. (1992) Genetics of xanthan production in Xanthomonas campestris: the xana and xanb genes are involved in UDP-glucose and GDP-mannose biosynthesis. J Bacteriol 174: Kornfeld, R., and Kornfeld, S. (1985) Assembly of asparagine-linked oligosaccharides. Annu Rev Biochem 54: Kowarik, M., Young, N.M., Numao, S., Schulz, B.L., Hug, I., Callewaert, N., Mills, D.C., Watson, D.C., Hernandez, M., Kelly, J.F., Wacker, M., and Aebi, M. (2006) Definition of the bacterial N-glycosylation site consensus sequence. Embo J 25: Kreppel, L.K., Blomberg, M.A., and Hart, G.W. (1997) Dynamic glycosylation of nuclear and cytosolic proteins. Cloning and characterization of a unique O-GlcNAc transferase with multiple tetratricopeptide repeats. J Biol Chem 272: Lagrimini, L.M., Burkhart, W., Moyer, M., and Rothstein, S. (1987) Molecular cloning of complementary DNA encoding the lignin-forming peroxidase from tobacco: Molecular analysis and tissue-specific expression. Proc Natl Acad Sci U S A 84: Laine, A.C., Gomord, V., and Faye, L. (1991) Xylose-specific antibodies as markers of subcompartmentation of terminal glycosylation in the Golgi apparatus of sycamore cells. FEBS Lett 295: Lam, E., Kato, N., and Lawton, M. (2001) Programmed cell death, mitochondria and the plant hypersensitive response. Nature 411: Lanctot, P.M., Leclerc, P.C., Clement, M., Auger-Messier, M., Escher, E., Leduc, R., and Guillemette, G. (2005) Importance of N-glycosylation positioning for cell-surface expression, targeting, affinity and quality control of the human AT1 receptor. Biochem J 390: Larsen, J.C., Szymanski, C., and Guerry, P. (2004) N-linked protein glycosylation is required for full competence in Campylobacter jejuni J Bacteriol 186: Lee, J., Klusener, B., Tsiamis, G., Stevens, C., Neyt, C., Tampakaki, A.P., Panopoulos, N.J., Noller, J., Weiler, E.W., Cornelis, G.R., Mansfield, J.W., and Nurnberger, T. (2001) HrpZ(Psph) from the plant pathogen Pseudomonas syringae pv. phaseolicola binds to lipid bilayers and forms an ion-conducting pore in vitro. Proc Natl Acad Sci U S A 98: Leela, J., and Sharma, G. (2000) Studies on xanthan production from Xanthomonas campestris. Bioproc Biosystems Eng 23: Lerouge, P., Cabanes-Macheteau, M., Rayon, C., Fischette-Laine, A.C., Gomord, V., and Faye, L. (1998) N-glycoprotein biosynthesis in plants: recent developments and future trends. Plant Mol Biol 38: Lerouxel, O., Mouille, G., Andeme-Onzighi, C., Bruyant, M.P., Seveno, M., Loutelier- Bourhis, C., Driouich, A., Hofte, H., and Lerouge, P. (2005) Mutants in DEFECTIVE GLYCOSYLATION, an Arabidopsis homolog of an oligosaccharyltransferase complex subunit, show protein underglycosylation and defects in cell differentiation and growth. Plant J 42:
229 Bibliographie Lerouxel, O., Cavalier, D.M., Liepman, A.H., and Keegstra, K. (2006) Biosynthesis of plant cell wall polysaccharides - a complex process. Curr Opin Plant Biol 9: Lewis, M. (2005) The lac repressor. C R Biol 328: Leyns, F., De Cleene, M., J, S., and J, D.L. (1984) The host range of the genus Xanthomonas. Bot Rev 50: Li, X., and Roseman, S. (2004) The chitinolytic cascade in Vibrios is regulated by chitin oligosaccharides and a two-component chitin catabolic sensor/kinase. Proc Natl Acad Sci U S A 101: Lim, S.H., So, B.H., Wang, J.C., Song, E.S., Park, Y.J., Lee, B.M., and Kang, H.W. (2008) Functional analysis of pilq gene in Xanthomonas oryzae pv. oryzae, bacterial blight pathogen of rice. J Microbiol 46: Lindgren, S.W., Stojiljkovic, I., and Heffron, F. (1996) Macrophage killing is an essential virulence mechanism of Salmonella typhimurium. Proc Natl Acad Sci U S A 93: Linton, D., Dorrell, N., Hitchen, P.G., Amber, S., Karlyshev, A.V., Morris, H.R., Dell, A., Valvano, M.A., Aebi, M., and Wren, B.W. (2005) Functional analysis of the Campylobacter jejuni N-linked protein glycosylation pathway. Mol Microbiol 55: Lipp, E.K., Huq, A., and Colwell, R.R. (2002) Effects of global climate on infectious disease: the cholera model. Clin Microbiol Rev 15: Logan, S.M., Kelly, J.F., Thibault, P., Ewing, C.P., and Guerry, P. (2002) Structural heterogeneity of carbohydrate modifications affects serospecificity of Campylobacter flagellins. Mol Microbiol 46: Logan, S.M. (2006) Flagellar glycosylation - a new component of the motility repertoire? Microbiology 152: Loh, J., Carlson, R.W., York, W.S., and Stacey, G. (2002) Bradyoxetin, a unique chemical signal involved in symbiotic gene regulation. Proc Natl Acad Sci U S A 99: Lohmiller, S., Hantke, K., Patzer, S.I., and Braun, V. (2008) TonB-dependent maltose transport by Caulobacter crescentus. Microbiology 154: Love, D.C., Kochan, J., Cathey, R.L., Shin, S.H., and Hanover, J.A. (2003) Mitochondrial and nucleocytoplasmic targeting of O-linked GlcNAc transferase. J Cell Sci 116: Love, D.C., and Hanover, J.A. (2005) The hexosamine signaling pathway: deciphering the "O-GlcNAc code". Sci STKE 2005: re13. Lu, G.T., Ma, Z.F., Hu, J.R., Tang, D.J., He, Y.Q., Feng, J.X., and Tang, J.L. (2007) A novel locus involved in extracellular polysaccharide production and virulence of Xanthomonas campestris pathovar campestris. Microbiology 153: Lubas, W.A., Frank, D.W., Krause, M., and Hanover, J.A. (1997) O-Linked GlcNAc transferase is a conserved nucleocytoplasmic protein containing tetratricopeptide repeats. J Biol Chem 272: Lukowitz, W., Nickle, T.C., Meinke, D.W., Last, R.L., Conklin, P.L., and Somerville, C.R. (2001) Arabidopsis cyt1 mutants are deficient in a mannose-1-phosphate guanylyltransferase and point to a requirement of N-linked glycosylation for cellulose biosynthesis. Proc Natl Acad Sci U S A 98: Lummerzheim, M., de Oliviveira, D., Castresana, C., Miguens, F., Louzada, E., Roby, D., Van Montagu, M., and Timmerman, B. (1993) Identification of compatible and incompatible interactions between Arabidopsis thaliana and Xanthomonas campestris pv. campestris and characterization of the hypersensitive response. Mol Plant Microbe Interact 6: Mackey, D., and McFall, A.J. (2006) MAMPs and MIMPs: proposed classifications for inducers of innate immunity. Mol Microbiol 61:
230 Bibliographie Magalhaes, P.O., Lopes, A.M., Mazzola, P.G., Rangel-Yagui, C., Penna, T.C., and Pessoa, A., Jr. (2007) Methods of endotoxin removal from biological preparations: a review. J Pharm Pharm Sci 10: Malamy, J., Carr, J.P., Klessig, D.F., and Raskin, I. (1990) Salicylic Acid: A Likely Endogenous Signal in the Resistance Response of Tobacco to Viral Infection. Science 250: Maldonado, A.M., Doerner, P., Dixon, R.A., Lamb, C.J., and Cameron, R.K. (2002) A putative lipid transfer protein involved in systemic resistance signalling in Arabidopsis. Nature 419: Maor, R., and Shirasu, K. (2005) The arms race continues: battle strategies between plants and fungal pathogens. Curr Opin Microbiol 8: Marceau, M., Forest, K., Beretti, J.L., Tainer, J., and Nassif, X. (1998) Consequences of the loss of O-linked glycosylation of meningococcal type IV pilin on piliation and pilusmediated adhesion. Mol Microbiol 27: Marenda, M., Brito, B., Callard, D., Genin, S., Barberis, P., Boucher, C., and Arlat, M. (1998) PrhA controls a novel regulatory pathway required for the specific induction of Ralstonia solanacearum hrp genes in the presence of plant cells. Mol Microbiol 27: Martin, G.B., Brommonschenkel, S.H., Chunwongse, J., Frary, A., Ganal, M.W., Spivey, R., Wu, T., Earle, E.D., and Tanksley, S.D. (1993) Map-based cloning of a protein kinase gene conferring disease resistance in tomato. Science 262: Marx, C.J., and Lidstrom, M.E. (2002) Broad-host-range cre-lox system for antibiotic marker recycling in gram-negative bacteria. Biotechniques 33: McAnulla, C., Edwards, A., Sanchez-Contreras, M., Sawers, R.G., and Downie, J.A. (2007) Quorum-sensing-regulated transcriptional initiation of plasmid transfer and replication genes in Rhizobium leguminosarum biovar viciae. Microbiology 153: McClain, D.A., Lubas, W.A., Cooksey, R.C., Hazel, M., Parker, G.J., Love, D.C., and Hanover, J.A. (2002) Altered glycan-dependent signaling induces insulin resistance and hyperleptinemia. Proc Natl Acad Sci U S A 99: Meibom, K.L., Li, X.B., Nielsen, A.T., Wu, C.Y., Roseman, S., and Schoolnik, G.K. (2004) The Vibrio cholerae chitin utilization program. Proc Natl Acad Sci U S A 101: Melchers, L.S., Apotheker-de Groot, M., van der Knaap, J.A., Ponstein, A.S., Sela-Buurlage, M.B., Bol, J.F., Cornelissen, B.J., van den Elzen, P.J., and Linthorst, H.J. (1994) A new class of tobacco chitinases homologous to bacterial exo-chitinases displays antifungal activity. Plant J 5: Melo, N.S., Nimtz, M., Conradt, H.S., Fevereiro, P.S., and Costa, J. (1997) Identification of the human Lewis(a) carbohydrate motif in a secretory peroxidase from a plant cell suspension culture (Vaccinium myrtillus L.). FEBS Lett 415: Melotto, M., Underwood, W., and He, S.Y. (2008) Role of stomata in plant innate immunity and foliar bacterial diseases. Annu Rev Phytopathol 46: Mengin-Lecreulx, D., van Heijenoort, J., and Park, J.T. (1996) Identification of the mpl gene encoding UDP-N-acetylmuramate: L-alanyl-gamma-D-glutamyl-mesodiaminopimelate ligase in Escherichia coli and its role in recycling of cell wall peptidoglycan. J Bacteriol 178: Mescher, M.F., and Strominger, J.L. (1976) Purification and characterization of a prokaryotic glycoprotein from cell-envelope of Halobacterium salinarium. J. Biol. Chem. 251: Metraux, J.P., Streit, L., and Staub, T. (1988) A pathogenesis-related protein in cucumber is a chitinase. Physiol. Mol. Plant Pathol 33:
231 Bibliographie Metz, M., Dahlbeck, D., Morales, C.Q., Al Sady, B., Clark, E.T., and Staskawicz, B.J. (2005) The conserved Xanthomonas campestris pv. vesicatoria effector protein XopX is a virulence factor and suppresses host defense in Nicotiana benthamiana. Plant J 41: Meyer, D. (2005) Etude de la virulence et du régulome de la bactérie phytopathogène Xanthomonas campestris pv. campestris. Thèse. Meyer, D., Lauber, E., Roby, D., Arlat, M., and Kroj, T. (2005) Optimization of pathogenicity assays tu study Arabidopsdis thaliana-xanthomonas campestris pv. campestris pathosystem. Molecular Plant Pathology 6: Meyer, D., Cunnac, S., Gueneron, M., Declercq, C., Van Gijsegem, F., Lauber, E., Boucher, C., and Arlat, M. (2006) PopF1 and PopF2, two proteins secreted by the type III protein secretion system of Ralstonia solanacearum, are translocators belonging to the HrpF/NopX family. J Bacteriol 188: Miller, J.H. (1992) A short course in molecular genetics. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY. Molinari, M. (2007) N-glycan structure dictates extension of protein folding or onset of disposal. Nat Chem Biol 3: Moore, S.E. (1999) Oligosaccharide transport: pumping waste from the ER into lysosomes. Trends Cell Biol 9: Morales, C.Q., Posada, J., Macneale, E., Franklin, D., Rivas, I., Bravo, M., Minsavage, J., Stall, R.E., and Whalen, M.C. (2005) Functional analysis of the early chlorosis factor gene. Mol Plant Microbe Interact 18: Mousavi, A., and Hotta, Y. (2005) Glycine-rich proteins: a class of novel proteins. Appl Biochem Biotechnol 120: Moyrand, F., Fontaine, T., and Janbon, G. (2007) Systematic capsule gene disruption reveals the central role of galactose metabolism on Cryptococcus neoformans virulence. Mol Microbiol 64: Muramatsu, H., Tachikui, H., Ushida, H., Song, X., Qiu, Y., Yamamoto, S., and Muramatsu, T. (2001) Molecular cloning and expression of endo-beta-n-acetylglucosaminidase D, which acts on the core structure of complex type asparagine-linked oligosaccharides. J Biochem 129: Muzzarelli, R.A. (1997) Human enzymatic activities related to the therapeutic administration of chitin derivatives. Cell Mol Life Sci 53: Naim, H.Y., and Lentze, M.J. (1992) Impact of O-glycosylation on the function of human intestinal lactase-phlorizin hydrolase. Characterization of glycoforms varying in enzyme activity and localization of O-glycoside addition. J Biol Chem 267: Nalin, D.R., Daya, V., Reid, A., Levine, M.M., and Cisneros, L. (1979) Adsorption and growth of Vibrio cholerae on chitin. Infect Immun 25: Nambu, T., Minamino, T., Macnab, R.M., and Kutsukake, K. (1999) Peptidoglycanhydrolyzing activity of the FlgJ protein, essential for flagellar rod formation in Salmonella typhimurium. J Bacteriol 181: Neugebauer, H., Herrmann, C., Kammer, W., Schwarz, G., Nordheim, A., and Braun, V. (2005) ExbBD-dependent transport of maltodextrins through the novel MalA protein across the outer membrane of Caulobacter crescentus. J Bacteriol 187: Neuhaus, F.C., and Baddiley, J. (2003) A continuum of anionic charge: structures and functions of D-alanyl-teichoic acids in gram-positive bacteria. Microbiol Mol Biol Rev 67: Newman, M.A., Conrads-Strauch, J., Scofield, G., Daniels, M.J., and Dow, J.M. (1994) Defense-related gene induction in Brassica campestris in response to defined mutants 142
232 Bibliographie of Xanthomonas campestris with altered pathogenicity. Mol Plant Microbe Interact 7: Newman, M.A., Dow, J.M., Molinaro, A., and Parrilli, M. (2007) Priming, induction and modulation of plant defence responses by bacterial lipopolysaccharides. J Endotoxin Res 13: Nikaido, H. (2003) Molecular basis of bacterial outer membrane permeability revisited. Microbiol Mol Biol Rev 67: Noel, L., Thieme, F., Nennstiel, D., and Bonas, U. (2001) cdna-aflp analysis unravels a genome-wide hrpg-regulon in the plant pathogen Xanthomonas campestris pv. vesicatoria. Mol Microbiol 41: Noel, L., Thieme, F., Nennstiel, D., and Bonas, U. (2002) Two novel type III-secreted proteins of Xanthomonas campestris pv. vesicatoria are encoded within the hrp pathogenicity island. J Bacteriol 184: Noel, L., Thieme, F., Gabler, J., Buttner, D., and Bonas, U. (2003) XopC and XopJ, two novel type III effector proteins from Xanthomonas campestris pv. vesicatoria. J Bacteriol 185: Noga, E.J., Smolowitz, R., and Khoo, L.H. (2000) Pathology of shell disease in the blue crab, Callinectes sapidus Rathbun, (Decapoda: Portunidae). J Fish Dis 23: Nurnberger, T., Brunner, F., Kemmerling, B., and Piater, L. (2004) Innate immunity in plants and animals: striking similarities and obvious differences. Immunol Rev 198: O'Donnell, N., Zachara, N.E., Hart, G.W., and Marth, J.D. (2004) Ogt-dependent X- chromosome-linked protein glycosylation is a requisite modification in somatic cell function and embryo viability. Mol Cell Biol 24: Oger, P., and Farrand, S.K. (2002) Two opines control conjugal transfer of an Agrobacterium plasmid by regulating expression of separate copies of the quorum-sensing activator gene trar. J Bacteriol 184: Ojanen-Reuhs, T., Kalkkinen, N., Westerlund-Wikstrom, B., van Doorn, J., Haahtela, K., Nurmiaho-Lassila, E.L., Wengelnik, K., Bonas, U., and Korhonen, T.K. (1997) Characterization of the fima gene encoding bundle-forming fimbriae of the plant pathogen Xanthomonas campestris pv. vesicatoria. J Bacteriol 179: Oke, V., and Long, S.R. (1999) Bacterial genes induced within the nodule during the Rhizobium-legume symbiosis. Mol Microbiol 32: Okushima, Y., Koizumi, N., Kusano, T., and Sano, H. (2000) Secreted proteins of tobacco cultured BY2 cells: identification of a new member of pathogenesis-related proteins. Plant Mol Biol 42: Olivier, N.B., Chen, M.M., Behr, J.R., and Imperiali, B. (2006) In vitro biosynthesis of UDP- N,N'-diacetylbacillosamine by enzymes of the Campylobacter jejuni general protein glycosylation system. Biochemistry 45: Onsando, J. (1992) Black rot of crucifers. Diseases of Vegetables and Oil Seed Crops. 2: Opdenakker, G., Rudd, P.M., Ponting, C.P., and Dwek, R.A. (1993) Concepts and principles of glycobiology. Faseb J 7: Opdenakker, G., Rudd, P.M., Wormald, M., Dwek, R.A., and Van Damme, J. (1995) Cells regulate the activities of cytokines by glycosylation. Faseb J 9: Orikoshi, H., Nakayama, S., Miyamoto, K., Hanato, C., Yasuda, M., Inamori, Y., and Tsujibo, H. (2005) Roles of four chitinases (chia, chib, chic, and chid) in the chitin degradation system of marine bacterium Alteromonas sp. strain O-7. Appl Environ Microbiol 71: Oxley, D., and Bacic, A. (1995) Microheterogeneity of N-glycosylation on a stylar selfincompatibility glycoprotein of Nicotiana alata. Glycobiology 5:
233 Bibliographie Park, J.T. (1995) Why does Escherichia coli recycle its cell wall peptides? Mol Microbiol 17: Park, J.T., Raychaudhuri, D., Li, H., Normark, S., and Mengin-Lecreulx, D. (1998) MppA, a periplasmic binding protein essential for import of the bacterial cell wall peptide L- alanyl-gamma-d-glutamyl-meso-diaminopimelate. J Bacteriol 180: Park, J.T., and Uehara, T. (2008) How bacteria consume their own exoskeletons (turnover and recycling of cell wall peptidoglycan). Microbiol Mol Biol Rev 72: , table of contents. Parker, J.E., Barber, C.E., Fan, M.J., and Daniels, M.J. (1993) Interaction of Xanthomonas campestris with Arabidopsis thaliana: characterization of a gene from X. c. pv. raphani that confers avirulence to most A. thaliana accessions. Mol Plant Microbe Interact 6: Paulick, M.G., and Bertozzi, C.R. (2008) The glycosylphosphatidylinositol anchor: a complex membrane-anchoring structure for proteins. Biochemistry 47: Pearce, S.R., Mimmack, M.L., Gallagher, M.P., Gileadi, U., Hyde, S.C., and Higgins, C.F. (1992) Membrane topology of the integral membrane components, OppB and OppC, of the oligopeptide permease of Salmonella typhimurium. Mol Microbiol 6: Pesci, E.C., Milbank, J.B., Pearson, J.P., McKnight, S., Kende, A.S., Greenberg, E.P., and Iglewski, B.H. (1999) Quinolone signaling in the cell-to-cell communication system of Pseudomonas aeruginosa. Proc Natl Acad Sci U S A 96: Pfalz, M., Vogel, H., Mitchell-Olds, T., and Kroymann, J. (2007) Mapping of QTL for resistance against the crucifer specialist herbivore Pieris brassicae in a new Arabidopsis inbred line population, Da(1)-12xEi-2. PLoS ONE 2: e578. Pieterse, C., Van Wees SCM, Ton J, Van Pelt JA, and LC, V.L. (2002) Signalling in rhizobacteria-induced systemic resistance in Arabidopsis thaliana. Plant Biol 4: Pieterse, C.M., and Van Loon, L.C. (2004) NPR1: the spider in the web of induced resistance signaling pathways. Curr Opin Plant Biol 7: Plumbridge, J., and Kolb, A. (1993) DNA loop formation between Nag repressor molecules bound to its two operator sites is necessary for repression of the nag regulon of Escherichia coli in vivo. Mol Microbiol 10: Plumbridge, J. (1995) Co-ordinated regulation of amino sugar biosynthesis and degradation: the NagC repressor acts as both an activator and a repressor for the transcription of the glmus operon and requires two separated NagC binding sites. Embo J 14: Plumbridge, J., and Pellegrini, O. (2004) Expression of the chitobiose operon of Escherichia coli is regulated by three transcription factors: NagC, ChbR and CAP. Mol Microbiol 52: Plumbridge, J.A. (1989) Sequence of the nagbacd operon in Escherichia coli K12 and pattern of transcription within the nag regulon. Mol Microbiol 3: Plumbridge, J.A. (1991) Repression and induction of the nag regulon of Escherichia coli K- 12: the roles of nagc and naga in maintenance of the uninduced state. Mol Microbiol 5: Plumbridge, J.A., Cochet, O., Souza, J.M., Altamirano, M.M., Calcagno, M.L., and Badet, B. (1993) Coordinated regulation of amino sugar-synthesizing and -degrading enzymes in Escherichia coli K-12. J Bacteriol 175: Poplawsky, A., Walters, D., Rouviere, P., and Chun, W. (2005) A gene for a dioxygenase-like protein determines the production of the DF signal in Xanthomonas campestris pv. campestris. MoL Plant Pathol. 6: Poplawsky, A.R., and Chun, W. (1997) pigb determines a diffusible factor needed for extracellular polysaccharide slime and xanthomonadin production in Xanthomonas campestris pv. campestris. J Bacteriol 179:
234 Bibliographie Poplawsky, A.R., and Chun, W. (1998) Xanthomonas campestris pv. campestris requires a functional pigb for epiphytic survival and host infection. Mol Plant Microbe Interact 11: Poplawsky, A.R., Chun, W., Slater, H., Daniels, M.J., and Dow, J.M. (1998) Synthesis of extracellular polysaccharide, extracellular enzymes, and xanthomonadin in Xanthomonas campestris: evidence for the involvement of two intercellular regulatory signals. Molecular plant Microbe Interaction 11: Postma, P.W., and Lengeler, J.W. (1985) Phosphoenolpyruvate:carbohydrate phosphotransferase system of bacteria. Microbiol Rev 49: Postma, P.W., Lengeler, J.W., and Jacobson, G.R. (1993) Phosphoenolpyruvate:carbohydrate phosphotransferase systems of bacteria. Microbiol Rev 57: Poulicek, M., Gaill, F., and Goffinet, G. (1998) Chitin biodegradation in marine environments. ACS Symp. Ser. 707: Power, P.M., and Jennings, M.P. (2003) The genetics of glycosylation in Gram-negative bacteria. FEMS Microbiol Lett 218: Power, P.M., Roddam, L.F., Rutter, K., Fitzpatrick, S.Z., Srikhanta, Y.N., and Jennings, M.P. (2003) Genetic characterization of pilin glycosylation and phase variation in Neisseria meningitidis. Mol Microbiol 49: Prade, R.A., Zhan, D., Ayoubi, P., and Mort, A.J. (1999) Pectins, pectinases and plantmicrobe interactions. Biotechnol Genet Eng Rev 16: Priem, B., Morvan, H., Hafez, A.M.A., and Morvan, C. (1990) Influence of a plant glycan of the oligomannoside type on the growth of flax plantelets. CR Acad Sc Paris 311: Priem, B., and Gross, K.C. (1992) Mannosyl- and Xylosyl-Containing Glycans Promote Tomato (Lycopersicon esculentum Mill.) Fruit Ripening. Plant Physiol 98: Priem, B., Gitti, R., Bush, C.A., and Gross, K.C. (1993) Structure of ten free N-glycans in ripening tomato fruit. Arabinose is a constituent of a plant N-glycan. Plant Physiol 102: Priem, B., Morvan, H., and Gross, K.C. (1994) Unconjugated N-glycans as a new class of plant oligosaccharins. Biochem Soc Trans 22: Priyadarshini, R., de Pedro, M.A., and Young, K.D. (2007) Role of peptidoglycan amidases in the development and morphology of the division septum in Escherichia coli. J Bacteriol 189: Pruzzo, C., Vezzulli, L., and Colwell, R.R. (2008) Global impact of Vibrio cholerae interactions with chitin. Environ Microbiol 10: Qian, W., Jia, Y., Ren, S.X., He, Y.Q., Feng, J.X., Lu, L.F., Sun, Q., Ying, G., Tang, D.J., Tang, H., Wu, W., Hao, P., Wang, L., Jiang, B.L., Zeng, S., Gu, W.Y., Lu, G., Rong, L., Tian, Y., Yao, Z., Fu, G., Chen, B., Fang, R., Qiang, B., Chen, Z., Zhao, G.P., Tang, J.L., and He, C. (2005) Comparative and functional genomic analyses of the pathogenicity of phytopathogen Xanthomonas campestris pv. campestris. Genome Res 15: Racape, J., Belbahri, L., Engelhardt, S., Lacombe, B., Lee, J., Lochman, J., Marais, A., Nicole, M., Nurnberger, T., Parlange, F., Puverel, S., and Keller, H. (2005) Ca2+dependent lipid binding and membrane integration of PopA, a harpin-like elicitor of the hypersensitive response in tobacco. Mol Microbiol 58: Rahme, L.G., Mindrinos, M.N., and Panopoulos, N.J. (1992) Plant and environmental sensory signals control the expression of hrp genes in Pseudomonas syringae pv. phaseolicola. J Bacteriol 174: Ratledge, C., and Dover, L.G. (2000) Iron metabolism in pathogenic bacteria. Annu Rev Microbiol 54:
235 Bibliographie Ray, S.K., Rajeshwari, R., and Sonti, R.V. (2000) Mutants of Xanthomonas oryzae pv. oryzae deficient in general secretory pathway are virulence deficient and unable to secrete xylanase. Mol Plant Microbe Interact 13: Ray, S.K., Rajeshwari, R., Sharma, Y., and Sonti, R.V. (2002) A high-molecular-weight outer membrane protein of Xanthomonas oryzae pv. oryzae exhibits similarity to nonfimbrial adhesins of animal pathogenic bacteria and is required for optimum virulence. Mol Microbiol 46: Rayon, C., Cabanes-Macheteau, M., Loutelier-Bourhis, C., Salliot-Maire, I., Lemoine, J., Reiter, W.D., Lerouge, P., and Faye, L. (1999) Characterization of N-glycans from Arabidopsis. Application to a fucose-deficient mutant. Plant Physiol 119: Rayon, R., Gomord, V., Faye, L., and Lerouge, P. (1996) N-glycosylation of phytohemagglutinin expressed in bean cotyledons or in transgenic tobacco plants. Plant Physiol Biochem 34: Reguera, G., and Kolter, R. (2005) Virulence and the environment: a novel role for Vibrio cholerae toxin-coregulated pili in biofilm formation on chitin. J Bacteriol 187: Reiko, T.L., Gordan, L., and Yuan, C.L. (2005) Glycoproteomics: protein modifications for versatile functions. Meeting report. EMbo reports 6. Reiter, W.D., Chapple, C.C., and Somerville, C.R. (1993) Altered Growth and Cell Walls in a Fucose-Deficient Mutant of Arabidopsis. Science 261: Rigali, S., Derouaux, A., Giannotta, F., and Dusart, J. (2002) Subdivision of the helix-turnhelix GntR family of bacterial regulators in the FadR, HutC, MocR, and YtrA subfamilies. J Biol Chem 277: Roberts, G., Tarelli, E., Homer, K.A., Philpott-Howard, J., and Beighton, D. (2000) Production of an endo-beta-n-acetylglucosaminidase activity mediates growth of Enterococcus faecalis on a high-mannose-type glycoprotein. J Bacteriol 182: Roberts, G., Homer, K.A., Tarelli, E., Philpott-Howard, J., Devriese, L.A., and Beighton, D. (2001) Distribution of endo-beta-n-acetylglucosaminidase amongst enterococci. J Med Microbiol 50: Roden, J.A., Belt, B., Ross, J.B., Tachibana, T., Vargas, J., and Mudgett, M.B. (2004) A genetic screen to isolate type III effectors translocated into pepper cells during Xanthomonas infection. Proc Natl Acad Sci U S A 101: Rogers, M.J., Ohgi, T., Plumbridge, J., and Soll, D. (1988) Nucleotide sequences of the Escherichia coli nage and nagb genes: the structural genes for the N- acetylglucosamine transport protein of the bacterial phosphoenolpyruvate: sugar phosphotransferase system and for glucosamine-6-phosphate deaminase. Gene 62: Roine, E., Wei, W., Yuan, J., Nurmiaho-Lassila, E.L., Kalkkinen, N., Romantschuk, M., and He, S.Y. (1997) Hrp pilus: an hrp-dependent bacterial surface appendage produced by Pseudomonas syringae pv. tomato DC3000. Proc Natl Acad Sci U S A 94: Roine, E., Raineri, D.M., Romantschuk, M., Wilson, M., and Nunn, D.N. (1998) Characterization of type IV pilus genes in Pseudomonas syringae pv. tomato DC3000. Mol Plant Microbe Interact 11: Rojas, C.M., Ham, J.H., Deng, W.L., Doyle, J.J., and Collmer, A. (2002) HecA, a member of a class of adhesins produced by diverse pathogenic bacteria, contributes to the attachment, aggregation, epidermal cell killing, and virulence phenotypes of Erwinia chrysanthemi EC16 on Nicotiana clevelandii seedlings. Proc Natl Acad Sci U S A 99: Romantschuk, M., and Bamford, D.H. (1986) The causal agent of halo blight in bean, Pseudomonas syringae pv. phaseolicola, attaches to stomata via its pili. Microb Pathog 1:
236 Bibliographie Ronald, P.C., and Staskawicz, B.J. (1988) The avirulence gene avrbs1 from Xanthomonas campestris pv. vesicatoria encodes a 50-kD protein. Mol Plant Microbe Interact 1: Rostand, K.S., and Esko, J.D. (1997) Microbial adherence to and invasion through proteoglycans. Infect Immun 65: 1-8. Roth, J., Taatjes, D.J., Lucocq, J.M., and P.M., C. (1988) Light and electron microscopical detection of sugar residues in tissue secretions by gold labeled lectins and glycoproteins. II. Applications in the study of the topology of Golgi apparatus glycosylation steps and the regional distribution of lectin binding sites in the plasma membrane. Acta Histochem. Suppl.-Band XXXVI, S: Rudd, P.M., Wormald, M.R., Stanfield, R.L., Huang, M., Mattsson, N., Speir, J.A., DiGennaro, J.A., Fetrow, J.S., Dwek, R.A., and Wilson, I.A. (1999) Roles for glycosylation of cell surface receptors involved in cellular immune recognition. J Mol Biol 293: Ruddock, L.W., and Molinari, M. (2006) N-glycan processing in ER quality control. J Cell Sci 119: Ryan, R.P., Fouhy, Y., Lucey, J.F., Crossman, L.C., Spiro, S., He, Y.W., Zhang, L.H., Heeb, S., Camara, M., Williams, P., and Dow, J.M. (2006a) Cell-cell signaling in Xanthomonas campestris involves an HD-GYP domain protein that functions in cyclic di-gmp turnover. Proc Natl Acad Sci U S A 103: Ryan, R.P., Fouhy, Y., Lucey, J.F., and Dow, J.M. (2006b) Cyclic di-gmp signaling in bacteria: recent advances and new puzzles. J Bacteriol 188: Ryan, R.P., Fouhy, Y., Lucey, J.F., Jiang, B.L., He, Y.Q., Feng, J.X., Tang, J.L., and Dow, J.M. (2007) Cyclic di-gmp signalling in the virulence and environmental adaptation of Xanthomonas campestris. Mol Microbiol 63: Saier, M.H., Jr., and Reizer, J. (1994) The bacterial phosphotransferase system: new frontiers 30 years later. Mol Microbiol 13: Saint-Jore-Dupas, C., Nebenfuhr, A., Boulaflous, A., Follet-Gueye, M.L., Plasson, C., Hawes, C., Driouich, A., Faye, L., and Gomord, V. (2006) Plant N-glycan processing enzymes employ different targeting mechanisms for their spatial arrangement along the secretory pathway. Plant Cell 18: Salanoubat, M., Genin, S., Artiguenave, F., Gouzy, J., Mangenot, S., Arlat, M., Billault, A., Brottier, P., Camus, J.C., Cattolico, L., Chandler, M., Choisne, N., Claudel-Renard, C., Cunnac, S., Demange, N., Gaspin, C., Lavie, M., Moisan, A., Robert, C., Saurin, W., Schiex, T., Siguier, P., Thebault, P., Whalen, M., Wincker, P., Levy, M., Weissenbach, J., and Boucher, C.A. (2002) Genome sequence of the plant pathogen Ralstonia solanacearum. Nature 415: Sasmal, D., Guhathakurta, B., Ghosh, A.N., Pal, C.R., and Datta, A. (1992) N-acetyl-Dglucosamine-specific lectin purified from Vibrio cholerae 01. FEMS Microbiol Lett 77: Saxon, E., and Bertozzi, C.R. (2001) Chemical and biological strategies for engineering cell surface glycosylation. Annu Rev Cell Dev Biol 17: Schafer, A., Tauch, A., Jager, W., Kalinowski, J., Thierbach, G., and Puhler, A. (1994) Small mobilizable multi-purpose cloning vectors derived from the Escherichia coli plasmids pk18 and pk19: selection of defined deletions in the chromosome of Corynebacterium glutamicum. Gene 145: Schalk, I.J., Yue, W.W., and Buchanan, S.K. (2004) Recognition of iron-free siderophores by TonB-dependent iron transporters. Mol Microbiol 54: Schauer, K., Gouget, B., Carriere, M., Labigne, A., and de Reuse, H. (2007) Novel nickel transport mechanism across the bacterial outer membrane energized by the TonB/ExbB/ExbD machinery. Mol Microbiol 63:
237 Bibliographie Schauer, K., Rodionov, D.A., and de Reuse, H. (2008) New substrates for TonB-dependent transport: do we only see the 'tip of the iceberg'? Trends Biochem Sci 33: Schirm, M., Soo, E.C., Aubry, A.J., Austin, J., Thibault, P., and Logan, S.M. (2003) Structural, genetic and functional characterization of the flagellin glycosylation process in Helicobacter pylori. Mol Microbiol 48: Schirm, M., Arora, S.K., Verma, A., Vinogradov, E., Thibault, P., Ramphal, R., and Logan, S.M. (2004) Structural and genetic characterization of glycosylation of type a flagellin in Pseudomonas aeruginosa. J Bacteriol 186: Schmidt, D.M., Hubbard, B.K., and Gerlt, J.A. (2001) Evolution of enzymatic activities in the enolase superfamily: functional assignment of unknown proteins in Bacillus subtilis and Escherichia coli as L-Ala-D/L-Glu epimerases. Biochemistry 40: Schoenhofen, I.C., McNally, D.J., Vinogradov, E., Whitfield, D., Young, N.M., Dick, S., Wakarchuk, W.W., Brisson, J.R., and Logan, S.M. (2006) Functional characterization of dehydratase/aminotransferase pairs from Helicobacter and Campylobacter: enzymes distinguishing the pseudaminic acid and bacillosamine biosynthetic pathways. J Biol Chem 281: Schroter, K., Flaschel, E., Puhler, A., and Becker, A. (2001) Xanthomonas campestris pv. campestris secretes the endoglucanases ENGXCA and ENGXCB: construction of an endoglucanase-deficient mutant for industrial xanthan production. Appl Microbiol Biotechnol 55: Schulte, R., and Bonas, U. (1992) Expression of the Xanthomonas campestris pv. vesicatoria hrp gene cluster, which determines pathogenicity and hypersensitivity on pepper and tomato, is plant inducible. J Bacteriol 174: Schultze, M., and Kondorosi, A. (1996) The role of lipochitooligosaccharides in root nodule organogenesis and plant cell growth. Curr Opin Genet Dev 6: Schurr, U., and Schulze, E. (1995) The concentration of xylem sap constituents in root exudate, and in sap from intact, transpiring castor bean plants (Ricinus communis L.). Plant, Cell and Environment 18: Scott, J.E. (1992) Supramolecular organization of extracellular matrix glycosaminoglycans, in vitro and in the tissues. Faseb J 6: Seibert, C.M., and Raushel, F.M. (2005) Structural and catalytic diversity within the amidohydrolase superfamily. Biochemistry 44: Sels, J., Mathys, J., De Coninck, B.M., Cammue, B.P., and De Bolle, M.F. (2008) Plant pathogenesis-related (PR) proteins: A focus on PR peptides. Plant Physiol Biochem. Servant, G., Dudley, D.T., Escher, E., and Guillemette, G. (1996) Analysis of the role of N- glycosylation in cell-surface expression and binding properties of angiotensin II type-2 receptor of rat pheochromocytoma cells. Biochem J 313 ( Pt 1): Shaad, N.W., Gabrielson, R.L., and M.W., M. (1980) Hot Acidified Cupric Acetate Soaks for Eradication of Xanthomonas campestris from Crucifer Seeds. Appl Environ Microbiol 39: Sheldon, P.S., and Bowles, D.J. (1992) The glycoprotein precursor of concanavalin A is converted to an active lectin by deglycosylation. Embo J 11: Shen, Y., and Ronald, P. (2002) Molecular determinants of disease and resistance in interactions of Xanthomonas oryzae pv. oryzae and rice. Microbes Infect 4: Shevchik, V.E., and Hugouvieux-Cotte-Pattat, N. (1997) Identification of a bacterial pectin acetyl esterase in Erwinia chrysanthemi Mol Microbiol 24: Shigemasa, Y., and Minami, S. (1996) Applications of chitin and chitosan for biomaterials. Biotechnol Genet Eng Rev 13: Shultz, T., and Gabrielson, R. (1986) Xanthomonas campestris pv.campestris in Western washington seed fields: occurence and survival. phytopathology:
238 Bibliographie Simpson, A.J., and Reinach, F.C., and Arruda, P., and Abreu, F.A., and Acencio, M., and Alvarenga, R., and Alves, L.M., and Araya, J.E., and Baia, G.S., and Baptista, C.S., and Barros, M.H., and Bonaccorsi, E.D., and Bordin, S., and Bove, J.M., and Briones, M.R., and Bueno, M.R., and Camargo, A.A., and Camargo, L.E., and Carraro, D.M., and Carrer, H., and Colauto, N.B., and Colombo, C., and Costa, F.F., and Costa, M.C., and Costa-Neto, C.M., and Coutinho, L.L., and Cristofani, M., and Dias-Neto, E., and Docena, C., and El-Dorry, H., and Facincani, A.P., and Ferreira, A.J., and Ferreira, V.C., and Ferro, J.A., and Fraga, J.S., and Franca, S.C., and Franco, M.C., and Frohme, M., and Furlan, L.R., and Garnier, M., and Goldman, G.H., and Goldman, M.H., and Gomes, S.L., and Gruber, A., and Ho, P.L., and Hoheisel, J.D., and Junqueira, M.L., and Kemper, E.L., and Kitajima, J.P., and Krieger, J.E., and Kuramae, E.E., and Laigret, F., and Lambais, M.R., and Leite, L.C., and Lemos, E.G., and Lemos, M.V., and Lopes, S.A., and Lopes, C.R., and Machado, J.A., and Machado, M.A., and Madeira, A.M., and Madeira, H.M., and Marino, C.L., and Marques, M.V., and Martins, E.A., and Martins, E.M., and Matsukuma, A.Y., and Menck, C.F., and Miracca, E.C., and Miyaki, C.Y., and Monteriro-Vitorello, C.B., and Moon, D.H., and Nagai, M.A., and Nascimento, A.L., and Netto, L.E., and Nhani, A., Jr., and Nobrega, F.G., and Nunes, L.R., and Oliveira, M.A., and de Oliveira, M.C., and de Oliveira, R.C., and Palmieri, D.A., and Paris, A., and Peixoto, B.R., and Pereira, G.A., and Pereira, H.A., Jr., and Pesquero, J.B., and Quaggio, R.B., and Roberto, P.G., and Rodrigues, V., and de, M.R.A.J., and de Rosa, V.E., Jr., and de Sa, R.G., and Santelli, R.V., and Sawasaki, H.E., and da Silva, A.C., and da Silva, A.M., and da Silva, F.R., and da Silva, W.A., Jr., and da Silveira, J.F., and Silvestri, M.L., and Siqueira, W.J., and de Souza, A.A., and de Souza, A.P., and Terenzi, M.F., and Truffi, D., and Tsai, S.M., and Tsuhako, M.H., and Vallada, H., and Van Sluys, M.A., and Verjovski-Almeida, S., and Vettore, A.L., and Zago, M.A., and Zatz, M., and Meidanis, J., and Setubal, J.C. (2000) The genome sequence of the plant pathogen Xylella fastidiosa. The Xylella fastidiosa Consortium of the Organization for Nucleotide Sequencing and Analysis. Nature 406: Simpson, R., and Johnson, L.J. (1990) Arabidopsis thaliana as a host for Xanthomonas campestris pv. campestris. Mol Plant Microbe Interact 3: Singh, P., Ghosh, S., and Datta, A. (2001) Attenuation of virulence and changes in morphology in Candida albicans by disruption of the N-acetylglucosamine catabolic pathway. Infect Immun 69: Slater, H., Alvarez-Morales, A., Barber, C.E., Daniels, M.J., and Dow, J.M. (2000) A twocomponent system involving an HD-GYP domain protein links cell-cell signalling to pathogenicity gene expression in Xanthomonas campestris. Mol Microbiol 38: Slawson, C., Housley, M.P., and Hart, G.W. (2006) O-GlcNAc cycling: how a single sugar post-translational modification is changing the way we think about signaling networks. J Cell Biochem 97: Sly, W.S., and Fischer, H.D. (1982) The phosphomannosyl recognition system for intracellular and intercellular transport of lysosomal enzymes. J Cell Biochem 18: Smith, H. (2007) Studies on bacterial pathogenicity since 1950 and their future. In Virulence Mechanisms of Bacterial Pathogens (Brogden, K., ed.). ASM Press: 329. Sohanpal, B.K., El-Labany, S., Lahooti, M., Plumbridge, J.A., and Blomfield, I.C. (2004) Integrated regulatory responses of fimb to N-acetylneuraminic (sialic) acid and GlcNAc in Escherichia coli K-12. Proc Natl Acad Sci U S A 101: Sohanpal, B.K., Friar, S., Roobol, J., Plumbridge, J.A., and Blomfield, I.C. (2007) Multiple co-regulatory elements and IHF are necessary for the control of fimb expression in 149
239 Bibliographie response to sialic acid and N-acetylglucosamine in Escherichia coli K-12. Mol Microbiol 63: Somssich, I.E., Schmelzer, E., Bollmann, J., and Hahlbrock, K. (1986) Rapid activation by fungal elicitor of genes encoding "pathogenesis-related" proteins in cultured parsley cells. Proc Natl Acad Sci U S A 83: Souza-Fernandes, A.B., Pelosi, P., and Rocco, P.R. (2006) Bench-to-bedside review: the role of glycosaminoglycans in respiratory disease. Crit Care 10: 237. Spiro, R.G. (2002) Protein glycosylation: nature, distribution, enzymatic formation, and disease implications of glycopeptide bonds. Glycobiology 12: 43R-56R. Staskawicz, B.J., Dahlbeck, D., and Keen, N.T. (1984) Cloned avirulence gene of Pseudomonas syringae pv. glycinea determines race-specific incompatibility on Glycine max (L.) Merr. Proc Natl Acad Sci U S A 81: Stimson, E., Virji, M., Makepeace, K., Dell, A., Morris, H.R., Payne, G., Saunders, J.R., Jennings, M.P., Barker, S., Panico, M., and et al. (1995) Meningococcal pilin: a glycoprotein substituted with digalactosyl 2,4-diacetamido-2,4,6-trideoxyhexose. Mol Microbiol 17: Strasser, R., Altmann, F., Mach, L., Glossl, J., and Steinkellner, H. (2004) Generation of Arabidopsis thaliana plants with complex N-glycans lacking beta1,2-linked xylose and core alpha1,3-linked fucose. FEBS Lett 561: Strasser, R., Stadlmann, J., Svoboda, B., Altmann, F., Glossl, J., and Mach, L. (2005) Molecular basis of N-acetylglucosaminyltransferase I deficiency in Arabidopsis thaliana plants lacking complex N-glycans. Biochem J 387: Strasser, R., Schoberer, J., Jin, C., Glossl, J., Mach, L., and Steinkellner, H. (2006) Molecular cloning and characterization of Arabidopsis thaliana Golgi alpha-mannosidase II, a key enzyme in the formation of complex N-glycans in plants. Plant J 45: Strasser, R., Bondili, J.S., Vavra, U., Schoberer, J., Svoboda, B., Glossl, J., Leonard, R., Stadlmann, J., Altmann, F., Steinkellner, H., and Mach, L. (2007) A unique beta1,3- galactosyltransferase is indispensable for the biosynthesis of N-glycans containing Lewis a structures in Arabidopsis thaliana. Plant Cell 19: Strobel, G.A. (1977) Bacterial phytotoxins. Annu Rev Microbiol 31: Strobel, G.A. (1982) Phytotoxins. Annu Rev Biochem 51: Sturm, A., Van Kuik, J.A., Vliegenthart, J.F., and Chrispeels, M.J. (1987) Structure, position, and biosynthesis of the high mannose and the complex oligosaccharide side chains of the bean storage protein phaseolin. J Biol Chem 262: Sturm, A. (1991) Heterogeneity of the complex N-linked oligosaccharides at specific glycosylation sites of two secreted carrot glycoproteins. Eur J Biochem 199: Sudbery, P., Gow, N., and Berman, J. (2004) The distinct morphogenic states of Candida albicans. Trends Microbiol 12: Suginta, W. (2007) Identification of chitin binding proteins and characterization of two chitinase isoforms from Vibrio alginolyticus 283. Enzyme Microb Technol 41: Sumegi, M., Hunyadi-Gulyas, E., Medzihradszky, K.F., and Udvardy, A. (2003) 26S proteasome subunits are O-linked N-acetylglucosamine-modified in Drosophila melanogaster. Biochem Biophys Res Commun 312: Sun, H., Zusman, D.R., and Shi, W. (2000) Type IV pilus of Myxococcus xanthus is a motility apparatus controlled by the frz chemosensory system. Curr Biol 10: Sun, W., Dunning, F.M., Pfund, C., Weingarten, R., and Bent, A.F. (2006) Within-species flagellin polymorphism in Xanthomonas campestris pv campestris and its impact on elicitation of Arabidopsis FLAGELLIN SENSING2-dependent defenses. Plant Cell 18:
240 Bibliographie Suzuki, T., Park, H., and Lennarz, W.J. (2002a) Cytoplasmic peptide:n-glycanase (PNGase) in eukaryotic cells: occurrence, primary structure, and potential functions. Faseb J 16: Suzuki, T., Yano, K., Sugimoto, S., Kitajima, K., Lennarz, W.J., Inoue, S., Inoue, Y., and Emori, Y. (2002b) Endo-beta-N-acetylglucosaminidase, an enzyme involved in processing of free oligosaccharides in the cytosol. Proc Natl Acad Sci U S A 99: Suzuki, T. (2007) Cytoplasmic peptide:n-glycanase and catabolic pathway for free N-glycans in the cytosol. Semin Cell Dev Biol 18: Svitil, A.L., Chadhain, S., Moore, J.A., and Kirchman, D.L. (1997) Chitin Degradation Proteins Produced by the Marine Bacterium Vibrio harveyi Growing on Different Forms of Chitin. Appl Environ Microbiol 63: Swords, K.M., Dahlbeck, D., Kearney, B., Roy, M., and Staskawicz, B.J. (1996) Spontaneous and induced mutations in a single open reading frame alter both virulence and avirulence in Xanthomonas campestris pv. vesicatoria avrbs2. J Bacteriol 178: Szymanski, C.M., Yao, R., Ewing, C.P., Trust, T.J., and Guerry, P. (1999) Evidence for a system of general protein glycosylation in Campylobacter jejuni. Mol Microbiol 32: Szymanski, C.M., Logan, S.M., Linton, D., and Wren, B.W. (2003) Campylobacter--a tale of two protein glycosylation systems. Trends Microbiol 11: Szymanski, C.M., and Wren, B.W. (2005) Protein glycosylation in bacterial mucosal pathogens. Nat Rev Microbiol 3: Tacket, C.O., Taylor, R.K., Losonsky, G., Lim, Y., Nataro, J.P., Kaper, J.B., and Levine, M.M. (1998) Investigation of the roles of toxin-coregulated pili and mannose-sensitive hemagglutinin pili in the pathogenesis of Vibrio cholerae O139 infection. Infect Immun 66: Takahashi, N., Hitotsuya, H., Hanzawa, H., Arata, Y., and Kurihara, Y. (1990) Structural study of asparagine-linked oligosaccharide moiety of taste-modifying protein, miraculin. J Biol Chem 265: Takeuchi, K., Taguchi, F., Inagaki, Y., Toyoda, K., Shiraishi, T., and Ichinose, Y. (2003) Flagellin glycosylation island in Pseudomonas syringae pv. glycinea and its role in host specificity. J Bacteriol 185: Tamber, S., Ochs, M.M., and Hancock, R.E. (2006) Role of the novel OprD family of porins in nutrient uptake in Pseudomonas aeruginosa. J Bacteriol 188: Tang, J.L., Liu, Y.N., Barber, C.E., Dow, J.M., Wootton, J.C., and Daniels, M.J. (1991) Genetic and molecular analysis of a cluster of rpf genes involved in positive regulation of synthesis of extracellular enzymes and polysaccharide in Xanthomonas campestris pathovar campestris. Mol Gen Genet 226: Tang, X., Xiao, Y., and Zhou, J.M. (2006) Regulation of the type III secretion system in phytopathogenic bacteria. Mol Plant Microbe Interact 19: Tarsi, R., and Pruzzo, C. (1999) Role of surface proteins in Vibrio cholerae attachment to chitin. Appl Environ Microbiol 65: Techkarnjanaruk, S., and Goodman, A. (1999) Multiple genes involved in chitin degradation from the marine bacterium Pseudoaltermonas sp. strain S91. Microbiology 145: Templin, M.F., Ursinus, A., and Holtje, J.V. (1999) A defect in cell wall recycling triggers autolysis during the stationary growth phase of Escherichia coli. Embo J 18: Terras, F.R., Eggermont, K., Kovaleva, V., Raikhel, N.V., Osborn, R.W., Kester, A., Rees, S.B., Torrekens, S., Van Leuven, F., Vanderleyden, J., and et al. (1995) Small 151
241 Bibliographie cysteine-rich antifungal proteins from radish: their role in host defense. Plant Cell 7: Thelin, K.H., and Taylor, R.K. (1996) Toxin-coregulated pilus, but not mannose-sensitive hemagglutinin, is required for colonization by Vibrio cholerae O1 El Tor biotype and O139 strains. Infect Immun 64: Thibault, P., Logan, S.M., Kelly, J.F., Brisson, J.R., Ewing, C.P., Trust, T.J., and Guerry, P. (2001) Identification of the carbohydrate moieties and glycosylation motifs in Campylobacter jejuni flagellin. J Biol Chem 276: Thieme, F., Szczesny, R., Urban, A., Kirchner, O., Hause, G., and Bonas, U. (2007) New type III effectors from Xanthomonas campestris pv. vesicatoria trigger plant reactions dependent on a conserved N-myristoylation motif. Mol Plant Microbe Interact 20: Thomson, N.R., Nasser, W., McGowan, S., Sebaihia, M., and Salmond, G.P. (1999) Erwinia carotovora has two KdgR-like proteins belonging to the IciR family of transcriptional regulators: identification and characterization of the RexZ activator and the KdgR repressor of pathogenesis. Microbiology 145 ( Pt 7): Titgemeyer, F., Reizer, J., Reizer, A., and Saier, M.H., Jr. (1994) Evolutionary relationships between sugar kinases and transcriptional repressors in bacteria. Microbiology 140 ( Pt 9): Torres, M.A., Jones, J.D., and Dangl, J.L. (2006) Reactive oxygen species signaling in response to pathogens. Plant Physiol 141: Tsuge, S., Nakayama, T., Terashima, S., Ochiai, H., Furutani, A., Oku, T., Tsuno, K., Kubo, Y., and Kaku, H. (2006) Gene involved in transcriptional activation of the hrp regulatory gene hrpg in Xanthomonas oryzae pv. oryzae. J Bacteriol 188: Uehara, T., and Park, J.T. (2002) Role of the murein precursor UDP-N-acetylmuramyl-L-Alagamma-D-Glu-meso-diaminopimelic acid-d-ala-d-ala in repression of betalactamase induction in cell division mutants. J Bacteriol 184: Uehara, T., and Park, J.T. (2003) Identification of MpaA, an amidase in Escherichia coli that hydrolyzes the gamma-d-glutamyl-meso-diaminopimelate bond in murein peptides. J Bacteriol 185: Uehara, T., and Park, J.T. (2004) The N-acetyl-D-glucosamine kinase of Escherichia coli and its role in murein recycling. J Bacteriol 186: Uehara, T., Suefuji, K., Valbuena, N., Meehan, B., Donegan, M., and Park, J.T. (2005) Recycling of the anhydro-n-acetylmuramic acid derived from cell wall murein involves a two-step conversion to N-acetylglucosamine-phosphate. J Bacteriol 187: Uehara, T., Suefuji, K., Jaeger, T., Mayer, C., and Park, J.T. (2006) MurQ Etherase is required by Escherichia coli in order to metabolize anhydro-n-acetylmuramic acid obtained either from the environment or from its own cell wall. J Bacteriol 188: Uehara, T., and Park, J.T. (2007) An anhydro-n-acetylmuramyl-l-alanine amidase with broad specificity tethered to the outer membrane of Escherichia coli. J Bacteriol 189: Umemoto, J., Bhavanandan, V.P., and Davidson, E.A. (1977) Purification and properties of an endo-alpha-n-acetyl-d-galactosaminidase from Diplococcus pneumoniae. J Biol Chem 252: Ursinus, A., Steinhaus, H., and Holtje, J.V. (1992) Purification of a nocardicin A-sensitive LD-carboxypeptidase from Escherichia coli by affinity chromatography. J Bacteriol 174: Van den Steen, P., Rudd, P.M., Dwek, R.A., and Opdenakker, G. (1998) Concepts and principles of O-linked glycosylation. Crit Rev Biochem Mol Biol 33:
242 Bibliographie Van der Biezen, E.A., and Jones, J.D. (1998) Plant disease-resistance proteins and the genefor-gene concept. Trends Biochem Sci 23: van der Hoorn, R.A., Wulff, B.B., Rivas, S., Durrant, M.C., van der Ploeg, A., de Wit, P.J., and Jones, J.D. (2005) Structure-function analysis of cf-9, a receptor-like protein with extracytoplasmic leucine-rich repeats. Plant Cell 17: Van der Linden, E.C.M., De Graaf, T.W., Anbergen, M.G., Dekker, R.M., Van Ommen, E.C.R., Van de Eijnden, D.H., and Van Dijk, W. (1994) Preparative affinity electrophoresis of different glycoforms of serum glycoproteins: application for the study of inflammation-induced expression of sialyl-lewisx groups on [alpha]1-acid glycoprotein (orosmucoid). Glycosyl. Dis. 1: Van Dijk, W. (1995) [alpha]1-acid glycoprotein. In Alavi,A. and Axford,J.S. (eds.), Glycoimmunology-Advances in Experimental Medicine and Biology,. Plenum Press, New York, pp. Vol. 376: van Doorn, J., Boonekamp, P.M., and Oudega, B. (1994) Partial characterization of fimbriae of Xanthomonas campestris pv. hyacinthi. Mol Plant Microbe Interact 7: Van Gijsegem, F., Vasse, J., Camus, J.C., Marenda, M., and Boucher, C. (2000) Ralstonia solanacearum produces hrp-dependent pili that are required for PopA secretion but not for attachment of bacteria to plant cells. Mol Microbiol 36: van Ree, R., and Aalberse, R.C. (1993) Pollen-vegetable food crossreactivity: serological and clinical relevance of crossreactive IgE. Clin Immunoassay J 16: Vanderslice, R.W., Doherty, D.H., Capage, M.A., Betlach, M.R., Hassler, R.A., Henderson, N.M., Ryan-Graniero, J., and Tecklenburg, M. (1990) Genetic engineering of polysaccharide structure in Xanthomonas campestris. In Biomedical and Biotechnological Advances in Industrial Polysaccharides: Van Loon, L.C. (1982) Regulation of changes in proteins and enzymes associated with active defense against virus, in: R.K.S. Wood (Ed.), infection, Active Defense Mechanisms in Plants. Plenum Press, New York: Vargas, C., Tegos, G., Vartholomatos, G., Drainas, C., Ventosa, A., and Nieto, J.J. (1999) Genetic organization of the mobilization region of the plasmid phe1 from Halomonas elongata. Syst Appl Microbiol 22: Varki, A. (1992) Diversity in the sialic acids. Glycobiology 2: Varki, A. (1993) Biological roles of oligosaccharides: all of the theories are correct. Glycobiology 3: Vauterin, L., Hoste, B., Kersters, K., and Swings, J. (1995) Reclassification of Xanthomonas. Int J Syst Bacteriol 45: Vera, P., and Conejero, V. (1988) Pathogenesis-Related Proteins of Tomato : P-69 as an Alkaline Endoproteinase. Plant Physiol 87: Verberne, M.C., Hoekstra, J., Bol, J.F., and Linthorst, H.J. (2003) Signaling of systemic acquired resistance in tobacco depends on ethylene perception. Plant J 35: Verma, D.P. (2001) Cytokinesis and Building of the Cell Plate in Plants. Annu Rev Plant Physiol Plant Mol Biol 52: Vijayakumar, S., Merkx-Jacques, A., Ratnayake, D.B., Gryski, I., Obhi, R.K., Houle, S., Dozois, C.M., and Creuzenet, C. (2006) Cj1121c, a novel UDP-4-keto-6-deoxy- GlcNAc C-4 aminotransferase essential for protein glycosylation and virulence in Campylobacter jejuni. J Biol Chem 281: Voelker, T.A., Herman, E.M., and Chrispeels, M.J. (1989) In vitro mutated phytohemagglutinin genes expressed in tobacco seeds: role of glycans in protein targeting and stability. Plant Cell 1: Vogan, C.L., Powell, A., and Rowley, A.F. (2008) Shell disease in crustaceans - just chitin recycling gone wrong? Environ Microbiol 10:
243 Bibliographie Vogler, A.P., and Lengeler, J.W. (1989) Analysis of the nag regulon from Escherichia coli K12 and Klebsiella pneumoniae and of its regulation. Mol Gen Genet 219: Voisin, S., Kus, J.V., Houliston, S., St-Michael, F., Watson, D., Cvitkovitch, D.G., Kelly, J., Brisson, J.R., and Burrows, L.L. (2007) Glycosylation of Pseudomonas aeruginosa strain Pa5196 type IV pilins with mycobacterium-like alpha-1,5-linked d-araf oligosaccharides. J Bacteriol 189: Vollmer, W., Blanot, D., and de Pedro, M.A. (2008a) Peptidoglycan structure and architecture. FEMS Microbiol Rev 32: Von Bodman, S.B., Bauer, W.D., and Coplin, D.L. (2003) Quorum sensing in plantpathogenic bacteria. Annu Rev Phytopathol 41: von Schaewen, A., Sturm, A., O'Neill, J., and Chrispeels, M.J. (1993) Isolation of a mutant Arabidopsis plant that lacks N-acetyl glucosaminyl transferase I and is unable to synthesize Golgi-modified complex N-linked glycans. Plant Physiol 102: Vorholter, F.J., Schneiker, S., Goesmann, A., Krause, L., Bekel, T., Kaiser, O., Linke, B., Patschkowski, T., Ruckert, C., Schmid, J., Sidhu, V.K., Sieber, V., Tauch, A., Watt, S.A., Weisshaar, B., Becker, A., Niehaus, K., and Puhler, A. (2008) The genome of Xanthomonas campestris pv. campestris B100 and its use for the reconstruction of metabolic pathways involved in xanthan biosynthesis. J Biotechnol 134: Vosseller, K., Wells, L., Lane, M.D., and Hart, G.W. (2002) Elevated nucleocytoplasmic glycosylation by O-GlcNAc results in insulin resistance associated with defects in Akt activation in 3T3-L1 adipocytes. Proc Natl Acad Sci U S A 99: Wacker, M., Linton, D., Hitchen, P.G., Nita-Lazar, M., Haslam, S.M., North, S.J., Panico, M., Morris, H.R., Dell, A., Wren, B.W., and Aebi, M. (2002) N-linked glycosylation in Campylobacter jejuni and its functional transfer into E. coli. Science 298: Wacker, M., Feldman, M.F., Callewaert, N., Kowarik, M., Clarke, B.R., Pohl, N.L., Hernandez, M., Vines, E.D., Valvano, M.A., Whitfield, C., and Aebi, M. (2006) Substrate specificity of bacterial oligosaccharyltransferase suggests a common transfer mechanism for the bacterial and eukaryotic systems. Proc Natl Acad Sci U S A 103: Wagegg, W., and Braun, V. (1981) Ferric citrate transport in Escherichia coli requires outer membrane receptor protein FecA. J Bacteriol 145: Wandersman, C., and Delepelaire, P. (2004) Bacterial iron sources: from siderophores to hemophores. Annu Rev Microbiol 58: Wang, L., Rong, W., and He, C. (2008) Two Xanthomonas extracellular polygalacturonases, PghAxc and PghBxc, are regulated by type III secretion regulators HrpX and HrpG and are required for virulence. Mol Plant Microbe Interact 21: Wang, L.H., He, Y., Gao, Y., Wu, J.E., Dong, Y.H., He, C., Wang, S.X., Weng, L.X., Xu, J.L., Tay, L., Fang, R.X., and Zhang, L.H. (2004) A bacterial cell-cell communication signal with cross-kingdom structural analogues. Mol Microbiol 51: Wassenaar, T.M., and Gaastra, W. (2001) Bacterial virulence: can we draw the line? FEMS Microbiol Lett 201: 1-7. Weber, E., and Koebnik, R. (2005) Domain structure of HrpE, the Hrp pilus subunit of Xanthomonas campestris pv. vesicatoria. J Bacteriol 187: Weber, E., and Koebnik, R. (2006) Positive selection of the Hrp pilin HrpE of the plant pathogen Xanthomonas. J Bacteriol 188: Weerapana, E., and Imperiali, B. (2006) Asparagine-linked protein glycosylation: from eukaryotic to prokaryotic systems. Glycobiology 16: 91R-101R. Wei, Y., Zhang, Z., Andersen, C.H., Schmelzer, E., Gregersen, P.L., Collinge, D.B., Smedegaard-Petersen, V., and Thordal-Christensen, H. (1998) An epidermis/papillaspecific oxalate oxidase-like protein in the defence response of barley attacked by the powdery mildew fungus. Plant Mol Biol 36:
244 Bibliographie Wei, Z.M., Sneath, B.J., and Beer, S.V. (1992) Expression of Erwinia amylovora hrp genes in response to environmental stimuli. J Bacteriol 174: Wells, L., Vosseller, K., and Hart, G.W. (2001) Glycosylation of nucleocytoplasmic proteins: signal transduction and O-GlcNAc. Science 291: Wells, L., and Hart, G.W. (2003) O-GlcNAc turns twenty: functional implications for posttranslational modification of nuclear and cytosolic proteins with a sugar. FEBS Lett 546: Whalen, M.C., Wang, J.F., Carland, F.M., Heiskell, M.E., Dahlbeck, D., Minsavage, G.V., Jones, J.B., Scott, J.W., Stall, R.E., and Staskawicz, B.J. (1993) Avirulence gene avrrxv from Xanthomonas campestris pv. vesicatoria specifies resistance on tomato line Hawaii Mol Plant Microbe Interact 6: Whitchurch, C.B., Leech, A.J., Young, M.D., Kennedy, D., Sargent, J.L., Bertrand, J.J., Semmler, A.B., Mellick, A.S., Martin, P.R., Alm, R.A., Hobbs, M., Beatson, S.A., Huang, B., Nguyen, L., Commolli, J.C., Engel, J.N., Darzins, A., and Mattick, J.S. (2004) Characterization of a complex chemosensory signal transduction system which controls twitching motility in Pseudomonas aeruginosa. Mol Microbiol 52: White, R.J., and Pasternak, C.A. (1967) The purification and properties of N- acetylglucosamine 6-phosphate deacetylase from Escherichia coli. Biochem J 105: White, R.J. (1968) Control of amino sugar metabolism in Escherichia coli and isolation of mutants unable to degrade amino sugars. Biochem J 106: Whiteway, M., and Oberholzer, U. (2004) Candida morphogenesis and host-pathogen interactions. Curr Opin Microbiol 7: Wiggerich, H.G., Klauke, B., Koplin, R., Priefer, U.B., and Puhler, A. (1997) Unusual structure of the tonb-exb DNA region of Xanthomonas campestris pv. campestris: tonb, exbb, and exbd1 are essential for ferric iron uptake, but exbd2 is not. J Bacteriol 179: Wiggerich, H.G., and Puhler, A. (2000) The exbd2 gene as well as the iron-uptake genes tonb, exbb and exbd1 of Xanthomonas campestris pv. campestris are essential for the induction of a hypersensitive response on pepper (Capsicum annuum). Microbiology 146 ( Pt 5): Williams, P. (1980) Black rot: a continuing threat to world crucifers. Plant Dis 64: Williams, P. (2007) Quorum sensing, communication and cross-kingdom signalling in the bacterial world. Microbiology 153: Wilson, I.B. (2002) Glycosylation of proteins in plants and invertebrates. Curr Opin Struct Biol 12: Wisniewski-Dye, F., and Vial, L. (2008) Phase and antigenic variation mediated by genome modifications. Antonie Van Leeuwenhoek 94: Wolgemuth, C., Hoiczyk, E., Kaiser, D., and Oster, G. (2002) How myxobacteria glide. Curr Biol 12: Wopereis, S., Lefeber, D.J., Morava, E., and Wevers, R.A. (2006) Mechanisms in protein O- glycan biosynthesis and clinical and molecular aspects of protein O-glycan biosynthesis defects: a review. Clin Chem 52: Wormald, M.R., and Dwek, R.A. (1999) Glycoproteins: glycan presentation and protein-fold stability. Structure 7: R Wu, H., de Graaf, B., Mariani, C., and Cheung, A.Y. (2001) Hydroxyproline-rich glycoproteins in plant reproductive tissues: structure, functions and regulation. Cell Mol Life Sci 58: Xiao, X., Wang, F., Saito, A., Majka, J., Schlosser, A., and Schrempf, H. (2002) The novel Streptomyces olivaceoviridis ABC transporter Ngc mediates uptake of N- acetylglucosamine and N,N'-diacetylchitobiose. Mol Genet Genomics 267:
245 Bibliographie Xiao, Y., Lu, Y., Heu, S., and Hutcheson, S.W. (1992) Organization and environmental regulation of the Pseudomonas syringae pv. syringae 61 hrp cluster. J Bacteriol 174: Xu, R.Q., Blanvillain, S., Feng, J.X., Jiang, B.L., Li, X.Z., Wei, H.Y., Kroj, T., Lauber, E., Roby, D., Chen, B., He, Y.Q., Lu, G.T., Tang, D.J., Vasse, J., Arlat, M., and Tang, J.L. (2008) AvrAC(Xcc8004), a type III effector with a leucine-rich repeat domain from Xanthomonas campestris pathovar campestris confers avirulence in vascular tissues of Arabidopsis thaliana ecotype Col-0. J Bacteriol 190: Yan, Y., Scott, D.J., Wilkinson, T.N., Ji, J., Tregear, G.W., and Bathgate, R.A. (2008) Identification of the N-linked glycosylation sites of the human relaxin receptor and effect of glycosylation on receptor function. Biochemistry 47: Yang, C., Rodionov, D.A., Li, X., Laikova, O.N., Gelfand, M.S., Zagnitko, O.P., Romine, M.F., Obraztsova, A.Y., Nealson, K.H., and Osterman, A.L. (2006) Comparative genomics and experimental characterization of N-acetylglucosamine utilization pathway of Shewanella oneidensis. J Biol Chem 281: Yao, J., and Allen, C. (2007) The plant pathogen Ralstonia solanacearum needs aerotaxis for normal biofilm formation and interactions with its tomato host. J Bacteriol 189: Yesilkaya, H., Manco, S., Kadioglu, A., Terra, V.S., and Andrew, P.W. (2008) The ability to utilize mucin affects the regulation of virulence gene expression in Streptococcus pneumoniae. FEMS Microbiol Lett 278: Yoshima, H., Matsumoto, A., Mizuochi, T., Kawasaki, T., and Kobata, A. (1981) Comparative study of the carbohydrate moieties of rat and human plasma alpha 1-acid glycoproteins. J Biol Chem 256: Young, N.M., Brisson, J.R., Kelly, J., Watson, D.C., Tessier, L., Lanthier, P.H., Jarrell, H.C., Cadotte, N., St Michael, F., Aberg, E., and Szymanski, C.M. (2002) Structure of the N-linked glycan present on multiple glycoproteins in the Gram-negative bacterium, Campylobacter jejuni. J Biol Chem 277: Yun, M.H., Torres, P.S., El Oirdi, M., Rigano, L.A., Gonzalez-Lamothe, R., Marano, M.R., Castagnaro, A.P., Dankert, M.A., Bouarab, K., and Vojnov, A.A. (2006) Xanthan induces plant susceptibility by suppressing callose deposition. Plant Physiol 141: Zachara, N.E., and Hart, G.W. (2004a) O-GlcNAc modification: a nutritional sensor that modulates proteasome function. Trends Cell Biol 14: Zachara, N.E., and Hart, G.W. (2004b) O-GlcNAc a sensor of cellular state: the role of nucleocytoplasmic glycosylation in modulating cellular function in response to nutrition and stress. Biochim Biophys Acta 1673: Zachara, N.E., and Hart, G.W. (2006) Cell signaling, the essential role of O-GlcNAc! Biochim Biophys Acta 1761: Zahner, D., and Hakenbeck, R. (2000) The Streptococcus pneumoniae beta-galactosidase is a surface protein. J Bacteriol 182: Zampini, M., Pruzzo, C., Bondre, V.P., Tarsi, R., Cosmo, M., Bacciaglia, A., Chhabra, A., Srivastava, R., and Srivastava, B.S. (2005) Vibrio cholerae persistence in aquatic environments and colonization of intestinal cells: involvement of a common adhesion mechanism. FEMS Microbiol Lett 244: Zhang, G.F., and Staehelin, L.A. (1992) Functional Compartmentation of the Golgi Apparatus of Plant Cells : Immunocytochemical Analysis of High-Pressure Frozen- and Freeze- Substituted Sycamore Maple Suspension Culture Cells. Plant Physiol 99: Zhang, L., and Birch, R.G. (1997) The gene for albicidin detoxification from Pantoea dispersa encodes an esterase and attenuates pathogenicity of Xanthomonas albilineans to sugarcane. Proc Natl Acad Sci U S A 94:
246 Bibliographie Zhang, L., Xu, J., and Birch, R.G. (1999) Engineered detoxification confers resistance against a pathogenic bacterium. Nat Biotechnol 17: Zhang, Z., Collinge, D.B., and Thordal-Christensen, H. (1995) Germin-like oxalate oxidase, a H2O2-producing enzyme, accumulates in barley attacked by the powdery mildew fungus. Plant J: Zhao, Y., Blumer, S.E., and Sundin, G.W. (2005) Identification of Erwinia amylovora genes induced during infection of immature pear tissue. J Bacteriol 187: Zhao, Y.Y., Takahashi, M., Gu, J.G., Miyoshi, E., Matsumoto, A., Kitazume, S., and Taniguchi, N. (2008) Functional roles of N-glycans in cell signaling and cell adhesion in cancer. Cancer Sci 99: Zhou, J.M., and Chai, J. (2008) Plant pathogenic bacterial type III effectors subdue host responses. Curr Opin Microbiol 11: Zipfel, C., Robatzek, S., Navarro, L., Oakeley, E.J., Jones, J.D., Felix, G., and Boller, T. (2004) Bacterial disease resistance in Arabidopsis through flagellin perception. Nature 428: Zipfel, C., and Felix, G. (2005) Plants and animals: a different taste for microbes? Curr Opin Plant Biol 8: Zipfel, C., Kunze, G., Chinchilla, D., Caniard, A., Jones, J.D., Boller, T., and Felix, G. (2006) Perception of the bacterial PAMP EF-Tu by the receptor EFR restricts Agrobacteriummediated transformation. Cell 125: Zipfel, C. (2008) Pattern-recognition receptors in plant innate immunity. Curr Opin Immunol 20:
247 AUTHOR : Alice BOULANGER TITLE : Analysis of a new CUT system involved in acquisition and utilization of N- acetylglucosamine by Xanthomonas campestris pathovar campestris. PhD SUPERVISOR : Matthieu ARLAT PhD CO-SUPERVISOR : Emmanuelle LAUBER Abstract N-acetylglucosamine (GlcNAc) is an amino sugar that carries out important roles in a broad range of cells from bacteria to plants and animals. Most marine bacteria and insect pathogens have developed sophisticated mechanisms for the catabolism of the second most abundant biopolymer in nature, chitin, which is a GlcNAc homopolymer. However, whether nonchitinolytic bacteria find GlcNAc in their environment and what is the natural source of this molecule remain obscure. The data presented here suggest that the plant pathogenic bacterium Xanthomonas campestris pv. campestris (Xcc), the causal agent of black rot disease of Brassicaceae, encounters and exploits GlcNAc of plant origin during infection. Characterization of the Xcc GlcNAc utilization pathway and its complex regulatory network led to the identification of specific traits as compared to other bacteria and most notably the source of GlcNAc, i.e. glycans from plant glycosylated proteins. An outer membrane transporter and glycoside hydrolases belonging to the Xcc GlcNAc utilization pathway were shown to play a direct role in the generation of GlcNAc in planta. KEYWORDS : Xanthomonas campestris pv. campestris, N-acetylglucosamine, TonBdépendent Transporters, glycan, pathogenicity, CUT locus, plant cell wall, Arabidopsis thaliana.
248 AUTEUR : Alice BOULANGER TITRE : Analyse d un nouveau système CUT impliqué dans l acquisition et l utilisation du N- acétylglucosamine par Xanthomonas campestris pathovar campestris. DIRECTEUR DE THESE : Matthieu ARLAT CO-DIRECTEUR DE THESE : Emmanuelle LAUBER Résumé Le N-acétylglucosamine (GlcNAc) est un sucre aminé ayant un rôle important dans de nombreux processus cellulaires chez les cellules procaryotes et eucaryotes. La plupart des bactéries marines et des bactéries pathogènes d insectes ont développé des mécanismes sophistiqués permettant le catabolisme de la chitine, un homopolymère de GlcNAc. La chitine est le second biopolymère le plus abondant dans la nature après la cellulose. Une bactérie non-chitinolytique rencontre-t-elle du GlcNAc dans l environnement? Et si oui, quelle est la source naturelle de cette molécule? Les données obtenues au cours de ma thèse suggèrent que la bactérie phytopathogène Xanthomonas campestris pv. campestris (Xcc), l agent responsable de la pourriture noire chez les Brassicacées, rencontre et exploite du GlcNAc provenant de la plante, au cours de l infection. La caractérisation de la voie d utilisation du GlcNAc chez Xcc et de son réseau de régulation a permis l identification de particularités par rapport aux autres bactéries, et notamment en ce qui concerne la source de GlcNAc. En effet, le GlcNAc utilisé au cours de l infection par Xcc semble provenir de la dégradation des glycanes des glycoprotéines végétales. Nous avons montré qu un transporteur de la membrane externe, ainsi que des glycosides hydrolases jouent un rôle direct dans la génération du GlcNAc in planta. MOTS-CLES : Xanthomonas campestris pv. campestris, N-acétylglucosamine, Transporteurs TonB-dépendants, glycane, pouvoir pathogène, CUT locus, paroi végétale, Arabidopsis thaliana.
COUSIN Fabien KERGOURLAY Gilles. 19 octobre 2007. de l hôte par les. Master 2 MFA Responsable : UE Incidence des paramètres environnementaux
 COUSIN Fabien KERGOURLAY Gilles 19 octobre 2007 Inhibition des défenses de l hôte par les bactéries pathogènes Master 2 MFA Responsable : UE Incidence des paramètres environnementaux Gwennola ERMEL I Détection
COUSIN Fabien KERGOURLAY Gilles 19 octobre 2007 Inhibition des défenses de l hôte par les bactéries pathogènes Master 2 MFA Responsable : UE Incidence des paramètres environnementaux Gwennola ERMEL I Détection
TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY)
 TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY) Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste Direction de l innovation scientifique et technologique Au Laboratoire
TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY) Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste Direction de l innovation scientifique et technologique Au Laboratoire
Travaux dirigés de Microbiologie Master I Sciences des Génomes et des Organismes Janvier 2015
 Andrew Tolonen [email protected] Travaux dirigés de Microbiologie Master I Sciences des Génomes et des Organismes Janvier 2015 A- Généralités I- La vie sur terre telle que nous la connaissons ne
Andrew Tolonen [email protected] Travaux dirigés de Microbiologie Master I Sciences des Génomes et des Organismes Janvier 2015 A- Généralités I- La vie sur terre telle que nous la connaissons ne
Les OGM. 5 décembre 2008. Nicole Mounier
 Les OGM 5 décembre 2008 Nicole Mounier Université Claude Bernard Lyon 1 CGMC, bâtiment Gregor Mendel 43, boulevard du 11 Novembre 1918 69622 Villeurbanne Cedex OGM Organismes Génétiquement Modifiés Transfert
Les OGM 5 décembre 2008 Nicole Mounier Université Claude Bernard Lyon 1 CGMC, bâtiment Gregor Mendel 43, boulevard du 11 Novembre 1918 69622 Villeurbanne Cedex OGM Organismes Génétiquement Modifiés Transfert
TD de Biochimie 4 : Coloration.
 TD de Biochimie 4 : Coloration. Synthèse de l expérience 2 Les questions posées durant l expérience 2 Exposé sur les méthodes de coloration des molécules : Générique Spécifique Autres Questions Pourquoi
TD de Biochimie 4 : Coloration. Synthèse de l expérience 2 Les questions posées durant l expérience 2 Exposé sur les méthodes de coloration des molécules : Générique Spécifique Autres Questions Pourquoi
En vue de l'obtention du
 THÈSE En vue de l'obtention du DOCTORAT DE L UNIVERSITÉ DE TOULOUSE Délivré par L'Institut National Polytechnique de Toulouse Discipline ou spécialité : Génétique et physiologie moléculaires des plantes
THÈSE En vue de l'obtention du DOCTORAT DE L UNIVERSITÉ DE TOULOUSE Délivré par L'Institut National Polytechnique de Toulouse Discipline ou spécialité : Génétique et physiologie moléculaires des plantes
MASTER (LMD) PARCOURS MICROORGANISMES, HÔTES, ENVIRONNEMENTS (MHE)
 MASTER (LMD) PARCOURS MICROORGANISMES, HÔTES, ENVIRONNEMENTS (MHE) RÉSUMÉ DE LA FORMATION Type de diplôme : Master (LMD) Domaine ministériel : Sciences, Technologies, Santé Mention : BIOLOGIE DES PLANTES
MASTER (LMD) PARCOURS MICROORGANISMES, HÔTES, ENVIRONNEMENTS (MHE) RÉSUMÉ DE LA FORMATION Type de diplôme : Master (LMD) Domaine ministériel : Sciences, Technologies, Santé Mention : BIOLOGIE DES PLANTES
EXERCICES : MECANISMES DE L IMMUNITE : pages 406 407 408 409 410
 EXERCICES : MECANISMES DE L IMMUNITE : pages 406 407 408 409 410 EXERCICE 1 PAGE 406 : EXPERIENCES A INTERPRETER Question : rôles respectifs du thymus et de la moelle osseuse dans la production des lymphocytes.
EXERCICES : MECANISMES DE L IMMUNITE : pages 406 407 408 409 410 EXERCICE 1 PAGE 406 : EXPERIENCES A INTERPRETER Question : rôles respectifs du thymus et de la moelle osseuse dans la production des lymphocytes.
Dr E. CHEVRET UE2.1 2013-2014. Aperçu général sur l architecture et les fonctions cellulaires
 Aperçu général sur l architecture et les fonctions cellulaires I. Introduction II. Les microscopes 1. Le microscope optique 2. Le microscope à fluorescence 3. Le microscope confocal 4. Le microscope électronique
Aperçu général sur l architecture et les fonctions cellulaires I. Introduction II. Les microscopes 1. Le microscope optique 2. Le microscope à fluorescence 3. Le microscope confocal 4. Le microscope électronique
ULBI 101 Biologie Cellulaire L1. Le Système Membranaire Interne
 ULBI 101 Biologie Cellulaire L1 Le Système Membranaire Interne De la nécessité d un SMI Le volume augmente comme le cube de la dimension linéaire, alors que la surface n'est augmentée que du carré Une
ULBI 101 Biologie Cellulaire L1 Le Système Membranaire Interne De la nécessité d un SMI Le volume augmente comme le cube de la dimension linéaire, alors que la surface n'est augmentée que du carré Une
Cellules procaryotes Service histologie Pr.k.mebarek
 Cellules procaryotes Service histologie Pr.k.mebarek I) Les cellules procaryotes II) Les cellules eucaryotes o 1) Caractéristiques générales des cellules eucaryotes o 2) Organisation des cellules eucaryotes
Cellules procaryotes Service histologie Pr.k.mebarek I) Les cellules procaryotes II) Les cellules eucaryotes o 1) Caractéristiques générales des cellules eucaryotes o 2) Organisation des cellules eucaryotes
GénoToul 2010, Hôtel de Région Midi Pyrénées, Toulouse, 10 décembre 2010
 GénoToul 2010, Hôtel de Région Midi Pyrénées, Toulouse, 10 décembre 2010 Analyse de la diversité moléculaire des régions génomiques de 30 gènes du développement méristématique dans une core collection
GénoToul 2010, Hôtel de Région Midi Pyrénées, Toulouse, 10 décembre 2010 Analyse de la diversité moléculaire des régions génomiques de 30 gènes du développement méristématique dans une core collection
Chapitre III Le phénotype immunitaire au cours de la vie
 Chapitre III Le phénotype immunitaire au cours de la vie Le phénotype immunitaire d un individu caractérise sa capacité à répondre, grâce aux effecteurs de l immunité adaptative, aux différents agents
Chapitre III Le phénotype immunitaire au cours de la vie Le phénotype immunitaire d un individu caractérise sa capacité à répondre, grâce aux effecteurs de l immunité adaptative, aux différents agents
CHAPITRE 3 LA SYNTHESE DES PROTEINES
 CHAITRE 3 LA SYNTHESE DES ROTEINES On sait qu un gène détient dans sa séquence nucléotidique, l information permettant la synthèse d un polypeptide. Ce dernier caractérisé par sa séquence d acides aminés
CHAITRE 3 LA SYNTHESE DES ROTEINES On sait qu un gène détient dans sa séquence nucléotidique, l information permettant la synthèse d un polypeptide. Ce dernier caractérisé par sa séquence d acides aminés
Correction TP 7 : L organisation de la plante et ses relations avec le milieu
 Correction TP 7 : L organisation de la plante et ses relations avec le milieu (TP multiposte : groupes de 4 élèves qui se répartissent sur les 4 postes une fois chaque poste travaillé, un bilan sera établi
Correction TP 7 : L organisation de la plante et ses relations avec le milieu (TP multiposte : groupes de 4 élèves qui se répartissent sur les 4 postes une fois chaque poste travaillé, un bilan sera établi
Génétique et génomique Pierre Martin
 Génétique et génomique Pierre Martin Principe de la sélections Repérage des animaux intéressants X Accouplements Programmés Sélection des meilleurs mâles pour la diffusion Index diffusés Indexation simultanée
Génétique et génomique Pierre Martin Principe de la sélections Repérage des animaux intéressants X Accouplements Programmés Sélection des meilleurs mâles pour la diffusion Index diffusés Indexation simultanée
3: Clonage d un gène dans un plasmide
 3: Clonage d un gène dans un plasmide Le clonage moléculaire est une des bases du génie génétique. Il consiste à insérer un fragment d'adn (dénommé insert) dans un vecteur approprié comme un plasmide par
3: Clonage d un gène dans un plasmide Le clonage moléculaire est une des bases du génie génétique. Il consiste à insérer un fragment d'adn (dénommé insert) dans un vecteur approprié comme un plasmide par
Conférence technique internationale de la FAO
 Décembre 2009 ABDC-10/7.2 F Conférence technique internationale de la FAO Biotechnologies agricoles dans les pays en développement: choix et perspectives pour les cultures, les forêts, l élevage, les pêches
Décembre 2009 ABDC-10/7.2 F Conférence technique internationale de la FAO Biotechnologies agricoles dans les pays en développement: choix et perspectives pour les cultures, les forêts, l élevage, les pêches
PARTIE II : RISQUE INFECTIEUX ET PROTECTION DE L ORGANISME. Chapitre 1 : L Homme confronté aux microbes de son environnement
 PARTIE II : RISQUE INFECTIEUX ET PROTECTION DE L ORGANISME Chapitre 1 : L Homme confronté aux microbes de son environnement I- Les microbes dans notre environnement Qu est-ce qu un microbe? Où se trouvent-ils?
PARTIE II : RISQUE INFECTIEUX ET PROTECTION DE L ORGANISME Chapitre 1 : L Homme confronté aux microbes de son environnement I- Les microbes dans notre environnement Qu est-ce qu un microbe? Où se trouvent-ils?
Chapitre 7 : Structure de la cellule Le noyau cellulaire
 UE2 : Structure générale de la cellule Chapitre 7 : Structure de la cellule Le noyau cellulaire Professeur Michel SEVE Année universitaire 2010/2011 Université Joseph Fourier de Grenoble - Tous droits
UE2 : Structure générale de la cellule Chapitre 7 : Structure de la cellule Le noyau cellulaire Professeur Michel SEVE Année universitaire 2010/2011 Université Joseph Fourier de Grenoble - Tous droits
Hépatite chronique B Moyens thérapeutiques
 Hépatite chronique B Moyens thérapeutiques Dr Olfa BAHRI Laboratoire de Virologie Clinique Institut Pasteur de Tunis INTRODUCTION Plus de 300. 10 6 porteurs chroniques de VHB dans le monde Hépatite chronique
Hépatite chronique B Moyens thérapeutiques Dr Olfa BAHRI Laboratoire de Virologie Clinique Institut Pasteur de Tunis INTRODUCTION Plus de 300. 10 6 porteurs chroniques de VHB dans le monde Hépatite chronique
Biomarqueurs en Cancérologie
 Biomarqueurs en Cancérologie Définition, détermination, usage Biomarqueurs et Cancer: définition Anomalie(s) quantitative(s) ou qualitative(s) Indicative(s) ou caractéristique(s) d un cancer ou de certaines
Biomarqueurs en Cancérologie Définition, détermination, usage Biomarqueurs et Cancer: définition Anomalie(s) quantitative(s) ou qualitative(s) Indicative(s) ou caractéristique(s) d un cancer ou de certaines
Les cytokines et leurs récepteurs. Laurence Guglielmi [email protected]
 Les cytokines et leurs récepteurs Laurence Guglielmi [email protected] l i@ i 1 Les cytokines et leurs récepteurs 2 mécanismes principaux d interactions cellulaires : - contact membranaire
Les cytokines et leurs récepteurs Laurence Guglielmi [email protected] l i@ i 1 Les cytokines et leurs récepteurs 2 mécanismes principaux d interactions cellulaires : - contact membranaire
Master de Bioinformatique et Biologie des Systèmes Toulouse http://m2pbioinfo.biotoul.fr Responsable : Pr. Gwennaele Fichant
 Master de Bioinformatique et Biologie des Systèmes Toulouse http://m2pbioinfo.biotoul.fr Responsable : Pr. Gwennaele Fichant Parcours: Master 1 : Bioinformatique et biologie des Systèmes dans le Master
Master de Bioinformatique et Biologie des Systèmes Toulouse http://m2pbioinfo.biotoul.fr Responsable : Pr. Gwennaele Fichant Parcours: Master 1 : Bioinformatique et biologie des Systèmes dans le Master
Biochimie I. Extraction et quantification de l hexokinase dans Saccharomyces cerevisiae 1. Assistants : Tatjana Schwabe Marcy Taylor Gisèle Dewhurst
 Biochimie I Extraction et quantification de l hexokinase dans Saccharomyces cerevisiae 1 Daniel Abegg Sarah Bayat Alexandra Belfanti Assistants : Tatjana Schwabe Marcy Taylor Gisèle Dewhurst Laboratoire
Biochimie I Extraction et quantification de l hexokinase dans Saccharomyces cerevisiae 1 Daniel Abegg Sarah Bayat Alexandra Belfanti Assistants : Tatjana Schwabe Marcy Taylor Gisèle Dewhurst Laboratoire
Thème sélection génétique des plantes hybridation et génie génétique
 Thème sélection génétique des plantes hybridation et génie génétique Exemple d activité : recenser, extraire et exploiter des informations afin de comprendre les caractéristiques et les limites de la modification
Thème sélection génétique des plantes hybridation et génie génétique Exemple d activité : recenser, extraire et exploiter des informations afin de comprendre les caractéristiques et les limites de la modification
que dois-tu savoir sur le diabète?
 INVENTIV HEALTH COMMUNICATIONS - TERRE NEUVE - FRHMG00277 - Avril 2013 - Lilly - Tous droits de reproduction réservés. que dois-tu savoir sur le diabète? Lilly France 24 boulevard Vital Bouhot CS 50004-92521
INVENTIV HEALTH COMMUNICATIONS - TERRE NEUVE - FRHMG00277 - Avril 2013 - Lilly - Tous droits de reproduction réservés. que dois-tu savoir sur le diabète? Lilly France 24 boulevard Vital Bouhot CS 50004-92521
(ERWINIA PECTINOLYTIQUES)
 TESTS BIOCHIMIQUES CLASSIQUES POUR L IDENTIFICATION DES PECTOBACTERIUM (ERWINIA PECTINOLYTIQUES) ET DES PSEUDOMONAS FLUORESCENTS Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste
TESTS BIOCHIMIQUES CLASSIQUES POUR L IDENTIFICATION DES PECTOBACTERIUM (ERWINIA PECTINOLYTIQUES) ET DES PSEUDOMONAS FLUORESCENTS Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste
IMMUNOLOGIE. La spécificité des immunoglobulines et des récepteurs T. Informations scientifiques
 IMMUNOLOGIE La spécificité des immunoglobulines et des récepteurs T Informations scientifiques L infection par le VIH entraîne des réactions immunitaires de l organisme qui se traduisent par la production
IMMUNOLOGIE La spécificité des immunoglobulines et des récepteurs T Informations scientifiques L infection par le VIH entraîne des réactions immunitaires de l organisme qui se traduisent par la production
2 C est quoi la chimie?
 PARTIE 1 AVANT LA CHIMIE VERTE... 2 C est quoi la chimie? L inconnu étant source d angoisse, nous allons essayer de définir les grands domaines de la chimie pour mieux la connaître, l appréhender et donc
PARTIE 1 AVANT LA CHIMIE VERTE... 2 C est quoi la chimie? L inconnu étant source d angoisse, nous allons essayer de définir les grands domaines de la chimie pour mieux la connaître, l appréhender et donc
C. Magdo, Altis Semiconductor (Corbeil-Essonne) > NOTE D APPLICATION N 2
 C. Magdo, Altis Semiconductor (Corbeil-Essonne) - JANVIER 2008 INTRODUCTION La fabrication de semi-conducteurs nécessite un environnement de production extrêmement stable en température et hygrométrie.
C. Magdo, Altis Semiconductor (Corbeil-Essonne) - JANVIER 2008 INTRODUCTION La fabrication de semi-conducteurs nécessite un environnement de production extrêmement stable en température et hygrométrie.
Intrants médicamenteux en agriculture et en santé : les écosystèmes microbiens sont-ils un problème ou une solution?
 Les Rencontres de l Inra au Salon de l agriculture Intrants médicamenteux en agriculture et en santé : les écosystèmes microbiens sont-ils un problème ou une solution? Lundi 23 février 2015 Programme 14h30
Les Rencontres de l Inra au Salon de l agriculture Intrants médicamenteux en agriculture et en santé : les écosystèmes microbiens sont-ils un problème ou une solution? Lundi 23 février 2015 Programme 14h30
Liste des matières enseignées
 Liste des matières enseignées Domaine : Sciences de la Nature et de la Vie Filière : Biologie Parcours : Tronc Commun Semestre1 VHG Coefficient Cours TD/TP Crédits/s. unité crédits U.E fondamental : 13
Liste des matières enseignées Domaine : Sciences de la Nature et de la Vie Filière : Biologie Parcours : Tronc Commun Semestre1 VHG Coefficient Cours TD/TP Crédits/s. unité crédits U.E fondamental : 13
Le rôle de l endocytose dans les processus pathologiques
 UE7 Cours n 9 C. LAMAZE 24.11.11 Elise GODEAU (partie1) Guillaume MERGENTHALER (partie2) Le rôle de l endocytose dans les processus pathologiques SOMMAIRE : I. L endocytose à récepteurs : la voie des clathrines
UE7 Cours n 9 C. LAMAZE 24.11.11 Elise GODEAU (partie1) Guillaume MERGENTHALER (partie2) Le rôle de l endocytose dans les processus pathologiques SOMMAIRE : I. L endocytose à récepteurs : la voie des clathrines
AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS
 AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS CONCOURS EXTERNE ÉPREUVES D ADMISSION session 2010 TRAVAUX PRATIQUES DE CONTRE-OPTION DU SECTEUR A CANDIDATS DES SECTEURS B ET C
AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS CONCOURS EXTERNE ÉPREUVES D ADMISSION session 2010 TRAVAUX PRATIQUES DE CONTRE-OPTION DU SECTEUR A CANDIDATS DES SECTEURS B ET C
Mise en place d une plateforme de gestion de matériels biologiques : quels avantages pour les chercheurs?
 Mise en place d une plateforme de gestion de matériels biologiques : quels avantages pour les chercheurs? Dr Xavier Manival, Laboratoire IMoPA, CR, CNRS Françoise Tisserand-Bedri, Documentaliste, Inist-CNRS
Mise en place d une plateforme de gestion de matériels biologiques : quels avantages pour les chercheurs? Dr Xavier Manival, Laboratoire IMoPA, CR, CNRS Françoise Tisserand-Bedri, Documentaliste, Inist-CNRS
Domaine : Sciences, Technologies et Santé Mention : Nutrition, Sciences des aliments, Agroalimentaire
 Contexte Domaine : Sciences, Technologies et Santé Mention : Nutrition, Sciences des aliments, Agroalimentaire Fédération des spécialités de Master des 5 pôles universitaires partenaires de la région Nord-Pas-de-Calais
Contexte Domaine : Sciences, Technologies et Santé Mention : Nutrition, Sciences des aliments, Agroalimentaire Fédération des spécialités de Master des 5 pôles universitaires partenaires de la région Nord-Pas-de-Calais
ACIDES BASES. Chap.5 SPIESS
 ACIDES BASES «Je ne crois pas que l on me conteste que l acide n ait des pointes Il ne faut que le goûter pour tomber dans ce sentiment car il fait des picotements sur la langue.» Notion d activité et
ACIDES BASES «Je ne crois pas que l on me conteste que l acide n ait des pointes Il ne faut que le goûter pour tomber dans ce sentiment car il fait des picotements sur la langue.» Notion d activité et
4 : MÉTHODES D ANALYSE UTILISÉES EN ÉCOLOGIE MICROBIENNE
 4 : MÉTHODES D ANALYSE UTILISÉES EN ÉCOLOGIE MICROBIENNE L écologie microbienne (ou étude des micro-organismes de l environnement) étudie : les relations entre les différentes populations de micro-organismes
4 : MÉTHODES D ANALYSE UTILISÉES EN ÉCOLOGIE MICROBIENNE L écologie microbienne (ou étude des micro-organismes de l environnement) étudie : les relations entre les différentes populations de micro-organismes
L immunoenzymologie. Technique puissante couramment utilisée e en recherche et en diagnostic cificité des anticorps pour leurs nes
 L immunoenzymologie Technique puissante couramment utilisée e en recherche et en diagnostic Basée e sur la très s grande spécificit cificité des anticorps pour leurs antigènes nes Test qualitatif Détection
L immunoenzymologie Technique puissante couramment utilisée e en recherche et en diagnostic Basée e sur la très s grande spécificit cificité des anticorps pour leurs antigènes nes Test qualitatif Détection
5. Matériaux en contact avec l eau
 Monitoring de la qualité Microbiologique de l eau potable dans les réseaux de distributions Intérêt de l utilisation d un kit de mesure rapide de la flore totale UTLISATIONS 1. Surveillance de Réseau mixte
Monitoring de la qualité Microbiologique de l eau potable dans les réseaux de distributions Intérêt de l utilisation d un kit de mesure rapide de la flore totale UTLISATIONS 1. Surveillance de Réseau mixte
Fiche technique. Comment lutter contre les nématodes parasites des cultures maraichères par la solarisation?
 Institut National de la Recherche Agronomique du Niger Réseau National des Chambres d'agriculture du Niger Fiche technique RECA Réseau National des Chambres N d Agriculture du Niger iger Comment lutter
Institut National de la Recherche Agronomique du Niger Réseau National des Chambres d'agriculture du Niger Fiche technique RECA Réseau National des Chambres N d Agriculture du Niger iger Comment lutter
Présentation Générale
 Mars 2009 Présentation Générale 1- Le Master Recherche en Sciences de la Vie et de la Santé à Nice Objectifs, environnement scientifique, organisation Enseignements, les spécialités, les cours et les stages
Mars 2009 Présentation Générale 1- Le Master Recherche en Sciences de la Vie et de la Santé à Nice Objectifs, environnement scientifique, organisation Enseignements, les spécialités, les cours et les stages
Parasites externes du chat et du chien
 Parasites externes du chat et du chien Identification, prévention et traitement Les tiques Les tiques transmettent des maladies parfois mortelles. La prévention est la meilleure arme. 1 - Où les trouve-t-on?
Parasites externes du chat et du chien Identification, prévention et traitement Les tiques Les tiques transmettent des maladies parfois mortelles. La prévention est la meilleure arme. 1 - Où les trouve-t-on?
ANTICORPS POLYCLONAUX ANTI IMMUNOGLOBULINES
 L OUTIL IDEAL POUR TOUTES LES DETECTIONS IMMUNOCHIMIQUES pour toutes les techniques immunodosages (EIA/ELISA) dot/ westernblot immunohistochimie immunocytochimie cytométrie en flux quel que soit le système
L OUTIL IDEAL POUR TOUTES LES DETECTIONS IMMUNOCHIMIQUES pour toutes les techniques immunodosages (EIA/ELISA) dot/ westernblot immunohistochimie immunocytochimie cytométrie en flux quel que soit le système
Hémochromatose génétique non liée à HFE-1 : quand et comment la rechercher? Cécilia Landman 11 décembre 2010
 Hémochromatose génétique non liée à HFE-1 : quand et comment la rechercher? Cécilia Landman 11 décembre 2010 Métabolisme du fer : hepcidine Fer absorbé par les entérocytes des villosités duodénales : transporteur
Hémochromatose génétique non liée à HFE-1 : quand et comment la rechercher? Cécilia Landman 11 décembre 2010 Métabolisme du fer : hepcidine Fer absorbé par les entérocytes des villosités duodénales : transporteur
1. La famille d accueil de Nadja est composée de combien de personnes? 2. Un membre de la famille de Mme Millet n est pas Français. Qui est-ce?
 1 LA FAMILLE 1.1 Lecture premier texte Nadja va passer quatre mois de la prochaine année scolaire en France. Aujourd hui, elle a reçu cette lettre de sa famille d accueil. Chère Nadja, Je m appelle Martine
1 LA FAMILLE 1.1 Lecture premier texte Nadja va passer quatre mois de la prochaine année scolaire en France. Aujourd hui, elle a reçu cette lettre de sa famille d accueil. Chère Nadja, Je m appelle Martine
ÉCOLES NORMALES SUPÉRIEURES ÉCOLE NATIONALE DES PONTS ET CHAUSSÉES CONCOURS D ADMISSION SESSION 2013 FILIÈRE BCPST COMPOSITION DE BIOLOGIE
 ÉCOLES NORMALES SUPÉRIEURES ÉCOLE NATIONALE DES PONTS ET CHAUSSÉES CONCOURS D ADMISSION SESSION 2013 FILIÈRE BCPST COMPOSITION DE BIOLOGIE Épreuve commune aux ENS de Cachan, Lyon, Paris et de l ENPC Durée
ÉCOLES NORMALES SUPÉRIEURES ÉCOLE NATIONALE DES PONTS ET CHAUSSÉES CONCOURS D ADMISSION SESSION 2013 FILIÈRE BCPST COMPOSITION DE BIOLOGIE Épreuve commune aux ENS de Cachan, Lyon, Paris et de l ENPC Durée
Contrôle et modulation de la réponse immunitaire par Brucella abortus
 AIX-MARSEILLE UNIVERSITE Faculté des sciences de Luminy Ecole Doctorale des Sciences de la Vie et de la Santé THESE DE DOCTORAT Biologie - Spécialité : Immunologie En vue d'obtenir le titre de DOCTEUR
AIX-MARSEILLE UNIVERSITE Faculté des sciences de Luminy Ecole Doctorale des Sciences de la Vie et de la Santé THESE DE DOCTORAT Biologie - Spécialité : Immunologie En vue d'obtenir le titre de DOCTEUR
La notion de croissance (végétale) en sixième et en première S.
 La notion de croissance (végétale) en sixième et en première S. Activité proposée : La notion de croissance est abordée en classe de 6 ème et elle est traitée en première S. Montrez sur cet exemple qu
La notion de croissance (végétale) en sixième et en première S. Activité proposée : La notion de croissance est abordée en classe de 6 ème et elle est traitée en première S. Montrez sur cet exemple qu
Nouveau. TRIMAXX, le raccourcisseur qui en fait un MAXX.
 Coup de tonnerre dans les raccourcisseurs Nouveau. TRIMAXX, le raccourcisseur qui en fait un MAXX. Trimaxx est un nouveau raccourcisseur pour céréales à paille et féveroles doté d une formulation Son absorption
Coup de tonnerre dans les raccourcisseurs Nouveau. TRIMAXX, le raccourcisseur qui en fait un MAXX. Trimaxx est un nouveau raccourcisseur pour céréales à paille et féveroles doté d une formulation Son absorption
Bases de données des mutations
 Bases de données des mutations CFMDB CFTR2 CFTR-France / Registre Corinne THEZE, Corinne BAREIL Laboratoire de génétique moléculaire Montpellier Atelier Muco, Lille, 25-27 septembre 2014 Accès libre http://www.genet.sickkids.on.ca/app
Bases de données des mutations CFMDB CFTR2 CFTR-France / Registre Corinne THEZE, Corinne BAREIL Laboratoire de génétique moléculaire Montpellier Atelier Muco, Lille, 25-27 septembre 2014 Accès libre http://www.genet.sickkids.on.ca/app
Plateforme Transgenèse/Zootechnie/Exploration Fonctionnelle IBiSA. «Anexplo» Service Transgenèse. Catalogue des prestations
 Plateforme Transgenèse/Zootechnie/Exploration Fonctionnelle IBiSA «Anexplo» Service Transgenèse Catalogue des prestations 04/01/12 - Page 1 sur 8 Présentation du service de Transgenèse Le service de Transgenèse
Plateforme Transgenèse/Zootechnie/Exploration Fonctionnelle IBiSA «Anexplo» Service Transgenèse Catalogue des prestations 04/01/12 - Page 1 sur 8 Présentation du service de Transgenèse Le service de Transgenèse
BREVET D ÉTUDES PROFESSIONNELLES AGRICOLES SUJET
 SESSION 2010 France métropolitaine Option : élevage canin et félin BREVET D ÉTUDES PROFESSIONNELLES AGRICOLES ÉPREUVE E DU DEUXIÈME GROUPE Durée : 2 heures Matériel(s) et document(s) autorisé(s) : Calculatrice
SESSION 2010 France métropolitaine Option : élevage canin et félin BREVET D ÉTUDES PROFESSIONNELLES AGRICOLES ÉPREUVE E DU DEUXIÈME GROUPE Durée : 2 heures Matériel(s) et document(s) autorisé(s) : Calculatrice
MYRIAD. l ADN isolé n est à présent plus brevetable!
 MYRIAD La Cour Suprême des Etats-Unis revient sur plus de 30 ans de pratique : l ADN isolé n est à présent plus brevetable! Mauvaise passe pour les inventions en biotechnologies sur le territoire américain.
MYRIAD La Cour Suprême des Etats-Unis revient sur plus de 30 ans de pratique : l ADN isolé n est à présent plus brevetable! Mauvaise passe pour les inventions en biotechnologies sur le territoire américain.
Structure quantique cohérente et incohérente de l eau liquide
 Structure quantique cohérente et incohérente de l eau liquide Prof. Marc HENRY Chimie Moléculaire du Solide Institut Le Bel, 4, Rue Blaise Pascal 67070 Strasbourg Cedex, France Tél: 03.68.85.15.00 e-mail:
Structure quantique cohérente et incohérente de l eau liquide Prof. Marc HENRY Chimie Moléculaire du Solide Institut Le Bel, 4, Rue Blaise Pascal 67070 Strasbourg Cedex, France Tél: 03.68.85.15.00 e-mail:
MABioVis. Bio-informatique et la
 MABioVis Modèles et Algorithmes pour la Bio-informatique et la Visualisation Visite ENS Cachan 5 janvier 2011 MABioVis G GUY MELANÇON (PR UFR Maths Info / EPI GRAVITE) (là, maintenant) - MABioVis DAVID
MABioVis Modèles et Algorithmes pour la Bio-informatique et la Visualisation Visite ENS Cachan 5 janvier 2011 MABioVis G GUY MELANÇON (PR UFR Maths Info / EPI GRAVITE) (là, maintenant) - MABioVis DAVID
Une conférence-débat proposée par l Institut National de la Recherche Agronomique
 Economies d'énergies dans les procédés agro-alimentaires : l'optimisation coût/qualité, un équilibre pas si facile à maîtriser Une conférence-débat proposée par l Institut National de la Recherche Agronomique
Economies d'énergies dans les procédés agro-alimentaires : l'optimisation coût/qualité, un équilibre pas si facile à maîtriser Une conférence-débat proposée par l Institut National de la Recherche Agronomique
Il est bien établi que le réseau d eau hospitalier peut
 Les micro-organismes de l eau impliqués dans les infections nosocomiales Depuis 2001 chez Pall, en charge de l information scientifique et réglementaire dans les domaines d applications couverts par la
Les micro-organismes de l eau impliqués dans les infections nosocomiales Depuis 2001 chez Pall, en charge de l information scientifique et réglementaire dans les domaines d applications couverts par la
Base de données bibliographiques Pubmed-Medline
 Chapitre 1 ; Domaine 1 ; Documentation ; Champs référentiels 1.1.1, 1.1.2 et 1.1.3 Base de données bibliographiques Pubmed-Medline D r Patrick Deschamps,, 30 mai 2007 PLAN C2i métiers de la santé Introduction
Chapitre 1 ; Domaine 1 ; Documentation ; Champs référentiels 1.1.1, 1.1.2 et 1.1.3 Base de données bibliographiques Pubmed-Medline D r Patrick Deschamps,, 30 mai 2007 PLAN C2i métiers de la santé Introduction
La Greffe de Cellules Souches Hématopoïétiques
 La Greffe de Cellules Souches Hématopoïétiques Professeur Ibrahim Yakoub-Agha CHRU de LILLE (Illustration de J. Cloup, extraite du CD-Rom «greffe de Moelle» réalisé par la société K Noë) La moelle osseuse
La Greffe de Cellules Souches Hématopoïétiques Professeur Ibrahim Yakoub-Agha CHRU de LILLE (Illustration de J. Cloup, extraite du CD-Rom «greffe de Moelle» réalisé par la société K Noë) La moelle osseuse
Vaccinologie et Stratégie de Développement des Vaccins
 Vaccinologie et Stratégie de Développement des Vaccins Vaccinologie 1977 - Terme utilisé par Jonas Salk. 1983 - Rassemble tous les aspects des vaccinations : biologiques, immunologiques et cliniques ainsi
Vaccinologie et Stratégie de Développement des Vaccins Vaccinologie 1977 - Terme utilisé par Jonas Salk. 1983 - Rassemble tous les aspects des vaccinations : biologiques, immunologiques et cliniques ainsi
L INSUFFISANCE CARDIAQUE
 L INSUFFISANCE CARDIAQUE EXISTE-T-IL DES TRAITEMENTS À BASE DE CELLULES SOUCHES POUR L INSUFFISANCE CARDIAQUE? Bien qu aucun traitement à base de cellules souches pour l insuffisance cardiaque n ait encore
L INSUFFISANCE CARDIAQUE EXISTE-T-IL DES TRAITEMENTS À BASE DE CELLULES SOUCHES POUR L INSUFFISANCE CARDIAQUE? Bien qu aucun traitement à base de cellules souches pour l insuffisance cardiaque n ait encore
Prévenir la colonisation par Campylobacter chez les poulets de chair. Dr. Wael Abdelrahman Consultant technique, Probiotiques volailles
 Prévenir la colonisation par Campylobacter chez les poulets de chair Dr. Wael Abdelrahman Consultant technique, Probiotiques volailles Prévenir la colonisation par Campylobacter chez les poulets de chair
Prévenir la colonisation par Campylobacter chez les poulets de chair Dr. Wael Abdelrahman Consultant technique, Probiotiques volailles Prévenir la colonisation par Campylobacter chez les poulets de chair
Prix Pierre Potier L innovation en chimie au bénéfice de l environnement
 Prix Pierre Potier L innovation en chimie au bénéfice de l environnement A l initiative de François Loos Ministre délégué à l Industrie Page 1 Prix Pierre Potier L innovation en chimie au bénéfice de l
Prix Pierre Potier L innovation en chimie au bénéfice de l environnement A l initiative de François Loos Ministre délégué à l Industrie Page 1 Prix Pierre Potier L innovation en chimie au bénéfice de l
Le Monde des insectes, son importance pour l Homme et l apport de l étude des insectes aux sciences du vivant.
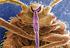 MEDAILLE D OR DU CNRS 2011 Le Monde des insectes, son importance pour l Homme et l apport de l étude des insectes aux sciences du vivant. Extrait de l allocution prononcée le 19 juin 2007 par Jules Hoffmann,
MEDAILLE D OR DU CNRS 2011 Le Monde des insectes, son importance pour l Homme et l apport de l étude des insectes aux sciences du vivant. Extrait de l allocution prononcée le 19 juin 2007 par Jules Hoffmann,
Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic de cancer
 Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
Papa, pourquoi je ne peux pas manger la même nourriture que toi?
 1 Papa, pourquoi je ne peux pas manger la même nourriture que toi? Un livret pour les enfants qui sont PCU par Gerda Lundberg, Association PCU de Suède 2 Traduit de l anglais Mme Yvonne Miller Berlie (A.P.E.P.)
1 Papa, pourquoi je ne peux pas manger la même nourriture que toi? Un livret pour les enfants qui sont PCU par Gerda Lundberg, Association PCU de Suède 2 Traduit de l anglais Mme Yvonne Miller Berlie (A.P.E.P.)
Chapitre 4 : cohabiter avec les micro-organismes. Contrat-élève 3 ème
 Chapitre 4 : cohabiter avec les micro-organismes Mais, que dois-je savoir? Pour rattraper un cours manquant, retrouve-le sur le site du collège dans la rubrique «enseignements» : http://colleges.acrouen.fr/courbet/spipuser/
Chapitre 4 : cohabiter avec les micro-organismes Mais, que dois-je savoir? Pour rattraper un cours manquant, retrouve-le sur le site du collège dans la rubrique «enseignements» : http://colleges.acrouen.fr/courbet/spipuser/
TECHNIQUES DE LABORATOIRE POUR LE DIAGNOSTIC DES BACTÉRIES PHYTOPATHOGÈNES
 TECHNIQUES DE LABORATOIRE POUR LE DIAGNOSTIC DES BACTÉRIES PHYTOPATHOGÈNES Ce document a pour objectif de présenter les diverses techniques utilisées au Laboratoire de diagnostic en phytoprotection pour
TECHNIQUES DE LABORATOIRE POUR LE DIAGNOSTIC DES BACTÉRIES PHYTOPATHOGÈNES Ce document a pour objectif de présenter les diverses techniques utilisées au Laboratoire de diagnostic en phytoprotection pour
Séquence 2. L expression du patrimoine génétique. Sommaire
 Séquence 2 L expression du patrimoine génétique Sommaire 1. La synthèse des protéines 2. Phénotypes, génotypes et environnement Synthèse de la séquence 2 Exercices de la séquence 2 Glossaire des séquences
Séquence 2 L expression du patrimoine génétique Sommaire 1. La synthèse des protéines 2. Phénotypes, génotypes et environnement Synthèse de la séquence 2 Exercices de la séquence 2 Glossaire des séquences
DIAPOSITIVE 1 Cette présentation a trait à la réglementation sur les thérapies cellulaires.
 Produits de thérapie cellulaire DIAPOSITIVE 1 Cette présentation a trait à la réglementation sur les thérapies cellulaires. DIAPOSITIVE 2 La fabrication des thérapies cellulaires est examinée par la Division
Produits de thérapie cellulaire DIAPOSITIVE 1 Cette présentation a trait à la réglementation sur les thérapies cellulaires. DIAPOSITIVE 2 La fabrication des thérapies cellulaires est examinée par la Division
Production d une protéine recombinante
 99 Production d une protéine recombinante Lic. B. PIRSON Lic. J-M. SERONT ISICHt - Mons Production de la protéine recombinante GFP (Green Fluorescent Protein d Aequoria victoria) par une bactérie ( E.
99 Production d une protéine recombinante Lic. B. PIRSON Lic. J-M. SERONT ISICHt - Mons Production de la protéine recombinante GFP (Green Fluorescent Protein d Aequoria victoria) par une bactérie ( E.
Master en Biochimie et Biologie moléculaire et cellulaire (BBMC)
 Master en Biochimie et Biologie moléculaire et cellulaire (BBMC) BIOLOGIE MOLÉCULAIRE EN CONDITIONS PHYSIOLOGIQUES ET PATHOLOGIQUES Département de Biologie Faculté de Médecine Université de Namur Master
Master en Biochimie et Biologie moléculaire et cellulaire (BBMC) BIOLOGIE MOLÉCULAIRE EN CONDITIONS PHYSIOLOGIQUES ET PATHOLOGIQUES Département de Biologie Faculté de Médecine Université de Namur Master
Rôle des acides biliaires dans la régulation de l homéostasie du glucose : implication de FXR dans la cellule bêta-pancréatique
 Rôle des acides biliaires dans la régulation de l homéostasie du glucose : implication de FXR dans la cellule bêta-pancréatique Tuteur : Anne Muhr-Tailleux cardiovasculaires et diabète (Equipe 1) Institut
Rôle des acides biliaires dans la régulation de l homéostasie du glucose : implication de FXR dans la cellule bêta-pancréatique Tuteur : Anne Muhr-Tailleux cardiovasculaires et diabète (Equipe 1) Institut
La résistance d'agents infectieux aux médicaments antimicrobiens
 DECLARATION COMMUNE DES ACADEMIES DU G SCIENCE 2013 La résistance d'agents infectieux aux médicaments antimicrobiens Une menace globale pour l'humanité Depuis l introduction dans les années 40 du premier
DECLARATION COMMUNE DES ACADEMIES DU G SCIENCE 2013 La résistance d'agents infectieux aux médicaments antimicrobiens Une menace globale pour l'humanité Depuis l introduction dans les années 40 du premier
Sérodiagnostic de la polyarthrite rhumatoïde
 1 ETSL Sérodiagnostic de la polyarthrite rhumatoïde TP 1 GABIN-GAUTHIER 13/11/2009 I. LA MALADIE... 2 II. TECHNIQUES QUALITATIVES... 2 1. PRINCIPE... 2 2. MODE OPERATOIRE... 3 2.1. WRST ou Waaler Rose
1 ETSL Sérodiagnostic de la polyarthrite rhumatoïde TP 1 GABIN-GAUTHIER 13/11/2009 I. LA MALADIE... 2 II. TECHNIQUES QUALITATIVES... 2 1. PRINCIPE... 2 2. MODE OPERATOIRE... 3 2.1. WRST ou Waaler Rose
I. La levure Saccharomyces cerevisiae: mode de vie
 LES LEVURES UE «levures» -5 avril: généralités (MN Simon) -6 avril: analyse génétique (MN Simon) -6 avril: Cycle cellulaire I: la réplication (E. bailly) -7 avril: Cycle cellulaire II: la mitose (E. Bailly)
LES LEVURES UE «levures» -5 avril: généralités (MN Simon) -6 avril: analyse génétique (MN Simon) -6 avril: Cycle cellulaire I: la réplication (E. bailly) -7 avril: Cycle cellulaire II: la mitose (E. Bailly)
LA A RESPIRATION CELLULAIRE
 Instructions aux professeurs Domaine : 1.1 Le transport de substances, réaction chimique de la respiration cellulaire, p. 6 Travail à réaliser : Les élèves répondent aux questions. Matériel : Feuilles
Instructions aux professeurs Domaine : 1.1 Le transport de substances, réaction chimique de la respiration cellulaire, p. 6 Travail à réaliser : Les élèves répondent aux questions. Matériel : Feuilles
RÉPERTOIRE RELÈVE SCIENTIFIQUE AU SERVICE DES ENTREPRISES AGROALIMENTAIRES. 2 e édition
 RELÈVE SCIENTIFIQUE AU SERVICE 2 e édition Juin 2011 Réalisé par : Partenaire financier du CQVB : Objectif : Ce répertoire vise à faciliter le maillage entre les étudiants-chercheurs universitaires et
RELÈVE SCIENTIFIQUE AU SERVICE 2 e édition Juin 2011 Réalisé par : Partenaire financier du CQVB : Objectif : Ce répertoire vise à faciliter le maillage entre les étudiants-chercheurs universitaires et
Sommaire de la séquence 8
 Sommaire de la séquence 8 Nous avons découvert dans la séquence 7 que les micro-organismes sont présents partout dans notre environnement et qu à la faveur d une lésion, ils sont capables de franchir nos
Sommaire de la séquence 8 Nous avons découvert dans la séquence 7 que les micro-organismes sont présents partout dans notre environnement et qu à la faveur d une lésion, ils sont capables de franchir nos
Que chaque instant de cette journée contribue à faire régner la joie dans ton coeur
 Que chaque instant de cette journée contribue à faire régner la joie dans ton coeur Des souhaits pour une vie des plus prospères et tous les voeux nécessaires pour des saisons extraordinaires! Meilleurs
Que chaque instant de cette journée contribue à faire régner la joie dans ton coeur Des souhaits pour une vie des plus prospères et tous les voeux nécessaires pour des saisons extraordinaires! Meilleurs
Isolation, storage and management of plant pathogenic bacterial strains. 4 March 2008 COST 873, York
 Isolation, storage and management of plant pathogenic bacterial strains Collect of samples This first step is very important because all other steps depend on this step. Moreover, the person who performs
Isolation, storage and management of plant pathogenic bacterial strains Collect of samples This first step is very important because all other steps depend on this step. Moreover, the person who performs
Normes internationales pour les mesures phytosanitaires (NIMPs)
 105 Annexe 3 Normes internationales pour les mesures phytosanitaires (NIMPs) On trouvera ci-après une description succincte des NIMP adoptées. Le texte intégral des NIMP peut être consulté sur le Site
105 Annexe 3 Normes internationales pour les mesures phytosanitaires (NIMPs) On trouvera ci-après une description succincte des NIMP adoptées. Le texte intégral des NIMP peut être consulté sur le Site
LES CYTOKININES. 1962: la molécule active du lait de coco a les caractéristiques d une base nucléique, l adénosine (base purique)
 LES CYTOKININES Les cytokinines (kutos, cellule; kinein, mouvoir, au sens de séparer) sont nécessaires à la division de cellules 1941: Blakeslee, essaie de créer des hybrides entre différentes espèces
LES CYTOKININES Les cytokinines (kutos, cellule; kinein, mouvoir, au sens de séparer) sont nécessaires à la division de cellules 1941: Blakeslee, essaie de créer des hybrides entre différentes espèces
Le conditionnel présent
 Le conditionnel présent EMPLOIS On emploie généralement le conditionnel présent pour exprimer: une supposition, une hypothèse, une possibilité, une probabilité ( certitude); Ça m'étonnerait! J'ai entendu
Le conditionnel présent EMPLOIS On emploie généralement le conditionnel présent pour exprimer: une supposition, une hypothèse, une possibilité, une probabilité ( certitude); Ça m'étonnerait! J'ai entendu
Biologie Appliquée. Dosages Immunologiques TD9 Mai 2015. Stéphanie Sigaut INSERM U1141 [email protected]
 Biologie Appliquée Dosages Immunologiques TD9 Mai 2015 Stéphanie Sigaut INSERM U1141 [email protected] 1 ELISA 2 3 4 [Ac] 5 6 7 8 9 Correction : Faire la moyenne D0-1 et D0-2 pour toute les valeurs
Biologie Appliquée Dosages Immunologiques TD9 Mai 2015 Stéphanie Sigaut INSERM U1141 [email protected] 1 ELISA 2 3 4 [Ac] 5 6 7 8 9 Correction : Faire la moyenne D0-1 et D0-2 pour toute les valeurs
Partie Observer : Ondes et matière CHAP 04-ACT/DOC Analyse spectrale : Spectroscopies IR et RMN
 Partie Observer : Ondes et matière CHAP 04-ACT/DOC Analyse spectrale : Spectroscopies IR et RMN Objectifs : Exploiter un spectre infrarouge pour déterminer des groupes caractéristiques Relier un spectre
Partie Observer : Ondes et matière CHAP 04-ACT/DOC Analyse spectrale : Spectroscopies IR et RMN Objectifs : Exploiter un spectre infrarouge pour déterminer des groupes caractéristiques Relier un spectre
MYCOTOXINES : changements règlementaires et analytiques
 MYCOTOXINES : changements règlementaires et analytiques E. MARENGUE ( LDA22 ) et S. HULOT ( IDAC ) PLAN 1) La problématique 2) Les évolutions règlementaires 3) L échantillonnage : étape clé 4) Les techniques
MYCOTOXINES : changements règlementaires et analytiques E. MARENGUE ( LDA22 ) et S. HULOT ( IDAC ) PLAN 1) La problématique 2) Les évolutions règlementaires 3) L échantillonnage : étape clé 4) Les techniques
SVE 222 & PCL-442. Fascicule de Travaux Pratiques
 SVE 222 & PCL-442 Fascicule de Travaux Pratiques 2014-2015 Institut Supérieur de l Education et de la Formation Continue Bassem Jamoussi & Radhouane Chakroun 1 Sommaire PCL 442/SVE222 - TP N 1 : Etude
SVE 222 & PCL-442 Fascicule de Travaux Pratiques 2014-2015 Institut Supérieur de l Education et de la Formation Continue Bassem Jamoussi & Radhouane Chakroun 1 Sommaire PCL 442/SVE222 - TP N 1 : Etude
N Y OU OÙ 1 Homophones grammaticaux de catégories différentes. ni n y ou où
 GRAMMATICAUX DE CATÉGORIES DIFFÉRENTES NI HOMOPHONES N Y OU OÙ 1 Homophones grammaticaux de catégories différentes ni n y ou où NI N Y ni : conjonction de coordination. ni est le pendant négatif de ou
GRAMMATICAUX DE CATÉGORIES DIFFÉRENTES NI HOMOPHONES N Y OU OÙ 1 Homophones grammaticaux de catégories différentes ni n y ou où NI N Y ni : conjonction de coordination. ni est le pendant négatif de ou
AMAMI Anaïs 3 C LORDEL Maryne. Les dons de cellules & de tissus.
 AMAMI Anaïs 3 C LORDEL Maryne Les dons de cellules & de tissus. Introduction : Une greffe (don) de cellules consiste à administrer à un patient dont un organe vital ne fonctionne plus correctement, une
AMAMI Anaïs 3 C LORDEL Maryne Les dons de cellules & de tissus. Introduction : Une greffe (don) de cellules consiste à administrer à un patient dont un organe vital ne fonctionne plus correctement, une
Démonstra*on du concept de détec*on
 Démonstra*on du concept de détec*on Enzyme Peroxydase de raifort (HRP) Chromogène (ABTS) Peroxyde d'hydrogène (H 2 O 2 ) Démonstra*on du concept de détec*on Enzyme Peroxydase de raifort (HRP) Chromogène
Démonstra*on du concept de détec*on Enzyme Peroxydase de raifort (HRP) Chromogène (ABTS) Peroxyde d'hydrogène (H 2 O 2 ) Démonstra*on du concept de détec*on Enzyme Peroxydase de raifort (HRP) Chromogène
Psoriasis & Sport. Pour un meilleur accès des personnes psoriasiques aux activités sportives. Qui le psoriasis touche-t-il?
 Psoriasis, let s sport together! Psoriasis & Sport Pour un meilleur accès des personnes psoriasiques aux activités sportives Qui le psoriasis touche-t-il? On estime que 2 à 3 % de la population belge est
Psoriasis, let s sport together! Psoriasis & Sport Pour un meilleur accès des personnes psoriasiques aux activités sportives Qui le psoriasis touche-t-il? On estime que 2 à 3 % de la population belge est
Observer : l'absence de noyau des hématies la petite taille des plaquettes la forme et la taille des noyaux (leucocytes) ACTIVITES ELEVES TS
 4.1 La réaction inflammatoire, un exemple de réponse innée 4.1.1 Les cellules de défense au microscope optique : Par l'observation d'une goutte de sang humain au microscope, repérer chaque type de cellule
4.1 La réaction inflammatoire, un exemple de réponse innée 4.1.1 Les cellules de défense au microscope optique : Par l'observation d'une goutte de sang humain au microscope, repérer chaque type de cellule
Les Infections Associées aux Soins
 Les Infections Associées aux Soins Dr Catherine Sartor EOH Conception Assistance Publique Hôpitaux de Marseille Ecole IFSI, Marseille, 12 septembre 2014 Définitions 2007 Infection Nosocomiale (IN) 1999
Les Infections Associées aux Soins Dr Catherine Sartor EOH Conception Assistance Publique Hôpitaux de Marseille Ecole IFSI, Marseille, 12 septembre 2014 Définitions 2007 Infection Nosocomiale (IN) 1999
STRUCTURE ET FONCTION DES PLURICELLULAIRES
 Plan de cours STRUCTURE ET FONCTION DES PLURICELLULAIRES 101-FYA-PT Pondération 3-1-2 Gilles Bourbonnais (C360) [email protected] Sciences de la Nature / PASC@L http://ici.cegep-ste-foy.qc.ca/profs/gbourbonnais/
Plan de cours STRUCTURE ET FONCTION DES PLURICELLULAIRES 101-FYA-PT Pondération 3-1-2 Gilles Bourbonnais (C360) [email protected] Sciences de la Nature / PASC@L http://ici.cegep-ste-foy.qc.ca/profs/gbourbonnais/
Liste des projets retenus en 2009
 Liste s projets retenus en 2009 Allocations doctorales pour l axe 1 (Environnement, Territoires et Agriculture) Directeur thèse projet d'accueil + adresse Ecole Doctorale 13 Marielle BOUIX et Théodore
Liste s projets retenus en 2009 Allocations doctorales pour l axe 1 (Environnement, Territoires et Agriculture) Directeur thèse projet d'accueil + adresse Ecole Doctorale 13 Marielle BOUIX et Théodore
L évidence écologique Une station d assainissement où il fait bon se
 PHYTOREM S.A. L évidence écologique Une station d assainissement où il fait bon se Le BAMBOU-ASSAINISSEMENT Le Procédé Sol EFFLUENTS EXPORTATION VERS LA TIGE Chaume ou tige Pollution organique et minérale
PHYTOREM S.A. L évidence écologique Une station d assainissement où il fait bon se Le BAMBOU-ASSAINISSEMENT Le Procédé Sol EFFLUENTS EXPORTATION VERS LA TIGE Chaume ou tige Pollution organique et minérale
