RESUME DES CARACTERISTIQUES DU PRODUIT
|
|
|
- Josselin Malenfant
- il y a 10 ans
- Total affichages :
Transcription
1 RESUME DES CARACTERISTIQUES DU PRODUIT spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 1/9
2 1. DENOMINATION DU MEDICAMENT Mitomycin-C Kyowa 2 mg, poudre pour solution injectable Mitomycin-C Kyowa 10 mg, poudre pour solution injectable Mitomycin-C Kyowa 20 mg, poudre pour solution intravésicale 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Mitomycin-C Kyowa 2 mg, 10 mg et 20 mg contiennent respectivement 2, 10 et 20 mg mitomycine par flacon. Pour la liste complète des excipients, voir rubrique FORME PHARMACEUTIQUE Poudre pour solution injectable Dose de 2 mg et 10 mg : destinée à l administration intraveineuse. Peut également être injectée par voie intra-artérielle et intravésicale. Poudre pour solution intravésicale Dose de 20 mg: uniquement par voie intravésicale. 4. DONNEES CLINIQUES 4.1 Indications thérapeutiques La Mitomycin-C Kyowa est recommandée dans divers types de cancers avancés, soit en combinaison avec d'autres cytostatiques, soit après échec de la thérapie primitive. En particulier, la Mitomycin-C Kyowa a été utilisée avec succès pour améliorer les symptômes subjectifs et objectifs dans les adénocarcinomes de l'estomac et du pancréas. Des résultats favorables ont été obtenus dans des cancers du sein et dans le cancer épidermoïde du col utérin bien que d'autres traitements ou d'autres associations soient habituellement préconisés. La Mitomycin-C Kyowa peut également être utile dans la prophylaxie des récidives et le traitement des tumeurs superficielles de la vessie ainsi que vis-à-vis des métastases hépatiques de cancers gastrointestinaux, dans le cancer pulmonaire, le cancer de la prostate et dans les cancers de la tête et du cou. 4.2 Posologie et mode d administration Mode d administration La Mitomycin-C Kyowa s'administre en milieu hospitalier : Dissoudre le contenu du flacon dans de l'eau pour préparations injectables, de solution physiologique à 0,9 % de chlorure sodique, ou de solution glucosée à 20 % à raison de : Posologie - 5 ml pour le flacon à 2 mg de Mitomycin-C Kyowa - 20 ml pour les flacons à 10 et 20 mg de Mitomycin-C Kyowa spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 2/9
3 Voie générale (Uniquement la dose de 2 mg et de 10 mg) La Mitomycin-C Kyowa est généralement administrée en injection intraveineuse, en prenant le plus grand soin de ne pas injecter en dehors de la veine, vu le risque de douleur et de nécrose locale. La dose usuelle se situe entre 6 et 12 mg/m 2, répétée à intervalles de 4 à 6 semaines suivant que d'autres cytostatiques sont ou non administrés en association, ou encore d'après le délai de récupération de la formule sanguine. Une posologie plus élevée peut être adoptée lorsque la Mitomycin-C Kyowa est utilisée seule. La dose sera adaptée selon l'âge et la condition physique du patient. Étant donné le caractère cumulatif de la dépression médullaire, les patients feront l'objet d'un bilan complet après chaque période de traitement et la dose sera réduite si des signes de toxicité se sont manifestés. Des doses supérieures à 20 mg/m 2 ne se sont pas montrées plus efficaces mais par contre plus toxiques que des doses plus faibles. Pour l'administration dans certains tissus spécifiquement, la Mitomycin-C Kyowa peut être également injectée par voie artérielle, notamment dans l'artère hépatique, ou dans les cavités pleurale et péritonéale. Instillations intravésicales (Dose de 2 mg, de 10 mg ou de 20 mg) Pour le traitement des tumeurs vésicales inaccessibles à la résection transuréthrale, la dose usuelle est de 30 à 40 mg en instillation intravésicale par voie urétrale 1 fois par semaine pendant 8 à 12 semaines, ou 1 fois par semaine pendant 4 semaines puis 1 fois par mois pendant 5 à 10 mois. Pour la prévention des récidives de tumeurs vésicales, la dose usuelle est de 20 à 40 mg en instillation intravésicale par voie urétrale 1 fois par semaine pendant 8 à 12 semaines. Dans l'un et l'autre cas, le produit doit être préalablement dissous selon la dose dans 20 à 60 ml d'eau distillée stérile, de solution physiologique saline ou de solution tampon-phosphate à ph 7,4. Population pédiatrique Voir rubrique Contre-indications - Hypersensibilité à la substance active ou à l un des excipients mentionnés à la rubrique L idiosyncrasie au produit lors d'un traitement antérieur. - Dépression médullaire importante, suite éventuellement à des traitements antérieurs. - Grossesse et lactation (voir plus loin à cette rubrique). Le dosage du 20 mg n est PAS adapté pour une utilisation par voie intraveineuse. 4.4 Mises en garde spéciales et précautions d emploi - Mitomycin-C Kyowa doit être administré avec précaution dans les cas suivants : patients atteints d un trouble de la fonction hépatique ou rénale, en raison de la manifestation potentiellement accentuée d effets indésirables ; patients atteints de dépression médullaire car l administration de Mitomycin-C Kyowa peut aggraver la dépression médullaire ; spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 3/9
4 patients atteints d une infection comme complication : l administration de Mitomycin-C Kyowa peut aggraver cette infection en raison d une dépression médullaire ; patients atteints de varicelle : des troubles systémiques mortels peuvent survenir. - La Mitomycin-C Kyowa doit être administrée sous la supervision d'un médecin expérimenté en chimiothérapie anticancéreuse et les patients doivent être suivis de très près lors de chaque période de traitement, en attachant une particulière attention à la formule sanguine, plaquettes comprises. Une nouvelle dose ne sera pas administrée tant que le nombre de leucocytes n'est pas revenu à 4.000/mm 3 et celui des plaquettes à /mm 3, au moins. - Les patients doivent être étroitement suivis au moyen d analyses de laboratoire fréquentes (analyses hématologiques, tests de fonction rénale et hépatique, etc.) car des effets indésirables graves tels qu une dépression médullaire peuvent se manifester. Si une anomalie est détectée, les mesures nécessaires (telles qu une diminution de la dose et l arrêt de l administration) doivent être appliquées. Mitomycin-C Kyowa doit être administré avec prudence car l utilisation prolongée de ce produit peut entraîner des effets indésirables pouvant se manifester de manière persistante. - Si l'affection continue à progresser après 2 périodes de traitement à la Mitomycin-C Kyowa, il y a lieu d arrêter ce dernier car les chances de réponse sont alors minimes. - Il convient d être particulièrement attentif à l apparition ou l aggravation éventuelle de maladies infectieuses et d hémorragies. - Il convient de prendre des précautions en cas d apparition éventuelle d une leucémie aiguë ou d un syndrome myélodysplasique (SMD) chez les patients qui ont été traités avec Mitomycin-C Kyowa en association avec d autres agents antinéoplasiques (voir aussi rubrique 4.5). - Mitomycin-C Kyowa doit être administré avec prudence aux enfants, chez lesquels il convient d être particulièrement attentif à l apparition d effets indésirables. L innocuité de Mitomycin-C Kyowa chez les bébés immatures, les nouveau-nés, les jeunes enfants et les enfants n a pas été confirmée. - Mitomycin-C Kyowa doit être administré avec prudence aux personnes âgées car celles-ci présentent souvent une diminution des fonctions physiologiques, une dépression médullaire (potentiellement persistante) et des troubles rénaux. Il convient de surveiller étroitement la condition du patient et d être particulièrement attentif à la dose et à l intervalle d administration. - Si l administration de Mitomycin-C Kyowa s avère nécessaire chez des enfants ou chez des patients en âge de procréer, il convient d évaluer l effet potentiel sur les gonades. L'effet de la Mitomycin-C Kyowa sur la fertilité est inconnu. - L'INJECTION INTRAVEINEUSE DE MITOMYCIN-C KYOWA DOIT ETRE PRATIQUEE AVEC LE PLUS GRAND SOIN POUR EVITER TOUTE EXTRAVASATION SUSCEPTIBLE DE PROVOQUER UNE ULCERATION LOCALE. EVITER EGALEMENT TOUT CONTACT AVEC LA PEAU ET LES YEUX. - Étant donné que l administration intraveineuse peut provoquer phlébite, thrombus, induration du site d injection, nécrose et douleur vasculaire, il faut injecter Mitomycin-C Kyowa le plus lentement possible et être extrêmement attentif au site et au mode d administration. - Une fuite extravasculaire du médicament en solution peut entraîner une induration tissulaire ou une nécrose du site d injection. C est pourquoi Mitomycin-C Kyowa doit être injecté avec prudence afin d éviter la fuite extravasculaire de la solution. spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 4/9
5 - L administration intra-artérielle peut provoquer des problèmes cutanés tels qu ulcère, induration tissulaire, douleur, rougeur, érythème, ampoules et érosion du tissu avoisinant se soldant éventuellement par une nécrose cutanée/musculaire. Si l un de ces symptômes se manifeste, il faut arrêter l administration et prendre les mesures qui s imposent. Des cas particuliers de trouble hépatique parenchymateux, bilome, cholangite (également sclérosante) et de nécrose du canal biliaire peuvent également se manifester après administration de Mitomycin-C Kyowa via l artère hépatique. - L afflux de Mitomycin-C Kyowa en solution vers d autres sites situés à proximité du site visé, lors d une administration artérielle hépatique, peut engendrer ulcération, hémorragie, perforations gastroduodénales. C est pourquoi la localisation de l extrémité du cathéter ainsi que la zone de distribution doivent être confirmées par radiographie ou par d autres moyens et il faut être attentif à une anomalie ou un déplacement éventuel du cathéter et à la vitesse de diffusion. Si l un de ces symptômes se développe, il faut arrêter l administration et prendre les mesures qui s imposent. - L administration intravésicale peut entraîner une calcinose, des contractions vésicales et une cystite associée à une dysurie et une pollakiurie, une perforation vésicale, une nécrose vésicale et pénienne. C est pourquoi il faut injecter Mitomycin-C Kyowa avec prudence. - Il est recommandé d utiliser la solution le plus rapidement possible après reconstitution parce que la puissance de Mitomycin-C Kyowa peut être réduite lorsqu une solution à faible ph a été utilisée comme liquide de reconstitution. En outre, il est déconseillé de mélanger ce médicament avec d autres solutions injectables à faible ph. - En cas de contact avec la peau, laver plusieurs fois avec de l'eau bicarbonatée puis éventuellement avec de l'eau. Pour ce qui est des yeux, laver aussi avec de l'eau bicarbonatée et surveiller la cornée plusieurs jours consécutivement pour dépister à temps une lésion cornéenne. - L apparition de divers types de tumeurs a été rapportée dans le cadre d expérimentations animales lors d une administration sous-cutanée chez la souris et lors d une administration intrapéritonéale ou intraveineuse chez le rat. 4.5 Interactions avec d autres médicaments et autres formes d interactions Une interaction potentielle de Mitomycin-C Kyowa avec d autres agents antinéoplasiques tels que la bléomycine et l adriamycine et avec la radiothérapie n est pas exclue (voir rubrique 4.8). Dans ce cas, les effets indésirables tels que la dépression médullaire peuvent se manifester de manière accentuée. Un essoufflement et un bronchospasme très grave ont parfois été observés lors de l administration de vinca-alcaloïdes, comme par exemple la vinblastine, et d autres agents antinéoplasiques tels que le sulfate de vindésine, chez des patients ayant reçu antérieurement de la mitomycine. 4.6 Fécondité, grossesse et allaitement Il est déconseillé d administrer Mitomycin-C Kyowa aux femmes (potentiellement) enceintes. Lors d expérimentations animales avec des souris, des effets tératogènes ont été observés tels qu une inhibition du développement, des becs-de-lièvre, une hypoplasie de la queue, une hypoplasie de la mâchoire, une ectrodactylie, etc. Les femmes allaitantes doivent interrompre l allaitement pendant la durée du traitement. L innocuité de Mitomycin-C Kyowa chez les femmes allaitantes n a pas été prouvée. 4.7 Effets sur l aptitude à conduire des véhicules et à utiliser des machines spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 5/9
6 Aucune étude n a été réalisée quant aux effets sur l aptitude à conduire un véhicule et à utiliser des machines. 4.8 Effets indésirables Infections et infestations parasitaires : Infections bactériennes, virales ou fongiques légères à modérées à différentes localisations et généralement réversibles avec un traitement approprié. Des cas de sepsis et de choc septique ont été rapportés. Tumeurs bénignes, malignes et non précisées : Syndrome myélodysplasique, leucémie myéloïde aiguë, leucémie aiguë Affections hématologiques et du système lymphatique : La toxicité principale de la Mitomycin-C Kyowa consiste en une dépression médullaire, thrombocytopénie et leucopénie en particulier. Le nadir se situe généralement aux environs de 4 semaines après le traitement; la toxicité est cumulative et comporte un risque croissant après chaque période d'administration. Une anémie hémolytique avec microangiopathie et un syndrome hémolytique-urémique ont été occasionnellement rapportés. Les patients doivent être observés méticuleusement au moyen de tests périodiques. Des mesures adaptées, comme l'arrêt du traitement, doivent être prises si des symptômes tels qu'une anémie avec érythrocytes fragmentés, thrombocytopénie et troubles de la fonction rénale sont constatés. Une pancytopénie, une neutropénie, une granulocytopénie, une neutropénie associée à de la fièvre, une érythropénie, une anémie, un purpura thrombotique thrombocytopénique et des hémorragies peuvent également se manifester. Les patients doivent être observés méticuleusement au moyen de tests périodiques. Des mesures adaptées, comme une réduction de la dose ou l'arrêt de l'administration, doivent être prises en cas d'apparition éventuelle de symptômes anormaux. Affections du système immunitaire : Démangeaison, éruption cutanée, rougeur, hypersensibilité, choc anaphylactique, réaction anaphylactoïde, éosinophilie, sudation, hypotension, dyspnée. Ces symptômes exigent l'arrêt immédiat du traitement et la prise de mesures adaptées. Troubles du métabolisme et de la nutrition : Anorexie, perte de poids. Affections vasculaires : De très rares cas d'hypertension ont été observés. Flush. Affections respiratoires et médiastinales : Toux, pneumonie interstitielle, caractérisée au début par de la dyspnée et une toux non productive, sont également des effets indésirables possible; une aggravation d'une cardiopathie induite par les anthracyclines et de la pneumonie interstitielle à la bléomycine peut se rencontrer. Une fibrose pulmonaire, un bronchospasme et une pneumonite peuvent également se manifester. Ces symptômes exigent un arrêt du traitement et la prise de mesures adaptées, comme l'administration d'hormone corticosurrénale. Affections gastro-intestinales : Des nausées et des vomissements sont parfois ressentis après le traitement mais ils sont en général légers et de brève durée. Une diarrhée, une constipation, un inconfort abdominal et une stomatite peuvent également se manifester. spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 6/9
7 Affections hépatobiliaires : Des troubles hépatiques parenchymateux, une cholécystite, une nécrose du canal biliaire et un ictère peuvent se manifester. La distribution du médicament dans le corps doit être confirmée photographiquement ou d'une autre façon. Des symptômes éventuellement anormaux exigent par ailleurs un arrêt du traitement et la prise de mesures adaptées. L injection dans l artère hépatique peut entraîner une atteinte hépatique et des voies biliaires. Affections de la peau et du tissu sous-cutané : Une coloration des ongles, des réactions cutanées et de l'alopécie ont été sporadiquement décrites. Des éruptions cutanées, un érythème et un prurit peuvent également apparaître. Affections du rein et des voies urinaires : Une toxicité rénale sévère a été occasionnellement rapportée après traitement; c'est pourquoi la fonction rénale doit être contrôlée au départ et après chaque période d'administration. De la cystite a également été rapportée après administration intravésicale. Une insuffisance rénale aiguë, des troubles rénaux, une hématurie, des contractions de la vessie et une protéinurie peuvent se manifester. Les patients doivent être observés méticuleusement au moyen de tests périodiques. Des mesures adaptées, comme l'arrêt du traitement, doivent être prises en cas de modification anormale éventuelle du taux de BUN (azote uréique sanguin), de créatinine, de clairance de la créatinine, etc. Troubles généraux et anomalies au site d administration : De la fièvre (frissons fébriles), un malaise, une phlébite au niveau du site d injection et un œdème peuvent apparaître. Une ulcération locale et de la cellulite peuvent être provoquées par l'extravasation du produit dans les tissus lors de l'injection intraveineuse. Déclaration des effets indésirables suspectés La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration: Belgique Agence fédérale des médicaments et des produits de santé Division Vigilance EUROSTATION II Place Victor Horta, 40/ 40 B-1060 Bruxelles Site internet: [email protected] Luxembourg Direction de la Santé Division de la Pharmacie et des Médicaments Villa Louvigny Allée Marconi L-2120 Luxembourg Site internet: Surdosage S'attendre à une inhibition complète de l'hématopoïèse : anémie aplastique, thrombocytopénie, agranulocytose. Instaurer le traitement dans une unité de soins intensifs en milieu stérile. 5. PROPRIETES PHARMACOLOGIQUES spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 7/9
8 5.1 Propriétés pharmacodynamiques Classe pharmacothérapeutique : antibiotique cytotoxique, code ATC: L01D C03. La Mitomycin-C Kyowa est un antibiotique antitumoral, antimitotique et cytostatique, produit par un actinomycète dénommé Streptomyces caespitosus. La Mitomycin-C Kyowa décompose l'acide désoxyribonucléique (ADN) des cellules cancéreuses en formant un complexe avec lui; d'autre part, elle inhibe la division des cellules tumorales en interférant dans la biosynthèse de l'adn. Par ces propriétés, la Mitomycin-C Kyowa se comporte comme un agent alkylant. 5.2 Propriétés pharmacocinétiques La Mitomycin-C Kyowa disparaît rapidement du sérum après administration intraveineuse; le temps nécessaire pour réduire de 50 % la concentration sérique après une injection en embol de 30 mg de Mitomycin-C Kyowa est de 17 minutes. Après injection intraveineuse de 30 mg, 20 mg ou 10 mg, les concentrations sériques maximales ont été respectivement de 2,4 µg/ml; 1,7 µg/ml et 0,52 µg/ml. La clairance de la Mitomycin-C Kyowa dépend principalement de sa transformation métabolique dans le foie, mais aussi dans d'autres tissus. La vitesse de diminution des concentrations plasmatiques est inversement proportionnelle à la concentration plasmatique maximale, probablement par suite d'une saturation des mécanismes de biodégradation. Approximativement 10 % de la dose de Mitomycin-C Kyowa sont excrétés inchangés dans les urines. Comme les voies de dégradation métabolique sont saturées par des doses relativement faibles du produit, le pourcentage de Mitomycin-C Kyowa éliminée dans l'urine augmente avec la dose. L'excrétion de la Mitomycin-C Kyowa est similaire chez l'enfant. 6. DONNEES PHARMACEUTIQUES 6.1 Liste des excipients Mitomycin-C Kyowa 2mg, 10mg et 20mg contiennent respectivement 48, 240 et 480 mg de chlorure de sodium par flacon. 6.2 Incompatibilités Sans objet. 6.3 Durée de conservation Mitomycin-C Kyowa 2 mg: 4 ans Mitomycin-C Kyowa 10 mg: 4 ans Mitomycin-C Kyowa 20 mg: 3 ans 6.4 Précautions particulières de conservation Conserver à température ambiante (15 à 25 C). Remarques concernant la conservation de la Mitomycin-C Kyowa après sa mise en solution: spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 8/9
9 - Les solutions de Mitomycin-C préparées à l'aide d'eau pour préparations injectables (pour administration par voie parentérale ou en instillation intravésicale) ou de tampon phosphate ph 7,4 (pour administration en instillation intravésicale) peuvent être conservées à la température ambiante pour autant que la concentration ne dépasse pas 0,8 mg/ml et ce au maximum pendant 5 jours. Les solutions dont les concentrations de Mitomycin-C Kyowa dépassent 0,8 mg/ml doivent être utilisées extemporanément. - Les solutions préparées à l'aide d'eau pour préparations injectables peuvent être conservées au réfrigérateur pour autant que la concentration n'en dépasse pas 0,6 mg/ml, et au maximum pendant 5 jours. La conservation de solutions préparées à l'aide de tampon phosphate ph 7,4 au réfrigérateur est déconseillée en raison du risque de précipitation. - Les solutions préparées à l'aide d'une solution physiologique à 0,9 % de chlorure sodique ou d'une solution glucosée sont à utiliser extemporanément. 6.5 Nature et contenu de l emballage extérieur Emballages de : - 10 flacons à 2 mg - 3 flacons à 10 mg - 2 flacons à 20 mg 6.6 Précautions particulières d élimination et manipulation Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur. 7. TITULAIRE DE L AUTORISATION DE MISE SUR LE MARCHE Takeda Belgium Chaussée de Gand Bruxelles 8. NUMEROS D AUTORISATION DE MISE SUR LE MARCHE Mitomycin-C Kyowa 2 mg: BE Mitomycin-C Kyowa 10 mg: BE Mitomycin-C Kyowa 20 mg: BE DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L AUTORISATION Date de première autorisation: 20/06/1961 Date de dernier renouvellement: 24/12/ DATE DE MISE A JOUR DU TEXTE 12/2014 Date d approbation : 01/2015 spc-market-fr-mitomycin-c-kyowa-dec14-apprjan15.docx 9/9
NOTICE : INFORMATIONS DU PATIENT. Keforal 500 mg comprimés pelliculés. Céfalexine monohydratée
 NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE
 Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Par fiole: L - asparaginase 10.000 U.I. Pour les excipients, cfr section 6.1. 3.
Résumé des Caractéristiques du Produit 1. DENOMINATION DU MEDICAMENT PARONAL 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Par fiole: L - asparaginase 10.000 U.I. Pour les excipients, cfr section 6.1. 3.
NOTICE : INFORMATION DE L'UTILISATEUR. DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc
 NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
NOTICE: INFORMATION DE L UTILISATEUR. Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain)
 NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral intramusculaire
 ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013
 NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
NOTICE : INFORMATION DE L UTILISATEUR. Delphi 0,1 % crème Acétonide de triamcinolone
 NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
French Version. Aciclovir Labatec 250 mg (For Intravenous Use Only) 02/2010. Product Information Leaflet for Aciclovir Labatec i.v.
 Product Information Leaflet for Aciclovir Labatec i.v. 250 mg French Version Aciclovir Labatec i.v. Composition Principe actif: Aciclovirum ut Acicloviri natricum (Praeparatio cryodesiccata). Excipients:
Product Information Leaflet for Aciclovir Labatec i.v. 250 mg French Version Aciclovir Labatec i.v. Composition Principe actif: Aciclovirum ut Acicloviri natricum (Praeparatio cryodesiccata). Excipients:
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT. Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl par comprimé enrobé.
 RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1. Dé nomination du mé dicame nt Bisolax 5 mg comprimés enrobés. 2. Composition qualitative e t quantitative Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1. Dé nomination du mé dicame nt Bisolax 5 mg comprimés enrobés. 2. Composition qualitative e t quantitative Bisolax 5 mg comprimés enrobés contient 5 mg de bisacodyl
COMMISSION DE LA TRANSPARENCE. Avis. 23 mai 2007
 COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
PIL Décembre 2009. Autres composants: acide tartrique, macrogol 4000, macrogol 1000, macrogol 400, butylhydroxyanisol.
 Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE
 L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE NEUCHATEL, Suisse, 7 avril/prnewswire/ -- - LA LENALIDOMIDE est évaluée par l EMEA comme thérapie orale pour
L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE NEUCHATEL, Suisse, 7 avril/prnewswire/ -- - LA LENALIDOMIDE est évaluée par l EMEA comme thérapie orale pour
Leucémies de l enfant et de l adolescent
 Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Information transmise sous l autorité de l Agence fédérale des médicaments et des produits de santé
 Les Direct Healthcare Professional Communications (DHPC) sont des courriers envoyés aux professionnels de la santé par les firmes pharmaceutiques, afin de les informer de risques potentiels apparus lors
Les Direct Healthcare Professional Communications (DHPC) sont des courriers envoyés aux professionnels de la santé par les firmes pharmaceutiques, afin de les informer de risques potentiels apparus lors
E04a - Héparines de bas poids moléculaire
 E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MÉDICAMENT Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Interféron
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MÉDICAMENT Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Interféron
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION. 10 octobre 2001
 COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
Notice publique PERDOLAN - PÉDIATRIE
 Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER
 ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER Dr Michael Hummelsberger, Pr Jean-Gabriel Fuzibet, Service de Médecine Interne, Hôpital l Archet, CHU Nice 1. ANEMIE L étiologie de l anémie
ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER Dr Michael Hummelsberger, Pr Jean-Gabriel Fuzibet, Service de Médecine Interne, Hôpital l Archet, CHU Nice 1. ANEMIE L étiologie de l anémie
COMMISSION DE LA TRANSPARENCE. Avis. 3 septembre 2008
 COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine
 KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
1 - Que faut-il retenir sur les anticoagulants oraux?
 La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR. Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant
 B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES :
 FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
 ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 1. DÉNOMINATION DU MÉDICAMENT Extavia 250 microgrammes/ml, poudre et solvant pour solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Un flacon
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 1. DÉNOMINATION DU MÉDICAMENT Extavia 250 microgrammes/ml, poudre et solvant pour solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Un flacon
L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ
 L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ Plan de la présentation Introduction L enfant Le cathéter court La voie veineuse centrale La voie intra-osseuse Plan de la présentation Le
L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ Plan de la présentation Introduction L enfant Le cathéter court La voie veineuse centrale La voie intra-osseuse Plan de la présentation Le
Protéger. son animal. la gamme FRONTLINE. grâce à la gamme. Contre les puces et les tiques. Efficace plusieurs semaines (1) Résistant à la pluie,
 la gamme Frontline Contre les puces et les tiques Efficace plusieurs semaines (1) Résistant à la pluie, aux bains et aux shampooings (2) Protéger son animal grâce à la gamme FRONTLINE La gamme FRONTLINE
la gamme Frontline Contre les puces et les tiques Efficace plusieurs semaines (1) Résistant à la pluie, aux bains et aux shampooings (2) Protéger son animal grâce à la gamme FRONTLINE La gamme FRONTLINE
E03 - Héparines non fractionnées (HNF)
 E03-1 E03 - Héparines non fractionnées (HNF) Les héparines sont des anticoagulants agissant par voie parentérale. 1. Modalités d u tilisation Mode d action : l héparine est un cofacteur de l antithrombine
E03-1 E03 - Héparines non fractionnées (HNF) Les héparines sont des anticoagulants agissant par voie parentérale. 1. Modalités d u tilisation Mode d action : l héparine est un cofacteur de l antithrombine
Le don de moelle osseuse :
 DON DE MOELLE OSSEUSE Le don de moelle osseuse : se décider aujourd hui, s engager pour longtemps LA MOELLE OSSEUSE ET SA GREFFE La moelle osseuse C est le tissu mou dans le centre du corps des os qui
DON DE MOELLE OSSEUSE Le don de moelle osseuse : se décider aujourd hui, s engager pour longtemps LA MOELLE OSSEUSE ET SA GREFFE La moelle osseuse C est le tissu mou dans le centre du corps des os qui
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
INFORMATIONS AUX PATIENTS ATTEINTS DE LEUCEMIE AIGUE MYELOBLASTIQUE
 Livret LAM page 1 INFORMATIONS AUX PATIENTS ATTEINTS DE LEUCEMIE AIGUE MYELOBLASTIQUE Dans certains cas les symptômes et le traitement peuvent différer de ce que y est présenté dans ce livret. A tout moment
Livret LAM page 1 INFORMATIONS AUX PATIENTS ATTEINTS DE LEUCEMIE AIGUE MYELOBLASTIQUE Dans certains cas les symptômes et le traitement peuvent différer de ce que y est présenté dans ce livret. A tout moment
NOTICE : INFORMATION DE L UTILISATEUR. Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants. Acide acétylsalicylique
 NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
Observation. Merci à l équipe de pharmaciens FormUtip iatro pour ce cas
 Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Insuffisance rénale. Définition. o Insuffisance rénale aiguë
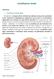 Insuffisance rénale Définition o Insuffisance rénale aiguë Se traduit par un brusque arrêt de la filtration des déchets du sang et de la production d urine. Associée à un déséquilibre de l organisme en
Insuffisance rénale Définition o Insuffisance rénale aiguë Se traduit par un brusque arrêt de la filtration des déchets du sang et de la production d urine. Associée à un déséquilibre de l organisme en
COMMISSION DE LA TRANSPARENCE AVIS. 10 mai 2006
 COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
Humira Solution pour injection dans un injecteur prérempli
 Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre
NOTICE : INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés Bisacodyl
 NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène
 NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
Stelara (ustekinumab)
 Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
Notice : information de l utilisateur. Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine
 Notice : information de l utilisateur Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine Veuillez lire attentivement cette notice avant de prendre ce médicament
Notice : information de l utilisateur Vesicare 5 mg, comprimés pelliculés Vesicare 10 mg, comprimés pelliculés succinate de solifénacine Veuillez lire attentivement cette notice avant de prendre ce médicament
Principales causes de décès selon le groupe d âge. 0 24 25 44 45 64 65 84 85 et plus
 Module 2 Exercice 1: Cellules souches hématopoïétiques 1. Causes de décès en Suisse (2010) La figure suivante montre les causes de décès les plus fréquentes en Suisse en 2010, telles qu elles ont été relevées
Module 2 Exercice 1: Cellules souches hématopoïétiques 1. Causes de décès en Suisse (2010) La figure suivante montre les causes de décès les plus fréquentes en Suisse en 2010, telles qu elles ont été relevées
Notice : Informations de l utilisateur. Pantomed 20 mg comprimés gastro-résistants. Pantoprazole
 Notice : Informations de l utilisateur Pantomed 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations
Notice : Informations de l utilisateur Pantomed 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations
Thérapeutique anti-vhc et travail maritime. O. Farret HIA Bégin
 Thérapeutique anti-vhc et travail maritime O. Farret HIA Bégin Introduction «L hépatite C est une maladie le plus souvent mineure, mais potentiellement cancérigène, qu on peut ne pas traiter et surveiller
Thérapeutique anti-vhc et travail maritime O. Farret HIA Bégin Introduction «L hépatite C est une maladie le plus souvent mineure, mais potentiellement cancérigène, qu on peut ne pas traiter et surveiller
MONOGRAPHIE. tocilizumab. Solution concentrée à 20 mg/ml pour perfusion. Solution à 162 mg/0,9 ml pour injection. Norme reconnue
 MONOGRAPHIE Pr ACTEMRA tocilizumab Solution concentrée à 20 mg/ml pour perfusion Solution à 162 mg/0,9 ml pour injection Norme reconnue Inhibiteur du récepteur d interleukine Le traitement par ACTEMRA
MONOGRAPHIE Pr ACTEMRA tocilizumab Solution concentrée à 20 mg/ml pour perfusion Solution à 162 mg/0,9 ml pour injection Norme reconnue Inhibiteur du récepteur d interleukine Le traitement par ACTEMRA
NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine
 NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament.
XARELTO (RIVAROXABAN) 2,5 MG - 15 MG - 20 MG, COMPRIMÉS PELLICULÉS GUIDE DE PRESCRIPTION
 Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament Xarelto 2,5 mg; 15 mg et 20 mg de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique
Les autorités de santé de l Union Européenne ont assorti la mise sur le marché du médicament Xarelto 2,5 mg; 15 mg et 20 mg de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique
COMMISSION DE LA TRANSPARENCE AVIS. 18 janvier 2006
 COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
NOTICE : INFORMATION DE L UTILISATEUR. Flunarizine
 NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI. http://www.infectiologie.org.tn
 HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI LES MOYENS THERAPEUTIQUES Les interférons La ribavirine Les nouveaux produits INTERFERONS 1957: activité antivirale Interférence
HVC CHRONIQUE MOYENS THERAPEUTIQUES ET BILAN PRE-THERAPEUTIQUE CHAKIB MARRAKCHI LES MOYENS THERAPEUTIQUES Les interférons La ribavirine Les nouveaux produits INTERFERONS 1957: activité antivirale Interférence
Professeur Diane GODIN-RIBUOT
 UE3-2 - Physiologie rénale Chapitre 5 : Mesure de la fonction rénale : la clairance rénale Professeur Diane GODIN-RIBUOT Année universitaire 2011/2012 Université Joseph Fourier de Grenoble - Tous droits
UE3-2 - Physiologie rénale Chapitre 5 : Mesure de la fonction rénale : la clairance rénale Professeur Diane GODIN-RIBUOT Année universitaire 2011/2012 Université Joseph Fourier de Grenoble - Tous droits
Bien vous soigner. avec des médicaments disponibles sans ordonnance. juin 2008. Douleur. de l adulte
 Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
Votre guide des définitions des maladies graves de l Assurance maladies graves express
 Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
Notice : information de l utilisateur
 Notice : information de l utilisateur ALIMTA 100 mg poudre pour solution à diluer pour perfusion ALIMTA 500 mg poudre pour solution à diluer pour perfusion Pemetrexed Veuillez lire attentivement l'intégralité
Notice : information de l utilisateur ALIMTA 100 mg poudre pour solution à diluer pour perfusion ALIMTA 500 mg poudre pour solution à diluer pour perfusion Pemetrexed Veuillez lire attentivement l'intégralité
Le traitement du paludisme d importation de l enfant est une urgence
 Le traitement du paludisme d importation de l enfant est une urgence Dominique GENDREL Necker-Enfants Malades Traiter en urgence en présence de trophozoïtes Plus de 80% des paludismes d importation en
Le traitement du paludisme d importation de l enfant est une urgence Dominique GENDREL Necker-Enfants Malades Traiter en urgence en présence de trophozoïtes Plus de 80% des paludismes d importation en
NOTICE: INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés. Bisacodyl
 NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
L'œsophage L'œsophage est un tube musculaire qui traverse de la bouche à l'estomac. Causes
 L'œsophage est un tube musculaire qui traverse de la bouche à l'estomac. Chez l'adulte moyen, il fait 25 cm à 30 cm (10 po à 14 po) de long et environ 2 cm (moins d'un pouce) de large. L'œsophage est constitué
L'œsophage est un tube musculaire qui traverse de la bouche à l'estomac. Chez l'adulte moyen, il fait 25 cm à 30 cm (10 po à 14 po) de long et environ 2 cm (moins d'un pouce) de large. L'œsophage est constitué
NOTICE: INFORMATION DE L UTILISATEUR
 NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
Carte de soins et d urgence
 Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
MONOGRAPHIE. Pr PEGASYS. peginterféron alfa-2a injectable. Seringues préremplies : 180 µg/0,5 ml. Flacons à usage unique : 180 µg/1 ml
 MONOGRAPHIE Pr PEGASYS peginterféron alfa2a injectable Seringues préremplies : 180 µg/0,5 ml Flacons à usage unique : 180 µg/1 ml Autoinjecteur ProClick : 180 µg/0,5 ml Modificateur de la réponse biologique
MONOGRAPHIE Pr PEGASYS peginterféron alfa2a injectable Seringues préremplies : 180 µg/0,5 ml Flacons à usage unique : 180 µg/1 ml Autoinjecteur ProClick : 180 µg/0,5 ml Modificateur de la réponse biologique
Infections urinaires chez l enfant
 Infections urinaires chez l enfant Questions et réponses pour diminuer vos inquiétudes Chers parents, Cette brochure a pour but de faciliter votre compréhension et de diminuer vos inquiétudes en vous
Infections urinaires chez l enfant Questions et réponses pour diminuer vos inquiétudes Chers parents, Cette brochure a pour but de faciliter votre compréhension et de diminuer vos inquiétudes en vous
1 of 5 02/11/2012 14:03
 1 of 5 02/11/2012 14:03 Le cancer du chat par Sandrine Cayet, docteur-vétérinaire Le cancer chez le chat n est pas une fatalité. Un cancer chez le chat, c est comme chez l homme, ça se diagnostique, ça
1 of 5 02/11/2012 14:03 Le cancer du chat par Sandrine Cayet, docteur-vétérinaire Le cancer chez le chat n est pas une fatalité. Un cancer chez le chat, c est comme chez l homme, ça se diagnostique, ça
MONOGRAPHIE DE PRODUIT
 MONOGRAPHIE DE PRODUIT Pr Aranesp MD (darbépoétine alfa) Fioles unidoses (15, 25, 40, 60, 100, 200, 325 et 500 µg/fiole) Seringues préremplies SingleJect MD (10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150,
MONOGRAPHIE DE PRODUIT Pr Aranesp MD (darbépoétine alfa) Fioles unidoses (15, 25, 40, 60, 100, 200, 325 et 500 µg/fiole) Seringues préremplies SingleJect MD (10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150,
Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic de cancer
 Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DÉNOMINATION DU MÉDICAMENT AVONEX 30 microgrammes poudre et solvant pour solution injectable 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque flacon
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DÉNOMINATION DU MÉDICAMENT AVONEX 30 microgrammes poudre et solvant pour solution injectable 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque flacon
INFORMATION & PRÉVENTION. Le cancer de la vessie
 INFORMATION & PRÉVENTION Le cancer de la vessie G R A N D P U B L I C Ce à quoi sert la vessie La vessie est une poche qui reçoit l urine produite par les reins, via les uretères*. Elle est constituée
INFORMATION & PRÉVENTION Le cancer de la vessie G R A N D P U B L I C Ce à quoi sert la vessie La vessie est une poche qui reçoit l urine produite par les reins, via les uretères*. Elle est constituée
DÉFICITS IMMUNITAIRE COMMUN VARIABLE
 DÉFICITS IMMUNITAIRE COMMUN VARIABLE Le présent livret a été rédigé à l attention des patients et de leurs familles. Il ne doit pas remplacer les conseils d un spécialiste en immunologie. 1 Egalement Disponible
DÉFICITS IMMUNITAIRE COMMUN VARIABLE Le présent livret a été rédigé à l attention des patients et de leurs familles. Il ne doit pas remplacer les conseils d un spécialiste en immunologie. 1 Egalement Disponible
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
 ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 Ce médicament fait l objet d une surveillance supplémentaire qui permettra l identification rapide de nouvelles informations relatives à la sécurité. Les
ANNEXE I RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT 1 Ce médicament fait l objet d une surveillance supplémentaire qui permettra l identification rapide de nouvelles informations relatives à la sécurité. Les
AMAMI Anaïs 3 C LORDEL Maryne. Les dons de cellules & de tissus.
 AMAMI Anaïs 3 C LORDEL Maryne Les dons de cellules & de tissus. Introduction : Une greffe (don) de cellules consiste à administrer à un patient dont un organe vital ne fonctionne plus correctement, une
AMAMI Anaïs 3 C LORDEL Maryne Les dons de cellules & de tissus. Introduction : Une greffe (don) de cellules consiste à administrer à un patient dont un organe vital ne fonctionne plus correctement, une
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT 2. COMPOSITION QUALITATIVE ET QUANTITATIVE 3. FORME PHARMACEUTIQUE 4. DONNEES CLINIQUES 4.1. Indications thérapeutiques 4.2.
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT 2. COMPOSITION QUALITATIVE ET QUANTITATIVE 3. FORME PHARMACEUTIQUE 4. DONNEES CLINIQUES 4.1. Indications thérapeutiques 4.2.
Bijsluiter FR versie Collier Propoxur Halsband B. NOTICE 1/5
 B. NOTICE 1/5 NOTICE COLLIER PROPOXUR HALSBAND pour chiens de petite taille et chats COLLIER PROPOXUR HALSBAND pour chiens de grande et moyenne taille 1. NOM ET ADRESSE DU TITULAIRE DE L AUTORISATION DE
B. NOTICE 1/5 NOTICE COLLIER PROPOXUR HALSBAND pour chiens de petite taille et chats COLLIER PROPOXUR HALSBAND pour chiens de grande et moyenne taille 1. NOM ET ADRESSE DU TITULAIRE DE L AUTORISATION DE
Information à un nouveau donneur de cellules souches du sang
 Information à un nouveau donneur de cellules souches du sang Pour des raisons de simplification, les dénominations masculines s appliquent également aux femmes. La transplantation de cellules souches du
Information à un nouveau donneur de cellules souches du sang Pour des raisons de simplification, les dénominations masculines s appliquent également aux femmes. La transplantation de cellules souches du
Atrovent HFA 20 mcg/bouffée solution pour inhalation en flacon pressurisé (bromure d'ipratropium)
 NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
Etablissement Français du Sang
 Etablissement Français du Sang LE LIEN ENTRE LA GÉNÉROSITÉ DES DONNEURS DE SANG ET LES BESOINS DES MALADES Document de préparation à l entretien médical préalable au don de sang Partie médicale La sécurité
Etablissement Français du Sang LE LIEN ENTRE LA GÉNÉROSITÉ DES DONNEURS DE SANG ET LES BESOINS DES MALADES Document de préparation à l entretien médical préalable au don de sang Partie médicale La sécurité
Carnet de suivi Lithium
 Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
NOTICE. DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine
 NOTICE ANSM Mis à jour le : 08/06/2010 Dénomination du médicament DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine Encadré Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE ANSM Mis à jour le : 08/06/2010 Dénomination du médicament DEBRICALM 100 mg, comprimé pelliculé Maléate de trimébutine Encadré Veuillez lire attentivement cette notice avant de prendre ce médicament.
Protégeons-nous ensemble!
 Grippe saisonnière. Protégeons-nous ensemble! Informations importantes pour vous et votre famille. www.sevaccinercontrelagrippe.ch www.ofsp.admin.ch B C Qu est-ce que la grippe saisonnière et quels en
Grippe saisonnière. Protégeons-nous ensemble! Informations importantes pour vous et votre famille. www.sevaccinercontrelagrippe.ch www.ofsp.admin.ch B C Qu est-ce que la grippe saisonnière et quels en
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MEDICAMENT Osigraft 3,3 mg poudre pour suspension implantable 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque flacon contient 3,3
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MEDICAMENT Osigraft 3,3 mg poudre pour suspension implantable 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque flacon contient 3,3
NOTICE. ANSM - Mis à jour le : 25/03/2014. Dénomination du médicament. PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole
 NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
Don de moelle osseuse. pour. la vie. Agence relevant du ministère de la santé. Agence relevant du ministère de la santé
 Don de moelle osseuse Engagez-VOUS pour la vie 1 Pourquoi devenir veilleur de vie? Le don de moelle osseuse peut sauver des vies La greffe de moelle osseuse représente une chance importante de guérison
Don de moelle osseuse Engagez-VOUS pour la vie 1 Pourquoi devenir veilleur de vie? Le don de moelle osseuse peut sauver des vies La greffe de moelle osseuse représente une chance importante de guérison
HEPATITES VIRALES 22/09/09. Infectieux. Mme Daumas
 HEPATITES VIRALES 22/09/09 Mme Daumas Infectieux Introduction I. Hépatite aigu II. Hépatite chronique III. Les différents types d hépatites A. Hépatite A 1. Prévention de la transmission 2. Vaccination
HEPATITES VIRALES 22/09/09 Mme Daumas Infectieux Introduction I. Hépatite aigu II. Hépatite chronique III. Les différents types d hépatites A. Hépatite A 1. Prévention de la transmission 2. Vaccination
NOTICE. TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé
 NOTICE ANSM Mis à jour le : 15/07/2014 Dénomination du médicament Encadré TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient
NOTICE ANSM Mis à jour le : 15/07/2014 Dénomination du médicament Encadré TRIMEBUTINE MYLAN CONSEIL 100 mg, comprimé Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient
Fibrillation atriale chez le sujet âgé
 Dr Benoit Blanchard LE HAVRE Le 18 MARS 2014 Fibrillation atriale chez le sujet âgé Le plus fréquent des trouble du rythme cardiaque, 750,000 personnes atteintes de FA en France, 100,000 nouveaux cas chaque
Dr Benoit Blanchard LE HAVRE Le 18 MARS 2014 Fibrillation atriale chez le sujet âgé Le plus fréquent des trouble du rythme cardiaque, 750,000 personnes atteintes de FA en France, 100,000 nouveaux cas chaque
Traiter la goutte sans être débordé
 Fédération des médecins omnipraticiens du Québec Traiter la goutte sans être débordé Hélène Demers et Michel Lapierre Vous voulez traiter et prévenir la goutte? Lisez ce qui suit! Les différentes phases
Fédération des médecins omnipraticiens du Québec Traiter la goutte sans être débordé Hélène Demers et Michel Lapierre Vous voulez traiter et prévenir la goutte? Lisez ce qui suit! Les différentes phases
COMMISSION DE LA TRANSPARENCE. Avis. 10 mars 2010
 COMMISSION DE LA TRANSPARENCE Avis 10 mars 2010 ARIXTRA 1,5 mg/0,3 ml, solution injectable en seringue pré-remplie - Boîte de 2 (CIP : 363 500-6) - Boîte de 7 (CIP : 363 501-2) - Boîte de 10 (CIP : 564
COMMISSION DE LA TRANSPARENCE Avis 10 mars 2010 ARIXTRA 1,5 mg/0,3 ml, solution injectable en seringue pré-remplie - Boîte de 2 (CIP : 363 500-6) - Boîte de 7 (CIP : 363 501-2) - Boîte de 10 (CIP : 564
NOTICE: INFORMATION DE L UTILISATEUR. Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl)
 NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
ACTUALITES THERAPEUTIQUES. Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012
 ACTUALITES THERAPEUTIQUES Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012 Traitement de fond Objectifs: Réduire le nombre de poussées Arrêter ou freiner la progression du handicap Les traitements disponibles
ACTUALITES THERAPEUTIQUES Dr Sophie PITTION (CHU Nancy) Metz, le 2 Juin 2012 Traitement de fond Objectifs: Réduire le nombre de poussées Arrêter ou freiner la progression du handicap Les traitements disponibles
TRAITEMENT DES TUMEURS HEPATIQUES. Paul Legmann Radiologie A Pôle Imagerie
 TRAITEMENT DES TUMEURS HEPATIQUES Paul Legmann Radiologie A Pôle Imagerie TRAITEMENT DES TUMEURS HEPATIQUES Carcinome hépato-cellulaire : Sans traitement : survie à 5 ans < à 5 % (CHC sur cirrhose) Traitement
TRAITEMENT DES TUMEURS HEPATIQUES Paul Legmann Radiologie A Pôle Imagerie TRAITEMENT DES TUMEURS HEPATIQUES Carcinome hépato-cellulaire : Sans traitement : survie à 5 ans < à 5 % (CHC sur cirrhose) Traitement
www.dondemoelleosseuse.fr
 Agence relevant du ministère de la santé www.dondemoelleosseuse.fr 01 Pourquoi devenir Veilleur de Vie? Le don de moelle osseuse peut sauver des vies. Chaque année, des milliers de personnes - enfants
Agence relevant du ministère de la santé www.dondemoelleosseuse.fr 01 Pourquoi devenir Veilleur de Vie? Le don de moelle osseuse peut sauver des vies. Chaque année, des milliers de personnes - enfants
La maladie de Berger Néphropathie à IgA
 Néphropathie à IgA La maladie Le diagnostic Les aspects génétiques Le traitement, la prise en charge, la prévention Vivre avec En savoir plus Madame, Monsieur, Cette fiche est destinée à vous informer
Néphropathie à IgA La maladie Le diagnostic Les aspects génétiques Le traitement, la prise en charge, la prévention Vivre avec En savoir plus Madame, Monsieur, Cette fiche est destinée à vous informer
DIAMICRON MR (Gliclazide) Monographie de produit Page 1 de 5
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr DIAMICRON MR Gliclazide Comprimés à libération modifiée de 30 mg Comprimés sécables à libération modifiée de 60 mg Le présent dépliant constitue la troisième
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr DIAMICRON MR Gliclazide Comprimés à libération modifiée de 30 mg Comprimés sécables à libération modifiée de 60 mg Le présent dépliant constitue la troisième
Maladie de Hodgkin ou lymphome de Hodgkin
 Maladie de Hodgkin ou lymphome de Hodgkin Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca MALADIE DE HODGKIN Ce que vous devez savoir Même si vous entendez parler du
Maladie de Hodgkin ou lymphome de Hodgkin Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca MALADIE DE HODGKIN Ce que vous devez savoir Même si vous entendez parler du
MINISTERE DE LA SANTE ET DES SOLIDARITES DIRECTION GENERALE DE LA SANTE- DDASS DE SEINE MARITIME
 Département des situations d urgence sanitaire Personne chargée du dossier : Evelyne FALIP/Nicole BOHIC Tél : 01 40 56 59 65/02 32 18 31 66 [email protected] MINISTERE DE LA SANTE ET DES SOLIDARITES
Département des situations d urgence sanitaire Personne chargée du dossier : Evelyne FALIP/Nicole BOHIC Tél : 01 40 56 59 65/02 32 18 31 66 [email protected] MINISTERE DE LA SANTE ET DES SOLIDARITES
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MEDICAMENT ImmunoGam, 312 UI/ml, solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque ml contient 312 UI d'immunoglobuline
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1 1. DENOMINATION DU MEDICAMENT ImmunoGam, 312 UI/ml, solution injectable. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque ml contient 312 UI d'immunoglobuline
Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM)
 Hématologie biologique (Pr Marc Zandecki) Faculté de Médecine CHU 49000 Angers France Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM) 1. Structure et mode d'action
Hématologie biologique (Pr Marc Zandecki) Faculté de Médecine CHU 49000 Angers France Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM) 1. Structure et mode d'action
MONOGRAPHIE DE PRODUIT
 MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
Conseils aux patients* Lutter activement. *pour les patients ayant subi une opération de remplacement de la hanche ou du genou
 Conseils aux patients* Lutter activement contre la thrombose *pour les patients ayant subi une opération de remplacement de la hanche ou du genou 2 Mentions légales Directeur de la publication : Bayer
Conseils aux patients* Lutter activement contre la thrombose *pour les patients ayant subi une opération de remplacement de la hanche ou du genou 2 Mentions légales Directeur de la publication : Bayer
