Humira Solution pour injection dans un injecteur prérempli
|
|
|
- Marie-Laure Pinard
- il y a 10 ans
- Total affichages :
Transcription
1 Humira Solution pour injection dans un injecteur prérempli ABBOTT OEMéd Qu est-ce que Humira et quand doit-il être utilisé? Humira est un médicament qui limite le processus inflammatoire dans le cadre du traitement de la polyarthrite rhumatoïde, de l arthrite psoriasique, de la maladie de Bechterew (spondylarthrite ankylosante), de la maladie de Crohn et du psoriasis. La substance active, l adalimumab, est un anticorps monoclonal humain produit par des méthodes biotechnologiques (technologie de l ADN recombinant). Les anticorps monoclonaux sont des protéines qui reconnaissent d autres protéines spécifiques et s y lient. Adalimumab agit en se liant à une protéine spécifique (le facteur de nécrose tumorale ou TNFα) qui est présente en hautes concentrations lors de maladies inflammatoires telles que la polyarthrite rhumatoïde, l arthrite psoriasique, la maladie de Bechterew (spondylarthrite ankylosante), la maladie de Crohn et le psoriasis. Polyarthrite rhumatoïde La polyarthrite rhumatoïde est une maladie inflammatoire des articulations. Humira est un médicament destiné au traitement de la polyarthrite rhumatoïde active modérée à sévère et est indiqué lorsque la réponse aux autres agents antirhumatismaux de fond (par exemple, le méthotrexate, la sulphasalazine ou l hydroxychloroquinine) n est pas suffisante pour limiter les douleurs et les oedèmes des articulations, les protéger de l effet néfaste de la polyarthrite rhumatoïde sur les cartilages et les os des articulations et les ralentir et améliorer la fonction physique corporelle. Humira peut aussi être utilisé lorsque l arthrite rhumatoïde vient d être diagnostiquée et n a pas été auparavant traitée par le méthotrexate. Arthrite psoriasique L arthrite psoriasique est une maladie inflammatoire des articulations qui peut survenir en liaison avec le psoriasis. Si vous souffrez d arthrite psoriasique, votre médecin vous a déjà prescrit d autres médicaments modifiant l évolution de la maladie, comme par exemple, le méthotrexate, auquel votre réponse n était pas suffisante. Humira ralentit l effet délétère du rhumatisme psoriasique sur le cartilage et sur l os et améliore les capacités fonctionnelles physiques. Maladie de Bechterew (spondylarthrite ankylosante) La maladie de Bechterew (spondylarthrite ankylosante) est une maladie inflammatoire de la colonne vertébrale. Si vous souffrez de la maladie de Bechterew (spondylarthrite ankylosante), votre médecin vous a déjà prescrit d autres médicaments. Si vous n avez pas eu d effets suffisants avec ces médicaments, Humira vous a été prescrit pour réduire les signes et symptômes de la maladie. Maladie de Crohn La maladie de Crohn est une maladie inflammatoire des voies digestives. Si vous souffrez de la maladie de Crohn, votre médecin vous a déjà prescrit d autres médicaments modifiant son évolution, auxquels vous n avez pas répondu de façon satisfaisante. Psoriasis Le psoriasis est une maladie inflammatoire de la peau. Si vous souffrez de psoriasis en plaques chronique modéré à sévère, Humira vous a été prescrit pour réduire les signes et symptômes de votre maladie. Vous ne devez prendre Humira que s il vous est prescrit par un médecin. Quand Humira ne doit-il pas être utilisé? Vous ne devez pas prendre Humira en cas d hypersensibilité (allergie) à l adalimumab ou à un autre composant d Humira. Si vous souffrez d une infection sérieuse, ce qui englobe également les cas de tuberculose active (voir «Quelles sont les précautions à observer lors de l utilisation d Humira?»). Si vous présentez des symptômes d infection tels que fièvre, plaies, abattement ou problèmes dentaires, vous devez absolument en informer votre médecin. Si vous souffrez de sclérose en plaques ou de névrite optique (inflammation du nerf optique) ainsi que de troubles sensoriels, votre médecin décidera si vous pouvez prendre Humira ou non. Si vous souffrez d insuffisance cardiaque modérée ou grave. Si vous avez eu par le passé une maladie cardiaque grave ou si vous en souffrez encore, il est important que vous en informiez votre médecin (voir «Quelles sont les précautions à observer lors de l utilisation d Humira?»). Quelles sont les précautions à observer lors de l utilisation d Humira? Au cours d un traitement par Humira, il se peut que vous contractiez des infections plus facilement. Il peut s agir d infections graves, y compris la tuberculose, d infections provoquées par des virus, des champignons ou des bactéries, d autres infections et d intoxication sanguine, qui, dans de rares cas, peuvent présenter un risque mortel. Il est très important que vous signaliez à votre médecin tout symptôme du type fièvre, plaies, manifestations de fatigue ou problèmes dentaires. Si vous souffrez d une infection, y compris présente depuis longtemps ou circonscrite (par ex. ulcère crural), veuillez consulter votre médecin avant de commencer le traitement par Humira. En cas d incertitude, veuillez consulter votre médecin ou votre pharmacien. Si vous avez souffert par le passé d infections à répétition ou si vous vous trouvez dans une situation augmentant le risque d infections, veuillez en informer votre médecin. Informez votre médecin si vous voyagez ou si vous séjournez dans des régions dans lesquelles se rencontrent la tuberculose ou des infections provoquées par des champignons, telles que l histoplasmose, la coccidiomycose ou la blastomycose. Comme des cas de tuberculose ont été rapportés chez les patients traités par Humira, votre médecin, avant de vous faire commencer un traitement par Humira, recherchera la présence éventuelle de signes et symptômes d une tuberculose. Cet examen inclut l établissement détaillé des antécédents médicaux, une radiographie du thorax et un test à la tuberculine. Il est extrêmement important que vous précisiez à votre médecin si vous avez déjà été atteint par la tuberculose ou si vous avez été en contact étroit avec une personne ayant la tuberculose. Il est aussi important que vous informiez votre médecin des autres médicaments que Seite 1
2 vous prenez. Si, au cours de votre traitement, des symptômes d une tuberculose (toux persistante, perte de poids, manque d entrain, fièvre) ou d une autre infection surviennent, veuillez le signaler immédiatement à votre médecin. Si vous êtes porteur du virus de l hépatite B (VHB), si vous souffrez d une infection active par ce virus ou si vous présentez un risque accru d infection par ce virus, veuillez en informer votre médecin. Humira peut entraîner une réactivation du VHB chez les personnes qui en sont porteuses. Dans quelques cas rares, en particulier lors de l utilisation concomitante de médicaments qui inhibent le système immunitaire, une réactivation de ce virus peut être potentiellement mortelle. Avant toute opération et avant tout traitement dentaire, vous devez informer le médecin que vous suivez un traitement par Humira. Si vous êtes atteint d une maladie neurologique, par exemple sclérose en plaques, votre médecin décidera si vous devez prendre Humira. Si vous observez des réactions allergiques (par exemple sensation d oppression dans la poitrine, essoufflement, vertiges, oedèmes ou éruptions cutanées), vous devez interrompre l injection d Humira et contacter immédiatement votre médecin. Pendant un traitement par Humira, certains vaccins (par exemple vaccin antipolio oral) ne doivent pas être administrés. Veuillez consulter votre médecin avant de vous faire vacciner. Si vous souffrez d insuffisance cardiaque légère et si vous êtes traité par Humira, votre médecin doit surveiller régulièrement votre état cardiaque. Si vous avez eu par le passé une maladie cardiaque grave ou si vous en souffrez encore, il est important que vous en informiez votre médecin. Contactez immédiatement votre médecin si vous observez de nouveaux signes d insuffisance cardiaque ou une aggravation des signes (par exemple essoufflement ou oedème des pieds). Votre médecin décidera si vous pouvez continuer le traitement par Humira ou non. Informez votre médecin lorsque des symptômes comme par ex. une fièvre continue, des hématomes, des saignements et des pâleurs apparaissent. Ceci est le signe d un trouble sanguin. La gaine de protection de l aiguille de la seringue contient du latex. Informez votre médecin si vous êtes allergique au latex. Parmi les patients prenant Humira ou d autres inhibiteurs du TNF, des cas rares de certains types de cancer ont été rapportés. Les patients présentant une forme évolutive grave de polyarthrite rhumatoïde et chez lesquels cette maladie est présente depuis longtemps peuvent présenter un risque supérieur à la moyenne de développement d une forme de cancer touchant le système lymphatique, qu on appelle lymphome. Si vous utilisez Humira, votre risque peut être accru. De plus, on a observé dans de rares cas, chez des patients suivant un traitement par Humira, des tumeurs cutanées qui n étaient pas des mélanomes. Utilisation d autres médicaments Humira peut être utilisé avec le méthotrexate ou d autres agents anti-rhumatismaux de fond (sulphasalazine, hydroxychloroquinine, leflunomide et préparations d or injectables), avec des stéroïdes ou des calmants (anti-inflammatoires non stéroïdiens inclus). Ce médicament peut affecter les réactions, l aptitude à la conduite et l aptitude à utiliser des outils ou des machines. Veuillez informez votre médecin ou votre pharmacien si vous souffrez d une autre maladie, si vous êtes allergique ou si vous prenez déjà d autres médicaments à usage interne ou externe (même en automédication!). Humira peut-il être utilisé pendant la grossesse ou l allaitement? L effet d Humira chez la femme enceinte n est pas connu et c est pourquoi Humira ne doit pas être utilisé pendant la grossesse. Pendant un traitement par Humira, il faut éviter de tomber enceinte en utilisant des mesures contraceptives adéquates. On ne sait pas si Humira passe dans le lait maternel. Pour cette raison il ne faut donc pas allaiter pendant le traitement par Humira. Comment utiliser Humira? Utiliser Humira en respectant très exactement la prescription de votre médecin. Si vous avez des doutes, consultez votre médecin ou votre pharmacien. La dose habituelle d adalimumab pour les patients adultes souffrant de polyarthrite rhumatoïde, d arthrite psoriasique et de la spondylarthrite ankylosante est de 40 mg toutes les deux semaines, en injection sous-cutanée, sous la peau. Votre médecin peut aussi vous prescrire d autres agents anti-rhumatismaux de fond à utiliser avec Humira. Si vous suivez un traitement par Humira contre la polyarthrite rhumatoïde sans méthotrexate, votre médecin peut décider de vous prescrire 40 mg d adalimumab une fois par semaine. Le schéma posologique usuel pour le traitement de la maladie de Crohn commence la semaine 0 par une dose de 160 mg (en 4 injections administrées soit le même jour, soit réparties sur deux jours consécutifs avec 2 injections par jour). La deuxième dose, administrée la semaine 2, est de 80 mg (2 injections). Par la suite, le médicament est administré en dose de 40 mg (1 injection) une semaine sur deux. Le schéma posologique usuel pour les patients adultes souffrant de psoriasis est une dose initiale de 80 mg (2 injections), suivie d une dose de 40 mg (1 injection) toutes les deux semaines, en commençant une semaine après l administration de la dose initiale. Après une formation sur l auto-injection, vous pourrez pratiquer vous-même l injection ou une autre personne formée pourra la pratiquer pour vous (par exemple un membre de votre famille ou un ami); votre médecin ou son assistant peut aussi faire l injection. Vous trouverez à la fin de la présente notice des instructions détaillées pour l auto-injection. Vous devez vous injecter Humira aussi longtemps que votre médecin vous l a prescrit. Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l efficacité du médicament est trop faible ou au contraire trop forte. Si vous avez pris plus d Humira que vous ne le deviez Si vous vous êtes injecté Humira par erreur plus souvent que votre médecin ne vous l avait prescrit, consultez votre médecin. Prenez avec vous l emballage d origine et la seringue prête à l emploi, même si elle est vide. Si vous avez oublié de prendre Humira Si vous oubliez une injection, vous devez vous injecter la dose suivante d Humira, dès que vous y pensez. Injectez-vous ensuite la dose suivante, comme d habitude, le jour où elle était prévue à l origine, comme si vous n aviez pas oublié la dose précédente. Quels effets secondaires Humira peut-il provoquer? L utilisation d Humira peut provoquer les effets secondaires suivants: Si vous remarquez l un des signes suivants, veuillez en informer immédiatement votre médecin ou votre pharmacien: Seite 2
3 Éruption cutanée sévère, urticaire ou autres signes d une réaction allergique. Gonflement du visage, des mains ou des pieds. Difficultés à respirer ou à avaler. Essoufflement à l effort ou au repos. Signes et symptômes pouvant signaler une maladie hématopoïétique: fièvre durable, épanchements sanguins, pâleur. Signes de problèmes de foie, comme par exemple coloration jaune des yeux ou de la peau, urines brun foncé, démangeaisons, perte d appétit ou nausées. Si vous remarquez l un des signes suivants, veuillez en informer le plus rapidement possible votre médecin ou votre pharmacien: Signes d une infection comme par exemple fièvre, malaises, plaies, problèmes de dents, brûlure à la miction. Sensation de faiblesse ou de fatigue. Toux. Démangeaisons. Engourdissement. Vision double. Faiblesses des bras ou des jambes. Les symptômes décrits ci-dessus peuvent être des signes des effets secondaires présentés ci-dessous et qui ont été observés avec Humira: très fréquents ( 1 patient/10), fréquents ( 1 patient/100 et <1 patient/10), occasionnels ( 1 patient/1000 et <1 patient/ 100), rares (<1 patient/1000). Voies respiratoires Fréquents: Toux, maux de gorge, infections des voies respiratoires supérieures (refroidissement, coryza, infection des sinus), infections des voies respiratoires inférieures (bronchite, pneumonie). Occasionnels: Asthme. Peau Très fréquents: Réactions sur le site d injection (incluant douleur, oedème, rougeur ou démangeaison). Fréquents: Démangeaisons, chute des cheveux. Occasionnels: Verrues, modifications de la peau (psoriasis, eczéma ou infections), ralentissement de la cicatrisation. Rares: Cancer de la peau. Système gastro-intestinal Fréquents: Nausées, diarrhées, maux de ventre, aphtes. Occasionnels: Problèmes de ventre (vomissements, troubles digestifs, constipation), saignement rectal, troubles de l appétit, modification du goût. Oreilles Occasionnels: Troubles d oreilles. Yeux Fréquents: Inflammation oculaire. Occasionnels: Troubles de la vue, inflammation du nerf optique. Rares: Glaucome. Système nerveux et psychisme Fréquents: Torpeur, vertiges, maux de tête. Occasionnels: Angoisses, dépression, sensation de somnolence et troubles du sommeil, maladies nerveuses (par exemple sclérose en plaques). Infections Fréquents: Infection des voies urinaires, boutons de fièvre, zona. Occasionnels: Symptômes grippaux, infections graves (par exemple septicémie), infections articulaires, infections fongiques. Coeur Occasionnels: Sensation que le coeur bat rapidement, hypertension. Autres Occasionnels: Faiblesse musculaire, troubles de la miction (par exemple présence de sang dans l urine, envies plus fréquentes), augmentation des pertes de sang menstruelles, douleurs dans la poitrine. Autres effets secondaires observés chez des patients suivant un traitement par Humira: tuberculose et autres infections opportunistes (infections survenant lorsque les défenses contre les maladies sont affaiblies); maladie du poumon. Si vous remarquez d autres effets secondaires, veuillez-en informer votre médecin ou votre pharmacien. A quoi faut-il encore faire attention? Conserver les médicaments hors de la portée des enfants. Conserver au réfrigérateur (2 8 C). Ne pas congeler. Conserver l injecteur prérempli dans son emballage d origine pour le protéger son contenu de la lumière. Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient. Pour de plus amples renseignements, consulter votre médecin ou pharmacien. Ces personnes disposent d une information détaillée destinée aux professionnels. Seite 3
4 Instructions de préparation et d administration de l injection d Humira Les instructions suivantes expliquent comment injecter Humira. Veuillez lire attentivement ces instructions et les suivre étape par étape. Votre médecin ou son assistant vous expliquera comment vous injecter Humira. N essayez en aucun cas de vous injecter le médicament vous-même tant que vous n avez pas bien compris comment on prépare et on administre une injection. Cette injection ne doit pas être mélangée avec un autre médicament dans le même injecteur prérempli. 1) Préparation Se laver soigneusement les mains. Placer les objets suivants sur une surface propre: Injecteur prérempli de la solution d injection d Humira. Tampon imbibé d alcool. Vérifier la date de péremption portée sur l injecteur prérempli. Ne pas utiliser le produit si cette date est dépassée. Maintenir l injecteur prérempli avec le capuchon gris (portant le numéro «1») vers le haut. Vérifier l aspect de la solution d injection d Humira à travers la fenêtre située sur le côté de l injecteur prérempli. Elle doit être claire et incolore. Si la solution d injection est trouble ou teintée ou si vous constatez la présence de flocons ou de particules, elle ne doit pas être utilisée. Ne pas utiliser l injecteur prérempli s il a été congelé ou s il a été éxposé directement à la lumière du soleil. Enlever les deux capuchons, le capuchon gris et aussi le rouge, seulement juste avant l injection. 2) Choix et préparation du point d injection Choisir un point d injection sur votre cuisse ou votre ventre (en évitant la zone située autour du nombril). Changer à chaque fois le point d injection pour éviter qu il ne s infecte. Chaque nouvelle injection doit être distante d au moins 3 cm du point d injection précédent. Ne pas pratiquer l injection dans une zone où la peau est rouge ou dure ni dans une zone d épanchement de sang. Ce sont des signes d une infection possible. Nettoyer le point d injection avec le tampon imbibé d alcool fourni, en appliquant des mouvements circulaires. Ne plus toucher cette zone avant l injection. 3) Injection d Humira Ne pas secouer l injecteur prérempli. Enlever les deux capuchons, le capuchon gris et aussi le rouge, seulement juste avant l injection. Tenir la partie grise de l injecteur prérempli avec une main. Placer la main au milieu de l injecteur prérempli de façon à ce qu elle ne recouvre ni le capuchon gris portant le numéro (1) ni le capuchon rouge portant le numéro (2). Maintenir l injecteur prérempli dans la main de sorte que le capuchon gris portant le numéro (1) soit orienté vers le bas. Enlever avec la seconde main le capuchon gris (1) et poser le capuchon ailleurs. Vérifier que la protection de l aiguille a été enlevée en même temps que le capuchon. Cela ne fait rien si quelques petites gouttes de liquide sortent de l aiguille. Ne pas essayer de toucher l aiguille dans le cylindre. Ne pas remettre le capuchon gris en place, vous risquez d endommager l aiguille. Retirer le capuchon rouge (portant le numéro «2»). L injecteur prérempli est maintenant prêt à l emploi. Appuyer sur le bouton rouge d injection uniquement quand l injecteur prérempli est bien positionné, vous libérez sinon la solution d injection. Ne pas remettre en place le capuchon rouge, cela pourrait libérer la solution d injection. Saisir avec précaution d une main la zone de peau nettoyée et la maintenir fermement. Prendre l injecteur prérempli dans la main de façon à ne pas toucher le bouton rouge d injection et que le bouton rouge d injection soit orienté loin du corps. Placer verticalement (90 degrés) l extrémité blanche de l injecteur prérempli sur la peau de sorte à pouvoir bien voir l une des fenêtres. C est normal si une ou plusieurs bulles apparaissent dans la fenêtre. Appuyer l injecteur prérempli avec précaution sur le point d injection (rester sans bouger au même endroit). Une fois prêt pour l injection, appuyer sur le bouton rouge d injection avec l index ou le pouce. Vous entendez un clic sonore et vous sentez une piqûre. Cela signifie que l aiguille a été déclenchée et que la solution est injectée. Pendant l injection, maintenir l injecteur prérempli avec une pression constante pendant env. 10 secondes au même endroit, pour garantir une injection complète. Pendant l injection, un repère jaune est visible dans la fenêtre. L injection est terminée, lorsque le repère jaune ne bouge plus. Retirer l injecteur prérempli du point d injection en maintenant le même angle droit. Ce faisant, le manchon blanc de l aiguille passe par-dessus l aiguille et s enclenche. Ne pas essayer de toucher l aiguille. Le manchon blanc de l aiguille est là pour vous éviter de toucher l aiguille. Un léger saignement peut survenir au point d injection. Appuyer donc par mesure de précaution sur le point d injection pendant environ 10 secondes avec un morceau de bandage. Ne pas frotter le point d injection! Si vous le souhaitez, vous pouvez mettre un pansement. 4) Elimination des matériaux usagés N utiliser chaque injecteur prérempli que pour une injection. Ne jamais reboucher l injecteur prérempli avec un des capuchons que vous avez enlevés. Immédiatement après l injection d Humira, jeter l injecteur prérempli d Humira utilisé dans un conteneur spécial suivant les instructions de votre médecin, de votre infirmière ou de votre pharmacien. Conserver ce récipient hors de portée des enfants. Seite 4
5 Que contient Humira? Humira est une solution pour injection contenant 40 mg de la substance active adalimumab dissoute dans 0,8 ml. Les autres composants son les suivants: mannitol, acide citrique monohydraté, citrate de sodium, dihydrate de dihydrogénophosphate de sodium, dihydrate de phosphate disodique, chlorure de sodium, Polysorbat 80, hydroxyde de sodium et eau pour injection. Numéro d autorisation (Swissmedic). Où obtenez-vous Humira? Quels sont les emballages disponibles sur le marché? En pharmacie, sur ordonnance médicale. Humira 40 mg solution pour injection dans injecteur prérempli existe sous forme d une solution stérile de 40 mg d adalimumab dissous dans 0,8 ml (solution stérile). Conditionnement avec 1 injecteur prérempli et 1 tampon imbibé d alcool. Titulaire de l autorisation Abbott AG, 6341 Baar. Cette notice d emballage a été vérifiée pour la dernière fois en août 2009 par l autorité de contrôle des médicaments (Swissmedic). Ce texte a été approuvé par les autorités et sa publication a été officiellement accordée à la société Documed SA. Copyright 2010 by Documed SA. Toute utilisation et reproduction sans autorisation est illicite. [ ] Seite 5
Stelara (ustekinumab)
 Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
Les autorités de santé de l Union européenne ont assorti la mise sur le marché du médicament Stelara de certaines conditions. Le plan obligatoire de minimisation des risques en Belgique, dont cette information
NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR. Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant
 B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR. Delphi 0,1 % crème Acétonide de triamcinolone
 NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
MONOGRAPHIE. tocilizumab. Solution concentrée à 20 mg/ml pour perfusion. Solution à 162 mg/0,9 ml pour injection. Norme reconnue
 MONOGRAPHIE Pr ACTEMRA tocilizumab Solution concentrée à 20 mg/ml pour perfusion Solution à 162 mg/0,9 ml pour injection Norme reconnue Inhibiteur du récepteur d interleukine Le traitement par ACTEMRA
MONOGRAPHIE Pr ACTEMRA tocilizumab Solution concentrée à 20 mg/ml pour perfusion Solution à 162 mg/0,9 ml pour injection Norme reconnue Inhibiteur du récepteur d interleukine Le traitement par ACTEMRA
PIL Décembre 2009. Autres composants: acide tartrique, macrogol 4000, macrogol 1000, macrogol 400, butylhydroxyanisol.
 Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Assurance Maladie Obligatoire Commission de la Transparence des médicaments. Avis 2 23 Octobre 2012
 Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 2 23 Octobre 2012 Titre I : Nom du médicament, DCI, forme pharmaceutique, dosage, présentation HUMIRA (DCI : Adalimumab
Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 2 23 Octobre 2012 Titre I : Nom du médicament, DCI, forme pharmaceutique, dosage, présentation HUMIRA (DCI : Adalimumab
Bien vous soigner. avec des médicaments disponibles sans ordonnance. juin 2008. Douleur. de l adulte
 Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
NOTICE: INFORMATION DE L UTILISATEUR. Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain)
 NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE : INFORMATION DE L'UTILISATEUR. DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc
 NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
Communiqué. Abbott présente à Santé Canada une demande d homologation d HUMIRA pour le traitement du psoriasis POUR PUBLICATION IMMÉDIATE
 POUR PUBLICATION IMMÉDIATE Communiqué Abbott présente à Santé Canada une demande d homologation d HUMIRA pour le traitement du psoriasis Media: Sylvie Légaré (514) 832-7268 Abbott Gabrielle Collu 514)
POUR PUBLICATION IMMÉDIATE Communiqué Abbott présente à Santé Canada une demande d homologation d HUMIRA pour le traitement du psoriasis Media: Sylvie Légaré (514) 832-7268 Abbott Gabrielle Collu 514)
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
NOTICE: INFORMATION DE L UTILISATEUR
 NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
NOTICE: INFORMATION DE L UTILISATEUR LANSOPRAZOLE TEVA 15 mg GÉLULES GASTRO-RÉSISTANTES LANSOPRAZOLE TEVA 30 mg GÉLULES GASTRO-RÉSISTANTES lansoprazole Veuillez lire attentivement cette notice avant de
vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé)
 EMA/90006/2015 EMEA/H/C/001104 Résumé EPAR à l intention du public vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé) Le présent document est un résumé du rapport européen public d évaluation
EMA/90006/2015 EMEA/H/C/001104 Résumé EPAR à l intention du public vaccin pneumococcique polyosidique conjugué (13-valent, adsorbé) Le présent document est un résumé du rapport européen public d évaluation
et l utilisation des traitements biologiques
 et l utilisation des traitements biologiques Choisir le meilleur traitement pour retrouver la qualité de vie que vous êtes en droit d avoir Les agents biologiques (biothérapies) Étant les plus récents
et l utilisation des traitements biologiques Choisir le meilleur traitement pour retrouver la qualité de vie que vous êtes en droit d avoir Les agents biologiques (biothérapies) Étant les plus récents
http://www.aroma-zone.com - [email protected]
 HUILE ESSENTIELLE DE BASILIC TROPICAL Revigorante et vitalisante, tonique puissante du système nerveux. Digestive, antispasmodique. Stress, fatigue, dépression, insomnie Flatulence, indigestion, nausée,
HUILE ESSENTIELLE DE BASILIC TROPICAL Revigorante et vitalisante, tonique puissante du système nerveux. Digestive, antispasmodique. Stress, fatigue, dépression, insomnie Flatulence, indigestion, nausée,
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine
 KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
Institut WanXiang Historique de santé du patient
 Institut WanXiang Historique de santé du patient Merci de remplir ce questionnaire aussi complètement que possible et d indiquer les zones d incompréhension avec un point d'interrogation. En plus de toutes
Institut WanXiang Historique de santé du patient Merci de remplir ce questionnaire aussi complètement que possible et d indiquer les zones d incompréhension avec un point d'interrogation. En plus de toutes
Traitements topiques. Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames. Soulagent les démangeaisons.
 SANS ORDONNANCE Solutions pour le bain et la douche : Huiles Farine d avoine Sels d Epsom Sels de al Mer Morte Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames.
SANS ORDONNANCE Solutions pour le bain et la douche : Huiles Farine d avoine Sels d Epsom Sels de al Mer Morte Utiliser conformément aux instructions figurant sur l emballage. Aident à éliminer les squames.
Atrovent HFA 20 mcg/bouffée solution pour inhalation en flacon pressurisé (bromure d'ipratropium)
 NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
DIAMICRON MR (Gliclazide) Monographie de produit Page 1 de 5
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr DIAMICRON MR Gliclazide Comprimés à libération modifiée de 30 mg Comprimés sécables à libération modifiée de 60 mg Le présent dépliant constitue la troisième
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr DIAMICRON MR Gliclazide Comprimés à libération modifiée de 30 mg Comprimés sécables à libération modifiée de 60 mg Le présent dépliant constitue la troisième
La vaccination, une bonne protection
 Vaccin contre l hépatite A et l hépatite B La personne qui reçoit ce vaccin se protège contre l hépatite A, l hépatite B et leurs complications. L hépatite A et l hépatite B sont des infections du foie
Vaccin contre l hépatite A et l hépatite B La personne qui reçoit ce vaccin se protège contre l hépatite A, l hépatite B et leurs complications. L hépatite A et l hépatite B sont des infections du foie
NOTICE : INFORMATION DE L UTILISATEUR. Flunarizine
 NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
NOTICE : INFORMATION DE L UTILISATEUR SIBELIUM 10 mg, comprimé sécable Flunarizine Veuillez lire attentivement l'intégralité de cette notice avant de prendre ce médicament. Gardez cette notice, vous pourriez
Notice : Informations de l utilisateur. Pantomed 20 mg comprimés gastro-résistants. Pantoprazole
 Notice : Informations de l utilisateur Pantomed 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations
Notice : Informations de l utilisateur Pantomed 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations
NOTICE : INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés Bisacodyl
 NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
Brûlures d estomac. Mieux les comprendre pour mieux les soulager
 Brûlures d estomac Mieux les comprendre pour mieux les soulager Définition et causes Brûlures d estomac Mieux les comprendre pour mieux les soulager Vous arrive-t-il de ressentir une douleur à l estomac
Brûlures d estomac Mieux les comprendre pour mieux les soulager Définition et causes Brûlures d estomac Mieux les comprendre pour mieux les soulager Vous arrive-t-il de ressentir une douleur à l estomac
TROISIÈME PARTIE : INFORMATION POUR LE PATIENT
 TROISIÈME PARTIE : INFORMATION POUR LE PATIENT REBIF (Interféron bêta-1a) Solution pour injection dans des seringues préremplies Ce livret représente la troisième partie de la «Monographie de produit»
TROISIÈME PARTIE : INFORMATION POUR LE PATIENT REBIF (Interféron bêta-1a) Solution pour injection dans des seringues préremplies Ce livret représente la troisième partie de la «Monographie de produit»
NOTICE : INFORMATIONS DU PATIENT. Keforal 500 mg comprimés pelliculés. Céfalexine monohydratée
 NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
NOTICE : INFORMATIONS DU PATIENT Keforal 500 mg comprimés pelliculés Céfalexine monohydratée Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes
Le guide du bon usage des médicaments
 Le guide du bon usage des médicaments Les médicaments sont là pour vous aider mais......ils ont parfois du mal à vivre ensemble. Votre médecin et votre pharmacien peuvent adapter votre traitement pour
Le guide du bon usage des médicaments Les médicaments sont là pour vous aider mais......ils ont parfois du mal à vivre ensemble. Votre médecin et votre pharmacien peuvent adapter votre traitement pour
MONOGRAPHIE DE PRODUIT
 MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
NOTICE : INFORMATIONS DE L'UTILISATEUR. PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole
 NOTICE : INFORMATIONS DE L'UTILISATEUR PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole Veuillez lire attentivement l'intégralité de cette notice car elle contient des informations importantes
NOTICE : INFORMATIONS DE L'UTILISATEUR PANTOZOL Control 20 mg, comprimé gastrorésistant Pantoprazole Veuillez lire attentivement l'intégralité de cette notice car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR. Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants. Acide acétylsalicylique
 NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
Notice publique PERDOLAN - PÉDIATRIE
 Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène
 NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Nurofen 400 Fastcaps, 400 mg capsules (molles) Ibuprofène Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
Notice : Information de l utilisateur. Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable interféron bêta-1b
 Notice : Information de l utilisateur Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable interféron bêta-1b Veuillez lire attentivement cette notice avant d utiliser ce médicament
Notice : Information de l utilisateur Betaferon 250 microgrammes/ml, poudre et solvant pour solution injectable interféron bêta-1b Veuillez lire attentivement cette notice avant d utiliser ce médicament
Mieux informé sur la maladie de reflux
 Information destinée aux patients Mieux informé sur la maladie de reflux Les médicaments à l arc-en-ciel Mise à jour de l'information: septembre 2013 «Maladie de reflux» Maladie de reflux La maladie de
Information destinée aux patients Mieux informé sur la maladie de reflux Les médicaments à l arc-en-ciel Mise à jour de l'information: septembre 2013 «Maladie de reflux» Maladie de reflux La maladie de
N o de contrat : Je demande par la présente une révision de la surprime concernant le numéro de contrat susmentionné. Signé à ce jour de 20
 RÉVISION DE SURPRIME Nom : Prénom : Date de naissance : - - Année Mois Jour N o de contrat : Je demande par la présente une révision de la surprime concernant le numéro de contrat susmentionné. Signé à
RÉVISION DE SURPRIME Nom : Prénom : Date de naissance : - - Année Mois Jour N o de contrat : Je demande par la présente une révision de la surprime concernant le numéro de contrat susmentionné. Signé à
NOTICE : INFORMATION DE L UTILISATEUR. Acidozol 10 mg, gélules gastro-résistantes Oméprazole
 La notice, 1/4/2014 NOTICE : INFORMATION DE L UTILISATEUR Acidozol 10 mg, gélules gastro-résistantes Oméprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient
La notice, 1/4/2014 NOTICE : INFORMATION DE L UTILISATEUR Acidozol 10 mg, gélules gastro-résistantes Oméprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient
Ce que les femmes enceintes doivent savoir au sujet de la grippe H1N1 (appelée grippe porcine auparavant)
 Ce que les femmes enceintes doivent savoir au sujet de la grippe H1N1 (appelée grippe porcine auparavant) 3 mai 2009, 15 h HNE Sur cette page : Que dois-je faire si je contracte ce nouveau virus et que
Ce que les femmes enceintes doivent savoir au sujet de la grippe H1N1 (appelée grippe porcine auparavant) 3 mai 2009, 15 h HNE Sur cette page : Que dois-je faire si je contracte ce nouveau virus et que
QUESTIONNAIRE SUR LA SANTE RESPIRATOIRE ET ALLERGIQUE DES ECOLIERS ET LEUR ENVIRONNEMENT SCOLAIRE
 Santé et pollution intérieure dans les écoles : Réseau d observation en Europe QUESTIONNAIRE SUR LA SANTE RESPIRATOIRE ET ALLERGIQUE DES ECOLIERS ET LEUR ENVIRONNEMENT SCOLAIRE A compléter par les enfants
Santé et pollution intérieure dans les écoles : Réseau d observation en Europe QUESTIONNAIRE SUR LA SANTE RESPIRATOIRE ET ALLERGIQUE DES ECOLIERS ET LEUR ENVIRONNEMENT SCOLAIRE A compléter par les enfants
NOTICE: INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés. Bisacodyl
 NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013
 NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
NOTICE : INFORMATION DE L UTILISATEUR Version 3.0, 04/2013 1 NOTICE : INFORMATION DE L UTILISATEUR ALEVE 220 mg, comprimés pelliculés Naproxène sodique Veuillez lire attentivement cette notice avant de
La maladie de Still de l adulte
 La maladie de Still de l adulte Syndrome de Wissler-Fanconi La maladie Le diagnostic Le traitement, la prise en charge, la prévention Vivre avec En savoir plus Madame, Monsieur Cette fiche est destinée
La maladie de Still de l adulte Syndrome de Wissler-Fanconi La maladie Le diagnostic Le traitement, la prise en charge, la prévention Vivre avec En savoir plus Madame, Monsieur Cette fiche est destinée
L AUTO-INJECTION DU MÉTHOTREXATE
 L AUTO-INJECTION DU MÉTHOTREXATE Simple et facile Pour vous, pour la vie L auto-injection du Méthotrexate par Aline Morin, Infirmière clinicienne Clinique externe de rhumatologie Édition révisée Hôpital
L AUTO-INJECTION DU MÉTHOTREXATE Simple et facile Pour vous, pour la vie L auto-injection du Méthotrexate par Aline Morin, Infirmière clinicienne Clinique externe de rhumatologie Édition révisée Hôpital
Psoriasis et biothérapies
 A qui s adressent les biothérapies? Comment agissent les biothérapies? Quels bénéfices puis-je attendre d une biothérapie? Comment puis-je contribuer au succès de mon traitement? Qu est-ce qu une biothérapie?
A qui s adressent les biothérapies? Comment agissent les biothérapies? Quels bénéfices puis-je attendre d une biothérapie? Comment puis-je contribuer au succès de mon traitement? Qu est-ce qu une biothérapie?
Protégeons-nous ensemble!
 Grippe saisonnière. Protégeons-nous ensemble! Informations importantes pour vous et votre famille. www.sevaccinercontrelagrippe.ch www.ofsp.admin.ch B C Qu est-ce que la grippe saisonnière et quels en
Grippe saisonnière. Protégeons-nous ensemble! Informations importantes pour vous et votre famille. www.sevaccinercontrelagrippe.ch www.ofsp.admin.ch B C Qu est-ce que la grippe saisonnière et quels en
NOTICE : INFORMATION DE L UTILISATEUR. Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés. ambrisentan
 NOTICE : INFORMATION DE L UTILISATEUR Version 17 Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés ambrisentan Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR Version 17 Volibris 5 mg comprimés pelliculés Volibris 10 mg comprimés pelliculés ambrisentan Veuillez lire attentivement cette notice avant de prendre ce médicament.
QU EST-CE QUE LA TUBERCULOSE?
 QU EST-CE QUE LA TUBERCULOSE? Information pour les patients TABLE DES MATIÈRES INTRODUCTION 1 LA TUBERCULOSE GÉNÉRALITÉS 1.1 Qu est-ce que la tuberculose? 1.2 La tuberculose est-elle toujours contagieuse?
QU EST-CE QUE LA TUBERCULOSE? Information pour les patients TABLE DES MATIÈRES INTRODUCTION 1 LA TUBERCULOSE GÉNÉRALITÉS 1.1 Qu est-ce que la tuberculose? 1.2 La tuberculose est-elle toujours contagieuse?
LA PERTE DE CONSCIENCE
 CES QUELQUES NOTIONS PEUVENT SAUVER DES VIES. PENSEZ Y SV D URGENCES Pompiers et service médical urgent : 100 Police : 101 L'HEMORRAGIE Comment reconnaître une hémorragie? Le sang s'écoule abondamment
CES QUELQUES NOTIONS PEUVENT SAUVER DES VIES. PENSEZ Y SV D URGENCES Pompiers et service médical urgent : 100 Police : 101 L'HEMORRAGIE Comment reconnaître une hémorragie? Le sang s'écoule abondamment
Questionnaire Médical
 Nom et prénom(s) de l élève: Date de naissance: Questionnaire Médical Ce formulaire est à compléter, avant de commencer l année scolaire, pour les nouveaux élèves ainsi que pour les élèves poursuivant
Nom et prénom(s) de l élève: Date de naissance: Questionnaire Médical Ce formulaire est à compléter, avant de commencer l année scolaire, pour les nouveaux élèves ainsi que pour les élèves poursuivant
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT
 IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
NOTICE. ANSM - Mis à jour le : 25/03/2014. Dénomination du médicament. PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole
 NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
NOTICE ANSM - Mis à jour le : 25/03/2014 Dénomination du médicament PANTOPRAZOLE RATIOPHARM CONSEIL 20 mg, comprimé gastro-résistant Pantoprazole Encadré Veuillez lire attentivement cette notice avant
Guide. Parcours. Guide à l usage des professionnels de santé confrontés à des. patients traités par anti-tnfa. bon usage anti-tnfα
 Parcours bon usage anti-tnfα Guide Guide à l usage des professionnels de santé confrontés à des patients traités par anti-tnfa Rhumatismes inflammatoires chroniques Maladies inflammatoires chroniques de
Parcours bon usage anti-tnfα Guide Guide à l usage des professionnels de santé confrontés à des patients traités par anti-tnfa Rhumatismes inflammatoires chroniques Maladies inflammatoires chroniques de
NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine
 NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament.
NOTICE : INFORMATION DE L UTILISATEUR MS Direct 10 mg comprimé enrobé MS Direct 20 mg comprimé enrobé sulfate de morphine Veuillez lire attentivement l intégralité de cette notice avant de prendre ce médicament.
NOTICE: INFORMATION DE L UTILISATEUR. Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl)
 NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
I Identification du bénéficiaire (nom, prénom, N d affiliation à l O.A.) : II Eléments à attester par un médecin spécialiste en rhumatologie :
 ANNEXE A : Formulaire de première demande Formulaire de première demande de remboursement de la spécialité HUMIRA pour une spondylarthrite axiale sévère sans signes radiographiques de spondylarthrite ankylosante
ANNEXE A : Formulaire de première demande Formulaire de première demande de remboursement de la spécialité HUMIRA pour une spondylarthrite axiale sévère sans signes radiographiques de spondylarthrite ankylosante
La drépanocytose. Sikkelcelziekte (Frans)
 La drépanocytose Sikkelcelziekte (Frans) Qu est-ce que la drépanocytose? La drépanocytose est une maladie causée par un changement héréditaire du pigment rouge dans les globules rouges : l hémoglobine.
La drépanocytose Sikkelcelziekte (Frans) Qu est-ce que la drépanocytose? La drépanocytose est une maladie causée par un changement héréditaire du pigment rouge dans les globules rouges : l hémoglobine.
Date: Avant de commencer, nous aimerions savoir à qui nous devons un immense MERCI! pour t avoir référé à nous
 1 457 route 105, unité 2 Chelsea (QC) J9B 1L2 (819) 827-4499 Fax : (819) 827-4459 [email protected] www.chelseachiro.com Formulaire pour les nouveaux Petits Date: Avant de commencer, nous aimerions
1 457 route 105, unité 2 Chelsea (QC) J9B 1L2 (819) 827-4499 Fax : (819) 827-4459 [email protected] www.chelseachiro.com Formulaire pour les nouveaux Petits Date: Avant de commencer, nous aimerions
MONOGRAPHIE DE PRODUIT. étanercept. Solution injectable en seringues préremplies
 MONOGRAPHIE DE PRODUIT Pr Enbrel MD étanercept Solution injectable en seringues préremplies 50 mg/ml et Poudre lyophilisée pour reconstitution présentée en flacons 25 mg/flacon Norme de pharmacopée reconnue
MONOGRAPHIE DE PRODUIT Pr Enbrel MD étanercept Solution injectable en seringues préremplies 50 mg/ml et Poudre lyophilisée pour reconstitution présentée en flacons 25 mg/flacon Norme de pharmacopée reconnue
COMMISSION DE LA TRANSPARENCE AVIS. 10 mai 2006
 COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
Carnet de suivi Lithium
 Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
HEPATITES VIRALES 22/09/09. Infectieux. Mme Daumas
 HEPATITES VIRALES 22/09/09 Mme Daumas Infectieux Introduction I. Hépatite aigu II. Hépatite chronique III. Les différents types d hépatites A. Hépatite A 1. Prévention de la transmission 2. Vaccination
HEPATITES VIRALES 22/09/09 Mme Daumas Infectieux Introduction I. Hépatite aigu II. Hépatite chronique III. Les différents types d hépatites A. Hépatite A 1. Prévention de la transmission 2. Vaccination
SOS HÉPATITES 03 25 06 12 12
 SOS HÉPATITES 03 25 06 12 12 TRAITEMENT ANTI-HÉPATITE C La bithérapie VIRAFÉRONPEG ET RÉBÉTOL en pratique IRAF RONPEG VIRAFÉRONPEG VIRAFERONPEG VIRAFÉRONPEG Informations utiles A quoi sert ViraféronPeg?
SOS HÉPATITES 03 25 06 12 12 TRAITEMENT ANTI-HÉPATITE C La bithérapie VIRAFÉRONPEG ET RÉBÉTOL en pratique IRAF RONPEG VIRAFÉRONPEG VIRAFERONPEG VIRAFÉRONPEG Informations utiles A quoi sert ViraféronPeg?
Cette intervention aura donc été décidée par votre chirurgien pour une indication bien précise.
 Qu est-ce qu une arthroscopie? Il s agit d une intervention chirurgicale mini-invasive dont le but est d explorer l articulation du genou et de traiter la lésion observée dans le même temps. Comment se
Qu est-ce qu une arthroscopie? Il s agit d une intervention chirurgicale mini-invasive dont le but est d explorer l articulation du genou et de traiter la lésion observée dans le même temps. Comment se
CARDIOLOGIE LA MÉDICATION POUR L'INSUFFISANCE CARDIAQUE
 CARDIOLOGIE LA MÉDICATION POUR L'INSUFFISANCE CARDIAQUE La médication est importante, elle aidera à améliorer le travail du cœur et à éliminer le surplus d'eau. Il est important de prendre la médication
CARDIOLOGIE LA MÉDICATION POUR L'INSUFFISANCE CARDIAQUE La médication est importante, elle aidera à améliorer le travail du cœur et à éliminer le surplus d'eau. Il est important de prendre la médication
Comment ça va? Quand ça ne va pas. 4 comment ça va?
 Comment ça va? 1 Voici quatre dialogues. Dites à quelle situation de communication correspond chacun d eux. Situation a) : consultation chez un médecin. Situation b) : salutations dans la rue, par simple
Comment ça va? 1 Voici quatre dialogues. Dites à quelle situation de communication correspond chacun d eux. Situation a) : consultation chez un médecin. Situation b) : salutations dans la rue, par simple
La prise en charge de votre polyarthrite rhumatoïde
 G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre polyarthrite rhumatoïde Vivre avec une polyarthrite rhumatoïde Décembre 2008 Pourquoi ce guide? Votre médecin traitant
G U I D E - A F F E C T I O N D E L O N G U E D U R É E La prise en charge de votre polyarthrite rhumatoïde Vivre avec une polyarthrite rhumatoïde Décembre 2008 Pourquoi ce guide? Votre médecin traitant
NOTICE : INFORMATION DE L UTILISATEUR. Pantogastrix 20 mg comprimés gastro-résistants Pantoprazole
 NOTICE : INFORMATION DE L UTILISATEUR Pantogastrix 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations
NOTICE : INFORMATION DE L UTILISATEUR Pantogastrix 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations
le traitement de la douleur
 le traitement de la douleur Chère patiente, cher patient Vous allez bientôt être admis dans l un des hôpitaux de jour de l az groeninge en vue d un traitement de la douleur. Dans cette brochure, vous trouverez
le traitement de la douleur Chère patiente, cher patient Vous allez bientôt être admis dans l un des hôpitaux de jour de l az groeninge en vue d un traitement de la douleur. Dans cette brochure, vous trouverez
TRAITEMENT DE LA POLYARTHRITE RHUMATOIDE
 TRAITEMENT DE LA POLYARTHRITE RHUMATOIDE RÉVOLUTION DES PRINCIPES DE TRAITEMENT Mise à disposition de nouvelles molécules Traitements de fond classiques ( Méthotrexate, Salazopyrine ) : plus efficaces
TRAITEMENT DE LA POLYARTHRITE RHUMATOIDE RÉVOLUTION DES PRINCIPES DE TRAITEMENT Mise à disposition de nouvelles molécules Traitements de fond classiques ( Méthotrexate, Salazopyrine ) : plus efficaces
Notre système. Immunitaire
 Notre système Immunitaire Notre système Immunitaire Edito L association I.R.I.S. salue l initiative de Sara Lebien, qui en écrivant cet ouvrage et en proposant une illustration gaie et coloré a rendu l
Notre système Immunitaire Notre système Immunitaire Edito L association I.R.I.S. salue l initiative de Sara Lebien, qui en écrivant cet ouvrage et en proposant une illustration gaie et coloré a rendu l
Fiche documentaire FAIRE LES PRODUITS D USAGE DOMESTIQUE SANS DANGER POUR L AIR
 Fiche documentaire FAIRE LES PRODUITS D USAGE DOMESTIQUE SANS DANGER POUR L AIR Les produits d usage domestique comprennent les produits de nettoyage (p. ex., les nettoie-vitres et les produits de nettoyage
Fiche documentaire FAIRE LES PRODUITS D USAGE DOMESTIQUE SANS DANGER POUR L AIR Les produits d usage domestique comprennent les produits de nettoyage (p. ex., les nettoie-vitres et les produits de nettoyage
Le psoriasis est une maladie qui touche environ 2 à 3 % de la population et qui se
 Le psoriasis est une maladie fréquente Le psoriasis est une maladie qui touche environ 2 à 3 % de la population et qui se traduit le plus souvent par des plaques rouges sur la peau, légèrement surélevées
Le psoriasis est une maladie fréquente Le psoriasis est une maladie qui touche environ 2 à 3 % de la population et qui se traduit le plus souvent par des plaques rouges sur la peau, légèrement surélevées
Parasites externes du chat et du chien
 Parasites externes du chat et du chien Identification, prévention et traitement Les tiques Les tiques transmettent des maladies parfois mortelles. La prévention est la meilleure arme. 1 - Où les trouve-t-on?
Parasites externes du chat et du chien Identification, prévention et traitement Les tiques Les tiques transmettent des maladies parfois mortelles. La prévention est la meilleure arme. 1 - Où les trouve-t-on?
Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés
 Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Developé pour le Centre
Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Médicaments contre la douleur Ce que vous devez savoir au sujet des analgésiques opiacés Developé pour le Centre
LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI
 LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI? LA MÉTHAMPHÉTAMINE est un produit stupéfiant illicite, synthétisé à partir de substances chimiques, également connu sous le nom de «crystal» ou «crystalmet», «ice»,
LA MÉTHAMPHÉTAMINE LE CRYSTAL C EST QUOI? LA MÉTHAMPHÉTAMINE est un produit stupéfiant illicite, synthétisé à partir de substances chimiques, également connu sous le nom de «crystal» ou «crystalmet», «ice»,
Vous et votre traitement anticoagulant par AVK (antivitamine K)
 Ce carnet a été réalisé sous la coordination de l Agence française de sécurité sanitaire des produits de santé (Afssaps). Vous et votre traitement anticoagulant par AVK (antivitamine K) Carte à découper
Ce carnet a été réalisé sous la coordination de l Agence française de sécurité sanitaire des produits de santé (Afssaps). Vous et votre traitement anticoagulant par AVK (antivitamine K) Carte à découper
Etablissement Français du Sang
 Etablissement Français du Sang LE LIEN ENTRE LA GÉNÉROSITÉ DES DONNEURS DE SANG ET LES BESOINS DES MALADES Document de préparation à l entretien médical préalable au don de sang Partie médicale La sécurité
Etablissement Français du Sang LE LIEN ENTRE LA GÉNÉROSITÉ DES DONNEURS DE SANG ET LES BESOINS DES MALADES Document de préparation à l entretien médical préalable au don de sang Partie médicale La sécurité
Notice : ROACCUTANE. AcnéFight. Consultez :
 Consultez : Notice : ROACCUTANE AcnéFight Retrouvez l évolution de mes traitements Roaccutane sur ce site : http://montraitementroaccutane.over-blog.com/ NOTICE : INFORMATION DE L UTILISATEUR ISOCURAL
Consultez : Notice : ROACCUTANE AcnéFight Retrouvez l évolution de mes traitements Roaccutane sur ce site : http://montraitementroaccutane.over-blog.com/ NOTICE : INFORMATION DE L UTILISATEUR ISOCURAL
Le VIH et votre foie
 Le VIH et votre foie Le VIH et votre foie Que dois-je savoir au sujet de mon foie? Votre foie joue un rôle incroyablement important. Il filtre votre sang en éliminant les substances nocives (toxiques)
Le VIH et votre foie Le VIH et votre foie Que dois-je savoir au sujet de mon foie? Votre foie joue un rôle incroyablement important. Il filtre votre sang en éliminant les substances nocives (toxiques)
NOTICE : INFORMATION DE L UTILISATEUR. Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés. sumatriptan
 NOTICE : INFORMATION DE L UTILISATEUR Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés sumatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament. - Gardez
NOTICE : INFORMATION DE L UTILISATEUR Sumatriptan Sandoz 50 mg comprimés Sumatriptan Sandoz 100 mg comprimés sumatriptan Veuillez lire attentivement cette notice avant de prendre ce médicament. - Gardez
QUESTIONNAIRE D ÉVALUATION POUR FEMME ENCEINTE
 QUESTIONNAIRE D ÉVALUATION POUR FEMME ENCEINTE Date : Prénom : Nom : Votre âge : ans Date de naissance : Adresse : Ville : Code postal : Téléphone (résidence) : Téléphone (bureau) : Courriel : Occupation
QUESTIONNAIRE D ÉVALUATION POUR FEMME ENCEINTE Date : Prénom : Nom : Votre âge : ans Date de naissance : Adresse : Ville : Code postal : Téléphone (résidence) : Téléphone (bureau) : Courriel : Occupation
NOTICE : INFORMATION DE L UTILISATEUR. Sporanox 100 mg gélules Itraconazole
 NOTICE : INFORMATION DE L UTILISATEUR Sporanox 100 mg gélules Itraconazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour vous.
NOTICE : INFORMATION DE L UTILISATEUR Sporanox 100 mg gélules Itraconazole Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour vous.
GUIDE PRATIQUE N 1 HERPES ASSOCIATION HERPES. Agissons contre l herpès
 GUIDE PRATIQUE N 1 HERPES ASSOCIATION HERPES Agissons contre l herpès L Herpès : une maladie très répandue En France, on estime qu environ 10 millions de personnes sont porteuses du virus de l herpès à
GUIDE PRATIQUE N 1 HERPES ASSOCIATION HERPES Agissons contre l herpès L Herpès : une maladie très répandue En France, on estime qu environ 10 millions de personnes sont porteuses du virus de l herpès à
Vivez votre féminité sans souffrir.
 Vivez votre féminité sans souffrir. PERDOFEMINA (lysinate d ibuprofène) est un médicament pour les adultes et les enfants à partir de 12 ans. Pas d utilisation prolongée sans avis médical. Ne pas administrer
Vivez votre féminité sans souffrir. PERDOFEMINA (lysinate d ibuprofène) est un médicament pour les adultes et les enfants à partir de 12 ans. Pas d utilisation prolongée sans avis médical. Ne pas administrer
1 La scintigraphie myocardique au Persantin ou Mibi Persantin
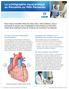 La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
Vivre avec l insuffisance cardiaque Information pour les patients et leur famille
 Vivre avec l insuffisance cardiaque Information pour les patients et leur famille EPICORE CENTRE Division of Cardiology 213 Heritage Medical Research Centre University of Alberta Edmonton, AB T6G 2S2 Phone:
Vivre avec l insuffisance cardiaque Information pour les patients et leur famille EPICORE CENTRE Division of Cardiology 213 Heritage Medical Research Centre University of Alberta Edmonton, AB T6G 2S2 Phone:
Patchs contre la douleur contenant des dérivés de morphine. Réponses aux questions les plus fréquentes
 Patchs contre la douleur contenant des dérivés de morphine Réponses aux questions les plus fréquentes Introduction Quel objectif? Ce document constitue une aide dans la gestion au quotidien de votre douleur.
Patchs contre la douleur contenant des dérivés de morphine Réponses aux questions les plus fréquentes Introduction Quel objectif? Ce document constitue une aide dans la gestion au quotidien de votre douleur.
NOTICE. PANTOPRAZOLE MYLAN CONSEIL 20 mg, comprimé gastro résistant
 NOTICE ANSM Mis à jour le : 05/09/2014 Dénomination du médicament Encadré PANTOPRAZOLE MYLAN CONSEIL 20 mg, comprimé gastro résistant Veuillez lire attentivement cette notice avant de prendre ce médicament.
NOTICE ANSM Mis à jour le : 05/09/2014 Dénomination du médicament Encadré PANTOPRAZOLE MYLAN CONSEIL 20 mg, comprimé gastro résistant Veuillez lire attentivement cette notice avant de prendre ce médicament.
Exemple de Projet d Accueil Individualisé ELEVE CONCERNE
 Exemple de Projet d Accueil Individualisé Circulaire projet d accueil n 2003-135 du 08/09/2003 (Bulletin Officiel n 34 du 18/9/2003) Circulaire restauration scolaire n 2001-118 du 25/06/2001(BO Spécial
Exemple de Projet d Accueil Individualisé Circulaire projet d accueil n 2003-135 du 08/09/2003 (Bulletin Officiel n 34 du 18/9/2003) Circulaire restauration scolaire n 2001-118 du 25/06/2001(BO Spécial
Les Arbres décisionnels
 Les Arbres décisionnels Les aides à la décision plainte-traitement (ou arbres décisionnels ) sont tirés de travaux effectués dans le cadre de l Organisation Mondiale de la Santé. Ils sont destinés à soutenir
Les Arbres décisionnels Les aides à la décision plainte-traitement (ou arbres décisionnels ) sont tirés de travaux effectués dans le cadre de l Organisation Mondiale de la Santé. Ils sont destinés à soutenir
Le Livre des Infections Sexuellement Transmissibles
 Le Livre des Infections Sexuellement Transmissibles sommaire Qu est-ce qu une IST? p. 5 La blennorragie gonococcique p. 7 La chlamydiose p. 8 L hépatite B p. 9 L herpès génital p. 10 Les mycoplasmes et
Le Livre des Infections Sexuellement Transmissibles sommaire Qu est-ce qu une IST? p. 5 La blennorragie gonococcique p. 7 La chlamydiose p. 8 L hépatite B p. 9 L herpès génital p. 10 Les mycoplasmes et
313-40013-B MIS À JOUR EN MARS 2013
 313-40013-B MIS À JOUR EN MARS 2013 SOMMAIRE 1 - La vaccination, comment ça marche? 3, 4 et 5 2 - Les vaccins détériorent-ils LA protection naturelle contre les maladies? 6 3 - Avec autant de vaccins,
313-40013-B MIS À JOUR EN MARS 2013 SOMMAIRE 1 - La vaccination, comment ça marche? 3, 4 et 5 2 - Les vaccins détériorent-ils LA protection naturelle contre les maladies? 6 3 - Avec autant de vaccins,
NOTICE : INFORMATION DU PATIENT. MAALOX CONTROL 20 mg comprimés gastro-résistants Pantoprazole
 NOTICE : INFORMATION DU PATIENT MAALOX CONTROL 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations
NOTICE : INFORMATION DU PATIENT MAALOX CONTROL 20 mg comprimés gastro-résistants Pantoprazole Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT
 ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT Simponi 50 mg, solution injectable en stylo prérempli. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Un stylo prérempli de 0,5
ANNEXE I RESUME DES CARACTERISTIQUES DU PRODUIT 1. DENOMINATION DU MEDICAMENT Simponi 50 mg, solution injectable en stylo prérempli. 2. COMPOSITION QUALITATIVE ET QUANTITATIVE Un stylo prérempli de 0,5
Leucémies de l enfant et de l adolescent
 Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Tableau récapitulatif : composition nutritionnelle de la spiruline
 Tableau récapitulatif : composition nutritionnelle de la spiruline (Valeur énergétique : 38 kcal/10 g) Composition nutritionnelle Composition pour 10 g Rôle Protéines (végétales) 55 à 70 % Construction
Tableau récapitulatif : composition nutritionnelle de la spiruline (Valeur énergétique : 38 kcal/10 g) Composition nutritionnelle Composition pour 10 g Rôle Protéines (végétales) 55 à 70 % Construction
Gyselle 20/30 SPIRIG HEALTHCARE
 Gyselle 20/30 SPIRIG HEALTHCARE OEMéd Qu est-ce que Gyselle 20/Gyselle 30 et quand doit-il être utilisé? Gyselle 20/Gyselle 30 est un médicament anticonceptionnel hormonal, appelé contraceptif oral ou
Gyselle 20/30 SPIRIG HEALTHCARE OEMéd Qu est-ce que Gyselle 20/Gyselle 30 et quand doit-il être utilisé? Gyselle 20/Gyselle 30 est un médicament anticonceptionnel hormonal, appelé contraceptif oral ou
