MONOGRAPHIE DE PRODUIT
|
|
|
- Roland Giroux
- il y a 9 ans
- Total affichages :
Transcription
1 MONOGRAPHIE DE PRODUIT VOLUVEN MD hydroxyéthylamidon 130/0,4 (à 6 %) dans une solution de chlorure de sodium à 0,9 % pour injection Liquide de remplissage vasculaire Fresenius Kabi Canada Une division de Calea Ltd. Mississauga, ON, L4W 4Y3 Canada Date de révision: 21 juin 2013 N de contrôle d'homologation : Monographie de produit: VOLUVEN MD ver 3.2 Page 1 de 27
2 Table des matières PARTIE I : RENSEIGNEMENTS POUR LE PROFESSIONNEL DE LA SANTÉ... 3 RENSEIGNEMENTS SOMMAIRES SUR LE PRODUIT... 3 INDICATIONS ET UTILISATION CLINIQUE... 3 CONTRE-INDICATIONS... 4 MISES EN GARDE ET PRÉCAUTIONS... 4 EFFETS INDÉSIRABLES... 7 INTERACTIONS MÉDICAMENTEUSES... 8 POSOLOGIE ET ADMINISTRATION... 8 SURDOSAGE... 9 MODE D'ACTION ET PHARMACOLOGIE CLINIQUE... 9 ENTREPOSAGE ET STABILITÉ INSTRUCTIONS PARTICULIÈRES DE MANIPULATION FORMES POSOLOGIQUES, COMPOSITION ET CONDITIONNEMENT PARTIE II : RENSEIGNEMENTS SCIENTIFIQUES RENSEIGNEMENTS PHARMACEUTIQUES ESSAIS CLINIQUES PHARMACOLOGIE DÉTAILLÉE MICROBIOLOGIE TOXICOLOGIE RÉRÉRENCES PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Monographie de produit: VOLUVEN MD ver 3.2 Page 2 de 27
3 VOLUVEN MD Hydroxyéthylamidon 130/0,4 à 6 % dans une solution de chlorure de sodium à 0,9 % pour injection PARTIE I : RENSEIGNEMENTS POUR LE PROFESSIONNEL DE LA SANTÉ RENSEIGNEMENTS SOMMAIRES SUR LE PRODUIT Voie d'administration Intraveineuse Forme et puissance de la dose Solution de perfusion / hydroxyéthylamidon 130/0,4 à 6 % dans une solution de chlorure de sodium à 0,9 % pour injection Ingrédients non médicamenteux Chlorure de sodium Eau pour injection ph ajusté au moyen de l'hydroxyde de sodium ou de l'acide chlorhydrique INDICATIONS ET UTILISATION CLINIQUE VOLUVEN MD est indiqué dans le traitement de l'hypovolémie, lorsqu'une expansion du volume plasmatique est nécessaire. Il ne constitue ni un substitut des globules rouges ni un substitut des facteurs de coagulation dans le plasma. Monographie de produit: VOLUVEN MD ver 3.2 Page 3 de 27
4 CONTRE-INDICATIONS VOLUVEN MD est contre-indiqué chez les patients : présentant une surcharge liquidienne (hyperhydratation), particulièrement dans les cas d œdème pulmonaire et d insuffisance cardiaque congestive; présentant une sepsie; présentant une insuffisance rénale accompagnée d oligurie ou d anurie qui n est pas reliée à l hypovolémie; présentant une maladie hépatique grave; recevant un traitement de dialyse; présentant une hypernatrémie grave ou une hyperchlorémie grave; présentant une hypersensibilité connue à l amidon hydroxéthylé; présentant un saignement intracrânien. MISES EN GARDE ET PRÉCAUTIONS Mises en garde et précautions graves Chez les patients souffrant d hypovolémie exigeant des soins intensifs ou urgents, une évaluation approfondie du risque d induire une lésion rénale ou une insuffisance hépatique doit être effectuée avant d amorcer le traitement par VOLUVEN MD. L utilisation de solutions cristalloïdes devrait être envisagée au lieu d utiliser VOLUVEN MD chez les patients jugés à risque d avoir ces effets indésirables. Généralités : L'hyperhydratation causée par une surdose doit être évitée en tout temps. En particulier, si les patients souffrent d'insuffisance cardiaque ou de dysfonctionnements rénaux chroniques, il est nécessaire de prendre les risques d'hyperhydratation en considération; la posologie doit tenir compte de ces troubles. En cas de déshydratation grave, un cristalloïde doit être administré en premier. Carcinogenèse et mutagenèse : Voir PARTIE II : RENSEIGNEMENTS SCIENTIFIQUES Toxicologie Étude de mutagénicité. Hématologique : La prudence est de mise avant d administrer VOLUVEN MD aux patients présentant de graves troubles de saignements (ex., cas graves de la maladie de von Willebrand). Monographie de produit: VOLUVEN MD ver 3.2 Page 4 de 27
5 L'administration de quantités significatives d'hydroxyéthylamidon risque, en raison de l'hémodilution, d'altérer de manière temporaire le mécanisme de coagulation et de diminuer l'hématocrite et le nombre de protéines plasmatiques. Hépatique/biliaire/pancréatique : L amylase sérique peut augmenter durant l administration de VOLUVEN MD et peut interférer avec le diagnostic de pancréatite. La concentration élevée d amylase est causée par la formation d un complexe enzyme-substrat regroupant l amylase et l hydroxyéthylamidon, qui est sujet à une élimination lente et qui ne doit pas être considéré comme un diagnostic de pancréatite. Immunitaire : Des réactions anaphylactoïdes (symptômes pseudo-grippaux légers, bradycardie, tachycardie, bronchospasme, œdème pulmonaire non cardiaque) ont été signalées avec des solutions contenant de l amidon hydroxyéthylé. Si une réaction d hypersensibilité survient, il faut cesser immédiatement l administration du médicament; le traitement approprié ainsi que les mesures de soutien nécessaires devraient être mis en place jusqu à la résolution des symptômes (veuillez consulter la section EFFETS INDÉSIRABLES). Rénal : Il est important de fournir du liquide en quantité suffisante et de surveiller régulièrement la fonction rénale ainsi que l'équilibre électrolytique des liquides. Les électrolytes sériques doivent être surveillés. Peau : Le prurit (les démangeaisons) est une complication reconnue de l'administration d'amidons hydroxyéthylés, bien qu'elle soit généralement plus fréquente avec l'utilisation prolongée de doses élevées. Toutefois, l'apparition du prurit causé par l'hea peut être retardée, généralement d'une à six semaines après l'exposition, et ce prurit peut être grave et d'une persistance soutenue (pouvant s'étaler sur des semaines et même des mois). Il est généralement insensible aux traitements. Cependant, le poids moléculaire réduit, le degré de substitution moindre, l'entreposage diminué dans les tissus et la persistance intravasculaire, conjointement avec la demi-vie plasmatique plus courte de HEA 130/0,4, peuvent contribuer à diminuer la fréquence de prurit causé par l'utilisation de ce médicament. Monographie de produit: VOLUVEN MD ver 3.2 Page 5 de 27
6 Populations particulières Femmes enceintes : On ne dispose pas d'études adéquates et bien contrôlées sur l'utilisation de VOLUVEN MD chez la femme enceinte. Les études effectuées chez l'animal n'ont cependant pas mis en évidence d'effet nocif sur le plan du développement de l'embryon ou du fœtus, de la gestation, de la parturition ou du développement postnatal. Depuis sa mise en marché, VOLUVEN MD n'a fait l'objet d'aucune notification d'effet indésirable en cas d utilisation chez la femme enceinte. Des effets embryotoxiques ont été observés chez des lapines lorsque l HEA 130/0,4 à 10 % dans une solution de chlorure de sodium à 0,9 % a été administré selon une dose de 50 ml/kg de poids corporel/jour. Aucune preuve de tératogénicité n a été observée. VOLUVEN MD doit être utilisé au cours de la grossesse uniquement si les avantages potentiels justifient les risques potentiels pour le fœtus. Femmes qui allaitent : On ne sait pas si l'hea 130/0,4 est excrété dans le lait maternel humain. Puisque plusieurs types de médicaments sont excrétés dans le lait maternel, la précaution est de mise lorsque le VOLUVEN MD est administré à une femme qui allaite. Une décision quant à la poursuite/cessation de l allaitement ou l abandon/continuation de la thérapie par VOLUVEN MD devrait être prise en tenant compte des bienfaits de l allaitement pour l enfant et des bienfaits de la thérapie par VOLUVEN MD pour la mère. Pédiatrie : On ne dispose que de données limitées sur d utilisation de VOLUVEN MD chez l'enfant. Dans le cadre d interventions chirurgicales non cardiaques chez 41 enfants incluant des nouveau-nés et de jeunes enfants (< 2 ans), une dose moyenne de 16 ± 9 ml/kg a été administrée de façon sécuritaire et a été bien tolérée pour la stabilisation des paramètres hémodynamiques. La tolérance à ce produit administré en milieu peropératoire était comparable à l albumine à 5 %. VOLUVEN MD peut être administré aux enfants prématurés et aux nouveau-nés, mais uniquement après avoir soigneusement évalué les risques et les avantages. Gériatrie : Sur l'ensemble des patients inclus dans les essais cliniques portant sur VOLUVEN MD (N= 471), 25 % étaient âgés de 65 à 75 ans, tandis que 7 % avaient 75 ans ou plus. Aucune différence globale sur le plan de l innocuité ou de l efficacité n'a été observée entre ces personnes et les Monographie de produit: VOLUVEN MD ver 3.2 Page 6 de 27
7 sujets jeunes. Aucune autre observation n'a permis d identifier un risque spécifique à l'administration de VOLUVEN MD dans ce groupe de patients. EFFETS INDÉSIRABLES Les effets indésirables associés à VOLUVEN MD, signalés de manière spontanée dans le cadre d'essais cliniques et au sein de la littérature médicale, comprennent : Troubles du système immunitaire Rare : Des réactions anaphylactoïdes (hypersensibilité, faibles symptômes similaires à ceux de la grippe, bradycardie, tachycardie, bronchospasme, œdème pulmonaire non cardiaque) ont été signalées avec l utilisation de solutions contenant de l hydroxyéthylamidon (veuillez consulter la section MISES EN GARDE ET PRÉCAUTIONS). Anomalies dans les épreuves hématologiques et les observations chimiques cliniques (investigations) Fréquent (en fonction de la dose) : Augmentation de l amylase sérique (veuillez consulter la section MISES EN GARDE ET PRÉCAUTION). Fréquent (en fonction de la dose): Pour les doses élevées, les effets de dilution peuvent fréquemment contribuer à une dilution correspondante des composants sanguins tels que les facteurs de coagulation et d'autres protéines plasmatiques, ainsi qu'une diminution de l'hématocrite. Troubles cutanés et sous-cutanés Fréquent (en fonction de la dose) : Prurit, démangeaisons (veuillez consulter la section MISES EN GARDE ET PRÉCAUTIONS). Troubles sanguins et du système lymphatique Rare (en présence de fortes doses) : Des troubles de coagulation du sang au-delà des effets de dilution peuvent survenir selon la dose administrée. Monographie de produit: VOLUVEN MD ver 3.2 Page 7 de 27
8 Tableau : Fréquence d'observation des effets indésirables du médicament Catégorie du système d'organe Troubles sanguins et du système lymphatique Troubles du système immunitaire Troubles de la peau et de l'épiderme Anomalies dans les épreuves hématologiques et les observations chimiques cliniques (investigations) Effet indésirable du médicament Troubles de coagulation du sang au-delà des effets de dilution Réactions anaphylactoïdes Prurit Augmentation de l'amylase sérique Diminution de l'hématocrite Diminution des protéines plasmatiques Fréquence d'observation Rares (dans le cadre de doses élevées) (> 0,01 % à 0,1 %) Rares (> 0,01 % à 0,1 %) Fréquentes (en fonction de la dose) ( 1 % à < 10 %) Fréquentes (en fonction de la dose) ( 1 % à < 10 %) Fréquentes (en fonction de la dose) ( 1 % à < 10 %) Fréquentes (en fonction de la dose) ( 1 % à < 10 %) INTERACTIONS MÉDICAMENTEUSES Aucune interaction entre VOLUVEN MD et d autres médicaments ou produits nutritionnels n est connue ni n a été signalée à ce jour. Il faut toutefois éviter de mélanger VOLUVEN MD avec d'autres médicaments. POSOLOGIE ET ADMINISTRATION VOLUVEN MD (HEA 130/0,4 à 6 % dans une solution de chlorure de sodium à 0,9 % pour injection) est administré par perfusion intraveineuse uniquement. Le volume total ainsi que la vitesse de perfusion dépendent de la situation clinique et de l'état du patient. Comme tout autre liquide intraveineux, VOLUVEN MD doit être administré conformément aux pratiques cliniques reconnues relativement à la gestion des électrolytes et des liquides. Monographie de produit: VOLUVEN MD ver 3.2 Page 8 de 27
9 Dans le cadre d'essais cliniques, des perfusions allant jusqu'à 33 ml/kg/jour étaient fréquemment utilisées. L expérience est limitée en ce qui concerne des perfusions de doses entre 33 ml/kg/jour et 50 ml/kg/jour. Les premiers 10 à 20 ml doivent être perfusés lentement, en surveillant étroitement le patient en raison du potentiel de réactions anaphylactoïdes. VOLUVEN MD peut être administré de façon répétitive sur plusieurs jours selon les besoins du patient. La dose et la durée du traitement dépendent de la durée et de l étendue de l hypovolémie, des paramètres hémodynamiques et de l hémodilution. Enfants : On ne dispose que de données cliniques limitées sur l'utilisation de VOLUVEN MD chez l'enfant. Chez 41 enfants, dont des nouveau-nés et des nourrissons (< 2 ans), l'administration d'une dose moyenne de 16 ± 9 ml/kg en vue de stabiliser l hémodynamique s'est révélée inoffensive et bien tolérée. La posologie pour les enfants doit être adaptée aux besoins colloïdaux de chaque patient, en prenant en compte l'état de la maladie, l'état hémodynamique ainsi que le niveau d'hydratation. SURDOSAGE Comme chez l'ensemble des substituts de volume, le surdosage de VOLUVEN MD peut causer la congestion du système circulatoire (par ex., un œdème pulmonaire). Dans ce cas, la perfusion doit cesser immédiatement et un diurétique doit être administré, si cela s'avère nécessaire. Pour obtenir de l information additionnelle au sujet de la gestion d une surdose soupçonnée de médicament, veuillez contacter votre Centre anti-poison régional. MODE D'ACTION ET PHARMACOLOGIE CLINIQUE VOLUVEN MD contient le l hydroxyéthylamidon (HEA 130/0,4) à 6 %, un tétra-amidon. L HEA 130/0,4 est un colloïde artificiel, un amidon de troisième génération, utilisé pour le remplissage vasculaire. Il est caractérisé par sa substitution molaire des groupes d hydroxyéthyles (0,4), son poids moléculaire moyen ( Da), sa concentration (6 %) et son ratio de substitution (ratio C 2 /C 6 ) d environ 9:1. Son effet sur l expansion du volume intravasculaire et l hémodilution est basé sur ces paramètres ainsi que sur la dose administrée et la vitesse de perfusion. L'hydroxyéthylamidon 130/0,4 est un dérivé de l'amidon de maïs cireux et soluble, qui consiste principalement en polymère de glucose (amylopectine) composé surtout d'unités de glucose liées Monographie de produit: VOLUVEN MD ver 3.2 Page 9 de 27
10 α-1,4 avec plusieurs branches α-1,6. Le poids moléculaire moyen ( Da), le faible degré de substitution (0,4) et le faible écart de distribution du poids moléculaire de l'hydroxyéthylamidon (HEA 130/0,4) contenu dans le VOLUVEN MD contribuent à ses effets bénéfiques sur la pharmacocinétique, sur le volume intravasculaire et sur l'hémodilution. Pharmacodynamique Une perfusion de 500 ml de VOLUVEN MD en 30 minutes à des volontaires en bonne santé a entraîné une augmentation de volume en plateau et non expansive d'environ 100 % du volume perfusé, d une durée de 4 à 6 heures environ. Une compensation isovolémique de sang par VOLUVEN MD préserve le volume sanguin pendant au moins 6 heures. Pharmacocinétique Le profil pharmacocinétique du HEA est complexe et dépend largement de sa substitution molaire et de son poids moléculaire. En administration intraveineuse, les molécules plus petites que le seuil rénal ( à Da) sont éliminées facilement et rapidement dans l urine, alors que les molécules ayant un poids moléculaire plus élevé sont métabolisées par l'amylase plasmatique avant d'être éliminées par la voie rénale. Immédiatement après la perfusion, le poids moléculaire moyen in vivo de VOLUVEN MD dans le plasma se situe entre et Da. Celui-ci demeure au-dessus du seuil rénal tout au long de la période de traitement. Le volume de distribution de VOLUVEN MD, à la suite de l'administration intraveineuse de 500 ml à des volontaires en santé, est de 5,9 litres. Les concentrations plasmatiques de VOLUVEN MD demeurent à 75 % de la concentration de pointe 30 minutes après la perfusion et elles diminuent rapidement à 14 %, 6 heures après la perfusion. Les concentrations plasmatiques de VOLUVEN MD reviennent aux niveaux de base 24 heures après la perfusion. Suite à l'administration intraveineuse de 500 ml, la clairance plasmatique de VOLUVEN MD était de 31,4 ml/min avec une ASC de 14,3 mg/ml/h, conformément à la pharmacocinétique non linéaire. Une seule dose de 500 ml de VOLUVEN MD se solde par une élimination urinaire d environ 62 % au bout de 72 heures. VOLUVEN MD est éliminé par circulation systémique avec une t 1/2 α de 1,4 h et une demi-vie terminale (t 1/2ß ) de 12,1 h, à la suite de l'administration d'une seule dose de 500 ml. La cinétique de VOLUVEN MD est semblable, qu'il s'agisse d'une administration en une seule dose ou en plusieurs doses. Aucune accumulation plasmatique significative ne s'est produite suite à l'administration quotidienne de 500 ml d'une solution à 10 % contenant de la solution d'hea 130/0,4, au cours d'une période de dix jours. Les taux d'élimination urinaire étaient d'environ 70 %, au bout de 72 heures. Au cours d'un essai expérimental sur des rats au moyen de doses de 7 ml par kg de poids corporel par jour d'hea 130/0,4 à 10 % administrées à plusieurs reprises au cours d'une période Monographie de produit: VOLUVEN MD ver 3.2 Page 10 de 27
11 de 18 jours, l'entreposage dans les tissus correspondait à 0,6 % du total de la dose administrée, 52 jours après la dernière administration. Populations particulières et états pathologiques Insuffisance rénale : une seule administration intraveineuse de VOLUVEN MD (500 ml) à des sujets aux prises avec des troubles rénaux, variant de bénins à graves, a résulté en une augmentation modérée de l'aire sous la courbe selon un facteur de 1,7 (intervalle de confiance à 95 %, 1,44 ; 2,07), seulement chez les sujets avec une Cl Cr < 50 ml/min comparé à > 50 ml/min. Toutefois, la demi-vie terminale et la concentration de pointe du HEA n'ont pas été affectées par les troubles rénaux. Les concentrations plasmiques de VOLUVEN MD retournent aux niveaux de base 24 heures après la perfusion. 59 % de la solution d'hea 130/0,4 a été récupéré dans l'urine des sujets avec une Cl Cr > 30 ml/min, contre 51 % chez ceux avec une Cl Cr se situant entre 15 et 30 ml/min. Il n'y a pas de données disponibles sur l'utilisation de VOLUVEN MD dans le cadre de dialyses. Insuffisance hépatique : les données pharmacocinétiques chez les patients aux prises avec une insuffisance hépatique ne sont pas disponibles. Âge : les données pharmacocinétiques chez les personnes âgées et les enfants ne sont pas disponibles. Monographie de produit: VOLUVEN MD ver 3.2 Page 11 de 27
12 ENTREPOSAGE ET STABILITÉ À utiliser immédiatement après l'ouverture du sac. La solution est conçue pour une administration intraveineuse au moyen d'équipement stérile. Utilisez uniquement des solutions claires et des contenants intacts. Les médicaments administrés par voie parentérale devraient faire l'objet d'une inspection visuelle en vue d'en vérifier la limpidité et de déceler des particules, du précipité, de la décoloration et des fuites avant de procéder à l'administration. Les solutions qui ont un aspect flou, qui contiennent des particules ou du précipité, ou alors qui comportent de la décoloration ou des fuites ne doivent pas être utilisées. Jetez la portion inutilisée de la solution de médicament. N'utilisez pas un contenant de VOLUVEN MD ayant dépassé sa date de péremption. Entreposage du sac freeflex MD : de 15 à 25 C pendant 3 ans. Ne pas congeler. INSTRUCTIONS PARTICULIÈRES DE MANIPULATION Avant d'administrer au patient le produit contenu dans les sacs de plastique, suivez les directives suivantes : Contenant freeflex MD de solution intraveineuse Ces instructions constituent uniquement des lignes directrices pour l'utilisation de ce produit. Veuillez vous reporter aux lignes directrices de votre service. Monographie de produit: VOLUVEN MD ver 3.2 Page 12 de 27
13 1. Vérifiez la composition de la solution, le numéro de lot et la date de péremption. Inspectez le contenant afin de déceler des dommages ou une fuite; si le contenant est endommagé ne l utilisez pas. 2. Utilisez la languette d ouverture pour retirer le suremballage. 3. Localisez le port de perfusion bleu (pour administration). 4. Détachez le couvercle inviolable bleu du port de perfusion du sac freeflex MD. Monographie de produit: VOLUVEN MD ver 3.2 Page 13 de 27
14 7. Accrochez le sac au support pour perfusion. Appuyez sur la chambre à gouttes afin d obtenir le niveau de liquide. Amorcez le nécessaire à perfusion. Connectez et ajustez la vitesse de perfusion. 5. Fermez la roulette du régulateur de débit. Insérez le perforateur jusqu à ce que le collier en plastique transparent du port touche l épaulement du perforateur. 6. Utilisez un nécessaire à perfusion standard sans évent et fermez l ouverture d entrée d air. MISES EN GARDE 1. Ne retirez pas d avance le contenant freeflex MD IV de son suremballage, le suremballage doit être retiré immédiatement avant l utilisation. 2. Les produits pour administration parentérale devraient être vérifiés visuellement avant l administration afin de déceler des particules ou de la décoloration, lorsque la solution et le contenant le permettent. 3. Administrez la solution seulement si elle est claire, exempte de particules et que le contentant freeflex MD IV n est pas endommagé. 4. VOLUVEN MD doit être utilisé immédiatement après l insertion dans le sac du perforateur du nécessaire pour perfusion. 5. Cessez la perfusion si une réaction indésirable survient. Monographie de produit: VOLUVEN MD ver 3.2 Page 14 de 27
15 6. Ne procédez pas à une aération. 7. Il est recommandé de changer les nécessaires à perfusion pour de nouveaux au moins une fois par 24 heures. 8. Pour usage unique seulement. Jetez la portion inutilisée. Incompatibilités Le mélange avec d'autres médicaments n'est pas recommandé. Si, dans des cas exceptionnels, un mélange avec d'autres médicaments s'avère nécessaire, il est important de considérer soigneusement la compatibilité (l'opacification ou la précipitation), l'injection hygiénique et le mélange approprié. Monographie de produit: VOLUVEN MD ver 3.2 Page 15 de 27
16 FORMES POSOLOGIQUES, COMPOSITION ET CONDITIONNEMENT VOLUVEN MD (hydroxyéthylamidon 130/0,4 à 6 % dans une solution de chlorure de sodium à 0,9 %) est fourni stérile et sans substance pyrogène dans des sacs en plastique (freeflex MD ) de 250 ou 500 ml. La composition de chaque 100 ml est la suivante : Amidon poly (O-2-hydroxyéthyle) 6,00 g (Substitution molaire : 0,4) (Poids moléculaire moyen : Da) Chlorure de sodium 0,90 g ph ajusté au moyen d hydroxyde de sodium ou quantité suffisante d acide chlorhydrique à 25 % Eau pour injection quantité suffisante Concentration approximative d électrolytes (mmol/litre): Sodium (Na + ) 154,0 Chlorure (Cl - ) 154,0 Osmolarité théorique (mosmol/litre) 308 Acidité de titrage (mmol NaOH/litre) < 1,0 ph 4,0 à 5,5 VOLUVEN MD, HEA 130/0,4 à 6 % dans une solution de chlorure de sodium à 0,9 % pour injection, est fourni dans les principaux contenants suivants dans les tailles d emballage suivantes : Sac en polyoléfine (freeflex MD ) muni d'une pellicule de suremballage : 30 sacs de 250 ml par boîte; 20 sacs de 500 ml par boîte. Monographie de produit: VOLUVEN MD ver 3.2 Page 16 de 27
17 PARTIE II : RENSEIGNEMENTS SCIENTIFIQUES RENSEIGNEMENTS PHARMACEUTIQUES Substance pharmaceutique Description de la substance pharmaceutique L'amidon hydroxyéthylé est un dérivé de l'amylopectine, qui est un composant extrêmement ramifié de l'amidon. L'amylopectine est rapidement hydrolysée par l'amylase des humains et des animaux. Afin de réduire la dégradation métabolique, les résidus de glucose de l'amylopectine entrent en réaction avec l'oxyde d'éthylène. Les groupes d'hydroxyéthyle peuvent être introduits dans trois positions (C 2,C 3, et C 6 ) des résidus de glucose. Le degré et la forme de substitution, exprimés en termes du ratio C 2 /C 6, déterminent la dégradation enzymatique du HEA. L HEA 130/0,4 contenu dans VOLUVEN MD est caractérisé par sa substitution molaire, son poids moléculaire et son ratio C 2 /C 6. Nom propre ou nom usuel : Hydroxyéthylamidon (HEA) (130/0,4) Nom chimique : Amidon poly (0-2-hydroxyéthyle) Formule développée : Poids moléculaire moyen : de à daltons Monographie de produit: VOLUVEN MD ver 3.2 Page 17 de 27
18 Poids moléculaire (pm) : le poids moléculaire indique le poids moyen. Le pm du HEA 130/0,4 se situe entre et daltons, se qui correspond à environ 609 à 830 unités de glucose partiellement hydroxyéthylées. Substitution molaire (SM) : le ratio de groupes hydroxyéthyles, relativement aux unités de glucose, est nommé substitution molaire (SM). La substitution molaire (SM) pour cette substance est de 0,4 (0,38 à 0,45), un tétra-amidon, et détermine le ratio molaire des groupes hydroxyéthyles, relativement aux unités de glucose. Ratio C 2 /C 6 : ce paramètre fournit des renseignements relatifs à la position préférentielle de l'hydroxyéthylation et il reflète la réactivité intrinsèque de la fonctionnalité alcoolique primaire et secondaire aux positions respectives de l'anneau de glucose. La valeur du ratio C 2 /C 6 de l'hea 130/0,4 doit être supérieure à 8. Caractéristiques du produit : L'hydroxyéthylamidon (HEA 130/0,4 à 6 %, tétra-amidon) en solution de chlorure de sodium isotonique est incolore et limpide. Monographie de produit: VOLUVEN MD ver 3.2 Page 18 de 27
19 ESSAIS CLINIQUES Un essai prospectif, contrôlé, randomisé, à double insu et multicentrique, comprenant 100 patients, qui a évalué VOLUVEN MD (hydroxyéthylamidon 130/0,4 à 6 %), comparé à de l'héta-amidon 450/0,7 à 6 % approuvé aux États-Unis, contenant une solution saline à 0,9 %, pour la substitution de volume peropératoire dans le cadre d'une chirurgie orthopédique majeure. Le paramètre d'efficacité primaire était le volume total requis de solution colloïdale. La variable d'efficacité primaire, soit le volume total requis de solution colloïdale pour une substitution de volume peropératoire, était identique pour les deux groupes étudiés. Le volume moyen était de 1613 ± 778 ml pour VOLUVEN MD et de 1584 ± 958,4 ml pour l'héta-amidon. Le ratio VOLUVEN MD /héta-amidon a été évalué à 1,024, dans un intervalle de confiance de 95 % [0,84;1,25]. Les résultats des quatre principales variables de sécurité sont indiqués dans le tableau suivant : Variable Moyenne Ratio VOLUVEN MD /héta-amidon VOLUVEN MD Héta-amidon Estimé I.C. à 95 % N=49 N=51 Perte de globules rouges calculée [l] 1,17 1,31 0,910 [0,720;1,141] Facteur VIII [%] 100,5 81,4 1,244 [1,000;1,563] Facteur von Willebrand [%] Plasma frais congelé (ml) 97,7 88,7 1,128 [0,991;1,285] ,723 [0,000;2,437] On a observé une différence significative entre les groupes étudiés au niveau de l'apport de liquides pour la somme des globules rouges du culot globulaire, du sang récupéré et du sang d'autres sources, en termes de ml/kg de poids corporel (8,0 ml/kg contre 13,8 ml/kg). Il n'y avait pas de différence significative en termes d'effets indésirables entre les deux groupes. Trois cas de coagulopathies graves se sont produits, mais uniquement dans le groupe traité à l'héta-amidon. Toutefois, les trois cas avait également reçu des doses élevées (plus de 3000 ml), reconnues comme augmentant le risque d'effet du médicament sur le système de coagulation. Relativement aux critères d'efficacité secondaires de stabilité hémodynamique, de température corporelle, de paramètres hémodynamiques, de tension artérielle, de pression veineuse centrale, de fréquence cardiaque, de fibrinogène et de plaquettes, il n'y avait pas de différence statistiquement significative entre les deux groupes de traitement. Monographie de produit: VOLUVEN MD ver 3.2 Page 19 de 27
20 PHARMACOLOGIE DÉTAILLÉE L'effet pharmacodynamique du HEA 130/0,4 à 6 % a été examiné dans le cadre d'un modèle de choc sur des rats conscients et d'un modèle alternatif sur des chiens. Dans les deux études, le groupe témoin a reçu le HEA 200/0,5 à 6 % (penta-amidon). La solution d'hea 130/0,4 à 6 % avait la même efficacité que la solution d'hea 200/0,5 à 6 % dans le maintien des fonctions cardio-respiratoires durant l'hémodilution isovolémique chez des beagles. Aucune administration supplémentaire de colloïde ne s'est avérée nécessaire au cours de la période de suivi de 3 heures. Il n'y a eu aucune différence de survie à long terme entre les rats du groupe ayant reçu une seule administration de solution HEA 130/0,4 à 6 % et ceux du groupe ayant reçu une seule administration de solution HEA 200/0,5 à 6 %, à la suite d'un choc hémorragique provoqué (perte de sang de 67 % et de 50 %). Dans le volet ayant reçu la solution d'hea 130/0,4 à 6 %, le groupe ayant subi une perte de sang de 67 % a eu un taux de survie de 83 %, puisqu'un animal est mort. Toutefois, le décès d'un animal est normal dans le cadre de ce type d'expérience. Dans le groupe correspondant ayant reçu la solution d'hea 200/0,5 à 6 %, le taux de survie s'est élevé à 100 %. La perfusion d une solution physiologique de Ringer a résulté en un taux de survie de 50 %, à la suite d'une perte de sang de 50 % et à un taux de survie de 0 % à la suite d'une perte de sang de 67 %. En conclusion, dans le cadre de cette expérience avec des rats, la solution d'hea 130/0,4 à 6 % a eu un effet salvateur équivalent à la solution d'hea 200/0,5 à 6 %. Après plusieurs administrations intraveineuses de 0,7 g par kg de poids corporel par jour, de solution d'hea 130/0,4 à 10 % ou de solution d'hea 200/0,5 à 10 %, pendant 18 jours consécutifs, la concentration d'hea plasmatique chez les rats traités avec de la solution d'hea 130/0,4 à 10 % était inférieure à celle des rats traités avec la solution d'hea 200/0,5 à 10 %. La solution d'hea 130/0,4 à 10 % était éliminée plus rapidement que l'hea 200/0,5 à 10 %. Chez les rats des deux groupes, des signes évidents d'entreposage d'hea dans les tissus ont été décelés dans les ganglions lymphatiques et dans la rate. Plusieurs vacuoles vides ont été observées dans les cellules macrophages. Une vacuolisation cellulaire minime a été décelée dans le foie et les reins. Aucune différence histochimique entre les deux groupes n'a été observée. Par conséquent, une étude avec des solutions radiomarquées 14 C-HEA 130/0,4 à 10 % et 14 C- HEA 200/0,5 à 10 % a été réalisée. Chez les animaux traités avec l'hea 130, le niveau de radioactivité a diminué, passant de 4,3 % de la dose administrée totale (2,6 g d'hea 130/animal) le 3e jour à 0,6 % le 52e jour. Chez les animaux traités avec l'hea 200/0,5, l'activité du carbone 14 a diminué, passant de 7,7 % de la dose administrée totale (2,7 g d'hea 200/animal) le 3e jour, à 2,45 % le 52e jour. Ces résultats confirment l'élimination plus rapide de la solution d'hea 130/0,4 et sa persistance moindre dans les tissus. Monographie de produit: VOLUVEN MD ver 3.2 Page 20 de 27
21 MICROBIOLOGIE Sans objet. TOXICOLOGIE Toxicité des administrations répétées La perfusion intraveineuse de 90 ml par kg de poids corporel par jour d HEA 130/0,4 à 10 %, perfusé durant 3 heures par jour chez des rats et des chiens durant une période de 3 mois, s est soldé par la constatation d aucun signe de toxicité excessive, sauf pour une surcharge de travail pour les reins et le foie, la capture et le métabolisme de l hydroxyéthylamidon dans le système réticulo-endothélial, dans la parenchyme hépatique et dans d autres tissus associés à l état non physiologique des animaux durant la période d étude. Toxicité affectant le système de reproduction L HEA 130/0,4 n a pas eu d effet tératogénique chez les rates et les lapines. Des effets embryolétals ont été observés chez des lapines lors d administrations de doses de 50 ml/kg de poids corporel/jour d HEA 130/0,4 à 10 %. Chez les rates, l injection par bolus de cette dose durant la grossesse et l allaitement a réduit le poids corporel des rejetons et induit des retards de développement. Cependant, les effets toxiques sur l embryon/fœtus chez les rates et les lapines ont été observés uniquement lorsque la dose administrée était maternellement toxique. Des signes de surcharge liquidienne ont été observés chez les mères. Des études de fertilité sur des animaux directement exposés n ont pas été menées. Étude des propriétés mutagènes Aucun effet mutagène n'a été observé relativement à la solution d'hea 130/0,4 à 10 %, à la suite des tests d'activité mutagène suivants : dosage de mutation inverse de la Salmonella typhimurium (in vitro), cellules de mammifères dans le dosage in vitro de mutation génique (HPRT), évaluation de l'activité clastogène des lymphocytes périphériques humains de culture (in vitro) et test cytogénétique de la moelle osseuse sur des rats Sprague-Dawley. Étude de la sensibilisation Au cours d'une étude de sensibilisation cutanée, 30 cobayes Dunkin-Hartley mâles ont été traités de manière intradermique et topique avec une solution non diluée d'hea 130/0,4 à 10 % afin d'examiner l'irritation locale causée par cette dernière. Les animaux du groupe témoin ont été traités avec une solution isotonique de NaCl (groupe témoin négatif). Le groupe témoin positif a été traité avec du bichromate de potassium. Monographie de produit: VOLUVEN MD ver 3.2 Page 21 de 27
22 Aucune irritation cutanée après l'application de la solution d'hea 130/0,4 à 10 % n'a été observée. La solution d'hea 130/0,4 à 10 % ne comporte aucune propriété de sensibilisation. Étude d'absence d'antigénicité Une étude sur cinq cobayes Dunkin-Hartley femelles a été réalisée afin de démontrer l'absence d'antigénicité de la solution d'hea 130/0,4 à 10 % chez les cobayes sensibilisés. Après la période de sensibilisation de 48 jours, les animaux ont reçu 3 ml d'hea 130/0,4 à 10 % par intraveineuse. Aucune propriété de sensibilisation du HEA 130/0,4 à 10 % n'a été observée chez ce modèle animal. Étude de compatibilité sanguine Une étude visant à examiner les propriétés hémolytiques de la solution d'hea 130/0,4 à 10 % sur les globules rouges humains a été réalisée. Une solution non diluée d'hea 130/0,4 à 10 % n'a eu aucun effet hémolytique sur les globules rouges humains. Dans une étude in vitro, VOLUVEN MD et l HEA 130/0,4 à 6 % dans une solution isotonique d électrolytes pour injection, n ont ni l un ni l autre causé d hémolyse dans le sang humain complet. Étude de tolérance locale Dans une étude de tolérance locale, 12 lapins himalayens (6 mâles et 6 femelles) on reçu une seule perfusion intraveineuse (300 ml d HEA 130/0,4 à 10 %/3 heures/animal), une perfusion intra-artérielle (300 ml d HEA 130/0,4 à 10 %/3 heures/animal), une perfusion paraveineuse (0,5 ml d HEA 130/0,4 à 10 %/animal) et une injection sous-cutanée (1 ml d HEA 130/0,4 à 10 %/animal). La solution isotonique saline (NaCl à 0,9 %) a servi de témoin négatif. Dans le cadre de ces conditions d'expérience, la solution d'hea 130/0,4 à 10 % a démontré une bonne tolérance locale chez les lapins à la suite d'une perfusion intraveineuse d'un niveau de dose correspondant à environ quatre à cinq fois le niveau administré aux humains. Les examens microscopiques n'ont pas décelé de changement local lié à la substance injectée. Dans une autre étude de tolérance locale menée chez des lapins blancs de la Nouvelle-Zélande, VOLUVEN MD et l HEA 130/0,4 à 6 % dans une solution isotonique d électrolytes pour injection ont tous deux été administrés au site prévu d administration intraveineuse ainsi qu à des sites d injection non conventionnels (intra-artériel, paraveineux, sous-cutané et intramusculaire). VOLUVEN MD et l HEA 130/0,4 à 6 % dans une solution isotonique d électrolytes pour injection ont tous deux montré une bonne tolérance locale chez les lapins après une perfusion intraveineuse et aucune différence n a été signalée entre les deux solutions d HEA. Monographie de produit: VOLUVEN MD ver 3.2 Page 22 de 27
23 RÉFÉRENCES 1. Bork K. Pruritus precipitated by hydroxyethyl starch: a review. Brit J Dermatol 2005; 152: Ellger B, Freyhoff J, van Aken H et al. High-dose volume replacement using HES 130/0.4 during major surgery: Impact on coagulation and incidence of postoperative itching. Ned Tijdschr Anesth 2006; 19: Gandhi S, Warltier D, Weiskopf R, et al. Volume substitution therapy with HES 130/0.4 (VOLUVEN ) versus HES 450/0.7 (hetastarch) during major orthopedic surgery. Crit. Care 2005; 9(Suppl 1): Hoffmann JN, Vollmar B, Laschke M, et al. Hydroxyethyl Starch (130 kd), but Not Crystalloid Volume Support, Improves Microcirculation during Normotensive Endotoxemia. Anesthesiology 2002; 97: Gallandat Huet RCG, Siemons AW, Baus D, et al. A novel hydroxyethyl starch (VOLUVEN) for effective perioperative plasma volume substitution in cardiac surgery. Can J Anaesth 2000; 47: Ickx BE, Rigolet M, Van der Linden PJ. Cardiovascular and metabolic response to acute normovolemic Anemia. Anesthesiology 2000; 93: Jungheinrich C, Scharpf R, Wargenau M, et al. The pharmacokinetics and tolerability of an intravenous infusion of the new hydroxyethyl starch 130/0.4 (6%, 500mL) in mild-tosevere renal impairment. Anesth Analg 2002; 95: Jungheinrich C, Sauermann W, Bepperling F, Vogt NH. Volume efficacy and reduced influence on measures of coagulation using hydroxyethyl starch 130/0.4 (6%) with an optimised in vivo molecular weight in orthopaedic surgery a randomised, double-blind study. Drugs R D 2004; 5: Jungheinrich C, Neff T. Pharmacokinetics of Hydroxyethyl Starch. Clin Pharmacokinet 2005; 44: Kasper SM, Strömich A, Kampe S, et al. Evaluation of a new hydroxyethyl starch solution (HES 130/0.4) in patients undergoing preoperative autologous blood donation. J Clin Anesth 2001; 13: Kasper SM, Meinert P, Kampe S, et al. Large-dose Hydroxyethyl Starch 130/0.4 Does Not Increase Blood Loss and Transfusion Requirements in Coronary Artery Bypass Surgery Compared with Hydroxyethyl Starch 200/0.5 at Recommended Doses. Anesthesiology 2003; 99: Koehler H, Kirch W, Weihrauch TR, et al. Macroamylasia after treatment with hydroxyethyl starch. Eur J Clin Invest 1977; 7: Köhler H, Zschiederich H, Linfante A, et al. The elimination of Hydroxyethyl Starch 200/0.5, Dextran 40 and Oxypolygelatin. Klin Wochenschr 1982; 60: Monographie de produit: VOLUVEN MD ver 3.2 Page 23 de 27
24 14. Kozek-Langenecker S. Effects of Hydroxyethyl Starch Solutions on Hemostasis. Anesthesiology 2005; 103: Langeron O, Doelberg M, Eng-Than A, et al. Volume replacement during major orthopedic surgery: a new 6% hydroxyethyl starch solution (HES 130/0.4) might reduce blood loss. Anesth Analg 2001; 92: Leuschner J, Opitz J, Winkler A, Scharpf R, Bepperling F. Tissue storage of 14 C-labelled hydroxyethyl starch (HES) 130/0.4 and HES 200/0.5 after repeated intravenous administration to rats. Drugs R D 2003; 4(6): Lochbühler H, Galli C, Hagemann H, Hydroxyethyl starch HES 130/0.4 in paediatric surgery: results of an explorative, controlled, multicenter safety study. Crit Care 2003; 7: Neff TA, Dölberg M, Jungheinrich C, et al. Repetitive large-dose, infusion of the novel hydroxyethyl starch HES 130/0.4 in patients with severe head injury. Anesth Analg, 2003; 96: Rudolf J. Hydroxyethyl Starch for Hypervolemic Hemodilution in Patients with Acute Ischemic Stroke: A Randomized, Placebo-Controlled Phase II Safety Study, Cerebrovascular Diseases 2002; 14: Standl T, Burmeister MC, Schroeder F, et al. Hydroxyethyl starch (HES) 130/0.4 provides larger and faster increases in tissue oxygenation in comparison with prehemodilution values of HES 70/0.5 or HES 200/0.5 in volunteers undergoing achte normovolemic hemodilution. Anesth Analg 2003; 96: Van der Linden Ph, De Hert S, Deraedt D, et al. Hydroxyethyl Starch 130/0.4 Versus Modified Fluid Gelatin for Volume Expansion in Cardiac Surgery Patients: The Effects on Perioperative Bleeding and Transfusion Needs. Anesth. Analg. 2005; 101: Waitzinger J, Bepperling F, Pabst G, et al. Pharmacokinetics and tolerability of a new hydroxyethyl starch (HES) specification [HES (130/0.4)] after single-dose infusion of 6% or 10% solutions in healthy volunteers. Clin Drug Invest 1998; 16: Waitzinger J, Bepperling, F, Pabst G, et al. Effect of a new hydroxyethyl starch (HES) specification [6% HES (130/0.4)] on blood and plasma volumes after bleeding in 12 healthy male volunteers. Clin Drug Invest 1999; 17: Waitzinger J, Bepperling F, Pabst G, et al. Hydroxyethyl starch (HES) [130/0.4], a new HES specification. Pharmacokinetics and safety after multiple infusions of 10% solution in healthy volunteers. Drugs R D 2003; 4: Monographie de produit: VOLUVEN MD ver 3.2 Page 24 de 27
25 IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR VOLUVEN MD Hydroxyéthylamidon 130/0,4 à 6 % dans une solution de chlorure de sodium à 0,9 % pour injection Le présent dépliant constitue la troisième et dernière partie d une «monographie de produit» publiée à la suite de l approbation de la vente au Canada de VOLUVEN MD et s adresse tout particulièrement aux consommateurs. Le présent dépliant n est qu un résumé et ne donne donc pas tous les renseignements pertinents au sujet de la VOLUVEN MD. Pour toute question au sujet de ce médicament, communiquez avec votre médecin ou votre pharmacien. AU SUJET DE CE MÉDICAMENT Les raisons d utiliser ce médicament : VOLUVEN MD, une solution qui doit être administrée dans une veine, est utilisée pour le traitement d un volume de sang trop faible (pas assez de sang dans votre corps). VOLUVEN MD n est pas un substitut de globules rouges ni un substitut des facteurs de coagulation dans le plasma. Les effets de ce médicament : VOLUVEN MD fait partie d un groupe de médicaments connus comme des liquides de remplissage vasculaire. VOLUVEN MD fonctionne durant plusieurs heures en augmentant le volume du sang en circulation. Les circonstances où il est déconseillé d utiliser ce médicament : Votre médecin ne vous administrera pas le VOLUVEN MD si : vous avez trop de liquide dans votre corps; vous avez une infection généralisée grave; vous avez été diagnostiqué d un œdème pulmonaire faisant en sorte que vos poumons contiennent trop de liquide; vous avez été diagnostiqué d une insuffisance cardiaque congestive (un trouble faisant en sorte que votre cœur est incapable de faire parvenir suffisamment de sang aux autres organes de votre corps); vous avez une insuffisance rénale, vous produisez peu ou pas d'urine et ce trouble n'est pas causé par un faible volume sanguin; vous recevez un traitement de dialyse (un traitement par rein artificiel); vous avez une maladie hépatique grave; vous souffrez de saignements à l'intérieur ou autour du cerveau (hémorragie intracrânienne); vous avez une concentration extrêmement élevée de sodium ou de chlorure dans votre sang; vous êtes allergique (hypersensible) à l'amidon hydroxyéthylé ou à tout autre ingrédient de ce médicament. L ingrédient médicinal est : Hydroxyéthylamidon 130/0,4 à 6 % dans une solution de chlorure de sodium à 0,9 % pour injection. Les ingrédients non médicinaux sont : Chlorure de sodium, eau pour injection ; ph ajusté au moyen d hydroxyde de sodium ou d acide hydrochlorique. Concentration approximative d électrolytes par litre : sodium (Na + ) 154 mmol, chlorure (Cl - ) 154 mmol.. Les formes posologiques sont : Solution pour perfusion. L'hydroxyéthylamidon 130/0,4 à 6 % dans une solution de chlorure de sodium à 0,9 % pour injection est fourni dans des sacs en plastique de 250 ou 500 ml. MISES EN GARDE ET PRÉCAUTIONS Consultez votre médecin ou votre personnel infirmier AVANT d utiliser VOLUVEN MD si : avez des troubles rénaux ou cardiaques; souffrez de troubles de saignement. Autres mises en garde et précautions. Votre médecin doit s'assurer de ne pas dépasser la dose recommandée afin de ne pas entraîner d'hyperhydratation qui risque de modifier les conditions sanguines, telles que la capacité de coagulation du sang, ou d'altérer certains facteurs sanguins (hématocrite, protéines sanguines). Votre médecin peut surveiller votre fonction rénale, les électrolytes dans votre sang et votre équilibre liquidien afin de maintenir une hydratation adéquate. Ce médicament peut augmenter de manière temporaire la concentration d'enzyme amylase sérique et pourrait nuire au diagnostic de l'inflammation du pancréas (la pancréatite). Des démangeaisons ou des réactions allergiques à la suite de l administration de VOLUVEN MD peuvent survenir. Informez votre médecin si vous remarquez des symptômes inhabituels. Monographie de produit: VOLUVEN MD ver 3.2 Page 25 de 27
26 IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT Utilisation durant la grossesse VOLUVEN MD doit être utilisé au cours de la grossesse uniquement si les avantages potentiels justifient les risques potentiels pour le fœtus. Femmes qui allaitent On ne sait pas si l'hea 130/0,4 est excrété dans le lait maternel humain. Puisque plusieurs médicaments sont excrétés dans le lait maternel, la prudence est de mise lorsque VOLUVEN MD est considéré pour une femme qui allaite. Vous et votre médecin devrez décider de poursuivre/cesser l allaitement ou d abandonner/continuer la thérapie par VOLUVEN MD en tenant compte des bienfaits de l allaitement pour votre enfant et des bienfaits de la thérapie par VOLUVEN MD pour vous. INTERACTIONS MÉDICAMENTEUSES Compte tenu du caractère lacunaire des études d'interactions, il faut cependant éviter tout mélange avec d'autres médicaments. UTILISATION APPROPRIÉE DE CE MÉDICAMENT VOLUVEN MD est administré uniquement par perfusion intraveineuse. La dose et la durée du traitement devraient être individualisées. Le médecin traitant déterminera la dose appropriée. Surdose : En cas de surdosage du médicament, votre médecin cessera immédiatement la perfusion et si nécessaire, vous administrera des thérapies afin d éliminer l excès d eau de votre corps et il peut également contacter immédiatement le Centre anti-poison régional. PROCÉDURES À SUIVRE EN CE QUI CONCERNE LES EFFETS SECONDAIRES Démangeaisons. Résultats anormaux d épreuves sanguines, tels que la diminution de l hématocrite ou des protéines plasmatiques. La concentration l amylase sérique peut augmenter durant l administration de VOLUVEN MD et peut interférer avec le diagnostic de l inflammation du pancréas (pancréatite); cependant, VOLUVEN MD ne cause pas la pancréatite. EFFETS SECONDAIRES GRAVES : FRÉQUENCE ET PROCÉDURES À SUIVRE Symptôme / effet Rare Réactions allergiques produisant des symptômes semblables à ceux de la grippe; c.-à-d., fièvre, mal de tête, rythme cardiaque lent, rythme cardiaque rapide, bronchite, liquide dans les poumons non relié à des troubles cardiaques. Ecchymoses et saignements inhabituels. Informez votre médecin ou le personnel infirmier Seulement pour les cas graves Dans tous les cas Le médecin cessera le traitement Il ne s agit pas de la liste complète des effets secondaires possibles. Si vous ressentez un effet inattendu après avoir reçu VOLUVEN MD, informez votre médecin ou le personnel infirmier de la situation. COMMENT CONSERVER LE MÉDICAMENT Utilisez uniquement des solutions limpides et des contenants intacts. Les produits de médicaments administrés par voie parentérale devraient faire l'objet d'une inspection visuelle en vue de vérifier la limpidité et de déceler des particules, du précipité, de la décoloration et des fuites avant de procéder à l'administration. Les solutions qui ont un aspect flou, qui contiennent des particules ou du précipité, ou alors qui comportent de la décoloration ou des fuites ne doivent pas être utilisées. Jetez la portion inutilisée de la solution de médicament. N'utilisez pas VOLUVEN MD après sa date de péremption. Entreposage du sac freeflex MD : de 15 à 25 C. Ce produit doit être utilisé immédiatement après l'ouverture du Monographie de produit: VOLUVEN MD ver 3.2 Page 26 de 27
27 IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT contenant. Ne pas congeler. DÉCLARATION DES EFFETS INDÉSIRABLES SOUPÇONNÉS Vous pouvez déclarer les effets indésirables soupçonnés associés à l utilisation des produits de santé au Programme Canada Vigilance de l une des 3 façons suivantes : En ligne Par téléphone, en composant le numéro sans frais ; En remplissant un formulaire de déclaration de Canada Vigilance et en le faisant parvenir - par télécopieur, au numéro sans frais par la poste au: Programme Canada Vigilance Santé Canada Indice postal 0701D Ottawa (Ontario) K1A 0K9 Distribué par : Fresenius Kabi Canada Une division de Calea Ltd Skymark Ave. Unit 2 Mississauga (Ontario) L4W 4Y3 Canada Date de révision : 21 juin 2013 Voluven et freeflex sont des marques de commerce déposées de Fresenius Kabi AG. Les étiquettes affranchies, le formulaire de déclaration de Canada Vigilance ainsi que les lignes directrices concernant la déclaration d effets indésirables sont disponibles sur le site Web de MedEffet MC Canada à REMARQUE : Pour obtenir des renseignements relatifs à la gestion des effets secondaires, veuillez communiquer avec votre professionnel de la santé. Le Programme Canada Vigilance ne fournit pas de conseils médicaux. POUR DE PLUS AMPLES RENSEIGNEMENTS Le présent document et la monographie de produit complète, préparés pour les professionnels de la santé, peuvent être consultés à : ou en communiquant avec Fresenius Kabi Canada par téléphone au numéro sans frais suivant : La présente brochure a été préparée par Fresenius Kabi Deutschland GmbH D Bad Homburg vor der Höhe Allemagne Monographie de produit: VOLUVEN MD ver 3.2 Page 27 de 27
Notice publique PERDOLAN - PÉDIATRIE
 Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
Notice publique PERDOLAN - PÉDIATRIE Lisez attentivement cette notice jusqu'à la fin car elle contient des informations importantes pour vous. Ce médicament est délivré sans ordonnance. Néanmoins, vous
COMMISSION DE LA TRANSPARENCE AVIS. 19 octobre 2011
 COMMISSION DE LA TRANSPARENCE AVIS 19 octobre 2011 PEDIAVEN AP-HP G15, solution pour perfusion 1000 ml de solution en poche bi-compartiment, boîte de 4 (CIP: 419 999-0) PEDIAVEN AP-HP G20, solution pour
COMMISSION DE LA TRANSPARENCE AVIS 19 octobre 2011 PEDIAVEN AP-HP G15, solution pour perfusion 1000 ml de solution en poche bi-compartiment, boîte de 4 (CIP: 419 999-0) PEDIAVEN AP-HP G20, solution pour
NOTICE: INFORMATION DE L UTILISATEUR. Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain)
 NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
NOTICE: INFORMATION DE L UTILISATEUR Immukine 100 microgrammes/0,5 ml solution injectable (Interféron gamma-1b recombinant humain) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser
PIL Décembre 2009. Autres composants: acide tartrique, macrogol 4000, macrogol 1000, macrogol 400, butylhydroxyanisol.
 Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
Notice publique MOTILIUM Veuillez lire attentivement l intégralité de cette notice avant d utiliser ce médicament. Gardez cette notice, vous pourriez avoir besoin de la relire. Si vous avez d autres questions,
NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR. Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant
 B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
B. NOTICE 1 NOTICE : INFORMATIONS DESTINÉES A L UTILISATEUR Firazyr 30 mg solution injectable en seringue pré-remplie Icatibant Veuillez lire attentivement l intégralité de cette notice avant d utiliser
L AUTOGREFFE QUELQUES EXPLICATIONS
 L AUTOGREFFE QUELQUES EXPLICATIONS Le traitement de votre maladie nécessite une Chimiothérapie intensive. Cette chimiothérapie qui utilise de fortes doses de médicaments antimitotiques est plus efficace
L AUTOGREFFE QUELQUES EXPLICATIONS Le traitement de votre maladie nécessite une Chimiothérapie intensive. Cette chimiothérapie qui utilise de fortes doses de médicaments antimitotiques est plus efficace
ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR
 Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
Dénomination du médicament ANNEXE IIIB NOTICE : INFORMATION DE L UTILISATEUR LYSOPAÏNE MAUX DE GORGE AMBROXOL CITRON 20 mg SANS SUCRE, pastille édulcorée au sorbitol et au sucralose. Chlorhydrate d ambroxol
E04a - Héparines de bas poids moléculaire
 E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
E04a - 1 E04a - Héparines de bas poids moléculaire Les héparines de bas poids moléculaire (HBPM) sont un mélange inhomogène de chaînes polysaccharidiques obtenues par fractionnement chimique ou enzymatique
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE
 GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
GUIDE D INFORMATIONS A LA PREVENTION DE L INSUFFISANCE RENALE SOURCES : ligues reins et santé A LA BASE, TOUT PART DES REINS Organes majeurs de l appareil urinaire, les reins permettent d extraire les
NOTICE : INFORMATION DE L'UTILISATEUR. DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc
 NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
NOTICE : INFORMATION DE L'UTILISATEUR DAKTOZIN 2,5 mg/150 mg pommade Nitrate de miconazole et oxyde de zinc Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
Insuffisance cardiaque
 Insuffisance cardiaque Connaître son évolution pour mieux la vivre Guide d accompagnement destiné au patient et ses proches Table des matières L évolution habituelle de l insuffisance cardiaque 5 Quelles
Insuffisance cardiaque Connaître son évolution pour mieux la vivre Guide d accompagnement destiné au patient et ses proches Table des matières L évolution habituelle de l insuffisance cardiaque 5 Quelles
DON DE SANG. Label Don de Soi
 DON DE SANG Label Don de Soi 2015 SOMMAIRE Les différents types de dons p.3 Le don de sang total Le don de plasma Le don de plaquettes Le don de moelle osseuse Que soigne-t-on avec un don de sang? p.7
DON DE SANG Label Don de Soi 2015 SOMMAIRE Les différents types de dons p.3 Le don de sang total Le don de plasma Le don de plaquettes Le don de moelle osseuse Que soigne-t-on avec un don de sang? p.7
NOTICE : INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés Bisacodyl
 NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
NOTICE : INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament. Elle contient des informations importante s pour
Nouveaux Anticoagulants. Dr JF Lambert Service d hématologie CHUV
 Nouveaux Anticoagulants Dr JF Lambert Service d hématologie CHUV Plan Petit rappel d hémostase Anticoagulant oraux classiques Les nouveaux anticoagulants (NAC) Dosage? Comment passer de l'un à l'autre
Nouveaux Anticoagulants Dr JF Lambert Service d hématologie CHUV Plan Petit rappel d hémostase Anticoagulant oraux classiques Les nouveaux anticoagulants (NAC) Dosage? Comment passer de l'un à l'autre
Le don de moelle osseuse :
 DON DE MOELLE OSSEUSE Le don de moelle osseuse : se décider aujourd hui, s engager pour longtemps LA MOELLE OSSEUSE ET SA GREFFE La moelle osseuse C est le tissu mou dans le centre du corps des os qui
DON DE MOELLE OSSEUSE Le don de moelle osseuse : se décider aujourd hui, s engager pour longtemps LA MOELLE OSSEUSE ET SA GREFFE La moelle osseuse C est le tissu mou dans le centre du corps des os qui
Livret des nouveaux anticoagulants oraux. Ce qu il faut savoir pour bien gérer leur utilisation
 Livret des nouveaux anticoagulants oraux Ce qu il faut savoir pour bien gérer leur utilisation DONNÉES DU PATIENT Nom Adresse Tél MÉDECIN TRAITANT Nom Adresse Tél SPÉCIALISTE Nom Hôpital Tél MÉDICAMENT
Livret des nouveaux anticoagulants oraux Ce qu il faut savoir pour bien gérer leur utilisation DONNÉES DU PATIENT Nom Adresse Tél MÉDECIN TRAITANT Nom Adresse Tél SPÉCIALISTE Nom Hôpital Tél MÉDICAMENT
Parasites externes du chat et du chien
 Parasites externes du chat et du chien Identification, prévention et traitement Les tiques Les tiques transmettent des maladies parfois mortelles. La prévention est la meilleure arme. 1 - Où les trouve-t-on?
Parasites externes du chat et du chien Identification, prévention et traitement Les tiques Les tiques transmettent des maladies parfois mortelles. La prévention est la meilleure arme. 1 - Où les trouve-t-on?
Anémie et maladie rénale chronique. Phases 1-4
 Anémie et maladie rénale chronique Phases 1-4 Initiative de qualité en matière d issue des maladies rénales de la National Kidney Foundation Saviez-vous que l initiative de qualité en matière d issue des
Anémie et maladie rénale chronique Phases 1-4 Initiative de qualité en matière d issue des maladies rénales de la National Kidney Foundation Saviez-vous que l initiative de qualité en matière d issue des
Leucémies de l enfant et de l adolescent
 Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
NOTICE : INFORMATION DE L UTILISATEUR. Delphi 0,1 % crème Acétonide de triamcinolone
 NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
NOTICE : INFORMATION DE L UTILISATEUR Delphi 0,1 % crème Acétonide de triamcinolone Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes
COMMISSION DE LA TRANSPARENCE AVIS. 18 janvier 2006
 COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
Le RIVAROXABAN (XARELTO ) dans l embolie pulmonaire
 Le RIVAROXABAN (XARELTO ) dans l embolie pulmonaire Dr Florence Parent Service de Pneumologie et Soins Intensifs de Pneumologie Hôpital Bicêtre, AP-HP Inserm U999. Université Paris-Sud Traitement anticoagulant
Le RIVAROXABAN (XARELTO ) dans l embolie pulmonaire Dr Florence Parent Service de Pneumologie et Soins Intensifs de Pneumologie Hôpital Bicêtre, AP-HP Inserm U999. Université Paris-Sud Traitement anticoagulant
Les nouveaux anticoagulants oraux (NAC)
 Les nouveaux anticoagulants oraux (NAC) Dr Jean-Marie Vailloud Cardiologue libéral/ salarié (CHU/clinique) Pas de lien d'intérêt avec une entreprise pharmaceutique Adhérent à l'association Mieux Prescrire
Les nouveaux anticoagulants oraux (NAC) Dr Jean-Marie Vailloud Cardiologue libéral/ salarié (CHU/clinique) Pas de lien d'intérêt avec une entreprise pharmaceutique Adhérent à l'association Mieux Prescrire
AMAMI Anaïs 3 C LORDEL Maryne. Les dons de cellules & de tissus.
 AMAMI Anaïs 3 C LORDEL Maryne Les dons de cellules & de tissus. Introduction : Une greffe (don) de cellules consiste à administrer à un patient dont un organe vital ne fonctionne plus correctement, une
AMAMI Anaïs 3 C LORDEL Maryne Les dons de cellules & de tissus. Introduction : Une greffe (don) de cellules consiste à administrer à un patient dont un organe vital ne fonctionne plus correctement, une
Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM)
 Hématologie biologique (Pr Marc Zandecki) Faculté de Médecine CHU 49000 Angers France Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM) 1. Structure et mode d'action
Hématologie biologique (Pr Marc Zandecki) Faculté de Médecine CHU 49000 Angers France Surveillance biologique d'un traitement par Héparine de Bas Poids Moléculaire (HBPM) 1. Structure et mode d'action
Bien vous soigner. avec des médicaments disponibles sans ordonnance. juin 2008. Douleur. de l adulte
 Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
Bien vous soigner avec des médicaments disponibles sans ordonnance juin 2008 Douleur de l adulte Douleur de l adulte Ce qu il faut savoir La douleur est une expérience sensorielle et émotionnelle désagréable,
COMMISSION DE LA TRANSPARENCE. Avis. 3 septembre 2008
 COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
Professeur Diane GODIN-RIBUOT
 UE3-2 - Physiologie rénale Chapitre 5 : Mesure de la fonction rénale : la clairance rénale Professeur Diane GODIN-RIBUOT Année universitaire 2011/2012 Université Joseph Fourier de Grenoble - Tous droits
UE3-2 - Physiologie rénale Chapitre 5 : Mesure de la fonction rénale : la clairance rénale Professeur Diane GODIN-RIBUOT Année universitaire 2011/2012 Université Joseph Fourier de Grenoble - Tous droits
NOTICE: INFORMATION DE L UTILISATEUR. Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl)
 NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
NOTICE: INFORMATION DE L UTILISATEUR Dulcolax bisacodyl 5 mg comprimés enrobés (bisacodyl) Veuillez lire attentivement cette notice avant de prendre ce médicament. Elle contient des informations importantes
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR Pr BETASERON Interféron bêta-1b Le présent dépliant constitue la troisième et dernière partie de la monographie de produit publiée à la suite de l approbation
Transfusions sanguines, greffes et transplantations
 Transfusions sanguines, greffes et transplantations Chiffres clés en 2008 La greffe d organes est pratiquée depuis plus de 50 ans. 4 620 malades ont été greffés. 1 563 personnes ont été prélevées. 222
Transfusions sanguines, greffes et transplantations Chiffres clés en 2008 La greffe d organes est pratiquée depuis plus de 50 ans. 4 620 malades ont été greffés. 1 563 personnes ont été prélevées. 222
La Greffe de Cellules Souches Hématopoïétiques
 La Greffe de Cellules Souches Hématopoïétiques Professeur Ibrahim Yakoub-Agha CHRU de LILLE (Illustration de J. Cloup, extraite du CD-Rom «greffe de Moelle» réalisé par la société K Noë) La moelle osseuse
La Greffe de Cellules Souches Hématopoïétiques Professeur Ibrahim Yakoub-Agha CHRU de LILLE (Illustration de J. Cloup, extraite du CD-Rom «greffe de Moelle» réalisé par la société K Noë) La moelle osseuse
FICHE D INFORMATION AVANT UNE TRANSFUSION
 FICHE D INFORMATION AVANT UNE TRANSFUSION Madame, Monsieur, Si votre état de santé nécessite une transfusion sanguine, ce document est destiné à vous informer sur les avantages et les risques de la transfusion,
FICHE D INFORMATION AVANT UNE TRANSFUSION Madame, Monsieur, Si votre état de santé nécessite une transfusion sanguine, ce document est destiné à vous informer sur les avantages et les risques de la transfusion,
Nouveaux anticoagulants oraux (NOAC)
 Nouveaux anticoagulants oraux (NOAC) Mécanisme d action Suivi biologique: comment et quand? A.Demulder IRIS-Lab 15/05/2013 1 Anticoagulants «traditionnels»: HNF Parentéral Suivi biologique avec ajustement
Nouveaux anticoagulants oraux (NOAC) Mécanisme d action Suivi biologique: comment et quand? A.Demulder IRIS-Lab 15/05/2013 1 Anticoagulants «traditionnels»: HNF Parentéral Suivi biologique avec ajustement
L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE
 L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE NEUCHATEL, Suisse, 7 avril/prnewswire/ -- - LA LENALIDOMIDE est évaluée par l EMEA comme thérapie orale pour
L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE NEUCHATEL, Suisse, 7 avril/prnewswire/ -- - LA LENALIDOMIDE est évaluée par l EMEA comme thérapie orale pour
Toxicité à long-terme d un herbicide Roundup et d un maïs modifié génétiquement pour tolérer le Roundup
 A l attention de toutes les personnes qui se méfient des jugements de valeur fussent-ils émis par des scientifiques- et qui préfèrent capter les informations à leur source pour s en faire une opinion personnelle.
A l attention de toutes les personnes qui se méfient des jugements de valeur fussent-ils émis par des scientifiques- et qui préfèrent capter les informations à leur source pour s en faire une opinion personnelle.
Le Don de Moelle Ça fait pas d mal!
 Le Don de Moelle Ça fait pas d mal! J ai de 18 à 50 ans Le Don de Moelle Osseuse Ça m intéresse -1 je demande des infos, je réfléchis. -2 je contacte le centre EFS le plus proche de chez moi. 3- je suis
Le Don de Moelle Ça fait pas d mal! J ai de 18 à 50 ans Le Don de Moelle Osseuse Ça m intéresse -1 je demande des infos, je réfléchis. -2 je contacte le centre EFS le plus proche de chez moi. 3- je suis
Guide de Mobilisation. de cellules souches pour mon. Autogreffe AVEC LE SOUTIEN DE. Carnet d informations et de suivi pour le patient et sa famille
 Guide de Mobilisation de cellules souches pour mon Autogreffe Carnet d informations et de suivi Carnets pour d informations le patient et sa et famille de suivi pour le patient et sa famille AVEC LE SOUTIEN
Guide de Mobilisation de cellules souches pour mon Autogreffe Carnet d informations et de suivi Carnets pour d informations le patient et sa et famille de suivi pour le patient et sa famille AVEC LE SOUTIEN
ANTICORPS POLYCLONAUX ANTI IMMUNOGLOBULINES
 L OUTIL IDEAL POUR TOUTES LES DETECTIONS IMMUNOCHIMIQUES pour toutes les techniques immunodosages (EIA/ELISA) dot/ westernblot immunohistochimie immunocytochimie cytométrie en flux quel que soit le système
L OUTIL IDEAL POUR TOUTES LES DETECTIONS IMMUNOCHIMIQUES pour toutes les techniques immunodosages (EIA/ELISA) dot/ westernblot immunohistochimie immunocytochimie cytométrie en flux quel que soit le système
Carnet de suivi Lithium
 Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
Carnet de suivi Lithium Brochure d information sur les troubles bipolaires et leur traitement par lithium Nom : Ce carnet est important Si vous le trouvez, merci de le faire parvenir à l adresse cidessous
Les anticoagulants. PM Garcia Sam Hamati. sofomec 2008
 Les anticoagulants PM Garcia Sam Hamati sofomec 2008 1 Les anticoagulants sofomec 2008 point de vue HAS AVK = 13% des hospitalisations pour accidents iatrogènes 17 000 hospitalisations / an /France pas
Les anticoagulants PM Garcia Sam Hamati sofomec 2008 1 Les anticoagulants sofomec 2008 point de vue HAS AVK = 13% des hospitalisations pour accidents iatrogènes 17 000 hospitalisations / an /France pas
LES NOUVEAUX ANTICOAGULANTS
 LES NOUVEAUX ANTICOAGULANTS Pr. Alessandra Bura-Rivière, Service de Médecine Vasculaire Hôpital Rangueil, 1 avenue Jean Poulhès, 31059 Toulouse cedex 9 INTRODUCTION Depuis plus de cinquante ans, les héparines
LES NOUVEAUX ANTICOAGULANTS Pr. Alessandra Bura-Rivière, Service de Médecine Vasculaire Hôpital Rangueil, 1 avenue Jean Poulhès, 31059 Toulouse cedex 9 INTRODUCTION Depuis plus de cinquante ans, les héparines
The consent form is also available in English.
 Université McGill et hôpitaux affiliés Centre universitaire de santé McGill (CUSM) Hôpital général juif - Sir Mortimer B. Davis The Sir Mortimer B. Davis - Jewish General Hospital Centre hospitalier de
Université McGill et hôpitaux affiliés Centre universitaire de santé McGill (CUSM) Hôpital général juif - Sir Mortimer B. Davis The Sir Mortimer B. Davis - Jewish General Hospital Centre hospitalier de
Que sont les. inhibiteurs?
 Que sont les inhibiteurs? TABLE DES MATIÈRES Publié par la Fédération mondiale de l hémophilie (FMH) Fédération mondiale de l hémophilie, 2010 La FMH encourage la redistribution de ses publications à des
Que sont les inhibiteurs? TABLE DES MATIÈRES Publié par la Fédération mondiale de l hémophilie (FMH) Fédération mondiale de l hémophilie, 2010 La FMH encourage la redistribution de ses publications à des
MONOGRAPHIE DE PRODUIT
 MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
MONOGRAPHIE DE PRODUIT Pr ESBRIET Capsules de pirfénidone 267 mg Antifibrosant et anti-inflammatoire Hoffmann-La Roche Limitée 7070 Mississauga Road Mississauga (Ontario) L5N 5M8 Canada Date de révision
Vous et votre traitement anticoagulant par AVK (antivitamine K)
 Ce carnet a été réalisé sous la coordination de l Agence française de sécurité sanitaire des produits de santé (Afssaps). Vous et votre traitement anticoagulant par AVK (antivitamine K) Carte à découper
Ce carnet a été réalisé sous la coordination de l Agence française de sécurité sanitaire des produits de santé (Afssaps). Vous et votre traitement anticoagulant par AVK (antivitamine K) Carte à découper
Votre guide des définitions des maladies graves de l Assurance maladies graves express
 Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
QU EST-CE QUE LA PROPHYLAXIE?
 QU EST-CE QUE LA PROPHYLAXIE? TABLES DES MATIÈRES Publié par la Fédération mondiale de l hémophilie (FMH) Fédération mondiale de l hémophilie, 2014 La FMH encourage la traduction et la redistribution de
QU EST-CE QUE LA PROPHYLAXIE? TABLES DES MATIÈRES Publié par la Fédération mondiale de l hémophilie (FMH) Fédération mondiale de l hémophilie, 2014 La FMH encourage la traduction et la redistribution de
Monitoring de l hémoglobine au bloc opératoire Place d une mesure continue non invasive. C Decoene PH CHRU Lille
 Monitoring de l hémoglobine au bloc opératoire Place d une mesure continue non invasive C Decoene PH CHRU Lille objectif Le taux d hémoglobine intervient dans : Le transport d O2 L hémostase L équilibre
Monitoring de l hémoglobine au bloc opératoire Place d une mesure continue non invasive C Decoene PH CHRU Lille objectif Le taux d hémoglobine intervient dans : Le transport d O2 L hémostase L équilibre
TROISIÈME PARTIE : INFORMATION POUR LE PATIENT
 TROISIÈME PARTIE : INFORMATION POUR LE PATIENT REBIF (Interféron bêta-1a) Solution pour injection dans des seringues préremplies Ce livret représente la troisième partie de la «Monographie de produit»
TROISIÈME PARTIE : INFORMATION POUR LE PATIENT REBIF (Interféron bêta-1a) Solution pour injection dans des seringues préremplies Ce livret représente la troisième partie de la «Monographie de produit»
Le parcours en greffe de cellules hématopoïétiques : greffe allogénique
 Le parcours en greffe de cellules hématopoïétiques : greffe allogénique Introduction Cette brochure vise à vous familiariser avec la greffe de cellules hématopoïétiques (GCH). Elle présente en quelques
Le parcours en greffe de cellules hématopoïétiques : greffe allogénique Introduction Cette brochure vise à vous familiariser avec la greffe de cellules hématopoïétiques (GCH). Elle présente en quelques
ORDONNANCE COLLECTIVE
 ORDONNANCE COLLECTIVE Assurer le suivi des personnes recevant un Page 1 de 12 O.C. 6.5 Professionnels visés : Les infirmières qui possèdent la formation, les connaissances et les compétences nécessaires,
ORDONNANCE COLLECTIVE Assurer le suivi des personnes recevant un Page 1 de 12 O.C. 6.5 Professionnels visés : Les infirmières qui possèdent la formation, les connaissances et les compétences nécessaires,
M.S - Direction de la réglementation et du contentieux - BASE DE DONNEES. REFERENCE : B O N 5070 du 2 janvier 2003
 REFERENCE : B O N 5070 du 2 janvier 2003 Décret n 2-01-1643 du 2 chaabane 1423 9/10/2002 pris pour l'application de la loi n 16-98 relative au don, au prélèvement et à la transplantation d'organes et de
REFERENCE : B O N 5070 du 2 janvier 2003 Décret n 2-01-1643 du 2 chaabane 1423 9/10/2002 pris pour l'application de la loi n 16-98 relative au don, au prélèvement et à la transplantation d'organes et de
NOTICE : INFORMATION DE L UTILISATEUR. Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants. Acide acétylsalicylique
 NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
NOTICE : INFORMATION DE L UTILISATEUR Asaflow 80 mg, comprimés gastro-résistants Asaflow 160 mg, comprimés gastro-résistants Acide acétylsalicylique Veuillez lire attentivement cette notice avant d utiliser
Suivi Biologique des Nouveaux Anticoagulants
 Suivi Biologique des Nouveaux Anticoagulants M.M. Samama, M-H. Horellou, C. Flaujac, J. Conard Groupe Hémostase-Thrombose Hôtel-Dieu L. Le Flem, C. Guinet, F. Depasse Biomnis - Ivry sur Seine TFPI TFPI
Suivi Biologique des Nouveaux Anticoagulants M.M. Samama, M-H. Horellou, C. Flaujac, J. Conard Groupe Hémostase-Thrombose Hôtel-Dieu L. Le Flem, C. Guinet, F. Depasse Biomnis - Ivry sur Seine TFPI TFPI
Un environnement sans fumée pour vos enfants. Comment y parvenir?
 Un environnement sans fumée pour vos enfants. Comment y parvenir? Renseignements sur la fumée secondaire et tertiaire Qu est-ce que la fumée secondaire? La fumée secondaire est une combinaison de fumée
Un environnement sans fumée pour vos enfants. Comment y parvenir? Renseignements sur la fumée secondaire et tertiaire Qu est-ce que la fumée secondaire? La fumée secondaire est une combinaison de fumée
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES :
 FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
FIPROTEC, PIPETTES CONTRE PUCES ET TIQUES : FIPROTEC 50 MG SOLUTION SPOT-ON POUR CHAT Composition :Une pipette de 0,50 ml contient 50 mg de Fipronil. Indications d utilisation : Chez les chats : - Traitement
WHA63.12 Disponibilité, innocuité et qualité des produits sanguins 4,5
 WHA63/200/REC/ WHA63.2 Disponibilité, innocuité et qualité des produits sanguins... 9 WHA63.2 Disponibilité, innocuité et qualité des produits sanguins 4,5 La Soixante-Troisième Assemblée mondiale de la
WHA63/200/REC/ WHA63.2 Disponibilité, innocuité et qualité des produits sanguins... 9 WHA63.2 Disponibilité, innocuité et qualité des produits sanguins 4,5 La Soixante-Troisième Assemblée mondiale de la
GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral intramusculaire
 ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
ésumé des Caractéristiques du Produit 1 sur 5 21/09/2010 14:31 Mis à jour : 16/02/2010 1. DENOMINATION DU MEDICAMENT GONADOTROPHINE CHORIONIQUE ENDO 5000 U.I./1 ml, lyophilisat et solution pour usage parentéral
Diatélic DP : télémédecine pour la prévention des aggravations de santé des dialysés à domicile
 DP : télémédecine pour la prévention des aggravations de santé des dialysés à domicile Jacques CHANLIAU, François CHARPILLET, Pierre-Yves DURAND, Robert HERVY, Jean-Pierre THOMESSE, Luis VEGA Résumé. DP
DP : télémédecine pour la prévention des aggravations de santé des dialysés à domicile Jacques CHANLIAU, François CHARPILLET, Pierre-Yves DURAND, Robert HERVY, Jean-Pierre THOMESSE, Luis VEGA Résumé. DP
1 La scintigraphie myocardique au Persantin ou Mibi Persantin
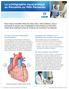 La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
La scintigraphie myocardique au Persantin ou Mibi Persantin Pour mieux connaître l état de votre cœur, votre médecin vous a demandé de passer une scintigraphie myocardique au Persantin. Cette fiche explique
L INSUFFISANCE CARDIAQUE
 L INSUFFISANCE CARDIAQUE EXISTE-T-IL DES TRAITEMENTS À BASE DE CELLULES SOUCHES POUR L INSUFFISANCE CARDIAQUE? Bien qu aucun traitement à base de cellules souches pour l insuffisance cardiaque n ait encore
L INSUFFISANCE CARDIAQUE EXISTE-T-IL DES TRAITEMENTS À BASE DE CELLULES SOUCHES POUR L INSUFFISANCE CARDIAQUE? Bien qu aucun traitement à base de cellules souches pour l insuffisance cardiaque n ait encore
Carte de soins et d urgence
 Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
Direction Générale de la Santé Carte de soins et d urgence Emergency and Healthcare Card Porphyries Aiguës Hépatiques Acute Hepatic Porphyrias Type de Porphyrie* Déficit en Ala déhydrase Ala Dehydrase
Informations sur le rivaroxaban (Xarelto md ) et l apixaban (Eliquis md )
 Informations sur le rivaroxaban (Xarelto md ) et l apixaban (Eliquis md ) Préambule Ce document présente plusieurs informations utiles pour les prescripteurs afin de les aider lors de l utilisation du
Informations sur le rivaroxaban (Xarelto md ) et l apixaban (Eliquis md ) Préambule Ce document présente plusieurs informations utiles pour les prescripteurs afin de les aider lors de l utilisation du
VOUS et VOTRE NOUVEAU TRAITEMENT anticoagulant Eliquis, Pradaxa, Xarelto
 VOUS et VOTRE NOUVEAU TRAITEMENT anticoagulant Eliquis, Pradaxa, Xarelto Carnet-conseils appartenant à :.... Adresse :......................... Tel :............................ Médecin Généraliste : Adresse
VOUS et VOTRE NOUVEAU TRAITEMENT anticoagulant Eliquis, Pradaxa, Xarelto Carnet-conseils appartenant à :.... Adresse :......................... Tel :............................ Médecin Généraliste : Adresse
Nouveaux anticoagulants oraux : gestion des accidents hémorragiques
 Nouveaux anticoagulants oraux : gestion des accidents hémorragiques PY Cordier Service de Réanimation HIA Laveran - Marseille Février 2014 Introduction Anticoagulants oraux : historique Antivitamines K
Nouveaux anticoagulants oraux : gestion des accidents hémorragiques PY Cordier Service de Réanimation HIA Laveran - Marseille Février 2014 Introduction Anticoagulants oraux : historique Antivitamines K
Fibrillation atriale chez le sujet âgé
 Dr Benoit Blanchard LE HAVRE Le 18 MARS 2014 Fibrillation atriale chez le sujet âgé Le plus fréquent des trouble du rythme cardiaque, 750,000 personnes atteintes de FA en France, 100,000 nouveaux cas chaque
Dr Benoit Blanchard LE HAVRE Le 18 MARS 2014 Fibrillation atriale chez le sujet âgé Le plus fréquent des trouble du rythme cardiaque, 750,000 personnes atteintes de FA en France, 100,000 nouveaux cas chaque
Atrovent HFA 20 mcg/bouffée solution pour inhalation en flacon pressurisé (bromure d'ipratropium)
 NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
NOTICE ATROVENT HFA 20 MCG/BOUFFEE SOLUTION POUR INHALATION EN FLACON PRESSURISE (BPI n 0250-03 du 27.07.2005) Veuillez lire attentivement l'intégralité de cette notice avant d'utiliser ce médicament.
French Version. Aciclovir Labatec 250 mg (For Intravenous Use Only) 02/2010. Product Information Leaflet for Aciclovir Labatec i.v.
 Product Information Leaflet for Aciclovir Labatec i.v. 250 mg French Version Aciclovir Labatec i.v. Composition Principe actif: Aciclovirum ut Acicloviri natricum (Praeparatio cryodesiccata). Excipients:
Product Information Leaflet for Aciclovir Labatec i.v. 250 mg French Version Aciclovir Labatec i.v. Composition Principe actif: Aciclovirum ut Acicloviri natricum (Praeparatio cryodesiccata). Excipients:
En considérant que l effet anticoagulant du dabigatran débute dans les 2 heures suivant la prise du médicament :
 Informations sur le dabigatran (Pradaxa md ) Préambule : Ce document présente plusieurs informations utiles pour les prescripteurs afin de les aider lors de l utilisation du dabigatran (Pradaxa md ). L
Informations sur le dabigatran (Pradaxa md ) Préambule : Ce document présente plusieurs informations utiles pour les prescripteurs afin de les aider lors de l utilisation du dabigatran (Pradaxa md ). L
Acides et bases. Acides et bases Page 1 sur 6
 Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
Le don de cellules souches. M.Lambermont Pascale Van Muylder
 Le don de cellules souches M.Lambermont Pascale Van Muylder 1 Pourquoi avons-nous recours à la greffe de CSH? Certaines maladies causent la destruction ou un fonctionnement anormal de la moelle osseuse.
Le don de cellules souches M.Lambermont Pascale Van Muylder 1 Pourquoi avons-nous recours à la greffe de CSH? Certaines maladies causent la destruction ou un fonctionnement anormal de la moelle osseuse.
Soins infirmiers et gestion des risques
 Soins infirmiers et gestion des risques I. Principe de précaution Hippocrate disait «soulager le malade et ne pas lui nuire» Cet adage «primun non cere» est le principe de la base de la médecine II. La
Soins infirmiers et gestion des risques I. Principe de précaution Hippocrate disait «soulager le malade et ne pas lui nuire» Cet adage «primun non cere» est le principe de la base de la médecine II. La
sur la valve mitrale À propos de l insuffisance mitrale et du traitement par implantation de clip
 À propos de l insuffisance mitrale et du traitement par implantation de clip sur la valve mitrale Support destiné aux médecins en vue d informer les patients. À propos de l insuffisance mitrale L insuffisance
À propos de l insuffisance mitrale et du traitement par implantation de clip sur la valve mitrale Support destiné aux médecins en vue d informer les patients. À propos de l insuffisance mitrale L insuffisance
Information à un nouveau donneur de cellules souches du sang
 Information à un nouveau donneur de cellules souches du sang Pour des raisons de simplification, les dénominations masculines s appliquent également aux femmes. La transplantation de cellules souches du
Information à un nouveau donneur de cellules souches du sang Pour des raisons de simplification, les dénominations masculines s appliquent également aux femmes. La transplantation de cellules souches du
1 - Que faut-il retenir sur les anticoagulants oraux?
 La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
La nouvelle convention pharmaceutique offre l opportunité aux pharmaciens d accompagner les patients traités par anticoagulants oraux au long cours afin de prévenir les risques iatrogéniques. Les anticoagulants
Des déficiences présentes
 Des déficiences présentes Comment se fait-il que dans certains cas, le système immunitaire ne fonctionne pas convenablement? Problèmes : 1. Pourquoi certains enfants sont-ils mis sous bulle plastique?
Des déficiences présentes Comment se fait-il que dans certains cas, le système immunitaire ne fonctionne pas convenablement? Problèmes : 1. Pourquoi certains enfants sont-ils mis sous bulle plastique?
Comprendre la mort cérébrale
 Comprendre la mort cérébrale Imprimeur de la Reine pour l Ontario, 2010. Adaptation et reproduction autorisées. 1 Comprendre la mort cérébrale Il est difficile d imaginer une expérience plus douloureuse
Comprendre la mort cérébrale Imprimeur de la Reine pour l Ontario, 2010. Adaptation et reproduction autorisées. 1 Comprendre la mort cérébrale Il est difficile d imaginer une expérience plus douloureuse
Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS)
 Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS) Édition Conseil du médicament www.cdm.gouv.qc.ca Coordination Anne Fortin, pharmacienne Élaboration Conseil du médicament Fédération
Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS) Édition Conseil du médicament www.cdm.gouv.qc.ca Coordination Anne Fortin, pharmacienne Élaboration Conseil du médicament Fédération
Observation. Merci à l équipe de pharmaciens FormUtip iatro pour ce cas
 Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
Cas clinique M. ZAC Observation Mr ZAC ans, 76 ans, 52 kg, est admis aux urgences pour des algies fessières invalidantes, résistantes au AINS. Ses principaux antécédents sont les suivants : une thrombopénie
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR. ANDROGEL Gel de testostérone à 1 %
 PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR ANDROGEL Gel de testostérone à 1 % Le présent dépliant constitue la troisième et dernière partie d une «monographie de produit» publiée à la suite de l
PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR ANDROGEL Gel de testostérone à 1 % Le présent dépliant constitue la troisième et dernière partie d une «monographie de produit» publiée à la suite de l
La lutte contre la tuberculose est régie par l arrêté royal du 17 octobre 2002.
 Le diagnostic de la tuberculose bovine La lutte contre la tuberculose est régie par l arrêté royal du 17 octobre 2002. 1. Tuberculination Dans la première phase d une infection de tuberculose bovine (Mycobacterium
Le diagnostic de la tuberculose bovine La lutte contre la tuberculose est régie par l arrêté royal du 17 octobre 2002. 1. Tuberculination Dans la première phase d une infection de tuberculose bovine (Mycobacterium
CONCOURS DE L INTERNAT EN PHARMACIE
 Ministère de l enseignement supérieur et de la recherche Ministère de la santé et des sports CONCOURS DE L INTERNAT EN PHARMACIE Valeurs biologiques usuelles Edition de Novembre 2009 (6 pages) Conseil
Ministère de l enseignement supérieur et de la recherche Ministère de la santé et des sports CONCOURS DE L INTERNAT EN PHARMACIE Valeurs biologiques usuelles Edition de Novembre 2009 (6 pages) Conseil
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine
 KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
KARDEGIC 75 mg, poudre pour solution buvable en sachet-dose Acétylsalicylate de DL-Lysine Veuillez lire attentivement cette notice avant d'utiliser ce médicament. Elle contient des informations importantes
Item 169 : Évaluation thérapeutique et niveau de preuve
 Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
et l utilisation des traitements biologiques
 et l utilisation des traitements biologiques Choisir le meilleur traitement pour retrouver la qualité de vie que vous êtes en droit d avoir Les agents biologiques (biothérapies) Étant les plus récents
et l utilisation des traitements biologiques Choisir le meilleur traitement pour retrouver la qualité de vie que vous êtes en droit d avoir Les agents biologiques (biothérapies) Étant les plus récents
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT
 IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
IMPORTANT : VEUILLEZ LIRE ATTENTIVEMENT PARTIE III : RENSEIGNEMENTS POUR LE CONSOMMATEUR PROMETRIUM Progestérone en capsules Le présent dépliant constitue la troisième et dernière partie de la «monographie
Innovations thérapeutiques en transplantation
 Innovations thérapeutiques en transplantation 3èmes Assises de transplantation pulmonaire de la région Est Le 16 octobre 2010 Dr Armelle Schuller CHU Strasbourg Etat des lieux en transplantation : 2010
Innovations thérapeutiques en transplantation 3èmes Assises de transplantation pulmonaire de la région Est Le 16 octobre 2010 Dr Armelle Schuller CHU Strasbourg Etat des lieux en transplantation : 2010
INSUFFISANCE HÉPATIQUE
 INSUFFISANCE HÉPATIQUE EXISTE-T-IL DES TRAITEMENTS À BASE DE CELLULES SOUCHES POUR L INSUFFISANCE HÉPATIQUE? Bien qu aucun traitement à base de cellules souches pour l insuffisance hépatique ne soit approuvé
INSUFFISANCE HÉPATIQUE EXISTE-T-IL DES TRAITEMENTS À BASE DE CELLULES SOUCHES POUR L INSUFFISANCE HÉPATIQUE? Bien qu aucun traitement à base de cellules souches pour l insuffisance hépatique ne soit approuvé
L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ
 L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ Plan de la présentation Introduction L enfant Le cathéter court La voie veineuse centrale La voie intra-osseuse Plan de la présentation Le
L ACCÈS VEINEUX DE COURTE DURÉE CHEZ L ENFANT ET LE NOUVEAU-NÉ Plan de la présentation Introduction L enfant Le cathéter court La voie veineuse centrale La voie intra-osseuse Plan de la présentation Le
RAID PIEGES ANTI-FOURMIS x 2 1/5 Date de création/révision: 25/10/1998 FICHE DE DONNEES DE SECURITE NON CLASSE
 RAID PIEGES ANTI-FOURMIS x 2 1/5 RAISON SOCIALE JOHNSONDIVERSEY FICHE DE DONNEES DE SECURITE RISQUES SPECIFIQUES NON CLASSE 1 IDENTIFICATION DU PRODUIT ET DE LA SOCIETE - NOM DU PRODUIT RAID PIEGES ANTI-FOURMIS
RAID PIEGES ANTI-FOURMIS x 2 1/5 RAISON SOCIALE JOHNSONDIVERSEY FICHE DE DONNEES DE SECURITE RISQUES SPECIFIQUES NON CLASSE 1 IDENTIFICATION DU PRODUIT ET DE LA SOCIETE - NOM DU PRODUIT RAID PIEGES ANTI-FOURMIS
Apixaban. Rivaroxaban. Dabigatran (Pradaxa ) (Xarelto ) (Eliquis ) 6X (ClCr 10-30ml/min)
 dapté et modifié de: J.Eikelboom et l. Circulation. 2010;121:1523-1532 Apixaban (Eliquis ) Rivaroxaban (Xarelto ) Dabigatran (Pradaxa ) Mécanisme d action Inhibiteurs directs du FXa Inhibiteur direct du
dapté et modifié de: J.Eikelboom et l. Circulation. 2010;121:1523-1532 Apixaban (Eliquis ) Rivaroxaban (Xarelto ) Dabigatran (Pradaxa ) Mécanisme d action Inhibiteurs directs du FXa Inhibiteur direct du
NOTICE: INFORMATION DE L UTILISATEUR. Bisolax 5 mg comprimés enrobés. Bisacodyl
 NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
NOTICE: INFORMATION DE L UTILISATEUR Bisolax 5 mg comprimés enrobés Bisacodyl Veuillez lire attentivement cette notice avant d utiliser ce médicament car elle contient des informations importantes pour
Le dropéridol n est pas un traitement à considérer pour le traitement de la migraine à l urgence
 Le dropéridol n est pas un traitement à considérer pour le traitement de la migraine à l urgence On pose fréquemment le diagnostic de migraine sévère à l urgence. Bien que ce soit un diagnostic commun,
Le dropéridol n est pas un traitement à considérer pour le traitement de la migraine à l urgence On pose fréquemment le diagnostic de migraine sévère à l urgence. Bien que ce soit un diagnostic commun,
CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE
 CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE BAXTER_CLINIMIX N9G15 E et N12G20E_Avis CT_14-02-2007.pdf BAXTER_CLINIMIX N9G15E N12G20E N14G30 N17G35_Avis CT_12-12-2001.pdf BAXTER_CLINIMIX changement
CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE BAXTER_CLINIMIX N9G15 E et N12G20E_Avis CT_14-02-2007.pdf BAXTER_CLINIMIX N9G15E N12G20E N14G30 N17G35_Avis CT_12-12-2001.pdf BAXTER_CLINIMIX changement
Campagne nationale pour l élimination des fistules obstétricales en Mauritanie
 Campagne nationale pour l élimination des fistules obstétricales en Mauritanie Contexte de la fistule obstétricale Situation en Mauritanie Progrès au niveau Pays/ Mise en œuvre Défis pour les années à
Campagne nationale pour l élimination des fistules obstétricales en Mauritanie Contexte de la fistule obstétricale Situation en Mauritanie Progrès au niveau Pays/ Mise en œuvre Défis pour les années à
Avis 29 mai 2013. XYZALL 5 mg, comprimé B/14 (CIP : 34009 358 502 4-9) B/28 (CIP : 34009 358 505 3-9) Laboratoire UCB PHARMA SA.
 COMMISSION DE LA TRANSPARENCE Avis 29 mai 2013 XYZALL 5 mg, comprimé B/14 (CIP : 34009 358 502 4-9) B/28 (CIP : 34009 358 505 3-9) Laboratoire UCB PHARMA SA DCI Code ATC (2012) Motif de l examen Liste
COMMISSION DE LA TRANSPARENCE Avis 29 mai 2013 XYZALL 5 mg, comprimé B/14 (CIP : 34009 358 502 4-9) B/28 (CIP : 34009 358 505 3-9) Laboratoire UCB PHARMA SA DCI Code ATC (2012) Motif de l examen Liste
Hémostase et Endocardite Surveillance des anticoagulants. Docteur Christine BOITEUX
 Hémostase et Endocardite Surveillance des anticoagulants Docteur Christine BOITEUX Théorie Endocardites et anticoagulation POUR Thromboses Emboles septiques CONTRE Favorise emboles septiques et diffusion
Hémostase et Endocardite Surveillance des anticoagulants Docteur Christine BOITEUX Théorie Endocardites et anticoagulation POUR Thromboses Emboles septiques CONTRE Favorise emboles septiques et diffusion
