Lignes directrices pour l application d un système de management de la qualité dans les laboratoires d analyse des drogues
|
|
|
- Pierre Cousineau
- il y a 8 ans
- Total affichages :
Transcription
1 Lignes directrices pour l application d un système de management de la qualité dans les laboratoires d analyse des drogues Notre engagement: la qualité et l amélioration continue
2 Crédits photo: Bibliothèque de l UNODC; UNODC/Ioulia Kondratovitch; Alessandro Scotti.
3 Section scientifique et du laboratoire OFFICE DES NATIONS UNIES CONTRE LA DROGUE ET LE CRIME Vienne Lignes directrices pour l application d un système de management de la qualité dans les laboratoires d analyse des drogues Notre engagement: la qualité et l amélioration continue NATIONS UNIES New York, 2009
4 Remerciements Le présent manuel a été élaboré par la Section scientifique et du laboratoire de l Office des Nations Unies contre la drogue et le crime (UNODC), sous la direction du juge Tettey. Nous remercions chaleureusement toutes les personnes qui y ont participé (équipe en charge: Iphigenia Naidis et Satu Turpeinen). La Section scientifique et du laboratoire tient à remercier le docteur Pirjo Lillsunde, de l Unité de recherche sur les drogues de l Institut finlandais de santé publique, qui a mis au point la première version du présent manuel. La Section scientifique et du laboratoire adresse également ses remerciements aux membres du Comité permanent du Programme international de contrôle de la qualité de l UNODC, D r Robert Anderson, D r Robert Bramley, D r David Clarke et D r Pirjo Lillsunde, qui ont examiné et finalisé le texte*. Enfin, la Section scientifique et du laboratoire remercie le Comité du laboratoire de la Coopération européenne d accréditation pour ses précieux commentaires. *Les coordonnées des personnes susmentionnées peuvent être obtenues auprès de la Section scientifique et du laboratoire de l UNODC [Boîte postale 500, 1400 Vienne (Autriche)]. ST/NAR/37 PUBLICATION DES NATIONS UNIES Numéro de vente: F.09.XI.10 ISBN La présente publication n a pas été revue par les services d édition.
5 Table des matières 1. AVANT-PROPOS: OBJET DU MANUEL INTRODUCTION SYSTÈME DE MANAGEMENT DE LA QUALITÉ Politique qualité Manuel qualité EXIGENCES EN MATIÈRE D ADMINISTRATION Organisation du laboratoire Maîtrise de la documentation Revue des demandes des clients Sous-traitance du travail d analyse Achat de services et de fournitures Services aux clients Réclamations Actions correctives et préventives Contrôle des enregistrements/chaîne de responsabilité Audits internes Revues de direction EXIGENCES TECHNIQUES Introduction Personnel Installations et conditions ambiantes Santé et sécurité Méthodes d essai, validation des méthodes et procédures d essai Équipement Normes de référence, matériaux et réactifs Manipulation des objets d essai Rapport sur les résultats Contrôle de la qualité, tests d aptitude et comparaisons interlaboratoires Bibliographie Annexe Modèle de manuel qualité Pages iii
6
7 1. Avant-propos: objet du manuel Les services de détection et de répression ainsi que d autres clients des laboratoires d analyse des drogues, comme la police, les douanes, les procureurs et les avocats de la défense, ont besoin de résultats d analyse qui soient: Fiables; Valides; Fondés sur des procédures normalisées; Compatibles avec les résultats obtenus par d autres laboratoires; Conformes aux normes admises comme preuve par les différents systèmes judiciaires, administratifs et juridiques; Obtenus de manière effective et efficiente dans les délais requis; D un bon rapport qualité-prix. La qualité des analyses et des résultats de ces laboratoires a des conséquences importantes pour le système de justice, la détection et la répression ainsi que pour la prévention du crime et la politique de santé, de même que pour l harmonisation internationale et l échange et la coordination au niveau mondial d informations et de données sur les drogues [1]. La compatibilité et l acceptation des résultats de laboratoire entre pays sont facilitées par leur conformité à la norme ISO/CEI 17025:2005 (ISO 17025) [2], à la norme internationale de qualité des laboratoires d étalonnages et d essai et aux recommandations connexes de la Conférence internationale sur l agrément des laboratoires d essai (ILAC G19:2002) applicables aux laboratoires de police scientifique [3]. La conformité à la norme ISO assure également la conformité aux exigences de la norme ISO 9001 concernant les laboratoires d analyse de drogues. Cependant, la conformité à la norme ISO 9001 seule ne signifie pas la conformité à la norme ISO 17025, la norme ISO 9001 ne traitant pas de la compétence technique des laboratoires d essai. Les lignes directrices ci-dessous, qui concernent spécifiquement les laboratoires d analyse des drogues, sont fondées sur les principes généraux établis par la norme ISO Elles prennent également en compte les Principes recommandés d assurance de qualité et de bonnes pratiques de laboratoire de l UNODC [4], les 1
8 2 Lignes directrices pour l application d un système de management de la qualité recommandations du SWGDRUG [5], les exigences de l American Society of Crime Laboratory Directors Laboratory Accreditation Manual [6], les lignes directrices SOFT/AAFS intitulées Forensic Toxicology Laboratory Guidelines [7] et les lignes directrices européennes pour les laboratoires de dépistage de drogues sur le lieu de travail [8, 9]. L attachement à la qualité est le principe de base d un laboratoire de criminalistique. Le présent manuel vise à fournir des lignes directrices aux laboratoires de criminali stique pour qu ils atteignent un niveau élevé de qualité, utilisent les techniques appropriées pour trouver les réponses et s améliorent en permanence. Il est conçu comme un manuel pratique et aborde des domaines qui ne sont pas explicitement traités en profondeur par la norme ISO Le présent manuel se propose de servir d introduction aux systèmes de management de la qualité des laboratoires et de fournir des lignes directrices pratiques aux autorités nationales et aux analystes pour les aider à appliquer ces systèmes en se fondant sur les meilleures pratiques de laboratoire. La meilleure pratique peut varier selon les laboratoires en raison de différences dans le niveau des ressources dont ils disposent et dans les prescriptions légales applicables. Par exemple, à l échelle internationale, on peut considérer que la meilleure pratique repose sur l utilisation de la LC-SM-SM, mais de nombreux laboratoires ne possèdent pas l instrumentation nécessaire pour cette technique, ce qui ne les empêche pas d obtenir de bons résultats. De même, certains pays exigent des analyses quantitatives des drogues ou l identification d isomères spécifiques, d autres non. L expression meilleure pratique doit donc être entendue comme la meilleure pratique réalisable dans un laboratoire et un pays donnés, pour autant que les travaux effectués répondent aux exigences indiquées dans le présent document. Il existe différentes manières d obtenir le résultat final et ces lignes directrices aideront les directeurs de laboratoire à garantir que la leur se situe à un niveau international. Le respect par tous les laboratoires d analyse des drogues des lignes directrices qui suivent est essentiel pour garantir l harmonisation de leur performance à l échelle mondiale. Ces lignes directrices peuvent également servir de guide non seulement aux laboratoires, mais aussi aux auditeurs et inspecteurs lors de l évaluation pendant le processus d accréditation. L accréditation externe selon la norme ISO est le processus par lequel un organisme d accréditation autorisé reconnaît formellement qu un laboratoire est compétent pour effectuer des tâches spécifiques. Au cours du processus d accréditation, le laboratoire doit démontrer que sa direction, ses opérations, son personnel, ses procédures, son équipement, ses installations et ses procédures en matière de sûreté, de santé et de sécurité satisfont aux normes de qualité établies. Bien que cela puisse exiger l investissement de ressources importantes, l obtention de la certification ISO accroît la confiance des directeurs de laboratoires, des autorités de détection et de répression et des autres clients quant à la performance du laboratoire. L accréditation externe est par conséquent un objectif à rechercher lors de l élabora-
9 Lignes directrices pour l application d un système de management de la qualité 3 tion d un système de management de la qualité (SMQ); de fait, de nombreux laboratoires d essai sont désormais accrédités dans plusieurs pays. À l avenir, il se peut que seuls les laboratoires d analyse des drogues agréés soient autorisés à effectuer des analyses de toxicologie médico-légale ou à exercer en tant que laboratoires de police criminelle. L UNODC aide les laboratoires à instaurer et à mettre en œuvre un système de management de la qualité de diverses manières, notamment en leur fournissant des échantillons de référence des substances placées sous contrôle, en élaborant des manuels sur les méthodes recommandées, en leur offrant des opportunités de formation, en leur permettant de participer au programme pour les exercices collaboratifs internationaux (ICE) et en facilitant l échange d informations, de matériaux et de données [10]. Des exemples sont donnés dans tout le manuel pour clarifier les différents points abordés. Ceux-ci sont précédés des termes par exemple. Les exemples donnés en l occurrence ne sont pas exhaustifs et visent uniquement à illustrer les différents points abordés.
10 2. Introduction Les laboratoires qui suivent les lignes directrices pratiques présentées dans ce document doivent satisfaire aux exigences de la norme ISO Ces lignes directrices sont fondées sur des considérations théoriques mais aussi sur l expérience pratique acquise au cours du processus d accréditation des laboratoires. Elles visent à assurer l identification correcte des substances, à faire en sorte que les processus entrepris résistent à un examen juridique et à offrir des garanties pour protéger les droits des individus. Le but des lignes directrices est d améliorer la qualité des services de laboratoire et de définir des critères communs d assurance qualité. Le présent manuel met l accent à la fois sur les exigences techniques (importance d une formation adéquate du personnel, installations d essais et conditions environnementales appropriées, validation des méthodes, accès à l équipement requis étalons de référence, contrôle de la qualité et communication des résultats) et sur les exigences en matière de management (contrôle des documents, satisfaction des besoins des clients, actions préventives et correctives, la nécessité d audits réguliers de la conformité au système de management de la qualité et amélioration permanente de la performance du laboratoire). Les lignes directrices s appliquent à toutes les étapes clefs du processus de dépistage des drogues, de la collecte et de l analyse d échantillons à l interprétation et à la présentation des résultats. Les laboratoires qui exécutent toutes ces étapes doivent veiller à ce que les lignes directrices énoncées dans le présent document soient intégralement respectées. Lorsque des clients exécutent une ou plusieurs étapes du processus au sein de leur organisation (par exemple la collecte d échantillons ou l interprétation/la revue des résultats), le laboratoire est tenu de veiller à ce que le client comprenne toutes les implications de ces activités dans le processus de dépistage des drogues. 4
11 3. Système de management de la qualité Le laboratoire doit avoir un système de management de la qualité (SMQ) couvrant toutes ses activités, y compris l échantillonnage, l analyse et la communication des résultats, que ces activités soient effectuées au sein de l installation principale du laboratoire, dans des installations mobiles ou temporaires ou en des sites extérieurs tels qu un laboratoire clandestin, au bord d une route ou sur le lieu de saisies importantes de drogues. Le système d assurance de qualité comprend tous les documents se rapportant aux politiques, systèmes et procédures appliqués par le laboratoire ainsi qu aux instructions, le cas échéant, qui visent à garantir la qualité des résultats, à assurer le respect des exigences juridictionnelles et réglementaires et à satisfaire les besoins des clients. La hiérarchie du système de management de la qualité est présentée à la figure 1. Figure 1. Hiérarchie du système de management de la qualité Norme ISO/IEC Prescriptions législatives et juridictionnelles et autres exigences réglementaires et institutionnelles Système de management de la qualité Instructions et recommandations extérieures au laboratoire (par exemple normes internationales) Politique qualité MANUEL QUALITÉ Code de déontologie Politiques, systèmes, procédures, instructions, enregistrements etc. Exigences des clients 5
12 6 Lignes directrices pour l application d un système de management de la qualité 3.1. Politique qualité [11] Le laboratoire doit avoir un exposé concis de la direction générale indiquant la volonté de cette dernière d adhérer aux principes de qualité dans tous les aspects du travail du laboratoire. Ce document doit également comporter les éventuels codes de pratique ou de déontologie qui s appliquent. Cette déclaration constitue la politique qualité du laboratoire [4]. L ensemble du personnel, du directeur de rang le plus élevé aux assistants, est tenu d adhérer à cette politique qualité. L exposé de la politique doit comprendre au moins les points suivants: Déclaration par la direction de son engagement à l égard de la qualité et de l amélioration permanente de la performance du laboratoire; Une déclaration de la direction indiquant que la qualité du travail du laboratoire est adaptée à son objectif, dans ce sens qu il résistera à tout examen scientifique et juridique et remplira les conditions convenues avec le client en matière budgétaire et en termes de délais; Une déclaration de la direction par laquelle celle-ci s engage à fournir les ressources nécessaires pour gérer et appliquer le système qualité; Une déclaration indiquant que tous les membres du personnel ont un rôle à jouer pour faire en sorte que le travail du laboratoire soit effectué conformément aux exigences d ISO et d autres codes de pratique applicables au travail en question, ainsi qu à toutes les prescriptions juridictionnelles, réglementaires et de sécurité pertinentes spécifiées dans le système de management de la qualité du laboratoire; Le personnel responsable du système de management de la qualité doit avoir directement accès au niveau hiérarchique le plus élevé de la direction au sujet de la politique qualité du laboratoire Manuel qualité Le laboratoire doit disposer d un manuel décrivant succinctement le système de management de la qualité, indiquant l organisation et le format des documents ainsi que les rôles et responsabilités des membres du personnel chargés d administrer le système et les procédures techniques. Le manuel qualité doit également documenter les aspects administratifs, organisationnels et scientifiques du travail du laboratoire qui sont nécessaires à sa bonne administration. La documentation doit être facile à se procurer dans le laboratoire et accessible à l ensemble du personnel concerné. Elle doit être constamment révisée et mise à jour pour que tous changements des circonstances soient pris en compte.
13 Lignes directrices pour l application d un système de management de la qualité 7 L utilisation de procédures documentées garantit que les travaux effectués sont contrôlés et répondent aux objectifs fixés, que les exigences des normes internationales de qualité sont respectées et que les résultats des analyses de matériaux saisis ou d échantillons biologiques peuvent être utilisés avec confiance dans toute procédure judiciaire ultérieure.
14 4. Exigences en matière d administration 4.1. Organisation du laboratoire Le manuel qualité doit préciser les éléments suivants: L organisation et la structure administrative du laboratoire et sa place au sein de toute organisation plus grande ainsi que les relations entre le management de la qualité, les opérations techniques et les services d appui. En outre, si le laboratoire fait partie d une organisation plus vaste, les responsabilités de toute personne de cette organisation associée participant aux travaux du laboratoire ou pouvant avoir une influence sur ces travaux devraient être définies; La personne légalement responsable du travail du laboratoire en cas d action en justice (par exemple, par un client). Cette responsabilité légale peut incomber, par exemple, au directeur de l organisation à laquelle est rattaché le laboratoire, au directeur du laboratoire ou aux scientifiques; La responsabilité, l autorité et les relations entre tous les membres du personnel qui dirigent, exécutent ou vérifient les travaux influant sur la qualité des résultats; Les membres du personnel qui ont une autorité managériale et technique en matière de management de la qualité, leurs responsabilités spécifiques, leurs suppléants désignés et les moyens mis à leur disposition pour s acquitter de leurs fonctions. Il doit comprendre: Un responsable de la qualité qui, indépendamment de ses autres fonctions et responsabilités, aurait la responsabilité et le pouvoir de faire en sorte que le système qualité soit mis en œuvre et suivi à tout moment, aurait un accès direct au plus haut niveau de la direction où sont prises les décisions concernant la politique ou les ressources du laboratoire; éditerait et tiendrait à jour le manuel qualité; contrôlerait les pratiques du laboratoire; validerait les nouvelles procédures techniques; sélectionnerait, formerait et évaluerait les auditeurs internes; recommanderait des activités de formation pour améliorer la qualification du personnel du laboratoire; et proposerait des améliorations du système qualité; 8
15 Lignes directrices pour l application d un système de management de la qualité 9 Un directeur technique ou le personnel chargé d opérations techniques spécifiques, la fourniture des ressources nécessaires pour assurer la qualité requise de ces opérations, l enquête sur les problèmes et leur résolution et l évaluation des dossiers d étalonnage et d entretien des instruments. Les dispositions prises pour assurer que la direction et le personnel du laboratoire ne subissent pas de pressions et d influences internes et externes commerciales, financières et autres indues, susceptibles de nuire à la qualité de leur travail et qu ils ne sont pas associés à des activités qui auraient pour effet de diminuer la confiance dans la compétence, l impartialité, le jugement ou l intégrité opérationnelle du laboratoire. La réputation d un laboratoire est plus facile à perdre qu à rétablir; Les garanties pour assurer la protection des informations confidentielles et le respect des droits de propriété des clients, y compris les procédures de sauvegarde et de stockage des données et la transmission des résultats; Les dispositions adoptées pour la supervision du personnel effectuant le travail de laboratoire par les membres du personnel ayant eux-mêmes démontré leur compétence dans ce domaine Maîtrise de la documentation Un système de management de la qualité (SMQ) ne peut fonctionner efficacement que si les politiques, systèmes, procédures et méthodes sont documentés et tenus à jour. La maîtrise de la documentation est le mécanisme par lequel les documents du système de management de la qualité sont créés, modifiés, examinés, approuvés, diffusés et archivés de manière que l ensemble du personnel utilise les dernières versions autorisées. Le directeur qualité doit veiller à ce que tous les aspects du travail du laboratoire soient documentés dans le SMQ et que les nouveaux documents soient établis par des personnes compétentes et autorisées par le personnel désigné avant d être publiés. Il doit également veiller à ce que tous les documents soient périodiquement revus et, le cas échéant, révisés de manière à tenir compte des changements de circonstances et incorporer la meilleure pratique de laboratoire. Une fois approuvés, le directeur qualité doit faire le nécessaire pour qu ils soient mis à la disposition de tout le personnel sur le lieu de travail. Lorsque des modifications ont été apportées à des documents existants, le directeur qualité doit s assurer qu elles sont mises en évidence dans les versions les plus récentes. Tous les documents du SMQ doivent être identifiés de manière unique et porter le nom/la signature de la personne qui les a autorisés. Chaque page d un document
16 10 Lignes directrices pour l application d un système de management de la qualité doit être numérotée individuellement page x de y pages et comporter l identifiant unique du document du SMQ la date d émission et la version. Le système d identification des pages limite au minimum le risque d omission non détectée de pages courantes et de rétention non détectées de pages obsolètes. Si les documents sont tenus et distribués électroniquement, ils doivent être accessibles en lecture seulement et ne pouvoir être modifiés que par le personnel autorisé. Il faudrait tenir une liste principale portant la date de publication et, le cas échéant, un enregistrement complet de toutes les versions, les dates auxquelles elles ont été établies, le nom de la personne habilitée et la liste de distribution. Elle pourrait être complétée par une feuille jointe à chaque document et donnant les mêmes informations. Le laboratoire peut accepter que des modifications mineures soient apportées à la main aux documents imprimés pour corriger des fautes de frappe, mais ces modifications doivent être apportées à l encre permanente, datées et autorisées. Une version révisée doit toutefois être publiée dès que possible. Les documents non valides ou périmés doivent être rapidement retirés de manière à éviter leur utilisation accidentelle. Une copie de chaque document périmé doit être conservée à des fins légales ou de sauvegarde des connaissances et porter une marque appropriée (par exemple la mention non valide ) Revue des demandes des clients Le laboratoire doit avoir des procédures pour garantir que les exigences des clients sont correctement définies, documentées et comprises et qu il dispose des moyens permettant d y répondre avant d accepter (par contrat) de faire le travail. C est ce qui est appelé Revue des contrats dans la norme ISO L accord peut être écrit ou oral, mais s il est oral il doit par la suite être confirmé par écrit. Si le laboratoire n a pas les moyens nécessaires, il doit essayer de convenir avec le client des tâches qu il pourrait effectuer ou confier à un sous traitant avant d entreprendre des travaux quelconques. Tout accord révisé doit également être documenté. Le contrat doit être revu par le client et le laboratoire. Si de nouvelles exigences sont formulées par le client, ou si le laboratoire n est pas en mesure de respecter l accord initial ou les nouvelles exigences du client, les parties doivent en discuter et conclure un contrat révisé. Il faudrait également garder des traces de toutes les communications entre le client et le laboratoire au sujet du travail effectué. Ce sera un moyen d assurer la compréhension commune des exigences, des responsabilités et du travail à effectuer par le laboratoire, ses clients et toutes les autres parties concernées.
17 Lignes directrices pour l application d un système de management de la qualité Sous-traitance du travail d analyse Si le laboratoire fait appel à un tiers (sous-traitant) pour effectuer le travail en son nom, il doit avoir des politiques et procédures documentées assurant que ce tiers est compétent pour effectuer le travail Achat de services et de fournitures Le laboratoire doit avoir une politique et une ou plusieurs procédure(s) pour la sélection et l achat des services, des réactifs et des produits consommables susceptibles d influer sur la qualité de ses travaux, ainsi qu une procédure pour la réception et le stockage des réactifs et des produits consommables et pour garantir que les services, les réactifs et les produits consommables sont conformes aux spécifications techniques du système de management de la qualité avant d être achetés ou utilisés. Le laboratoire doit garder une trace des mesures prises pour vérifier la conformité et les résultats de ces vérifications Service aux clients Le laboratoire doit s assurer qu il comprend les besoins de ses clients et les tenir informés de la progression de son travail. Il doit aussi demander à ses clients un retour d information sur sa performance. Les réactions, tant négatives que positives, sont importantes pour améliorer les services du laboratoire. La confidentialité du client doit à tout moment être respectée Réclamations Le laboratoire doit avoir un système pour traiter efficacement les réclamations des clients qui comporterait l obligation d informer les clients de toutes mesures prises pour régler le problème et éviter sa répétition. Il faudrait conserver des dossiers de toutes les réclamations et actions correctives et les mettre à profit pour améliorer le management de la qualité dans le laboratoire. Le fait de ne pas répondre aux réclamations des clients peut nuire à la relation client-laboratoire Actions correctives et préventives Lorsque le travail effectué par le laboratoire n est pas conforme à son système de management de la qualité (par exemple s il s écarte d un mode opératoire ou des
18 12 Lignes directrices pour l application d un système de management de la qualité exigences des clients), la norme ISO parle de non-conformité. Le laboratoire doit avoir des systèmes (par exemple, vérification du travail au sein du laboratoire, dossier ou audit du SMQ, information en retour du personnel/client) pour reconnaître quand une non-conformité s est produite et comment la gérer. Ce processus doit comporter une enquête sur les causes de la non-conformité, l évaluation de son importance, l information du client si nécessaire et l autorisation de modifier, livrer ou rappeler le travail non conforme. Tout doit être fait pour détecter les non-conformités avant la remise des résultats au client, car la communication de résultats incorrects peut porter gravement atteinte à la relation laboratoire-client et conduire à des erreurs judiciaires. Si la non-conformité se reproduit sans que des mesures plus générales aient été adoptées (par exemple, modification du SMQ ou perfectionnement du personnel), des actions préventives doivent être autorisées au niveau approprié pour éviter la répétition du problème. Toutes les non-conformités, actions correctives et actions préventives doivent être enregistrées. L efficacité des actions correctives doit être vérifiée par le personnel autorisé afin de garantir que le travail est désormais conforme aux exigences du SMQ/client. Il faudrait également suivre les actions préventives pour s assurer (par exemple par un audit) que les non conformités ne se répètent pas. La reconnaissance des non-conformités et la mise en œuvre d actions correctives et préventives sont essentielles pour l amélioration continue de l efficacité de la performance du laboratoire Contrôle des enregistrements/chaîne de responsabilité Le laboratoire doit avoir des systèmes pour la création, l identification, la gestion, le stockage, le mouvement/la transmission, le retrait et d élimination de tous les enregistrements, sur support papier ou sous forme électronique. Tous les enregistrements du laboratoire sur support papier doivent être facilement lisibles, identifiables sans ambiguïté (porter par exemple la date, l auteur et le nombre de pages) et rédigés à l encre permanente. Le crayon papier ne doit pas être utilisé. Aucun enregistrement ne doit être supprimé. Les modifications et corrections apportées à la main ne doivent pas occulter les données initiales et doivent être signées/paraphées et datées. Des mesures doivent également être prises pour sauvegarder les enregistrements électroniques originaux (par exemple en créant des sauvegardes de fichiers informatiques), identifier toute modification éventuelle (par exemple au moyen d un journal d audit électronique que certains fabricants proposent avec le logiciel) et assurer leur intégrité et confidentialité. Tous les enregistrements doivent être systématiquement archivés pour permettre une consultation facile. En même temps, ils doivent être traités comme confidentiels, la
19 Lignes directrices pour l application d un système de management de la qualité 13 protection des données et les prescriptions légales relatives au droit à la vie privée, notamment, doivent être respectées et l accès à ces enregistrements doit être limité au personnel autorisé. Les enregistrements peuvent être subdivisés en enregistrements qualitatifs et enregistrements techniques. Les enregistrements qualitatifs comprennent les rapports d audit, les essais d aptitude, les retours d information des clients, les actions correctives et préventives et les revues de direction. Les enregistrements doivent être identifiables sans ambiguïté (porter par exemple la date, le nom de l auteur et le nombre de pages) et gardés en un lieu sûr et réglementé accessible au seul personnel autorisé. La durée de conservation de ces enregistrements (par exemple, compte tenu des prescriptions légales) doit être définie. Les enregistrements à éliminer doivent être traités comme des déchets confidentiels et incinérés ou déchiquetés. Les enregistrements techniques comprennent tous les documents relatifs aux essais, y compris les formulaires de soumission des échantillons, les documents de la chaîne de responsabilité, les notes de travail (y compris les dessins et diagrammes), les photographies, les enregistrements de conversations téléphoniques, les spectres, données d étalonnage et autres données du contrôle de la qualité, les paramètres opérationnels des instruments et les sorties d imprimante, les rapports, déclarations, et autres, les registres de maintenance des instruments et les dossiers de formation, de compétence et d autorisation du personnel. Ces enregistrements doivent être effectués au moment où le travail est exécuté. Chaque donnée enregistrée doit pouvoir être reliée à l analyste/examinateur et, le cas échéant, à un essai ou à un résultat identifié sans ambiguïté. Il doit ressortir clairement de l enregistrement qui a effectué toutes les phases de l analyse/examen et quand chaque étape de l analyse/examen a eu lieu (par exemple au moyen des dates pertinentes). Tous les enregistrements doivent contenir suffisamment d informations pour permettre de tracer l audit pour montrer qui a fait quoi et quand. Les conclusions essentielles (par exemple les odeurs et les observations visuelles comme les tests colorimétriques qui ne peuvent pas être confirmées indépendamment plus tard à partir de l enregistrement, les calculs et les transferts de données qui ne font pas partie d un processus électronique validé) doivent être vérifiées, de préférence par une deuxième personne autorisée. Le laboratoire doit avoir des procédures documentées pour la revue globale des enregistrements par les personnes autorisées. Chaque enregistrement doit indiquer que ces contrôles et revues ont été effectués, quand et par qui. Ces mentions peuvent être apportées de différentes manières (par exemple par une note en regard de chaque résultat, une note ajoutée au résumé des résultats ou une déclaration à cet effet jointe aux enregistrements). Si l auditeur ou le vérificateur de l essai récuse un point quelconque de l enregistrement initial, la ou les raison(s) de son désaccord et les mesures prises en conséquence doivent être consignées.
20 14 Lignes directrices pour l application d un système de management de la qualité En général, les enregistrements nécessaires pour étayer les conclusions doivent être tels qu en l absence de l analyste ou de l examinateur un autre analyste/examinateur puisse évaluer ce qui avait été fait, interpréter les données [12] et, le cas échéant, refaire le travail. Quand le résultat d un essai ou une observation est rejeté, la (les) raison(s) doive(nt) en être indiquée(s). Cette information est nécessaire pour qu un autre analyste puisse comprendre comment l essai a été géré. Les enregistrements techniques doivent être conservés dans un lieu sûr et protégé pour prévenir les dommages, la détérioration, l accès non autorisé ou la perte, pendant une période qui dépend des besoins du client et des règlements pertinents en vigueur dans le pays. La durée de conservation peut aussi dépendre de la nature de l infraction en cause, de sorte que les enregistrements concernant des infractions graves, telles que homicide et trafic de drogues, sont conservés plus longtemps que ceux relatifs à des infractions mineures, telles que la simple possession d une substance placée sous contrôle. Cela signifie que certains enregistrements peuvent être conservés indéfiniment, détruits à l issue de la procédure judiciaire ou être soumis à des dispositions intermédiaires. Les enregistrements voués à la destruction doivent être traités comme des déchets confidentiels et être incinérés ou déchiquetés Audits internes Le laboratoire doit effectuer périodiquement, conformément à une procédure et à un calendrier prédéfinis, un audit de toutes ses activités (par exemple de chaque méthode d essai) pour vérifier que toutes ses opérations sont conformes aux exigences du SMQ. Les audits doivent être organisés par le directeur qualité au moins une fois par an et exécutés et consignés par un personnel qualifié formé, indépendant, chaque fois que les ressources le permettent, de l activité soumise à l audit. Lorsque les conclusions de l audit jettent un doute sur l efficacité des opérations ou sur la correction ou la validité du travail du laboratoire, ces conclusions doivent être discutées par l auditeur, le directeur qualité et le personnel concerné et des actions correctives appropriées doivent être adoptées. Le laboratoire doit rapidement informer les clients par écrit si l audit révèle que les résultats étaient incorrects. Le secteur d activités faisant l objet de l audit, les conclusions de l audit et les actions correctives doivent être enregistrés. Les audits futurs de la même activité doivent évaluer l efficacité des actions correctives adoptées afin d identifier les enseignements tirés et, partant, d améliorer la performance du laboratoire Revues de direction Le directeur qualité doit organiser une revue annuelle du SMQ et des activités d essais pour s assurer qu elles demeurent appropriées et efficaces ou identifier tous
Introduction à l ISO/IEC 17025:2005
 Introduction à l ISO/IEC 17025:2005 Relation avec d autres normes de Management de la Qualité Formation Assurance Qualité LNCM, Rabat 27-29 Novembre 2007 Marta Miquel, EDQM-CoE 1 Histoire de l ISO/IEC
Introduction à l ISO/IEC 17025:2005 Relation avec d autres normes de Management de la Qualité Formation Assurance Qualité LNCM, Rabat 27-29 Novembre 2007 Marta Miquel, EDQM-CoE 1 Histoire de l ISO/IEC
Système de management H.A.C.C.P.
 NM 08.0.002 Norme Marocaine 2003 Système de management H.A.C.C.P. Exigences Norme Marocaine homologuée par arrêté du Ministre de l'industrie, du Commerce et des Télécommunications N 386-03 du 21 Février
NM 08.0.002 Norme Marocaine 2003 Système de management H.A.C.C.P. Exigences Norme Marocaine homologuée par arrêté du Ministre de l'industrie, du Commerce et des Télécommunications N 386-03 du 21 Février
REF01 Référentiel de labellisation des laboratoires de recherche_v3
 Introduction Le présent référentiel de labellisation est destiné aux laboratoires qui souhaitent mettre en place un dispositif de maîtrise de la qualité des mesures. La norme ISO 9001 contient essentiellement
Introduction Le présent référentiel de labellisation est destiné aux laboratoires qui souhaitent mettre en place un dispositif de maîtrise de la qualité des mesures. La norme ISO 9001 contient essentiellement
Appendice 2. (normative) Structure de niveau supérieur, texte de base identique, termes et définitions de base communs
 Appendice 2 (normative) Structure de niveau supérieur, texte de base identique, termes et définitions de base communs NOTE Dans les propositions de Texte identique, XXX désigne un qualificatif de norme
Appendice 2 (normative) Structure de niveau supérieur, texte de base identique, termes et définitions de base communs NOTE Dans les propositions de Texte identique, XXX désigne un qualificatif de norme
Audit interne. Audit interne
 Définition de l'audit interne L'Audit Interne est une activité indépendante et objective qui donne à une organisation une assurance sur le degré de maîtrise de ses opérations, lui apporte ses conseils
Définition de l'audit interne L'Audit Interne est une activité indépendante et objective qui donne à une organisation une assurance sur le degré de maîtrise de ses opérations, lui apporte ses conseils
Glossaire de termes relatifs à l assurance de la qualité et aux bonnes pratiques de laboratoire
 Glossaire de termes relatifs à l assurance de la qualité et aux bonnes pratiques de laboratoire Notre engagement: la qualité et l amélioration continue Photos Couverture: en haut à gauche; istockphoto.com/yegor
Glossaire de termes relatifs à l assurance de la qualité et aux bonnes pratiques de laboratoire Notre engagement: la qualité et l amélioration continue Photos Couverture: en haut à gauche; istockphoto.com/yegor
Annexe 4 Bonnes pratiques de fabrication des produits pharmaceutiques : Principes généraux 1
 Annexe 4 Bonnes pratiques de fabrication des produits pharmaceutiques : Principes généraux 1 Note d introduction Généralités Glossaire Gestion de la qualité dans l industrie pharmaceutique : principes
Annexe 4 Bonnes pratiques de fabrication des produits pharmaceutiques : Principes généraux 1 Note d introduction Généralités Glossaire Gestion de la qualité dans l industrie pharmaceutique : principes
Politique et Standards Santé, Sécurité et Environnement
 Politique et Standards Santé, Sécurité et Environnement Depuis la création de Syngenta en 2000, nous avons accordé la plus haute importance à la santé, à la sécurité et à l environnement (SSE) ainsi qu
Politique et Standards Santé, Sécurité et Environnement Depuis la création de Syngenta en 2000, nous avons accordé la plus haute importance à la santé, à la sécurité et à l environnement (SSE) ainsi qu
POLITIQUE ET LIGNES DIRECTRICES EN MATIERE DE TRACABILITE DES RESULTATS DE MESURE
 BELAC 2-003 Rev 1-2014 POLITIQUE ET LIGNES DIRECTRICES EN MATIERE DE TRACABILITE DES RESULTATS DE MESURE Les versions des documents du système de management de BELAC telles que disponibles sur le site
BELAC 2-003 Rev 1-2014 POLITIQUE ET LIGNES DIRECTRICES EN MATIERE DE TRACABILITE DES RESULTATS DE MESURE Les versions des documents du système de management de BELAC telles que disponibles sur le site
Documentation du système de management de la qualité
 Documentation du système de management de la qualité ISO/IEC 17025:2005 ISO/TR 10013:2001 Formation Assurance Qualité LNCM, Rabat 27-29 Novembre 2007 Marta Miquel, EDQM-CoE 1 ISO/TR 10013:2001 Lignes directrices
Documentation du système de management de la qualité ISO/IEC 17025:2005 ISO/TR 10013:2001 Formation Assurance Qualité LNCM, Rabat 27-29 Novembre 2007 Marta Miquel, EDQM-CoE 1 ISO/TR 10013:2001 Lignes directrices
L assurance de la qualité à votre service
 Atelier L assurance de la qualité à votre service Présentation de Jean-Marie Richard 24 et 25 novembre Sujets Qu est-ce que l assurance de la qualité? Initiation aux concepts de l assurance de la qualité.
Atelier L assurance de la qualité à votre service Présentation de Jean-Marie Richard 24 et 25 novembre Sujets Qu est-ce que l assurance de la qualité? Initiation aux concepts de l assurance de la qualité.
FLEGT Note d Information
 Série 20 Note FLEGT Note APPLICATION DES REGLEMENTATIONS FORESTIERES, GOUVERNANCE ET ECHANGES COMMERCIAUX Directives sur le Contrôle Indépendant INTRODUCTION Le Plan d action de l UE pour l application
Série 20 Note FLEGT Note APPLICATION DES REGLEMENTATIONS FORESTIERES, GOUVERNANCE ET ECHANGES COMMERCIAUX Directives sur le Contrôle Indépendant INTRODUCTION Le Plan d action de l UE pour l application
évaluation des risques professionnels
 évaluation des professionnels Inventaire des Etablissement : Faculté de Médecine Unité de travail : Laboratoire de Biochimie Médicale Année : 2013 Locaux Bureaux Salle de Microscopie Culture cellulaire
évaluation des professionnels Inventaire des Etablissement : Faculté de Médecine Unité de travail : Laboratoire de Biochimie Médicale Année : 2013 Locaux Bureaux Salle de Microscopie Culture cellulaire
SERIE OCDE LES PRINCIPES DE BONNES PRATIQUES DE LABORATOIRE ET LA VERIFICATION DU RESPECT DE CES PRINCIPES. Numéro 2 (révisé)
 DIFFUSION GÉNÉRALE OCDE/GD(95)66 SERIE OCDE LES PRINCIPES DE BONNES PRATIQUES DE LABORATOIRE ET LA VERIFICATION DU RESPECT DE CES PRINCIPES Numéro 2 (révisé) ORIENTATIONS A L INTENTION DES AUTORITES DE
DIFFUSION GÉNÉRALE OCDE/GD(95)66 SERIE OCDE LES PRINCIPES DE BONNES PRATIQUES DE LABORATOIRE ET LA VERIFICATION DU RESPECT DE CES PRINCIPES Numéro 2 (révisé) ORIENTATIONS A L INTENTION DES AUTORITES DE
Sommaire des documents de la base documentaire 15189 v2012 01/11/2013
 La base documentaire a été complètement révisée pour être en conformité avec cette version 2012 de l ISO 15189. La cartographie des différents processus du LBM a également été modifiée (suppression du
La base documentaire a été complètement révisée pour être en conformité avec cette version 2012 de l ISO 15189. La cartographie des différents processus du LBM a également été modifiée (suppression du
Bureau du surintendant des institutions financières. Audit interne des Services intégrés : Services de la sécurité et de l administration
 Bureau du surintendant des institutions financières Audit interne des Services intégrés : Services de la sécurité et de l administration Avril 2014 Table des matières 1. Contexte... 3 2. Objectif, délimitation
Bureau du surintendant des institutions financières Audit interne des Services intégrés : Services de la sécurité et de l administration Avril 2014 Table des matières 1. Contexte... 3 2. Objectif, délimitation
Validation des processus de production et de préparation du service (incluant le logiciel)
 Validation des processus de production et de préparation du service (incluant le logiciel) Traduction non officielle du document Réponses et décisions de EK-Med 3.9 B 18 publié sur le site Web de l organisme
Validation des processus de production et de préparation du service (incluant le logiciel) Traduction non officielle du document Réponses et décisions de EK-Med 3.9 B 18 publié sur le site Web de l organisme
LES DOUCHES ET LES BASSINS OCULAIRES D URGENCE
 LES DOUCHES ET LES BASSINS OCULAIRES D URGENCE LES DOUCHES ET LES BASSINS OCULAIRES D URGENCE Tous les jours, des milliers de Néo-Brunswickois travaillent près de produits chimiques dangereux. Même si
LES DOUCHES ET LES BASSINS OCULAIRES D URGENCE LES DOUCHES ET LES BASSINS OCULAIRES D URGENCE Tous les jours, des milliers de Néo-Brunswickois travaillent près de produits chimiques dangereux. Même si
Format d Évaluation et Dossier Type. Évaluation des Propositions de Première Étape
 Format d Évaluation et Dossier Type Évaluation des Propositions de Première Étape Édition d Essai Septembre 2011 PRÉFACE Le présent Format d'évaluation et le dossier type ont été préparés par la Banque
Format d Évaluation et Dossier Type Évaluation des Propositions de Première Étape Édition d Essai Septembre 2011 PRÉFACE Le présent Format d'évaluation et le dossier type ont été préparés par la Banque
Méthodologie d Ouverture, de Dépouillement et d Evaluation des Offres Relatives à la Consultation 09 S V.E.De.R
 Programme Projet Instrument Européen de Voisinage et de Partenariat - Coopération Transfrontalière Italie- "Valorisation Energétique des Résidus V.E.De.R PS2.3/02" Composante.2 Communication et Diffusion
Programme Projet Instrument Européen de Voisinage et de Partenariat - Coopération Transfrontalière Italie- "Valorisation Energétique des Résidus V.E.De.R PS2.3/02" Composante.2 Communication et Diffusion
Marquage CE Mode d emploi SOMMAIRE : I. Les produits concernés
 Marquage CE Mode d emploi Août 2014 SOMMAIRE : I. Les produits concernés II. Les acteurs concernés a. Le fabricant b. Le mandataire c. L importateur d. Le distributeur III. La mise en conformité des produits
Marquage CE Mode d emploi Août 2014 SOMMAIRE : I. Les produits concernés II. Les acteurs concernés a. Le fabricant b. Le mandataire c. L importateur d. Le distributeur III. La mise en conformité des produits
MANUEL DES POLITIQUES, PROCÉDURES ET RÈGLEMENTS ADMINISTRATIFS
 MANUEL DES POLITIQUES, PROCÉDURES ET RÈGLEMENTS ADMINISTRATIFS POLITIQUE EN MATIÈRE DE SURVEILLANCE VIDÉO Code : Politique 2.13 Date d entrée en vigueur : Le 30 avril 2007 Nombre de pages : 11 et annexe
MANUEL DES POLITIQUES, PROCÉDURES ET RÈGLEMENTS ADMINISTRATIFS POLITIQUE EN MATIÈRE DE SURVEILLANCE VIDÉO Code : Politique 2.13 Date d entrée en vigueur : Le 30 avril 2007 Nombre de pages : 11 et annexe
PARTIE 5 NOTICE HYGIENE ET SECURITE
 de en Martinik NOTICE HYGIENE ET SECURITE BUREAU VERITAS ASEM Dossier n 6078462 Révision 2 Octobre 2014 Page 1 de en Martinik SOMMAIRE 1. INTRODUCTION... 3 1.1 OBJET DE LA NOTICE... 3 1.2 CADRE REGLEMENTAIRE...
de en Martinik NOTICE HYGIENE ET SECURITE BUREAU VERITAS ASEM Dossier n 6078462 Révision 2 Octobre 2014 Page 1 de en Martinik SOMMAIRE 1. INTRODUCTION... 3 1.1 OBJET DE LA NOTICE... 3 1.2 CADRE REGLEMENTAIRE...
I. Définitions et exigences
 I. Définitions et exigences Classes d indicateurs chimiques [1] Stérilisation : synthèse des normes ayant trait Exigences générales : Chaque indicateur doit porter un marquage clair mentionnant le type
I. Définitions et exigences Classes d indicateurs chimiques [1] Stérilisation : synthèse des normes ayant trait Exigences générales : Chaque indicateur doit porter un marquage clair mentionnant le type
Marquage CE des Granulats
 REFERENTIEL SECTORIEL POUR LA Page 1 sur 11 MAÎTRISE DE LA PRODUCTION DES GRANULATS (Système d'attestation de conformité 2+) SOMMAIRE : Article 1 Objet et domaine d application Article 2 Intervenants dans
REFERENTIEL SECTORIEL POUR LA Page 1 sur 11 MAÎTRISE DE LA PRODUCTION DES GRANULATS (Système d'attestation de conformité 2+) SOMMAIRE : Article 1 Objet et domaine d application Article 2 Intervenants dans
La gestion documentaire les bases d'un système de management de la qualité
 La gestion documentaire les bases d'un système de management de la qualité 8 ème journée professionnelle de l ANTAB - 21 Octobre 2011 Fatima TOUBAIS Ingénieur qualité Accréditation des Laboratoires Direction
La gestion documentaire les bases d'un système de management de la qualité 8 ème journée professionnelle de l ANTAB - 21 Octobre 2011 Fatima TOUBAIS Ingénieur qualité Accréditation des Laboratoires Direction
Tremplins de la Qualité. Tome 2
 Tome 2 CET OUVRAGE EST UN GUIDE D INTERPRETATION DE LA NORME NF EN ISO 9001 VERSION 2000 AVANTPROPOS Ce guide d aide à la rédaction du Manuel de Management de la Qualité a été rédigé par la Fédération
Tome 2 CET OUVRAGE EST UN GUIDE D INTERPRETATION DE LA NORME NF EN ISO 9001 VERSION 2000 AVANTPROPOS Ce guide d aide à la rédaction du Manuel de Management de la Qualité a été rédigé par la Fédération
1. Procédure. 2. Les faits
 Avis relatif à la notification en vue d un contrôle préalable reçue du délégué à la protection des données de la Banque européenne d investissement concernant l enregistrement des conversations téléphoniques
Avis relatif à la notification en vue d un contrôle préalable reçue du délégué à la protection des données de la Banque européenne d investissement concernant l enregistrement des conversations téléphoniques
Administration canadienne de la sûreté du transport aérien
 Administration canadienne de la sûreté du transport aérien Norme relative au système de gestion des fournisseurs de services de contrôle de l ACSTA Octobre 2009 La présente norme est assujettie aux demandes
Administration canadienne de la sûreté du transport aérien Norme relative au système de gestion des fournisseurs de services de contrôle de l ACSTA Octobre 2009 La présente norme est assujettie aux demandes
A009 Maîtrise des enregistrements
 28.11.2014 Version 11 Page 1 de 8 A009 Maîtrise des enregistrements Modifications : pages 2, 5 South Lane Tower I 1, avenue du Swing L-4367 Belvau Tél.: (+352) 2477 4360 Fa: (+352) 2479 4360 olas@ilnas.etat.lu
28.11.2014 Version 11 Page 1 de 8 A009 Maîtrise des enregistrements Modifications : pages 2, 5 South Lane Tower I 1, avenue du Swing L-4367 Belvau Tél.: (+352) 2477 4360 Fa: (+352) 2479 4360 olas@ilnas.etat.lu
Questionnaire de vérification pour l implantation de la norme ISO 14001 dans une entreprise
 Questionnaire de vérification pour l implantation de la norme ISO 14001 dans une entreprise Questionnaire de vérification pour l implantation de la norme ISO 14001 dans une entreprise La politique environnementale
Questionnaire de vérification pour l implantation de la norme ISO 14001 dans une entreprise Questionnaire de vérification pour l implantation de la norme ISO 14001 dans une entreprise La politique environnementale
Vérification de la sécurité des données fiscales. Rapport final Approuvé par le Comité de vérification interne le 29 juin 2005
 Rapport final Approuvé par le Comité de vérification interne le 29 juin 2005 Division de la vérification et de l évaluation Mars 2005 Table des matières Énoncé du vérificateur... 1 I. Introduction...
Rapport final Approuvé par le Comité de vérification interne le 29 juin 2005 Division de la vérification et de l évaluation Mars 2005 Table des matières Énoncé du vérificateur... 1 I. Introduction...
Garantir aux enfants une protection maximale. Commission européenne DG Entreprises et industrie
 SÉCURITÉ DES JOUETS Garantir aux enfants une protection maximale Commission européenne DG Entreprises et industrie Fotolia Orange Tuesday L Union européenne (UE) compte environ 80 millions d enfants de
SÉCURITÉ DES JOUETS Garantir aux enfants une protection maximale Commission européenne DG Entreprises et industrie Fotolia Orange Tuesday L Union européenne (UE) compte environ 80 millions d enfants de
Liste de contrôle d auto-évaluation pour le niveau de confinement 1 pour les phytoravageurs
 Bureau du confinement des biorisques et de la sécurité Office of Biohazard, Containment and Safety Direction générale des sciences Science Branch 59, promenade Camelot 59 Camelot Drive Ottawa ON K1A 0Y9
Bureau du confinement des biorisques et de la sécurité Office of Biohazard, Containment and Safety Direction générale des sciences Science Branch 59, promenade Camelot 59 Camelot Drive Ottawa ON K1A 0Y9
SECTION 2 DÉFINITIONS
 DIRECTIVES SUR LA CONCEPTION, L APPLICATION, L ÉVALUATION ET L HOMOLOGATION DE SYSTÈMES D INSPECTION ET DE CERTIFICATION DES IMPORTATIONS ET DES EXPORTATIONS ALIMENTAIRES SECTION 1 OBJECTIFS CAC/GL 26-1997
DIRECTIVES SUR LA CONCEPTION, L APPLICATION, L ÉVALUATION ET L HOMOLOGATION DE SYSTÈMES D INSPECTION ET DE CERTIFICATION DES IMPORTATIONS ET DES EXPORTATIONS ALIMENTAIRES SECTION 1 OBJECTIFS CAC/GL 26-1997
OFFICE DES NATIONS UNIES CONTRE LA DROGUE ET LE CRIME Vienne
 OFFICE DES NATIONS UNIES CONTRE LA DROGUE ET LE CRIME Vienne Mécanisme d examen de l application de la Convention des Nations Unies contre la corruption Documents de base NATIONS UNIES Vienne, 2010 Résolutions
OFFICE DES NATIONS UNIES CONTRE LA DROGUE ET LE CRIME Vienne Mécanisme d examen de l application de la Convention des Nations Unies contre la corruption Documents de base NATIONS UNIES Vienne, 2010 Résolutions
Lignes directrices concernant les contrôles à l importation dans le domaine de la sécurité et de la conformité des produits
 COMMISSION EUROPÉENNE DIRECTION GÉNÉRALE FISCALITÉ ET UNION DOUANIÈRE Sécurité et sûreté, facilitation des échanges et coordination internationale Protection des citoyens et application des DPI Lignes
COMMISSION EUROPÉENNE DIRECTION GÉNÉRALE FISCALITÉ ET UNION DOUANIÈRE Sécurité et sûreté, facilitation des échanges et coordination internationale Protection des citoyens et application des DPI Lignes
ISO 9001. Comment procéder. pour les PME. Recommandations de l ISO/TC 176
 ISO 9001 pour les PME Comment procéder Recommandations de l ISO/TC 176 ISO 9001 pour les PME Comment procéder Recommandations de l ISO/TC 176 Secrétariat central de l ISO 1, chemin de la Voie-Creuse Case
ISO 9001 pour les PME Comment procéder Recommandations de l ISO/TC 176 ISO 9001 pour les PME Comment procéder Recommandations de l ISO/TC 176 Secrétariat central de l ISO 1, chemin de la Voie-Creuse Case
Ministère des Transports. Lignes directrices pour l aménagement routier lié à l aménagement foncier
 Ministère des Transports Lignes directrices pour l aménagement routier lié à l aménagement foncier AVANT-PROPOS Aménagement routier Les travaux d aménagement des voies publiques («aménagements routiers»)
Ministère des Transports Lignes directrices pour l aménagement routier lié à l aménagement foncier AVANT-PROPOS Aménagement routier Les travaux d aménagement des voies publiques («aménagements routiers»)
Système d autorisation de mise en circulation de lots du CBER : vue d ensemble du processus actuel
 Système d autorisation de mise en circulation de lots du CBER : vue d ensemble du processus actuel DIAPOSITIVE 1 Cette présentation a trait au système d autorisation de mise en circulation de lots du CBER.
Système d autorisation de mise en circulation de lots du CBER : vue d ensemble du processus actuel DIAPOSITIVE 1 Cette présentation a trait au système d autorisation de mise en circulation de lots du CBER.
Guide de la pratique sur les réserves aux traités 2011
 Guide de la pratique sur les réserves aux traités 2011 Texte adopté par la Commission du droit international à sa soixante-troisième session, en 2011, et soumis à l Assemblée générale dans le cadre de
Guide de la pratique sur les réserves aux traités 2011 Texte adopté par la Commission du droit international à sa soixante-troisième session, en 2011, et soumis à l Assemblée générale dans le cadre de
Guide des inspections de l OIAC concernant les produits chimiques des tableaux 2 et 3
 1. But Guide des inspections de l OIAC concernant les produits chimiques des tableaux 2 et 3 Le présent guide a pour objectif d aider les entreprises à préparer les inspections de l Organisation pour l
1. But Guide des inspections de l OIAC concernant les produits chimiques des tableaux 2 et 3 Le présent guide a pour objectif d aider les entreprises à préparer les inspections de l Organisation pour l
Dossier de demande d autorisation temporaire d exploiter une centrale d enrobage à chaud SRTP le Petit Nazé ARGENTRE (53) Indice : 1.
 Dossier de demande d autorisation temporaire d exploiter une centrale d enrobage à chaud SRTP le Petit Nazé ARGENTRE (53) Indice : 1 Juin 2015 NOTICE D HYGIENE ET DE SECURITE P. 2 sur 8 SOMMAIRE 1 Hygiène...
Dossier de demande d autorisation temporaire d exploiter une centrale d enrobage à chaud SRTP le Petit Nazé ARGENTRE (53) Indice : 1 Juin 2015 NOTICE D HYGIENE ET DE SECURITE P. 2 sur 8 SOMMAIRE 1 Hygiène...
CONVENTION ASSURANCE QUALITÉ (QAA) FONCTION NÉGOCIANT
 1. Préambule 1.1 Généralités La présente convention d assurance qualité (QAA) définit les exigences posées aux fournisseurs REHAU en matière d assurance qualité. La QAA REHAU constitue des règles destinées
1. Préambule 1.1 Généralités La présente convention d assurance qualité (QAA) définit les exigences posées aux fournisseurs REHAU en matière d assurance qualité. La QAA REHAU constitue des règles destinées
Droits et obligations des travailleurs et des employeurs
 Droits et obligations des travailleurs et des employeurs La Loi sur la santé et la sécurité du travail (LSST) vise à assurer des conditions de santé et de sécurité minimales dans les entreprises québécoises.
Droits et obligations des travailleurs et des employeurs La Loi sur la santé et la sécurité du travail (LSST) vise à assurer des conditions de santé et de sécurité minimales dans les entreprises québécoises.
SERIE OCDE LES PRINCIPES DE BONNES PRATIQUES DE LABORATOIRE ET LA VERIFICATION DU RESPECT DE CES PRINCIPES NUMÉRO 3 (RÉVISÉ)
 DIFFUSION GÉNÉRALE OCDE/GD(95)67 SERIE OCDE LES PRINCIPES DE BONNES PRATIQUES DE LABORATOIRE ET LA VERIFICATION DU RESPECT DE CES PRINCIPES NUMÉRO 3 (RÉVISÉ) ORIENTATIONS A L INTENTION DES AUTORITES DE
DIFFUSION GÉNÉRALE OCDE/GD(95)67 SERIE OCDE LES PRINCIPES DE BONNES PRATIQUES DE LABORATOIRE ET LA VERIFICATION DU RESPECT DE CES PRINCIPES NUMÉRO 3 (RÉVISÉ) ORIENTATIONS A L INTENTION DES AUTORITES DE
REGLES DE CERTIFICATION MARQUE NF DENTAIRE PARTIE 3 OBTENTION DE LA CERTIFICATION
 REGLES DE CERTIFICATION MARQUE NF DENTAIRE PARTIE 3 OBTENTION DE LA CERTIFICATION SOMMAIRE 3.1. Constitution du dossier de demande 3.2. Processus d'évaluation initiale Rev. 9 mai 2012 PROCESSUS D'OBTENTION
REGLES DE CERTIFICATION MARQUE NF DENTAIRE PARTIE 3 OBTENTION DE LA CERTIFICATION SOMMAIRE 3.1. Constitution du dossier de demande 3.2. Processus d'évaluation initiale Rev. 9 mai 2012 PROCESSUS D'OBTENTION
POLITIQUE EN MATIÈRE DE SURVEILLANCE VIDÉO (adoptée le 15 janvier 2010)
 POLITIQUE EN MATIÈRE DE SURVEILLANCE VIDÉO (adoptée le 15 janvier 2010) Note : Le générique masculin est utilisé sans discrimination uniquement dans le but d alléger le texte. 1. Introduction La Commission
POLITIQUE EN MATIÈRE DE SURVEILLANCE VIDÉO (adoptée le 15 janvier 2010) Note : Le générique masculin est utilisé sans discrimination uniquement dans le but d alléger le texte. 1. Introduction La Commission
Evaluation de la conformité du Système de validation Vaisala Veriteq vlog à la norme 21 CFR Part 11
 / Livre blanc Evaluation de la conformité du Système de validation Vaisala Veriteq vlog à la norme 21 CFR Part 11 La norme 21 CFR Part 11 traduit l opinion de la FDA selon laquelle les risques de falsification,
/ Livre blanc Evaluation de la conformité du Système de validation Vaisala Veriteq vlog à la norme 21 CFR Part 11 La norme 21 CFR Part 11 traduit l opinion de la FDA selon laquelle les risques de falsification,
Acides et bases. Acides et bases Page 1 sur 6
 Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
POLITIQUES EN MATIÈRE DE GARDE D ENFANTS
 POLITIQUES EN MATIÈRE DE GARDE D ENFANTS Règlement 22(1) La demande de licence pour fournir et offrir des services de garderie familiale comporte les éléments suivants : (b.1) une copie du code de conduite
POLITIQUES EN MATIÈRE DE GARDE D ENFANTS Règlement 22(1) La demande de licence pour fournir et offrir des services de garderie familiale comporte les éléments suivants : (b.1) une copie du code de conduite
Nettoyeur en bâtiment/nettoyeuse en bâtiment. Règlement d apprentissage et d examen de fin d apprentissage
 80101 Nettoyeur en bâtiment/nettoyeuse en bâtiment Gebäudereiniger/Gebäudereinigerin Pulitore di edifici/pulitrice di edifici A. Règlement d apprentissage et d examen de fin d apprentissage B. Programme
80101 Nettoyeur en bâtiment/nettoyeuse en bâtiment Gebäudereiniger/Gebäudereinigerin Pulitore di edifici/pulitrice di edifici A. Règlement d apprentissage et d examen de fin d apprentissage B. Programme
ANNEXE A LA CIRCULAIRE SUR LE CONTROLE INTERNE ET L AUDIT INTERNE TABLE DES MATIERES
 PPB-2006-8-1-CPA ANNEXE A LA CIRCULAIRE SUR LE CONTROLE INTERNE ET L AUDIT INTERNE TABLE DES MATIERES Introduction 0. Base légale 1. Le contrôle interne 1.1. Définition et éléments constitutifs 1.2. Mesures
PPB-2006-8-1-CPA ANNEXE A LA CIRCULAIRE SUR LE CONTROLE INTERNE ET L AUDIT INTERNE TABLE DES MATIERES Introduction 0. Base légale 1. Le contrôle interne 1.1. Définition et éléments constitutifs 1.2. Mesures
Ministère des Affaires Étrangères et de la Coopération Internationale. Programme d appui au secteur de la santé- 8 ÈME FED
 République du Mali Ministère des Affaires Étrangères et de la Coopération Internationale Programme d appui au secteur de la santé- 8 ÈME FED Mars 2006 Elaboration d un guide concernant les grossistes sur
République du Mali Ministère des Affaires Étrangères et de la Coopération Internationale Programme d appui au secteur de la santé- 8 ÈME FED Mars 2006 Elaboration d un guide concernant les grossistes sur
CNAC. Appel à commentaires. Missions d examen. préparé par le Conseil des normes d audit et de certification
 Appel à commentaires Missions d examen préparé par le Conseil des normes d audit et de certification Date limite de réception des commentaires : le 11 avril 2011 CNAC APPEL À COMMENTAIRES MISSIONS D EXAMEN
Appel à commentaires Missions d examen préparé par le Conseil des normes d audit et de certification Date limite de réception des commentaires : le 11 avril 2011 CNAC APPEL À COMMENTAIRES MISSIONS D EXAMEN
REGLES INTERNES AU TRANSFERT DE DONNEES A CARACTERE PERSONNEL
 REGLES INTERNES AU TRANSFERT DE DONNEES A CARACTERE PERSONNEL L important développement à l international du groupe OVH et de ses filiales, conduit à l adoption des présentes règles internes en matière
REGLES INTERNES AU TRANSFERT DE DONNEES A CARACTERE PERSONNEL L important développement à l international du groupe OVH et de ses filiales, conduit à l adoption des présentes règles internes en matière
Rapport de certification
 Rapport de certification NetApp Data ONTAP v8.1.1 7-Mode Préparé par : le Centre de la sécurité des télécommunications Canada à titre d organisme de certification dans le cadre du Schéma canadien d évaluation
Rapport de certification NetApp Data ONTAP v8.1.1 7-Mode Préparé par : le Centre de la sécurité des télécommunications Canada à titre d organisme de certification dans le cadre du Schéma canadien d évaluation
NORME INTERNATIONALE D AUDIT 330 REPONSES DE L AUDITEUR AUX RISQUES EVALUES
 NORME INTERNATIONALE D AUDIT 330 REPONSES DE L AUDITEUR AUX RISQUES EVALUES Introduction (Applicable aux audits d états financiers pour les périodes ouvertes à compter du 15 décembre 2009) SOMMAIRE Paragraphe
NORME INTERNATIONALE D AUDIT 330 REPONSES DE L AUDITEUR AUX RISQUES EVALUES Introduction (Applicable aux audits d états financiers pour les périodes ouvertes à compter du 15 décembre 2009) SOMMAIRE Paragraphe
Commentaires sur le projet de lignes directrices (G3) pour l évaluation de la durabilité de la Global Reporting Initiative
 Le 28 mars 2006 Commentaires sur le projet de lignes directrices (G3) pour l évaluation de la durabilité de la Global Reporting Initiative Nous sommes heureux d avoir l occasion de présenter nos commentaires
Le 28 mars 2006 Commentaires sur le projet de lignes directrices (G3) pour l évaluation de la durabilité de la Global Reporting Initiative Nous sommes heureux d avoir l occasion de présenter nos commentaires
Conseil économique et social
 Nations Unies ECE/CECI/2015/7 Conseil économique et social Distr. générale 26 juin 2015 Français Original : anglais Commission économique pour l Europe Comité de l innovation, de la compétitivité et des
Nations Unies ECE/CECI/2015/7 Conseil économique et social Distr. générale 26 juin 2015 Français Original : anglais Commission économique pour l Europe Comité de l innovation, de la compétitivité et des
Arrêté royal du 27 mars 1998 relatif à la politique du bien-être des travailleurs lors de l exécution de leur travail (M.B. 31.3.
 Arrêté royal du 27 mars 1998 relatif à la politique du bien-être des travailleurs lors de l exécution de leur travail (M.B. 31.3.1998) Modifié par: (1) arrêté royal du 3 mai 1999 relatif aux missions et
Arrêté royal du 27 mars 1998 relatif à la politique du bien-être des travailleurs lors de l exécution de leur travail (M.B. 31.3.1998) Modifié par: (1) arrêté royal du 3 mai 1999 relatif aux missions et
Loi fédérale sur l agrément et la surveillance des réviseurs
 Loi fédérale sur l agrément et la surveillance des réviseurs (Loi sur la surveillance de la révision, LSR) 221.302 du 16 décembre 2005 (Etat le 1 er janvier 2013) L Assemblée fédérale de la Confédération
Loi fédérale sur l agrément et la surveillance des réviseurs (Loi sur la surveillance de la révision, LSR) 221.302 du 16 décembre 2005 (Etat le 1 er janvier 2013) L Assemblée fédérale de la Confédération
Outil d autoévaluation LPRPDE. Loi sur la protection des renseignements personnels et les documents électroniques
 Outil d autoévaluation LPRPDE Loi sur la protection des renseignements personnels et les documents électroniques table des matières Utilité de cet outil... 3 Utilisation de cet outil... 4 PARTIE 1 : Guide
Outil d autoévaluation LPRPDE Loi sur la protection des renseignements personnels et les documents électroniques table des matières Utilité de cet outil... 3 Utilisation de cet outil... 4 PARTIE 1 : Guide
Loi fédérale sur l agrément et la surveillance des réviseurs
 Loi fédérale sur l agrément et la surveillance des réviseurs (Loi sur la surveillance de la révision, LSR) 221.302 du 16 décembre 2005 (Etat le 1 er septembre 2007) L Assemblée fédérale de la Confédération
Loi fédérale sur l agrément et la surveillance des réviseurs (Loi sur la surveillance de la révision, LSR) 221.302 du 16 décembre 2005 (Etat le 1 er septembre 2007) L Assemblée fédérale de la Confédération
GROUPE DE CONTACT DES DIRECTEURS
 GROUPE DE CONTACT DES DIRECTEURS PREMIÈRE ÉDITION (4 Juin 2014) LISTE DE CONTROLE POUR ENGAGER UN BON CONSULTANT I. Travaux préparatoires en interne II. Critères personnels concernant le consultant III.
GROUPE DE CONTACT DES DIRECTEURS PREMIÈRE ÉDITION (4 Juin 2014) LISTE DE CONTROLE POUR ENGAGER UN BON CONSULTANT I. Travaux préparatoires en interne II. Critères personnels concernant le consultant III.
Standard de contrôle de sécurité WLA
 Standard de contrôle de sécurité WLA Standard de sécurité et d intégrité des activités de loterie et de jeu WLA-SCS:2012 Association mondiale des loteries (World Lottery Association) Édition Novembre 2014
Standard de contrôle de sécurité WLA Standard de sécurité et d intégrité des activités de loterie et de jeu WLA-SCS:2012 Association mondiale des loteries (World Lottery Association) Édition Novembre 2014
Manuel d assurance qualité ISO 9001:2000. Copie originale
 Manuel d assurance qualité ISO 9001:2000 Copie originale Approuvé par : Hugue Meloche ing. Page 1 de 24 Propriété intellectuelle Ce document, élaboré par Groupe Meloche Inc. pour sa compagnie située à
Manuel d assurance qualité ISO 9001:2000 Copie originale Approuvé par : Hugue Meloche ing. Page 1 de 24 Propriété intellectuelle Ce document, élaboré par Groupe Meloche Inc. pour sa compagnie située à
Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire
 1 2 3 4 Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire Partie 1 Chapitre 3: Locaux et matériel 5 6 7 8 9 10 11 12 13 PRINCIPE Les locaux et le matériel doivent être situés,
1 2 3 4 Bonnes Pratiques de Fabrication des médicaments à usage humain et vétérinaire Partie 1 Chapitre 3: Locaux et matériel 5 6 7 8 9 10 11 12 13 PRINCIPE Les locaux et le matériel doivent être situés,
ASSOCIATION CANADIENNE DES COURTIERS DE FONDS MUTUELS
 Le 12 septembre 2013 Introduction ASSOCIATION CANADIENNE DES COURTIERS DE FONDS MUTUELS PRINCIPE DIRECTEUR N O 2 DE L ACFM NORMES MINIMALES DE SURVEILLANCE DES COMPTES Le présent Principe directeur fixe
Le 12 septembre 2013 Introduction ASSOCIATION CANADIENNE DES COURTIERS DE FONDS MUTUELS PRINCIPE DIRECTEUR N O 2 DE L ACFM NORMES MINIMALES DE SURVEILLANCE DES COMPTES Le présent Principe directeur fixe
Parties communes et services
 Parties communes et services Ergonomie pratique en 128 points CHECKPOINT 95 Mettre des vestiaires et des sanitaires à la disposition des employés pour garantir un bon niveau d'hygiène et de propreté. POURQUOI
Parties communes et services Ergonomie pratique en 128 points CHECKPOINT 95 Mettre des vestiaires et des sanitaires à la disposition des employés pour garantir un bon niveau d'hygiène et de propreté. POURQUOI
Organisme Notifié N 1826 REFERENTIEL POUR LA CERTIFICATION DE CONFORMITE CE DES PLOTS RETROREFLECHISSANTS
 ASCQUER Référentiel pour la certification de conformité CE Organisme Notifié N 1826 REFERENTIEL POUR LA CERTIFICATION DE CONFORMITE CE DES PLOTS RETROREFLECHISSANTS EN 1463 partie 1 & 2 Révision n 2 Edition
ASCQUER Référentiel pour la certification de conformité CE Organisme Notifié N 1826 REFERENTIEL POUR LA CERTIFICATION DE CONFORMITE CE DES PLOTS RETROREFLECHISSANTS EN 1463 partie 1 & 2 Révision n 2 Edition
Mécanisme d examen de l application de la Convention des Nations Unies contre la corruption Documents de base
 Mécanisme d examen de l application de la Convention des Nations Unies contre la corruption Documents de base NATIONS UNIES Office DES NATIONS UNIES CONTRE LA DROGUE ET LE CRIME Vienne Mécanisme d examen
Mécanisme d examen de l application de la Convention des Nations Unies contre la corruption Documents de base NATIONS UNIES Office DES NATIONS UNIES CONTRE LA DROGUE ET LE CRIME Vienne Mécanisme d examen
TABLE DE MATIERES. Pourquoi les Organisations doivent-elles être accréditées?...
 TABLE DE MATIERES Qu est-ce que SADCAS? Pourquoi les Organisations doivent-elles être accréditées?... En quoi les Organismes d Accréditation peuvent être bénéfiques jusqu aux derniers utilisateurs?.. Le
TABLE DE MATIERES Qu est-ce que SADCAS? Pourquoi les Organisations doivent-elles être accréditées?... En quoi les Organismes d Accréditation peuvent être bénéfiques jusqu aux derniers utilisateurs?.. Le
Recours aux entreprises extérieures
 RECOMMANDATION R429 Recommandations adoptées par le Comité technique national de la chimie, du caoutchouc et de la plasturgie le 21 novembre 2006. Cette recommandation annule et remplace la recommandation
RECOMMANDATION R429 Recommandations adoptées par le Comité technique national de la chimie, du caoutchouc et de la plasturgie le 21 novembre 2006. Cette recommandation annule et remplace la recommandation
Assemblée des États Parties
 Cour pénale internationale Assemblée des États Parties Distr. : générale 29 octobre 2013 ICC-ASP/12/47 FRANÇAIS Original : anglais Douzième session The Hague, 20-28 novembre 2013 Rapport de la Commission
Cour pénale internationale Assemblée des États Parties Distr. : générale 29 octobre 2013 ICC-ASP/12/47 FRANÇAIS Original : anglais Douzième session The Hague, 20-28 novembre 2013 Rapport de la Commission
RÈGLES DE CERTIFICATION D ENTREPRISE
 RÈGLES DE CERTIFICATION D ENTREPRISE Fabrication et transformation de matériaux et d emballages destinés au contact des aliments : respect des règles d hygiène (méthode HACCP) Réf. Rédacteur LNE PP/GLB
RÈGLES DE CERTIFICATION D ENTREPRISE Fabrication et transformation de matériaux et d emballages destinés au contact des aliments : respect des règles d hygiène (méthode HACCP) Réf. Rédacteur LNE PP/GLB
Guide de travail pour l auto-évaluation:
 Guide de travail pour l auto-évaluation: Gouvernance d entreprise comité d audit Mars 2015 This document is also available in English. Conditions d application Le Guide de travail pour l auto-évaluation
Guide de travail pour l auto-évaluation: Gouvernance d entreprise comité d audit Mars 2015 This document is also available in English. Conditions d application Le Guide de travail pour l auto-évaluation
L application doit être validée et l infrastructure informatique doit être qualifiée.
 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 Annexe 11: Systèmes informatisés
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 Annexe 11: Systèmes informatisés
Rapport de certification
 Rapport de certification Évaluation EAL 3 + du produit Symantec Risk Automation Suite 4.0.5 Préparé par : Le Centre de la sécurité des télécommunications Canada à titre d organisme de certification dans
Rapport de certification Évaluation EAL 3 + du produit Symantec Risk Automation Suite 4.0.5 Préparé par : Le Centre de la sécurité des télécommunications Canada à titre d organisme de certification dans
Le marquage CE vous ouvre les portes du marché européen!
 Le marquage CE vous ouvre les portes du marché européen! Commission européenne Entreprises et industrie Table des matières Qu est-ce que le marquage CE? Qu est-ce que le marquage CE? 3 Obligations légales
Le marquage CE vous ouvre les portes du marché européen! Commission européenne Entreprises et industrie Table des matières Qu est-ce que le marquage CE? Qu est-ce que le marquage CE? 3 Obligations légales
Politique de gestion contractuelle de la SHDM
 Politique de gestion contractuelle de la SHDM Adoptée par les membres du conseil d administration le 22 octobre 2013 Direction des affaires juridiques et corporatives Politique de gestion contractuelle
Politique de gestion contractuelle de la SHDM Adoptée par les membres du conseil d administration le 22 octobre 2013 Direction des affaires juridiques et corporatives Politique de gestion contractuelle
Rapport de certification
 Rapport de certification Memory Arrays avec Memory Gateways Version 5.5.2 Préparé par : Le Centre de la sécurité des télécommunications à titre d organisme de certification dans le cadre du Schéma canadien
Rapport de certification Memory Arrays avec Memory Gateways Version 5.5.2 Préparé par : Le Centre de la sécurité des télécommunications à titre d organisme de certification dans le cadre du Schéma canadien
GUIDE D APPLICATION DE LA RÉGLEMENTATION
 GUIDE D APPLICATION DE LA RÉGLEMENTATION G-121 LA RADIOPROTECTION DANS LES ÉTABLISSEMENTS D ENSEIGNEMENT, DE SANTÉ ET DE RECHERCHE Publie par la Commission de controle de l'energie atomique Mai 2000 Commission
GUIDE D APPLICATION DE LA RÉGLEMENTATION G-121 LA RADIOPROTECTION DANS LES ÉTABLISSEMENTS D ENSEIGNEMENT, DE SANTÉ ET DE RECHERCHE Publie par la Commission de controle de l'energie atomique Mai 2000 Commission
L HABILITATION EN ÉLECTRICITÉ Démarche en vue de l habilitation du personnel
 Prévention et Gestion des Risques Professionnels Sécurité Sociale Caisse régionale d assurance maladie Alsace-Moselle L HABILITATION EN ÉLECTRICITÉ Démarche en vue de l habilitation du personnel Note Technique
Prévention et Gestion des Risques Professionnels Sécurité Sociale Caisse régionale d assurance maladie Alsace-Moselle L HABILITATION EN ÉLECTRICITÉ Démarche en vue de l habilitation du personnel Note Technique
Sécurité nucléaire. Résolution adoptée le 26 septembre 2014, à la neuvième séance plénière
 L atome pour la paix Conférence générale GC(58)/RES/11 Septembre 2014 Distribution limitée Français Original : anglais Cinquante-huitième session ordinaire Point 14 de l ordre du jour (GC(58)/22) Sécurité
L atome pour la paix Conférence générale GC(58)/RES/11 Septembre 2014 Distribution limitée Français Original : anglais Cinquante-huitième session ordinaire Point 14 de l ordre du jour (GC(58)/22) Sécurité
Etude des possibilités de passerelles entre les CQP des Entreprises de l industrie pharmaceutique et les CQP des industries chimiques
 Etude des possibilités de passerelles entre les CQP des Entreprises de l industrie et les CQP des industries chimiques @ COPYRIGHT LEEM - Page 1 sur 51 Sommaire 1 - Finalités des passerelles... 3 2 - Principes
Etude des possibilités de passerelles entre les CQP des Entreprises de l industrie et les CQP des industries chimiques @ COPYRIGHT LEEM - Page 1 sur 51 Sommaire 1 - Finalités des passerelles... 3 2 - Principes
DIRECTION DES SERVICES PROFESSIONNELS GESTION DES STUPÉFIANTS ET DES DROGUES CONTRÔLÉES EN PHARMACIE COMMUNAUTAIRE
 NUMÉRO 152 : JUIN 2005 DIRECTION DES SERVICES PROFESSIONNELS GESTION DES STUPÉFIANTS ET DES DROGUES CONTRÔLÉES EN PHARMACIE COMMUNAUTAIRE Depuis quelques années, le Bureau des substances contrôlés (BSC)
NUMÉRO 152 : JUIN 2005 DIRECTION DES SERVICES PROFESSIONNELS GESTION DES STUPÉFIANTS ET DES DROGUES CONTRÔLÉES EN PHARMACIE COMMUNAUTAIRE Depuis quelques années, le Bureau des substances contrôlés (BSC)
Qualité Sécurité Environnement
 Qualité Sécurité Environnement FORMATION AUDIT CONSEIL EXPERTISE >> Catalogue 2014 Nos innovations: e-learning, évaluation des compétences personnalisation Formation Hygiène Alimentaire ISO 9001 : 2008...
Qualité Sécurité Environnement FORMATION AUDIT CONSEIL EXPERTISE >> Catalogue 2014 Nos innovations: e-learning, évaluation des compétences personnalisation Formation Hygiène Alimentaire ISO 9001 : 2008...
Services de conciliation en assurance Cadre de collaboration et de surveillance. Approuvé par le CCRRA en juin 2015
 Services de conciliation en assurance Cadre de collaboration et de Approuvé par le CCRRA en juin 2015 Mise à jour du Forum conjoint des autorités de réglementation du marché financier Réseau de conciliation
Services de conciliation en assurance Cadre de collaboration et de Approuvé par le CCRRA en juin 2015 Mise à jour du Forum conjoint des autorités de réglementation du marché financier Réseau de conciliation
Rapport de certification
 Rapport de certification Évaluation EAL 2 + du produit Data Loss Prevention Version 11.1.1 Préparé par : Le Centre de la sécurité des télécommunications Canada à titre d organisme de certification dans
Rapport de certification Évaluation EAL 2 + du produit Data Loss Prevention Version 11.1.1 Préparé par : Le Centre de la sécurité des télécommunications Canada à titre d organisme de certification dans
Lignes directrices à l intention des praticiens
 Janvier 2005 Lignes directrices à l intention des praticiens Visiter notre site Web : www.cga-pdnet.org/fr-ca Le praticien exerçant seul ou au sein d un petit cabinet et l indépendance Le Code des principes
Janvier 2005 Lignes directrices à l intention des praticiens Visiter notre site Web : www.cga-pdnet.org/fr-ca Le praticien exerçant seul ou au sein d un petit cabinet et l indépendance Le Code des principes
RAPPORT DE LA PRESIDENTE DU CONSEIL DE SURVEILLANCE A L'ASSEMBLEE GENERALE ORDINAIRE ANNUELLE DU 15 JUIN
 " PRECIA " Société Anonyme à Directoire et à Conseil de Surveillance Au capital de 2 200 000 Siège social à VEYRAS - 07000 PRIVAS R.C.S. AUBENAS B. 386.620.165 (1966 B 16) RAPPORT DE LA PRESIDENTE DU CONSEIL
" PRECIA " Société Anonyme à Directoire et à Conseil de Surveillance Au capital de 2 200 000 Siège social à VEYRAS - 07000 PRIVAS R.C.S. AUBENAS B. 386.620.165 (1966 B 16) RAPPORT DE LA PRESIDENTE DU CONSEIL
EVALUATION DU RISQUE CHIMIQUE
 EVALUATION DU RISQUE CHIMIQUE Cette évaluation doit être systématique, quelle que soit l activité de l entreprise, même s il n y a pas d exposition a priori du fait des activités de travail. L'objectif
EVALUATION DU RISQUE CHIMIQUE Cette évaluation doit être systématique, quelle que soit l activité de l entreprise, même s il n y a pas d exposition a priori du fait des activités de travail. L'objectif
CHARTE DU COMITÉ DES RESSOURCES HUMAINES ET DE RÉMUNÉRATION DU CONSEIL D ADMINISTRATION DE TIM HORTONS INC.
 CHARTE DU COMITÉ DES RESSOURCES HUMAINES ET DE RÉMUNÉRATION DU CONSEIL D ADMINISTRATION DE TIM HORTONS INC. Adoptée le 28 septembre 2009 (Modification la plus récente : novembre 2013) La présente charte
CHARTE DU COMITÉ DES RESSOURCES HUMAINES ET DE RÉMUNÉRATION DU CONSEIL D ADMINISTRATION DE TIM HORTONS INC. Adoptée le 28 septembre 2009 (Modification la plus récente : novembre 2013) La présente charte
Banque européenne d investissement. Charte de l Audit interne
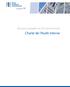 Charte de l Audit interne Juin 2013 Juin 2013 page 1 / 6 Juin 2013 page 2 / 6 1. Politique L Audit interne est une fonction essentielle dans la gestion de la Banque. Il aide la Banque en produisant des
Charte de l Audit interne Juin 2013 Juin 2013 page 1 / 6 Juin 2013 page 2 / 6 1. Politique L Audit interne est une fonction essentielle dans la gestion de la Banque. Il aide la Banque en produisant des
Conditions Générales du RME
 1. Champ d application 1 2. Règlement RME 1 3. Prestations du RME 1 3.1 Généralités 1 3.2 Enregistrement 1 3.3 Liste des Méthodes 2 3.4 Conditions d Enregistrement 2 3.5 Demandes d enregistrement 2 3.6
1. Champ d application 1 2. Règlement RME 1 3. Prestations du RME 1 3.1 Généralités 1 3.2 Enregistrement 1 3.3 Liste des Méthodes 2 3.4 Conditions d Enregistrement 2 3.5 Demandes d enregistrement 2 3.6
GLOSSAIRE DU SOUTIEN EN CAS DE RECOURS EN JUSTICE
 SOLUTIONS DE GESTION DE DOCUMENTS GLOSSAIRE DU SOUTIEN EN CAS DE RECOURS EN JUSTICE Le jargon du métier Initiation au soutien en cas de recours en justice Ce glossaire présente la terminologie et les notions
SOLUTIONS DE GESTION DE DOCUMENTS GLOSSAIRE DU SOUTIEN EN CAS DE RECOURS EN JUSTICE Le jargon du métier Initiation au soutien en cas de recours en justice Ce glossaire présente la terminologie et les notions
Pour la création d une maison d assistants maternels
 CHARTE DÉPARTEMENTALE Pour la création d une maison d assistants maternels Mars 2011 CHARTE DÉPARTEMENTALE Pour la création d une maison d assistants maternels Le Code de l Action Sociale et des Familles
CHARTE DÉPARTEMENTALE Pour la création d une maison d assistants maternels Mars 2011 CHARTE DÉPARTEMENTALE Pour la création d une maison d assistants maternels Le Code de l Action Sociale et des Familles
Conditions pour devenir un auditeur CanadaGAP
 Conditions pour devenir un auditeur CanadaGAP Pour être admissibles aux postes d auditeurs du programme CanadaGAP, tous les nouveaux candidats ayant reçu la formation après le 1 er avril 2015 doivent remplir
Conditions pour devenir un auditeur CanadaGAP Pour être admissibles aux postes d auditeurs du programme CanadaGAP, tous les nouveaux candidats ayant reçu la formation après le 1 er avril 2015 doivent remplir
Document d information 1. Principaux aspects de la proposition de la Commission COM (2000) 716 du point de vue de l alimentation animale
 Proposition de la Commission COM (2000) 716 établissant les principes généraux et les prescriptions générales du droit alimentaire, instituant l Autorité Alimentaire Européenne et fixant des procédures
Proposition de la Commission COM (2000) 716 établissant les principes généraux et les prescriptions générales du droit alimentaire, instituant l Autorité Alimentaire Européenne et fixant des procédures
