TECHNIQUES DE BASE EN CHIMIE ORGANIQUE
|
|
|
- Émilie Laroche
- il y a 10 ans
- Total affichages :
Transcription
1 TECHNIQUES DE BASE EN CHIMIE ORGANIQUE La synthèse organique suit en général le schéma suivant : Synthèse Séparation des produits Caractérisation du produit Pur? Oui Fin. Evaluation du rendement Non Purification La réaction de synthèse elle même se fait souvent dans un solvant (pour mettre les réactifs en contact) et à l aide d un montage de chauffage à reflux pour chauffer le milieu réactionnel. A l issue de cette synthèse, on obtient souvent un mélange de produit. Il est alors nécessaire de mettre en œuvre des techniques permettant de séparer et d extraire le produit désiré du mélange réactionnel. Il faut ensuite s assurer que le produit final est bien le produit recherché. Il faudra donc connaître les méthodes permettant d identifier un produit et d en contrôler la pureté. Si le produit n est pas pur, on pourra procéder à une purification. Une fois le produit pur obtenu, on en détermine la quantité de matière pour évaluer le rendement de la synthèse. 1
2 FICHE 1 : LE CHAUFFAGE A REFLUX Quand? Cette technique est utilisée pour accélérer (ou permettre) une réaction trop lente à température ambiante. Pourquoi? La température est un facteur cinétique : augmenter la température permet d accélérer la réaction. (En outre, le chauffage permet généralement d augmenter la solubilité des réactifs dans le solvant.) Néanmoins, si les réactifs ou les produits sont volatils, ils risquent de s évaporer. En adaptant un réfrigérant au dessus du système de chauffage, les vapeurs se recondensent et retombent dans le ballon. Le système de reflux permet donc de ne perdre ni réactifs ni produits. Le montage : 1 : Réfrigérant à boules 2 : Ballon 3 : Chauffe ballon, ou plaque chauffante + bain d huile (ou d eau si la température n excède pas 100 C) 4 : Sortie d eau 5 : Entrée d eau (par le bas du réfrigérant) 6 : Mélange réactionnel 7 : Support élévateur Le ballon doit être fixé solidement à la potence à l aide d une pince serrée sur la partie rodée de manière à tenir sans l aide du chauffe ballon. Il doit être placé suffisement haut pour pouvoir enlever rapidement le système de chauffage du ballon en baissant le support élévateur au cas où la réaction s emballerait. C est le premier élément à placer. Les rodages doivent être graissés. On placera pour cela un trait vertical de graisse sur la partie mâle du rodage ; une rotation de la verrerie lors de l emboîtement permettra de répartir la graisse uniformément. Le réfrigérant doit ensuite être placé sur le ballon, bien vertical, et maintenu à l aide d une pince. Cette pince ne doit pas être serrée, le réfirigérant est fragile. Conseils : Allumer la circulation d eau avant la mise en route du chauffage pour vérifier l absence de fuites. Lors du chauffage à reflux, il faut agiter le milieu réactionnel. Si le chauffe- ballon possède un dispositif d agitation magnétique, on placera un aimant (appelé turbulent, ici en forme d olive) dans le ballon. Si non, on dépose souvent quelques grains de pierre ponce (ou des billes de verre) pour réguler l'ébullition. Un thermomètre n'est pas nécessaire car la température n'a pas à être contrôlée en général. Il faut simplement chauffer le système pour l amener à ébullition. Ne jamais boucher le réfrigérant en haut : cela provoquerait une élévation de pression, voire une explosion. Questions pratiques : Pourquoi l eau froide arrive- t- elle par le bas dans le réfrigérant? Ceci permet de remplir totalement le réfrigérant, et d apporter l eau froide à l endroit où les vapeurs sont les plus chaudes. Que veut dire «chauffer au reflux du solvant pendant 10 minutes»? Si dans un protocole apparaît cette phrase, il faut compter les 10 minutes à partir du moment où le solvant est au reflux, et non dès que le chauffage est mis en marche. 2
3 FICHE 2 : LES METHODES DE SEPARATION 2A. Séparation d un liquide et d un solide : la FILTRATION SOUS VIDE ET L ESSORAGE Quand? A la fin ou au cours d une synthèse, on utilise cette méthode quand on souhaite séparer un solide d un liquide. Le principe : Pour cela, on réalise une filtration. Pour que celle- ci soit plus rapide et plus efficace, le liquide est souvent aspiré à l aide d une trompe à eau ou d une pompe : on parle alors de filtration sous vide ou filtration sur Büchner. Si on cherche à récupérer le solide, cette opération est appelée essorage du solide. Si c est le liquide qui doit être récupéré, on parle de filtration. Le montage : 1 : Solide 2 : Papier filtre 3 : Entonnoir Büchner, 4 : Fiole à vide 5 : Filtrat 6 : Cône en caoutchouc qui assure l étanchéité de la jonction La fiole à vide doit être fixée au bâti de la paillasse à l aide d une pince trois- doigts. Humidifier le papier filtre avec le solvant de la réaction (ou le solvant de lavage le cas échéant). Ajouter le mélange à filtrer dans le Büchner puis ouvrir le robinet de la trompe à eau. Si on cherche à récupérer le solide (essorage), rincer le ballon avec du solvant de façon à bien récupérer tout le solide. Ecraser le solide avec un tapon. Lorsque tout le liquide est passé dans la fiole à vide, casser le vide en décollant le Büchner de la fiole (ou tournant le robinet sur le tuyau s il y en a un), puis fermer le robinet de la trompe à eau. On peut ensuite récupérer le solide (ou le liquide, selon la phase qui nous intéresse). Complément : Comment débarrasser le solide isolé de quelques impuretés? Le lavage Pour améliorer la séparation et obtenir un solide plus pur, on peut réaliser un lavage. Pour cela, on utilise un solvant dans lequel le solide n est pas soluble. Après un premier essorage, on casse le vide, puis on ajoute le solvant de lavage (bien froid de préférence, pour minimiser la solubilité du produit). On triture le solide à l aide d un agitateur en verre (sans gratter le papier filtre) puis on refait le vide. On peut répéter l opération plusieurs fois. Cette étape permet d éliminer certaines impuretés emprisonnées sans le solide. Une fois le solide essoré, il est encore humide : dans une coupelle, on peut le placer entre deux papiers filtre et le presser à l aide d un tapon. Questions pratiques : Comment faire si le filtrat est trouble? Cela signifie que des particules de solide sont passées à travers le filtre. Il faut alors recommencer la filtration en utilisant un filtre moins poreux. 3
4 FICHE 2 : LES METHODES DE SEPARATION 2B. Séparation de deux liquides non miscibles : LA DECANTATION Quand? Au cours d une synthèse, on peut avoir à séparer deux phases liquides non miscibles, en général une phase organique et une phase aqueuse. Le principe : Les deux phases n ayant pas la même densité, il est possible de les séparer par décantation à l aide d une ampoule à décanter. Les phases se placent de bas en haut par ordre décroissant de densité. Il suffit alors d isoler la phase souhaitée. Vérifier que le robinet est fermé. Placer un bécher sous l ampoule à décanter. Mettre le mélange dans l ampoule. Fermer l ampoule à l aide d un bouchon. Retourner l ampoule et placer l ouverture vers le fond de la paillasse (jamais vers quelqu un!). Ouvrir le robinet pour dégazer. Refermer le robinet et agiter vigoureusement l ampoule. Dégazer de nouveau vers un endroit dégagé. Répéter l opération tant que du gaz s échappe lors du dégazage. Placer ensuit l ampoule sur l anneau, enlever le bouchon et attendre la démixtion (séparation des phases). On peut ensuite récupérer la phase voulue à l aide du robinet. Questions pratiques : Comment identifier la phase aqueuse et la phase organique? La phase la plus dense est située en dessous : une comparaison des densités permet de connaître à priori la position de la phase aqueuse. Néanmoins, la présence de solutés peut changer la densité de la phase. Pour identifier avec certitude la phase aqueuse, on peut ajouter quelques gouttes d eau pour voir à quelle phase elles s ajoutent, ou bien ajouter un volume conséquent d eau ou de solvant organique et chercher la phase dont le volume augmente. Complément : Comment éliminer l eau qui resterait dans la phase organique? Le séchage Si la phase d intérêt est la phase organique, et qu on a éliminé la phase aqueuse, on procède après la séparation au SECHAGE DE LA PHASE ORGANIQUE afin d éliminer les dernières traces d eau. Pour ce faire, on utilise du sulfate de magnésium anhydre MgSO 4. Il s agit d un solide très hydrophile. Lorsque cette poudre est versée sur une phase organique humide, elle capte l eau et s agglomère : MgSO 4 (s)+ H 2 O (l)!! MgSO 4,7H 2 O. Manipulation : Commencer par mettre une ou deux spatules de MgSO 4 et agiter à l aide d une baguette de verre ; si tout le sulfate de magnésium est coagulé au fond, en ajouter puis agiter à nouveau. Répéter l opération jusqu à ce que le sulfate de magnésium ne s agglomère plus et forme une pluie de cristaux fine. Agiter quelques minutes à l aide d un agitateur magnétique. Eliminer le solide par filtration simple (à l aide d un entonnoir et d un filtre plissé, voir ci- contre). 4
5 FICHE 2 : LES METHODES DE SEPARATION 2C. Passage d un soluté d une phase à une autre : L EXTRACTION ET LE LAVAGE Quand? En fin de synthèse, il arrive qu on souhaite faire passer dans un solvant S 2 un composé A qui se trouve (au moins en partie) dans un solvant S 1. Lorsque le but est de récupérer A dans le solvant S 2, on dit que l on fait une extraction de A par le solvant S 2. Lorsque le but est d éliminer A de la phase S 1, par exemple lorsque c est une impureté ou un reste de réactif, on dit qu on procède au lavage de S 1 par le solvant S 2. Le principe : S 1 et S 2 doivent être non miscibles. En général, l un des deux est l eau et constitue la phase aqueuse, l autre est un solvant organique (acétate d éthyle, éther, dichlorométhane, hexane ) et constitue la phase organique. On utilise la différence de solubilité. A doit être plus soluble dans le solvant S 2 que dans le solvant S 1. Il aura alors tendance à quitter la phase S 1 pour la phase S 2. Pour l extraction d un produit A d une phase S 1 vers une phase S 2 : on ajoute à la phase à extraire (S 1 ) un volume à peu près équivalent de la phase d extraction (S 2 ). On utilise ensuite une ampoule à décanter (voir 2B), et on sépare les deux phases après avoir bien agité. On garde la phase d extraction (S 2 ), puis on répète l opération sur la phase à extraire (S 1 ). Plus on répète le processus, meilleur est l extraction (par exemple, il est plus efficace d utiliser 3 fois 30 ml de S 2 plutôt qu 1 fois 90mL de S 2 ). Pour le lavage d une phase S 1 : on ajoute à la phase à laver (S 1 ) un volume à peu près équivalent de la phase de lavage (S 2 ). On utilise ensuite une ampoule à décanter (voir 2B), et on sépare les deux phases après avoir bien agité. On garde la phase lavée (S 1 ), puis on répète l opération avec un nouveau volume de phase de lavage (S 2 ). Complément : Comment diminuer l affinité d un composé organique pour la phase aqueuse (et ainsi diminuer la quantité perdue dans la phase aqueuse)? Le relargage Afin d améliorer l extraction d un composé vers une phase organique, un sel (très souvent le chlorure de sodium NaCl(s)) peut être ajouté à la phase aqueuse. Cette étape, appelée relargage, permet de mobiliser les molécules d eau encore piégée dans la phase organique (déshydratation de la phase organique) et de diminuer la solubilité du produit d intérêt dans la phase aqueuse. En effet, les ions Na + et Cl - ont une forte affinité pour l eau : les molécules d eau solvatent en priorité ces ions, ce qui entraîne une diminution de la solubilité des composés organiques dans l eau : ces composés organiques sont relargués dans la phase organique. Les molécules d eau éventuellement présentes dans la phase organique sont fortement attirées vers la phase aqueuse : la séparation des phases est améliorée. 5
6 FICHE 2 : LES METHODES DE SEPARATION 2D. Séparation de deux liquides miscibles ou non miscibles : LA DISTILLATION Quand? : La distillation permet de séparer deux liquides miscibles. Elle peut être utilisée : Au cours ou à l issue d une synthèse pour récupérer le produit. Afin d extraire un composé d une substance naturelle. Afin de déplacer un équilibre dans le sens de formation du produit en l éliminant au fur et à mesure du milieu réactionnel. Le principe : Les liquides à séparer n ont pas la même température d ébullition. Le composé le plus volatil se vaporisera plus facilement et composera la majeure partie des vapeurs. Il est ainsi possible de créer une phase gazeuse ayant une composition différente du mélange initial. Par condensation de ces vapeurs, un liquide appelé distillat peut être récupéré avec une concentration élevée en composé le plus volatil (attention, ce composé n est pas pur en général). Le ballon s enrichit en composé le moins volatil. Montage : Montage de distillation simple Montage de distillation fractionnée Introduire le mélange à distiller dans le ballon. Monter le dispositif, sans serrer les pinces hors des parties rodées. Démarrer la circulation d'eau dans le réfrigérant. Démarrer le chauffage, puis surveiller la température en tête de colonne. Cette température est celle des vapeurs qui se condensent dans le réfrigérant. Lorsque la composition de la vapeur reste fixe, la température en tête de colonne reste fixe. On observe alors un pallier de température. Quand la température de tête de colonne commence à remonter, c est que la composition des vapeurs change : changer alors le flacon récupérateur. Remarques : Le choix du montage dépend du mélange à distiller (voir cours en 2 ème année). Pour faciliter l ébullition, on peut baisser la pression au sein du milieu réactionnel. On parle alors de distillation sous pression réduite. 6
7 FICHE 2 : LES METHODES DE SEPARATION 2E. Evaporation du solvant à l aide L EVAPORATEUR ROTATIF Quand? A l issue d une synthèse, le composé d intérêt peut se trouver en solution dans un solvant organique qu il faut éliminer. Le principe : L évaporateur rotatif permet de réaliser une distillation rapide et efficace du solvant, sans exposer les molécules synthétisées (parfois fragiles) à un chauffage trop important grâce à une diminution de la pression. En effet, plus la pression diminue, plus la température d ébullition du solvant diminue. L évaporateur rotatif : Remarque : La dépression peut être obtenu par différents moyens : - Une trompe à eau (permettant d obtenir une dépression modérée). - Une pompe à membrane, qui génère une dépression plus importante. Déroulement : Faire circuler l'eau dans le réfrigérant. Préchauffer le bain- marie. Fixer le ballon contenant le solvant à extraire au conduit de vapeur à l'aide d'un clip adapté. Déclencher le système d obtention du vide. Mettre le ballon en rotation. Descendre le ballon pour le mettre en contact avec l'eau du bain- marie. Fermer doucement le robinet de mise sous vide pour mettre progressivement l'ensemble de l'appareil sous pression réduite. L'extraction commencée, on aperçoit des gouttes de solvant se condenser sur le réfrigérant et dans le ballon récepteur. Remarque : Parfois les vapeurs n'apparaissent pas et ne sont pas condensées : elles sont entraînées directement dans la trompe à eau ou la pompe, ce qui endommage la pompe. C'est le cas de solvant très volatil. Attention dans le cas des tels solvants (comme le diéthyléther) à ne pas trop abaisser la pression. Fin de la manipulation : Le produit, débarrassé de tout solvant, est en général obtenu sous forme de poudre ou d une huile. L'extraction terminée, retirer le ballon du système de chauffage au bain- marie et couper la rotation. S assurer que tout le solvant s est évaporé. Remettre l'ensemble à la pression atmosphérique en ouvrant doucement le robinet de mise sous vide. Enlever le clip et retirer le ballon dans le prolongement du conduit. Le ballon de récupération du solvant doit être vidé à la fin de chaque utilisation de l évaporateur rotatif. Questions pratiques : Quel est l intérêt de la rotation? La rotation du ballon plaque le liquide sur les parois ce qui a pour effet d augmenter la surface de contact avec la source thermique et ainsi d homogénéiser le chauffage. 7
8 FICHE 3 : LES METHODES DE CONTROLE DE LA PURETE 3A. Mesure de la TEMPERATURE DE FUSION D UN SOLIDE Quand? On se sert de cette méthode pour contrôler la pureté d un solide à l issue d une synthèse. Pourquoi? La température de fusion est une grandeur caractéristique d un corps pur. Vérifier la température de fusion du produit d une synthèse et la comparer aux données de la littérature permet de vérifier la pureté d un produit : si la température ne correspond pas (est plus basse en général), le produit n est pas pur. Si la température correspond (à plus ou moins 1 C, l incertitude du banc étant un général de ±1 C), on ne peut pas conclure de manière catégorique mais le produit peut être pur (il faut compéter la caractérisation par d autres méthodes). On utilise un banc Kofler : il s agit d un banc en métal qui présente un gradient de température d un bout à l autre du banc. Il s agit d un objet chaud, il doit donc être manipulé sans gants. Etalonner le banc à l aide du produit de référence dont la température de fusion est la plus proche du produit à tester. Pour cela : Ø Placer sur le banc une pointe de spatule du produit étalon une dizaine de degré en dessous de sa température de fusion. Ø Déplacer les grains de solide lentement vers la partie plus chaude. Ø Une fois que la fusion commence, continuer à pousser le solide de façon à obtenir une moitié du composé à l état liquide et l autre toujours à l état solide. Ø Repérer la limite de fusion à l aide du curseur rabattable. Ø Déplacer l index mobile de sorte à amener son extrémité sur la valeur de température de fusion du solide étalon. Ø Nettoyer le banc, en poussant le reste de solide étalon avec un morceau de coton sec perpendiculairement au banc. Placer ensuite sur le banc une pointe de spatule du produit à tester du côté des basses températures (ne pas en mettre trop). A l aide de la spatule, pousser doucement l échantillon vers les hautes températures jusqu à voir fondre les premiers cristaux. Lire alors la température de fusion en plaçant le curseur à la limite entre le solide et les cristaux fondus. Nettoyer le banc à l aide d un coton imbibé d alcool (transversalement au banc). Questions pratiques : Qu indique une température de fusion différente de la température tabulée? Si la température de fusion observée est plus basse que la température tabulée, cela est généralement dû à la présence d impuretés. Il faut alors procéder à une purification du solide, par exemple par recristallisation. Si la température de fusion observée est plus haute que la température tabulée, cela est généralement dû à la présence de solvants peu volatils (de l eau par exemple). Ce solvant s évapore sur le banc, en consommant de l énergie, et retarde la fusion du produit. Pour se débarasser de ce solvant, il faut sécher plus longtemps le produit en le replaçant à l étuve. 8
9 FICHE 3 : LES METHODES DE CONTROLE DE LA PURETE 3B. La CHROMATOGRAPHIE SUR COUCHE MINCE (CCM) Quand? A la fin d une synthèse, on peut réaliser une CCM pour vérifier la pureté d un produit (solide ou liquide) et l identifier. Pourquoi? Le rapport frontal d un composé dans un éluant donné est une grandeur caractéristique. Mesurer un rapport frontal permet donc de s assurer de la nature d un composé en le comparant avec un produit de référence. De plus, lorsque l éluant est bien choisi, on peut séparer les constituants d un mélange. En testant un produit, on peut ainsi s assurer de sa pureté ou au contraire identifier les différents composés présents. Le principe : Cette méthode est basée sur la plus ou moins grande affinité de chaque constituant pour la phase stationnaire (plaque de silice) et la phase mobile (éluant). a. Préparation de la cuve Verser l éluant dans la cuve, sur une hauteur de 0,5 à 1 cm. Fermer la cuve pour la saturer en vapeurs d éluant. La cuve est placée sur la paillasse de manière à pouvoir y déposer la plaque et l en ressortir sans avoir à déplacer la cuve. b. Préparation des échantillons Préparer les échantillons à déposer en solubilisant tous les produits à déposer dans un solvant volatil (une pointe de spatule dans 1mL). On pourra déposer par exemple : le produit à analyser, les réactifs de départ, un échantillon commercial du produit synthétisé c. Préparation de la plaque Ne jamais mettre les doigts sur la plaque. On la saisit par les bords ou avec une pince. A 1 cm du bas de la plaque, tracer à la règle un trait au crayon à papier (sans appuyer pour ne pas détériorer la couche de silice). Cette ligne est appelée ligne de dépôt. Repérer avec le crayon les différents emplacements de dépôt en indiquant succinctement en dessous de quoi il s agit (par exemple P pour produit, R pour référence ). Les dépôts doivent être distants d au minimum 0,5 cm les uns des autres et des bords. Effectuer les dépôts à l aide d un capillaire, placé perpendiculairement à la plaque de silice. Les taches ne doivent pas excéder 2mm de diamètre. Sécher la plaque à l air ou à l aide d un sèche- cheveux. Conseil : Il est recommandé si possible de contrôler la taille des dépôts sous la lampe UV : Ø Si les taches sont trop larges, elles risquent de se recouvrir lors de l élution. Il faut alors recommencer en diluant d avantage les échantillons. Ø Si les taches sont trop peu visibles, on peut réitérer le dépôt. d. Elution de la plaque Déposer la plaque dans la cuve, le plus verticalement possible en prenant soin que la ligne de dépôt ne touche pas l éluant (attention donc à ne pas mettre trop d éluant dans la cuve). Refermer la cuve, et ne plus la déplacer pendant toute la migration de l éluant. Quand le front de l éluant arrive à environ 1 cm du bord supérieur de la plaque, retirer la plaque de la cuve et repérer immédiatement le front de l éluant par un trait de crayon. Sécher la plaque, à l air ou au sèche- cheveux. 9
10 e. Révélation de la plaque Si les taches sont colorées, le résultat est visible. Sinon il faut révéler la plaque à l aide d une des méthodes suivantes. Ø A la lampe UV : les plaques utilisées sont (en général) recouvertes d une substance fluorescente : placée sous une lampe UV, la plaque emet une lumière verte. Si les composés déposés sur la plaque absorbent le rayonnement UV, les dépôts apparaitront sous la lampe UV sous forme de taches sombres (car les composés déposés empêchent la plaque de fluorescer). Cette méthode pourra être utilisée pour les composés qui absorbent dans l UV, par exemple ceux qui possèdent des doubles liaisons conjuguées (par exemple les dérivés du benzène). Entourer les tâches sous la lampe UV en protégeant vos yeux à l aide de lunettes adaptées. Ø Avec un révélateur chimique : le diiode est souvent utilisé pour la révélation de composés organiques car il forme avec ces composés des complexes bruns. Pour cela, placer la plaque dans une cuve contenant des cristaux de diiode. Des taches brunes apparaissent aux endroits où le diiode réagit avec les dépôts. f. Calcul des rapports frontaux distance parcourue par le composé Rf = distance parcourue par l éluant Ex : Rf 1 =r 1 /R La distance parcourue par le composé est mesurée au centre de la tache, ou en haut de la traînée le cas échéant. Remarque : deux composés différents peuvent avoir des rapports frontaux proches, attention donc à ne pas conclure sur cette seule donnée. g. Commentaires et présentation des résultats On présentera les résultats de la façon suivante : Conditions : - Plaque (silice en général) - Eluant - Mode de révélation Plaque de CCM (collée ou dessinée) - Légende des dépôts - Calcul des rapports frontaux Interprétation : - S il s agit d un produit formé en TP, conclure sur la pureté du produit : si plusieurs taches apparaissent, le produit n est pas pur. - Comparer les rapports frontaux (produit synthétisé, réactifs, références) et conclure quand à la composition du produit analysé. 10
11 FICHE 3 : LES METHODES DE CONTROLE DE LA PURETE 3C. Contrôle de la pureté d un liquide : MESURE DE L INDICE DE REFRACTION Quand? : Lorsque le produit d une synthèse est liquide, la vérification de son indice de réfraction constitue un test de pureté. Pourquoi? L indice de réfraction n d un liquide est défini par le rapport entre la vitesse de la lumière dans le vide et dans ce liquide. (Remarque : Expérimentalement cette détermination se fera par rapport à l air et non au vide). L indice de réfraction, à une température donnée et une longueur d onde donnée, est une caractéristique physique d un composé pur. Principe : L indice de réfraction d un liquide est habituellement compris entre 1,3000 et 1,7000. L indice de réfraction varie avec la température et la longueur d onde de la lumière utilisée et bien sûr la nature du liquide. Le plus souvent, la lumière employée est la raie D du sodium, on fera alors apparaître cette information à l aide d un indice inférieur : n D. On indiquera également, à l aide d un indice supérieur, la température à laquelle la mesure a été effectuée. On trouve l indice de réfraction tabulé à 20 C soit n 20 D. L indice de réfraction diminue avec un accroissement de température Remarque : Si la mesure a été effectuée à une température différente de 20 C, on pourra appliquer une correction afin de comparer cette valeur à celle théorique. La formule suivante sera appliquée : n D 20 = n D T - 0,00045.(T- 20) où T est la température en C Plus l indice de réfraction mesuré est proche de l indice de réfraction tabulé, plus le liquide est susceptible d être pur. En TP, on considèrera qu un liquide est susceptible d être pur lorsque son indice est égal à l indice tabulé ±0,001. Protocole : L indice de réfraction est mesuré à l aide d un réfractomètre d Abbe. Vérifier que le bain thermostaté est allumé et réglé à 20 C. Sinon relever la température de la pièce et utiliser la formule ci- dessus. Allumer la lampe. Déposer quelques gouttes de l échantillon entre les deux faces du prisme. Attention à ne pas toucher le prisme (très fragile). Rabattre la face supérieure du prisme et fermez avec le loquet à gauche. Avec la molette 2, amener la frontière entre les zones sombres et claires au centre du réticule Avec la molette 1, ajuster afin d obtenir une séparation nette entre la zone sombre et la zone claire. Si vous n ajustez pas assez, une irisation bleue apparait, dans le cas contraire une irisation rouge apparait. Vous devez être à la limite. La lecture de l indice de réfraction se fait en bas. Le résultat de votre mesure doit comporter 5 chiffres significatifs. Sachant que le réfractomètre est précis à ± 0,0005, votre résultat sera, par exemple, de la forme : 1,5110 ± 0,0005 Vue par l oculaire : Sur l exemple à gauche, n=1,3170 ± 0,0005 Après la mesure, nettoyer le prisme avec un coton imbibé d éthanol que vous jetterez à la poubelle ensuite. Remarque : comme tout appareil de mesure le réfractomètre doit être étalonné. Cet étalonnage est réalisé par le technicien, les réglages restent stables sur la durée. 11
12 FICHE 4 : LES METHODES DE PURIFICATION 4A. LA RECRISTALLISATION Quand? Si à l issue d une synthèse le solide obtenu n est pas pur (information obtenu par l une des méthodes de contrôle de pureté, voir fiche 3), on peut le purifier par recristallisation. Le principe : Une recristallisation consiste à solubiliser à chaud un composé solide impur dans un minimum de solvant. On choisit un solvant dans lequel : Le produit à purifier est insoluble dans le solvant à froid, mais soluble dans le solvant à chaud. Les impuretés sont solubles à froid dans le solvant. En solubilisant l échantillon à chaud, le produit à purifier et les impuretés passent en solution. On refroidit ensuite le solvant : le composé à purifier, non soluble à froid, recristallise alors que les impuretés restent en solution : le produit a été purifié. Un essorage (voir fiche 2A) permet enfin d éliminer le solvant (avec les impuretés) et d isoler le solide purifié. Le montage : Fixation pince à lâche 2 vis et noix 2 réfrigérant à boules voire de Liebig Fixation pince ferme à 2 vis et noix 1 erlenmeyer barreau aimanté sortie de l'eau arrivée de l'eau 2 feuilles anglaises (ou tuyaux de caoutchouc) adaptées aux tubulures Placer le solide dans un erlenmeyer (ou dans un ballon) et le recouvrir du solvant de recristallisation. Réaliser le montage ci- contre (la plaque chauffante sera remplacée par un chauffe- ballon si on utilise un ballon). Porter à ébullition. Si tout le solide n est pas dissout, on ajoute un peu de solvant par le haut du réfrigérant. Une fois que le solide est dissous, transvaser le mélange dans un bécher propre. Laisser le bécher revenir à température ambiante jusqu à apparition des premiers cristaux. Refroidir ensuite éventuellement à l aide d un bain d eau ou de glace. Essorer sur Büchner et laver avec le solvant froid. Vérifier alors la pureté du produit. Questions pratiques : Que faire si le solide ne précipite pas? Ø On peut abaisser la solubilité du solide en plongeant le ballon dans un bain de glace (voir point suivant). Ø On peut ajouter un deuxième solvant, appelé co- solvant, dans lequel le produit pur est peu soluble. Ø Parfois un blocage cinétique empêche la recristallisation du solide. On peut alors amorcer cette recristallition en grattant le fond du ballon à l aide d une baguette de verre (de microéclats de verre joueront le rôle de points de nucléation). Ø Si trop de solvant a été ajouté, la recristallisation n a pas lieu. Il est alors nécessaire d éliminer tout le solvant à l évaporateur rotatif et de recommencer le protocole. Pourquoi laisser le bécher refroidir lentement? Si le solide cristallise trop vite, il va piéger une grande partie des impuretés, rendant la purification peu efficace. Il n est donc pas recommandé de mettre le bécher directement dans un bain de glace. 4B. LA DISTILLATION Quand? Si à l issue d une synthèse le liquide obtenu n est pas pur (information obtenu par l une des méthodes de contrôle de pureté), on peut le distiller. Principe, protocole : voir fiche 2D. 12
Savoir écouter, assimiler : s approprier
 PCSI TP-DI Chimie organique INITIATION A LA CHIMIE ORGANIQUE Travail élève : savoirs et actions Compétences attendues Au début du TP, quelques explications orales sur le déroulement de la séance, sur le
PCSI TP-DI Chimie organique INITIATION A LA CHIMIE ORGANIQUE Travail élève : savoirs et actions Compétences attendues Au début du TP, quelques explications orales sur le déroulement de la séance, sur le
CHROMATOGRAPHIE SUR COUCHE MINCE
 CHROMATOGRAPHIE SUR COUCHE MINCE I - PRINCIPE La chromatographie est une méthode physique de séparation de mélanges en leurs constituants; elle est basée sur les différences d affinité des substances à
CHROMATOGRAPHIE SUR COUCHE MINCE I - PRINCIPE La chromatographie est une méthode physique de séparation de mélanges en leurs constituants; elle est basée sur les différences d affinité des substances à
TECHNIQUES: Principes de la chromatographie
 TECHNIQUES: Principes de la chromatographie 1 Définition La chromatographie est une méthode physique de séparation basée sur les différentes affinités d un ou plusieurs composés à l égard de deux phases
TECHNIQUES: Principes de la chromatographie 1 Définition La chromatographie est une méthode physique de séparation basée sur les différentes affinités d un ou plusieurs composés à l égard de deux phases
Suivi d une réaction lente par chromatographie
 TS Activité Chapitre 8 Cinétique chimique Suivi d une réaction lente par chromatographie Objectifs : Analyser un protocole expérimental de synthèse chimique Analyser un chromatogramme pour mettre en évidence
TS Activité Chapitre 8 Cinétique chimique Suivi d une réaction lente par chromatographie Objectifs : Analyser un protocole expérimental de synthèse chimique Analyser un chromatogramme pour mettre en évidence
Fiche 23 : Au laboratoire
 Fiche 23 : Au laboratoire 05/03/2007 Au laboratoire Le port de la blouse est obligatoire. Le port des lunettes ou surlunettes est obligatoire (attention au port des lentilles de contact, autorisé mais
Fiche 23 : Au laboratoire 05/03/2007 Au laboratoire Le port de la blouse est obligatoire. Le port des lunettes ou surlunettes est obligatoire (attention au port des lentilles de contact, autorisé mais
Synthèse et propriétés des savons.
 Synthèse et propriétés des savons. Objectifs: Réaliser la synthèse d'un savon mise en évidence de quelques propriétés des savons. I Introduction: 1. Présentation des savons: a) Composition des savons.
Synthèse et propriétés des savons. Objectifs: Réaliser la synthèse d'un savon mise en évidence de quelques propriétés des savons. I Introduction: 1. Présentation des savons: a) Composition des savons.
Matériel de laboratoire
 Matériel de laboratoire MATERIAUX UTILISE... 1 L'APPAREILLAGE DE LABORATOIRE... 1 a) Les récipients à réaction... 2 b) La verrerie Graduée... 2 MATERIEL DE FILTRATION... 6 FILTRATION SOUS VIDE AVEC UN
Matériel de laboratoire MATERIAUX UTILISE... 1 L'APPAREILLAGE DE LABORATOIRE... 1 a) Les récipients à réaction... 2 b) La verrerie Graduée... 2 MATERIEL DE FILTRATION... 6 FILTRATION SOUS VIDE AVEC UN
(aq) sont colorées et donnent à la solution cette teinte violette, assimilable au magenta.»
 Chapitre 5 / TP 1 : Contrôle qualité de l'eau de Dakin par dosage par étalonnage à l'aide d'un spectrophotomètre Objectif : Vous devez vérifier la concentration massique d'un désinfectant, l'eau de Dakin.
Chapitre 5 / TP 1 : Contrôle qualité de l'eau de Dakin par dosage par étalonnage à l'aide d'un spectrophotomètre Objectif : Vous devez vérifier la concentration massique d'un désinfectant, l'eau de Dakin.
TP : Suivi d'une réaction par spectrophotométrie
 Nom : Prénom: n groupe: TP : Suivi d'une réaction par spectrophotométrie Consignes de sécurité de base: Porter une blouse en coton, pas de nu-pieds Porter des lunettes, des gants (en fonction des espèces
Nom : Prénom: n groupe: TP : Suivi d'une réaction par spectrophotométrie Consignes de sécurité de base: Porter une blouse en coton, pas de nu-pieds Porter des lunettes, des gants (en fonction des espèces
Comment suivre l évolution d une transformation chimique? + S 2 O 8 = I 2 + 2 SO 4
 Afin d optimiser leurs procédés, les industries chimiques doivent contrôler le bon déroulement de la réaction de synthèse menant aux espèces voulues. Comment suivre l évolution d une transformation chimique?
Afin d optimiser leurs procédés, les industries chimiques doivent contrôler le bon déroulement de la réaction de synthèse menant aux espèces voulues. Comment suivre l évolution d une transformation chimique?
TP n 1: Initiation au laboratoire
 Centre Universitaire d El-Tarf Institut des Sciences Agronomiques 3 ème année Contrôle de Qualité en Agroalimentaire TP n 1: Initiation au laboratoire Introduction L analyse de la matière vivante au laboratoire
Centre Universitaire d El-Tarf Institut des Sciences Agronomiques 3 ème année Contrôle de Qualité en Agroalimentaire TP n 1: Initiation au laboratoire Introduction L analyse de la matière vivante au laboratoire
33-Dosage des composés phénoliques
 33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
TP 3 diffusion à travers une membrane
 TP 3 diffusion à travers une membrane CONSIGNES DE SÉCURITÉ Ce TP nécessite la manipulation de liquides pouvant tacher les vêtements. Le port de la blouse est fortement conseillé. Les essuie tout en papier
TP 3 diffusion à travers une membrane CONSIGNES DE SÉCURITÉ Ce TP nécessite la manipulation de liquides pouvant tacher les vêtements. Le port de la blouse est fortement conseillé. Les essuie tout en papier
Spectrophotométrie - Dilution 1 Dilution et facteur de dilution. 1.1 Mode opératoire :
 Spectrophotométrie - Dilution 1 Dilution et facteur de dilution. 1.1 Mode opératoire : 1. Prélever ml de la solution mère à la pipette jaugée. Est-ce que je sais : Mettre une propipette sur une pipette
Spectrophotométrie - Dilution 1 Dilution et facteur de dilution. 1.1 Mode opératoire : 1. Prélever ml de la solution mère à la pipette jaugée. Est-ce que je sais : Mettre une propipette sur une pipette
TRAVAUX PRATIQUESDE BIOCHIMIE L1
 TRAVAUX PRATIQUESDE BICHIMIE L1 PRINTEMPS 2011 Les acides aminés : chromatographie sur couche mince courbe de titrage Etude d une enzyme : la phosphatase alcaline QUELQUES RECMMANDATINS IMPRTANTES Le port
TRAVAUX PRATIQUESDE BICHIMIE L1 PRINTEMPS 2011 Les acides aminés : chromatographie sur couche mince courbe de titrage Etude d une enzyme : la phosphatase alcaline QUELQUES RECMMANDATINS IMPRTANTES Le port
EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points)
 Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage
 PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage I) Qu'est-ce qu'un savon et comment le fabrique-t-on? D'après épreuve BAC Liban 2005 Physique-Chimie dans la cuisine Chapitre 3 1/6 1- En vous
PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage I) Qu'est-ce qu'un savon et comment le fabrique-t-on? D'après épreuve BAC Liban 2005 Physique-Chimie dans la cuisine Chapitre 3 1/6 1- En vous
SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION)
 Terminale S CHIMIE TP n 2b (correction) 1 SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION) Objectifs : Déterminer l évolution de la vitesse de réaction par une méthode physique. Relier l absorbance
Terminale S CHIMIE TP n 2b (correction) 1 SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION) Objectifs : Déterminer l évolution de la vitesse de réaction par une méthode physique. Relier l absorbance
SP. 3. Concentration molaire exercices. Savoir son cours. Concentrations : Classement. Concentration encore. Dilution :
 SP. 3 Concentration molaire exercices Savoir son cours Concentrations : Calculer les concentrations molaires en soluté apporté des solutions désinfectantes suivantes : a) Une solution de 2,0 L contenant
SP. 3 Concentration molaire exercices Savoir son cours Concentrations : Calculer les concentrations molaires en soluté apporté des solutions désinfectantes suivantes : a) Une solution de 2,0 L contenant
CODEX ŒNOLOGIQUE INTERNATIONAL. SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012)
 SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012) 1. OBJET, ORIGINE ET DOMAINE D APPLICATION Le sucre de raisin est obtenu exclusivement à partir du
SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012) 1. OBJET, ORIGINE ET DOMAINE D APPLICATION Le sucre de raisin est obtenu exclusivement à partir du
LE SPECTRE D ABSORPTION DES PIGMENTS CHLOROPHYLLIENS
 Fiche sujet-élève Les végétaux chlorophylliens collectent l énergie lumineuse grâce à différents pigments foliaires que l on peut classer en deux catégories : - les chlorophylles a et b d une part, - les
Fiche sujet-élève Les végétaux chlorophylliens collectent l énergie lumineuse grâce à différents pigments foliaires que l on peut classer en deux catégories : - les chlorophylles a et b d une part, - les
Exemple de cahier de laboratoire : cas du sujet 2014
 Exemple de cahier de laboratoire : cas du sujet 2014 Commentaires pour l'évaluation Contenu du cahier de laboratoire Problématique : Le glucose est un nutriment particulièrement important pour le sportif.
Exemple de cahier de laboratoire : cas du sujet 2014 Commentaires pour l'évaluation Contenu du cahier de laboratoire Problématique : Le glucose est un nutriment particulièrement important pour le sportif.
Niveau 2 nde THEME : L UNIVERS. Programme : BO spécial n 4 du 29/04/10 L UNIVERS
 Document du professeur 1/7 Niveau 2 nde THEME : L UNIVERS Physique Chimie SPECTRES D ÉMISSION ET D ABSORPTION Programme : BO spécial n 4 du 29/04/10 L UNIVERS Les étoiles : l analyse de la lumière provenant
Document du professeur 1/7 Niveau 2 nde THEME : L UNIVERS Physique Chimie SPECTRES D ÉMISSION ET D ABSORPTION Programme : BO spécial n 4 du 29/04/10 L UNIVERS Les étoiles : l analyse de la lumière provenant
direct serve EN DE NI ES PT CZ SK www.moulinex.com
 FR direct serve EN DE NI ES PT CZ SK www.moulinex.com 4 3 2 1 71mm 5 6 7 1 2 3 4 5 6 OK Click NO 7 8 9 150ml 10 Nous vous remercions d avoir choisi un appareil de la gamme Moulinex. CONSIGNES DE SECURITE
FR direct serve EN DE NI ES PT CZ SK www.moulinex.com 4 3 2 1 71mm 5 6 7 1 2 3 4 5 6 OK Click NO 7 8 9 150ml 10 Nous vous remercions d avoir choisi un appareil de la gamme Moulinex. CONSIGNES DE SECURITE
Les solutions. Chapitre 2 - Modèle. 1 Définitions sur les solutions. 2 Concentration massique d une solution. 3 Dilution d une solution
 Chapitre 2 - Modèle Les solutions 1 Définitions sur les solutions 1.1 Définition d une solution : Une solution est le mélange homogène et liquide d au moins deux espèces chimiques : Le soluté : c est une
Chapitre 2 - Modèle Les solutions 1 Définitions sur les solutions 1.1 Définition d une solution : Une solution est le mélange homogène et liquide d au moins deux espèces chimiques : Le soluté : c est une
EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points)
 BAC S 2011 LIBAN http://labolycee.org EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points) Les parties A et B sont indépendantes. A : Étude du fonctionnement d un spectrophotomètre
BAC S 2011 LIBAN http://labolycee.org EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points) Les parties A et B sont indépendantes. A : Étude du fonctionnement d un spectrophotomètre
259 VOLUMETRIE ET TITRATION DOSAGE DU NaOH DANS LE DESTOP
 259 VOLUMETRIE ET TITRATION DOSAGE DU NaOH DANS LE DESTOP A d a p t a t i o n : A. - M. F o u r n i e r ( C o p a d ), M. C a s a n o v a & H. J e n n y ( C d C ) 2 0 0 1 C o n c e p t i o n D. M a r g
259 VOLUMETRIE ET TITRATION DOSAGE DU NaOH DANS LE DESTOP A d a p t a t i o n : A. - M. F o u r n i e r ( C o p a d ), M. C a s a n o v a & H. J e n n y ( C d C ) 2 0 0 1 C o n c e p t i o n D. M a r g
FICHE 1 Fiche à destination des enseignants
 FICHE 1 Fiche à destination des enseignants 1S 8 (b) Un entretien d embauche autour de l eau de Dakin Type d'activité Activité expérimentale avec démarche d investigation Dans cette version, l élève est
FICHE 1 Fiche à destination des enseignants 1S 8 (b) Un entretien d embauche autour de l eau de Dakin Type d'activité Activité expérimentale avec démarche d investigation Dans cette version, l élève est
Mise en pratique : Etude de spectres
 Mise en pratique : Etude de spectres Introduction La nouvelle génération de spectromètre à détecteur CCD permet de réaliser n importe quel spectre en temps réel sur toute la gamme de longueur d onde. La
Mise en pratique : Etude de spectres Introduction La nouvelle génération de spectromètre à détecteur CCD permet de réaliser n importe quel spectre en temps réel sur toute la gamme de longueur d onde. La
Chauffer l eau avec le soleil Est-ce possible? Première étape :
 Chauffer l eau avec le soleil Est-ce possible? Première étape : Peut-on chauffer de l eau avec le soleil? Les différents groupes ont posé un simple récipient au soleil dans la cour. Le constat de l élévation
Chauffer l eau avec le soleil Est-ce possible? Première étape : Peut-on chauffer de l eau avec le soleil? Les différents groupes ont posé un simple récipient au soleil dans la cour. Le constat de l élévation
UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure
 UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure APPEL D OFFRES OUVERT SUR OFFRES DE PRIX 08/ENS/24 BORDEREAU DES PRIX-DETAIL ESTIMATIF Lot n 2 : Achat et installation de matériel pour l enseignement
UNIVERSITE MOHAMMED V Rabat Ecole Normale Supérieure APPEL D OFFRES OUVERT SUR OFFRES DE PRIX 08/ENS/24 BORDEREAU DES PRIX-DETAIL ESTIMATIF Lot n 2 : Achat et installation de matériel pour l enseignement
Capteur optique à dioxygène
 Capteur optique à dioxygène Référence PS- 2196 Connectique de la sonde mini DIN Tête de la sonde Embout de protection et stockage Port mini DIN du capteur Eléments inclus 1. Capteur à dioxygène optique
Capteur optique à dioxygène Référence PS- 2196 Connectique de la sonde mini DIN Tête de la sonde Embout de protection et stockage Port mini DIN du capteur Eléments inclus 1. Capteur à dioxygène optique
SALLE DE BAIN, DOUCHE, PLAN DE TRAVAIL CUISINE, PISCINE... Collage et jointoiement. L Epoxy facile
 SALLE DE BAIN, DOUCHE, PLAN DE TRAVAIL CUISINE, PISCINE... Collage et jointoiement L Epoxy facile DOMAINES D EMPLOI Recommandé pour salle de bain, douche, plan de travail cuisine, piscine, bassins thermaux,
SALLE DE BAIN, DOUCHE, PLAN DE TRAVAIL CUISINE, PISCINE... Collage et jointoiement L Epoxy facile DOMAINES D EMPLOI Recommandé pour salle de bain, douche, plan de travail cuisine, piscine, bassins thermaux,
Chapitre 02. La lumière des étoiles. Exercices :
 Chapitre 02 La lumière des étoiles. I- Lumière monochromatique et lumière polychromatique. )- Expérience de Newton (642 727). 2)- Expérience avec la lumière émise par un Laser. 3)- Radiation et longueur
Chapitre 02 La lumière des étoiles. I- Lumière monochromatique et lumière polychromatique. )- Expérience de Newton (642 727). 2)- Expérience avec la lumière émise par un Laser. 3)- Radiation et longueur
Planches pour le Diagnostic microscopique du paludisme
 République Démocratique du Congo Ministère de la Santé Programme National de Lutte Contre le Paludisme Planches pour le Diagnostic microscopique du paludisme Ces planches visent à améliorer le diagnostic
République Démocratique du Congo Ministère de la Santé Programme National de Lutte Contre le Paludisme Planches pour le Diagnostic microscopique du paludisme Ces planches visent à améliorer le diagnostic
Meine Flüssigkeit ist gefärbt*, comme disaient August Beer (1825-1863) et Johann Heinrich Lambert (1728-1777)
 1ère S Meine Flüssigkeit ist gefärbt*, comme disaient August Beer (1825-1863) et Johann Heinrich Lambert (1728-1777) Objectif : pratiquer une démarche expérimentale pour déterminer la concentration d une
1ère S Meine Flüssigkeit ist gefärbt*, comme disaient August Beer (1825-1863) et Johann Heinrich Lambert (1728-1777) Objectif : pratiquer une démarche expérimentale pour déterminer la concentration d une
Bleu comme un Schtroumpf Démarche d investigation
 TP Bleu comme un Schtroumpf Démarche d investigation Règles de sécurité Blouse, lunettes de protection, pas de lentilles de contact, cheveux longs attachés. Toutes les solutions aqueuses seront jetées
TP Bleu comme un Schtroumpf Démarche d investigation Règles de sécurité Blouse, lunettes de protection, pas de lentilles de contact, cheveux longs attachés. Toutes les solutions aqueuses seront jetées
LABORATOIRES DE CHIMIE Techniques de dosage
 LABORATOIRES DE CHIMIE Techniques de dosage Un dosage (ou titrage) a pour but de déterminer la concentration molaire d une espèce (molécule ou ion) en solution (généralement aqueuse). Un réactif de concentration
LABORATOIRES DE CHIMIE Techniques de dosage Un dosage (ou titrage) a pour but de déterminer la concentration molaire d une espèce (molécule ou ion) en solution (généralement aqueuse). Un réactif de concentration
Capteur à CO2 en solution
 Capteur à CO2 en solution Référence PS-2147CI Boîtier adaptateur Sonde ph Sonde température Sonde CO2 Page 1 sur 9 Introduction Cette sonde est conçue pour mesurer la concentration de CO 2 dans les solutions
Capteur à CO2 en solution Référence PS-2147CI Boîtier adaptateur Sonde ph Sonde température Sonde CO2 Page 1 sur 9 Introduction Cette sonde est conçue pour mesurer la concentration de CO 2 dans les solutions
Correction ex feuille Etoiles-Spectres.
 Correction ex feuille Etoiles-Spectres. Exercice n 1 1 )Signification UV et IR UV : Ultraviolet (λ < 400 nm) IR : Infrarouge (λ > 800 nm) 2 )Domaines des longueurs d onde UV : 10 nm < λ < 400 nm IR : 800
Correction ex feuille Etoiles-Spectres. Exercice n 1 1 )Signification UV et IR UV : Ultraviolet (λ < 400 nm) IR : Infrarouge (λ > 800 nm) 2 )Domaines des longueurs d onde UV : 10 nm < λ < 400 nm IR : 800
1) Teneur en amidon/glucose. a) (Z F) 0,9, b) (Z G) 0,9, où:
 L 248/8 Journal officiel de l Union européenne 17.9.2008 RÈGLEMENT (CE) N o 900/2008 DE LA COMMISSION du 16 septembre 2008 définissant les méthodes d analyse et autres dispositions de caractère technique
L 248/8 Journal officiel de l Union européenne 17.9.2008 RÈGLEMENT (CE) N o 900/2008 DE LA COMMISSION du 16 septembre 2008 définissant les méthodes d analyse et autres dispositions de caractère technique
M A N U E L D I N S T R U C T I O N S
 M A N U E L D I N S T R U C T I O N S FR RÈGLES GÉNÉRALES POUR L UTILISATION DE LA MACHINE SOMMAIRE Lire attentivement le manuel d instructions et les limitations de la garantie. La machine doit être branchée
M A N U E L D I N S T R U C T I O N S FR RÈGLES GÉNÉRALES POUR L UTILISATION DE LA MACHINE SOMMAIRE Lire attentivement le manuel d instructions et les limitations de la garantie. La machine doit être branchée
Janvier 2011 CHIMIE. Camille de BATTISTI. Acquérir la démarche expérimentale en chimie. ACADEMIE DE MONTPELLIER
 CHIMIE Camille de BATTISTI Janvier 2011 Acquérir la démarche expérimentale en chimie. ACADEMIE DE MONTPELLIER TABLE DES MATIERES Pages 1. LES OBJECTIFS VISÉS ET LE SOCLE COMMUN 2 1.1. Objectifs disciplinaires
CHIMIE Camille de BATTISTI Janvier 2011 Acquérir la démarche expérimentale en chimie. ACADEMIE DE MONTPELLIER TABLE DES MATIERES Pages 1. LES OBJECTIFS VISÉS ET LE SOCLE COMMUN 2 1.1. Objectifs disciplinaires
A B C Eau Eau savonneuse Eau + détergent
 1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
LE FILTRE A PARTICULES : SES PROBLEMATIQUES ET NOS SOLUTIONS
 LE FILTRE A PARTICULES : SES PROBLEMATIQUES ET NOS SOLUTIONS 1. NOTIONS DE BASE 2. CAUSES POSSIBLES DE DYSFONCTIONNEMENT 3. POURQUOI NETTOYER PLUTÔT QUE CHANGER? 4. METHODOLOGIE D APPLICATION FAP-NET (réf.
LE FILTRE A PARTICULES : SES PROBLEMATIQUES ET NOS SOLUTIONS 1. NOTIONS DE BASE 2. CAUSES POSSIBLES DE DYSFONCTIONNEMENT 3. POURQUOI NETTOYER PLUTÔT QUE CHANGER? 4. METHODOLOGIE D APPLICATION FAP-NET (réf.
Indicateur d'unité Voyant Marche/Arrêt
 Notice MESURACOLOR Colorimètre à DEL Réf. 22020 Indicateur d'unité Voyant Marche/Arrêt Indicateur Etalonnage Bouton Marche/Arrêt Indicateur de sélection de la longueur d'onde Indicateur de mode chronomètre
Notice MESURACOLOR Colorimètre à DEL Réf. 22020 Indicateur d'unité Voyant Marche/Arrêt Indicateur Etalonnage Bouton Marche/Arrêt Indicateur de sélection de la longueur d'onde Indicateur de mode chronomètre
Etudier le diagramme température-pression, en particulier le point triple de l azote.
 K4. Point triple de l azote I. BUT DE LA MANIPULATION Etudier le diagramme température-pression, en particulier le point triple de l azote. II. BASES THEORIQUES Etats de la matière La matière est constituée
K4. Point triple de l azote I. BUT DE LA MANIPULATION Etudier le diagramme température-pression, en particulier le point triple de l azote. II. BASES THEORIQUES Etats de la matière La matière est constituée
pka D UN INDICATEUR COLORE
 TP SPETROPHOTOMETRIE Lycée F.BUISSON PTSI pka D UN INDIATEUR OLORE ) Principes de la spectrophotométrie La spectrophotométrie est une technique d analyse qualitative et quantitative, de substances absorbant
TP SPETROPHOTOMETRIE Lycée F.BUISSON PTSI pka D UN INDIATEUR OLORE ) Principes de la spectrophotométrie La spectrophotométrie est une technique d analyse qualitative et quantitative, de substances absorbant
Mesure et détection de substances dangereuses : EX-OX-TOX (IS-013) Version CT-Q 2011-11-15
 Mesure et détection de substances dangereuses : EX-OX-TOX (IS-03) Version CT-Q 0--5 Groupe cible Collaborateurs qui doivent effectuer des mesures EX-OX-TOX sur un terrain d exploitation, les interpréter
Mesure et détection de substances dangereuses : EX-OX-TOX (IS-03) Version CT-Q 0--5 Groupe cible Collaborateurs qui doivent effectuer des mesures EX-OX-TOX sur un terrain d exploitation, les interpréter
Lecteur éditeur de chèques. i2200. Manuel utilisateur. Solutions de transactions et de paiement sécurisées
 Manuel utilisateur Lecteur éditeur de chèques i2200 Solutions de transactions et de paiement sécurisées Ingenico 2200 Avant Propos Merci d avoir choisi le Lecteur Editeur de chèque nouvelle génération
Manuel utilisateur Lecteur éditeur de chèques i2200 Solutions de transactions et de paiement sécurisées Ingenico 2200 Avant Propos Merci d avoir choisi le Lecteur Editeur de chèque nouvelle génération
Comprendre l Univers grâce aux messages de la lumière
 Seconde / P4 Comprendre l Univers grâce aux messages de la lumière 1/ EXPLORATION DE L UNIVERS Dans notre environnement quotidien, les dimensions, les distances sont à l échelle humaine : quelques mètres,
Seconde / P4 Comprendre l Univers grâce aux messages de la lumière 1/ EXPLORATION DE L UNIVERS Dans notre environnement quotidien, les dimensions, les distances sont à l échelle humaine : quelques mètres,
MANUEL DE L USAGER BRASSEUR À BEURRE D ÉRABLE CDL. Les Équipements d Érablière CDL inc.
 MANUEL DE L USAGER BRASSEUR À BEURRE D ÉRABLE CDL Merci d avoir choisi un brasseur à beurre d érable CDL. Nos 40 années d expérience au service des acériculteurs garantis que vous avez acquis un équipement
MANUEL DE L USAGER BRASSEUR À BEURRE D ÉRABLE CDL Merci d avoir choisi un brasseur à beurre d érable CDL. Nos 40 années d expérience au service des acériculteurs garantis que vous avez acquis un équipement
Fiche 19 La couleur des haricots verts et cuisson
 Fiche 19 La couleur des haricots verts et cuisson Objectif : Valider ou réfuter des «précisions culinaires»* permettant de "conserver une belle couleur verte" lors la cuisson des haricots verts frais (gousses
Fiche 19 La couleur des haricots verts et cuisson Objectif : Valider ou réfuter des «précisions culinaires»* permettant de "conserver une belle couleur verte" lors la cuisson des haricots verts frais (gousses
A. CARACTERISTIQUES TECHNIQUES.
 Page : 2 A. CARACTERISTIQUES TECHNIQUES. A.1. VUE D ENSEMBLE A.2. PRINCIPE DE FONCTIONNEMENT!" #! $! %&' ( ) * µ +, µ $# (& % ± -. /01)0$ ' &%(% 2 3,)/4 $ A.3. CARACTERISTIQUES MECANIQUES. PARAMETRES Valeur
Page : 2 A. CARACTERISTIQUES TECHNIQUES. A.1. VUE D ENSEMBLE A.2. PRINCIPE DE FONCTIONNEMENT!" #! $! %&' ( ) * µ +, µ $# (& % ± -. /01)0$ ' &%(% 2 3,)/4 $ A.3. CARACTERISTIQUES MECANIQUES. PARAMETRES Valeur
SCIENCES PHYSIQUES. Durée : 3 heures. L usage d une calculatrice est interdit pour cette épreuve. CHIMIE
 Banque «Agro-Véto» Technologie et Biologie AT - 0310 SCIECES PYSIQUES Durée : 3 heures L usage d une calculatrice est interdit pour cette épreuve. Si, au cours de l épreuve, un candidat repère ce qui lui
Banque «Agro-Véto» Technologie et Biologie AT - 0310 SCIECES PYSIQUES Durée : 3 heures L usage d une calculatrice est interdit pour cette épreuve. Si, au cours de l épreuve, un candidat repère ce qui lui
SVE 222 & PCL-442. Fascicule de Travaux Pratiques
 SVE 222 & PCL-442 Fascicule de Travaux Pratiques 2014-2015 Institut Supérieur de l Education et de la Formation Continue Bassem Jamoussi & Radhouane Chakroun 1 Sommaire PCL 442/SVE222 - TP N 1 : Etude
SVE 222 & PCL-442 Fascicule de Travaux Pratiques 2014-2015 Institut Supérieur de l Education et de la Formation Continue Bassem Jamoussi & Radhouane Chakroun 1 Sommaire PCL 442/SVE222 - TP N 1 : Etude
MEDIACLAVE. La stérilisation rapide, reproductible et sûre des milieux
 MEDIACLAVE La stérilisation rapide, reproductible et sûre des milieux MEDIACLAVE La stérilisation rapide, reproductible et sûre des milieux Les milieux de culture bactérienne sont très largement utilisé,
MEDIACLAVE La stérilisation rapide, reproductible et sûre des milieux MEDIACLAVE La stérilisation rapide, reproductible et sûre des milieux Les milieux de culture bactérienne sont très largement utilisé,
TPG 12 - Spectrophotométrie
 TPG 12 - Spectrophotométrie Travail par binôme Objectif : découvrir les conditions de validité et les utilisations possibles de la loi de Beer-Lambert I- Tracé de la rosace des couleurs Choisir un des
TPG 12 - Spectrophotométrie Travail par binôme Objectif : découvrir les conditions de validité et les utilisations possibles de la loi de Beer-Lambert I- Tracé de la rosace des couleurs Choisir un des
4. Conditionnement et conservation de l échantillon
 1. Objet S-II-3V1 DOSAGE DU MERCURE DANS LES EXTRAITS D EAU RÉGALE Description du dosage du mercure par spectrométrie d absorption atomique de vapeur froide ou par spectrométrie de fluorescence atomique
1. Objet S-II-3V1 DOSAGE DU MERCURE DANS LES EXTRAITS D EAU RÉGALE Description du dosage du mercure par spectrométrie d absorption atomique de vapeur froide ou par spectrométrie de fluorescence atomique
GUIDE D INSTRUCTION. Montage Entretien
 GUIDE D INSTRUCTION Montage Entretien INSTRUCTIONS PARTICULIÈRES Dès réception des marchandises, veuillez vérifier le bon état de l'emballage. Veuillez mentionner tout dégât éventuel de transport sur le
GUIDE D INSTRUCTION Montage Entretien INSTRUCTIONS PARTICULIÈRES Dès réception des marchandises, veuillez vérifier le bon état de l'emballage. Veuillez mentionner tout dégât éventuel de transport sur le
Objectifs pédagogiques : spectrophotomètre Décrire les procédures d entretien d un spectrophotomètre Savoir changer l ampoule d un
 CHAPITRE 6 : LE SPECTROPHOTOMETRE Objectifs pédagogiques : Citer les principaux éléments d un dun spectrophotomètre Décrire les procédures d entretien d un spectrophotomètre p Savoir changer l ampoule
CHAPITRE 6 : LE SPECTROPHOTOMETRE Objectifs pédagogiques : Citer les principaux éléments d un dun spectrophotomètre Décrire les procédures d entretien d un spectrophotomètre p Savoir changer l ampoule
Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu.
 Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu. Auteur : Dr. Wulfran FORTIN Professeur Agrégé de Sciences Physiques TZR -
Mesure du volume d'un gaz, à pression atmosphérique, en fonction de la température. Détermination expérimentale du zéro absolu. Auteur : Dr. Wulfran FORTIN Professeur Agrégé de Sciences Physiques TZR -
Exemples d utilisation de G2D à l oral de Centrale
 Exemples d utilisation de G2D à l oral de Centrale 1 Table des matières Page 1 : Binaire liquide-vapeur isotherme et isobare Page 2 : Page 3 : Page 4 : Page 5 : Page 6 : intéressant facile facile sauf
Exemples d utilisation de G2D à l oral de Centrale 1 Table des matières Page 1 : Binaire liquide-vapeur isotherme et isobare Page 2 : Page 3 : Page 4 : Page 5 : Page 6 : intéressant facile facile sauf
AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE
 AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE CONCOURS EXTERNE Session 2005 TRAVAUX PRATIQUES DE BIOCHIMIE PHYSIOLOGIE ALCOOL ET FOIE L éthanol, psychotrope puissant, est absorbé passivement dans l intestin
AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE CONCOURS EXTERNE Session 2005 TRAVAUX PRATIQUES DE BIOCHIMIE PHYSIOLOGIE ALCOOL ET FOIE L éthanol, psychotrope puissant, est absorbé passivement dans l intestin
2 e partie de la composante majeure (8 points) Les questions prennent appui sur six documents A, B, C, D, E, F (voir pages suivantes).
 SUJET DE CONCOURS Sujet Exploitation d une documentation scientifique sur le thème de l énergie 2 e partie de la composante majeure (8 points) Les questions prennent appui sur six documents A, B, C, D,
SUJET DE CONCOURS Sujet Exploitation d une documentation scientifique sur le thème de l énergie 2 e partie de la composante majeure (8 points) Les questions prennent appui sur six documents A, B, C, D,
Test d immunofluorescence (IF)
 Test d immunofluorescence (IF) 1.1 Prélèvement du cerveau et échantillonnage Avant toute manipulation, il est fondamental de s assurer que tout le personnel en contact avec un échantillon suspect soit
Test d immunofluorescence (IF) 1.1 Prélèvement du cerveau et échantillonnage Avant toute manipulation, il est fondamental de s assurer que tout le personnel en contact avec un échantillon suspect soit
Cafetière. Mode d Emploi. 1Notice cafetière v1.0
 Cafetière Mode d Emploi 1Notice cafetière v1.0 SOMMAIRE 1 CONSIGNES DE SÉCURITÉ... 3 2INSTALLATION DE L APPAREIL EN TOUTE SÉCURITÉ...4 3PRECAUTION CONCERNANT L UTILISATION DE L APPAREIL...5 4DESCRIPTION
Cafetière Mode d Emploi 1Notice cafetière v1.0 SOMMAIRE 1 CONSIGNES DE SÉCURITÉ... 3 2INSTALLATION DE L APPAREIL EN TOUTE SÉCURITÉ...4 3PRECAUTION CONCERNANT L UTILISATION DE L APPAREIL...5 4DESCRIPTION
ATTENTION! Après quelques mois d utilisation, un ordinateur s encrasse et surtout son ennemi mortel est la poussière.
 Après quelques mois d utilisation, un ordinateur s encrasse et surtout son ennemi mortel est la poussière. En effet, l ordinateur est un appareil qui consomme de l électricité dont une partie importante
Après quelques mois d utilisation, un ordinateur s encrasse et surtout son ennemi mortel est la poussière. En effet, l ordinateur est un appareil qui consomme de l électricité dont une partie importante
Masse volumique et densité relative à 20 C
 Méthode OIV-MA-AS2-01A Méthodes Type I Masse volumique et densité relative à 20 C 1. Définition La masse volumique est le quotient de la masse d'un certain volume de vin ou de moût à 20 C par ce volume.
Méthode OIV-MA-AS2-01A Méthodes Type I Masse volumique et densité relative à 20 C 1. Définition La masse volumique est le quotient de la masse d'un certain volume de vin ou de moût à 20 C par ce volume.
NOTICE TECHNIQUE D INSTALLATION & D UTILISATION
 NOTICE TECHNIQUE D INSTALLATION & D UTILISATION Plafond filtrant Lumispace Il est important de lire attentivement cette notice avant la maintenance du plafond Lumispace Ce document doit être remis au client
NOTICE TECHNIQUE D INSTALLATION & D UTILISATION Plafond filtrant Lumispace Il est important de lire attentivement cette notice avant la maintenance du plafond Lumispace Ce document doit être remis au client
Terrace Entretien. Entretien gønøral. Nettoyage aprłs installation. RØsistance chimique. Guide de taches. Remplacement d une planche
 Terrace Entretien Entretien gønøral Nettoyage aprłs installation RØsistance chimique Guide de taches Remplacement d une planche Terrasses AmØnagement extørieur www.deceuninck.be www.deceuninck.nl 08/2013
Terrace Entretien Entretien gønøral Nettoyage aprłs installation RØsistance chimique Guide de taches Remplacement d une planche Terrasses AmØnagement extørieur www.deceuninck.be www.deceuninck.nl 08/2013
NOTICE D INSTALLATION
 BALLON THERMODYNAMIQUE MONOBLOC EAU CHAUDE SANITAIRE NOTICE D INSTALLATION Lisez attentivement la notice d installation avant le montage de l appareil www.airtradecentre.com SOMMAIRE A. REMARQUES IMPORTANTES...
BALLON THERMODYNAMIQUE MONOBLOC EAU CHAUDE SANITAIRE NOTICE D INSTALLATION Lisez attentivement la notice d installation avant le montage de l appareil www.airtradecentre.com SOMMAIRE A. REMARQUES IMPORTANTES...
Marquage laser des métaux
 62 Colorer Marquage laser des métaux TherMark Produit à base aqueuse pour un nettoyage rapide. Appliquer une fine couche de produit sur le métal, laisser sécher moins de 2 minutes et graver au laser. L
62 Colorer Marquage laser des métaux TherMark Produit à base aqueuse pour un nettoyage rapide. Appliquer une fine couche de produit sur le métal, laisser sécher moins de 2 minutes et graver au laser. L
Unitecnic 2200 Unitecnic 2200 CS
 Unitecnic Unitecnic S Notice de pose Seules les vis rouges et bleues peuvent être dévissées. (changement de combinaison et de main) Tout autre démontage interne est interdit. (annulation de la garantie)
Unitecnic Unitecnic S Notice de pose Seules les vis rouges et bleues peuvent être dévissées. (changement de combinaison et de main) Tout autre démontage interne est interdit. (annulation de la garantie)
1S9 Balances des blancs
 FICHE 1 Fiche à destination des enseignants 1S9 Balances des blancs Type d'activité Étude documentaire Notions et contenus Compétences attendues Couleurs des corps chauffés. Loi de Wien. Synthèse additive.
FICHE 1 Fiche à destination des enseignants 1S9 Balances des blancs Type d'activité Étude documentaire Notions et contenus Compétences attendues Couleurs des corps chauffés. Loi de Wien. Synthèse additive.
Unitecnic 2210 Unitecnic 2210 CS
 Unitecnic Unitecnic S Notice de pose Adaptation de la main (sens de la porte) Par défaut, la serrure est configurée en main gauche (vue de l extérieur la serrure est à gauche sur la porte). Seules les
Unitecnic Unitecnic S Notice de pose Adaptation de la main (sens de la porte) Par défaut, la serrure est configurée en main gauche (vue de l extérieur la serrure est à gauche sur la porte). Seules les
TP 2: LES SPECTRES, MESSAGES DE LA LUMIERE
 TP 2: LES SPECTRES, MESSAGES DE LA LUMIERE OBJECTIFS : - Distinguer un spectre d émission d un spectre d absorption. - Reconnaître et interpréter un spectre d émission d origine thermique - Savoir qu un
TP 2: LES SPECTRES, MESSAGES DE LA LUMIERE OBJECTIFS : - Distinguer un spectre d émission d un spectre d absorption. - Reconnaître et interpréter un spectre d émission d origine thermique - Savoir qu un
Chapitre 7 Les solutions colorées
 Chapitre 7 Les solutions colorées Manuel pages 114 à 127 Choix pédagogiques. Ce chapitre a pour objectif d illustrer les points suivants du programme : - dosage de solutions colorées par étalonnage ; -
Chapitre 7 Les solutions colorées Manuel pages 114 à 127 Choix pédagogiques. Ce chapitre a pour objectif d illustrer les points suivants du programme : - dosage de solutions colorées par étalonnage ; -
Manuel d entretien. Présentation de votre chauffe-eau. Poignées de préhension (haut et bas) Protection intérieure par émaillage. Isolation thermique
 Présentation de votre chauffe-eau Poignées de préhension (haut et bas) Isolation thermique Protection intérieure par émaillage Canne de prise d eau chaude Doigt de gant du thermostat Anode magnésium Résistance
Présentation de votre chauffe-eau Poignées de préhension (haut et bas) Isolation thermique Protection intérieure par émaillage Canne de prise d eau chaude Doigt de gant du thermostat Anode magnésium Résistance
Calcaire ou eau agressive en AEP : comment y remédier?
 Calcaire ou eau agressive en AEP : comment y remédier? Les solutions techniques Principes et critères de choix Par Sébastien LIBOZ - Hydrogéologue Calcaire ou eau agressive en AEP : comment y remédier?
Calcaire ou eau agressive en AEP : comment y remédier? Les solutions techniques Principes et critères de choix Par Sébastien LIBOZ - Hydrogéologue Calcaire ou eau agressive en AEP : comment y remédier?
COMPOSANTS DE LA MACHINE
 FR COMPOSANTS DE LA MACHINE Voyant vapeur prête Interrupteur vapeur Interrupteur de distribution de café Voyant café prêt Couvercle du réservoir à eau Figure A Bouton de distribution vapeur et eau chaude
FR COMPOSANTS DE LA MACHINE Voyant vapeur prête Interrupteur vapeur Interrupteur de distribution de café Voyant café prêt Couvercle du réservoir à eau Figure A Bouton de distribution vapeur et eau chaude
STEAMY MINI. Nous vous félicitons pour l acquisition de l appareil «STEAMY - MINI», un appareil de grande qualité.
 REITEL Feinwerktechnik GmbH Senfdamm 20 D 49152 Bad Essen Allemagne Tel. (++49) 5472/94 32-0 Fax: (++49) 5472/9432-40 Mode d emploi STEAMY MINI Cher client, Nous vous félicitons pour l acquisition de l
REITEL Feinwerktechnik GmbH Senfdamm 20 D 49152 Bad Essen Allemagne Tel. (++49) 5472/94 32-0 Fax: (++49) 5472/9432-40 Mode d emploi STEAMY MINI Cher client, Nous vous félicitons pour l acquisition de l
Eau chaude sanitaire FICHE TECHNIQUE
 FICHE TECHNIQUE Eau chaude sanitaire 2 5 6 6 CONNAÎTRE > Les besoins d eau chaude sanitaire > Les modes de production > La qualité de l eau > Les réseaux de distribution > La température de l eau REGARDER
FICHE TECHNIQUE Eau chaude sanitaire 2 5 6 6 CONNAÎTRE > Les besoins d eau chaude sanitaire > Les modes de production > La qualité de l eau > Les réseaux de distribution > La température de l eau REGARDER
eedd LA PLANETE N EST PAS UNE POUBELLE 1/7
 eedd LA PLANETE N EST PAS UNE POUBELLE 1/7 I- ETUDE D UNE PHOTOGRAPHIE DE YANN ARTHUS-BERTRAND : Stockage d ordures dans la périphérie de Saint-Domingue en République dominicaine au cœur des Caraïbes Légende
eedd LA PLANETE N EST PAS UNE POUBELLE 1/7 I- ETUDE D UNE PHOTOGRAPHIE DE YANN ARTHUS-BERTRAND : Stockage d ordures dans la périphérie de Saint-Domingue en République dominicaine au cœur des Caraïbes Légende
A QUOI SERT LE NIVEAU DE CUVE?
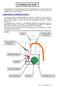 LE NIVEAU DE CUVE Les explications et les schémas qui suivent correspondent à ce que j ai compris du fonctionnement du carburateur MIKUNI qui équipe les BETA trial. Elles sont aussi valables pour les autres
LE NIVEAU DE CUVE Les explications et les schémas qui suivent correspondent à ce que j ai compris du fonctionnement du carburateur MIKUNI qui équipe les BETA trial. Elles sont aussi valables pour les autres
Mario Geiger octobre 08 ÉVAPORATION SOUS VIDE
 ÉVAPORATION SOUS VIDE 1 I SOMMAIRE I Sommaire... 2 II Évaporation sous vide... 3 III Description de l installation... 5 IV Travail pratique... 6 But du travail... 6 Principe... 6 Matériel... 6 Méthodes...
ÉVAPORATION SOUS VIDE 1 I SOMMAIRE I Sommaire... 2 II Évaporation sous vide... 3 III Description de l installation... 5 IV Travail pratique... 6 But du travail... 6 Principe... 6 Matériel... 6 Méthodes...
Application à l astrophysique ACTIVITE
 Application à l astrophysique Seconde ACTIVITE I ) But : Le but de l activité est de donner quelques exemples d'utilisations pratiques de l analyse spectrale permettant de connaître un peu mieux les étoiles.
Application à l astrophysique Seconde ACTIVITE I ) But : Le but de l activité est de donner quelques exemples d'utilisations pratiques de l analyse spectrale permettant de connaître un peu mieux les étoiles.
2 Trucs et Astuces 2
 Trucs et Astuces 2 2 Le chauffe-eau solaire 1.Les capteurs 2.Les circuits solaires 3.Le circuit sanitaire 4.Les systèmes d appoint 5.Fiches synthèse 6.Bon à savoir Trucs et Astuces 3 1 Les capteurs Trucs
Trucs et Astuces 2 2 Le chauffe-eau solaire 1.Les capteurs 2.Les circuits solaires 3.Le circuit sanitaire 4.Les systèmes d appoint 5.Fiches synthèse 6.Bon à savoir Trucs et Astuces 3 1 Les capteurs Trucs
Site : http://www.isnab.com mail : [email protected] SUJET ES - session 2003 Page 1 68-(7(6VHVVLRQ
 Site : http://www.isnab.com mail : [email protected] SUJET ES - session 003 Page 1 68-(7(6VHVVLRQ LE JUS E FRUIT 35(0,Ê5(3$57,(%LRFKLPLHSRLQWV L'analyse d'un jus de fruit révèle la présence d'un composé
Site : http://www.isnab.com mail : [email protected] SUJET ES - session 003 Page 1 68-(7(6VHVVLRQ LE JUS E FRUIT 35(0,Ê5(3$57,(%LRFKLPLHSRLQWV L'analyse d'un jus de fruit révèle la présence d'un composé
Portier Vidéo Surveillance
 Portier Vidéo Surveillance 1 Réf. 102212 Notice d installation et d utilisation INTRODUCTION : Ce vidéophone est un appareil qui associe un interphone et un système vidéo d une grande facilité d installation
Portier Vidéo Surveillance 1 Réf. 102212 Notice d installation et d utilisation INTRODUCTION : Ce vidéophone est un appareil qui associe un interphone et un système vidéo d une grande facilité d installation
Traitement de l eau par flux dynamique
 GmbH Traitement de l eau par flux dynamique afin de réduire les impuretés microbiologiques afin d empêcher l apparition de nouveaux germes dans les eaux de consommation et de process et Nouveau avec certificat
GmbH Traitement de l eau par flux dynamique afin de réduire les impuretés microbiologiques afin d empêcher l apparition de nouveaux germes dans les eaux de consommation et de process et Nouveau avec certificat
101 Adoptée : 12 mai 1981
 LIGNE DIRECTRICE DE L OCDE POUR LES ESSAIS DE PRODUITS CHIMIQUES 101 Adoptée : 12 mai 1981 «Spectres d'absorption UV-VIS» (Méthode spectrophotométrique) 1. I N T R O D U C T I O N I n f o r m a t i o n
LIGNE DIRECTRICE DE L OCDE POUR LES ESSAIS DE PRODUITS CHIMIQUES 101 Adoptée : 12 mai 1981 «Spectres d'absorption UV-VIS» (Méthode spectrophotométrique) 1. I N T R O D U C T I O N I n f o r m a t i o n
FICHE DE DONNEES DE SECURITE
 PAGE 1/7 DATE DE MISE A JOUR : 16/11/2011 1/ - IDENTIFICATION DU PRODUIT ET DE LA SOCIETE Identification du produit : Gaines, films, housses, et/ou sacs transparents et colorés en polyéthylène. Famille
PAGE 1/7 DATE DE MISE A JOUR : 16/11/2011 1/ - IDENTIFICATION DU PRODUIT ET DE LA SOCIETE Identification du produit : Gaines, films, housses, et/ou sacs transparents et colorés en polyéthylène. Famille
DOMAİNES D USAGE DOMAINES D USAGE INDUSTRIEL
 DOMAİNES D USAGE Dans le but d observer le rendement à l instant même de notre appareil magnétique à stopper la calcification, montez le, s il vous plait, sur un congélateur. Les blocs de glace obtenus
DOMAİNES D USAGE Dans le but d observer le rendement à l instant même de notre appareil magnétique à stopper la calcification, montez le, s il vous plait, sur un congélateur. Les blocs de glace obtenus
AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS
 AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS CONCOURS EXTERNE ÉPREUVES D ADMISSION session 2010 TRAVAUX PRATIQUES DE CONTRE-OPTION DU SECTEUR A CANDIDATS DES SECTEURS B ET C
AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS CONCOURS EXTERNE ÉPREUVES D ADMISSION session 2010 TRAVAUX PRATIQUES DE CONTRE-OPTION DU SECTEUR A CANDIDATS DES SECTEURS B ET C
NOTICE D UTILISATION. Masque de soudage protecteur de vision
 NOTICE D UTILISATION Masque de soudage protecteur de vision Attention : Lire attentivement le présent manuel dans son intégralité avant d utiliser le masque de soudage. Table des matières GUIDE DE L UTILISATEUR
NOTICE D UTILISATION Masque de soudage protecteur de vision Attention : Lire attentivement le présent manuel dans son intégralité avant d utiliser le masque de soudage. Table des matières GUIDE DE L UTILISATEUR
INSTRUCTIONS D INSTALLATION MODÈLE 300521
 INSTRUCTIONS D INSTALLATION MODÈLE 300521 WWW.BURCAM.COM 2190 Boul. Dagenais Ouest LAVAL (QUEBEC) CANADA H7L 5X9 TÉL: 514.337.4415 FAX: 514.337.4029 [email protected] Votre pompe a été soigneusement emballée
INSTRUCTIONS D INSTALLATION MODÈLE 300521 WWW.BURCAM.COM 2190 Boul. Dagenais Ouest LAVAL (QUEBEC) CANADA H7L 5X9 TÉL: 514.337.4415 FAX: 514.337.4029 [email protected] Votre pompe a été soigneusement emballée
Montage- und Gebrauchsanweisung Instructions on mounting and use Prescriptions de montage et mode d'emploi Montage- en gebruiksaanwijzing Istruzioni
 Montage- und Gebrauchsanweisung Instructions on mounting and use Prescriptions de montage et mode d'emploi Montage- en gebruiksaanwijzing Istruzioni di montaggio e d'uso Instrucciones de montaje y para
Montage- und Gebrauchsanweisung Instructions on mounting and use Prescriptions de montage et mode d'emploi Montage- en gebruiksaanwijzing Istruzioni di montaggio e d'uso Instrucciones de montaje y para
Séquence 9. Étudiez le chapitre 11 de physique des «Notions fondamentales» : Physique : Dispersion de la lumière
 Séquence 9 Consignes de travail Étudiez le chapitre 11 de physique des «Notions fondamentales» : Physique : Dispersion de la lumière Travaillez les cours d application de physique. Travaillez les exercices
Séquence 9 Consignes de travail Étudiez le chapitre 11 de physique des «Notions fondamentales» : Physique : Dispersion de la lumière Travaillez les cours d application de physique. Travaillez les exercices
