SYNTHESE ET DOSAGE DE L ACIDE DICHLOROCYANURIQUE :
|
|
|
- Guillaume Guérin
- il y a 9 ans
- Total affichages :
Transcription
1 SYNTHESE ET DOSAGE DE L ACIDE DICHLOROCYANURIQUE : Le Décret n du 7 avril 1981 donne, dans son article premier, la définition d une piscine : «Etablissement ou une partie d établissement qui comporte un ou plusieurs bassins artificiels utilisés pour les activités de bain ou de natation». Dans ces établissements, les eaux sont régénérées en circuit fermé, c est-à-dire que l eau, polluée progressivement par les baigneurs dans le bassin, y est réintroduite après traitement approprié. La section 2 du décret décrit les dispositions particulières aux piscines et prévoit que l eau des bassins doit être filtrée, désinfectée et désinfectante, ce qui implique un résiduel de chlore en permanence. L acide dichlorocyanurique (ou acide dichloroisocyanurique, symbolisé par ADCC) est un composé utilisé dans le traitement des eaux de piscine. Son nom en nomenclature officielle est le 1,3-dichloro-1,3,5-triazinane-2,4,6-trione. Il appartient à la famille des chlorocyanurique : résistants au stockage, à la lumière, peu toxiques, ils sont utilisés sous forme de poudre, pour le traitement des eaux de piscine. En effet, en milieu acide, sous l action de l eau, ces derniers libèrent de d acide hypochloreux (HClO) et remplacent avantageusement l eau de Javel. I. SYNTHESE DE L ACIDE DICHLOROCYANURIQUE : L ADCC s obtient par chloration de l acide cyanurique (AC) : Lorsqu on traite l AC par des quantités équimolaires d hypochlorite et d acide chlorhydrique, on obtient l ADCC suivant l équation de la réaction ci-dessous. Schéma I : (ClO - + HCl) AC ADCC L ajout d hypochlorite et d acide chlorhydrique dans des quantités équimolaires permet de former un intermédiaire réactionnel, l acide hypochloreux HClO, conduisant à la formation de l ADCC. L objectif de cette partie est de synthétiser l acide dichlorocyanurique à partir de l acide chlorocyanurique. La réaction doit se faire dans les limites strictes de ph : tout au long de la synthèse le ph doit rester dans l intervalle suivant : 2,8 < ph < 3,5. - En effet, en milieu plus acide (ph < 2,5), il y a formation de dichlore gazeux toxique Cl 2 (g). - A ph > 3,5, la réaction se fait plus difficilement et conduit à la formation de sous-produits. Burette de 25 cm 3 Solution d acide chlorhydrique HCl Solution d acide cyanurique (AC) Burette de 50 cm 3 Solution d hypochlorite de calcium Ca(ClO) 2 Bain de glace pilée 3.2 ph mètre 1 Pour ces raisons, il est indispensable de contrôler en permanence le ph à l aide d un ph-mètre. Etalonner le ph-mètre à l aide des solutions tampon 4 et 7 fournies et en suivant les instructions de la notice (régler la température pour une mesure au ph-mètre à 9 C, température du milieu réactionnel par la suite). Mode opératoire : à suivre de manière attentive pour les raisons citées précédemment. le port de la blouse et des lunettes est obligatoire durant toute la synthèse. Mettre en place deux burettes graduées comportant respectivement : - Burette de 25 ml : une solution d acide chlorhydrique à une concentration de 5,5 mol.l -1 - Burette de 50 ml : une solution d hypochlorite de calcium à 2 mol.l -1 en ions hypochlorite.
2 Sur l agitateur magnétique, placer un cristallisoir contenant de la glace pilée. Dans le bécher de 250 cm 3 introduire environ 45 ml d eau distillée et, tout en agitant, y ajouter exactement 5,0 g d acide cyanurique pesée à la balance. Rincer la coupelle de pesée à l aide de 15 ml d eau distillée. Délicatement, placer l électrode de ph-métrie en veillant bien à ce qu elle ne heurte pas le barreau aimanté. Agiter énergiquement, mesurer le ph. Réalisation de la synthèse : Le port d un masque est conseillé pour cette partie. Suivre scrupuleusement les instructions, en particulier au début de la manipulation. Lire attentivement l ensemble des opérations ci-dessous avant de débuter la manipulation. Tout au long de la manipulation, il est nécessaire de veiller à ce que l agitation soit efficace et la plus homogène possible. - Faire couler 1 goutte de la solution d hypochlorite de calcium : le ph croit ; compenser par une goutte d acide chlorhydrique afin de rester dans l intervalle 2,8 < ph < Etablir un débit constant lent au goutte à goutte en hypochlorite de calcium ( 1 à 2 gouttes par seconde) : le ph du milieu augmente. - Rectifier le ph par ajout d une à deux gouttes d acide chlorhydrique en veillant bien à ne pas descendre en dessous d un ph = 2,8 ; le but étant de rester à une valeur du ph proche de 3.5 en évitant cependant de passer au-dessus de cette valeur. - Si la zone basse de ph = 2,8 est atteinte, l ajout d acide doit être stoppé pour être repris lorsque le ph dépasse 3,5. Poursuivre ainsi jusqu à l addition d un volume de 36,5 ml de solution d hypochlorite de calcium. L ensemble de la manipulation doit durer environ 30 minutes. Après avoir vidé les 36.5 ml d hypochlorite de calcium, maintenir l agitation encore 15 minutes. Filtration sous pression réduite : Après les 15 min d agitation, réaliser la filtration sur verre fritté en versant avec précaution le contenu du bécher dans le filtre. Casser le vide, rincer le bécher avec 10 ml d eau distillée et essorer à nouveau en écrasant le solide sur la plaque fritée. Laver les cristaux avec 10 ml d eau supplémentaire et reprendre l essorage pendant 10 min environ afin de sécher au maximum les cristaux. Séchage : A l aide d une spatule, transférer tout le contenu du verre frité dans une coupelle en porcelaine préalablement pesée (noter la masse de votre coupelle). En veillant à ce que les cristaux soient bien étalés en couches minces dans la coupelle en porcelaine, placer celleci à l étuve ( C) durant 1 heure. Au bout d une heure, laisser refroidir et peser afin de déterminer la masse m exp d acide dichlorocyanurique obtenue par synthèse. Durant le séchage à l étude, réaliser la partie II) avant de revenir à la caractérisation ci-dessous. Caractérisation de l acide dichlorocyanurique : La fusion de l acide dichlorocyanurique ( C) se fait avec une décomposition simultanée de l acide ; ainsi, son identification par la détermination de son point de fusion n est pas un procédé fiable. On réalisera ici deux tests qualitatifs ci-après: 2
3 Test 1 : Dans deux tubes à essais, introduire 1 ml d acide acétique commercial. Ajouter dans chacun des deux tubes, 1 goutte d hélianthine (indicateur coloré acido-basique). Ajouter, respectivement dans chacun des tubes, une pointe de spatule : - D acide cyanurique (AC) commercial. - D acide dichlorocyanurique (ADCC) préparé, après l avoir écrasé en poudre très fine. Noter le résultat. Test 2 : Dans trois nouveaux tubes à essais, introduire 1 ml d acide acétique commercial. Ajouter, respectivement dans chacun des tubes, une pointe de spatule - D acide cyanurique (AC) commercial. - D acide dichlorocyanurique préparé lors de la synthèse (ADDC) et après l avoir écrasé en poudre très fine. - De dichlorocyanurate de sodium de référence (DCCNa) (produit industriel fourni, sel de l acide dichlorocyanurique). Dans chacun des trois tubes, ajouter environ 2 ml d une solution réductrice d iodure de potassium molaire. Noter le résultat. II. DOSAGE DU DICHLOROISOCYANURATE DE SODIUM : Il existe aujourd hui de nombreux produits commerciaux contenant du dichloroisocyanurate de sodium (DCCNa). Utilisé pour traité les eaux de piscines, il est aussi très rependu dans la composition de produits de nettoyage ménager et industriel. Le dosage réalisé ici sera effectué sur un produit se présentant sous forme de pastilles, dont l étiquette figure ci-dessous. Le but est de déterminer la teneur en DCCNa (sel de l ADCC) des pastilles. Le dosage repose sur la propriété du DCCNa d être décomposé par hydrolyse faiblement acide avec libération d acide hypochloreux selon le schéma suivant : (schéma II) Etiquette : 64 % (m/m) de dichloroisocyanurate de sodium dihydraté soit 35% de chlore actif. 1 pastille de 20 g dans 60 ml d eau donne 2,5% de chlore actif ( ) L acide hypochloreux formé HClO est alors dosé par iodométrie (réaction d oxydoréduction) classique L échantillon dosé est une masse m connue de pastilles. Afin de réaliser deux dosages (un premier dit «grossier» puis un second «précis») il est nécessaire de préparer 2 erlenmeyers comme indiqué ci-après : Peser dans une capsule une masse m = 0,20 g de pastilles commerciales. Transvaser le contenu de la capsule dans un erlenmeyer en rinçant bien à l eau distillée au dessus de l erlenmeyer. 3
4 Ajouter : - 20 ml environ d une solution molaire d iodure de potassium KI ml environ d acide acétique commercial. Boucher l erlenmeyer à l aide d un para-film et placer sous agitation durant 15 minutes. Au moment de réaliser le titrage, ajouter une pointe de spatule de thiodène. Titrer par une solution de thiosulfate de sodium Na 2 S 2 O 3 à 0,200 mol.l -1 jusqu à décoloration complète de la solution. Soit V E le volume versé pour atteindre l équivalence du dosage précis. III. QUESTIONS : Données : Acide cyanurique : (AC) Acide dichloroisocyanurique : (ADCC) Dichloroisocyanurate de sodium : (DCCNa) Aspect : Solide blanc Solide blanc chlorée Solide blanc chlorée odeur - Chlorée Chlorée Masse molaire (g.mol -1 ) Solubilité (g.l -1 ) , pka de quelques couples acide/base : HClO/ ClO - pka = 7,53 Couples de l eau : H 3 O + /H 2 O pk a = 0 et H 2 O/OH - pka = 14 Zone de virage et couleur Hélianthine : 3,1 < ph < 4,4 rouge / orange / jaune A propos de la synthèse : 1) Donner le nom de HClO et de ClO -. 2) HClO est un acide et ClO - est une base. a) Définir un acide et une base au sens de Bronsted et Lowry. b) Ecrire l équation de la réaction acidobasique entre HClO et l eau. c) Exprimer la constante d acidité du couple HClO/ ClO - c est-à-dire la constante de la réaction entre l acide et l eau pour former la base conjuguée. d) D après les documents fournis, déterminer la valeur de la constante d acidité. e) Calculer la valeur du rapport [HClO]/[ClO - ] à ph = 3. f) Justifier qu au cours de la synthèse, on se place à ce ph par ajout d acide chlorhydrique. 3) Rendement de la synthèse : a) Ecrire l équation de la réaction de formation de l acide dichlorocyanurique (ADCC) à partir de l acide cyanurique (AC) (schéma I), avec les coefficients stœchiométriques correctement ajustés. b) Calculer les quantités de matière initiale des réactifs mis en jeu en acide cyanurique (AC) et en acide hypochloreux HClO (formé in-situ à partir des ions hypochlorite) lors de cette réaction. c) En déduire la masse théorique d acide dichlorocyanurique (ADCC) formé en considérant la réaction totale. d) A partir de la masse obtenue expérimentalement, déterminer le rendement η de la synthèse réalisée. 4) En cas d addition trop importante d acide chlorhydrique au cours de la synthèse, en présence d acide hypochloreux, on constate la formation de dichlore Cl 2. Donner l équation de la réaction correspondante. 4
5 5) Caractérisation, test 1: D après les résultats obtenus lors du test 1, observer ce qu il se passe. Quel pouvoir à l ADCC en milieu acide? 6) Caractérisation, test 2 : a) Définir un oxydant et un réducteur en chimie. b) Les espèces I - et I 2 forment un couple oxydant/réducteur : écrire la demi-équation électronique (d échange d électrons) entre l oxydant et le réducteur du couple que forment les espèces I et I 2. c) Préciser le nom de chaque espèce, identifier l oxydant et le réducteur et écrire le couple ox/red pour ces espèces I et I 2. d) Comparer les propriétés oxydantes et/ou réductrices des espèces AC et ADCC mises en jeu lors de ce test. A propos du dosage en retour : Lors de la mise en solution en milieu acide de la poudre du produit commercial, il se produit (entre autres) une réaction d hydrolyse de la DCCNa avec formation d acide hypochloreux. L acide hypochloreux HClO formé est alors titré suivant un dosage dit «en retour» : cela consiste à faire réagir un excès de réducteur KI sur cet oxydant, puis de doser le produit ainsi formé lors de la première réaction par une solution titrante de thiosulfate de sodium. Couples oxydant / réducteur : HClO / Cl - I 2 / I - S 4 O / S 2 O 3 2-7) Ecrire l équation de la réaction d hydrolyse du DCCNa avec formation d HClO, en ajustant correctement les nombres stœchiométriques (schéma II) 8) Réaction (1) du dosage : a) Soit le couple auquel appartient l acide hypochloreux : écrire la demi-équation électronique (d échange d électrons) entre l oxydant et le réducteur de ce couple en milieu acide. b) En déduire l équation de la réaction d oxydoréduction qui a lieu en milieu acide entre l acide hypochloreux et les ions iodure I lorsqu on ajoute un excès d iodure de potassium KI. c) Exprimer la quantité de matière de diiode formé lors de cette réaction (1) en fonction de la quantité de matière d HClO présent initialement, en considérant la réaction totale. d) En déduire une relation entre la quantité de matière de diiode formé et la quantité de DCCNa présente dans la poudre ainsi dosée. 9) Réaction (2) du dosage : a) Soit le couple auquel appartient l ion thiosulfate S 2 O : écrire la demi-équation électronique (d échange d électrons) entre l oxydant et le réducteur de ce couple. b) En déduire l équation de la réaction d oxydoréduction qui a lieu entre les ions thiosulfate et le diiode I 2, produit de la réaction (1). c) Donner la relation à l équivalence entre la quantité de matière de diiode I 2 et la quantité de matière d ion thiosulfate S 2 O ) En déduire une relation entre les quantités de matière de thiosulfate et de DCCNa. 11) En déduire la masse de DCCNa présent dans les m grammes de poudre puis déterminer le pourcentage massique en DCCNa des pastilles du commerce. Comparer aux données de l étiquette. A propos des piscines : 12) Pourquoi le ph d une eau de piscine doit-il être inférieur à 7,5? Citer deux raisons. 13) Pourquoi le ph est-il maintenu au-dessus de 7? 14) Les baigneurs associent souvent une forte «odeur de chlore» à une eau de piscine «trop traitée» aux désinfectants. Est-ce le cas? expliquer. 5
6 A propos de la préparation de la solution d hypochlorite de calcium. Lorsqu on prépare une solution d hypochlorite de calcium il se forme un précipité. A quoi cela peut-il être dû? On donne la constante d équilibre relative à l équilibre de dissolution/précipitation: Pour l hydroxyde de calcium, dans le sens direct de la précipitation K = 1, ) Dissolution de l hypochlorite de calcium : a) Rappeler la formule de l ion hypochlorite. b) Le numéro atomique du Calcium est Z = 20. Préciser la structure électronique en couches de l atome de calcium. L ion calcium est- il un cation ou un anion? Donner sa formule en justifiant. c) En déduire la formule des cristaux d hypochlorite de calcium. d) Ecrire l équation de la réaction de dissolution de l hypochlorite de calcium dans l eau conduisant à la formation des ions hypochlorites et calcium hydratés. e) En considérant que cette réaction est totale, quelle est la concentration molaire effective en ions hypochlorite et calcium de la solution si la concentration molaire en soluté apporté est C = 1,0 mol.l -1 16) Lorsqu on met en solution les ions hypochlorite ClO -, ils réagissent avec l eau H 2 O suivant une réaction acidobasique. Ecrire l équation de la réaction qu il se produit. 17) Lors de la préparation d une solution d hypochlorite de calcium au laboratoire, on considère que le ph de la solution est de 11,5 au moment où tous les cristaux d hypochlorite de calcium sont dissous. a) Quelle est la concentration molaire en ions oxonium H 3 O + de cette solution à ce moment? b) En déduire la concentration molaire en ions hydroxyde OH -. c) Ecrire l équation de la réaction entre les ions calcium et les ions hydroxyde conduisant à un précipité d hydroxyde de calcium. d) Exprimer le quotient de réaction Q r,i à l état initial de ce système en fonction des concentrations molaires effectives initiales [Ca 2+ ] i et [OH - ] i. e) Calculer le quotient de réaction à l état initial. f) Comparer à la constante d équilibre K : ce quotient de réaction est-il inférieur, supérieur ou égale à la constante d équilibre K? g) Conclure quant à l évolution du système chimique. 18) La solubilité de l hypochlorite de calcium est en fait de 140 g.l -1 à 20 C. a) Rappeler la définition de la solubilité. b) Quelles sont les concentrations molaires effectives maximales en ions hypochlorite et en ions calcium d une solution saturée en hypochlorite de calcium? c) La réaction évoquée à la question 15)e) est-elle totale? Conclure sur la formation du précipité observé lors de la préparation de la solution d hypochlorite de calcium. 6
7 Complément : Traitement des eaux de piscine : : équipements publics-piscines et centres aquatiques Schéma d'une installation de piscine et ses annexes Pourquoi doit-on traiter les eaux de piscines? Une eau abandonnée à elle-même sans traitement devient très vite un bouillon de culture : elle perd de sa transparence, puis des algues se développent et elle devient verte. La plupart des micro-organismes peuvent survivre et se développer dans l'eau : le but du traitement de désinfection consiste à les tuer avant leur multiplication. On peut trouver dans l'eau des bactéries et des virus, des parasites (champignons, amibes) Produits : Différents traitements désinfectants chlore gazeux hypochlorites de sodium ou de calcium chlorocyanuriques brome liquide ozone ( en association avec les précédents pour un effet rémanent) Procédé électrolytique : on introduit du sel dans l'eau et par électrolyse on produit de l'eau de Javel Procédé par ultraviolet: ces rayonnements sont bactéricides mais ce traitement doit être associé à un produit désinfectant pour un effet rémanent 7
8 Action désinfectante du dichloroisocyanurate de sodium : Le dichloroisocyanurate de sodium réagit avec l'eau pour former du cyanurate de sodium et de l'acide hypochloreux Comme tout acide, le dissociation de l'acide hypochloreux en ion hypochlorite est influencé par le ph. Or c'est l'acide hypochloreux qui est le composé le plus actif dans les mécanismes de la désinfection ( l'ion hypochlorite est peu oxydant et peu bactéricide). En effet il ne porte pas de charge électrique et sa forme ressemble à celle de l'eau. La membrane cytoplasmique le laisse donc passer en même temps que l'eau, contrairement à ClO- qui ne pénètre pas du fait de sa charge négative. A l'intérieur de la cellule, HClO bloque toute activité enzymatique, entraînant ainsi la mort de la cellule. Odeur de chlore dans les piscines : Une concentration donnée de HOCl permettra de détruire 99 % des bactéries témoins telles que Escherichia coli en moins de 2 minutes de temps de contact, alors qu'un temps de contact de 100 minutes sera nécessaire en présence de ClO- à la même concentration. Dans les piscines, il y a un apport continuel de matières azotées sous forme d'urée (sueur,urine ). L'urée subit une hydrolyse avec formation d'ammoniac. (NH 2 ) 2 CO + H 2 O = 2 NH 3 + CO 2 L'ammoniac réagit avec l'acide hypochloreux pour former des chloramines. NH 3 + HClO = NHCl + H 2 O (formation de monochloramine) NHCl + HClO = NHCl 2 + H 2 O (formation de dichloramine) etc... Une oxydation plus poussée conduit à la destruction des chloramines avec formation de diazote. Les baigneurs apportent également dans l'eau des matières organiques plus complexes qui forment par réactions avec l'acide hypochloreux des chloramines organiques plus complexes qui forment par réactions avec l'acide hypochloreux des chloramines organiques plus complexes. Les chloramines sont des composés qui ont une action bactéricide très faible. Par contre elles sont fortement lacrymogènes et piquent les yeux, sont irritantes pour les muqueuses. Elles sont responsables en grande partie de «l'odeur de chlore» dans certaines piscines. Pour détruire les chloramines organiques, il faut un ph inférieur à 7,5 et une chloration suffisante. Une forte «odeur de chlore» dans une piscine et signe d'une sous-chloration. On comprend la nécessité de demander aux baigneurs de passer aux toilettes et de se doucher avant de se baigner dans une piscine... 8
9 Quel ph pour ma piscine? Le ph idéal pour une eau de piscine est compris entre 7,2 et 7,4 9
10 Liste du matériel : (prévoir 22 binômes) Glace pilée au frigo pour une poignée ou deux (x 22 binômes) Par binôme : Pour la synthèse : 2 burettes avec dispositif pour pouvoir les positionner bien au- dessus du becher + é poubelles différentes numérotés. Agitation magnétique + grand barreau aimanté. Petit cristallisoir Un becher de 250 ml 5 béchers de 100 ml Un ph-mètre + solutions tampons 4 et 7 + notice ph-mètre Un thermomètre Parafilm pour couvrir le becher de 250 ml durant la synthèse (pour Cl 2 ) Coupelle en plastique de pesée Spatule. Trompe à vide + verre frité + tube coudé en verre pour «écraser» la poudre Agitateur en verre Support tubes à essais + 6 tubes à essais Eprouvette graduée de 50 ml + éprouvette de 25 et éprouvette de 10 ml Capsule en porcelaine pour étuve 4 petites pipettes en plastique compte-gouttes. Crayons à verre (on peut en demander à Yvelines si tu n en as pas. ) Pour le dosage redox : Pissette d eau distillée 2 erlenmeyers de 250 ml 2 parafilms pour les deux erlens Paillasse ( pour 4 binômes) : Salle des balances avec l acide cyanurique (sans spatule) étiqueté ACIDE CYANURIQUE, et si possible dans autant de flacons qu il y a de balances, pour que cela aille assez vite car il va y avoir du monde. Etuve sur C ( dans la salle des balances? commune aux deux labos) Dans chaque salle, pour 4 binômes. Je pense qu il faudrait éviter de placer les bouteilles au-dessus des 4 paillasses, mais plutôt au milieu et en bas, au niveau des paillasses. Ce sont des élèves qui ne manipulent pas beaucoup, et les produits sont dangereux et concentrés. En mettant 3 postes par paillasses de 4 binômes, il reste un poste qu on peut réserver pour les différents produits. o Réserve d eau distillée o Solution de Ca(ClO) 2 à 2,25 mol.l -1 o Solution acide chlorhydrique à 5,5 mol.l -1 o Solution hélianthine 1g /L pour teste (il en faut très peu : 10 ou 20 ml pour 4 binômes ) o Thiodene + spatule o Solution KI à 1 mol.l -1 o Solution de K 2 S 2 O 3 à 0,200 mol.l -1 o Acide acétique commercial. o Pour 4 binômes, 1 pastille du commerce broyée dans une coupelle en porcelaine ou autre recouvert d un parafilm bien étiqueté DCCNa du commerce (pour dichlorocyanurate de sodium) o 2 Parafilms pour les deux erlens. 10
11 11
EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points)
 Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
Bac S 2015 Antilles Guyane http://labolycee.org EXERCICE II. SYNTHÈSE D UN ANESTHÉSIQUE : LA BENZOCAÏNE (9 points) La benzocaïne (4-aminobenzoate d éthyle) est utilisée en médecine comme anesthésique local
LABORATOIRES DE CHIMIE Techniques de dosage
 LABORATOIRES DE CHIMIE Techniques de dosage Un dosage (ou titrage) a pour but de déterminer la concentration molaire d une espèce (molécule ou ion) en solution (généralement aqueuse). Un réactif de concentration
LABORATOIRES DE CHIMIE Techniques de dosage Un dosage (ou titrage) a pour but de déterminer la concentration molaire d une espèce (molécule ou ion) en solution (généralement aqueuse). Un réactif de concentration
TP : Suivi d'une réaction par spectrophotométrie
 Nom : Prénom: n groupe: TP : Suivi d'une réaction par spectrophotométrie Consignes de sécurité de base: Porter une blouse en coton, pas de nu-pieds Porter des lunettes, des gants (en fonction des espèces
Nom : Prénom: n groupe: TP : Suivi d'une réaction par spectrophotométrie Consignes de sécurité de base: Porter une blouse en coton, pas de nu-pieds Porter des lunettes, des gants (en fonction des espèces
DÉTERMINATION DU POURCENTAGE EN ACIDE D UN VINAIGRE. Sommaire
 BACCALAURÉAT SÉRIE S Épreuve de PHYSIQUE CHIMIE Évaluation des compétences expérimentales Sommaire I. DESCRIPTIF DU SUJET DESTINÉ AUX PROFESSEURS... 2 II. LISTE DE MATÉRIEL DESTINÉE AUX PROFESSEURS ET
BACCALAURÉAT SÉRIE S Épreuve de PHYSIQUE CHIMIE Évaluation des compétences expérimentales Sommaire I. DESCRIPTIF DU SUJET DESTINÉ AUX PROFESSEURS... 2 II. LISTE DE MATÉRIEL DESTINÉE AUX PROFESSEURS ET
Capteur à CO2 en solution
 Capteur à CO2 en solution Référence PS-2147CI Boîtier adaptateur Sonde ph Sonde température Sonde CO2 Page 1 sur 9 Introduction Cette sonde est conçue pour mesurer la concentration de CO 2 dans les solutions
Capteur à CO2 en solution Référence PS-2147CI Boîtier adaptateur Sonde ph Sonde température Sonde CO2 Page 1 sur 9 Introduction Cette sonde est conçue pour mesurer la concentration de CO 2 dans les solutions
THEME 2. LE SPORT CHAP 1. MESURER LA MATIERE: LA MOLE
 THEME 2. LE SPORT CHAP 1. MESURER LA MATIERE: LA MOLE 1. RAPPEL: L ATOME CONSTITUANT DE LA MATIERE Toute la matière de l univers, toute substance, vivante ou inerte, est constituée à partir de particules
THEME 2. LE SPORT CHAP 1. MESURER LA MATIERE: LA MOLE 1. RAPPEL: L ATOME CONSTITUANT DE LA MATIERE Toute la matière de l univers, toute substance, vivante ou inerte, est constituée à partir de particules
BAC BLANC SCIENCES PHYSIQUES. Durée : 3 heures 30
 Terminales S1, S2, S3 2010 Vendredi 29 janvier BAC BLANC SCIENCES PHYSIQUES Durée : 3 heures 30 Toutes les réponses doivent être correctement rédigées et justifiées. Chaque exercice sera traité sur une
Terminales S1, S2, S3 2010 Vendredi 29 janvier BAC BLANC SCIENCES PHYSIQUES Durée : 3 heures 30 Toutes les réponses doivent être correctement rédigées et justifiées. Chaque exercice sera traité sur une
TRAVAUX PRATIQUESDE BIOCHIMIE L1
 TRAVAUX PRATIQUESDE BICHIMIE L1 PRINTEMPS 2011 Les acides aminés : chromatographie sur couche mince courbe de titrage Etude d une enzyme : la phosphatase alcaline QUELQUES RECMMANDATINS IMPRTANTES Le port
TRAVAUX PRATIQUESDE BICHIMIE L1 PRINTEMPS 2011 Les acides aminés : chromatographie sur couche mince courbe de titrage Etude d une enzyme : la phosphatase alcaline QUELQUES RECMMANDATINS IMPRTANTES Le port
259 VOLUMETRIE ET TITRATION DOSAGE DU NaOH DANS LE DESTOP
 259 VOLUMETRIE ET TITRATION DOSAGE DU NaOH DANS LE DESTOP A d a p t a t i o n : A. - M. F o u r n i e r ( C o p a d ), M. C a s a n o v a & H. J e n n y ( C d C ) 2 0 0 1 C o n c e p t i o n D. M a r g
259 VOLUMETRIE ET TITRATION DOSAGE DU NaOH DANS LE DESTOP A d a p t a t i o n : A. - M. F o u r n i e r ( C o p a d ), M. C a s a n o v a & H. J e n n y ( C d C ) 2 0 0 1 C o n c e p t i o n D. M a r g
Titre alcalimétrique et titre alcalimétrique complet
 Titre alcalimétrique et titre alcalimétrique complet A Introduction : ) Définitions : Titre Alcalimétrique (T.A.) : F m / L T.A. T.A.C. Définition : C'est le volume d'acide (exprimé en ml) à 0,0 mol.l
Titre alcalimétrique et titre alcalimétrique complet A Introduction : ) Définitions : Titre Alcalimétrique (T.A.) : F m / L T.A. T.A.C. Définition : C'est le volume d'acide (exprimé en ml) à 0,0 mol.l
Exemple de cahier de laboratoire : cas du sujet 2014
 Exemple de cahier de laboratoire : cas du sujet 2014 Commentaires pour l'évaluation Contenu du cahier de laboratoire Problématique : Le glucose est un nutriment particulièrement important pour le sportif.
Exemple de cahier de laboratoire : cas du sujet 2014 Commentaires pour l'évaluation Contenu du cahier de laboratoire Problématique : Le glucose est un nutriment particulièrement important pour le sportif.
SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION)
 Terminale S CHIMIE TP n 2b (correction) 1 SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION) Objectifs : Déterminer l évolution de la vitesse de réaction par une méthode physique. Relier l absorbance
Terminale S CHIMIE TP n 2b (correction) 1 SUIVI CINETIQUE PAR SPECTROPHOTOMETRIE (CORRECTION) Objectifs : Déterminer l évolution de la vitesse de réaction par une méthode physique. Relier l absorbance
K W = [H 3 O + ] [OH - ] = 10-14 = K a K b à 25 C. [H 3 O + ] = [OH - ] = 10-7 M Solution neutre. [H 3 O + ] > [OH - ] Solution acide
![K W = [H 3 O + ] [OH - ] = 10-14 = K a K b à 25 C. [H 3 O + ] = [OH - ] = 10-7 M Solution neutre. [H 3 O + ] > [OH - ] Solution acide K W = [H 3 O + ] [OH - ] = 10-14 = K a K b à 25 C. [H 3 O + ] = [OH - ] = 10-7 M Solution neutre. [H 3 O + ] > [OH - ] Solution acide](/thumbs/20/420627.jpg) La constante d autoprotolyse de l eau, K W, est égale au produit de K a par K b pour un couple acide/base donné : En passant en échelle logarithmique, on voit donc que la somme du pk a et du pk b d un
La constante d autoprotolyse de l eau, K W, est égale au produit de K a par K b pour un couple acide/base donné : En passant en échelle logarithmique, on voit donc que la somme du pk a et du pk b d un
Séquence 5 Réaction chimique par échange de protons et contrôle de la qualité par dosage
 Séquence 5 Réaction chimique par échange de protons et contrôle de la qualité par dosage Problématique La séquence 5, qui comporte deux parties distinctes, mais non indépendantes, traite de la réaction
Séquence 5 Réaction chimique par échange de protons et contrôle de la qualité par dosage Problématique La séquence 5, qui comporte deux parties distinctes, mais non indépendantes, traite de la réaction
pka D UN INDICATEUR COLORE
 TP SPETROPHOTOMETRIE Lycée F.BUISSON PTSI pka D UN INDIATEUR OLORE ) Principes de la spectrophotométrie La spectrophotométrie est une technique d analyse qualitative et quantitative, de substances absorbant
TP SPETROPHOTOMETRIE Lycée F.BUISSON PTSI pka D UN INDIATEUR OLORE ) Principes de la spectrophotométrie La spectrophotométrie est une technique d analyse qualitative et quantitative, de substances absorbant
Synthèse et propriétés des savons.
 Synthèse et propriétés des savons. Objectifs: Réaliser la synthèse d'un savon mise en évidence de quelques propriétés des savons. I Introduction: 1. Présentation des savons: a) Composition des savons.
Synthèse et propriétés des savons. Objectifs: Réaliser la synthèse d'un savon mise en évidence de quelques propriétés des savons. I Introduction: 1. Présentation des savons: a) Composition des savons.
Mesures calorimétriques
 TP N 11 Mesures calorimétriques - page 51 - - T.P. N 11 - Ce document rassemble plusieurs mesures qui vont faire l'objet de quatre séances de travaux pratiques. La quasi totalité de ces manipulations utilisent
TP N 11 Mesures calorimétriques - page 51 - - T.P. N 11 - Ce document rassemble plusieurs mesures qui vont faire l'objet de quatre séances de travaux pratiques. La quasi totalité de ces manipulations utilisent
ACIDES BASES. Chap.5 SPIESS
 ACIDES BASES «Je ne crois pas que l on me conteste que l acide n ait des pointes Il ne faut que le goûter pour tomber dans ce sentiment car il fait des picotements sur la langue.» Notion d activité et
ACIDES BASES «Je ne crois pas que l on me conteste que l acide n ait des pointes Il ne faut que le goûter pour tomber dans ce sentiment car il fait des picotements sur la langue.» Notion d activité et
TP n 1: Initiation au laboratoire
 Centre Universitaire d El-Tarf Institut des Sciences Agronomiques 3 ème année Contrôle de Qualité en Agroalimentaire TP n 1: Initiation au laboratoire Introduction L analyse de la matière vivante au laboratoire
Centre Universitaire d El-Tarf Institut des Sciences Agronomiques 3 ème année Contrôle de Qualité en Agroalimentaire TP n 1: Initiation au laboratoire Introduction L analyse de la matière vivante au laboratoire
(aq) sont colorées et donnent à la solution cette teinte violette, assimilable au magenta.»
 Chapitre 5 / TP 1 : Contrôle qualité de l'eau de Dakin par dosage par étalonnage à l'aide d'un spectrophotomètre Objectif : Vous devez vérifier la concentration massique d'un désinfectant, l'eau de Dakin.
Chapitre 5 / TP 1 : Contrôle qualité de l'eau de Dakin par dosage par étalonnage à l'aide d'un spectrophotomètre Objectif : Vous devez vérifier la concentration massique d'un désinfectant, l'eau de Dakin.
33-Dosage des composés phénoliques
 33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
33-Dosage des composés phénoliques Attention : cette manip a été utilisée et mise au point pour un diplôme (Kayumba A., 2001) et n a plus été utilisée depuis au sein du labo. I. Principes Les composés
L eau de Javel : sa chimie et son action biochimique *
 N 792 BULLETIN DE L UNION DES PHYSICIENS 451 L eau de Javel : sa chimie et son action biochimique * par Guy DURLIAT Département de biochimie ENS de Cachan - 61, avenue du Président Wilson - 94235 Cachan
N 792 BULLETIN DE L UNION DES PHYSICIENS 451 L eau de Javel : sa chimie et son action biochimique * par Guy DURLIAT Département de biochimie ENS de Cachan - 61, avenue du Président Wilson - 94235 Cachan
Étape 1 : Balancer la chimie de l'eau
 Étape 1 : Balancer la chimie de l'eau Au printemps surtout et durant l'été, il sera important de contrôler et d'ajuster certain paramètres qui constituent la chimie de l'eau. Cet étape est bien souvent
Étape 1 : Balancer la chimie de l'eau Au printemps surtout et durant l'été, il sera important de contrôler et d'ajuster certain paramètres qui constituent la chimie de l'eau. Cet étape est bien souvent
QU EST-CE QUE LA CHLORATION?
 QU EST-CE QUE LA CHLORATION? Qu est-ce que la chloration? Des micro-organismes peuvent être trouvés dans des rivières, lacs et eau souterraine. Même si ce ne sont pas tous les micro-organismes qui peuvent
QU EST-CE QUE LA CHLORATION? Qu est-ce que la chloration? Des micro-organismes peuvent être trouvés dans des rivières, lacs et eau souterraine. Même si ce ne sont pas tous les micro-organismes qui peuvent
CONSTRUCTION DES COMPETENCES DU SOCLE COMMUN CONTRIBUTION DES SCIENCES PHYSIQUES
 CONSTRUCTION DES COMPETENCES DU SOCLE COMMUN CONTRIBUTION DES SCIENCES PHYSIQUES Compétence du socle : Compétence 6 : Les compétences sociales et civiques. Contribution attendue : Utiliser un produit chimique
CONSTRUCTION DES COMPETENCES DU SOCLE COMMUN CONTRIBUTION DES SCIENCES PHYSIQUES Compétence du socle : Compétence 6 : Les compétences sociales et civiques. Contribution attendue : Utiliser un produit chimique
TS 31 ATTAQUE DE FOURMIS!
 FICHE 1 Fiche à destination des enseignants TS 31 ATTAQUE DE FOURMIS! Type d'activité ECE Notions et contenus du programme de Terminale S Compétences exigibles du programme de Terminale S TYPE ECE Evaluation
FICHE 1 Fiche à destination des enseignants TS 31 ATTAQUE DE FOURMIS! Type d'activité ECE Notions et contenus du programme de Terminale S Compétences exigibles du programme de Terminale S TYPE ECE Evaluation
TS1 TS2 02/02/2010 Enseignement obligatoire. DST N 4 - Durée 3h30 - Calculatrice autorisée
 TS1 TS2 02/02/2010 Enseignement obligatoire DST N 4 - Durée 3h30 - Calculatrice autorisée EXERCICE I : PRINCIPE D UNE MINUTERIE (5,5 points) A. ÉTUDE THÉORIQUE D'UN DIPÔLE RC SOUMIS À UN ÉCHELON DE TENSION.
TS1 TS2 02/02/2010 Enseignement obligatoire DST N 4 - Durée 3h30 - Calculatrice autorisée EXERCICE I : PRINCIPE D UNE MINUTERIE (5,5 points) A. ÉTUDE THÉORIQUE D'UN DIPÔLE RC SOUMIS À UN ÉCHELON DE TENSION.
SP. 3. Concentration molaire exercices. Savoir son cours. Concentrations : Classement. Concentration encore. Dilution :
 SP. 3 Concentration molaire exercices Savoir son cours Concentrations : Calculer les concentrations molaires en soluté apporté des solutions désinfectantes suivantes : a) Une solution de 2,0 L contenant
SP. 3 Concentration molaire exercices Savoir son cours Concentrations : Calculer les concentrations molaires en soluté apporté des solutions désinfectantes suivantes : a) Une solution de 2,0 L contenant
Rappels sur les couples oxydantsréducteurs
 CHAPITRE 1 TRANSFORMATIONS LENTES ET RAPIDES 1 Rappels sur les couples oxydantsréducteurs 1. Oxydants et réducteurs Un réducteur est une espèce chimique capable de céder au moins un électron Demi-équation
CHAPITRE 1 TRANSFORMATIONS LENTES ET RAPIDES 1 Rappels sur les couples oxydantsréducteurs 1. Oxydants et réducteurs Un réducteur est une espèce chimique capable de céder au moins un électron Demi-équation
Calcaire ou eau agressive en AEP : comment y remédier?
 Calcaire ou eau agressive en AEP : comment y remédier? Les solutions techniques Principes et critères de choix Par Sébastien LIBOZ - Hydrogéologue Calcaire ou eau agressive en AEP : comment y remédier?
Calcaire ou eau agressive en AEP : comment y remédier? Les solutions techniques Principes et critères de choix Par Sébastien LIBOZ - Hydrogéologue Calcaire ou eau agressive en AEP : comment y remédier?
Perrothon Sandrine UV Visible. Spectrophotométrie d'absorption moléculaire Étude et dosage de la vitamine B 6
 Spectrophotométrie d'absorption moléculaire Étude et dosage de la vitamine B 6 1 1.But et théorie: Le but de cette expérience est de comprendre l'intérêt de la spectrophotométrie d'absorption moléculaire
Spectrophotométrie d'absorption moléculaire Étude et dosage de la vitamine B 6 1 1.But et théorie: Le but de cette expérience est de comprendre l'intérêt de la spectrophotométrie d'absorption moléculaire
Chapitre 7 Les solutions colorées
 Chapitre 7 Les solutions colorées Manuel pages 114 à 127 Choix pédagogiques. Ce chapitre a pour objectif d illustrer les points suivants du programme : - dosage de solutions colorées par étalonnage ; -
Chapitre 7 Les solutions colorées Manuel pages 114 à 127 Choix pédagogiques. Ce chapitre a pour objectif d illustrer les points suivants du programme : - dosage de solutions colorées par étalonnage ; -
β-galactosidase A.2.1) à 37 C, en tampon phosphate de sodium 0,1 mol/l ph 7 plus 2-mercaptoéthanol 1 mmol/l et MgCl 2 1 mmol/l (tampon P)
 bioch/enzymo/tp-betagal-initiation-michaelis.odt JF Perrin maj sept 2008-sept 2012 page 1/6 Etude de la β-galactosidase de E. Coli : mise en évidence d'un comportement Michaélien lors de l'hydrolyse du
bioch/enzymo/tp-betagal-initiation-michaelis.odt JF Perrin maj sept 2008-sept 2012 page 1/6 Etude de la β-galactosidase de E. Coli : mise en évidence d'un comportement Michaélien lors de l'hydrolyse du
Suivi d une réaction lente par chromatographie
 TS Activité Chapitre 8 Cinétique chimique Suivi d une réaction lente par chromatographie Objectifs : Analyser un protocole expérimental de synthèse chimique Analyser un chromatogramme pour mettre en évidence
TS Activité Chapitre 8 Cinétique chimique Suivi d une réaction lente par chromatographie Objectifs : Analyser un protocole expérimental de synthèse chimique Analyser un chromatogramme pour mettre en évidence
Site : http://www.isnab.com mail : [email protected] SUJET ES - session 2003 Page 1 68-(7(6VHVVLRQ
 Site : http://www.isnab.com mail : [email protected] SUJET ES - session 003 Page 1 68-(7(6VHVVLRQ LE JUS E FRUIT 35(0,Ê5(3$57,(%LRFKLPLHSRLQWV L'analyse d'un jus de fruit révèle la présence d'un composé
Site : http://www.isnab.com mail : [email protected] SUJET ES - session 003 Page 1 68-(7(6VHVVLRQ LE JUS E FRUIT 35(0,Ê5(3$57,(%LRFKLPLHSRLQWV L'analyse d'un jus de fruit révèle la présence d'un composé
Table des matières. Acides et bases en solution aqueuse... 10. Oxydo Réduction... 26
 Annales de Chimie aux BTS 2000-2004 Table des matières Table des matières Table des matières... 1 Réactions chimiques...5 BTS Agroéquipement 2003 et BTS Maintenance et après vente des équipement de travaux
Annales de Chimie aux BTS 2000-2004 Table des matières Table des matières Table des matières... 1 Réactions chimiques...5 BTS Agroéquipement 2003 et BTS Maintenance et après vente des équipement de travaux
Physique Chimie. Réaliser les tests de reconnaissance des ions Cl -,
 Document du professeur 1/5 Niveau 3 ème Physique Chimie Programme A - La chimie, science de la transformation de la matière Connaissances Capacités Exemples d'activités Comment reconnaître la présence
Document du professeur 1/5 Niveau 3 ème Physique Chimie Programme A - La chimie, science de la transformation de la matière Connaissances Capacités Exemples d'activités Comment reconnaître la présence
Matériel de laboratoire
 Matériel de laboratoire MATERIAUX UTILISE... 1 L'APPAREILLAGE DE LABORATOIRE... 1 a) Les récipients à réaction... 2 b) La verrerie Graduée... 2 MATERIEL DE FILTRATION... 6 FILTRATION SOUS VIDE AVEC UN
Matériel de laboratoire MATERIAUX UTILISE... 1 L'APPAREILLAGE DE LABORATOIRE... 1 a) Les récipients à réaction... 2 b) La verrerie Graduée... 2 MATERIEL DE FILTRATION... 6 FILTRATION SOUS VIDE AVEC UN
Comment suivre l évolution d une transformation chimique? + S 2 O 8 = I 2 + 2 SO 4
 Afin d optimiser leurs procédés, les industries chimiques doivent contrôler le bon déroulement de la réaction de synthèse menant aux espèces voulues. Comment suivre l évolution d une transformation chimique?
Afin d optimiser leurs procédés, les industries chimiques doivent contrôler le bon déroulement de la réaction de synthèse menant aux espèces voulues. Comment suivre l évolution d une transformation chimique?
Acides et bases. Acides et bases Page 1 sur 6
 Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
Acides et bases Acides et bases Page 1 sur 6 Introduction Sont réputés acides et bases au sens des règles de sécurité en vigueur en Suisse, les solides ou liquides qui ont une réaction acide ou alcaline
Dosage de l'azote ammoniacal
 Page 1 / 15 Version : 2014 Date de création : 3 décembre 2007 Date de dernière modification : 1er décembre 2012 Dosage de l'azote ammoniacal Rédigé par : Thierry Cariou Eric Macé Visé par : Nicole Garcia,
Page 1 / 15 Version : 2014 Date de création : 3 décembre 2007 Date de dernière modification : 1er décembre 2012 Dosage de l'azote ammoniacal Rédigé par : Thierry Cariou Eric Macé Visé par : Nicole Garcia,
Vitesse d une réaction chimique
 Chimie chapitre itesse d une réaction chimique A. Avancement d un mobile et vitesse de déplacement Soit un mobile supposé ponctuel P se déplaçant le long d un axe x [Doc. ] : sa position instantanée est
Chimie chapitre itesse d une réaction chimique A. Avancement d un mobile et vitesse de déplacement Soit un mobile supposé ponctuel P se déplaçant le long d un axe x [Doc. ] : sa position instantanée est
4. Conditionnement et conservation de l échantillon
 1. Objet S-II-3V1 DOSAGE DU MERCURE DANS LES EXTRAITS D EAU RÉGALE Description du dosage du mercure par spectrométrie d absorption atomique de vapeur froide ou par spectrométrie de fluorescence atomique
1. Objet S-II-3V1 DOSAGE DU MERCURE DANS LES EXTRAITS D EAU RÉGALE Description du dosage du mercure par spectrométrie d absorption atomique de vapeur froide ou par spectrométrie de fluorescence atomique
CODEX ŒNOLOGIQUE INTERNATIONAL. SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012)
 SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012) 1. OBJET, ORIGINE ET DOMAINE D APPLICATION Le sucre de raisin est obtenu exclusivement à partir du
SUCRE DE RAISIN (MOUTS DE RAISIN CONCENTRES RECTIFIES) (Oeno 47/2000, Oeno 419A-2011, Oeno 419B-2012) 1. OBJET, ORIGINE ET DOMAINE D APPLICATION Le sucre de raisin est obtenu exclusivement à partir du
AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE
 AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE CONCOURS EXTERNE Session 2005 TRAVAUX PRATIQUES DE BIOCHIMIE PHYSIOLOGIE ALCOOL ET FOIE L éthanol, psychotrope puissant, est absorbé passivement dans l intestin
AGREGATION DE BIOCHIMIE GENIE BIOLOGIQUE CONCOURS EXTERNE Session 2005 TRAVAUX PRATIQUES DE BIOCHIMIE PHYSIOLOGIE ALCOOL ET FOIE L éthanol, psychotrope puissant, est absorbé passivement dans l intestin
C2 - DOSAGE ACIDE FAIBLE - BASE FORTE
 Fiche professeur himie 2 - DOSAGE AIDE FAIBLE - BASE FORTE Mots-clés : dosage, ph-métrie, acide faible, base forte, neutralisation, concentration. 1. Type d activité ette expérience permet aux élèves de
Fiche professeur himie 2 - DOSAGE AIDE FAIBLE - BASE FORTE Mots-clés : dosage, ph-métrie, acide faible, base forte, neutralisation, concentration. 1. Type d activité ette expérience permet aux élèves de
Bleu comme un Schtroumpf Démarche d investigation
 TP Bleu comme un Schtroumpf Démarche d investigation Règles de sécurité Blouse, lunettes de protection, pas de lentilles de contact, cheveux longs attachés. Toutes les solutions aqueuses seront jetées
TP Bleu comme un Schtroumpf Démarche d investigation Règles de sécurité Blouse, lunettes de protection, pas de lentilles de contact, cheveux longs attachés. Toutes les solutions aqueuses seront jetées
FICHE 1 Fiche à destination des enseignants
 FICHE 1 Fiche à destination des enseignants 1S 8 (b) Un entretien d embauche autour de l eau de Dakin Type d'activité Activité expérimentale avec démarche d investigation Dans cette version, l élève est
FICHE 1 Fiche à destination des enseignants 1S 8 (b) Un entretien d embauche autour de l eau de Dakin Type d'activité Activité expérimentale avec démarche d investigation Dans cette version, l élève est
Fiche de révisions sur les acides et les bases
 Fiche de révisions sur les s et les s A Définitions : : espèce chimique capable de libérer un (ou plusieurs proton (s. : espèce chimique capable de capter un (ou plusieurs proton (s. Attention! Dans une
Fiche de révisions sur les s et les s A Définitions : : espèce chimique capable de libérer un (ou plusieurs proton (s. : espèce chimique capable de capter un (ou plusieurs proton (s. Attention! Dans une
Burette TITRONIC Titrateurs TitroLine
 Burette TITRONIC Titrateurs TitroLine 22 rue de l'hermite 33520 BRUGES Tél. 05 56 16 20 16 - Fax 05 56 57 68 07 [email protected] - www.atlanticlabo-ics.fr Un pas en avant pour la titration
Burette TITRONIC Titrateurs TitroLine 22 rue de l'hermite 33520 BRUGES Tél. 05 56 16 20 16 - Fax 05 56 57 68 07 [email protected] - www.atlanticlabo-ics.fr Un pas en avant pour la titration
Fiche 23 : Au laboratoire
 Fiche 23 : Au laboratoire 05/03/2007 Au laboratoire Le port de la blouse est obligatoire. Le port des lunettes ou surlunettes est obligatoire (attention au port des lentilles de contact, autorisé mais
Fiche 23 : Au laboratoire 05/03/2007 Au laboratoire Le port de la blouse est obligatoire. Le port des lunettes ou surlunettes est obligatoire (attention au port des lentilles de contact, autorisé mais
BREVET DE TECHNICIEN SUPÉRIEUR QUALITÉ DANS LES INDUSTRIES ALIMENTAIRES ET LES BIO-INDUSTRIES
 ~--------------~~-----~- ----~-- Session 2009 BREVET DE TECNICIEN SUPÉRIEUR QUALITÉ DANS LES INDUSTRIES ALIMENTAIRES ET LES BIO-INDUSTRIES U22 - SCIENCES PYSIQUES Durée: 2 heures Coefficient : 3 Les calculatrices
~--------------~~-----~- ----~-- Session 2009 BREVET DE TECNICIEN SUPÉRIEUR QUALITÉ DANS LES INDUSTRIES ALIMENTAIRES ET LES BIO-INDUSTRIES U22 - SCIENCES PYSIQUES Durée: 2 heures Coefficient : 3 Les calculatrices
Les piscines à usage collectif Règles sanitaires. à usage collectif
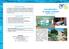 Déclaration d ouverture La déclaration d ouverture d une piscine (accompagnée d un dossier justificatif) est à adresser en 3 exemplaires à la mairie d implantation de l établissement et un exemplaire en
Déclaration d ouverture La déclaration d ouverture d une piscine (accompagnée d un dossier justificatif) est à adresser en 3 exemplaires à la mairie d implantation de l établissement et un exemplaire en
KIT ELISA dosage immunologique anti-bsa REF : ELISA A RECEPTION DU COLIS : Vérifier la composition du colis indiquée ci-dessous en pages 1 et 2
 KIT ELISA dosage immunologique anti-bsa REF : ELISA : 0033 (0)169922672 : 0033 (0)169922674 : www.sordalab.com @ : [email protected] A RECEPTION DU COLIS : Vérifier la composition du colis indiquée ci-dessous
KIT ELISA dosage immunologique anti-bsa REF : ELISA : 0033 (0)169922672 : 0033 (0)169922674 : www.sordalab.com @ : [email protected] A RECEPTION DU COLIS : Vérifier la composition du colis indiquée ci-dessous
Peroxyacide pour l'hygiène dans les industries agroalimentaires
 P3-oxonia active Description Peroxyacide pour l'hygiène dans les industries agroalimentaires Qualités Le P3-oxonia active est efficace à froid. Il n'est ni rémanent ni polluant. Il ne contient pas d'acide
P3-oxonia active Description Peroxyacide pour l'hygiène dans les industries agroalimentaires Qualités Le P3-oxonia active est efficace à froid. Il n'est ni rémanent ni polluant. Il ne contient pas d'acide
------- SESSION 2013 ÉPREUVE À OPTION. (durée : 4 heures coefficient : 6 note éliminatoire 4 sur 20) CHIMIE
 CNCURS SUR ÉPREUVES UVERT AUX CANDIDATS TITULAIRES D UN DIPLÔME U TITRE CNFÉRANT LE GRADE DE MASTER U D'UN DIPLÔME U TITRE HMLGUÉ U ENREGISTRÉ AU RÉPERTIRE NATINAL DES CERTIFICATINS PRFESSINNELLES AU NIVEAU
CNCURS SUR ÉPREUVES UVERT AUX CANDIDATS TITULAIRES D UN DIPLÔME U TITRE CNFÉRANT LE GRADE DE MASTER U D'UN DIPLÔME U TITRE HMLGUÉ U ENREGISTRÉ AU RÉPERTIRE NATINAL DES CERTIFICATINS PRFESSINNELLES AU NIVEAU
TITRONIC et TitroLine. Les nouveaux titrateurs et burettes
 TITRONIC et TitroLine Les nouveaux titrateurs et burettes Un pas en avant pour la titration Si vous cherchez l innovation: SI Analytics vous propose ses nouveaux TitroLine 6000 et 7000 et ses nouvelles
TITRONIC et TitroLine Les nouveaux titrateurs et burettes Un pas en avant pour la titration Si vous cherchez l innovation: SI Analytics vous propose ses nouveaux TitroLine 6000 et 7000 et ses nouvelles
1 ère partie : tous CAP sauf hôtellerie et alimentation CHIMIE ETRE CAPABLE DE. PROGRAMME - Atomes : structure, étude de quelques exemples.
 Référentiel CAP Sciences Physiques Page 1/9 SCIENCES PHYSIQUES CERTIFICATS D APTITUDES PROFESSIONNELLES Le référentiel de sciences donne pour les différentes parties du programme de formation la liste
Référentiel CAP Sciences Physiques Page 1/9 SCIENCES PHYSIQUES CERTIFICATS D APTITUDES PROFESSIONNELLES Le référentiel de sciences donne pour les différentes parties du programme de formation la liste
CHROMATOGRAPHIE SUR COUCHE MINCE
 CHROMATOGRAPHIE SUR COUCHE MINCE I - PRINCIPE La chromatographie est une méthode physique de séparation de mélanges en leurs constituants; elle est basée sur les différences d affinité des substances à
CHROMATOGRAPHIE SUR COUCHE MINCE I - PRINCIPE La chromatographie est une méthode physique de séparation de mélanges en leurs constituants; elle est basée sur les différences d affinité des substances à
TPG 12 - Spectrophotométrie
 TPG 12 - Spectrophotométrie Travail par binôme Objectif : découvrir les conditions de validité et les utilisations possibles de la loi de Beer-Lambert I- Tracé de la rosace des couleurs Choisir un des
TPG 12 - Spectrophotométrie Travail par binôme Objectif : découvrir les conditions de validité et les utilisations possibles de la loi de Beer-Lambert I- Tracé de la rosace des couleurs Choisir un des
L analyse chimique du vin avec Metrohm
 L analyse chimique du vin avec Metrohm Analyse von ph Wert, Gesamtsäure, freie und gesamte schwefelige Säure La titration tactile le 916 Ti-Touch Complément au ph mètre : 876 Manual Titrator Plus Exécution
L analyse chimique du vin avec Metrohm Analyse von ph Wert, Gesamtsäure, freie und gesamte schwefelige Säure La titration tactile le 916 Ti-Touch Complément au ph mètre : 876 Manual Titrator Plus Exécution
GUIDE DE BONNES PRATIQUES POUR LA COLLECTE DE PILES ET ACCUMULATEURS AU LUXEMBOURG
 GUIDE DE BONNES PRATIQUES POUR LA COLLECTE DE PILES ET ACCUMULATEURS AU LUXEMBOURG Version 1.0 1 Avant-propos Ce guide de bonnes pratiques a été préparé pour fournir des informations concernant la collecte
GUIDE DE BONNES PRATIQUES POUR LA COLLECTE DE PILES ET ACCUMULATEURS AU LUXEMBOURG Version 1.0 1 Avant-propos Ce guide de bonnes pratiques a été préparé pour fournir des informations concernant la collecte
A chaque couleur dans l'air correspond une longueur d'onde.
 CC4 LA SPECTROPHOTOMÉTRIE I) POURQUOI UNE SUBSTANCE EST -ELLE COLORÉE? 1 ) La lumière blanche 2 ) Solutions colorées II)LE SPECTROPHOTOMÈTRE 1 ) Le spectrophotomètre 2 ) Facteurs dont dépend l'absorbance
CC4 LA SPECTROPHOTOMÉTRIE I) POURQUOI UNE SUBSTANCE EST -ELLE COLORÉE? 1 ) La lumière blanche 2 ) Solutions colorées II)LE SPECTROPHOTOMÈTRE 1 ) Le spectrophotomètre 2 ) Facteurs dont dépend l'absorbance
BTS BAT 1 Notions élémentaires de chimie 1
 BTS BAT 1 Notions élémentaires de chimie 1 I. L ATOME NOTIONS EÉLEÉMENTAIRES DE CIMIE Les atomes sont des «petits grains de matière» qui constituent la matière. L atome est un système complexe que l on
BTS BAT 1 Notions élémentaires de chimie 1 I. L ATOME NOTIONS EÉLEÉMENTAIRES DE CIMIE Les atomes sont des «petits grains de matière» qui constituent la matière. L atome est un système complexe que l on
ChimGéné 1.3. Guide d utilisation. Auteur : Alain DEMOLLIENS Lycée Carnot - Dijon avec la collaboration de B. DIAWARA Ecole de Chimie de Paris
 ChimGéné 1.3 Guide d utilisation Auteur : Alain DEMOLLIENS Lycée Carnot - Dijon avec la collaboration de B. DIAWARA Ecole de Chimie de Paris INOVASYS 16 rue du Cap Vert 21800 Quétigny Tel : 03-80-71-92-02
ChimGéné 1.3 Guide d utilisation Auteur : Alain DEMOLLIENS Lycée Carnot - Dijon avec la collaboration de B. DIAWARA Ecole de Chimie de Paris INOVASYS 16 rue du Cap Vert 21800 Quétigny Tel : 03-80-71-92-02
Session 2011 PHYSIQUE-CHIMIE. Série S. Enseignement de Spécialité. Durée de l'épreuve: 3 heures 30 - Coefficient: 8
 PYSCSLl BACCALAU Session 20 PHYSIQUE-CHIMIE Série S Enseignement de Spécialité Durée de l'épreuve: 3 heures 30 - Coefficient: 8 L'usage des calculatrices est autorisé. Ce sujet ne nécessite pas de feuille
PYSCSLl BACCALAU Session 20 PHYSIQUE-CHIMIE Série S Enseignement de Spécialité Durée de l'épreuve: 3 heures 30 - Coefficient: 8 L'usage des calculatrices est autorisé. Ce sujet ne nécessite pas de feuille
TP 3 diffusion à travers une membrane
 TP 3 diffusion à travers une membrane CONSIGNES DE SÉCURITÉ Ce TP nécessite la manipulation de liquides pouvant tacher les vêtements. Le port de la blouse est fortement conseillé. Les essuie tout en papier
TP 3 diffusion à travers une membrane CONSIGNES DE SÉCURITÉ Ce TP nécessite la manipulation de liquides pouvant tacher les vêtements. Le port de la blouse est fortement conseillé. Les essuie tout en papier
DETERMINATION DE LA CONCENTRATION D UNE SOLUTION COLOREE
 P1S2 Chimie ACTIVITE n 5 DETERMINATION DE LA CONCENTRATION D UNE SOLUTION COLOREE Le colorant «bleu brillant FCF», ou E133, est un colorant artificiel (de formule C 37 H 34 N 2 Na 2 O 9 S 3 ) qui a longtemps
P1S2 Chimie ACTIVITE n 5 DETERMINATION DE LA CONCENTRATION D UNE SOLUTION COLOREE Le colorant «bleu brillant FCF», ou E133, est un colorant artificiel (de formule C 37 H 34 N 2 Na 2 O 9 S 3 ) qui a longtemps
Les solutions. Chapitre 2 - Modèle. 1 Définitions sur les solutions. 2 Concentration massique d une solution. 3 Dilution d une solution
 Chapitre 2 - Modèle Les solutions 1 Définitions sur les solutions 1.1 Définition d une solution : Une solution est le mélange homogène et liquide d au moins deux espèces chimiques : Le soluté : c est une
Chapitre 2 - Modèle Les solutions 1 Définitions sur les solutions 1.1 Définition d une solution : Une solution est le mélange homogène et liquide d au moins deux espèces chimiques : Le soluté : c est une
DU MAÏS AU PLASTIQUE GROUPE 2. SC2321 - Didactique spéciale en sciences naturelles
 SC2321 - Didactique spéciale en sciences naturelles Activité proposée à des élèves dans le cadre du Festival des Sciences 2005 Thème : «La ville» DU MAÏS AU PLASTIQUE GROUPE 2 CONTEMPRE XAVIER DUBUISSON
SC2321 - Didactique spéciale en sciences naturelles Activité proposée à des élèves dans le cadre du Festival des Sciences 2005 Thème : «La ville» DU MAÏS AU PLASTIQUE GROUPE 2 CONTEMPRE XAVIER DUBUISSON
EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points)
 BAC S 2011 LIBAN http://labolycee.org EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points) Les parties A et B sont indépendantes. A : Étude du fonctionnement d un spectrophotomètre
BAC S 2011 LIBAN http://labolycee.org EXERCICE 2 : SUIVI CINETIQUE D UNE TRANSFORMATION PAR SPECTROPHOTOMETRIE (6 points) Les parties A et B sont indépendantes. A : Étude du fonctionnement d un spectrophotomètre
1) Teneur en amidon/glucose. a) (Z F) 0,9, b) (Z G) 0,9, où:
 L 248/8 Journal officiel de l Union européenne 17.9.2008 RÈGLEMENT (CE) N o 900/2008 DE LA COMMISSION du 16 septembre 2008 définissant les méthodes d analyse et autres dispositions de caractère technique
L 248/8 Journal officiel de l Union européenne 17.9.2008 RÈGLEMENT (CE) N o 900/2008 DE LA COMMISSION du 16 septembre 2008 définissant les méthodes d analyse et autres dispositions de caractère technique
Meine Flüssigkeit ist gefärbt*, comme disaient August Beer (1825-1863) et Johann Heinrich Lambert (1728-1777)
 1ère S Meine Flüssigkeit ist gefärbt*, comme disaient August Beer (1825-1863) et Johann Heinrich Lambert (1728-1777) Objectif : pratiquer une démarche expérimentale pour déterminer la concentration d une
1ère S Meine Flüssigkeit ist gefärbt*, comme disaient August Beer (1825-1863) et Johann Heinrich Lambert (1728-1777) Objectif : pratiquer une démarche expérimentale pour déterminer la concentration d une
4 ème PHYSIQUE-CHIMIE TRIMESTRE 1. Sylvie LAMY Agrégée de Mathématiques Diplômée de l École Polytechnique. PROGRAMME 2008 (v2.4)
 PHYSIQUE-CHIMIE 4 ème TRIMESTRE 1 PROGRAMME 2008 (v2.4) Sylvie LAMY Agrégée de Mathématiques Diplômée de l École Polytechnique Les Cours Pi e-mail : [email protected] site : http://www.cours-pi.com
PHYSIQUE-CHIMIE 4 ème TRIMESTRE 1 PROGRAMME 2008 (v2.4) Sylvie LAMY Agrégée de Mathématiques Diplômée de l École Polytechnique Les Cours Pi e-mail : [email protected] site : http://www.cours-pi.com
Exercices sur le thème II : Les savons
 Fiche d'exercices Elève pour la classe de Terminale SMS page 1 Exercices sur le thème : Les savons EXERCICE 1. 1. L oléine, composé le plus important de l huile d olive, est le triglycéride de l acide
Fiche d'exercices Elève pour la classe de Terminale SMS page 1 Exercices sur le thème : Les savons EXERCICE 1. 1. L oléine, composé le plus important de l huile d olive, est le triglycéride de l acide
Test d immunofluorescence (IF)
 Test d immunofluorescence (IF) 1.1 Prélèvement du cerveau et échantillonnage Avant toute manipulation, il est fondamental de s assurer que tout le personnel en contact avec un échantillon suspect soit
Test d immunofluorescence (IF) 1.1 Prélèvement du cerveau et échantillonnage Avant toute manipulation, il est fondamental de s assurer que tout le personnel en contact avec un échantillon suspect soit
La fonte des glaces fait-elle monter le niveau de la mer?
 La fonte des glaces fait-elle monter le niveau de la mer? L effet de la fonte des glaces sur la variation du niveau de la mer est parfois source d erreur et de confusion. Certains prétendent qu elle est
La fonte des glaces fait-elle monter le niveau de la mer? L effet de la fonte des glaces sur la variation du niveau de la mer est parfois source d erreur et de confusion. Certains prétendent qu elle est
Classe : 1 ère STL Enseignement : Mesure et Instrumentation. d une mesure. Titre : mesure de concentration par spectrophotométrie
 Classe : 1 ère STL Enseignement : Mesure et Instrumentation THEME du programme : mesures et incertitudes de mesures Sous-thème : métrologie, incertitudes Extrait du BOEN NOTIONS ET CONTENUS Mesures et
Classe : 1 ère STL Enseignement : Mesure et Instrumentation THEME du programme : mesures et incertitudes de mesures Sous-thème : métrologie, incertitudes Extrait du BOEN NOTIONS ET CONTENUS Mesures et
TECHNIQUES: Principes de la chromatographie
 TECHNIQUES: Principes de la chromatographie 1 Définition La chromatographie est une méthode physique de séparation basée sur les différentes affinités d un ou plusieurs composés à l égard de deux phases
TECHNIQUES: Principes de la chromatographie 1 Définition La chromatographie est une méthode physique de séparation basée sur les différentes affinités d un ou plusieurs composés à l égard de deux phases
DEMANDE DE BREVET EUROPEEN. PLASSERAUD 84, rue d'amsterdam, F-75009 Paris (FR)
 Patentamt JEuropâisches European Patent Office @ Numéro de publication: 0 1 1 0 7 5 4 Office européen des brevets ^ ^ DEMANDE DE BREVET EUROPEEN Numéro de dépôt: 83402133.9 Int. Cl.3: C 07 C 103/183, C
Patentamt JEuropâisches European Patent Office @ Numéro de publication: 0 1 1 0 7 5 4 Office européen des brevets ^ ^ DEMANDE DE BREVET EUROPEEN Numéro de dépôt: 83402133.9 Int. Cl.3: C 07 C 103/183, C
SCIENCES PHYSIQUES. Durée : 3 heures. L usage d une calculatrice est interdit pour cette épreuve. CHIMIE
 Banque «Agro-Véto» Technologie et Biologie AT - 0310 SCIECES PYSIQUES Durée : 3 heures L usage d une calculatrice est interdit pour cette épreuve. Si, au cours de l épreuve, un candidat repère ce qui lui
Banque «Agro-Véto» Technologie et Biologie AT - 0310 SCIECES PYSIQUES Durée : 3 heures L usage d une calculatrice est interdit pour cette épreuve. Si, au cours de l épreuve, un candidat repère ce qui lui
La baignade en piscine est un plaisir
 La baignade en piscine est un plaisir et doit le rester. C est également un facteur d attrait touristique dans notre région. Cependant une piscine mal gérée et mal entretenue peut être la source d inconfort
La baignade en piscine est un plaisir et doit le rester. C est également un facteur d attrait touristique dans notre région. Cependant une piscine mal gérée et mal entretenue peut être la source d inconfort
TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY)
 TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY) Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste Direction de l innovation scientifique et technologique Au Laboratoire
TEST ELISA (ENZYME-LINKED IMMUNOSORBENT ASSEY) Lise Vézina, technicienne de laboratoire Michel Lacroix, agronome-phytopathologiste Direction de l innovation scientifique et technologique Au Laboratoire
Enseignement secondaire
 Enseignement secondaire Classe de IIIe Chimie 3e classique F - Musique Nombre de leçons: 1.5 Nombre minimal de devoirs: 4 devoirs par an Langue véhiculaire: Français I. Objectifs généraux Le cours de chimie
Enseignement secondaire Classe de IIIe Chimie 3e classique F - Musique Nombre de leçons: 1.5 Nombre minimal de devoirs: 4 devoirs par an Langue véhiculaire: Français I. Objectifs généraux Le cours de chimie
Fiche 19 La couleur des haricots verts et cuisson
 Fiche 19 La couleur des haricots verts et cuisson Objectif : Valider ou réfuter des «précisions culinaires»* permettant de "conserver une belle couleur verte" lors la cuisson des haricots verts frais (gousses
Fiche 19 La couleur des haricots verts et cuisson Objectif : Valider ou réfuter des «précisions culinaires»* permettant de "conserver une belle couleur verte" lors la cuisson des haricots verts frais (gousses
Niveau 2 nde THEME : L UNIVERS. Programme : BO spécial n 4 du 29/04/10 L UNIVERS
 Document du professeur 1/7 Niveau 2 nde THEME : L UNIVERS Physique Chimie SPECTRES D ÉMISSION ET D ABSORPTION Programme : BO spécial n 4 du 29/04/10 L UNIVERS Les étoiles : l analyse de la lumière provenant
Document du professeur 1/7 Niveau 2 nde THEME : L UNIVERS Physique Chimie SPECTRES D ÉMISSION ET D ABSORPTION Programme : BO spécial n 4 du 29/04/10 L UNIVERS Les étoiles : l analyse de la lumière provenant
SECTEUR 4 - Métiers de la santé et de l hygiène
 SECTEUR 4 - Métiers de la santé et de l hygiène A lire attentivement par les candidats Sujet à traiter par tous les candidats inscrit au BEP Les candidats répondront sur la copie. Les annexes éventuelles
SECTEUR 4 - Métiers de la santé et de l hygiène A lire attentivement par les candidats Sujet à traiter par tous les candidats inscrit au BEP Les candidats répondront sur la copie. Les annexes éventuelles
BACCALAURÉAT GÉNÉRAL PHYSIQUE-CHIMIE
 BAALAURÉAT GÉNÉRAL SESSIN 2015 PYSIQUE-IMIE Série S Durée de l épreuve : 3 heures 30 oefficient : 6 L usage de la calculatrice est autorisé e sujet ne nécessite pas de feuille de papier millimétré Le sujet
BAALAURÉAT GÉNÉRAL SESSIN 2015 PYSIQUE-IMIE Série S Durée de l épreuve : 3 heures 30 oefficient : 6 L usage de la calculatrice est autorisé e sujet ne nécessite pas de feuille de papier millimétré Le sujet
Indicateur d'unité Voyant Marche/Arrêt
 Notice MESURACOLOR Colorimètre à DEL Réf. 22020 Indicateur d'unité Voyant Marche/Arrêt Indicateur Etalonnage Bouton Marche/Arrêt Indicateur de sélection de la longueur d'onde Indicateur de mode chronomètre
Notice MESURACOLOR Colorimètre à DEL Réf. 22020 Indicateur d'unité Voyant Marche/Arrêt Indicateur Etalonnage Bouton Marche/Arrêt Indicateur de sélection de la longueur d'onde Indicateur de mode chronomètre
A B C Eau Eau savonneuse Eau + détergent
 1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
1L : Physique et chimie dans la cuisine Chapitre.3 : Chimie et lavage I. Les savons et les détergents synthétiques 1. Propriétés détergentes des savons Le savon est un détergent naturel, les détergents
U-31 CHIMIE-PHYSIQUE INDUSTRIELLES
 Session 200 BREVET de TECHNICIEN SUPÉRIEUR CONTRÔLE INDUSTRIEL et RÉGULATION AUTOMATIQUE E-3 SCIENCES PHYSIQUES U-3 CHIMIE-PHYSIQUE INDUSTRIELLES Durée : 2 heures Coefficient : 2,5 Durée conseillée Chimie
Session 200 BREVET de TECHNICIEN SUPÉRIEUR CONTRÔLE INDUSTRIEL et RÉGULATION AUTOMATIQUE E-3 SCIENCES PHYSIQUES U-3 CHIMIE-PHYSIQUE INDUSTRIELLES Durée : 2 heures Coefficient : 2,5 Durée conseillée Chimie
SALLE DE BAIN, DOUCHE, PLAN DE TRAVAIL CUISINE, PISCINE... Collage et jointoiement. L Epoxy facile
 SALLE DE BAIN, DOUCHE, PLAN DE TRAVAIL CUISINE, PISCINE... Collage et jointoiement L Epoxy facile DOMAINES D EMPLOI Recommandé pour salle de bain, douche, plan de travail cuisine, piscine, bassins thermaux,
SALLE DE BAIN, DOUCHE, PLAN DE TRAVAIL CUISINE, PISCINE... Collage et jointoiement L Epoxy facile DOMAINES D EMPLOI Recommandé pour salle de bain, douche, plan de travail cuisine, piscine, bassins thermaux,
Planches pour le Diagnostic microscopique du paludisme
 République Démocratique du Congo Ministère de la Santé Programme National de Lutte Contre le Paludisme Planches pour le Diagnostic microscopique du paludisme Ces planches visent à améliorer le diagnostic
République Démocratique du Congo Ministère de la Santé Programme National de Lutte Contre le Paludisme Planches pour le Diagnostic microscopique du paludisme Ces planches visent à améliorer le diagnostic
Spectrophotométrie - Dilution 1 Dilution et facteur de dilution. 1.1 Mode opératoire :
 Spectrophotométrie - Dilution 1 Dilution et facteur de dilution. 1.1 Mode opératoire : 1. Prélever ml de la solution mère à la pipette jaugée. Est-ce que je sais : Mettre une propipette sur une pipette
Spectrophotométrie - Dilution 1 Dilution et facteur de dilution. 1.1 Mode opératoire : 1. Prélever ml de la solution mère à la pipette jaugée. Est-ce que je sais : Mettre une propipette sur une pipette
PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage
 PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage I) Qu'est-ce qu'un savon et comment le fabrique-t-on? D'après épreuve BAC Liban 2005 Physique-Chimie dans la cuisine Chapitre 3 1/6 1- En vous
PHYSIQUE-CHIMIE DANS LA CUISINE Chapitre 3 : Chimie et lavage I) Qu'est-ce qu'un savon et comment le fabrique-t-on? D'après épreuve BAC Liban 2005 Physique-Chimie dans la cuisine Chapitre 3 1/6 1- En vous
MÉTHODE DE DÉSEMBOUAGE DE CIRCUITS DE CHAUFFAGE
 MÉTHODE DE DÉSEMBOUAGE DE CIRCUITS DE CHAUFFAGE (Radiateurs et planchers chauffants) Brevet de désembouage N 0116861 EURO FILTR'EAUX 18/22 RUE D ARRAS - F 92000 NANTERRE TÉL. : (33) 01 30 94 37 60 FAX
MÉTHODE DE DÉSEMBOUAGE DE CIRCUITS DE CHAUFFAGE (Radiateurs et planchers chauffants) Brevet de désembouage N 0116861 EURO FILTR'EAUX 18/22 RUE D ARRAS - F 92000 NANTERRE TÉL. : (33) 01 30 94 37 60 FAX
Chapitre 02. La lumière des étoiles. Exercices :
 Chapitre 02 La lumière des étoiles. I- Lumière monochromatique et lumière polychromatique. )- Expérience de Newton (642 727). 2)- Expérience avec la lumière émise par un Laser. 3)- Radiation et longueur
Chapitre 02 La lumière des étoiles. I- Lumière monochromatique et lumière polychromatique. )- Expérience de Newton (642 727). 2)- Expérience avec la lumière émise par un Laser. 3)- Radiation et longueur
REACTIONS D OXYDATION ET DE REDUCTION
 CHIMIE 2 e OS - 2008/2009 : Cours et exercices -19- CHAPITRE 5 : REACTIONS D OXYDATION ET DE REDUCTION Chacun d entre nous a déjà observé l apparition de rouille sur un objet en fer, ou de «vert-degris»
CHIMIE 2 e OS - 2008/2009 : Cours et exercices -19- CHAPITRE 5 : REACTIONS D OXYDATION ET DE REDUCTION Chacun d entre nous a déjà observé l apparition de rouille sur un objet en fer, ou de «vert-degris»
AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS
 AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS CONCOURS EXTERNE ÉPREUVES D ADMISSION session 2010 TRAVAUX PRATIQUES DE CONTRE-OPTION DU SECTEUR A CANDIDATS DES SECTEURS B ET C
AGRÉGATION DE SCIENCES DE LA VIE - SCIENCES DE LA TERRE ET DE L UNIVERS CONCOURS EXTERNE ÉPREUVES D ADMISSION session 2010 TRAVAUX PRATIQUES DE CONTRE-OPTION DU SECTEUR A CANDIDATS DES SECTEURS B ET C
TP N 3 La composition chimique du vivant
 Thème 1 : La Terre dans l'univers, la vie et l'évolution du vivant : une planète habitée Chapitre II : La nature du vivant TP N 3 La composition chimique du vivant Les conditions qui règnent sur terre
Thème 1 : La Terre dans l'univers, la vie et l'évolution du vivant : une planète habitée Chapitre II : La nature du vivant TP N 3 La composition chimique du vivant Les conditions qui règnent sur terre
