Avis 9 janvier Inscription dans une extension d indication
|
|
|
- Simone Pothier
- il y a 7 ans
- Total affichages :
Transcription
1 COMMISSION DE LA TRANSPARENCE Avis 9 janvier 2013 VOTRIENT 200 mg, Comprimé pelliculé B/30 (CIP ) VOTRIENT 400 mg, Comprimé pelliculé B/30 (CIP ) VOTRIENT 400 mg, Comprimé pelliculé B/60 (CIP ) Laboratoire GlaxoSmithKline DCI Code ATC (année) pazopanib L01XE (Inhibiteurs de protéines kinases) Motif de l examen: Inscription dans une extension d indication Liste(s) concernée(s) Indication(s) concernée(s) Sécurité Sociale (CSS L ) Collectivités (CSP L ) «Votrient est indiqué dans le traitement des patients adultes présentant des sous-types histologiques spécifiques de sarcome des tissus mous (STS) avancé, qui ont été préalablement traités par chimiothérapie au stade métastatique ou qui ont progressé dans les 12 mois suivant un traitement (neo) adjuvant.» HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 1/14
2 SMR ASMR Place dans la stratégie thérapeutique Le service médical rendu par VOTRIENT est important dans cette indication. VOTRIENT apporte une ASMR mineure (niveau IV) en termes d efficacité par rapport à la stratégie thérapeutique actuelle. VOTRIENT constitue une alternative thérapeutique dans la prise en charge des patients atteints d un sarcome des tissus mous métastatique, hors liposarcome et GIST, en échec à un traitement à base d anthracyclines ou d ifosfamide. HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 2/14
3 01 INFORMATIONS ADMINISTRATIVES ET REGLEMENTAIRES AMM (européenne centralisée) Conditions de prescription et de délivrance / statut particulier Date de l AMM (procédure centralisée) : 14 juin 2010 Rectificatif du 3 août 2012 Liste I Médicament soumis à prescription hospitalière. Prescription réservée aux spécialistes en oncologie ou en hématologie ou aux médecins compétents en cancérologie. Médicament nécessitant une surveillance particulière pendant le traitement. Classification ATC 2011 L L01 L01X L01XE L01XE11 : Antinéoplasiques et immunomodulateurs : Agents antinéoplasiques : Autres antinéoplasiques : Inhibiteurs de protéines kinases : Pazopanib 02 INDICATION(S) THERAPEUTIQUE(S) «Cancer du rein avancé (Renal Cell Carcinoma - RCC) Votrient est indiqué chez l'adulte en traitement de 1 ère ligne des cancers du rein avancés (RCC) et chez les patients préalablement traités par des cytokines à un stade avancé de leur maladie. Sarcome des tissus mous (Soft Tissue Sarcoma - STS) Votrient est indiqué dans le traitement des patients adultes présentant des sous-types histologiques spécifiques de sarcome des tissus mous (STS) avancé, qui ont été préalablement traités par chimiothérapie au stade métastatique ou qui ont progressé dans les 12 mois suivant un traitement (neo) adjuvant. L'efficacité et la sécurité du pazopanib ont été uniquement établies dans certains soustypes histologiques de STS (voir rubrique 5.1 du RCP).» 03 POSOLOGIE «Adultes La dose de pazopanib recommandée dans le traitement du RCC ou du STS est de 800 mg une fois par jour. Modifications de dose La dose devra être ajustée par paliers de 200 mg en fonction de la tolérance individuelle au traitement afin de pouvoir gérer les effets indésirables. La dose de pazopanib ne devra pas excéder 800 mg.» HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 3/14
4 04 BESOIN THERAPEUTIQUE 1, 2 Les sarcomes des tissus mous (STS) sont des affections rares (moins de 1% de l ensemble des affections malignes chez l adulte). Il s agit d un groupe hétérogène de cancers des tissus conjonctifs provenant de cellules mésenchymateuses et de leurs précurseurs. Il existe plusieurs sous-types histopathologiques de STS. - Au stade localisé, le traitement repose principalement sur la chirurgie et la radiothérapie. Le contrôle de la tumeur primitive et la prévention des rechutes locales nécessitent d abord une exérèse chirurgicale complète qui doit avoir aussi pour objectif de préserver la fonction. Le rôle de la chimiothérapie en traitement adjuvant est controversé. - Au stade métastatique, le traitement repose sur la chimiothérapie systémique. Les sarcomes des tissus mous sont peu chimiosensibles pour lesquelles un nombre limité de molécules efficaces sont disponibles : les anthracyclines, essentiellement la doxorubicine, l ifosfamide, et la dacarbazine. Ces produits sont utilisés seuls ou en association à la phase métastatique de la maladie ; en première ligne de traitements les pourcentages de réponses varient de 20 à 40% avec des durées de survie médiane de 12 à 18 mois. De nombreuses études randomisées ont permis d établir que : les associations sans anthracyclines sont moins actives que la doxorubicine seule à dose équivalente de doxorubicine, l adjonction d un deuxième produit donne des pourcentages de réponses parfois supérieurs mais au prix d une plus grande toxicité et sans modifier la survie la sensibilité à la chimiothérapie varie selon les sous types histologiques : les synovialosarcomes ont une sensibilité particulière à l ifosfamide, les liposarcomes indifférenciés sont les plus chimiosensibles, les leiomyosarcomes sont particulièrement sensibles à une association gemcitabine docétaxel, les angiosarcomes ont une sensibilité particulière au paclitaxel hebdomadaire Après échappement à un traitement incluant doxorubicine et ifosfamide en monothérapie ou en association, la trabectédine dispose d une AMM uniquement pour les liposarcomes ou les léiomyosarcomes. 1 Italiano A, Mathoulin-Pelissier S, Le Cesne A,Terrier P, Bonvalot S, Collin F, Michels JJ, Blay JY, Coindre JM and Bui B. Trends in Survival for Patients With Metastatic Soft-Tissue Sarcoma. Cancer 2011; 117: Le Cesne A, Cioffi A. Chimiothérapie des sarcomes des tissus mous métastatiques et localement avancés. Oncol. 2007;9(2): HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 4/14
5 05 COMPARATEURS CLINIQUEMENT PERTINENTS 05.1 Médicaments Il n existe pas d alternative médicamenteuse disposant d une AMM dans l indication actuelle de VOTRIENT. YONDELIS du laboratoire PHARMA MAR dispose d une AMM commune avec VOTRIENT uniquement dans un sous groupe histologique qui est le leiomyosarcome. - YONDELIS (trabectedine) 0,25 mg et 1mg, poudres pour solution à diluer pour perfusion, indiqué chez les patients atteints de sarcome des tissus mous évolué, après échec de traitements à base d anthracyclines ou d ifosfamide, ou chez les patients ne pouvant pas recevoir ces médicaments. Les données d efficacité ont principalement été obtenues chez des patients atteints de liposarcome et de léiomyosarcome (AMM 2007). Les données sur l apport thérapeutique de YONDELIS dans cette indication sont issues d une étude de phase II non comparative. Conclusion Il n y a pas de comparateur cliniquement pertinent de VOTRIENT. 06 INFORMATIONS SUR LE MEDICAMENT A L INTERNATIONAL Pays OUI/NON Si non pourquoi PRISE EN CHARGE Population(s) Celle de l AMM ou restreinte USA Oui Population AMM dans le sarcome UE Evaluation dans le sarcome en cours HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 5/14
6 07 ANALYSE DES DONNEES DISPONIBLES Le dossier de demande d inscription comporte : - une étude de phase II (étude VEG20002) non comparative, - une étude pivot de phase III (étude VEG110727) comparative versus placebo Efficacité Etude VEG20002 Etude de phase II non comparative dont l objectif était d évaluer l efficacité et la tolérance de VOTRIENT (pazopanib) chez des sujets présentant l un des quatre types de sarcome des tissus mous les plus fréquemment rencontrés dans la base EORTC (le léiomyosarcome, le liposarcome, le synovialosarcome et le fibrosarcome), en rechute après un traitement standard ou pour qui il n existait pas de traitement standard. Les patients ont été traités par VOTRIENT à la dose de 800 mg par jour per os jusqu à progression de la maladie, décès, survenue d événements indésirables inacceptables reliés au produit, maladies intercurrentes ou retrait du consentement du patient. Le critère de jugement principal d efficacité était le pourcentage de non progression (qui inclut : réponses complètes et partielles et stabilisation de la maladie) à 12 semaines, d après l évaluation de la maladie sur le scanner selon les critères RECIST. Les principaux critères secondaires d efficacité étaient : - la survie sans progression, définie comme l intervalle entre la date de la première prise de VOTRIENT et la première documentation de progression de la maladie ou le décès toutes causes. La progression était évaluée par l investigateur. - la survie globale, définie comme l intervalle de temps entre la date de la première prise de VOTRIENT et le décès, quelle qu en soit la cause. - le pourcentage de réponse, défini comme le pourcentage de patients ayant une réponse complète (CR) ou partielle (PR) selon les critères RECIST, sur la base de l évaluation des investigateurs. HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 6/14
7 Le pourcentage de non-progression à 12 semaines, ainsi que les principaux critères secondaires d efficacité sont résumés dans le tableau 1. Tableau 1 : Principaux résultats d'efficacité de l'étude VEG20002 Léiomyosarcomes Liposarcomes Critères d efficacité N=41 N=19 Synovialosarcomes N=37 Autres sarcomes N=41 HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 7/14 Total N=138 Pourcentage de non-progression à 12 semaines RC+RP+SD, n (%) 17 (41) 5 (26) 18 (49) 17 (41) 57 (41) (IC 90%) (28.4, 55.5) (11.0, 47.6) (34.3, 63.2) (28.4, 55.5) (34.2, 48.7) p-value a < <0.001 Survie sans progression (semaines) Médiane (IC 90%) b 17.2 (12.0, 24.1) Survie globale (mois) Médiane (IC 90%) b (7.1, 11.9) 6.5 (4.2, 19.3) 23.4 (11.7, 29.3) 10.3 (7.6, 13.2) 14.0 (12.0, 36.3) 9.8 (7.6, 11.3) 12.1 (12.0, 22.4) 10.6 (9.5, 11.7) (10.6, 17.6) Pourcentage de réponse globale RC+RP, n (%) 1 (2) 0 4 (11) 3 (7) 8 (6) (IC 90%) (0.1, 11.1) (0.0, 11.4) (3.8, 23.1) (2.0, 17.8) (2.9, 10.2) a. p-value = niveau de preuve associé au rejet de l hypothèse nulle d un pourcentage de non progression égal à 20% avec un risque alpha de 010. b. Estimations selon la méthode de Brookmeyer-Crowley. RC : Réponse complète RP : Réponse partielle SD : Stabilisation de la maladie L étude de phase II a démontré une activité antitumorale du pazopanib (pourcentage de nonprogression à 12 semaines > 40%) dans trois groupes histologiques de sarcome des tissus mous en rechute ou réfractaires : les léiomyosarcomes, les synovialosarcomes et les «autres sarcomes». Le manque d activité dans les liposarcomes dans cette étude a justifié la non inclusion de ce sous-type histologique dans l étude de phase III VEG Etude VEG L'efficacité et la tolérance du pazopanib (VOTRIENT) dans les sarcomes des tissus mous ont été évaluées dans un essai pivot de phase III, randomisé, en double aveugle, contrôlé versus placebo. Un total de 369 patients ayant un sarcome des tissus mous au stade avancé ont été randomisés pour recevoir soit du pazopanib à la dose de 800 mg une fois par jour soit du placebo. Les principaux critères d inclusion étaient : - âge de plus de 18 ans, - sarcome des tissus mous au stade métastatique, - progression de la tumeur pendant ou dans les 6 mois après un traitement antérieur pour la maladie avancée (ou 12 mois pour les patients n'ayant reçu qu'un traitement (néo)adjuvant par voie systémique) - parmi les lignes de traitements antérieurs, les patients devaient avoir reçu un traitement à base d anthracyclines ainsi que les chimiothérapies habituellement disponibles - les patients pouvaient avoir reçu un maximum de 4 lignes de traitements systémiques antérieures pour leur maladie avancée, dont au maximum deux schémas d association. Les traitements (néo)adjuvant et de maintenance ne rentraient pas dans ces critères, - tumeur de haut grade de malignité ou de grade intermédiaire. Les tumeurs de bas grade étaient également autorisées si la progression de la maladie était documentée, - une maladie mesurable selon les critères d'évaluation des tumeurs solides (critères RECIST v1.0), - un indice initial de performance OMS de 0 ou 1, - des fonctions d organes acceptables, Parmi les critères de non inclusion :
8 - les liposarcomes (tous les sous-types), tous les rhabdomyosarcomes qui n étaient ni alvéolaires ni pléomorphiques, les chondrosarcomes, les ostéosarcomes, les tumeurs d Ewing/PNET, les GIST, les dermatofibrosarcomes protuberans, les sarcomes myofibroblastiques inflammatoires, le mésothéliome malin et les tumeurs mésodermiques mixtes de l'utérus. - des métastases cérébrales ou lepto-méningées Le critère de jugement principal était la survie sans progression, définie comme l'intervalle de temps entre la date de randomisation et la première date de constatation d une progression de la maladie, ou le décès toutes causes. Un scanner a été réalisé toutes les 4 semaines jusqu'à la semaine 12, puis toutes les 8 semaines par la suite. Leur lecture centralisée, en aveugle, a été confiée à des radiologues indépendants. Les critères secondaires étaient : - la survie globale, définie comme l intervalle de temps entre la randomisation et le décès, quelle qu en soit la cause. - la survie sans progression dans les 3 types histologiques suivants : le léiomyosarcome, le synovialosarcome et les «autres» types histologiques de sarcomes éligibles. - le pourcentage de réponse, défini comme le pourcentage de patients ayant comme meilleure réponse globale une réponse complète (CR) ou partielle (PR) selon les critères RECIST v1.0, recueillie pendant la période comprise entre la première prise du traitement et la progression. - le délai de réponse, défini comme l intervalle de temps entre la randomisation et la première preuve documentée de CR ou PR (selon le statut enregistré en premier). - la durée de réponse, définie comme l intervalle de temps entre la première preuve documentée de CR ou PR et la première documentation de progression de la maladie ou le décès, quelle qu en soit la cause (selon l évènement qui survient en premier). - la tolérance incluant les événements indésirables, les événements indésirables graves, et les modifications par rapport à l entrée dans l étude des signes vitaux, dont l indice de performance OMS, des paramètres biologiques et de la fraction d éjection du ventricule gauche. - la qualité de vie des patients a également été évaluée en tant que critère exploratoire en utilisant la version 3 du questionnaire de qualité de vie (QLQ-C30) de l EORTC à l entrée dans l étude puis aux semaines 4, 8 et 12. Le questionnaire du groupe EuroQol-5D (EQ-5D) a également été utilisé à l entrée dans l étude et à la semaine 4. Résultats : Un total de 369 patients a été inclus. L âge médian des patients était de 55 ans (extrêmes : 18-83). Tous les patients inclus avaient un état général conservé avec un indice de performance OMS de 0 chez 48% et de 1 chez 52%. Quatre-vingt dix huit pour cent (98%) des sujets avaient préalablement reçu une anthracycline (doxorubicine), 70% de l ifosfamide et 56% des sujets avaient reçu au moins deux lignes de chimiothérapie pour le stade avancé avant d entrer dans l étude. La durée médiane de suivi des sujets (définie de la date de randomisation à la date du dernier contact ou décès) a été similaire dans les deux groupes de traitement (9,36 mois pour le groupe placebo et 10,04 mois dans le groupe VOTRIENT). HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 8/14
9 Tableau 2 : Etude VEG110727, Résultats d'efficacité globale dans le STS Critères d'évaluation / VOTRIENT Placebo HR (IC 95%) population de l'étude Survie sans progression (critère de jugement principal) Valeur du p bilatéral Population globale en ITT N = 246 N = 123 Médiane (semaines) 20,0 7,0 0,35 (0,26, 0,48) < 0,001 Léiomyosarcomes N = 109 N = 49 Médiane (semaines) 20,1 8,1 0,37 (0,23, 0,60) < 0,001 Synovialosarcomes N = 25 N = 13 Médiane (semaines) 17,9 4,1 0,43 (0,19, 0,98) 0,005 "Autres STS" N = 112 N = 61 Médiane (semaines) 20,1 4,3 0,39 (0,25, 0,60) < 0,001 Survie globale Population globale en ITT Médiane (mois) N = ,6 N = ,7 0,87 [0,67-1,12] 0,256 Léiomyosarcomes* Médiane (mois) N = ,7 N = 49 14,1 0,84 (0,56, 1,26 0,363 Synovialosarcomes* Médiane (mois) N = 25 8,7 N = 13 21,6 1,62 (0,79, 3,33) 0,115 "Autres STS"* Médiane (mois) N = ,3 N = 61 9,5 0,84 (0,59, 1,21) 0,325 Pourcentage de réponse (CR + PR) % [IC 95 %] Durée de la réponse Médiane (semaines) [IC 95 %] 4 [2,3-7,9) 38,9 [16,7, 40,0) 0 [0,0-3,0) HR = Hazard ratio; ITT = Intention de Traiter; RC = Réponse complète ; RP = Réponse partielle. * La survie globale pour les sous-groupes histologiques de STS respectifs (léiomyosarcome, synovialosarcome et autres STS) doit être interprétée avec prudence en raison du faible nombre de sujets et des intervalles de confiance larges La médiane de survie sans progression (critère principal) a été de 4,6 mois (20 semaines) dans le groupe VOTRIENT versus 1,6 mois (7 semaines) dans le groupe placebo soit une différence absolue de 3 mois en faveur du groupe VOTRIENT ; le Hazard Ratio (HR) ajusté en fonction de l indice de performance OMS et du traitement systémique antérieur a été de 0,35 [0,26 0,48], p<0,001. Les résultats sur le critère principal étaient cohérents entre la population globale et celle des sous groupes. Cependant, le sous groupe histologique synovialosarcome n a comporté que 38 patients au total avec un intervalle de confiance large du hazard ratio, par conséquent l effet du traitement ne peut être considéré comme établi dans ce sous groupe. HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 9/14
10 Résultats sur les critères secondaires : L'analyse finale de la survie globale effectuée à 76% (280/369) des évènements n'a montré aucune différence entre les deux groupes de traitement (HR =0,87, IC 95% [0,67 ; 1,12] p=0,256). Le pourcentage de réponse observé dans le groupe des patients traités par VOTRIENT a été de 4% et de 0% dans le groupe de patients recevant le placebo. Il s agissait exclusivement de réponses partielles. La durée médiane de réponse des patients ayant présenté une réponse partielle dans le groupe VOTRIENT a été de 38,9 semaines et le délai médian de réponse était de 8,4 semaines. Il n a pas été observé de différence entre les deux groupes sur le score global de la qualité de vie. Cependant une détérioration a été observée sur certains symptômes spécifiques tels que la diarrhée, la fatigue et les vomissements. Aucune donnée sur la qualité de vie n a été recueillie chez les patients dont la maladie a progressé ou au-delà de 12 semaines de suivi de l'étude Tolérance/Effets indésirables Les arrêts de traitement pour événements indésirables ont été de 20% dans le groupe VOTRIENT versus 5% dans le groupe placebo. Ces événements étaient principalement des augmentations des ALAT, une dyspnée, un dysfonctionnement ventriculaire gauche, une hypertension artérielle et des vomissements dans le groupe pazopanib. L incidence des événements indésirables de grades 3-4 a été plus élevée dans le groupe VOTRIENT (59%) que dans le groupe placebo (25%). Il s agissait principalement de fatigue, de douleurs tumorales, d hypertension artérielle, de diminution de l appétit, de dyspnée et de diarrhée Résumé & discussion Une étude randomisée, en double aveugle, a comparé le pazopanib (VOTRIENT) à la posologie de 800 mg/jour au placebo, chez 369 patients atteints d un sarcome métastatique des tissus mous hors liposarcome et GIST (tumeurs stromales gastro-intestinales). Tous les patients inclus avaient un état général conservé et 98% avaient préalablement reçu une anthracycline (doxorubicine), 70% de l ifosfamide et 56% des sujets avaient reçu au moins deux lignes de traitement antérieures pour le stade avancé. La médiane de survie sans progression (critère principal) a été plus longue avec VOTRIENT qu avec le placebo (4,6 mois versus 1,6 mois) soit une différence absolue de 3 mois (Hazard Ratio (HR) ajusté en fonction de l indice de performance OMS et du traitement antérieur de 0,35 [0,26 0,48]). Les résultats sur le critère principal étaient cohérents entre la population globale et celle des sous groupes. Cependant, l effet du traitement ne peut être considéré comme établi dans le sous groupe histologique synovialosarcome qui n a comporté que 38 patients au total et dont l intervalle de confiance du hazard ratio est large. L'analyse finale de la survie globale effectuée à 76% (280/369) des événements n'a montré aucune différence entre pazopanib et placebo (HR =0,87, IC 95% [0,67 ; 1,12] p=0,256). Le pourcentage de réponse observé dans le groupe des patients traités par VOTRIENT a été de 4% et de 0% dans le groupe de patients recevant le placebo. Il s agissait exclusivement de réponses partielles. Le score globale de la qualité de vie n a pas été différent entre pazopanib et placebo. Cependant une détérioration a été observée sur certains symptômes spécifiques tels que la diarrhée, la fatigue et les vomissements. Aucune donnée sur la qualité de vie n a été recueillie chez les patients dont la maladie a progressé ou au-delà de 12 semaines de suivi de l'étude. HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 10/14
11 Les arrêts de traitement pour événements indésirables (20% versus 5%) et les événements indésirables de grades 3-4 (59% vs 25%) ont été plus fréquents avec pazopanib qu avec placebo. La toxicité de VOTRIENT a été essentiellement hépatique (élévation des ALAT), digestive (vomissements, diarrhée) et cardiovasculaire (HTA, dysfonctionnement ventriculaire gauche). 08 PLACE DANS LA STRATEGIE THERAPEUTIQUE 1, 2 Au stade localisé du sarcome des tissus mous, le traitement repose principalement sur la chirurgie et la radiothérapie. Le contrôle de la tumeur primitive et la prévention des rechutes locales nécessitent d abord une exérèse chirurgicale complète qui doit avoir aussi pour objectif de préserver la fonction. Le rôle de la chimiothérapie donnée en traitement adjuvant est controversé. Au stade métastatique, le traitement repose sur la chimiothérapie systémique. Les sarcomes des tissus mous sont des tumeurs peu chimiosensibles pour lesquelles un nombre limité de molécules efficaces sont disponibles : les anthracyclines, essentiellement la doxorubicine, l ifosfamide, et la dacarbazine. Ces produits sont utilisés seuls ou en association à la phase métastatique de la maladie ; en première ligne de traitements les pourcentages de réponses varient de 20 à 40% avec des durées de survie médiane de 12 à 18 mois. De nombreuses études randomisées ont permis d établir que : les associations sans anthracyclines sont moins actives que la doxorubicine seule, à dose équivalente de doxorubicine, l adjonction d un deuxième produit donne des taux de réponses parfois supérieurs mais au prix d une plus grande toxicité et sans modifier la survie la sensibilité à la chimiothérapie varie selon les sous types histologiques : les synovialosarcomes ont une sensibilité particulière à l ifosfamide, les liposarcomes indifférenciés sont les plus chimiosensibles, les leiomyosarcomes sont particulièrement sensibles à une association gemcitabine docétaxel, les angiosarcomes ont une sensibilité particulière au paclitaxel hebdomadaire Après échappement à un traitement incluant doxorubicine et ifosfamide en monothérapie ou en association, la trabectédine dispose d une AMM uniquement pour les liposarcomes ou les léiomyosarcomes. VOTRIENT constitue une alternative thérapeutique dans la prise en charge des patients atteints d un sarcome des tissus mous métastatique (hors liposarcome et GIST) en échec à un traitement à base d anthracyclines ou d ifosfamide. HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 11/14
12 09 CONCLUSIONS DE LA COMMISSION Considérant l ensemble de ces informations et après débat et vote, la Commission estime : 09.1 Service Médical Rendu Les sarcomes des tissus mous sont des affections graves qui engagent le pronostic vital ; Ces spécialités entrent dans le cadre d un traitement spécifique du cancer à visée curative ; Le rapport efficacité/effet est important ; Il existe peu d alternatives médicamenteuses à ce stade de la maladie; Il s agit d un traitement de seconde intention et plus après échec d une chimiothérapie à base d anthracyclines ou d ifosfamide ; Intérêt de santé publique : Les sarcomes des tissus mous au stade avancé en échec à une chimiothérapie sont des affections graves pouvant engager le pronostic vital, et altérant de façon significative la qualité de vie des patients mais qui constituent un fardeau de santé publique faible du fait de leur rareté. L amélioration de la prise en charge de ces affections constitue un besoin de santé publique s inscrivant dans le cadre de priorités établies (2ème Plan national Maladie Rares , 2ème Plan Cancer ). Au vu des résultats présentés sur la survie sans progression (gain absolu de 3 mois), il est attendu un impact faible de VOTRIENT sur la morbidité des patients traités. Par ailleurs, au cours de l étude pivot, il n a pas été constaté d amélioration sur la survie globale ni sur la qualité de vie. Les données de qualité de vie sont toutefois difficilement interprétables dans la mesure où elles n ont été évaluées qu à court terme (12 semaines) et en l absence de validation du questionnaire EORTC QLQ-C30 dans cette pathologie. La transposabilité des résultats des essais cliniques à la pratique clinique est acceptable (effectif conséquent de patients français (20%), population incluse représentative des patients vus en pratique médicale). Un impact positif faible sur l organisation des soins est attendu en raison de la substitution possible de chimiothérapies par voie intra veineuse par VOTRIENT voie orale. Ainsi, la spécialité VOTRIENT devrait être en mesure d apporter une réponse partielle au besoin de santé publique identifié. En conséquence, un intérêt de santé publique est attendu pour cette spécialité dans cette indication. Cet intérêt est faible. Compte tenu de ces éléments, la Commission considère que le service médical rendu par VOTRIENT est important dans le traitement des patients adultes présentant des sous-types histologiques spécifiques de sarcome des tissus mous (STS) avancé (hors liposarcome et GIST), qui ont été préalablement traités par chimiothérapie au stade métastatique ou qui ont progressé dans les 12 mois suivant un traitement (neo) adjuvant Amélioration du Service Médical Rendu VOTRIENT apporte une amélioration du service médical rendu mineure (niveau IV) en termes d efficacité par rapport à la stratégie thérapeutique actuelle. HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 12/14
13 09.3 Population cible Les sarcomes sont des tumeurs rares avec une incidence d environ 6 nouveaux cas pour habitants par an, ce qui représente à peu près nouveaux cas estimés par an en France 3. Le calcul de la population cible qui suit repose sur les observations issues de l étude EMS (Rapport EMS 2012), étude prospective recueillant de manière exhaustive tous les cas de sarcomes diagnostiqués entre 2005 et Cette étude EMS a été réalisée en région Rhône-Alpes, qui représente plus de 10% de la population française. L étendue de la population et du territoire couverts par cette étude et le fait que le centre Léon Bérard fasse partie des 3 centres coordonnateurs du NETSARC sont un argument en faveur de la transposabilité de ces données à la prise en charge du sarcome au niveau national. Parmi les sarcomes diagnostiqués annuellement, 56,5% des sarcomes sont des sarcomes des tissus mous. Les sous types histologiques suivants n ont pas été considérés : - les liposarcomes pour lesquels un manque d efficacité a été identifié en phase II, - les GISTs pour lesquels il existe des traitements spécifiques et qui n ont pas été évalués dans l étude de phase III, - les ostéosarcomes qui ne sont pas des sarcomes des tissus mous. Ainsi en France chaque année sont diagnostiqués 2256 sarcomes de tissus mous (hors liposarcomes et hors GISTs). Parmi ces primo diagnostics, 19% sont métastatiques d emblée (n=429) et 26% des patients diagnostiqués avec un STM localisé (n=1827) progresseront vers une maladie métastatique (n=475). Ainsi, 904 cas de STM métastatiques (hors liposarcome et hors GISTs) sont attendus annuellement. En 1 ère ligne métastatique : - 69% des patients reçoivent un traitement systémique soit 624 patients dont 88,5% reçoivent une chimiothérapie soit 552 patients. Parmi lesquels 57,2% atteignent la seconde ligne soit 316 patients. - 31% des patients ne reçoivent pas de traitement systémique car ils ont été traités par anthracyclines en traitement adjuvant ou néoadjuvant et on rechuté dans les 12 mois suivant le traitement rendant impossible la mise en route d un traitement à base d anthracyclines en 1 ère ligne métastatique. Ce qui représente 280 patients Ainsi en considérant : Les patients ne recevant aucun traitement systémique en 1 ère ligne métastatique, n= 280 Les patients recevant un traitement systémique en seconde ligne de traitement n= 316 La population cible de VOTRIENT dans cette indication serait d environ 600 patients par an. 010 RECOMMANDATIONS DE LA COMMISSION La Commission donne un avis favorable à l'inscription de VOTRIENT sur la liste des spécialités remboursables aux assurés sociaux et/ou sur la liste des spécialités agréées à l usage des collectivités dans l indication «traitement des patients adultes présentant des sous-types histologiques spécifiques de sarcome des tissus mous (STS) avancé, qui ont été préalablement traités par chimiothérapie au stade métastatique ou qui ont progressé dans les 12 mois suivant un traitement (neo) adjuvant.» et à la posologie de l AMM. 3 Verhaeghe JL, Rios M, Leroux A, Sirveaux F, Henrot P, Blum A, Marchal F. Traitement des sarcomes des tissus mous de l adulte : quelle stratégie pour optimiser le traitement. e-mémoires de l'académie Nationale de Chirurgie 2011 ; 10 (1) : HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 13/14
14 Conditionnements Ils sont adaptés aux conditions de prescription selon l indication, la posologie et la durée de traitement. Taux de remboursement proposé : 100% HAS - Direction de l'evaluation Médicale, Economique et de Santé Publique 14/14
COMMISSION DE LA TRANSPARENCE. Avis. 23 mai 2007
 COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
COMMISSION DE LA TRANSPARENCE AVIS. 4 novembre 2009
 COMMISSION DE LA TRANSPARENCE AVIS 4 novembre 2009 IRESSA 250 mg, comprimé pelliculé Boîte de 30 (CIP 395 950-7) ASTRAZENECA géfitinib Liste I Médicament soumis à prescription hospitalière. Prescription
COMMISSION DE LA TRANSPARENCE AVIS 4 novembre 2009 IRESSA 250 mg, comprimé pelliculé Boîte de 30 (CIP 395 950-7) ASTRAZENECA géfitinib Liste I Médicament soumis à prescription hospitalière. Prescription
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION. 10 octobre 2001
 COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
COMMISSION DE LA TRANSPARENCE AVIS DE LA COMMISSION 10 octobre 2001 VIRAFERONPEG 50 µg 80 µg 100 µg 120 µg 150 µg, poudre et solvant pour solution injectable B/1 B/4 Laboratoires SCHERING PLOUGH Peginterféron
INTERFERON Traitement adjuvant du mélanome à haut risque de récidive. Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper
 INTERFERON Traitement adjuvant du mélanome à haut risque de récidive Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper Pourquoi proposer un TTT adjuvant? Probabilité de survie à 10 ans en fonction
INTERFERON Traitement adjuvant du mélanome à haut risque de récidive Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper Pourquoi proposer un TTT adjuvant? Probabilité de survie à 10 ans en fonction
COMMISSION DE LA TRANSPARENCE
 COMMISSION DE LA TRANSPARENCE Avis 2 avril 2014 DERMOVAL, gel flacon de 20 ml (CIP : 34009 326 130 4 5) DERMOVAL 0,05 POUR CENT, crème tube de 10 g (CIP : 34009 320 432 9 3) Laboratoire GLAXOSMITHKLINE
COMMISSION DE LA TRANSPARENCE Avis 2 avril 2014 DERMOVAL, gel flacon de 20 ml (CIP : 34009 326 130 4 5) DERMOVAL 0,05 POUR CENT, crème tube de 10 g (CIP : 34009 320 432 9 3) Laboratoire GLAXOSMITHKLINE
Cas clinique 2. Florence JOLY, Caen François IBORRA, Montpellier
 Cas clinique 2 Florence JOLY, Caen François IBORRA, Montpellier Cas clinique Patient de 60 ans, ATCD: HTA, IDM en 2007, hypercholestérolémie Juin 2008: Toux, dyspnée (sous 02) et anorexie progressive Bilan
Cas clinique 2 Florence JOLY, Caen François IBORRA, Montpellier Cas clinique Patient de 60 ans, ATCD: HTA, IDM en 2007, hypercholestérolémie Juin 2008: Toux, dyspnée (sous 02) et anorexie progressive Bilan
Cancer du rein métastatique Nouvelles approches thérapeutiques. Sophie Abadie-Lacourtoisie 20 mai 2006
 Cancer du rein métastatique Nouvelles approches thérapeutiques Sophie Abadie-Lacourtoisie 20 mai 2006 Cancer du rein à cellules claires métastatique (CRM) Plus de 30 % des CR deviendront métastatiques
Cancer du rein métastatique Nouvelles approches thérapeutiques Sophie Abadie-Lacourtoisie 20 mai 2006 Cancer du rein à cellules claires métastatique (CRM) Plus de 30 % des CR deviendront métastatiques
Item 169 : Évaluation thérapeutique et niveau de preuve
 Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
Avis 29 mai 2013. XYZALL 5 mg, comprimé B/14 (CIP : 34009 358 502 4-9) B/28 (CIP : 34009 358 505 3-9) Laboratoire UCB PHARMA SA.
 COMMISSION DE LA TRANSPARENCE Avis 29 mai 2013 XYZALL 5 mg, comprimé B/14 (CIP : 34009 358 502 4-9) B/28 (CIP : 34009 358 505 3-9) Laboratoire UCB PHARMA SA DCI Code ATC (2012) Motif de l examen Liste
COMMISSION DE LA TRANSPARENCE Avis 29 mai 2013 XYZALL 5 mg, comprimé B/14 (CIP : 34009 358 502 4-9) B/28 (CIP : 34009 358 505 3-9) Laboratoire UCB PHARMA SA DCI Code ATC (2012) Motif de l examen Liste
Les nouveaux anticoagulants oraux (NAC)
 Les nouveaux anticoagulants oraux (NAC) Dr Jean-Marie Vailloud Cardiologue libéral/ salarié (CHU/clinique) Pas de lien d'intérêt avec une entreprise pharmaceutique Adhérent à l'association Mieux Prescrire
Les nouveaux anticoagulants oraux (NAC) Dr Jean-Marie Vailloud Cardiologue libéral/ salarié (CHU/clinique) Pas de lien d'intérêt avec une entreprise pharmaceutique Adhérent à l'association Mieux Prescrire
Qu est-ce qu un sarcome?
 Qu est-ce qu un sarcome? Qu est-ce qu une tumeur? Une tumeur est une prolifération anormale de cellules. Les tumeurs ne devraient donc pas automatiquement être associées à un cancer. Certaines tumeurs
Qu est-ce qu un sarcome? Qu est-ce qu une tumeur? Une tumeur est une prolifération anormale de cellules. Les tumeurs ne devraient donc pas automatiquement être associées à un cancer. Certaines tumeurs
Assurance Maladie Obligatoire Commission de la Transparence des médicaments. Avis 1 23 Octobre 2012
 Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 1 23 Octobre 2012 Titre I : Nom du médicament, DCI, Forme pharmaceutique, Dosage, Présentation - ARANESP 10 µg, Darbépoétine
Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 1 23 Octobre 2012 Titre I : Nom du médicament, DCI, Forme pharmaceutique, Dosage, Présentation - ARANESP 10 µg, Darbépoétine
Création de procédures inter-services pour la gestion des essais de phase I à l Institut Gustave Roussy
 Création de procédures inter-services pour la gestion des essais de phase I à l Institut Gustave Roussy A.A. MOUSSA D. SCHWOB Institut de cancérologie Gustave-Roussy 94805 Villejuif cedex - FRANCE Plan
Création de procédures inter-services pour la gestion des essais de phase I à l Institut Gustave Roussy A.A. MOUSSA D. SCHWOB Institut de cancérologie Gustave-Roussy 94805 Villejuif cedex - FRANCE Plan
Essai Inter-groupe : FFCD UNICANCER FRENCH - GERCOR
 CLIMAT - PRODIGE 30 Etude de phase III randomisée évaluant l Intérêt de la colectomie première chez les patients porteurs d un cancer colique asymptomatique avec métastases hépatiques synchrones non résécables
CLIMAT - PRODIGE 30 Etude de phase III randomisée évaluant l Intérêt de la colectomie première chez les patients porteurs d un cancer colique asymptomatique avec métastases hépatiques synchrones non résécables
COMMISSION DE LA TRANSPARENCE AVIS. 18 janvier 2006
 COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
COMMISSION DE LA TRANSPARENCE AVIS 18 janvier 2006 ADVATE 1500 UI, poudre et solvant pour solution injectable 1 flacon(s) en verre de 1 500 UI - 1 flacon(s) en verre de 5 ml avec matériel(s) de perfusion(s)
Recommandations 2005. Prise en charge des patients adultes atteints d un mélanome cutané MO
 Recommandations 2005 Prise en charge des patients adultes atteints d un mélanome cutané MO Recommandations pour la Pratique Clinique : Standards, Options et Recommandations 2005 pour la prise en charge
Recommandations 2005 Prise en charge des patients adultes atteints d un mélanome cutané MO Recommandations pour la Pratique Clinique : Standards, Options et Recommandations 2005 pour la prise en charge
NAVELBINE voie orale
 DENOMINATION DU MEDICAMENT & FORME PHARMACEUTIQUE NAVELBINE voie orale CARACTERISTIQUES Dénomination commune : vinorelbine Composition qualitative et quantitative : Statut : A.M.M. A.T.U. Classe ATC :
DENOMINATION DU MEDICAMENT & FORME PHARMACEUTIQUE NAVELBINE voie orale CARACTERISTIQUES Dénomination commune : vinorelbine Composition qualitative et quantitative : Statut : A.M.M. A.T.U. Classe ATC :
Contenu et format des fichiers téléchargeables de la base de données publique des médicaments. Base de données publique des médicaments
 Contenu et format des fichiers téléchargeables de la base de données publique des médicaments Base de données publique des médicaments Date de mise à jour : 15/12/2014 Table des matières : 1. Présentation
Contenu et format des fichiers téléchargeables de la base de données publique des médicaments Base de données publique des médicaments Date de mise à jour : 15/12/2014 Table des matières : 1. Présentation
Avis 23 avril 2014. BARITEKAL 20 mg/ml, solution injectable Boîte de 10 ampoules de 5 ml (CIP : 34009 585 896 3 8) Laboratoire NORDIC PHARMA
 COMMISSION DE LA TRANSPARENCE Avis 23 avril 2014 BARITEKAL 20 mg/ml, solution injectable Boîte de 10 ampoules de 5 ml (CIP : 34009 585 896 3 8) Laboratoire NORDIC PHARMA DCI Code ATC (2012) Motif de l
COMMISSION DE LA TRANSPARENCE Avis 23 avril 2014 BARITEKAL 20 mg/ml, solution injectable Boîte de 10 ampoules de 5 ml (CIP : 34009 585 896 3 8) Laboratoire NORDIC PHARMA DCI Code ATC (2012) Motif de l
COMMISSION DE LA TRANSPARENCE AVIS. 7 janvier 2009
 COMMISSION DE LA TRANSPARENCE AVIS 7 janvier 2009 ZANEXTRA 20 mg/10 mg, comprimés pelliculés B/30, code CIP : 385 967.4 B/90, code CIP : 387 392.9 Laboratoires BOUCHARA RECORDATI Enalapril/Lercanidipine
COMMISSION DE LA TRANSPARENCE AVIS 7 janvier 2009 ZANEXTRA 20 mg/10 mg, comprimés pelliculés B/30, code CIP : 385 967.4 B/90, code CIP : 387 392.9 Laboratoires BOUCHARA RECORDATI Enalapril/Lercanidipine
Suivi ADOM. Claude Boiron Oncologie Médicale
 Suivi ADOM Claude Boiron Oncologie Médicale PLAN 1. Problématiques du traitement anti cancéreux per os 2. Objectifs du suivi ADOM 3. Procédures 4. Bilan Étude observationnelle Étude médico économique Étude
Suivi ADOM Claude Boiron Oncologie Médicale PLAN 1. Problématiques du traitement anti cancéreux per os 2. Objectifs du suivi ADOM 3. Procédures 4. Bilan Étude observationnelle Étude médico économique Étude
COMMISSION DE LA TRANSPARENCE. Avis. 10 mars 2010
 COMMISSION DE LA TRANSPARENCE Avis 10 mars 2010 ARIXTRA 1,5 mg/0,3 ml, solution injectable en seringue pré-remplie - Boîte de 2 (CIP : 363 500-6) - Boîte de 7 (CIP : 363 501-2) - Boîte de 10 (CIP : 564
COMMISSION DE LA TRANSPARENCE Avis 10 mars 2010 ARIXTRA 1,5 mg/0,3 ml, solution injectable en seringue pré-remplie - Boîte de 2 (CIP : 363 500-6) - Boîte de 7 (CIP : 363 501-2) - Boîte de 10 (CIP : 564
COMMISSION DE LA TRANSPARENCE. AVIS 1 er février 2012
 COMMISSION DE LA TRANSPARENCE AVIS 1 er février 2012 Le projet d avis adopté par la Commission de la Transparence le 16 novembre 2011 a fait l objet d une audition le 1 février 2012 XEPLION 25 mg, suspension
COMMISSION DE LA TRANSPARENCE AVIS 1 er février 2012 Le projet d avis adopté par la Commission de la Transparence le 16 novembre 2011 a fait l objet d une audition le 1 février 2012 XEPLION 25 mg, suspension
REFERENTIEL D AUTO-EVALUATION DES PRATIQUES EN ODONTOLOGIE
 REFERENTIEL D AUTO-EVALUATION DES PRATIQUES EN ODONTOLOGIE Janvier 2006 I. PROMOTEURS Association dentaire française (ADF). Haute Autorité de santé (HAS). II. SOURCE Agence nationale d accréditation et
REFERENTIEL D AUTO-EVALUATION DES PRATIQUES EN ODONTOLOGIE Janvier 2006 I. PROMOTEURS Association dentaire française (ADF). Haute Autorité de santé (HAS). II. SOURCE Agence nationale d accréditation et
CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE
 CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE BAXTER_CLINIMIX N9G15 E et N12G20E_Avis CT_14-02-2007.pdf BAXTER_CLINIMIX N9G15E N12G20E N14G30 N17G35_Avis CT_12-12-2001.pdf BAXTER_CLINIMIX changement
CLINIMIX AVIS DE LA COMMISSION DE LA TRANSPARENCE BAXTER_CLINIMIX N9G15 E et N12G20E_Avis CT_14-02-2007.pdf BAXTER_CLINIMIX N9G15E N12G20E N14G30 N17G35_Avis CT_12-12-2001.pdf BAXTER_CLINIMIX changement
Validation clinique des marqueurs prédictifs le point de vue du méthodologiste. Michel Cucherat UMR CNRS 5558 - Lyon
 Validation clinique des marqueurs prédictifs le point de vue du méthodologiste Michel Cucherat UMR CNRS 5558 - Lyon Marqueur prédictif - Définition Un marqueur prédictif est un marqueur qui prédit le bénéfice
Validation clinique des marqueurs prédictifs le point de vue du méthodologiste Michel Cucherat UMR CNRS 5558 - Lyon Marqueur prédictif - Définition Un marqueur prédictif est un marqueur qui prédit le bénéfice
27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013
 27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013 Les Nouveaux Anticoagulants Oraux (NACO) dans la maladie thrombo embolique veineuse INTRODUCTION Thrombose veineuse
27 ème JOURNEE SPORT ET MEDECINE Dr Roukos ABI KHALIL Digne Les Bains 23 novembre 2013 Les Nouveaux Anticoagulants Oraux (NACO) dans la maladie thrombo embolique veineuse INTRODUCTION Thrombose veineuse
Le RIVAROXABAN (XARELTO ) dans l embolie pulmonaire
 Le RIVAROXABAN (XARELTO ) dans l embolie pulmonaire Dr Florence Parent Service de Pneumologie et Soins Intensifs de Pneumologie Hôpital Bicêtre, AP-HP Inserm U999. Université Paris-Sud Traitement anticoagulant
Le RIVAROXABAN (XARELTO ) dans l embolie pulmonaire Dr Florence Parent Service de Pneumologie et Soins Intensifs de Pneumologie Hôpital Bicêtre, AP-HP Inserm U999. Université Paris-Sud Traitement anticoagulant
COMMISSION DE LA TRANSPARENCE AVIS. 10 mai 2006
 COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
COMMISSION DE LA TRANSPARENCE AVIS 10 mai 2006 METOJECT 10 mg/ml, solution injectable en seringue pré-remplie 1 seringue pré-remplie en verre de 0,75 ml avec aiguille : 371 754-3 1 seringue pré- remplie
ALK et cancers broncho-pulmonaires. Laurence Bigay-Gamé Unité d oncologie thoracique Hôpital Larrey, Toulouse
 ALK et cancers broncho-pulmonaires Laurence Bigay-Gamé Unité d oncologie thoracique Hôpital Larrey, Toulouse Toulouse, le 19 Février 2013 Adénocarcinomes : Lung Cancer Mutation Consortium Identification
ALK et cancers broncho-pulmonaires Laurence Bigay-Gamé Unité d oncologie thoracique Hôpital Larrey, Toulouse Toulouse, le 19 Février 2013 Adénocarcinomes : Lung Cancer Mutation Consortium Identification
COMMISSION DE LA TRANSPARENCE AVIS. 1 er octobre 2008
 COMMISSION DE LA TRANSPARENCE AVIS 1 er octobre 2008 Examen dans le cadre de la réévaluation du service médical rendu de la classe des IMAO B, en application de l article R 163-21 du code de la sécurité
COMMISSION DE LA TRANSPARENCE AVIS 1 er octobre 2008 Examen dans le cadre de la réévaluation du service médical rendu de la classe des IMAO B, en application de l article R 163-21 du code de la sécurité
Épidémiologie des accidents hémorragiques dus aux anticoagulants oraux
 Épidémiologie des accidents hémorragiques dus aux anticoagulants oraux Docteur Marie-Josèphe JEAN-PASTOR Centre Régional Pharmacovigilance Marseille-Provence-Corse Hôpital Sainte Marguerite AP-HM Tél :
Épidémiologie des accidents hémorragiques dus aux anticoagulants oraux Docteur Marie-Josèphe JEAN-PASTOR Centre Régional Pharmacovigilance Marseille-Provence-Corse Hôpital Sainte Marguerite AP-HM Tél :
ESMO 14. L oncogériatrie d un coup d éventail! Dr Elisabeth Carola UCOG Picardie
 ESMO 14 L oncogériatrie d un coup d éventail! Dr Elisabeth Carola UCOG Picardie Cancer du SEIN Taxotere hebdo pas mieux et plus toxique Perrone F et al Ann Oncol 2014 Phase III : CMF vs Taxotere hebdo
ESMO 14 L oncogériatrie d un coup d éventail! Dr Elisabeth Carola UCOG Picardie Cancer du SEIN Taxotere hebdo pas mieux et plus toxique Perrone F et al Ann Oncol 2014 Phase III : CMF vs Taxotere hebdo
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
Plan. Introduction. Les Nouveaux Anticoagulants Oraux et le sujet âgé. Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or
 Plan Introduction Les Nouveaux Anticoagulants Oraux et le sujet âgé Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or Introduction NACO: une actualité brûlante! AVK: Plus forte incidence
Plan Introduction Les Nouveaux Anticoagulants Oraux et le sujet âgé Audit de prescription au Centre Hospitalier Geriatrique du Mont d Or Introduction NACO: une actualité brûlante! AVK: Plus forte incidence
Association pour le soutien des personnes touchées par les GIST en Suisse
 GIST Groupe Suisse Association pour le soutien des personnes touchées par les GIST en Suisse Statuts 1. Nom et siège Le nom «Association pour le soutien des personnes touchées par les GIST en Suisse» désigne
GIST Groupe Suisse Association pour le soutien des personnes touchées par les GIST en Suisse Statuts 1. Nom et siège Le nom «Association pour le soutien des personnes touchées par les GIST en Suisse» désigne
Assurance Maladie Obligatoire Commission de la Transparence des médicaments. Avis 2 23 Octobre 2012
 Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 2 23 Octobre 2012 Titre I : Nom du médicament, DCI, forme pharmaceutique, dosage, présentation HUMIRA (DCI : Adalimumab
Assurance Maladie Obligatoire Commission de la Transparence des médicaments Avis 2 23 Octobre 2012 Titre I : Nom du médicament, DCI, forme pharmaceutique, dosage, présentation HUMIRA (DCI : Adalimumab
EVALUATION DES TECHNOLOGIES DE SANTÉ ANALYSE MÉDICO-ÉCONOMIQUE. Efficacité et efficience des hypolipémiants Une analyse centrée sur les statines
 EVALUATION DES TECHNOLOGIES DE SANTÉ ANALYSE MÉDICO-ÉCONOMIQUE Efficacité et efficience des hypolipémiants Une analyse centrée sur les statines Juillet 2010 Mise à jour Septembre 2010 1 Le rapport complet
EVALUATION DES TECHNOLOGIES DE SANTÉ ANALYSE MÉDICO-ÉCONOMIQUE Efficacité et efficience des hypolipémiants Une analyse centrée sur les statines Juillet 2010 Mise à jour Septembre 2010 1 Le rapport complet
ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER
 ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER Dr Michael Hummelsberger, Pr Jean-Gabriel Fuzibet, Service de Médecine Interne, Hôpital l Archet, CHU Nice 1. ANEMIE L étiologie de l anémie
ANEMIE ET THROMBOPENIE CHEZ LES PATIENTS ATTEINTS D UN CANCER Dr Michael Hummelsberger, Pr Jean-Gabriel Fuzibet, Service de Médecine Interne, Hôpital l Archet, CHU Nice 1. ANEMIE L étiologie de l anémie
Nouveaux anticoagulants oraux : aspects pratiques
 Nouveaux anticoagulants oraux : aspects pratiques Christelle MARQUIE CHRU de Lille Clinique de Cardiologie L i l l e 2 Université du Droit et de la Santé Les NOAG: QCM 1. ont les mêmes indications que
Nouveaux anticoagulants oraux : aspects pratiques Christelle MARQUIE CHRU de Lille Clinique de Cardiologie L i l l e 2 Université du Droit et de la Santé Les NOAG: QCM 1. ont les mêmes indications que
COMMISSION DE LA TRANSPARENCE AVIS. 14 mars 2012
 COMMISSION DE LA TRANSPARENCE AVIS 14 mars 2012 XARELTO 15 mg, comprimés pelliculés B/14 (CIP: 34009 219 225 1 6) B/28 (CIP: 34009 219 226 8 4) B/42 (CIP: 34009 219 227 4 5) B/10 (CIP: 34009 219 228 0
COMMISSION DE LA TRANSPARENCE AVIS 14 mars 2012 XARELTO 15 mg, comprimés pelliculés B/14 (CIP: 34009 219 225 1 6) B/28 (CIP: 34009 219 226 8 4) B/42 (CIP: 34009 219 227 4 5) B/10 (CIP: 34009 219 228 0
Pharmacologie des «nouveaux» anticoagulants oraux
 Pharmacologie des «nouveaux» anticoagulants oraux Apixaban, Dabigatran, Rivaroxaban Pr D. DEPLANQUE Département de Pharmacologie médicale EA 1046 et CIC 9301 INSERM-CHRU, Institut de Médecine Prédictive
Pharmacologie des «nouveaux» anticoagulants oraux Apixaban, Dabigatran, Rivaroxaban Pr D. DEPLANQUE Département de Pharmacologie médicale EA 1046 et CIC 9301 INSERM-CHRU, Institut de Médecine Prédictive
Essais précoces non comparatifs : principes et calcul du nombre de sujets nécessaire
 Essais précoces non comparatifs : principes et calcul du nombre de sujets nécessaire Sylvie CHABAUD Direction de la Recherche Clinique et de l Innovation : Centre Léon Bérard - Lyon Unité de Biostatistique
Essais précoces non comparatifs : principes et calcul du nombre de sujets nécessaire Sylvie CHABAUD Direction de la Recherche Clinique et de l Innovation : Centre Léon Bérard - Lyon Unité de Biostatistique
Annick.robinson@merck.com dquirion@national.ca 514 428-2890 514 843-2302
 Communiqué de presse Relations avec les médias : Annick Robinson Dominique Quirion Merck NATIONAL Annick.robinson@merck.com dquirion@national.ca 514 428-2890 514 843-2302 Relations avec les investisseurs
Communiqué de presse Relations avec les médias : Annick Robinson Dominique Quirion Merck NATIONAL Annick.robinson@merck.com dquirion@national.ca 514 428-2890 514 843-2302 Relations avec les investisseurs
Fiche Produit Profils Médicalisés PHMEV
 Guide méthodologique développé par l équipe de projets ci-dessous : Fiche Produit Profils Médicalisés PHMEV EQUIPE PROJET Chef de projet : Maryline CHARRA, Pharmacien Conseil Responsable de la mission
Guide méthodologique développé par l équipe de projets ci-dessous : Fiche Produit Profils Médicalisés PHMEV EQUIPE PROJET Chef de projet : Maryline CHARRA, Pharmacien Conseil Responsable de la mission
Innovations thérapeutiques en transplantation
 Innovations thérapeutiques en transplantation 3èmes Assises de transplantation pulmonaire de la région Est Le 16 octobre 2010 Dr Armelle Schuller CHU Strasbourg Etat des lieux en transplantation : 2010
Innovations thérapeutiques en transplantation 3èmes Assises de transplantation pulmonaire de la région Est Le 16 octobre 2010 Dr Armelle Schuller CHU Strasbourg Etat des lieux en transplantation : 2010
ELABORATION DU PLAN DE MONITORING ADAPTE POUR UNE RECHERCHE BIOMEDICALE A PROMOTION INSTITUTIONNELLE
 Référence HCL : Titre de l étude : ELABORATION DU PLAN DE MONITORING ADAPTE POUR UNE RECHERCHE BIOMEDICALE A PROMOTION INSTITUTIONNELLE Investigateur Coordonnateur : Méthode. Définition du niveau de risque
Référence HCL : Titre de l étude : ELABORATION DU PLAN DE MONITORING ADAPTE POUR UNE RECHERCHE BIOMEDICALE A PROMOTION INSTITUTIONNELLE Investigateur Coordonnateur : Méthode. Définition du niveau de risque
COMMISSION DE LA TRANSPARENCE AVIS. 14 mars 2012
 COMMISSION DE LA TRANSPARENCE AVIS 14 mars 2012 XARELTO 15 mg, comprimés pelliculés B/14 (CIP: 34009 219 225 1 6) B/28 (CIP: 34009 219 226 8 4) B/42 (CIP: 34009 219 227 4 5) B/10 (CIP: 34009 219 228 0
COMMISSION DE LA TRANSPARENCE AVIS 14 mars 2012 XARELTO 15 mg, comprimés pelliculés B/14 (CIP: 34009 219 225 1 6) B/28 (CIP: 34009 219 226 8 4) B/42 (CIP: 34009 219 227 4 5) B/10 (CIP: 34009 219 228 0
Les défibrillateurs cardiaques implantables
 Les défibrillateurs cardiaques implantables Etudes d'évaluation économique Etudes d'évaluation technologique Avant-propos Cette étude a été réalisée, à la demande de la Caisse Nationale de l'assurance
Les défibrillateurs cardiaques implantables Etudes d'évaluation économique Etudes d'évaluation technologique Avant-propos Cette étude a été réalisée, à la demande de la Caisse Nationale de l'assurance
Programme AcSé. Accès Sécurisé aux Innovations Thérapeutiques Deux études pilotes : AcSé - crizotinib et AcSé - vémurafenib
 Programme AcSé Accès Sécurisé aux Innovations Thérapeutiques Deux études pilotes : AcSé - crizotinib et AcSé - vémurafenib G. Vassal, J.Y. Blay, C. Cailliot, N. Hoog-Labouret, F. Denjean, M. Jimenez, A.L.
Programme AcSé Accès Sécurisé aux Innovations Thérapeutiques Deux études pilotes : AcSé - crizotinib et AcSé - vémurafenib G. Vassal, J.Y. Blay, C. Cailliot, N. Hoog-Labouret, F. Denjean, M. Jimenez, A.L.
COMMISSION DE LA TRANSPARENCE. 10 décembre 2008
 COMMISSION DE LA TRANSPARENCE AVIS 10 décembre 2008 VIRAFERONPEG 50 µg/ 0.5 ml, poudre et solvant pour solution injectable B/1 : code CIP 355 189.3 B/4 : code CIP 355 191.8 VIRAFERONPEG, stylo pré-rempli
COMMISSION DE LA TRANSPARENCE AVIS 10 décembre 2008 VIRAFERONPEG 50 µg/ 0.5 ml, poudre et solvant pour solution injectable B/1 : code CIP 355 189.3 B/4 : code CIP 355 191.8 VIRAFERONPEG, stylo pré-rempli
Assurance maladie grave
 ASSURANCE COLLECTIVE Le complément idéal à votre assurance collective Assurance maladie grave Votre partenaire de confiance. Assurance maladie grave La tranquillité d esprit à votre portée Les progrès
ASSURANCE COLLECTIVE Le complément idéal à votre assurance collective Assurance maladie grave Votre partenaire de confiance. Assurance maladie grave La tranquillité d esprit à votre portée Les progrès
COMMISSION DE LA TRANSPARENCE AVIS. 18 novembre 2009
 COMMISSION DE LA TRANSPARENCE AVIS 18 novembre 2009 LEDERTREXATE 5 mg, solution injectable B/1 ampoule de 2 ml (Code CIP : 315 012-5) LEDERTREXATE 25 mg, solution injectable B/1 ampoule de 1 ml (Code CIP
COMMISSION DE LA TRANSPARENCE AVIS 18 novembre 2009 LEDERTREXATE 5 mg, solution injectable B/1 ampoule de 2 ml (Code CIP : 315 012-5) LEDERTREXATE 25 mg, solution injectable B/1 ampoule de 1 ml (Code CIP
GUSTAVE ROUSSY À L ASCO
 GUSTAVE ROUSSY À L COMMUNIQUÉ DE PRESSE 29 MAI 02 JUIN THÉRAPIES CIBLÉES www.gustaveroussy.fr/asco Communiqué de presse Gustave Roussy au 51 e congrès de l American Society of Clinical Oncology THÉRAPIES
GUSTAVE ROUSSY À L COMMUNIQUÉ DE PRESSE 29 MAI 02 JUIN THÉRAPIES CIBLÉES www.gustaveroussy.fr/asco Communiqué de presse Gustave Roussy au 51 e congrès de l American Society of Clinical Oncology THÉRAPIES
COMMISSION DE LA TRANSPARENCE AVIS. 31 janvier 2007
 COMMISSION DE LA TRANSPARENCE AVIS 31 janvier 2007 NEUPRO 2 mg/24 h dispositif transdermique Sachet-dose, B/30 : 377 209-7 Sachet-dose, B/90 : 570 143-4 NEUPRO 4 mg/24 h dispositif transdermique Sachet-dose,
COMMISSION DE LA TRANSPARENCE AVIS 31 janvier 2007 NEUPRO 2 mg/24 h dispositif transdermique Sachet-dose, B/30 : 377 209-7 Sachet-dose, B/90 : 570 143-4 NEUPRO 4 mg/24 h dispositif transdermique Sachet-dose,
Avis 17 octobre 2012
 COMMISSION DE LA TRANSPARENCE Avis 17 octobre 2012 BETESIL 2,25 mg, emplâtre médicamenteux Boite de 8 emplâtres médicamenteux en sachets (CIP : 34009 377 977 4 0) Laboratoire GENEVRIER DCI Code ATC (2012)
COMMISSION DE LA TRANSPARENCE Avis 17 octobre 2012 BETESIL 2,25 mg, emplâtre médicamenteux Boite de 8 emplâtres médicamenteux en sachets (CIP : 34009 377 977 4 0) Laboratoire GENEVRIER DCI Code ATC (2012)
clinique d un médicament
 DU Recherche Clinique Calcul du nombre de sujets nécessaires (accent sur les phases III) S. THEZENAS I.C.M. (Ex CRLC Val d Aurelle) Unité de Biostatistiques Phases du développement clinique d un médicament
DU Recherche Clinique Calcul du nombre de sujets nécessaires (accent sur les phases III) S. THEZENAS I.C.M. (Ex CRLC Val d Aurelle) Unité de Biostatistiques Phases du développement clinique d un médicament
Format de l avis d efficience
 AVIS D EFFICIENCE Format de l avis d efficience Juillet 2013 Commission évaluation économique et de santé publique Ce document est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service documentation
AVIS D EFFICIENCE Format de l avis d efficience Juillet 2013 Commission évaluation économique et de santé publique Ce document est téléchargeable sur www.has-sante.fr Haute Autorité de santé Service documentation
Rapport sur les nouveaux médicaments brevetés Iressa
 Rapport sur les nouveaux médicaments brevetés Iressa Au titre de son initiative de transparence, le CEPMB publie les résultats des examens des prix des nouveaux médicaments brevetés effectués par les membres
Rapport sur les nouveaux médicaments brevetés Iressa Au titre de son initiative de transparence, le CEPMB publie les résultats des examens des prix des nouveaux médicaments brevetés effectués par les membres
Traitements néoadjuvants des cancers du rectum. Pr. G. Portier CHU Purpan - Toulouse
 Traitements néoadjuvants des cancers du rectum Pr. G. Portier CHU Purpan - Toulouse Journées Francophones d Hépato-gastroentérologie et d Oncologie Digestive 2010 CONFLITS D INTÉRÊT Pas de conflit d intérêt
Traitements néoadjuvants des cancers du rectum Pr. G. Portier CHU Purpan - Toulouse Journées Francophones d Hépato-gastroentérologie et d Oncologie Digestive 2010 CONFLITS D INTÉRÊT Pas de conflit d intérêt
Les facteurs de croissance lignée blanche Polynucléaires neutrophiles Grastims
 Les facteurs de croissance lignée blanche Polynucléaires neutrophiles Grastims 12 2014 HEMATOPOIESE Progéniteurs puis précurseurs Stimulation par facteur : activation spécifique de leur récepteur Moelle
Les facteurs de croissance lignée blanche Polynucléaires neutrophiles Grastims 12 2014 HEMATOPOIESE Progéniteurs puis précurseurs Stimulation par facteur : activation spécifique de leur récepteur Moelle
LES NOUVEAUX ANTICOAGULANTS
 LES NOUVEAUX ANTICOAGULANTS Pr. Alessandra Bura-Rivière, Service de Médecine Vasculaire Hôpital Rangueil, 1 avenue Jean Poulhès, 31059 Toulouse cedex 9 INTRODUCTION Depuis plus de cinquante ans, les héparines
LES NOUVEAUX ANTICOAGULANTS Pr. Alessandra Bura-Rivière, Service de Médecine Vasculaire Hôpital Rangueil, 1 avenue Jean Poulhès, 31059 Toulouse cedex 9 INTRODUCTION Depuis plus de cinquante ans, les héparines
Cancer bronchique primitif: données épidémiologiques récentes
 Cancer bronchique primitif: données épidémiologiques récentes Pr Jean Trédaniel Service de pneumologie et oncologie thoracique Groupe Hospitalier Paris Saint Joseph Université Paris Descartes Sources Données
Cancer bronchique primitif: données épidémiologiques récentes Pr Jean Trédaniel Service de pneumologie et oncologie thoracique Groupe Hospitalier Paris Saint Joseph Université Paris Descartes Sources Données
Placebo Effet Placebo. Pr Claire Le Jeunne Hôtel Dieu- Médecine Interne et Thérapeutique Faculté de Médecine Paris Descartes
 Placebo Effet Placebo Pr Claire Le Jeunne Hôtel Dieu- Médecine Interne et Thérapeutique Faculté de Médecine Paris Descartes Plan Définitions Placebo dans les essais thérapeutiques Effet placebo Médicaments
Placebo Effet Placebo Pr Claire Le Jeunne Hôtel Dieu- Médecine Interne et Thérapeutique Faculté de Médecine Paris Descartes Plan Définitions Placebo dans les essais thérapeutiques Effet placebo Médicaments
Votre guide des définitions des maladies graves de l Assurance maladies graves express
 Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
COMMISSION DE LA TRANSPARENCE. Avis. 3 septembre 2008
 COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
COMMISSION DE LA TRANSPARENCE Avis 3 septembre 2008 PRIVIGEN 100 mg/ml, solution pour perfusion Flacon en verre de 50 ml (CIP: 572 790-7 Flacon en verre de 100 ml (CIP: 572 791-3) Flacon en verre de 200
Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA. Doctorant: Camelia MICU (DEMETRIAN)
 UNIVERSITÉ DE MÉDECINE ET PHARMACIE DE CRAIOVA FACULTÉ DE MÉDECINE CONTRIBUTIONS A L'ÉTUDE CLINIQUE ET MORPHOLOGIQUE DES CANCERS DU POUMON Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA Doctorant:
UNIVERSITÉ DE MÉDECINE ET PHARMACIE DE CRAIOVA FACULTÉ DE MÉDECINE CONTRIBUTIONS A L'ÉTUDE CLINIQUE ET MORPHOLOGIQUE DES CANCERS DU POUMON Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA Doctorant:
Deux nouveaux anticoagulants oraux : Dabigatran et Rivaroxaban
 Deux nouveaux anticoagulants oraux : Dabigatran et Rivaroxaban Améliorations attendues et problèmes M.M. Samama, M-H. Horellou, J. Conard Groupe Hémostase-Thrombose Hôtel-Dieu L. Le Flem, C. Guinet, F.
Deux nouveaux anticoagulants oraux : Dabigatran et Rivaroxaban Améliorations attendues et problèmes M.M. Samama, M-H. Horellou, J. Conard Groupe Hémostase-Thrombose Hôtel-Dieu L. Le Flem, C. Guinet, F.
Avis 6 novembre 2013
 COMMISSION DE LA TRANSPARENCE Avis 6 novembre 2013 ISENTRESS, comprimé à croquer 25 mg Flacon de 60 comprimés (CIP : 3400926992408) ISENTRESS, comprimé à croquer sécable 100 mg Flacon de 60 comprimés (CIP
COMMISSION DE LA TRANSPARENCE Avis 6 novembre 2013 ISENTRESS, comprimé à croquer 25 mg Flacon de 60 comprimés (CIP : 3400926992408) ISENTRESS, comprimé à croquer sécable 100 mg Flacon de 60 comprimés (CIP
Traitement de l insuffisance rénale chronique terminale: Place de la greffe de donneur vivant
 Traitement de l insuffisance rénale chronique terminale: Place de la greffe de donneur vivant Pr Maryvonne Hourmant Service de Néphrologie-Immunologie clinique. CHU de Nantes Le constat Coût du traitement
Traitement de l insuffisance rénale chronique terminale: Place de la greffe de donneur vivant Pr Maryvonne Hourmant Service de Néphrologie-Immunologie clinique. CHU de Nantes Le constat Coût du traitement
Les soins infirmiers en oncologie : une carrière faite pour vous! Nom de la Présentatrice et section de l'acio
 Les soins infirmiers en oncologie : une carrière faite pour vous! Nom de la Présentatrice et section de l'acio Grandes lignes Pourquoi les soins en cancérologie sont-ils un enjeu de santé important? Les
Les soins infirmiers en oncologie : une carrière faite pour vous! Nom de la Présentatrice et section de l'acio Grandes lignes Pourquoi les soins en cancérologie sont-ils un enjeu de santé important? Les
COMMISSION DE LA TRANSPARENCE AVIS. 23 mai 2012
 COMMISSION DE LA TRANSPARENCE AVIS 23 mai 2012 SEGLOR 5 mg, gélule B/30 (CIP: 321 899-8) SEGLOR LYOC 5 mg, lyophilisat oral B/30 (CIP: 334 062-4) Laboratoire UCB PHARMA dihydroergotamine (mésilate de)
COMMISSION DE LA TRANSPARENCE AVIS 23 mai 2012 SEGLOR 5 mg, gélule B/30 (CIP: 321 899-8) SEGLOR LYOC 5 mg, lyophilisat oral B/30 (CIP: 334 062-4) Laboratoire UCB PHARMA dihydroergotamine (mésilate de)
Point d Information. Le PRAC a recommandé que le RCP soit modifié afin d inclure les informations suivantes:
 Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Point d Information Médicaments à base d ivabradine, de codéine, médicaments contenant du diméthyl fumarate, du mycophénolate mofétil/acide mycophénolique, de l octocog alpha, spécialité Eligard (contenant
Audit et Inspection Les contraintes extérieures B.Malivoir
 Audit et Inspection Les contraintes extérieures B.Malivoir Chef de projet Hémato-Onco CHRU Tours Vice Présidente CPP Région Ouest1 Le contexte juridique Directive 2001/20/CE du Parlement européen et du
Audit et Inspection Les contraintes extérieures B.Malivoir Chef de projet Hémato-Onco CHRU Tours Vice Présidente CPP Région Ouest1 Le contexte juridique Directive 2001/20/CE du Parlement européen et du
Révision des descriptions génériques Comment monter un dossier?
 DISPOSITIFS MEDICAUX Révision des descriptions génériques Comment monter un dossier? Guide pour le dossier déposé par les fabricants/distributeurs Adopté en séance de la CEPP* le 13 juillet 2005 *CEPP
DISPOSITIFS MEDICAUX Révision des descriptions génériques Comment monter un dossier? Guide pour le dossier déposé par les fabricants/distributeurs Adopté en séance de la CEPP* le 13 juillet 2005 *CEPP
Spondylarthropathies : diagnostic, place des anti-tnf et surveillance par le généraliste. Pr P. Claudepierre CHU Henri Mondor - Créteil
 Spondylarthropathies : diagnostic, place des anti-tnf et surveillance par le généraliste Pr P. Claudepierre CHU Henri Mondor - Créteil Le Diagnostic Objectif de la démarche diagnostique Diagnostic de SPONDYLARTHROPATHIE
Spondylarthropathies : diagnostic, place des anti-tnf et surveillance par le généraliste Pr P. Claudepierre CHU Henri Mondor - Créteil Le Diagnostic Objectif de la démarche diagnostique Diagnostic de SPONDYLARTHROPATHIE
Les nouveaux anticoagulants oraux sont arrivé! Faut il une surveillance biologique?
 Les nouveaux anticoagulants oraux sont arrivé! Faut il une surveillance biologique? Références : Pr Samama Journée de Biologie Praticienne Décembre 2011 I. Gouin-Thibault Journée de Biologie Clinique 2012
Les nouveaux anticoagulants oraux sont arrivé! Faut il une surveillance biologique? Références : Pr Samama Journée de Biologie Praticienne Décembre 2011 I. Gouin-Thibault Journée de Biologie Clinique 2012
Principe d un test statistique
 Biostatistiques Principe d un test statistique Professeur Jean-Luc BOSSON PCEM2 - Année universitaire 2012/2013 Faculté de Médecine de Grenoble (UJF) - Tous droits réservés. Objectifs pédagogiques Comprendre
Biostatistiques Principe d un test statistique Professeur Jean-Luc BOSSON PCEM2 - Année universitaire 2012/2013 Faculté de Médecine de Grenoble (UJF) - Tous droits réservés. Objectifs pédagogiques Comprendre
Les tests de génétique moléculaire pour l accès aux thérapies ciblées en France en 2011
 Mesure 21 SOINS ET VIE DES MALADES Les tests de génétique moléculaire pour l accès aux thérapies ciblées en France en 2011 COLLECTION Rapports & synthèses POUR UN ACCÈS AUX THÉRAPIES CIBLÉES : - LES PLATEFORMES
Mesure 21 SOINS ET VIE DES MALADES Les tests de génétique moléculaire pour l accès aux thérapies ciblées en France en 2011 COLLECTION Rapports & synthèses POUR UN ACCÈS AUX THÉRAPIES CIBLÉES : - LES PLATEFORMES
Pemetrexed, pionnier de la chimiothérapie histoguidée. Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var
 Pemetrexed, pionnier de la chimiothérapie histoguidée Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var SFPO Octobre 2009 EPIDEMIOLOGIE Incidence : 1.35 M par an dans le monde (12,4%) 28 000
Pemetrexed, pionnier de la chimiothérapie histoguidée Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var SFPO Octobre 2009 EPIDEMIOLOGIE Incidence : 1.35 M par an dans le monde (12,4%) 28 000
TUMEURS DU BAS APPAREIL URINAIRE
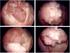 1 Plan de cours I - TUMEURS PRIMITIVES DE LA VESSIE c1 - Tumeurs papillaires non infiltrantes c2 - Tumeurs papillaires infiltrantes c3 - Carcinome in-situ en muqueuse plane D - Pronostic : II - TUMEURS
1 Plan de cours I - TUMEURS PRIMITIVES DE LA VESSIE c1 - Tumeurs papillaires non infiltrantes c2 - Tumeurs papillaires infiltrantes c3 - Carcinome in-situ en muqueuse plane D - Pronostic : II - TUMEURS
COMMISSION DE LA TRANSPARENCE
 COMMISSION DE LA TRANSPARENCE Avis 17 décembre 2014 ELIQUIS 2,5 mg, comprimés pelliculés B/60 (CIP : 34009 419 456 7 0) B/60 blister unitaire (CIP : 34009 419 457 3 1) ELIQUIS 5 mg, comprimés pelliculés
COMMISSION DE LA TRANSPARENCE Avis 17 décembre 2014 ELIQUIS 2,5 mg, comprimés pelliculés B/60 (CIP : 34009 419 456 7 0) B/60 blister unitaire (CIP : 34009 419 457 3 1) ELIQUIS 5 mg, comprimés pelliculés
INSUFFISANCE CARDIAQUE «AU FIL DES ANNEES»
 INSUFFISANCE CARDIAQUE «AU FIL DES ANNEES» v On ne guérit pas ( en général ) d une insuffisance cardiaque, mais on peut la stabiliser longtemps, très longtemps à condition v Le patient insuffisant cardiaque
INSUFFISANCE CARDIAQUE «AU FIL DES ANNEES» v On ne guérit pas ( en général ) d une insuffisance cardiaque, mais on peut la stabiliser longtemps, très longtemps à condition v Le patient insuffisant cardiaque
Essais cliniques de phase 0 : état de la littérature 2006-2009
 17 èmes Journées des Statisticiens des Centres de Lutte contre le Cancer 4 ème Conférence Francophone d Epidémiologie Clinique Essais cliniques de phase 0 : état de la littérature 2006-2009 Q Picat, N
17 èmes Journées des Statisticiens des Centres de Lutte contre le Cancer 4 ème Conférence Francophone d Epidémiologie Clinique Essais cliniques de phase 0 : état de la littérature 2006-2009 Q Picat, N
Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS)
 Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS) Édition Conseil du médicament www.cdm.gouv.qc.ca Coordination Anne Fortin, pharmacienne Élaboration Conseil du médicament Fédération
Algorithme d utilisation des anti-inflammatoires non stéroïdiens (AINS) Édition Conseil du médicament www.cdm.gouv.qc.ca Coordination Anne Fortin, pharmacienne Élaboration Conseil du médicament Fédération
Caisse Nationale de l'assurance Maladie des Travailleurs Salariés Sécurité Sociale
 Caisse Nationale de l'assurance Maladie des Travailleurs Salariés Sécurité Sociale Circulaire CNAMTS MMES et MM les Directeurs Date : - des Caisses Régionales d'assurance Maladie 27/03/96 - des Caisses
Caisse Nationale de l'assurance Maladie des Travailleurs Salariés Sécurité Sociale Circulaire CNAMTS MMES et MM les Directeurs Date : - des Caisses Régionales d'assurance Maladie 27/03/96 - des Caisses
Point d information Avril 2012. Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir
 Point d information Avril 2012 Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir Le dabigatran (PRADAXA), inhibiteur direct de la thrombine,
Point d information Avril 2012 Les nouveaux anticoagulants oraux (dabigatran et rivaroxaban) dans la fibrillation auriculaire : ce qu il faut savoir Le dabigatran (PRADAXA), inhibiteur direct de la thrombine,
Les nouveaux anticoagulants oraux, FA et AVC. Docteur Thalie TRAISSAC Hôpital Saint André CAPCV 15 février 2014
 Les nouveaux anticoagulants oraux, FA et AVC Docteur Thalie TRAISSAC Hôpital Saint André CAPCV 15 février 2014 Un AVC toutes les 4 minutes 1 130 000 AVC par an en France 1 770 000 personnes ont été victimes
Les nouveaux anticoagulants oraux, FA et AVC Docteur Thalie TRAISSAC Hôpital Saint André CAPCV 15 février 2014 Un AVC toutes les 4 minutes 1 130 000 AVC par an en France 1 770 000 personnes ont été victimes
Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic de cancer
 Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
Avis 15 mai 2013. B01AX05 (Antithrombotique). Inhibiteur sélectif indirect du facteur Xa
 COMMISSION DE LA TRANSPARENCE Avis 15 mai 2013 L avis adopté par la Commission de la Transparence le 23 janvier 2013 a fait l objet d une audition le 17 avril 2013 et d un examen des observations du laboratoire
COMMISSION DE LA TRANSPARENCE Avis 15 mai 2013 L avis adopté par la Commission de la Transparence le 23 janvier 2013 a fait l objet d une audition le 17 avril 2013 et d un examen des observations du laboratoire
Prise en charge de l embolie pulmonaire
 Prise en charge de l embolie pulmonaire Dr Serge Motte Liège 06.12.14 - Laack TA et Goyal DG, Emerg Med Clin N Am 2004; 961-983 2 PLAN Diagnostic Prise en charge: Phase aiguë: analyse de gravité Choix
Prise en charge de l embolie pulmonaire Dr Serge Motte Liège 06.12.14 - Laack TA et Goyal DG, Emerg Med Clin N Am 2004; 961-983 2 PLAN Diagnostic Prise en charge: Phase aiguë: analyse de gravité Choix
Ethique, don d organe et Agence de la Biomédecine
 Ethique, don d organe et Agence de la Biomédecine Patrick Niaudet Président du Conseil d Orientation de l ABM Servie de Néphrologie Pédiatrique Hôpital Necker-Enfants Malades, Paris Mon intervention ne
Ethique, don d organe et Agence de la Biomédecine Patrick Niaudet Président du Conseil d Orientation de l ABM Servie de Néphrologie Pédiatrique Hôpital Necker-Enfants Malades, Paris Mon intervention ne
L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE
 L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE NEUCHATEL, Suisse, 7 avril/prnewswire/ -- - LA LENALIDOMIDE est évaluée par l EMEA comme thérapie orale pour
L EMEA accepte d évaluer la demande d autorisation de mise sur le marché de la LENALIDOMIDE NEUCHATEL, Suisse, 7 avril/prnewswire/ -- - LA LENALIDOMIDE est évaluée par l EMEA comme thérapie orale pour
Indication (selon la monographie du médicament) : Traitement de l'adénocarcinome rénal métastatique
 Rapport sur les nouveaux médicaments brevetés Torisel Par souci de transparence, le CEPMB publie les résultats des examens des prix des nouveaux produits médicamenteux brevetés effectués par les membres
Rapport sur les nouveaux médicaments brevetés Torisel Par souci de transparence, le CEPMB publie les résultats des examens des prix des nouveaux produits médicamenteux brevetés effectués par les membres
TRAITEMENT DE L HÉPATITE B
 TRAITEMENT DE L HÉPATITE B P Mathurin Service d Hépatogastroentérologie Pr Paris Hôpital Claude Hurriez CHRU Lille CRITERES VIROLOGIQUES ET HISTOIRE NATURELLE 1 OBJECTIF THERAPEUTIQUE: Séroconversion HBe
TRAITEMENT DE L HÉPATITE B P Mathurin Service d Hépatogastroentérologie Pr Paris Hôpital Claude Hurriez CHRU Lille CRITERES VIROLOGIQUES ET HISTOIRE NATURELLE 1 OBJECTIF THERAPEUTIQUE: Séroconversion HBe
COMPARAISON DE QUATRE PROTOCOLES DE CHIMIOTHERAPIE POUR DES CANCERS DU POUMON NON A PETITES CELLULES (CBP NAPC) AVANCES
 COMPARAISON DE QUATRE PROTOCOLES DE CHIMIOTHERAPIE POUR DES CANCERS DU POUMON NON A PETITES CELLULES (CBP NAPC) AVANCES Approximativement, un tiers de tous les décès dus au cancer sont en relation avec
COMPARAISON DE QUATRE PROTOCOLES DE CHIMIOTHERAPIE POUR DES CANCERS DU POUMON NON A PETITES CELLULES (CBP NAPC) AVANCES Approximativement, un tiers de tous les décès dus au cancer sont en relation avec
Cancer colo-rectal : situation belge
 Cancer colo-rectal : situation belge J.-L. Van Laethem, MD, PhD Unité d'oncologie digestive Département médico-chirurgical de Gastro-entérologie Pas de conflit d intérêt déclaré Cancer du colon 7000 nouveaux
Cancer colo-rectal : situation belge J.-L. Van Laethem, MD, PhD Unité d'oncologie digestive Département médico-chirurgical de Gastro-entérologie Pas de conflit d intérêt déclaré Cancer du colon 7000 nouveaux
Fibrillation atriale chez le sujet âgé
 Dr Benoit Blanchard LE HAVRE Le 18 MARS 2014 Fibrillation atriale chez le sujet âgé Le plus fréquent des trouble du rythme cardiaque, 750,000 personnes atteintes de FA en France, 100,000 nouveaux cas chaque
Dr Benoit Blanchard LE HAVRE Le 18 MARS 2014 Fibrillation atriale chez le sujet âgé Le plus fréquent des trouble du rythme cardiaque, 750,000 personnes atteintes de FA en France, 100,000 nouveaux cas chaque
Le dropéridol n est pas un traitement à considérer pour le traitement de la migraine à l urgence
 Le dropéridol n est pas un traitement à considérer pour le traitement de la migraine à l urgence On pose fréquemment le diagnostic de migraine sévère à l urgence. Bien que ce soit un diagnostic commun,
Le dropéridol n est pas un traitement à considérer pour le traitement de la migraine à l urgence On pose fréquemment le diagnostic de migraine sévère à l urgence. Bien que ce soit un diagnostic commun,
Les différents types de cancers et leurs stades. Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07
 Les différents types de cancers et leurs stades Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07 CARCINOGENESE multiple steps, accumulation d altd altérations continuum lésionnel
Les différents types de cancers et leurs stades Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07 CARCINOGENESE multiple steps, accumulation d altd altérations continuum lésionnel
