LABORATOIRE MULTISITES DE BIOLOGIE MEDICALE
|
|
|
- Denise St-Amand
- il y a 9 ans
- Total affichages :
Transcription
1 LABORATOIRE MULTISITES DE BIOLOGIE MEDICALE Laboratoire ADEBIO - MQ-I-SMQ Page 1/50
2 1 INTRODUCTION Présentation du laboratoire Prestations Environnement du LBM ADEBIO DOMAINE D APPLICATION REFERENCES DOCUMENTATION DEFINITIONS ET ABREVIATIONS SYSTEME DE MANAGEMENT DE LA QUALITE Exigences générales (Chap ISO 15189) Documentation (Chap ISO 15189) Le manuel qualité (Chap. 4.2 ISO 15189) Maîtrise des documents (Chap. 4.3 ISO 15189) RESPONSABILITE DE LA DIRECTION Engagement de la direction (Chap. 4.2 ISO 15189) Ecoute client (Chap ISO 15189) Politique qualité (Chap. 4.2 ISO 15189) Planification (Chap. 4.2 ISO 15189) Objectifs qualité Planification du système de management de la qualité Responsabilité de la direction et communication (Chap. 4.1 ISO 15189) Revue de direction (Chap ISO 15189) MANAGEMENT DES RESSOURCES Ressources humaines Le personnel (Chap. 5.1 ISO 15189) Locaux environnement Matériel (Chap ISO 15189) Services externes et approvisionnements (Chapitre 4.6 ISO 15189) Maîtrise des processus achats et approvisionnements Informations relatives aux achats Vérification du produit acheté Informatique : gestion des informations du laboratoire (chap ISO 15189) REALISATION DES ANALYSES - (CHAP ISO 15189) Revue de contrat (Chapitre 4.4 ISO 15189) Détermination des exigences - besoins Revue des exigences Communication avec le client Processus pré analytique (chapitre 5.4) Processus analytique (chapitres 5.5 et 5.6) Processus post analytique Compte rendu de résultats (chapitre ISO 15189) Analyses transmises à des laboratoires sous-traitants (Chapitre 4.5 ISO 15189) 43 Laboratoire ADEBIO - MQ-I-SMQ Page 2/50
3 9 MESURES, ANALYSES ET AMELIORATION (CHAPITRES /11/ ) Généralités Surveillance et mesure (chapitre ) Satisfaction du client Evaluation et audits Mesure et surveillance des processus Indicateurs de qualité Identification et maîtrise des non-conformités (chapitre ) Définition Traitement de la non-conformité Actions correctives préventives amélioration continue (chapitres ) Planification pour l amélioration continue Actions correctives Actions préventives Evaluation des risques Laboratoire ADEBIO - MQ-I-SMQ Page 3/50
4 1 INTRODUCTION Le manuel qualité du laboratoire ADEBIO présente le système de management de la qualité mis en œuvre pour maîtriser l ensemble des processus de notre laboratoire dans le but d obtenir la satisfaction durable de nos clients, la reconnaissance de notre compétence et de garantir le respect de la réglementation en vigueur grâce à l efficacité de son organisation, la compétence de toute son équipe, l aptitude des équipements et des locaux. Ce document est connu et appliqué par chaque personne travaillant au laboratoire. L ensemble des salariés et professionnels de santé du laboratoire ADEBIO respectent le code d éthique suivant : La direction du laboratoire ADEBIO et son personnel reconnaissent ne prendre aucun engagement dans toute activité qui réduirait la confiance en la compétence, l impartialité, le jugement de l intégrité opérationnelle du laboratoire ADEBIO. 1.1 Présentation du laboratoire ADEBIO est un laboratoire multi sites composé de 7 sites, dont l autorisation administrative a été fixée par l arrêté ARS n Le LBM ADEBIO, statut juridique SELAS, résulte de la fusion de la SELARL CHALENDARD et de la SELARL REYNIER COSTAZ avec mise en place effective en juillet 2012 (arrêté ARS n ). Le laboratoire ADEBIO a été étendu à 7 sites, en 2013, par fusion à la SELARL DE CLERCQ PENEL DAYET (Valence rue Farnerie et rue Victor Hugo, Portes lès Valence, Guilherand Granges site AMP) selon l arrêté ARS n Effectif total du laboratoire ADEBIO : 103 personnes (dont 8 biologistes co-responsables et 2 biologistes médicaux) Laboratoire ADEBIO - MQ-I-SMQ Page 4/50
5 LES SITES ADEBIO Laboratoire ADEBIO site de GUILHERAND GRANGES Le Plaza 53, rue Jean Chièze Guilherand Granges Tel : Fax : Horaires d ouverture : lundi au vendredi 7h30 12h30 et 13h30 18h30 Samedi 8h 12h Laboratoire ADEBIO site de LIVRON 56, rue Léon Aubin Livron sur Drôme Tel : Horaires d ouverture : lundi au vendredi 7h30 12h et 14h30 18h Samedi 7h30 12h Fax : Laboratoire ADEBIO site de LA VOULTE 174, rue Louis Pasteur La Voulte sur Rhône Tel : Horaires d ouverture : lundi au vendredi 7h30 12h et 14h - 18h Samedi 7h30 12h Fax : Laboratoire ADEBIO site de PORTES LES VALENCE 8, rue Emile Zola Portes les Valence Tel : Horaires d ouverture : lundi au vendredi 7h00 18h Samedi 7h30 12h Fax : Laboratoire ADEBIO site de VALENCE CENTRE (siège social) 13 rue Farnerie Valence Tel : /67.09 Fax : Horaires d ouverture : lundi au vendredi 7h00 12h30 et 13h30 18h Samedi 7h30 12h30 Laboratoire ADEBIO site de VALENCE SUD 220, avenue Victor Hugo valence Tel : Fax : Horaires d ouverture : lundi au vendredi 7h00 12h30 et 13h30 18h Samedi 7h30 12h Laboratoire ADEBIO site de Biologie de la Reproduction (Centre Mistral) 180, rue Pierre Curie Guilherand Granges Tel : Horaires d ouverture : lundi au vendredi 7h00-17h00 Samedi 7h30 12h Fax : Laboratoire ADEBIO - MQ-I-SMQ Page 5/50
6 LES BIOLOGISTES lignes téléphoniques directes Jean-David CHALENDARD Pharmacien biologiste GUILHERAND GRANGES Céline COLMANT Pharmacien biologiste Jean-Pierre COSTAZ Pharmacien biologiste Brigitte CUISNIER Médecin biologiste Philippe DAYET Pharmacien biologiste Gilles DE CLERCQ Pharmacien biologiste Vincent PENEL Pharmacien biologiste Philippe REYNIER Pharmacien biologiste Marie-Gabrielle CATHALAN Pharmacien biologiste Emma DUVILLA Médecin biologiste LA VOULTE LIVRON PORTES LES V VALENCE CENTRE VALENCE SUD BIOLOGIE DE LA REPRODUCTION Centre Mistral Laboratoire ADEBIO - MQ-I-SMQ Page 6/50
7 Situation géographique des sites du laboratoire ADEBIO 1.2 Prestations Environnement du LBM ADEBIO Clients Patients ambulatoire ou hospitalisés Médecins Cabinets Médicaux Infirmières ou infirmiers libéraux Pharmacies Etablissements de santé Cabinets vétérinaires Prestations Prélèvements comptes rendus de résultats - Conseils Comptes rendus d analyses Information et conseil à l interprétation Conseil pour la réalisation des prélèvements Dispositifs à prélèvements Dispositifs à prélèvements - Comptes rendus de résultats Prélèvements comptes rendus de résultats - Conseils Comptes rendus de résultats Conseil à l interprétation Laboratoire ADEBIO - MQ-I-SMQ Page 7/50
8 Environnement du laboratoire ADEBIO Cabinets Médicaux Etablissements de Santé Cabinets Vétérinaires Lieux autorisés pour le dépôt des prélèvements Logistique CAISSES D'ASSURANCE MALADIE FOURNISSEURS LBM ADEBIO LBM Soustraitants Cabinets d Infirmiers Libéraux (Prélèvements) LBM Sous-traitants ponctuels Clientèle Directe LABORATOIRES SPECIALISES : Laboratoire BIOMNIS Hôpital de Valence LBM Etablissement Français du Sang (EFS) - ARS Rhône Alpes - COFRAC Laboratoire ADEBIO - MQ-I-SMQ Page 8/50
9 2 DOMAINE D APPLICATION Le système de management de la qualité est organisé selon les exigences de la norme ISO 15189:2012, les exigences réglementaires. Ce système couvre l ensemble des activités du laboratoire de biologie médicale. Les processus du laboratoire sont classés en trois grandes familles : Les processus de réalisation : processus pré analytique, analytique et post analytique Les processus de pilotage Management du SMQ Les processus supports Management des ressources Domaines de prestations du laboratoire ADEBIO Examens de biologie médicale réalisés couvrant les sous-familles (selon de document SH INF 50) : Biochimie générale et spécialisée (BIOCHBM) Hématocytologie (HEMATOBM) Hémostase (COAGBM) Immunohématologie (IMMUNOHEMATOBM) Auto-immunité (AUTOIMMUNOBM) Allergie (ALLERGBM) Sérologie infectieuse (ISEROBM) Bactériologie (BACTH) Parasitologie Mycologie (PARASITOMYCO) Spermiologie diagnostique (SPERMIOBM) Activités biologiques d AMP (AMPBIOBM) La direction du laboratoire a fait le choix de ne pas mentionner ou apposer le logotype COFRAC sur les supports suivants : papier à en-tête, documents ou supports correspondants à une prestation réalisée sous couvert de l accréditation, tout autre document ou support mobile ou non, y compris audiovisuel ou électronique, qu il soit à caractère technique commercial ou publicitaire. Les règles générales d utilisation, par le laboratoire, de la marque COFRAC respectent le document GEN REF 11, notamment l utilisation de la référence textuelle : «accréditation Cofrac n , Liste des sites accrédités et portée disponibles sur (*) PR-I-ANA-004-Procédure de gestion de Portée flexible type A ou B version applicable Tableau annexe portée d accréditation n Laboratoire ADEBIO - MQ-I-SMQ Page 9/50
10 3 REFERENCES DOCUMENTATION Principales références réglementaires Ordonnance n du 13 janvier 2010 relative à la biologie médicale. Code de la Santé Publique : Livre II Biologie Médicale Loi n du 30 mai 2013 portant réforme de la biologie médicale Principaux documents du COFRAC section Laboratoires (santé humaine) Guides techniques d'accréditation en biologie médicale : Document SH GTA 01, SH GTA 02, SH GTA 04, SH GTA 06, SH GTA 14 Guide technique d accréditation en parasitologie et mycologie médicale Document LAB GTA 12 (non géré) Exigences pour l accréditation des laboratoires de biologie médicale selon la norme ISO Documents SH REF 02, SH REF 04, SH REF 08 Documents spécifiques de la section santé humaine (SH REF, SH FORM, SH INF) Documents généraux opposables dont le document GEN REF 11 relatif aux règles d utilisation de la marque COFRAC. Principaux textes réglementaires applicables à l activité Décret n du 4 novembre 1976 modifié : condition d autorisation des LABM Décret n du 30 décembre 1975 modifié : formation spécialisée des directeurs et directeurs adjoints Décret n du 10 septembre 1990 : réglementation du diplôme d études spécialisées de biologie médicale. Circulaire DGS/PS 3 n 5607 du 13 décembre 1993 : conditions d exercice de la profession de technicien de laboratoire Décret n du 3 décembre 1980 : catégories de personnes habilitées à effectuer certains actes de prélèvement en vue d analyses de biologie médicale Arrêté du 3 décembre 1980 : délivrance du certificat de capacité Décret n du 15 mars 1993 : conditions à l exercice de la profession d infirmier. Décrets et arrêtés d application en lien avec l Ordonnance du 13 janvier 2010 Arrêté du 2 juin 2014 relatif aux règles de bonnes pratiques cliniques et biologiques en AMP Contrats de coopération Contrat de coopération avec le laboratoire CHAMPELY Contrat de coopération LAT (LATLUMTOX) Contrat de coopération avec EFS Valence Convention de sous-traitance BIOMNIS Normes internationales Norme NF EN ISO 15189:2012 Laboratoire de biologie médicale Exigences particulières concernant la qualité et la compétence Les documents contractuels généraux et sectoriels du COFRAC applicables section santé humaine (SH) Laboratoire ADEBIO - MQ-I-SMQ Page 10/50
11 4 DEFINITIONS ET ABREVIATIONS Définitions : Analyses : Examens biologiques qui concourent au diagnostic, au traitement ou à la prévention des maladies humaines ou qui font apparaître toute autre modification de l état physiologique Comptes rendus de résultats : Documents écrits, validés et signés par le biologiste comportant les résultats d analyses qualitatifs et/ou quantitatifs accompagnés de commentaires aussi souvent qu il est nécessaire. Contrôle interne de qualité (CIQ) Ensemble des opérations et activités opérationnelles d un site de production mises en œuvre pour assurer que les exigences relatives à la qualité des services sont satisfaites. Evaluation externe de la qualité ou Contrôle Externe de Qualité (CEQ - EEQ) : Vérification des résultats de mesures ou d observations effectuées en un lieu donné, par comparaison avec les résultats obtenus par d autres sites sur le même échantillon émis par une entité extérieure qui procède également à l analyse statistique des données. Echantillon biologique : Echantillon obtenu par l acte de prélèvement et sur lequel vont être effectuées une ou plusieurs analyses de biologie médicale. Qualification du personnel : Validation d une ou plusieurs compétences techniques acquises. Valeurs de référence : Résultats obtenus pour un constituant donné dans une population de référence dont les individus sont exempts de pathologie ou de traitement susceptibles de modifier ceux-ci. Validation des résultats d analyse Opération permettant d assurer qu un résultat a été obtenu dans des conditions techniques satisfaisantes et est compatible avec le dossier biologique du patient. Cette validation est à la fois technique et biologique. -La validation technique comporte la vérification de la conformité des conditions d exécution aux procédures et tient compte notamment des résultats obtenus sur les échantillons de contrôle. -La validation biologique est le contrôle de la vraisemblance et de la cohérence de l ensemble des résultats des analyses effectuées pour une personne compte tenu de son état clinique, des traitements thérapeutiques suivis et des résultats antérieurs. Abréviations : COFRAC : Comité Français d Accréditation OCIL : Organisme de comparaison inter laboratoires AES : Accident d exposition au sang ANSM : Agence Nationale de Santé et du Médicaments CNIL : Commission Nationale de l'informatique et des Libertés DRIRE : Direction Régionale de l'industrie et de la Recherche ARS : Agence Régionale de Santé Laboratoire ADEBIO - MQ-I-SMQ Page 11/50
12 Satisfaction CLIENT 5 SYSTEME DE MANAGEMENT DE LA QUALITE 5.1 Exigences générales (Chap ISO 15189) ADEBIO adopte les exigences de la norme :2012 pour la mise en œuvre du système de management de la qualité et son amélioration continue. PROCESSUS ET INTERACTIONS SCHEMA GENERAL 1. Responsabilité de la direction CLIENT Exigences 2. Management des ressources Eléments d entrée 3. Processus de réalisation : Pré analytique, Analytique, Post analytique 4. Mesures, analyses, améliorations Produit services Eléments de sortie Cf. cartographie et interaction des processus détaillées page suivante. Réalisation des analyses : Eléments d entrée - Exigences et attentes du client - Renseignements cliniques pertinents - Prescription médicale, produits fournis par le client - Respect des exigences réglementaires, normatives Eléments de sortie - Mise à disposition des comptes rendus de résultats répondant aux attentes des clients : patient, médecin - Respect des exigences réglementaires. Laboratoire ADEBIO - MQ-I-SMQ Page 12/50
13 Cartographie Processus et interactions P01 - ORGANISATION MANAGEMENT PROCESSUS DE PILOTAGE PROCESSUS DE REALISATION OU OPERATIONNELS CLIENTS Demandes d examens Revue de contrat P06 - Système documentaire Enregistrements P03 - Processus Pré analytique P07 - Achats - approvisionnements P08 - Sous-traitance Examens P04 - Processus Analytique P09 - Prestations de Conseils P10 - Ressources Humaines P05 - Processus Post analytique P11 - Locaux Environnement (Hygiène et sécurité) P12 - Gestion des matériels P13 - Gestion système d information - SIL Compte rendu de résultats Avis interprétation Services associés Evaluation Satisfaction CLIENTS PROCESSUS SUPPORTS P02 - AMELIORATION CONTINUE PROCESSUS DE PILOTAGE Laboratoire ADEBIO - MQ-I-SMQ Page 13/50
14 Les processus nécessaires pour le système de management de la qualité sont décrits (documents gérés) et comportent pour chaque processus : La finalité, le (les) pilote(s), la description (étapes), les principaux documents associés, l analyse de risque et les actions préventives, les modalités de surveillance et d évaluation (indicateurs qualité). Les objectifs et indicateurs qualité suivent la même logique par processus (1). (1) exigences ISO :2012 Laboratoire ADEBIO - MQ-I-SMQ Page 14/50
15 PROCESSUS Norme ISO DOCUMENTATION :2012 Liste des procédures (1) Processus de pilotage - direction Organisation - Management MQ-I-SMQ-002 Amélioration continue PR-I-REC-001 PR-I-NC-001 / 002 PR-I-AC-001 PR-I-AQI-001 / 002 PR-I-RDD-001 Processus de réalisation processus métier Pré analytique Analytique Post analytique Demandes d examens - accueil - revue de contrat Prélèvements Traitement échantillons Réalisation des analyses Validation technique Validation analytique Validation biologique Conservation élimination échantillons Transmission des comptes rendus de résultats PR-I-ACC-001 / 002 PR-I-RDC-001 PR-I-PRLV-001 PR-I-MYCO-003 PR-I-PRLV-002 / 003 PR-I-ECH-002 / 003 / 004 / 005 / 006 PR-I-ANA-001 / 002 / 003 / 004 PR-I-POST-002 PR-I-BIOCH-002 / 005 PR-I-HEM-001 PR-I-IH-001 PR-I-COAG-002 PR-I-BAC-001 PR-I-MYCO-001 PR-I-AQA-001 / 002 / 005 PR-I-POST-001 PR-I-ECH-006 PR-I-CRR-002 PR-I-CRR-001 PR-I-PDC-001 Processus supports ou de soutien Gestion du Personnel PR-I-GRH-001 PR-I-GRH-002 / 004 PR-I-GRH-005 / 006 / 008 Gestion des matériels 5.3 PR-I-LCE-003 PR-I-MAT-001 / 002 Système d information et SIL 5.10 PR-I Sous-traitance des examens 4.5 PR-I-ECH-002 Achats - Approvisionnements 4.6 PR-I-ACH-001 / SST-001 Locaux Environnement PR-I-LCE Hygiène et sécurité PR-I-LCE-001 Système documentaire 4.3 PR-I-MDD-001 / 003 / 004 Les procédures et documents relatifs au système de management de la qualité sont identifiés de manière univoque conformément aux exigences de la norme ISO Maîtrise des documents. (1) Les documents applicables sont gérés à l aide du logiciel qualité KALILAB. Laboratoire ADEBIO - MQ-I-SMQ Page 15/50
16 5.2 Documentation (Chap ISO 15189) Le manuel qualité (Chap. 4.2 ISO 15189) Le responsable qualité du laboratoire veille à la bonne gestion du manuel qualité. Il est responsable de sa rédaction ainsi que de sa révision et mise à jour. La vérification et approbation du Manuel Qualité sont sous la responsabilité de la direction du laboratoire. La diffusion et l archivage sont sous la responsabilité de l assistante qualité ou du responsable qualité. Le manuel qualité est découpé en chapitres, il comporte un numéro de version et une date d application, une pagination x/y. Le manuel qualité est tenu à jour par révision périodique sous l autorité et la responsabilité du responsable qualité, selon les dispositions de la procédure d élaboration gestion des documents. L ensemble du personnel est destinataire du manuel qualité, des documents référencés qui les concernent et des exigences relatives à leur mise en œuvre. Processus 01 ORGANISATION ET MANAGEMENT MQ-I-SMQ-002-Manuel qualité version applicable Laboratoire ADEBIO - MQ-I-SMQ Page 16/50
17 5.2.2 Maîtrise des documents (Chap. 4.3 ISO 15189) Structure du système documentaire : La maîtrise du système qualité et tous les processus du laboratoire reposent sur la mise en place de documents qualité classés par niveau selon une pyramide documentaire : MQ PROCEDURES MODES OPERATOIRES INSTRUCTIONS ENREGISTREMENTS RELATIFS A LA QUALITE ENREGISTREMENTS TECHNIQUES Tous les documents qualité du laboratoire sont répertoriés. Le laboratoire utilise un logiciel qualité avec lequel la gestion documentaire est progressivement organisée de façon maîtrisée (transfert des documents qualité). Logiciel KALILAB. La documentation externe est gérée et comporte : - les documents administratifs (ex : autorisations ARS/Arrêtés, ) - les documents réglementaires applicables au laboratoire. La veille réglementaire est alimentée par les Syndicats professionnels, l association LABAC (laboratoires accrédités) la consultation de sites Internet officiels spécialisés. Ex : sante.gouv.fr, ainsi que par les revues spécialisées de la profession. - les documents techniques : catalogues fournisseurs, manuels techniques, notices techniques des réactifs et des analyses de laboratoire. - la ou les normes, les documents contractuels généraux et sectoriels du COFRAC et guides techniques (GTA) et documents COFRAC (REF, FORM, ) de la section Santé Humaine : SH Laboratoire ADEBIO - MQ-I-SMQ Page 17/50
18 La documentation externe applicable au laboratoire et validée par le directeur du laboratoire ou le responsable qualité (selon la nature des documents) gérés à l aide de KALILAB pour les documents au format «pdf». Le suivi et la mise à jour de celles-ci sont assurés par les techniciennes référentes du laboratoire. Se reporter aux dispositions de la procédure élaboration et gestion des documents. Les informations d origine externe constituent une ressource fondamentale pour le développement continu des connaissances. Les besoins en information sont identifiés sur la base des besoins des biologistes et du personnel. Les sources d informations principales gérées sont les ouvrages et publications disponibles et la participation à différentes manifestations (congrès, colloques, recommandations HAS, sites officiels administration de la santé, recommandations scientifiques reconnues, ). Le laboratoire est abonné à des revues scientifiques. Le laboratoire a répertorié les accès Internet utiles et reconnus (pour certains, accessibles directement via le logiciel KALILAB ). Processus 06 SYSTEME DOCUMENTAIRE ET ENREGISTREMENTS Procédures associées : PR-I-MDD Gestion et élaboration des documents qualité PR-I-MDD-003 -Enregistrements et archivage relatifs à la qualité Version applicable Laboratoire ADEBIO - MQ-I-SMQ Page 18/50
19 6 RESPONSABILITE DE LA DIRECTION 6.1 Engagement de la direction (Chap. 4.2 ISO 15189) La direction du laboratoire ADEBIO s engage à : Mettre en place un système qualité conforme aux exigences réglementaires et aux bonnes pratiques professionnelles Appliquer les exigences de la norme internationale ISO :2012 dans le cadre de ses portées d accréditation et du système de management de la qualité. Organiser et mettre en œuvre les ressources adaptées aux besoins et attentes de nos clients : les patients, les médecins, les infirmières, les organismes payeurs (Caisse d'assurance Maladie, Mutuelles, compagnies d assurance), les pharmacies ainsi que les clients internes au laboratoire (secrétaires, infirmières, techniciennes, biologistes). Développer la compétence du personnel par la mise en place de plan annuel de formation, les qualifications et habilitations, véritable parcours de professionnalisation interne, avec nécessité de se familiariser avec la documentation concernant la qualité, appliquer la politique qualité et les procédures à tout moment. Impliquer le personnel dans les actions d amélioration continue par une prise en compte des besoins et attentes des clients, l enregistrement systématique des non conformités, réclamations et incidents qui constituent de véritables sources de progrès. Surveiller et améliorer le processus de réalisation des analyses, grâce notamment à la réalisation d un contrôle interne de qualité quotidien et un contrôle inter laboratoires volontaire pour l évaluation externe de la qualité. Développer les prestations de conseil et obtenir les renseignements cliniques pertinents, chaque fois que nécessaire, utiles à la réalisation des analyses et à l interprétation des résultats sous la forme d avis et interprétation. Maîtriser les situations à risque : procéder à l analyse de risque, l analyse de tendance et la criticité des risques (probabilité de survenue, fréquence, gravité). Activer la boucle préventive de l amélioration continue. Intégrer les évolutions technologiques dans la réalisation des examens et des prestations du laboratoire pour obtenir la satisfaction durable des clients grâce à une performance entretenue au plus haut niveau. Chaque membre du personnel du laboratoire adhère à ces engagements et met tout en œuvre pour participer activement à la réalisation de la politique qualité. Laboratoire ADEBIO - MQ-I-SMQ Page 19/50
20 6.2 Ecoute client (Chap ISO 15189) L écoute des clients du laboratoire ADEBIO est assurée par le recueil régulier d un faisceau d informations : Eléments de satisfaction ou réclamation Besoins nouveaux Prestations de conseils Exigences spécifiées : délais, degré d urgence, destinataires, renseignements cliniques, Des enquêtes de satisfaction sont effectuées régulièrement auprès des différentes catégories de clients (patients, médecins, préleveurs externes), analysées et exploitées pour dégager des axes d améliorations. Les résultats des enquêtes sont présentés en revue de direction et communiqués en interne. Les méthodes utilisées pour être à l écoute des clients (questionnaire, entretien ) tiennent compte des différents types de clients, des objectifs fixés, dans le respect des règles déontologiques de la profession. Prestations de conseils : Des rencontres régulières avec les professionnels de santé en relation avec le laboratoire sont organisées dans le but de détecter des besoins et attentes nouveaux, de vérifier la pertinence des services mis en place, d informer et de fournir des recommandations ou conseils visant à améliorer la qualité de la prise en charge des patients, la maîtrise de l étape pré analytique et la communication des renseignements cliniques pertinents. Ces rencontres concernent plus particulièrement les professionnels de santé du bassin de population couvert par le laboratoire : - les médecins (FMC, rencontres individuelles) - les infirmières et infirmiers libéraux et salariés (centre de soins, établissements de santé) - les pharmaciens d officines - les directeurs d établissements de santé Au cours de ces rencontres régulières, le principal objectif recherché est le développement de relation mutuellement bénéfique dans un esprit de concertation et de coopération avec comme finalité l amélioration des prestations du laboratoire pour renforcer la qualité et la sécurité des soins dispensés aux patients ou malades. Diffusion de bulletins biologiques à destination des médecins. A partir de cette écoute client, des actions d amélioration sont proposées, validées, planifiées et suivies dans le cadre des réunions internes FIAQ, RSA et/ou au cours de la revue de direction. Ce dispositif est mis en place de façon opérationnelle depuis janvier FIAQ : Fiche d Incidents et Amélioration Individuelle de la Qualité RSA : Réunion de suivi accréditation FMC : Formation Médicale Continue Laboratoire ADEBIO - MQ-I-SMQ Page 20/50
21 6.3 Politique qualité (Chap. 4.2 ISO 15189) Depuis 2008, notre laboratoire est accrédité par le COFRAC (selon la norme NF EN ISO 15189) sur les principaux secteurs d activités, comptant à ce jour les familles d examens : biochimie, hématocytologie, hémostase, sérologie infectieuse, mycologie (Attestation d accréditation n ). Aujourd hui, nous poursuivons notre effort pour que l ensemble de nos activités soit accrédité par le COFRAC. En 2014, nous demandons une extension de notre accréditation pour la famille d examens d immunohématologie. Les domaines des prestations, que le laboratoire ADEBIO offre à ses clients, sont repris dans le catalogue des prestations analytiques du laboratoire (manuel de prélèvements). Nous nous engageons : à poursuivre nos efforts dans la mise en place des bonnes pratiques professionnelles afin de garantir la qualité des résultats rendus. à développer par la formation et par une sensibilisation régulière, la culture qualité et la compétence du personnel et de la direction à appliquer le système de management de la qualité mis en place à satisfaire au mieux nos patients et nos différents partenaires. à poursuivre notre politique d accréditation de notre activité et répondre aux contraintes économiques. à nous conformer à la norme NF EN ISO en Santé Humaine. En cohérence avec notre politique qualité, grâce à notre potentiel humain et aux nouveaux outils technologiques mis en place, ADEBIO s est fixé les objectifs suivants : Maintenir une confiance permanente dans la qualité de nos prestations de services avec la contribution de tous les secteurs de notre laboratoire Développer une politique de prestations de conseil auprès des utilisateurs des services du laboratoire : patients, médecins, infirmiers, établissements de santé et correspondants Obtenir les renseignements cliniques pertinents chaque fois que possible Interpréter par des avis appropriés et commentaires les résultats d examens Renforcer nos compétences par une politique de formation dynamique Maîtriser nos processus «métiers», supports et nos processus d amélioration continue. Surveiller la performance analytique et nos délais. Surveiller l ensemble des processus à l aide d indicateurs de qualité suivis régulièrement Notre politique qualité s appuie sur l implication totale de toute l équipe du laboratoire dans l élaboration, le respect et le suivi des exigences du système qualité. Compétence, sérieux, qualité de l accueil, écoute, disponibilité et réactivité sont les vecteurs forts de notre laboratoire. Chaque membre du personnel du laboratoire adhère à cette politique qualité et met tout en œuvre pour contribuer activement à sa réalisation. Les directeurs du laboratoire ADEBIO Laboratoire ADEBIO - MQ-I-SMQ Page 21/50
22 6.4 Planification (Chap. 4.2 ISO 15189) Objectifs qualité Nos principaux objectifs qualité sont déterminés en cohérence avec l énoncé de notre politique qualité. Ils sont formalisés, analysés et ajustés au cours des revues de direction. Ils sont déclinés au niveau des activités, des processus et des fonctions concernées pour leur mise en œuvre. L atteinte des objectifs qualité est vérifiée au cours des réunions de revue de direction à partir des résultats des indicateurs de qualité. A titre indicatif, exemples d objectifs et indicateurs qualité Objectifs qualité Indicateurs qualité Fonctions Responsabilité Surveiller la nature et l évolution des réclamations «client» par an Baisse ou maintien du nombre des réclamations client par an Processus 02 AMELIORATION CONTINUE Impliquer l ensemble des acteurs du laboratoire dans la démarche d amélioration continue Processus 02 AMELIORATION CONTINUE Surveiller et mesurer la performance analytique Processus 04 ANALYTIQUE Prévenir les accidents d exposition au sang. Tendre vers zéro AES. Processus 11 LOCAUX ENVIRONNEMENT Former le personnel pour renforcer les compétences «métiers». Processus 10 RESSOURCES HUMAINES Maîtriser les prélèvements Processus 03 - PREANALYTIQUE Statistiques annuelles des réclamations. % de participation aux réunions FIAQ % de participation du personnel aux revues de direction Résultats CIQ EEQ CNQ ANSM Nombre d AES/an Nombre d heures de formation «métiers» par salarié par an Nombre d'incidents de prélèvements par mois Nombre de patients «reconvoqués» par mois Service qualité Direction Service qualité Techniciennes Biologistes Secteur technique Technicienne référente Hygiène et sécurité - CHSCT Direction Infirmières Secteur prélèvement Laboratoire ADEBIO - MQ-I-SMQ Page 22/50
23 6.4.2 Planification du système de management de la qualité (Chapitre ISO 15189) Pour atteindre de manière efficiente les objectifs qualité, le laboratoire planifie des actions d amélioration aux processus de réalisation des analyses, aux processus de soutien nécessaires à cette réalisation et aux processus de management. La direction du laboratoire veille au maintien de la cohérence du système de management de la qualité. Nos efforts sur la validation des méthodes d analyses sont à entretenir pour les portées accréditées. Cette planification s organise à partir des éléments suivants : Eléments d entrée Eléments de sortie Objectifs qualité du laboratoire Besoins et attentes des clients Exigences réglementaires normes Performance des processus Adéquation du produit et des services associés Non conformités et incidents Adéquation de la gestion documentaire Evaluation des fournisseurs Réunions FIAQ Réunion RSA Processus de Planification de la qualité Renforcement du savoir faire et des connaissances Ajustement des ressources (aménagement des locaux, personnel, matériels et fournitures) Amélioration des méthodes et de l organisation Suivi de nouveaux indicateurs de qualité Le Responsable Qualité est chargé de vérifier et de suivre le bon déroulement et l organisation de la planification du système de management de la qualité. Les résultats de la planification de la qualité (données de sortie) sont analysés au cours des revues de direction. Des ajustements éventuels sont décidés par la direction sous forme de plans d amélioration. La planification de la qualité donne lieu à des réunions avec la participation du personnel : réunion FIAQ : fiches d incidents et amélioration individuelle de la qualité. Réunions de revue de direction Fréquence : 1 par an. Des revues dénommée RSA sont effectuées à intervalles planifiés pour répondre aux exigences de la norme ISO :2012 revue des écarts des évaluations COFRAC, revue des valeurs de références, revue du plan d action de revue de direction, revue des méthodes d analyse des portées d accréditation (RSA, réunion technique). RSA : réunion suivi accréditation Laboratoire ADEBIO - MQ-I-SMQ Page 23/50
24 6.5 Responsabilité de la direction et communication (Chap. 4.1 ISO 15189) La direction du laboratoire ADEBIO est chargée de définir et de communiquer la politique et les objectifs qualité à l ensemble de l équipe du laboratoire. Pour déployer la politique et les objectifs qualité la direction du laboratoire a défini une organisation du système qualité faisant intervenir : - La direction du laboratoire Responsabilité technique - le responsable qualité - les correspondants qualité - l assistante qualité - les référentes par secteur d activité : o référentes secteur technique (sous forme de qualification habilitation) : Technicienne référente hématologie Technicienne référente hémostase Technicienne référente biochimie Technicienne référente bactériologie Technicienne référente mycologie o référente métrologie o correspondants métrologie o référente secrétariat accueil o référente prélèvements infirmières o référente hygiène et sécurité o référentes processus financier Les responsabilités et autorités sont décrites dans les fiches de fonction, les qualifications et habilitations (KALILAB ). Celles-ci reprennent les responsabilités, autorités, objectifs qualité afférents à chaque activité et poste de travail. Le logiciel qualité permet d enregistrer les qualifications et habilitations. Les qualifications et habilitations du personnel sont organisées, documentées et donnent lieu à des enregistrements permettant de prouver et suivre les aptitudes, les responsabilités. Processus RESSOURCES HUMAINES Procédures associées : PR-I-GRH Qualification habilitation du personnel PR-I-GRH Recrutement PR-I-GRH-005 -Organisation des ressources humaines Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 24/50
25 ORGANIGRAMME FONCTIONNEL ET HIERARCHIQUE (Chap. 5.1 ISO 15189) L organigramme nominatif à jour est disponible sur chaque site du laboratoire ADEBIO Laboratoire ADEBIO - MQ-I-SMQ Page 25/50
26 Organisation de la communication interne : Elle repose sur des réunions régulières, en interaction, qui impliquent toute l'équipe du laboratoire. Cette communication interne entretient la dynamique de management de la qualité en faisant intervenir toutes les fonctions du laboratoire. Remontées "Terrain" Non conformités Réclamations Suggestions (enquêtes, personnel) Accueil - secrétariat Prélèvements Techniques Logistique Comptes rendus "secteurs" Plan d'actions Diffusion secteur Comptes rendus "secteurs" Plan d'actions Remontées "Terrain" Non conformités Réunion FIAQ Réunion RSA Direction RQ Référent(e)s Comptes rendus "FIAQ" / RSA Plan d'actions Diffusion Comptes rendus "FIAQ" / RSA Plan d'actions Revue de direction Comptes rendus "Revue de direction" Plan d'actions Diffusion Cette communication interne est relayée par la messagerie KALILAB, le bulletin interne ADEBIO, la messagerie HEXALIS (SIL) FIAQ : fiches d incidents et amélioration individuelle de la qualité RSA : réunion de suivi accréditation Processus 01 ORGANISATION MANAGEMENT Processus - 02 AMELIORATION CONTINUE Procédures associées : PR-I-RDD-001-Revue de direction PR-I-GRH-005-Organisation des ressources humaines Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 26/50
27 6.6 Revue de direction (Chap ISO 15189) L organisation de revues de direction permet de mesurer l efficacité du système de management de la qualité mis en œuvre (ISO 15189:2012 chap. 4.15). La périodicité est annuelle. Ces réunions sont organisées par la direction du laboratoire, le responsable qualité à partir des données des différents éléments d entrée de la revue (non conformités produits et processus, réclamations, rapports et résultats des audits internes, état d avancement des actions correctives et préventives, enquêtes de satisfaction et retour d informations clients, le compte rendu de la revue de direction précédente, les modifications de la réglementation à prendre en compte, les propositions d amélioration). L équipe du laboratoire participe, par secteur, à la préparation et la présentation des données de revue de direction. La direction entérine les actions d amélioration à mettre en œuvre en cohérence avec la politique et les objectifs qualité du laboratoire. L ordre du jour de la revue de direction reprend les exigences de la norme ISO :2012. Le compte rendu de réunion validé par la direction du laboratoire comporte les conclusions et décisions communiquées à l ensemble du personnel du laboratoire. Les décisions sont formalisées dans un plan d amélioration suivi à l aide de KALILAB (gestion de projet). Processus 02 AMELIORATION CONTINUE Procédures associées : PR-I-RDD-001-Revue de direction PR I-NC-001- Identification Maîtrise des non conformités PR-I-AC-001-Actions correctives et actions préventives Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 27/50
28 7 MANAGEMENT DES RESSOURCES Les exigences de formation, compétences pour diriger un laboratoire relèvent du domaine réglementaire ainsi l organisation des locaux et les exigences d hygiène et de sécurité. L utilisation de l informatique de laboratoire respecte les dispositions de la CNIL et les recommandations du GBUI (Guide de Bonne Utilisation de l Informatique dans les Laboratoires de Biologie Médicale). La politique des ressources humaines du Laboratoire ADEBIO fixe les conditions favorables aux transformations liées à notre développement et créer les conditions pour l adaptation du laboratoire aux changements, en promouvant la démarche d amélioration continue, le développement des compétences et en incitant à la prise de responsabilités et l implication de chaque acteur du laboratoire dans le respect de trois principes fondamentaux COMMUNICATION CONCERTATION - COOPERATION Cinq axes majeurs sont mis en avant dans notre politique des ressources humaines : o Développer l efficacité et l efficience du travail en équipe o Développer la culture de la qualité o Motiver le personnel par des missions et responsabilités o Améliorer le partage de l information au sein du laboratoire o Responsabiliser et créer les conditions de l engagement des salariés 7.1 Ressources humaines Le personnel (Chap. 5.1 ISO 15189) La politique en matière de gestion du personnel est centrée sur la responsabilisation, le développement des compétences, l implication de chaque acteur dans le management de la qualité, la sécurité et la prévention des risques. Cette politique se traduit par une forte communication en interne : réunions de secteur, réunions FIAQ, RSA, participation active aux revues de direction. Le recrutement de personnel s appuie sur les définitions de fonction, les qualifications (niveau de compétence requis) en vue de répondre aux besoins immédiats et futurs. Le recrutement est conduit par le directeur du laboratoire en collaboration avec l équipe du secteur concerné avec l assistance du service ressources humaines. Un dossier individuel du personnel est ouvert et tenu régulièrement à jour. Il est également organisé, sur le logiciel qualité KALILAB rubrique personnel. Une déclaration à la CNIL, de ce traitement informatique, n NS-046, a été réalisée. Toute embauche définitive est précédée d'une période d'essai au cours de laquelle le directeur du laboratoire veillera aux points suivants : - Les connaissances générales - La pratique professionnelle - L'aptitude technique ainsi que la capacité d'adaptabilité à différents types de matériels - L'aptitude à s intégrer à l équipe - Le respect des procédures et des règles en vigueur et du code d éthique de la profession. - La compréhension et l'adaptation à la Politique Qualité mise en place au sein de l'entreprise A la fin de la période d essai, la direction décide alors de l'intégration de la personne dans le laboratoire. Laboratoire ADEBIO - MQ-I-SMQ Page 28/50
29 Chaque personne du laboratoire se voit attribuer une ou plusieurs fonctions décrivant les missions principales, attributions spécifiques à la fonction occupée. Un entretien individuel professionnel et d évaluation est effectué par le directeur du laboratoire avec chaque salarié pour formaliser des objectifs et identifier les besoins de formation. La formation continue du personnel est définie dans un plan annuel de formation validé par le directeur des ressources humaines en collaboration avec les biologistes responsables de site et le service ressources humaines à partir : - des projets prioritaires du laboratoire, - des besoins exprimés par le personnel, - des besoins de maintien à niveau des connaissances et des compétences du personnel. Des formations hors plan peuvent être réalisées si nécessaire. Les formations sont réalisées par des organismes externes ou par les personnes habilitées en interne. Le suivi de la réalisation du plan est sous la responsabilité du biologiste en charge des RH. Les attestations de formation externe ou interne sont suivies et classées dans les dossiers du personnel par l assistante qualité. Le laboratoire a mis en place un système d information pour permettre l acquisition et le maintien des connaissances en relation avec les secteurs d activité : - revues scientifiques, - note d informations, - compte rendu «relations extérieures» (rencontres IDE, médecins) - fiches biologiques - participation à des manifestations scientifiques (congrès, colloques) - e. formation (Medicinimage, ) Les qualification et habilitations sont documentées et validées par les biologistes (encadrement technique) pour les tâches et les activités qui nécessitent des compétences ou des autorisations particulières et par le responsable qualité (métrologie, audit interne). Pour le personnel technique, la qualification correspond à la confirmation par examen et/ou apport de preuves tangibles qu une ou plusieurs compétences techniques sont acquises. Une habilitation est une autorisation accordée à une personne ou une fonction d accomplir une action donnée en lien avec une qualification. Tout salarié du laboratoire est soumis au respect de la confidentialité et du secret professionnel. Un engagement de confidentialité est signé par chaque personne et est archivé dans le dossier du personnel. Processus RESSOURCES HUMAINES Procédures associées : PR-I-GRH-005-Organisation des ressources humaines PR-I-GRH-002-Recrutement PR-I-GRH-001-Qualification Habilitation du personnel PR-I-GRH-004-Règlement intérieur Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 29/50
30 7.2 Locaux environnement Matériel (Chap ISO 15189) Le laboratoire satisfait aux exigences réglementaires en matière de superficie allouée aux activités techniques, au secteur d activité nécessitant un confinement particulier (prévention des risques de contamination croisée), aux contrôles des accès et au stockage des DASRI avant leur élimination (local dédié). Les sols, surfaces de travail et sanitaires sont désinfectés selon des pratiques conformes à la profession. Des contrôles bactériologiques des surfaces sont organisés régulièrement (2/an - site technique activité mycologie. Toutes les 2 semaines pour l activité biologie de la reproduction). Cette démarche relève de l analyse de risque (notamment risque de contamination croisée et risque microbiologique plus largement) avec mise en place d une démarche préventive sous forme de contrôles de surfaces réguliers, planifiés. L accès au laboratoire et la circulation à l intérieur sont limités et définis par affichage. Tout visiteur ou intervenant extérieur s identifie dans un registre (date, nom, signature). Toutes les installations (extincteurs, électrique, gaz) font l objet de contrôles par des sociétés spécialisées agrées par la DRIRE. Un certificat de conformité est délivré. Le document unique relatif à la sécurité des travailleurs est tenu à jour en conformité avec la réglementation. Il a pour but de prévenir les risques et effets des incidents malencontreux. (Mise en place d un CHSCT nov. 2014) Le secteur bactériologie est isolé et répond aux exigences de confinements, un PSM type II garantit la sécurité de l opérateur et de l environnement. L accès est limité aux personnes autorisées : techniciennes, biologistes. Le secteur thérapeutique de biologie de la reproduction est isolé et répond aux exigences de confinements, avec des moyens appropriés : PSM type 2 (sécurité opérateur et environnement), accès par un SAS limité aux personnes autorisées : techniciens, biologistes, agent d entretien. Le laboratoire met à la disposition du personnel des moyens adaptés à l environnement de chaque poste de travail et à la sécurité inhérente aux conditions de travail : EPI, Equipement de protection collectif. Pour le secteur biologie de la reproduction : tenues spécifiques, opérations d entretien adaptées aux contraintes des zones concernées. Des consignes précises relatives à l hygiène et à la sécurité du personnel sont définies afin de prévenir tout risque pouvant nuire à la sécurité des personnes et à la qualité des analyses. La prise en charge des patients respecte les mesures de sécurité et de confidentialité. Les moyens mis en œuvre sont multiples : - Affichage des consignes de sécurité - Liste et conditions de stockage des produits dangereux - Règles de tri et élimination des déchets - Lavage des mains et règles d hygiène et dispositifs appropriés - Contrôles bactériologiques des surfaces - Affichage CNIL et réglementaire à l accueil - Salle de détente pour le personnel en dehors des secteurs techniques - Vestiaires du personnel avec casier individuel sécurisé dont l emplacement respecte le principe de la marche en avant (se changer avant d accéder aux secteurs techniques). - Sanitaires pour le personnel, distincts des sanitaires «clients» - Document Unique d identification et d évaluation des risques - Politique de désinfection des locaux avec prise en compte des zones à risques. - Limitation et contrôles des accès aux secteurs techniques Laboratoire ADEBIO - MQ-I-SMQ Page 30/50
31 Le document unique relatif à l évaluation des risques professionnels dans l unité de travail traduit l ensemble des moyens mis en œuvre au laboratoire pour la prévention des risques et accidents conformément au décret n du 5 novembre Le personnel est sensibilisé au risque incendie. Le personnel technique est formé aux premiers soins (AFPS) et/ou soins d urgence AFGSU. La direction du laboratoire s est engagée dans une politique de formation aux soins d urgence de niveau II pour le personnel technique en application des dispositions réglementaires relatives aux prélèvements sanguins réalisés à distance du laboratoire par ce personnel technique (actions de formations). AFPS : Attestation de Formation aux Premiers Soins. AFGSU : Attestation de Formation aux Gestes et Soins d Urgence PSM : Poste Sécurisé de Microbiologie DASRI : Déchets d Activité de Soins à Risque Infectieux. Matériel de mesure et d essais Le matériel est installé par le fournisseur ou le fabricant qui est responsable de sa mise en service et de son bon fonctionnement. Un dossier de vérification de méthode (portée flexible A) est constitué par le laboratoire et le personnel technique concerné, avec la preuve des essais de qualification à la mise en service. La maintenance préventive des équipements est réalisée par le personnel technique en suivant les instructions décrites dans les modes opératoires et consignes fournisseurs afin de maintenir le parc matériel en parfait état de fonctionnement et en appliquant les dispositions du fabricant. Toutes les actions de maintenance sont enregistrées sur le logiciel qualité. Les équipements sont référencés et identifiés. Un dossier de vie est organisé pour chaque matériel. Des visites de contrôle contractuelles sont réalisées par le fabricant ou son mandataire qui qualifie le matériel après intervention. Le laboratoire a mis en place une surveillance de ses équipements de mesure soumis à métrologie pour leur vérification et étalonnage. Sous la responsabilité du responsable qualité, la technicienne référente métrologie est responsable de la gestion des équipements soumis à la métrologie. Elle tient à jour la liste des matériels du laboratoire faisant l objet d étalonnage et de vérification et en coordination avec l équipe des correspondants métrologie. Les matériels (y compris les logiciels) sont gérés (à l aide du logiciel qualité KALILAB) : liste, fiche signalétique, fiche de vie (maintenances). Les grandeurs physiques sont documentées et font l objet de surveillance étalonnage et/ou vérification régulière : la température, les volumes, la vitesse (accélération) et le temps (centrifugation). Les opérations de vérifications et de raccordements aux étalons de références sont effectuées par des prestataires compétents, chaque fois que possible (attestations d accréditation gérées). Les certificats de vérification et d étalonnage sont conservés et disponibles. Pour la maîtrise des températures, le laboratoire est doté d une gestion centralisée des températures (VIGITEMP ), d une sonde de référence étalonnée pour réaliser l étalonnage des sondes de surveillance et d un module de caractérisation des enceintes thermiques (VIGICART2 ). Ces opérations sont réalisées en interne (hormis l étalonnage de la sonde de référence et des sondes VIGICART). Laboratoire ADEBIO - MQ-I-SMQ Page 31/50
32 Processus 11 LOCAUX ENVIRONNEMENTS Processus 12 GESTION DES MATERIELS Procédures associées : PR-I-LCE Sécurité Hygiène Installation des locaux PR-I-LCE Entretien - Maintenance matériels et locaux PR-I-LCE Tri et élimination des déchets PR-I-ACH Achats PR-I Gestion du système informatique et système d'information PR-I-MAT Maitrise des équipements de mesure PR-I-MAT CAT en cas de panne ou incident sur les équipements de mesures métrologie PR-I-ECH Transmission d'analyses aux laboratoires sous-traitants Versions applicables 7.3 Services externes et approvisionnements (Chapitre 4.6 ISO 15189) Maîtrise des processus achats et approvisionnements Politique d achats : La politique de sélection et d'utilisation de services, d'équipements et de consommables est fondée sur : - l'expression des besoins du laboratoire (cahier des charges) - le choix de prestataires de services informatiques expérimentés (antériorité, base clients,...) ou accrédités COFRAC (métrologie) - le choix des fournisseurs de DMDIV référencés au SFRL, ou dans les groupements d'achats de laboratoire, apportant la preuve de la maîtrise de la qualité par la certification NF EN ISO9001 et/ou ISO 13485, ou de prestataires accrédités (ex : métrologie, OCIL, ). - l'évaluation régulière des fournisseurs et prestataires dits "critiques" - la gestion de la liste des fournisseurs sélectionnés et approuvés - les contrôles et vérifications des produits et matériels achetés La politique des achats, définie par la Direction du laboratoire, comprend l achat de matériel, de consommables, de réactifs et de prestations de services. Les responsabilités en matière d'achats relèvent de la direction du laboratoire. Les points majeurs relatifs à la maîtrise des achats et approvisionnements : - définition de la politique d achats, - identification des fournisseurs potentiels, - évaluation et sélection des fournisseurs : o élaboration du questionnaire, o choix du fournisseur, o liste des fournisseurs approuvés o traitement des livraisons non conformes o suivi et évaluation des fournisseurs (critiques) - contrôle des commandes et livraisons de produits et matériels, - enregistrement des informations et suivi des fournisseurs en matière de Qualité (respect des délais, conformité des livraisons, documents techniques à fournir avec les produits,...). - le consommable du laboratoire de biologie de la reproduction est embryotesté et stérilisé aux rayons gamma. Aucune autre méthode de stérilisation n est acceptable. Un suivi des performances des fournisseurs sélectionnés est réalisé par le service qualité en collaboration avec les utilisateurs des produits et services. La synthèse globale sur l évaluation des Fournisseurs «critiques» est présentée en revue de direction. Le logiciel qualité KALILAB du laboratoire permet la gestion et le suivi des évaluations des fournisseurs critiques, de la liste des fournisseurs approuvés. Les enregistrements des évaluations sont conservés. PR-I-SST Evaluation - Sélection des fournisseurs - LBM sous-traitants - OCIL Laboratoire ADEBIO - MQ-I-SMQ Page 32/50
33 Les réactifs et consommables choisis lors de la validation de nos méthodes, sont enregistrés sur le logiciel de stock et seuls ces réactifs peuvent être commandés, une vérification à la livraison est systématiquement effectuée. Le laboratoire met en œuvre un système informatique de contrôle de l inventaire des produits et fournitures. Chaque secteur est responsable de la gestion des stocks. Les réactifs et consommables du laboratoire sont répertoriés. La gestion des stocks et approvisionnements se fait à l aide du logiciel qualité du laboratoire, dont la surveillance des produits périmés Informations relatives aux achats Tous les documents joints au produit acheté sont regroupés (service comptabilité) Vérification du produit acheté Toute livraison au laboratoire fait l objet d un contrôle à réception du produit livré, par rapport au bon de livraison et à la commande initiale. La mise en service d un équipement est accompagnée d un certificat de qualification d aptitude à l utilisation délivré par le fournisseur. Les essais pour établir les dossiers de vérification de méthodes sont organisés en rapport avec la politique d accréditation de la direction du laboratoire. Toute non-conformité fait l objet d un enregistrement et un traitement est effectué par le secteur ayant passé la commande auprès du fournisseur. La défaillance des fournisseurs est surveillée. Les données d évaluation, les non conformités sont présentées en revue de direction. Processus 07 ACHATS APPROVISIONNEMENTS Procédure associée : PR-I-SST Evaluation - Sélection des fournisseurs - LBM sous-traitants - OCIL PR-I-ACH Achats Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 33/50
34 7.4 Informatique : gestion des informations du laboratoire (chap ISO 15189) Le système informatique du laboratoire est sous la responsabilité d un biologiste médical coresponsable, administrateur informatique. Un contrat de maintenance (télémaintenance et intervention sur site) est établi avec le fournisseur du SIL. L accès au système et aux applications est limité par attribution d'un mot de passe et d un code utilisateur propre à chaque utilisateur. Le système informatique du laboratoire (SIL) est protégé, dans son accès, par des codes utilisateurs et mots de passes individuels conformes aux dispositions de la CNIL. Le responsable informatique du laboratoire attribue les autorisations d'utilisation du SIL au personnel, selon leur fonction et responsabilités respectives. Tous les fichiers système, programme et application sont sauvegardés quotidiennement avec les données relatives aux patients sur des supports distincts. Les supports sont stockés dans un lieu permettant de préserver l intégrité des données à tout moment et la confidentialité. Un registre des pannes, des modifications des paramétrages et des mises à jour des versions est régulièrement tenu. Le système informatique est déclaré à la CNIL conformément à la Loi n du 6 janvier 1978 relative à l informatique, aux fichiers et aux libertés. Les clients du laboratoire sont informés de ces dispositions réglementaires par affichage. Validation du SIL : Sous la responsabilité du responsable informatique du laboratoire, des tests de connexion informatique (interfaces, analyseurs) sont effectués. L utilisation de tableurs est protégée en écriture en accès, chaque fois que nécessaire. Les traitements informatiques pour effectuer des calculs en lien avec les analyses sont validés par des tests. Les preuves des essais et des tests sont conservées. Des conventions de preuves sont mises en place avec les médecins destinataires de résultats par voie électronique. La politique de protection des informations confidentielles s'appuie sur l'engagement de chaque membre de l'équipe du laboratoire traduit dans une clause de confidentialité et dans le règlement intérieur. La direction du laboratoire s'assure que les fournisseurs de DMDIV mis en œuvre au laboratoire sont signataires de la clause de confidentialité lors d interventions sur site (registre) et que le ou les prestataires informatiques respectent une clause de confidentialité contractuelle. Sources (portail KALILAB): ANSSI : CNIL : ASIP Santé : Processus 13 GESTION DU SYSTEME D INFORMATION - SIL Procédures associées : PR-I-ACH-001 : Achats PR-I-LCE-003 : Entretien - Maintenance matériels et locaux PR-I : Gestion du système informatique et système d'information PR-I-ACC-001 : Accueil enregistrement des dossiers règlements PR-I-CRR-002 : Compte-rendu de résultats PR-I-GRH-001 : Qualification-Habilitation du personnel Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 34/50
35 8 REALISATION DES ANALYSES - (Chap ISO 15189) 8.1 Revue de contrat (Chapitre 4.4 ISO 15189) Détermination des exigences - besoins Politique de revue de contrat : La politique du laboratoire, en matière de revue de contrat, est de formaliser, sous forme d'une convention, chaque fois que nécessaire et possible, les prestations de services en lien avec une structure de santé : EHPAD - Hôpitaux locaux, convention portant sur la réalisation du prélèvement en dehors du laboratoire. De manière générale, le laboratoire effectue une revue de contrat avant de s engager à réaliser les examens demandés. La revue de contrat précise les critères d acceptation des demandes d examens. Cette revue fait l objet d un enregistrement (SIL). Dans le cas où un patient se présente sans prescription médicale, la personne autorisée du laboratoire mène une revue de contrats, avant que le laboratoire ne s'engage à réaliser les examens de biologie médicale demandés, ceci afin d'assurer que les exigences implicites et explicites du patient, et les exigences normatives, législatives, réglementaires et les recommandations de bonnes pratiques sont bien prises en compte. Cette revue de contrats a également pour objectif de prouver que le LBM a les ressources et capacités nécessaires, par sa compétence et grâce à l'utilisation de méthodes répondant aux besoins cliniques du patient, pour réaliser les examens de biologie médicale demandés. Cette revue est réalisée lors de la prise en compte de la demande du patient et porte plus particulièrement sur critères suivants : renseignements cliniques pertinents utiles, conditions et délais de réalisation, modalités de communication des résultats, conditions de facturation et accord du patient sur les montants de la prestation de soins. Dans tous les cas le laboratoire incite vivement le patient a consulté son médecin habituel pour une prise en charge médicale efficiente Revue des exigences Les demandes d examens (information sur la réalisation des analyses, prélèvement, tarification, délai de rendu des résultats, destinataires, modalités de transmission des comptes rendus d analyses) sont vérifiées et enregistrées par le secrétariat du laboratoire. Toute modification portant sur la demande d examen est enregistrée et communiquée au personnel concerné (exemple : examen non réalisé à la demande du patient, ). L adaptation éventuelle de la prescription médicale est faite après échange avec le prescripteur, sauf en cas d urgence et d indisponibilité (CSP L ) dans le respect de la NABM ou des recommandations (HAS). En cas de sous-traitance, la secrétaire ou le biologiste informe le patient et s assure du respect des besoins, attentes et accord de celui-ci (examens HN, consentements, ) Communication avec le client Le personnel du secrétariat est autorisé à communiquer des informations relatives aux clients, dans le respect des règles de confidentialité. Les commentaires, avis et interprétations des résultats d analyses sont réservés exclusivement au biologiste. En cas d incidents ou anomalies (échantillons biologiques non conformes, délai de rendu des résultats non respecté ), le patient et/ou le médecin sont informés, le cas échéant. Une solution est recherchée, des enregistrements appropriés sont effectués. Laboratoire ADEBIO - MQ-I-SMQ Page 35/50
36 8.2 Processus pré analytique (chapitre 5.4) Débute à partir de l interprétation de la prescription médicale nécessaire à la réalisation du prélèvement. La revue de contrat ou revue des exigences est effectuée au cours de cette étape soit par la secrétaire du laboratoire au moment de l accueil du patient, soit par l infirmière pour un prélèvement effectué en dehors du laboratoire (patient à domicile, patient hospitalisé). Les prescriptions médicales sont accompagnées d une fiche de suivi médicale permettant l identification du patient et le recueil d informations utiles à la réalisation des analyses et la transmission des comptes rendus d analyses (renseignements cliniques pertinents). Voir également 8.4 La réalisation du prélèvement est effectuée par des professionnels de santé habilités selon des instructions spécifiques relatives au prélèvement et à la manipulation des échantillons primaires. (ou par le patient : urines, selles, sperme, ). La vérification de l identité des patients, en cohérence avec les procédures du laboratoire (vérification par identification positive) pour prévenir tout risque d erreur est systématiquement réalisée par le personnel habilité du laboratoire sensibilisé sur ce risque critique (Identitovigilance). Les fonctions, qualifications et habilitations pour la réalisation des prélèvements sont définies. Toute demande d examens est enregistrée sur le système informatique du laboratoire dans un dossier patient informatisé et identifié par un numéro unique. Les documents fournis par le patient sont scannés (chaque fois que possible) et joints à la demande d examens gérée dans le SIL. Tous les documents produits dans le processus de réalisation des analyses ainsi que les échantillons biologiques sont identifiés, étiquetés par un identifiant unique (numérique et code à barres). La communication avec les clients est formalisée et enregistrée à partir d une fiche de suivi qui accompagne chaque prélèvement. La traçabilité des évènements clés est organisée. Le personnel technique est autorisé à procéder à l aliquotage des échantillons, le cas échéant. En cas de fractionnement (aliquotage) des tubes primaires, un mode opératoire permet d éviter toute erreur d identification. Les échantillons sont ensuite transmis aux différents secteurs d activité. L aliquotage est limité au personnel technique autorisé. Les non conformités pré analytiques sont enregistrées, depuis janvier 2016, à l aide du logiciel HEXALIS (module qualité) dans les dossiers patients (NC ou réclamations contextuelles aux demandes d examens). Les flux de patients «entrées/sorties» sont conçus dans le respect de la confidentialité. Les échantillons biologiques sont conservés avant et après analyse dans des conditions garantissant la stabilité de leurs propriétés afin de permettre toute vérification éventuelle ou analyses complémentaires. Les documents et produits fournis par le client sont pris en charge dans des conditions optimum de sécurité et d intégrité. Les documents fournis par chaque patient sont regroupés dans une pochette plastique individuelle et/ou scanner dans le dossier de chaque patient. Les exigences particulières (urgent) sont signalées par un enregistrement. Tout dossier présentant une difficulté détectée après la prise en charge (information incomplète, anomalies d'identification, erreurs, ) fait l objet d un traitement particulier. Laboratoire ADEBIO - MQ-I-SMQ Page 36/50
37 Processus 03 - PREANALYTIQUE Procédures associées : PR-I-RDC-001 Revue de contrat PR-I-ACC Accueil - Enregistrement des dossiers Règlements PR-I-ECH Transmission d'analyses aux laboratoires sous-traitants PR-I-PRLV Prélèvements PR-I-PRLV Prise en charge / Transport des échantillons biologiques PR-I-PRLV-003 Prélèvement sanguin chez un enfant ou NN pédiatrie PR-I-PDC-001 Prestation de conseils Versions applicables 8.3 Processus analytique (chapitres 5.5 et 5.6) Les opérations relatives à la mise en œuvre des techniques analytiques sont réalisées selon les modes opératoires en vigueur au laboratoire et à disposition immédiate du personnel. Les méthodes d analyses sont évaluées et validées pour les sous-familles d examens des portées d accréditation (sous-famille d examens). Ce principe se développe avec le déploiement progressif de l accréditation à toutes les activités. La réalisation des analyses se fait par le personnel qualifié et habilité : technicien(ne)s, biologistes. La performance analytique est contrôlée par un programme de contrôles internes de qualité et par la participation à des programmes d évaluation externe de la qualité (par comparaisons inter laboratoires). Le laboratoire, chaque fois que cela est pertinent, est en mesure de déterminer l incertitude de mesure associée aux résultats. Le contrôle de qualité analytique (interne et externe) avant analyse participe à la validation de la production des analyses, étape sous la responsabilité des technicien(ne)s habilité(e)s et des biologistes de l encadrement technique. Les matériels utilisés pour la réalisation des analyses sont contrôlés et maintenus selon les préconisations des fabricants. La qualification du personnel technique est définie. Les habilitations sont documentées et enregistrées. Les échantillons biologiques sont stockés et conservés après analyse dans des conditions garantissant leur sécurité et leur intégrité, pour permettre d éventuels examens complémentaires ou vérifier l identité portée sur les échantillons (Identitovigilance). Notamment pour permettre la réalisation d analyses complémentaires ou la répétition des analyses. Toute la documentation technique d origine externe est validée pour application au laboratoire par la direction du laboratoire. La vérification des équipements de mesure est effectuée périodiquement pour établir la conformité métrologique. Revue des méthodes d analyses Les méthodes d analyses sont développées, conçues, validées par l industrie biomédicale et adoptées sans modification par le laboratoire. Les réactifs de laboratoire mis en œuvre sont inscrits à l ANSM : Agence National de Sécurité du Médicament et des Produits de Santé et/ou et conformes au marquage CE. Il est de la responsabilité du directeur du laboratoire de s assurer de la vérification des méthodes d analyses par le fabricant (industrie biomédicale). Laboratoire ADEBIO - MQ-I-SMQ Page 37/50
38 Le laboratoire établit un dossier de vérification ou de validation des méthodes d analyses selon la portée (type A ou B) et selon les dispositions des documents COFRAC SH Inf 50, SH GTA 04 pour les analyses de la portée d accréditation et selon les exigences du chapitre 5.5 de la norme ISO Processus 04 - ANALYTIQUE Procédures associées : PR-I-ANA-003 : Vérification - Validation des méthodes d analyse PR-I-POST-002 : Validation technique des résultats d'analyses PR-I-ANA-004 : Gestion portée flexible A ou B PR-I-AQA-002 : Gestion du Contrôle Interne de Qualité PR-I-AQA-001 : Gestion du contrôle de qualité Externe et National PR-I-AQA Résultats hors limites d'un CIQ PR-I-ECH-006 : conservation des échantillons biologiques PR-I-BIOCH-002 : Biochimie Immunoanalyses COBAS 6000 PR-I-BIOCH-005 : Hémoglobine glycquée G8 TOSOH PR-I-HEM-001 : Hématologie PR-I-IH-001 : Immunohématologie IH1000 PR-I-COAG-002 : Hémostase STA-R STAGO PR-I-BAC-001 : Bactériologie PR-I-MYCO-001 : Mycologie Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 38/50
39 8.4 Processus post analytique Compte rendu de résultats (chapitre ISO 15189) Le biologiste est responsable de la revue (validation biologique) et la mise en forme des comptes rendus de résultats. Il vérifie la conformité des résultats d analyses par validation biologique informatique et engage sa responsabilité en signant le compte rendu d analyses. Le biologiste s assure, également, que les résultats sont lisibles et ne comportent pas d erreur de transcription. Les comptes rendus de résultats signés par le biologiste peuvent être communiqués aux destinataires par distribution ou envoi postal. La transmission des résultats d analyses est effectuée par tous les moyens disponibles de traitement de l information, à savoir : la distribution postale classique ou automatisée, la distribution organisée par le laboratoire (tournée de distribution), le courrier électronique avec transmission sécurisée via HPRIM médecin, HPRIM Net, la télétransmission par fax. Les recommandations de la CNIL sont appliquées pour la transmission des données nominatives. Pour l activité biologie de la reproduction, les médecins du Centre AMP(1) ont accès aux résultats sur le logiciel commun MEDIFIRST. (1) : Assistance Médicale à la Procréation. Les comptes rendus de résultats d analyses sont édités sur papier à entête comportant les mentions réglementaires concernant le laboratoire et le patient. Figurent notamment : -le libellé des analyses -les résultats d analyses -les valeurs de références tenant compte du sexe et de l âge (chaque fois que cela est pertinent et possible). -les commentaires éventuels : avis et interprétation, le cas échéant. -la méthode ou technique utilisée -le laboratoire sous-traitant éventuel -résultat partiel ou définitif Les résultats qui se situent dans les intervalles «d alerte» ou «critiques» sont diffusés et communiqués sans délais, après accord du biologiste. Ces transmissions sont enregistrées (HPRIM, téléphones) dans le dossier patient HEXALIS. Des conventions de preuves sont mises en place avec les médecins destinataires des résultats par transmission électronique (démarche en cours de déploiement). En pratique, tous les résultats d examens courants (ou de routine) sont communiqués dans la demi-journée suivant le prélèvement de l échantillon (exception : les prélèvements réalisés en fin de journée et dont la conservation est possible sont traités à j+1, dans la demi-journée suivante). La modification éventuelle de résultats, après diffusion, fait l objet de disposition, d enregistrements et conservation appropriés. HPRIM : Harmoniser et Promouvoir l Informatique Médicale Processus 05 - POSTANALYTIQUE Procédures associées : PR-I-POST-001 : Validation biologique PR-I-CRR-002 : Compte rendus de résultats PR-I-CRR-001 : Résultats pathologiques à téléphoner PR-I-PDC-001 Prestation de conseils PR-I-ECH-006 : conservation des échantillons biologiques PR-I-ECH-004 : Gestion de la sérothèque Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 39/50
40 ETAPES DES PROCESSUS DE REALISATION DES ANALYSES PROCESSUS PREANALYTIQUE (Chapitre 5.4 ISO 15189) Médecin Patient Clients EXIGENCES Préleveur externe Pharmacies Etablissements de santé Prélèvement «entrants» «sortants» Transport PROCESSUS PRE ANALYTIQUE Demande d examens Prescriptions médicales Manuels ou guides de prélèvement PRISE EN CHARGE DES DEMANDES D'EXAMENS REVUE DE CONTRAT PRELEVEMENT TRAITEMENT DES ECHANTILLONS Fiche de prélèvement étiquettes Echantillons biologiques identifiés Dossier enregistré Instruction Conditions de transport Processus ANALYTIQUE Transport Clients internes : techniciennes et biologistes Laboratoires sous traitants Laboratoire ADEBIO - MQ-I-SMQ Page 40/50
41 PROCESSUS ANALYTIQUE (chapitre ISO 15189) «entrants» «sortants» Instructions réception, étiquetage, centrifugation, aliquotage, stockage, conservation TRAITEMENT DES ECHANTILLONS BIOLOGIQUES Etiquetage Centrifugation - Vérification PROCESSUS ANALYTIQUE Procédures et modes opératoires sur la réalisation des analyses PREPARATION ET CONTROLE TECHNIQUE CONTROLE INTERNE ET EXTERNE DE QUALITE REALISATION DES ANALYSES METHODES VALIDEES CONTROLES VALIDATION ANALYTIQUE CONSERVATION DES ECHANTILLONS BIOLOGIQUES Résultats d analyses validés au plan analytique Processus POSTANALYTIQUE Clients internes : biologistes - secrétaires Laboratoire ADEBIO - MQ-I-SMQ Page 41/50
42 PROCESSUS POSTANALYTIQUE (Chapitre ISO 15189) «entrants» «sortants» PROCESSUS POST ANALYTIQUE Résultats d analyses validés techniquement VALIDATION BIOLOGIQUE DES RESULTATS REVUE DES COMPTES RENDUS DE RESULTATS PAR LE BIOLOGISTE AVIS - INTERPRETATIONS TRANSMISSION - DIFFUSION DES COMPTES RENDUS DE RESULTATS Comptes rendus signés et traités selon les exigences spécifiées Patient Médecin Clients RETOUR - SATISFACTION Chapitre 4.8 ISO Procédures associées : PR-I-REC-001-Traitement des réclamations clients PR-I-RDC-001-Revue de contrat PR-I-ACC-001-Accueil-Enregistrement des dossiers - Règlements PR-I-MDD-004-Gestion de la confidentialité et protection des informations confidentielles PR-I-ANA-003 : Procédure de validation des méthodes d analyses PR-I-ANA-004 : Procédure de gestion de portée flexible A ou B PR-I-NC-002: Procédure de réactovigilance Versions applicables. Laboratoire ADEBIO - MQ-I-SMQ Page 42/50
43 8.5 Analyses transmises à des laboratoires sous-traitants (Chapitre 4.5 ISO 15189) Politique de sous-traitance : Le Laboratoire peut être amené à transmettre des analyses ne faisant pas partie du champ de l accréditation ou qu il ne réalise pas dans les situations suivantes : Systématique : o Examens de biologie médicale spécialisés non réalisés au Laboratoire (hors catalogue ADEBIO), o Optimisation des plateaux techniques avec mise en place de contrat de coopération. Occasionnel : o Back up ou procédure dite «dégradée» en cas de panne prolongée d un analyseur Certains examens peuvent être sous-traités à des laboratoires dits référents et reconnus par nos pairs, dans ce cas les résultats rendus ne sont pas couverts par l accréditation et le patient est informé de la sous-traitance, le cas échéant. Le laboratoire vérifie la compétence du laboratoire sous-traitant spécialisé (annexe technique et portée d accréditation COFRAC). Les laboratoires sous-traitants sont évalués et peuvent faire l objet d une visite d audit par le responsable qualité du Laboratoire et la technicienne référente du poste concerné, le cas échéant. Les accords négociés, les exigences pré analytiques et post analytiques sont définis, documentés (manuel de prélèvement, guide, fiches, ). La sous-traitance d analyses en cas de panne est documentée. Les procédures établies permettent de vérifier l adéquation des méthodes d analyses mises en œuvre par le laboratoire sous-traitant. La sous-traitance en cas de panne fait l objet d un enregistrement dans le dossier du patient. Les biologistes des sites concernés, du laboratoire ADEBIO, s assurent que les résultats des examens transmis par le laboratoire sous-traitant sont revus et communiqués aux destinataires : médecins prescripteurs (et aux patients, sauf indication contraire). Les délais de réalisation des examens sous-traités sont surveillés quotidiennement (journal des incomplets SIL HEXALIS) par les biologistes des sites concernés. Processus 07 ACHATS APPROVISIONNEMENTS Processus 05 - POSTANALYTIQUE Procédure associée : PR-I-SST Evaluation - Sélection des fournisseurs - LBM sous-traitants OCIL PR-I-ECH-002 Transmission d analyses aux sous-traitants PR-I-ANA Conduite à tenir en cas de panne prolongée analyseur PR-I-CRR Compte rendu de résultats Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 43/50
44 9 MESURES, ANALYSES ET AMELIORATION (Chapitres /11/ ) 9.1 Généralités Politique en matière d amélioration continue : La direction du laboratoire ADEBIO inscrit la démarche d'amélioration continue comme une composante majeure de son système de management de la qualité et de sa politique qualité. Les enregistrements systématiques des non conformités, des réclamations, de toute nature, impliquent l'ensemble de l'équipe du laboratoire. Afin de maîtriser et améliorer les prestations auprès de nos clients utilisateurs des prestations du laboratoire (patients, médecins, IDE, pharmacies, ), une dynamique de progrès, adaptée aux besoins des clients et impliquant le personnel du laboratoire ADEBIO, est mise en place. Les contrôles et la surveillance de la qualité des processus et des prestations du laboratoire sont établis par le responsable qualité et validés par les biologistes co-responsables. L ensemble de l équipe du laboratoire participe à la dynamique d amélioration continue qui porte sur les axes majeurs suivants : Amélioration continue des prestations de services associées au compte rendu de résultats : - Optimiser les délais de réalisation - Assurer des prestations de service performantes et adaptées - Avis et interprétation associés aux résultats (chaque fois que possible) Amélioration continue des processus : - Diminuer du nombre de non conformités détectées à tous les niveaux de la réalisation des analyses et au niveau des processus supports - Analyser les risques et conduire des analyses de tendance - Engager des actions correctives et préventives Amélioration continue de la satisfaction des clients : - Réaliser régulièrement des enquêtes de satisfaction - Favoriser tout retour «client» et l enregistrement des réclamations - Rencontrer les professionnels de santé : infirmières, médecins, pharmaciens, directeurs d établissements de santé. Laboratoire ADEBIO - MQ-I-SMQ Page 44/50
45 Traitement des NC Enquête de satisfaction clients Audits internes Evaluations externes Objectifs qualité Indicateurs qualité Réclamations Résultats CIQ, EEQ Maîtrise des travaux non conformes Mesure et surveillance Indicateurs qualité Analyse statistique des données Analyse de risque - Analyse de tendance Plan d action pour l amélioration Actions correctives, préventives, Validation, mise en œuvre, suivi, évaluation efficacité Revue de Direction Laboratoire ADEBIO - MQ-I-SMQ Page 45/50
46 9.2 Surveillance et mesure (chapitre ) Satisfaction du client Conformément à la politique qualité du laboratoire, les besoins des clients sont recherchés et identifiés grâce à des enquêtes de satisfaction. Les réclamations sont enregistrées et régulièrement exploitées. Toutes ces données sont traitées et analysées au cours des réunions qualité et revues de direction. Le laboratoire réalise des enquêtes de satisfaction de manière périodique afin de vérifier l adéquation entre les attentes des clients et les prestations fournies. Les recueils de données sont effectués sous forme : - de questionnaire d évaluation diffusé aux patients, aux infirmières, aux médecins - d enregistrement des réclamations ou tout retour d information de la part des médecins, patients, IDE, Une exploitation et une analyse sont réalisées par le service qualité. Les résultats sont diffusés à l ensemble du personnel pour une meilleure prise en compte des besoins des clients. Les actions correctives et préventives qui en découlent sont mises en œuvre et revues Evaluation et audits Audits internes : Une procédure définit les modalités de planification, réalisation, enregistrement et exploitation des audits internes. La mise en place, la revue et l'amélioration du système de management qualité du laboratoire est assurée par la réalisation régulière d'audits qualité internes. Ceux-ci portent sur l ensemble du système qualité, les processus, les documents. Un planning annuel d audits internes est défini et géré (KALILAB ). Ce planning tient compte de la complexité des processus ou activité. Les écarts ou non conformités constatés lors d'un audit interne font l'objet d'actions d amélioration (curatives, correctives ou préventives) et d une revue annuelle. Des audits ponctuels peuvent être déclenchés, le cas échéant, par la direction ou le responsable qualité dès que la situation l exige. Les audits sont réalisés par le personnel habilité auditeur interne, le responsable qualité ou par un auditeur externe indépendant (compétences justifiées, vérifiées). Les audits internes sont réalisés par un auditeur indépendant de l activité auditée. Le personnel ne doit pas auditer ses propres activités. Les rapports et les constats d audit sont enregistrés, diffusés aux personnes concernées et régulièrement suivis avec un bilan annuel réalisé dans le cadre des réunions de revue de direction. La direction évalue l efficacité du système et décide des actions correctives nécessaires à engager dans un délai raisonnable et convenu. Laboratoire ADEBIO - MQ-I-SMQ Page 46/50
47 La revue périodique des prescriptions, la pertinence des procédures et exigences concernant les échantillons s appuient sur : - La surveillance des tubes surnuméraires - La révision du manuel de prélèvement - L adaptation de la prescription, le cas échéant (voir revue de contrat), par les biologistes après accord du médecin. Les retours d informations de la part des utilisateurs sont organisés (enquêtes, enregistrement des réclamations). Voir chapitre Les suggestions du personnel sont favorisées et prises en compte, notamment au cours des différentes réunions : FIAQ, RSA, revue de direction. Voir chapitres 6.4 et 6.5 Procédure associée : PR-I-AQI-001-Audit interne Version applicable Mesure et surveillance des processus Indicateurs de qualité Les indicateurs qualité sont élaborés en cohérence avec les axes majeurs de la politique qualité et en adéquation avec les objectifs qualité. Ces indicateurs sont définis au niveau des processus et sont revus annuellement en revue de direction. Les processus font l objet de mesure et de surveillance afin de prévenir tout risque de nonconformité du produit ou service. La surveillance des processus permet de démontrer l aptitude de chaque processus à atteindre les résultats prévus. (cf. 5.1 Manuel qualité - Exigences générales (Chap ISO 15189). Analyse de risque (analyse de processus AMDEC diagramme causes/effets : 5M) Méthodes à priori : gestion des risques prévisibles d une activité ou processus Décrire les processus (management, réalisation, support/soutien) Identifier les facteurs de risques Réduire l occurrence de ces risques par des actions de prévention visant à maîtriser les causes potentielles. Méthodes à postériori : gestion des risques après la survenue d évènements indésirables Organiser la remontée d informations déclaration (alertes réactovigilance ANSM, informatique, ) Rechercher les causes des évènements jugés inacceptables Organiser le retour d expérience pour mettre en place les actions correctives et préventives Des documents d enregistrement permettent l exploitation de ces mesures et l ensemble du personnel est mobilisé pour rechercher l amélioration des processus dans chaque secteur du laboratoire. Les objectifs et indicateurs de qualité sont des données d entrée de la revue de direction. Laboratoire ADEBIO - MQ-I-SMQ Page 47/50
48 9.3 Identification et maîtrise des non-conformités (chapitre ) Définition Une non-conformité est définie comme une "Non satisfaction aux exigences spécifiées" (procédures, modes opératoires, instructions, enregistrements, ) Traitement de la non-conformité Les non conformités sont enregistrées (KALILAB, HEXALIS ) régulièrement suivies, exploitées. Ce sont des données d entrée de la revue de direction, sous la responsabilité du responsable qualité. La reprise des activités techniques, suite à une non-conformité quelconque de ses analyses, est sous l autorité du biologiste responsable. Responsabilité pour autoriser les dérogations : le biologiste du site ou le biologiste responsable technique, le cas échéant. Toutes les données issues des non conformités, enquêtes de satisfaction, réclamations, retour d informations, contrôles de qualité analytiques sont enregistrées, analysées et exploitées. Les données sont présentées en revue de direction. Processus 01 ORGANISATION MANAGEMENT Processus 02 AMELIORATION CONTINUE Procédure associée : PR-I-NC-001- Identification Maîtrise des non conformités PR-I-RDD-001 Revue de direction Version applicable Laboratoire ADEBIO - MQ-I-SMQ Page 48/50
49 9.4 Actions correctives préventives amélioration continue (chapitres ) Planification pour l amélioration continue Au cours des réunions qualité, revue de direction, le personnel et la direction se concertent et coopèrent pour rechercher et mettre en œuvre des solutions d amélioration sous forme d actions correctives, préventives ou actions d amélioration. La Méthode de Résolution de Problème est à la base de la recherche des causes des problèmes, des conséquences et des solutions possibles (diagramme d Hishikawa ou cause/effet ou 5M). L analyse de risque par processus est mise en œuvre et documentée pour identifier les moyens de préventions à mettre en œuvre. Le responsable qualité, et/ou les personnes responsables des actions et fonctions concernées, vérifient l efficacité des actions Actions correctives L analyse des réclamations client, des non conformités, des écarts détectés (constats) lors des audits internes et évaluations externes (COFRAC), permet de décider d actions correctives (ou préventives) à mettre en place afin d'éliminer les causes de non conformités dans un délai raisonnable et convenu. Les actions correctives sont enregistrées et font l objet d une revue Ce suivi peut prendre différentes formes : Réunion de travail périodique (faire le point et réorienter certaines actions,...) Rédaction de plans d amélioration avec planification (exemple : actions issues de la revue de direction). Les actions correctives sont clôturées lorsque le directeur du laboratoire ou le responsable qualité a statué sur l'efficacité de l'action par rapport aux objectifs fixés. Cette appréciation peut être réalisée grâce à la réalisation d'audits de suivi planifié lorsque l'échéance de mise en place est passée. En cas d'inefficacité avérée, de nouvelles actions correctives sont alors recherchées Actions préventives Evaluation des risques L évaluation des risques repose principalement sur : - Les dispositions de la procédure de gestion des risques - L approche processus (voir chapitre 5.1 et Manuel qualité) - Les dossiers de vérification (validation) des méthodes d analyses - Le document unique d évaluation et identification des risques (Hygiène et sécurité) Des actions préventives sont mises en place suite à l analyse de risque (analyse des processus AMDEC diagramme cause/effet 5M), à la détection ou à l identification d'un risque potentiel ou d une non-conformité potentielle. Laboratoire ADEBIO - MQ-I-SMQ Page 49/50
50 Exemples de risques : - La modification organisationnelle du laboratoire nécessitant la redéfinition des tâches et des fonctions du personnel. - L'intégration de nouveaux matériels dans le processus analytique qui nécessite la définition de nouvelles dispositions (procédures, modes opératoires, enregistrements, ), la formation du personnel, la qualification et habilitation, la vérification ou validation des méthodes d analyses. - Les mises à jour des versions des logiciels utilisés - Des situations dangereuses (risque sécurité) nécessitant la définition de méthodes (procédures, modes opératoires) ou des aménagements des locaux ou installations. - Risques électrique, chimiques, bactériologiques, biologiques AES, TMS, (voir document unique - CHSCT) Les actions préventives sont enregistrées et revues régulièrement. Une évaluation de leur efficacité est établie par le responsable désigné : biologistes et/ou le responsable qualité afin de clôturer l'action. Le bilan des actions correctives et préventives est présenté en revue de direction. Processus 01 ORGANISATION MANAGEMENT Processus 02 AMELIORATION CONTINUE Procédures associées : PR-I-REC-001 Traitement des réclamations clients PR-I-NC-001- Identification Maîtrise des non conformités PR-I-NC Procédure de réactovigilance PR-I-AC-001-Actions correctives Actions préventives PR-I-RDD-001-Revue de direction PR-I-AQI-001-Audit interne Versions applicables Laboratoire ADEBIO - MQ-I-SMQ Page 50/50
Manuel qualité du laboratoire
 Laboratoire de biologie médicale des Hôpitaux Universitaires de Strasbourg Pôle de biologie 1 place de l Hôpital BP 426 67091 Strasbourg Cedex Manuel qualité du laboratoire Version 04 Rédaction : Cellule
Laboratoire de biologie médicale des Hôpitaux Universitaires de Strasbourg Pôle de biologie 1 place de l Hôpital BP 426 67091 Strasbourg Cedex Manuel qualité du laboratoire Version 04 Rédaction : Cellule
Sommaire des documents de la base documentaire 15189 v2012 01/11/2013
 La base documentaire a été complètement révisée pour être en conformité avec cette version 2012 de l ISO 15189. La cartographie des différents processus du LBM a également été modifiée (suppression du
La base documentaire a été complètement révisée pour être en conformité avec cette version 2012 de l ISO 15189. La cartographie des différents processus du LBM a également été modifiée (suppression du
Mise en œuvre de l accréditation dans un laboratoire de biologie médicale privé
 Mise en œuvre de l accréditation dans un laboratoire de biologie médicale privé SELARL ANALYS / SELARL ANALYS-I Une démarche d accréditation multisites Journée du 29 Juin 2010 Thierry Avellan [email protected]
Mise en œuvre de l accréditation dans un laboratoire de biologie médicale privé SELARL ANALYS / SELARL ANALYS-I Une démarche d accréditation multisites Journée du 29 Juin 2010 Thierry Avellan [email protected]
MANUEL ASSURANCE QUALITE MANUEL QUALITE CENTRE DE BIOLOGIE DU LANGUEDOC
 MANUEL ASSURANCE QUALITE Ref : MAQ-COMM-TOUS-001-14 Version : 14 Applicable le : 09-01-2015 MANUEL QUALITE CENTRE DE BIOLOGIE DU LANGUEDOC BEGUIER E. - CALIEZ T. - FONTES C. -JEANE. KERDRANVAT H. - LE
MANUEL ASSURANCE QUALITE Ref : MAQ-COMM-TOUS-001-14 Version : 14 Applicable le : 09-01-2015 MANUEL QUALITE CENTRE DE BIOLOGIE DU LANGUEDOC BEGUIER E. - CALIEZ T. - FONTES C. -JEANE. KERDRANVAT H. - LE
La version électronique fait foi
 Page 1/6 Localisation : Classeur VERT Disponible sur Intranet A revoir : 10/2015 Objet : La présente procédure a pour objet de décrire les responsabilités et les principes pour la réalisation des prélèvements.
Page 1/6 Localisation : Classeur VERT Disponible sur Intranet A revoir : 10/2015 Objet : La présente procédure a pour objet de décrire les responsabilités et les principes pour la réalisation des prélèvements.
Audit interne. Audit interne
 Définition de l'audit interne L'Audit Interne est une activité indépendante et objective qui donne à une organisation une assurance sur le degré de maîtrise de ses opérations, lui apporte ses conseils
Définition de l'audit interne L'Audit Interne est une activité indépendante et objective qui donne à une organisation une assurance sur le degré de maîtrise de ses opérations, lui apporte ses conseils
BRANCHE DU NÉGOCE ET PRESTATIONS DE SERVICES
 Septembre 2014 CARTOGRAPHIE DES MÉTIERS DES PRESTATAIRES BRANCHE DU NÉGOCE ET PRESTATIONS DE SERVICES DANS LES DOMAINES MÉDICO-TECHNIQUES www.metiers-medico-techniques.fr CPNEFP de la branche Négoce et
Septembre 2014 CARTOGRAPHIE DES MÉTIERS DES PRESTATAIRES BRANCHE DU NÉGOCE ET PRESTATIONS DE SERVICES DANS LES DOMAINES MÉDICO-TECHNIQUES www.metiers-medico-techniques.fr CPNEFP de la branche Négoce et
La gestion documentaire les bases d'un système de management de la qualité
 La gestion documentaire les bases d'un système de management de la qualité 8 ème journée professionnelle de l ANTAB - 21 Octobre 2011 Fatima TOUBAIS Ingénieur qualité Accréditation des Laboratoires Direction
La gestion documentaire les bases d'un système de management de la qualité 8 ème journée professionnelle de l ANTAB - 21 Octobre 2011 Fatima TOUBAIS Ingénieur qualité Accréditation des Laboratoires Direction
Référentiel Officine
 Référentiel Officine Inscrire la formation dans la réalité et les besoins de la pharmacie d officine de demain - Ce référentiel décrit dans le cadre des missions et des activités du pharmacien d officine
Référentiel Officine Inscrire la formation dans la réalité et les besoins de la pharmacie d officine de demain - Ce référentiel décrit dans le cadre des missions et des activités du pharmacien d officine
Manuel Management Qualité ISO 9001 V2000. Réf. 20000-003-002 Indice 13 Pages : 13
 Réf. 20000-003-002 Indice 13 Pages : 13 Manuel Management Qualité ISO 9001 V2000 EVOLUTIONS INDICE DATE NATURE DE L'EVOLUTION 00 09/06/2000 Edition Originale 01 29/09/2000 Modification suite à audit interne
Réf. 20000-003-002 Indice 13 Pages : 13 Manuel Management Qualité ISO 9001 V2000 EVOLUTIONS INDICE DATE NATURE DE L'EVOLUTION 00 09/06/2000 Edition Originale 01 29/09/2000 Modification suite à audit interne
MANUEL Q S E. Mise à jour : Mai 2014. Qualité - Sécurité - Environnement
 MANUEL Q S E Mise à jour : Mai 2014 Qualité - Sécurité - Environnement Editorial BÂTIMENTS - Privé - Public - Industriel La société RIVASI BTP est implantée dans la Drôme et les Bouches-du-Rhône. Elle
MANUEL Q S E Mise à jour : Mai 2014 Qualité - Sécurité - Environnement Editorial BÂTIMENTS - Privé - Public - Industriel La société RIVASI BTP est implantée dans la Drôme et les Bouches-du-Rhône. Elle
Système Management Environnemental
 Système Management Environnemental Laboratoire de Touraine Laboratoire de Touraine Laboratoire de Touraine - Bassin Eaux Pluviales Environnemental Politique Qualité Sécurité Environnement Sommaire Norme
Système Management Environnemental Laboratoire de Touraine Laboratoire de Touraine Laboratoire de Touraine - Bassin Eaux Pluviales Environnemental Politique Qualité Sécurité Environnement Sommaire Norme
Références : norme ISO 15189 et documents COFRAC applicables au laboratoire. Laboratoire Benezech Delhoume
 MANUEL D ASSURANCE LABORATOIRE Références : norme ISO 15189 et documents COFRAC applicables au laboratoire Laboratoire Benezech Delhoume 1 rue Père Colombier 81000 ALBI Tel : 05 63 77 78 90 Fax : 05 63
MANUEL D ASSURANCE LABORATOIRE Références : norme ISO 15189 et documents COFRAC applicables au laboratoire Laboratoire Benezech Delhoume 1 rue Père Colombier 81000 ALBI Tel : 05 63 77 78 90 Fax : 05 63
PROCEDURE ENREGISTREMENT
 Page 1 sur 7 ANNULE ET REMPLACE LES DOCUMENTS SUIVANTS référence 04/PR/001/02/V01 04/PR/001/02/V02 04/PR/001/02/V03 04/PR/001/02/V04 04/PR/001/02/V05 04/PR/001/02/V06 04/PR/001/02/V07 04/PR/001/02/V08
Page 1 sur 7 ANNULE ET REMPLACE LES DOCUMENTS SUIVANTS référence 04/PR/001/02/V01 04/PR/001/02/V02 04/PR/001/02/V03 04/PR/001/02/V04 04/PR/001/02/V05 04/PR/001/02/V06 04/PR/001/02/V07 04/PR/001/02/V08
SERVICES TECHNIQUES CENTRE HOSPITALIER. d AURILLAC. 1er congrès de l AFGRIS
 SERVICES TECHNIQUES CENTRE HOSPITALIER henri MONDOR d AURILLAC 1er congrès de l AFGRIS METHODE D ANALYSE ET DE PREVENTION DES RISQUES ET CERTIFICATION ISO 9002 Un couple pertinent pour les services techniques
SERVICES TECHNIQUES CENTRE HOSPITALIER henri MONDOR d AURILLAC 1er congrès de l AFGRIS METHODE D ANALYSE ET DE PREVENTION DES RISQUES ET CERTIFICATION ISO 9002 Un couple pertinent pour les services techniques
GESTION DES RISQUES Cartographie COVIRISQ
 GESTION DES RISQUES Cartographie COVIRISQ PLAN Préambule Historique de la démarche Cartographie Organigramme Situation actuelle Constat Préambule OVE comprend : Un secteur social Un secteur médico-social
GESTION DES RISQUES Cartographie COVIRISQ PLAN Préambule Historique de la démarche Cartographie Organigramme Situation actuelle Constat Préambule OVE comprend : Un secteur social Un secteur médico-social
Accréditation des laboratoires de ais
 Accréditation des laboratoires de biologie médicale m français ais Hélène MEHAY Directrice de la section Santé Humaine Cofrac 52 rue Jacques Hillairet 75012 Paris Journée FHF Centre 30 juin 2015 1 L accréditation
Accréditation des laboratoires de biologie médicale m français ais Hélène MEHAY Directrice de la section Santé Humaine Cofrac 52 rue Jacques Hillairet 75012 Paris Journée FHF Centre 30 juin 2015 1 L accréditation
MINISTERE DES TECHNOLOGIES COMMUNICATION CENTRE NATIONAL DE L INFORMATIQUE DE L INFORMATION ET DE LA MANUEL DE MANAGEMENT DE LA QUALITE
 MINISTERE DES TECHNOLOGIES DE L INFORMATION ET DE LA COMMUNICATION CENTRE NATIONAL DE L INFORMATIQUE MANUEL DE MANAGEMENT DE LA QUALITE ISO 9001 VERSION 2008 V14 du 25 AVRIL 2012 CNI MANUEL DE MANAGEMENT
MINISTERE DES TECHNOLOGIES DE L INFORMATION ET DE LA COMMUNICATION CENTRE NATIONAL DE L INFORMATIQUE MANUEL DE MANAGEMENT DE LA QUALITE ISO 9001 VERSION 2008 V14 du 25 AVRIL 2012 CNI MANUEL DE MANAGEMENT
Livret d accueil. Notice - modèle type de livret d accueil Conseils pour assurer une intégration réussie. Livret d accueil.
 1 Notice - modèle type de livret d accueil Conseils pour assurer une intégration réussie Janvier 2014 2 NOTICE L intégration d un jeune embauché dans une entreprise et au sein d une équipe de travail est
1 Notice - modèle type de livret d accueil Conseils pour assurer une intégration réussie Janvier 2014 2 NOTICE L intégration d un jeune embauché dans une entreprise et au sein d une équipe de travail est
CERTIFICATION CERTIPHYTO
 CONDITIONS GENERALES DE CERTIFICATION MONOSITE Indice 2 Page 1/12 «Distribution de produits phytopharmaceutiques, Application en prestation de service de produits phytopharmaceutiques, Conseil à l utilisation
CONDITIONS GENERALES DE CERTIFICATION MONOSITE Indice 2 Page 1/12 «Distribution de produits phytopharmaceutiques, Application en prestation de service de produits phytopharmaceutiques, Conseil à l utilisation
BREVET DE TECHNICIEN SUPERIEUR
 DIRECTION GENERALE DE L ENSEIGNEMENT SUPERIEUR BREVET DE TECHNICIEN SUPERIEUR «Services et prestations des secteurs sanitaire et social» Septembre 2007 Arrêté portant définition et fixant les conditions
DIRECTION GENERALE DE L ENSEIGNEMENT SUPERIEUR BREVET DE TECHNICIEN SUPERIEUR «Services et prestations des secteurs sanitaire et social» Septembre 2007 Arrêté portant définition et fixant les conditions
Certification OHSAS 18001 Santé et sécurité au travail : exemple d'application dans une AASQA (AIRFOBEP)
 Certification OHSAS 18001 Santé et sécurité au travail : exemple d'application dans une AASQA (AIRFOBEP) BouAlem MESBAH - AIRFOBEP? 3 Questions avant de commencer Du document unique au SMS Du SMS à l OHSAS
Certification OHSAS 18001 Santé et sécurité au travail : exemple d'application dans une AASQA (AIRFOBEP) BouAlem MESBAH - AIRFOBEP? 3 Questions avant de commencer Du document unique au SMS Du SMS à l OHSAS
Tremplins de la Qualité. Tome 2
 Tome 2 CET OUVRAGE EST UN GUIDE D INTERPRETATION DE LA NORME NF EN ISO 9001 VERSION 2000 AVANTPROPOS Ce guide d aide à la rédaction du Manuel de Management de la Qualité a été rédigé par la Fédération
Tome 2 CET OUVRAGE EST UN GUIDE D INTERPRETATION DE LA NORME NF EN ISO 9001 VERSION 2000 AVANTPROPOS Ce guide d aide à la rédaction du Manuel de Management de la Qualité a été rédigé par la Fédération
La métrologie au laboratoire. vigitemp 10. centrale de surveillance et de traçabilité vigitemp kit de cartographie vigicart
 La métrologie au laboratoire vigitemp 10 centrale de surveillance et de traçabilité vigitemp kit de cartographie vigicart La métrologie au laboratoire vigitemp 10 Base de données Utilisateur Principe général
La métrologie au laboratoire vigitemp 10 centrale de surveillance et de traçabilité vigitemp kit de cartographie vigicart La métrologie au laboratoire vigitemp 10 Base de données Utilisateur Principe général
Qualité Sécurité Environnement
 Qualité Sécurité Environnement FORMATION AUDIT CONSEIL EXPERTISE >> Catalogue 2014 Nos innovations: e-learning, évaluation des compétences personnalisation Formation Hygiène Alimentaire ISO 9001 : 2008...
Qualité Sécurité Environnement FORMATION AUDIT CONSEIL EXPERTISE >> Catalogue 2014 Nos innovations: e-learning, évaluation des compétences personnalisation Formation Hygiène Alimentaire ISO 9001 : 2008...
Réseau National de Laboratoires * * * * * * * * * *
 République du Sénégal Ministère de la Santé et de l Action Sociale Direction Générale de la Santé Direction des Laboratoires Réseau National de Laboratoires * * * * * * * * * * PLAN DE FORMATION DES PERSONNELS
République du Sénégal Ministère de la Santé et de l Action Sociale Direction Générale de la Santé Direction des Laboratoires Réseau National de Laboratoires * * * * * * * * * * PLAN DE FORMATION DES PERSONNELS
Unité de Recherche Clinique St Louis - Lariboisière Fernand Widal Le 03 Février 2012
 Visite de pré-sélection Visite de Mise en place Murielle COURREGES-VIAUD, ARC Laurence GUERY, ARC responsable Assurance Qualité Véronique JOUIS, Coordinatrice des ARCs Responsable Logistique Unité de Recherche
Visite de pré-sélection Visite de Mise en place Murielle COURREGES-VIAUD, ARC Laurence GUERY, ARC responsable Assurance Qualité Véronique JOUIS, Coordinatrice des ARCs Responsable Logistique Unité de Recherche
REF01 Référentiel de labellisation des laboratoires de recherche_v3
 Introduction Le présent référentiel de labellisation est destiné aux laboratoires qui souhaitent mettre en place un dispositif de maîtrise de la qualité des mesures. La norme ISO 9001 contient essentiellement
Introduction Le présent référentiel de labellisation est destiné aux laboratoires qui souhaitent mettre en place un dispositif de maîtrise de la qualité des mesures. La norme ISO 9001 contient essentiellement
Valorisation des résultats de la recherche. Objet et domaine d application du manuel Qualité...2
 Valorisation des résultats de la recherche Version : décembre 2003 Objet et domaine d application du manuel...2 Champ d application du manuel 2 Périmètre d application du manuel 2 Terminologie 2 Présentation
Valorisation des résultats de la recherche Version : décembre 2003 Objet et domaine d application du manuel...2 Champ d application du manuel 2 Périmètre d application du manuel 2 Terminologie 2 Présentation
La biologie médicale en France : présent et avenir. Académie Nationale de Pharmacie Mercredi 4 Février 2015
 La biologie médicale en France : présent et avenir Académie Nationale de Pharmacie Mercredi 4 Février 2015 Les fondamentaux de la biologie médicale en France Une discipline jeune, apparue dans les années
La biologie médicale en France : présent et avenir Académie Nationale de Pharmacie Mercredi 4 Février 2015 Les fondamentaux de la biologie médicale en France Une discipline jeune, apparue dans les années
Diplôme d Etat d infirmier Référentiel de compétences
 Annexe II Diplôme d Etat d infirmier Référentiel de compétences Les référentiels d activités et de compétences du métier d infirmier diplômé d Etat ne se substituent pas au cadre réglementaire. En effet,
Annexe II Diplôme d Etat d infirmier Référentiel de compétences Les référentiels d activités et de compétences du métier d infirmier diplômé d Etat ne se substituent pas au cadre réglementaire. En effet,
LE PROJET QUALITE-GESTION DES RISQUES- DEVELOPPEMENT DURABLE
 LE PROJET QUALITE-GESTION DES RISQUES- DEVELOPPEMENT DURABLE 1 LA POLITIQUE QUALITE-GESTION DES RISQUES Depuis 2003, la Direction s engage à poursuivre, la démarche qualité et à développer une gestion
LE PROJET QUALITE-GESTION DES RISQUES- DEVELOPPEMENT DURABLE 1 LA POLITIQUE QUALITE-GESTION DES RISQUES Depuis 2003, la Direction s engage à poursuivre, la démarche qualité et à développer une gestion
COMPTE RENDU D ACCREDITATION DE L'HOPITAL ET INSTITUT DE FORMATION EN SOINS INFIRMIERS CROIX-ROUGE FRANÇAISE
 COMPTE RENDU D ACCREDITATION DE L'HOPITAL ET INSTITUT DE FORMATION EN SOINS INFIRMIERS CROIX-ROUGE FRANÇAISE Chemin de la Bretèque 76230 BOIS-GUILLAUME Mois de juin 2001 SOMMAIRE COMMENT LIRE LE «COMPTE
COMPTE RENDU D ACCREDITATION DE L'HOPITAL ET INSTITUT DE FORMATION EN SOINS INFIRMIERS CROIX-ROUGE FRANÇAISE Chemin de la Bretèque 76230 BOIS-GUILLAUME Mois de juin 2001 SOMMAIRE COMMENT LIRE LE «COMPTE
SOMMAIRE 1 LA POLITIQUE GENERALE ET LA POLITIQUE QUALITE 2 UNE ORGANISATION PROFESSIONNELLE FORTE ET GARANTE DE SES MEMBRES 3 NOTRE SMQ
 Manuel Qualité 5 place du Rosoir 21000 DIJON Tél. : 03.80.59.65.20 Fax : 03.80.53.09.50 Mèl : [email protected] www.bfc.experts-comptables.fr SOMMAIRE 1 LA POLITIQUE GENERALE ET LA POLITIQUE
Manuel Qualité 5 place du Rosoir 21000 DIJON Tél. : 03.80.59.65.20 Fax : 03.80.53.09.50 Mèl : [email protected] www.bfc.experts-comptables.fr SOMMAIRE 1 LA POLITIQUE GENERALE ET LA POLITIQUE
LA VERSION ELECTRONIQUE FAIT FOI
 CONDITIONS D ACCREDITATION D ORGANISMES MULTISITES OU ORGANISES EN RESEAU OU METTANT EN COMMUN DES MOYENS GEN PROC 10 Révision 03 CONDITIONS D ACCREDITATION D ORGANISMES MULTISITES OU ORGANISES EN RESEAU
CONDITIONS D ACCREDITATION D ORGANISMES MULTISITES OU ORGANISES EN RESEAU OU METTANT EN COMMUN DES MOYENS GEN PROC 10 Révision 03 CONDITIONS D ACCREDITATION D ORGANISMES MULTISITES OU ORGANISES EN RESEAU
REFERENTIEL D ACTIVITES ET DE COMPETENCES CQP AIDE DENTAIRE
 REFERENTIEL D ACTIVITES ET DE COMPETENCES CQP AIDE DENTAIRE 1 ACTIVITES TECHNIQUES AIDE DENTAIRE / GESTION DU RISQUE INFECTIEUX Préparer et entretenir la salle de soins Entretenir la salle de stérilisation
REFERENTIEL D ACTIVITES ET DE COMPETENCES CQP AIDE DENTAIRE 1 ACTIVITES TECHNIQUES AIDE DENTAIRE / GESTION DU RISQUE INFECTIEUX Préparer et entretenir la salle de soins Entretenir la salle de stérilisation
Projet de santé. Nom du site : N Finess : (Sera prochainement attribué par les services de l ARS) Statut juridique : Raison Sociale :
 Projet de santé Nom du site : N Finess : (Sera prochainement attribué par les services de l ARS) Statut juridique : Raison Sociale : Adresse du siège social : Téléphone : Mail : Version : Etablie en date
Projet de santé Nom du site : N Finess : (Sera prochainement attribué par les services de l ARS) Statut juridique : Raison Sociale : Adresse du siège social : Téléphone : Mail : Version : Etablie en date
UDSG CLASSIFICATION DOSSIER DOCUMENTAIRE
 UDSG CLASSIFICATION DOSSIER DOCUMENTAIRE 2 SOMMAIRE I. LES FAMILLES PROFESSIONNELLES... 5 II. LES FONCTIONS GENERIQUES... 12 FAMILLE ETUDES ET CONCEPTION......... 15 ASSISTANT D ETUDES ET CONCEPTION...16
UDSG CLASSIFICATION DOSSIER DOCUMENTAIRE 2 SOMMAIRE I. LES FAMILLES PROFESSIONNELLES... 5 II. LES FONCTIONS GENERIQUES... 12 FAMILLE ETUDES ET CONCEPTION......... 15 ASSISTANT D ETUDES ET CONCEPTION...16
Nouveau jeune collaborateur
 Insérez le logo de l'entreprise LIVRET D'ACCUEIL Nouveau jeune collaborateur Livret d accueil de : Prénom NOM ACCUEIL ACCOMPAGNEMENT Nous sommes heureux de vous accueillir au sein de notre entreprise.
Insérez le logo de l'entreprise LIVRET D'ACCUEIL Nouveau jeune collaborateur Livret d accueil de : Prénom NOM ACCUEIL ACCOMPAGNEMENT Nous sommes heureux de vous accueillir au sein de notre entreprise.
Accueil et Formations du personnel recruté en Stérilisation Centrale. Présenté par Dany GAUDELET et le Dr. Julien MOLINA
 Accueil et Formations du personnel recruté en Stérilisation Centrale Présenté par Dany GAUDELET et le Dr. Julien MOLINA PLAN Introduction Réglementation Circuit du personnel Procédure de Formation Accueil
Accueil et Formations du personnel recruté en Stérilisation Centrale Présenté par Dany GAUDELET et le Dr. Julien MOLINA PLAN Introduction Réglementation Circuit du personnel Procédure de Formation Accueil
CATALOGUE DE FORMATIONS 2014 2015
 CATALOGUE DE FORMATIONS 2014 2015 Professionnels de l alimentation 06.47.75.88.57 HQSA Consulting [email protected] Numéro de déclaration de prestataire de formation : SIRET SIRET : 804 : 284 284 420
CATALOGUE DE FORMATIONS 2014 2015 Professionnels de l alimentation 06.47.75.88.57 HQSA Consulting [email protected] Numéro de déclaration de prestataire de formation : SIRET SIRET : 804 : 284 284 420
Partager l expérience de l ASECNA dans la mise en œuvre du SMS et du SMQ :
 Objet de la présentation Partager l expérience de l ASECNA dans la mise en œuvre du SMS et du SMQ : Défis rencontrés Avantages acquis Contenu de la présentation Qu est ce que l ASECNA? Planification de
Objet de la présentation Partager l expérience de l ASECNA dans la mise en œuvre du SMS et du SMQ : Défis rencontrés Avantages acquis Contenu de la présentation Qu est ce que l ASECNA? Planification de
Charte de la Banque ADN et de Cellules de Généthon
 Sommaire 1. PREAMBULE... 2 2. DEFINITIONS... 2 3. CADRE LEGAL... 3 4. ORGANISATION DE LA BACG... 4 5. PRESTATIONS DE LA BACG... 5 6. MODALITES DE CONTRIBUTION ET D UTILISATION DES SERVICES... 5 7. REGLES
Sommaire 1. PREAMBULE... 2 2. DEFINITIONS... 2 3. CADRE LEGAL... 3 4. ORGANISATION DE LA BACG... 4 5. PRESTATIONS DE LA BACG... 5 6. MODALITES DE CONTRIBUTION ET D UTILISATION DES SERVICES... 5 7. REGLES
Certification ISO 9001 de la prise en charge médicamenteuse
 Certification ISO 9001 de la prise en charge médicamenteuse Jeudi 9 avril 2015 1 Sommaire Présentation de la Maison de santé Marie Galène La démarche de certification ISO 9001 à Marie Galène Pourquoi cette
Certification ISO 9001 de la prise en charge médicamenteuse Jeudi 9 avril 2015 1 Sommaire Présentation de la Maison de santé Marie Galène La démarche de certification ISO 9001 à Marie Galène Pourquoi cette
L'AUDIT DES SYSTEMES D'INFORMATION
 L'AUDIT DES SYSTEMES D'INFORMATION ESCI - Bourg en Bresse (2005 2006) Audit s Système d'information - P2 1 lan d'ensemble Audit s Systèmes d'information GENERALITES SUR L'AUDIT AUDIT FONCTIONNEL OU D'APPLICATION
L'AUDIT DES SYSTEMES D'INFORMATION ESCI - Bourg en Bresse (2005 2006) Audit s Système d'information - P2 1 lan d'ensemble Audit s Systèmes d'information GENERALITES SUR L'AUDIT AUDIT FONCTIONNEL OU D'APPLICATION
Mél : Nom de l ACMO : Mél ACMO :
 Etat des lieux en hygiène et sécurité dans un établissement scolaire Rectorat Inspection en Hygiène et sécurité Dossier suivi par M. Gilbert ROUSSEAU Téléphone 05 57 57 39 82 Fax 05 57 57 87 40 Mél: [email protected]
Etat des lieux en hygiène et sécurité dans un établissement scolaire Rectorat Inspection en Hygiène et sécurité Dossier suivi par M. Gilbert ROUSSEAU Téléphone 05 57 57 39 82 Fax 05 57 57 87 40 Mél: [email protected]
MANAGEMENT PAR LA QUALITE ET TIC
 Garantir une organisation performante pour satisfaire ses clients et ses partenaires, telle est la finalité d une certification «qualité». On dénombre de nombreux référentiels dont le plus connu et le
Garantir une organisation performante pour satisfaire ses clients et ses partenaires, telle est la finalité d une certification «qualité». On dénombre de nombreux référentiels dont le plus connu et le
MANAGEMENT PAR LA QUALITE ET TIC
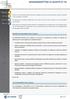 MANAGEMENT PAR LA QUALITE ET TIC Lorraine Garantir une organisation performante pour satisfaire ses clients et ses partenaires, telle est la finalité d une certification «qualité». On dénombre de nombreux
MANAGEMENT PAR LA QUALITE ET TIC Lorraine Garantir une organisation performante pour satisfaire ses clients et ses partenaires, telle est la finalité d une certification «qualité». On dénombre de nombreux
La formation en matière de santé et de sécurité au travail
 Guide pratique 6 / 6 MINISTÈRE DU BUDGET, DES COMPTES PUBLICS, MINISTÈRE MINISTÈRE DU BUDGET, DE DU LA BUDGET, FONCTION DES COMPTES DES COMPTES PUBLIQUE PUBLICS, PUBLICS, ET DE LA RÉFORME DE L ETAT DE
Guide pratique 6 / 6 MINISTÈRE DU BUDGET, DES COMPTES PUBLICS, MINISTÈRE MINISTÈRE DU BUDGET, DE DU LA BUDGET, FONCTION DES COMPTES DES COMPTES PUBLIQUE PUBLICS, PUBLICS, ET DE LA RÉFORME DE L ETAT DE
Domaine Santé. Plan d études cadre Modules complémentaires santé. HES-SO, les 5 et 6 mai 2011. 1 PEC Modules complémentaires santé
 Domaine Santé Plan d études cadre Modules complémentaires santé HES-SO, les 5 et 6 mai 2011 1 PEC Modules complémentaires santé Plan d études cadre Modules complémentaires santé 1. Finalité des modules
Domaine Santé Plan d études cadre Modules complémentaires santé HES-SO, les 5 et 6 mai 2011 1 PEC Modules complémentaires santé Plan d études cadre Modules complémentaires santé 1. Finalité des modules
HAS / Service Qualité de l Information Médicale / Février 2007 1
 Référentiel d évaluation des centres de santé HAS / Service Qualité de l Information Médicale / Février 2007 1 Sommaire Introduction p. 3 et 4 Référentiel d évaluation p. 5 à 8 Référentiel d évaluation
Référentiel d évaluation des centres de santé HAS / Service Qualité de l Information Médicale / Février 2007 1 Sommaire Introduction p. 3 et 4 Référentiel d évaluation p. 5 à 8 Référentiel d évaluation
BONNES PRATIQUES DE PHARMACIE HOSPITALIERE
 MINISTERE DE L EMPLOI ET DE LA SOLIDARITE MINISTERE DELEGUE A LA SANTE DIRECTION DE L HOSPITALISATION ET DE L ORGANISATION DES SOINS BONNES PRATIQUES DE PHARMACIE HOSPITALIERE 1 ère édition juin 2001 SOMMAIRE
MINISTERE DE L EMPLOI ET DE LA SOLIDARITE MINISTERE DELEGUE A LA SANTE DIRECTION DE L HOSPITALISATION ET DE L ORGANISATION DES SOINS BONNES PRATIQUES DE PHARMACIE HOSPITALIERE 1 ère édition juin 2001 SOMMAIRE
LE FINANCEMENT. MSPD Eric Fretillere Conseil Régional de l Ordre des Médecins d Aquitaine CDOM 47Page 1
 LE FINANCEMENT Il ne faut pas se le cacher, le financement est une difficulté et de nombreuses maisons médicales dans les 10 dernières années, qui fonctionnaient de manière satisfaisante, sont «décédées»
LE FINANCEMENT Il ne faut pas se le cacher, le financement est une difficulté et de nombreuses maisons médicales dans les 10 dernières années, qui fonctionnaient de manière satisfaisante, sont «décédées»
Ce document est la propriété de la MAP. Il ne peut être utilisé, reproduit ou communiqué sans son autorisation. MECANIQUE AERONAUTIQUE PYRENEENNE
 MANUEL MANAGEMENT QUALITE Révision janvier 2010 Ce document est la propriété de la MAP. Il ne peut être utilisé, reproduit ou communiqué sans son autorisation. MECANIQUE AERONAUTIQUE PYRENEENNE Place d
MANUEL MANAGEMENT QUALITE Révision janvier 2010 Ce document est la propriété de la MAP. Il ne peut être utilisé, reproduit ou communiqué sans son autorisation. MECANIQUE AERONAUTIQUE PYRENEENNE Place d
Notre écoute et notre réactivité
 2010 Manuel Qualité Politique qualité Notre écoute et notre réactivité sont la garantie de notre capacité à réaliser des prestations d un haut niveau de qualité. Il s agit de remplir les missions fixées
2010 Manuel Qualité Politique qualité Notre écoute et notre réactivité sont la garantie de notre capacité à réaliser des prestations d un haut niveau de qualité. Il s agit de remplir les missions fixées
COMPTE-RENDU D ACCREDITATION DE LA CLINIQUE LA LIRONDE. Saint-Clément-de-Rivière 34980 Saint-Gély-du-Fesc
 COMPTE-RENDU D ACCREDITATION DE LA CLINIQUE LA LIRONDE Saint-Clément-de-Rivière 34980 Saint-Gély-du-Fesc Avril 2003 SOMMAIRE COMMENT LIRE LE «COMPTE-RENDU D ACCREDITATION»... p.3 PARTIE 1 PRESENTATION
COMPTE-RENDU D ACCREDITATION DE LA CLINIQUE LA LIRONDE Saint-Clément-de-Rivière 34980 Saint-Gély-du-Fesc Avril 2003 SOMMAIRE COMMENT LIRE LE «COMPTE-RENDU D ACCREDITATION»... p.3 PARTIE 1 PRESENTATION
OUVERTURE ET MISE EN PLACE
 OUVERTURE ET MISE EN PLACE Estelle Marcault 20/01/2012 URC PARIS NORD 1 Ouverture et mise en place Trois types de visites/ réunions peuvent avoir lieu : Visite de sélection Réunion investigateur Visite
OUVERTURE ET MISE EN PLACE Estelle Marcault 20/01/2012 URC PARIS NORD 1 Ouverture et mise en place Trois types de visites/ réunions peuvent avoir lieu : Visite de sélection Réunion investigateur Visite
RAPPORT DE TRANSPARENCE
 RAPPORT DE TRANSPARENCE 2013 21, rue de Sarre B.P 75857 57078 METZ CEDEX 03 En application des dispositions de l article 40 de la directive 2006/43/CE du Parlement Européen et du conseil du 17 mai 2006
RAPPORT DE TRANSPARENCE 2013 21, rue de Sarre B.P 75857 57078 METZ CEDEX 03 En application des dispositions de l article 40 de la directive 2006/43/CE du Parlement Européen et du conseil du 17 mai 2006
PROFIL DE POSTE DU CONDUCTEUR AMBULANCIER SMUR :
 PROFIL DE POSTE DU CONDUCTEUR AMBULANCIER SMUR : IDENTIFICATION DU POSTE : Titre de la fonction : Conducteur Ambulancier SMUR*. Etablissement : Centre Hospitalier Régional Universitaire de Brest. Service
PROFIL DE POSTE DU CONDUCTEUR AMBULANCIER SMUR : IDENTIFICATION DU POSTE : Titre de la fonction : Conducteur Ambulancier SMUR*. Etablissement : Centre Hospitalier Régional Universitaire de Brest. Service
Métiers de la Qualité, Sécurité, Environnement
 Les fiches Métiers de l Observatoire du Travail Temporaire Emploi, compétences et trajectoires d intérimaires cadres Métiers de la Qualité, Sécurité, Environnement Ingénieur méthodeordonnancement Qualité
Les fiches Métiers de l Observatoire du Travail Temporaire Emploi, compétences et trajectoires d intérimaires cadres Métiers de la Qualité, Sécurité, Environnement Ingénieur méthodeordonnancement Qualité
SYSTÈME DE MANAGEMENT DE LA QUALITÉ
 SYSTÈME DE MANAGEMENT DE LA QUALITÉ Version Objet des modifications 30/10/2009 Conception initiale du manuel 10/02/2011 Amélioration n 1 du système 17/02/2012 Amélioration n 2 du système Etabli & Vérifié
SYSTÈME DE MANAGEMENT DE LA QUALITÉ Version Objet des modifications 30/10/2009 Conception initiale du manuel 10/02/2011 Amélioration n 1 du système 17/02/2012 Amélioration n 2 du système Etabli & Vérifié
ARRÊTÉ du. relatif au cahier des charges de santé de la maison de santé mentionné à l article L. 6323-3 du code de la santé publique.
 RÉPUBLIQUE FRANÇAISE Ministère du travail, de l emploi NOR : ARRÊTÉ du relatif au cahier des charges de santé de la maison de santé mentionné à l article L. 6323-3 du code de la santé publique. Le ministre
RÉPUBLIQUE FRANÇAISE Ministère du travail, de l emploi NOR : ARRÊTÉ du relatif au cahier des charges de santé de la maison de santé mentionné à l article L. 6323-3 du code de la santé publique. Le ministre
L Assurance Qualité DOSSIER L ASSURANCE QUALITE
 DOSSIER L ASSURANCE QUALITE L Assurance Qualité DOSSIER N D4-2-GW0301 Satisfaction.fr 164 ter rue d Aguesseau 92100 Boulogne Billancourt 01.48.25.76.76 http://www.satisfaction.fr/ Page 1 Définition Normalisée.
DOSSIER L ASSURANCE QUALITE L Assurance Qualité DOSSIER N D4-2-GW0301 Satisfaction.fr 164 ter rue d Aguesseau 92100 Boulogne Billancourt 01.48.25.76.76 http://www.satisfaction.fr/ Page 1 Définition Normalisée.
Liège, le 29 juillet 2013. APPEL INTERNE et EXTERNE AUX CANDIDATURES N 2013-085
 Centre Hospitalier Universitaire de Liège Domaine Universitaire du Sart Tilman B35 4000 LIEGE 1 www.chuliege.be Département de Gestion des Ressources Humaines Service Recrutement Liège, le 29 juillet 2013
Centre Hospitalier Universitaire de Liège Domaine Universitaire du Sart Tilman B35 4000 LIEGE 1 www.chuliege.be Département de Gestion des Ressources Humaines Service Recrutement Liège, le 29 juillet 2013
ACCOMPAGNEMENT A LA CERTIFICATION ISO 9001 DE L AGENCE POUR LA RECHERCHE ET L INNOVATION EN CHAMPAGNE-ARDENNE - CARINNA
 1 APPEL D OFFRES ACCOMPAGNEMENT A LA CERTIFICATION ISO 9001 DE L AGENCE POUR LA RECHERCHE ET L INNOVATION EN CHAMPAGNE-ARDENNE - CARINNA JUILLET 2013 2 1. OBJET DE L APPEL D OFFRE Réalisation d un accompagnement
1 APPEL D OFFRES ACCOMPAGNEMENT A LA CERTIFICATION ISO 9001 DE L AGENCE POUR LA RECHERCHE ET L INNOVATION EN CHAMPAGNE-ARDENNE - CARINNA JUILLET 2013 2 1. OBJET DE L APPEL D OFFRE Réalisation d un accompagnement
REFERENTIEL DE CERTIFICATION
 REFERENTIEL DE CERTIFICATION Référentiel I4 NF 285 Edition : Janvier 2015 N de révision : 4 ORGANISMES CERTIFICATEURS CNPP Cert. Route de la Chapelle Réanville CD 64 - CS 22265 F- 27950 SAINT-MARCEL Tél.
REFERENTIEL DE CERTIFICATION Référentiel I4 NF 285 Edition : Janvier 2015 N de révision : 4 ORGANISMES CERTIFICATEURS CNPP Cert. Route de la Chapelle Réanville CD 64 - CS 22265 F- 27950 SAINT-MARCEL Tél.
DISTRIBUTION DU TRAITEMENT MEDICAMENTEUX PAR VOIE ORALE PAR L INFIRMIERE : RISQUE DE NON PRISE DU TRAITEMENT MEDICAMENTEUX PAR LE PATIENT
 INSTITUT DE FORMATION DES CADRES DE SANTE ASSISTANCE PUBLIQUE HOPITAUX DE PARIS ACTIVITE PROFESSIONNELLE N 8 : LE CADRE GERE LES RISQUES CONCERNANT LES PRESTATIONS, LES CONDITIONS DE TRAVAIL DES PERSONNELS,
INSTITUT DE FORMATION DES CADRES DE SANTE ASSISTANCE PUBLIQUE HOPITAUX DE PARIS ACTIVITE PROFESSIONNELLE N 8 : LE CADRE GERE LES RISQUES CONCERNANT LES PRESTATIONS, LES CONDITIONS DE TRAVAIL DES PERSONNELS,
Hygiène alimentaire en restauration collective
 1 2 3 4 5 6 7 Catalogue 2011 Audit, conseil et formation Hygiène alimentaire en restauration collective Laboratoire Départemental de la Côte-d'Or Sommaire 1 2 3 4 5 6 7 Sensibilisation à l hygiène alimentaire
1 2 3 4 5 6 7 Catalogue 2011 Audit, conseil et formation Hygiène alimentaire en restauration collective Laboratoire Départemental de la Côte-d'Or Sommaire 1 2 3 4 5 6 7 Sensibilisation à l hygiène alimentaire
BTS Assistant de manager(s) LES FINALITES PROFESSIONNELLES
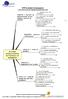 BTS Assistant de manager(s) LES FINALITES PROFESSIONNELLES 1 FINALITÉ 1 Soutien à la communication et aux relations internes et externes L assistant facilite la communication à tous les niveaux (interpersonnel,
BTS Assistant de manager(s) LES FINALITES PROFESSIONNELLES 1 FINALITÉ 1 Soutien à la communication et aux relations internes et externes L assistant facilite la communication à tous les niveaux (interpersonnel,
Catalogue Formation 2015
 Catalogue Formation 2015 Because you care about CONSUMERS HEALTH HACCP Expertise, votre partenaire en sécurité des aliments Présentation du catalogue Pourquoi faire de la formation? Formation préventive
Catalogue Formation 2015 Because you care about CONSUMERS HEALTH HACCP Expertise, votre partenaire en sécurité des aliments Présentation du catalogue Pourquoi faire de la formation? Formation préventive
Les obligations de l'exploitant
 Guide technique : Sécurité > Les obligations de l'exploitant > Les obligations de l'exploitant Les obligations de l'exploitant L exploitant assiste aux visites de la commission de sécurité, ou s y fait
Guide technique : Sécurité > Les obligations de l'exploitant > Les obligations de l'exploitant Les obligations de l'exploitant L exploitant assiste aux visites de la commission de sécurité, ou s y fait
Livret d accueil des stagiaires
 Livret d accueil des stagiaires SOMMAIRE : I/ Présentation du service II/Le métier de manipulateur III/ Modalités d encadrement IV/ Votre stage V/ Bilan global de votre stage I/ Présentation du service
Livret d accueil des stagiaires SOMMAIRE : I/ Présentation du service II/Le métier de manipulateur III/ Modalités d encadrement IV/ Votre stage V/ Bilan global de votre stage I/ Présentation du service
Recours aux entreprises extérieures
 RECOMMANDATION R429 Recommandations adoptées par le Comité technique national de la chimie, du caoutchouc et de la plasturgie le 21 novembre 2006. Cette recommandation annule et remplace la recommandation
RECOMMANDATION R429 Recommandations adoptées par le Comité technique national de la chimie, du caoutchouc et de la plasturgie le 21 novembre 2006. Cette recommandation annule et remplace la recommandation
Qualité et gestion des risques
 formation 2007 Qualité et gestion des risques Qualité et certification HAS Démarche qualité Qualité et certification ISO Qualité en imagerie Qualité au laboratoire Management des risques Risques spécifiques
formation 2007 Qualité et gestion des risques Qualité et certification HAS Démarche qualité Qualité et certification ISO Qualité en imagerie Qualité au laboratoire Management des risques Risques spécifiques
FORMATION DU PERSONNEL. Année. Plan prévisionnel 2015 des actions de formation du personnel de l Université du Havre
 DU PERSONNEL Année Plan prévisionnel 2015 des actions de formation du personnel de l Université du Havre 1. LE PLAN DE. L élaboration du plan de formation. La direction des ressources humaines est chargée
DU PERSONNEL Année Plan prévisionnel 2015 des actions de formation du personnel de l Université du Havre 1. LE PLAN DE. L élaboration du plan de formation. La direction des ressources humaines est chargée
RÈGLES DE CERTIFICATION D ENTREPRISE
 RÈGLES DE CERTIFICATION D ENTREPRISE Fabrication et transformation de matériaux et d emballages destinés au contact des aliments : respect des règles d hygiène (méthode HACCP) Réf. Rédacteur LNE PP/GLB
RÈGLES DE CERTIFICATION D ENTREPRISE Fabrication et transformation de matériaux et d emballages destinés au contact des aliments : respect des règles d hygiène (méthode HACCP) Réf. Rédacteur LNE PP/GLB
TRAVAUX DU GROUPE GUINEE/CONAKRY ET BISSAO
 TRAVAUX DU GROUPE GUINEE/CONAKRY ET BISSAO PLAN DE PRESENTATION BREVE PRESENTATION DES DEUX PAYS - GUINEE/CONAKRY GUINEE BISSAO Population = 7 156 406hbts dont 51% de femmes et 46% de jeunes, - 1 200 000
TRAVAUX DU GROUPE GUINEE/CONAKRY ET BISSAO PLAN DE PRESENTATION BREVE PRESENTATION DES DEUX PAYS - GUINEE/CONAKRY GUINEE BISSAO Population = 7 156 406hbts dont 51% de femmes et 46% de jeunes, - 1 200 000
GUIDE POUR LA MISE SUR LE MARCHÉ DE DISPOSITIFS MÉDICAUX SUR MESURE APPLIQUE AU SECTEUR DENTAIRE
 Actualisation Mai 2012 Direction de l'evaluation des Dispositifs Médicaux Département Surveillance du Marché GUIDE POUR LA MISE SUR LE MARCHÉ DE DISPOSITIFS MÉDICAUX SUR MESURE APPLIQUE AU SECTEUR DENTAIRE
Actualisation Mai 2012 Direction de l'evaluation des Dispositifs Médicaux Département Surveillance du Marché GUIDE POUR LA MISE SUR LE MARCHÉ DE DISPOSITIFS MÉDICAUX SUR MESURE APPLIQUE AU SECTEUR DENTAIRE
Rôle de l Assurance Qualité dans la recherche clinique
 Rôle de l Assurance Qualité dans la recherche clinique Pôle Qualité / Gestion des Risques 05 Janvier 2012 Plan La qualité d une recherche c est quoi? Bonnes Pratiques Cliniques (BPC) Responsabilités des
Rôle de l Assurance Qualité dans la recherche clinique Pôle Qualité / Gestion des Risques 05 Janvier 2012 Plan La qualité d une recherche c est quoi? Bonnes Pratiques Cliniques (BPC) Responsabilités des
Système de management H.A.C.C.P.
 NM 08.0.002 Norme Marocaine 2003 Système de management H.A.C.C.P. Exigences Norme Marocaine homologuée par arrêté du Ministre de l'industrie, du Commerce et des Télécommunications N 386-03 du 21 Février
NM 08.0.002 Norme Marocaine 2003 Système de management H.A.C.C.P. Exigences Norme Marocaine homologuée par arrêté du Ministre de l'industrie, du Commerce et des Télécommunications N 386-03 du 21 Février
La Qualité de SFR Business Team
 La Qualité de SFR Business Team au service de ses clients Faire équipe avec vous est la promesse de SFR Business Team faite à son marché. Présent et performant sur l ensemble des segments, de la TPE au
La Qualité de SFR Business Team au service de ses clients Faire équipe avec vous est la promesse de SFR Business Team faite à son marché. Présent et performant sur l ensemble des segments, de la TPE au
La démarche qualité dans les laboratoires d analyses de biologie médicale privés franciliens
 R E N N E S Pharmacien inspecteur de santé publique Promotion : 2006-2007 Date du Jury : Septembre 2007 La démarche qualité dans les laboratoires d analyses de biologie médicale privés franciliens Rochanak
R E N N E S Pharmacien inspecteur de santé publique Promotion : 2006-2007 Date du Jury : Septembre 2007 La démarche qualité dans les laboratoires d analyses de biologie médicale privés franciliens Rochanak
Elaborer des Tableaux de Bord Ressources Humaines
 Elaborer des Tableaux de Bord Ressources Humaines Pré-requis à la mise en place d un tableau de bord des ressources humaines Le recueil de données a été le point de départ du diagnostic quantitatif des
Elaborer des Tableaux de Bord Ressources Humaines Pré-requis à la mise en place d un tableau de bord des ressources humaines Le recueil de données a été le point de départ du diagnostic quantitatif des
Qualité. Sécurité Alimentaire
 Le service Qualité Présentation du Service Démarche Qualité Qualité Réalisation des dossiers d agrément sanitaire pour les cuisines centrales >60 affermés API Réalisation des dossiers d accréditation en
Le service Qualité Présentation du Service Démarche Qualité Qualité Réalisation des dossiers d agrément sanitaire pour les cuisines centrales >60 affermés API Réalisation des dossiers d accréditation en
MANUEL QUALITE HYGIENE SECURITE ET ENVIRONNEMENT
 MANUEL QUALITE HYGIENE SECURITE ET ENVIRONNEMENT 1/9 AVANT PROPOS Le présent manuel QHSE reflète toutes les dispositions mises en place par IOTA, relatives au système de management intégré (SMI). Aucunes
MANUEL QUALITE HYGIENE SECURITE ET ENVIRONNEMENT 1/9 AVANT PROPOS Le présent manuel QHSE reflète toutes les dispositions mises en place par IOTA, relatives au système de management intégré (SMI). Aucunes
Sécurité Sanitaire des Aliments. Saint-Pierre, le 19 novembre 2013. Olivier BOUTOU. Les outils de la qualité sanitaire dans les pays du sud
 Sécurité Sanitaire des Aliments Saint-Pierre, le 19 novembre 2013 Olivier BOUTOU Les outils de la qualité sanitaire dans les pays du sud Faisons connaissance Missions au sein d AFNOR Animation de formation
Sécurité Sanitaire des Aliments Saint-Pierre, le 19 novembre 2013 Olivier BOUTOU Les outils de la qualité sanitaire dans les pays du sud Faisons connaissance Missions au sein d AFNOR Animation de formation
A N N E X E 1. Introduction : référentiel d activités professionnelles page 7. Référentiel de certification page 21
 A N N E X E 1 Introduction : référentiel d activités professionnelles page 7 Référentiel de certification page 21 - Compétences professionnelles page 21 - Connaissances associées page 55 - Unités constitutives
A N N E X E 1 Introduction : référentiel d activités professionnelles page 7 Référentiel de certification page 21 - Compétences professionnelles page 21 - Connaissances associées page 55 - Unités constitutives
ADDITIF AU RAPPORT DE CERTIFICATION V2010 CLINIQUE CHIRURGICALE DU LIBOURNAIS
 ADDITIF AU RAPPORT DE CERTIFICATION V2010 CLINIQUE CHIRURGICALE DU LIBOURNAIS 119 rue de la marne - 33500 - Libourne NOVEMBRE 2014 SOMMAIRE PREAMBULE 1. Présentation du document 2. Les niveaux de certification
ADDITIF AU RAPPORT DE CERTIFICATION V2010 CLINIQUE CHIRURGICALE DU LIBOURNAIS 119 rue de la marne - 33500 - Libourne NOVEMBRE 2014 SOMMAIRE PREAMBULE 1. Présentation du document 2. Les niveaux de certification
Assurance de la qualité Initiation
 Assurance de la qualité Initiation Définition et principe La qualité, c est : L aptitude d un ensemble de caractéristiques intrinsèques à satisfaire des exigences ISO 9000 2000 3.1.1 Série des normes ayant
Assurance de la qualité Initiation Définition et principe La qualité, c est : L aptitude d un ensemble de caractéristiques intrinsèques à satisfaire des exigences ISO 9000 2000 3.1.1 Série des normes ayant
Organiser une permanence d accès aux soins de santé PASS
 Établissements de santé Droits et accueil des usagers Organiser une permanence d accès aux soins de santé PASS Recommandations et indicateurs Préface Faire face aux inégalités de santé qui touchent tout
Établissements de santé Droits et accueil des usagers Organiser une permanence d accès aux soins de santé PASS Recommandations et indicateurs Préface Faire face aux inégalités de santé qui touchent tout
Maisons de Santé Pluridisciplinaires. Conditions d éligibilité à des soutiens financiers
 Maisons de Santé Pluridisciplinaires Conditions d éligibilité à des soutiens financiers Les maisons de santé pluridisciplinaires (MSP) visent à offrir à la population, sur un même lieu, un ensemble de
Maisons de Santé Pluridisciplinaires Conditions d éligibilité à des soutiens financiers Les maisons de santé pluridisciplinaires (MSP) visent à offrir à la population, sur un même lieu, un ensemble de
Les mentions et abréviations employées se lisent donc de la façon suivante :
 CIRCULAIRE AD 94-2 DU 18 JANVIER 1994 Tri et conservation des archives des établissements publics de santé : documents produits après 1968 par les services administratifs chargés de la gestion des hospitalisations
CIRCULAIRE AD 94-2 DU 18 JANVIER 1994 Tri et conservation des archives des établissements publics de santé : documents produits après 1968 par les services administratifs chargés de la gestion des hospitalisations
Secteur Protégé d Hématologie
 INFORMATIONS PATIENTS Secteur Protégé d Hématologie Centre accrédité de greffe de moelle osseuse et de cellules souches d hématopoïétiques Le Secteur d Hématologie est destiné à des patients atteints de
INFORMATIONS PATIENTS Secteur Protégé d Hématologie Centre accrédité de greffe de moelle osseuse et de cellules souches d hématopoïétiques Le Secteur d Hématologie est destiné à des patients atteints de
Déclarations européennes de la pharmacie hospitalière
 Déclarations européennes de la pharmacie hospitalière Les pages qui suivent constituent les Déclarations européennes de la pharmacie hospitalière. Elles représentent l expression consensuelle de ce que
Déclarations européennes de la pharmacie hospitalière Les pages qui suivent constituent les Déclarations européennes de la pharmacie hospitalière. Elles représentent l expression consensuelle de ce que
Union des Coopératives Agricoles de l ALlier Approuvé par :
 Manuel Qualité et HACCP Indice : I Union des Coopératives Agricoles de l ALlier Approuvé par : Jacky COURRIER Directeur de COOPACA Jean-Claude MICHEL Directeur de Val limagne.coop La force d un groupe
Manuel Qualité et HACCP Indice : I Union des Coopératives Agricoles de l ALlier Approuvé par : Jacky COURRIER Directeur de COOPACA Jean-Claude MICHEL Directeur de Val limagne.coop La force d un groupe
Laissez-nous. prendre soin. de vous. Recrutement - Intérim - Services
 Laissez-nous prendre soin de vous Recrutement - Intérim - Services affirmer Nos différences Adecco Medical, filiale santé du leader mondial des solutions RH, a bâti une relation de confiance avec ses clients,
Laissez-nous prendre soin de vous Recrutement - Intérim - Services affirmer Nos différences Adecco Medical, filiale santé du leader mondial des solutions RH, a bâti une relation de confiance avec ses clients,
Mise au point sur LA MAINTENANCE DES DISPOSITIFS MEDICAUX. Octobre 2011. www.afssaps.fr. Agence française de sécurité sanitaire des produits de santé
 Octobre 2011 Mise au point sur LA MAINTENANCE DES DISPOSITIFS MEDICAUX Agence française de sécurité sanitaire des produits de santé 143-147 boulevard Anatole France F-93285 Saint-Denis Cedex www.afssaps.fr
Octobre 2011 Mise au point sur LA MAINTENANCE DES DISPOSITIFS MEDICAUX Agence française de sécurité sanitaire des produits de santé 143-147 boulevard Anatole France F-93285 Saint-Denis Cedex www.afssaps.fr
Un métier en évolution pour répondre aux nouvelles. Face à ces évolutions, un nouveau métier
 Les métiers de la pharmacovigilance Des métiers en évolution dans une industrie de haute technologie et d'innovation Une mission d'évaluation et de gestion des risques liés à l'utilisation des médicaments
Les métiers de la pharmacovigilance Des métiers en évolution dans une industrie de haute technologie et d'innovation Une mission d'évaluation et de gestion des risques liés à l'utilisation des médicaments
dossier de presse nouvelle activité au CHU de Tours p a r t e n a r i a t T o u r s - P o i t i e r s - O r l é a n s
 dossier de presse nouvelle activité au CHU de Tours lat ransplantation hépatique p a r t e n a r i a t T o u r s - P o i t i e r s - O r l é a n s Contact presse Anne-Karen Nancey - Direction de la communication
dossier de presse nouvelle activité au CHU de Tours lat ransplantation hépatique p a r t e n a r i a t T o u r s - P o i t i e r s - O r l é a n s Contact presse Anne-Karen Nancey - Direction de la communication
FNSA 91, avenue de la République 75011 PARIS
 Dossier de candidature QUALITASS FNSA 91, avenue de la République 75011 PARIS Documents à fournir Option 1 : Pièces à fournir (obligatoire dans le cadre d une première demande) Ou Option 2 : Engagement
Dossier de candidature QUALITASS FNSA 91, avenue de la République 75011 PARIS Documents à fournir Option 1 : Pièces à fournir (obligatoire dans le cadre d une première demande) Ou Option 2 : Engagement
