Le traitement chirurgical du cancer bronchique non à petites cellules
|
|
|
- Robert Grondin
- il y a 8 ans
- Total affichages :
Transcription
1 Série «considérations chirurgicales pour le pneumologue» Coordonnée par V. Ninane et G. Decker Le traitement chirurgical du cancer bronchique non à petites cellules P. de Leyn 1, G. Decker 1, 2 1 Hôpital universitaire de Leuven, Leuven, Belgique. 2 Chirurgie Thoracique, Centre Hospitalier Luxembourg, Luxembourg. Tirés à part : P. de Leyn Hôpital universitaire de Leuven, Herestraat 49, 3000 Leuven, Belgique. Paul.deleyn@uz.kuleuven.ac.be Réception version princeps à la Revue : Retour aux auteurs pour révision : Réception 1 ère version revisée : Acceptation définitive : Résumé Introduction La chirurgie reste la meilleure option thérapeutique à visée curative pour les stades précoces de cancer bronchique non-à-petites-cellules (CBNPC). Cet article analyse la situation actuelle et les perspectives de la chirurgie du CBNPC. État des connaissances L intervention chirurgicale débute par stadification peropératoire qui comprend une dissection systématique des ganglions hilaires et médiastinaux et se poursuit par une résection complète, déterminant majeur du pronostic. Perspectives La stratégie d économie du parenchyme pulmonaire explique le développement de lobectomies souvent élargies avec bronchoplastie (sleeve) en remplacement de la pneumonectomie. La thoracoscopie a une place dans la stadification invasive du cancer bronchique et la résection des CBNPC périphériques T1N0 (lobectomie thoracoscopique vidéo-assistée) avec des résultats en terme de survie pour ces petites tumeurs périphériques au moins aussi bons qu après chirurgie ouverte. En cas d atteinte ganglionnaire médiastinale (N2), un traitement systémique d induction est administré dans la plupart des centres et les répondeurs ont une survie significativement améliorée par rapport aux non-répondeurs. La re-stadification médiastinale après traitement d induction reste pour le moment très imprécise. Pour les tumeurs localement avancées (ct4), de nouvelles techniques et approches chirurgicales rendent réalisables des résections carénaires, vertébrales ou de la veine cave avec une morbidité et mortalité acceptable mais des études complémentaires sont nécessaires. Conclusions Une sélection rigoureuse des patients, une technique chirurgicale méticuleuse avec une prise en charge per- et postopératoire adéquate ont permis de réduire la morbidité et la mortalité de la chirurgie du CBNPC. L évolution des techniques chirurgicales et la multidisciplinarité devraient permettre d améliorer encore les résultats de ce traitement qui reste associé aux meilleures chances de guérison. Mots-clés : Cancer bronchique Chirurgie Chimiothérapie Thoracoscopie SPLF, tous droits réservés 971
2 P. De Leyn, G. Decker Surgical treatment of non-small cell lung cancer P. De Leyn, G. Decker Summary Introduction Surgery remains the best option for curative treatment of early stages Non-small cell lung cancer (NSCLC). In this article we review the current status and future perspectives of surgical treatment of NSCLC. State of art An important part of the surgical procedure is the final determination of the staging with evaluation of the resectablity of the tumor and its nodal status. This requires a systematic hilar and mediastinal nodal dissection and a complete resection that remains a major prognostic factor. Perspectives In order to preserve pulmonary function, lobectomies with the use of broncho- or arterioplasty have been developed with reduction in the number of pneumonectomies. For peripheral T1N0 NSCLC, videoassisted (VATS) lobectomy has become technically feasible with survival, in non-randomised studies, at least as good as the survival after open resection. While VATS has a clear role in staging of lung cancer, its role in the treatment of lung cancer however remains debatable. In case of involved mediastinal nodes (N2 disease) induction therapy is given in many centers and patients with mediastinal downstaging have a significantly better survival than nonresponders. Restaging of the mediastinum is at the moment far from accurate. In case of locally advanced tumour (ct4), new surgical techniques and approaches make resection of carina, vena cava superior, vertebrae feasible with acceptable morbidity and mortality but additional studies are required. Conclusions Surgery remains the treatment of choice for curative treatment of NSCLC. The evolution of surgical techniques and the use of multimodality treatment further improve the results of surgical management. Rigorous patient selection, meticulous surgical technique and adequate peri- and postoperative management can keep operative morbidity and morbidity acceptable. Key-words: Lung cancer Surgery Chemotherapy Thoracoscopie. Paul.deleyn@uz.kuleuven.ac.be Introduction Le cancer bronchique est la première cause de mortalité par cancer. Globalement, 80 % des nouveaux cas de cancer bronchiques sont de type non à petites cellules (CBNAPC). Malheureusement, la plupart des cas sont diagnostiqués à un stade avancé et seulement 15 % des patients présentent lors du diagnostic une maladie localisée au poumon. Pour les patients à un stade précoce de la maladie (stades I et II) ainsi que pour des patients sélectionnés ayant une maladie localement avancée (stade IIIa) la résection chirurgicale complète de la tumeur reste le meilleur espoir de guérison. La survie du patient après résection chirurgicale dépend du stade anatomopathologique définitif de la tumeur. Cet article discutera l étendu de la résection pulmonaire et des curages ganglionnaires, la place de la chirurgie dans le cancer localement avancé, la place de la thoracoscopie dans le traitement du cancer bronchique, la morbidité et mortalité actuelle des résections pulmonaires ainsi que du rôle éventuel de traitements adjuvants après une résection complète du cancer bronchique. Étendue de la résection chirurgicale Résection pulmonaire Résections anatomiques Il est bien établi qu une résection anatomique (lobectomie ou pneumonectomie) est préférable à une résection limitée ou «à la demande» de la tumeur pulmonaire car ces dernières ont un taux supérieur de récidives locales et une moindre survie à long terme. Les termes résection «en-coin» ou «à la demande» se réfèrent à une résection du parenchyme pulmonaire comportant la tumeur qui est non anatomique, c est-à-dire qui ne suit pas les divisions anatomiques lobaires voire segmentaires. Le parenchyme pulmonaire y est réséqué en sectionnant à travers des structures bronchiques, vasculaires et lymphatiques, laissant donc en place des structures pouvant augmenter le risque de récidive locale. Le Lung Cancer Study Group a rapporté la première étude prospective contrôlée multicentrique et randomisée qui a comparé la lobectomie avec des résections plus limitées pour des tumeurs non à petites cellules T1N0 [1]. Seules des tumeurs T1N0 étaient incluses dans l étude. Le chirurgien devait avoir la conviction que la tumeur était complètement réséquable au moyen d une résection «en coin». Pendant l intervention le traitement était tiré au sort entre une lobectomie ou une résection limitée mais macroscopiquement complète. Au total sur 247 patients éligibles, 122 patients ont eu une résection limitée et 125 ont bénéficié d une lobectomie. Le taux de récidive par patient et année était de 0,101 dans le groupe résection limitée contre 0,057 dans le groupe lobectomie. Cette différence de 75 % était statistiquement significative. Le délai jusqu à la récidive était également 972
3 Le traitement chirurgical du cancer bronchique non à petites cellules Fig. 1. Lobectomie avec bronchoplastie du lobe supérieur droit. significativement différent. La fonction respiratoire n a pu être évaluée chez tous les patients. Néanmoins à 6 mois, la fonction respiratoire était significativement meilleure dans le groupe avec une résection plus limitée. Cette différence s est ensuite significativement estompée à 12 et 18 mois de suivi. La survie était identique dans les deux groupes jusqu à 48 mois. À partir de là, la survie était meilleure dans le groupe ayant eu une lobectomie. D autres études plus petites ont étudié la même question [2, 3]. Dans la plupart de ces études, les patients qui ont eu une résection limitée avaient une mauvaise fonction respiratoire ou une comorbidité importante. Dans l étude de Pittsburgh rapportée par Landreneau, 41 patients atteints de cancer non à petites cellules ont eu une résection limitée par voie ouverte, 60 % une résection limitée par voie thoracoscopique et 118 patients ont eu une lobectomie avec lymphadénectomie [2]. La survie à 5 ans était respectivement de 58 % et 65 % après résection non-anatomique ouverte et thoracoscopique contre 70 % après lobectomie ouverte (p = 0,02). Il faut souligner que les décès non liés au cancer étaient plus fréquents après résection limitée (38 %) qu après lobectomie (18 %). Une étude japonaise a comparé des petites tumeurs T1 traitées par résection limitée ou par lobectomie. Il n y avait pas de différence en terme de fonction respiratoire préopératoire ni en morbidité liée au geste chirurgical. La survie globale à 5 ans était de 93 % après segmentectomie contre 88 % dans le groupe lobectomie. Il n y avait pas de différence significative en terme de mortalité due au cancer bronchique ni en récidive tumorale [3]. Néanmoins, cette étude n était pas randomisée et la taille des tumeurs était significativement plus grande dans le groupe des patients traités par lobectomie que dans celui traité par segmentectomie, ce qui a pu favorablement influencer les résultats du groupe segmentectomie. Sur la base de ces études, nous devons conclure que la résection anatomique (lobectomie) reste le standard du traitement chirurgical du cancer bronchique même pour des tumeurs T1 de moins de 3 cm de diamètre. Il est cependant évident que pour des patients, qui sur le plan fonctionnel, ne pourraient tolérer une lobectomie, une résection non-anatomique est justifiée pour des tumeurs de moins de 3 cm ou toute autre tumeur localisée dans le tiers extérieur (périphérique) du parenchyme pulmonaire. Classiquement, chaque fois qu une lobectomie ne permet pas une résection complète, une bi-lobectomie voire pneumonectomie s imposait pour les patients qui avaient une réserve respiratoire suffisante pour un tel geste. Actuellement ces résections parenchymateuses majeures peuvent souvent être évitées par une lobectomie avec bronchoplastie (sleeve resection). Lobectomie avec bronchoplastie (Sleeve lobectomy) Quand la tumeur envahit l origine d une bronche lobaire, une lobectomie simple est insuffisante. Dans ce cas une pneumonectomie peut être évitée et une résection complète obtenue au moyen d une lobectomie élargie emportant la division bronchique envahie suivie d une réimplantation du lobe restant sur la bronche souche. Il s agit d une lobectomie avec bronchoplastie ou sleeve lobectomy. La bronchoplastie la plus souvent réalisée est la bronchoplastie du lobe superieur droit (fig. 1). Ce type de résection peut également être pratiqué quand des ganglions N1 sont fixés à l origine de la bronche lobaire à réséquer. Une sleeve lobectomie semble adéquate pour environ 5 à 8 % de toutes les résections pour cancer bronchique. La réalisation des lobectomies avec bronchoplastie diminue le nombre de pneumonectomies avec des résultats oncologiques similaires. Ainsi, dans notre centre pendant la période , 648 résections majeures pour cancer bronchique non à petites cellules ont été réalisées, dont 287 pneumonectomies (44 %) [4]. En comparaison, en 2002 et 2003, seules 15,6 % de ces résections étaient des pneumo SPLF, tous droits réservés 973
4 P. De Leyn, G. Decker nectomies. L avantage est qu après une lobectomie avec bronchoplastie, les patients bénéficient d une meilleure qualité de vie car ils gardent une meilleure réserve respiratoire qu après pneumonectomie. Par ailleurs, une résection subséquente reste plus souvent possible si une nouvelle tumeur primitive devait ultérieurement apparaître. Particulièrement après chimio- ou radio-chimiothérapie d induction, une pneumonectomie devrait être évitée aussi souvent que possible car dans ce contexte elle est grevée d un risque de mortalité élevé. Dans la mesure où, après un traitement d induction, un curage ganglionnaire radical est réalisé, ce qui entraîne une dévascularisation bronchique, la question se pose également de savoir si une résection lobaire avec bronchoplastie peut être réalisée en toute sécurité. Rendina et coll. [5] ont rapporté une série de 27 patients opérés par lobectomie avec bronchoplastie après traitement d induction. Des complications majeures sont survenues chez 11 % des patients et il n y a eu aucun décès post-opératoire. La survie à 4 ans dans cette série était de 39 %. Dans notre propre expérience de lobectomies et bronchoplasties après traitement d induction aucune mortalité n est à signaler. Sur la base de ces observations, nous croyons en la faisabilité des résections avec bronchoplastie après un traitement d induction systémique, mais le chirurgien doit garder à l esprit que souvent, l intervention est techniquement plus difficile dans ce contexte. La survie à 5 ans après lobectomie et bronchoplastie se situe entre 45 et 50 % [4, 6, 7]. Dans une étude rétrospective [4] nous avons analysé la survie des patients porteurs d un carcinome épidermoïde aux stades T2-3N0-1 après pneumonectomie ou après lobectomie avec bronchoplastie. Nous n avons trouvé aucune différence de survie puisque dans ce sous-groupe de patients la survie à 5 ans était de 48,1 % après pneumonectomie contre 50,2 % après lobectomie avec bronchoplastie. Okada et coll. [8] ont comparé la survie après lobectomie et bronchoplastie ou après pneumonectomie en fonction du stade d envahissement ganglionnaire. Un groupe apparié de 60 patients opérés par lobectomie avec bronchoplastie était comparé à un groupe similaire de patients pneumonectomisés. La mortalité opératoire était de 0 % dans le groupe avec bronchoplastie contre 2 % dans le groupe avec pneumonectomie. Une récidive locale est survenue chez 5 patients (8 %) après lobectomie et bronchoplastie versus 6patients (10%) après pneumonectomie. La survie à 5 ans était significativement meilleure après lobectomie et bronchoplastie (48 %) que pour les patients pneumonectomisés (29 %). Pour les patients ayant des métastases ganglionnaires N1 chez lesquels une résection complète peut être obtenue par l une ou l autre de ces techniques, la lobectomie avec bronchoplastie a également été recommandée plutôt que la pneumonectomie [9]. La même technique de bronchoplastie permet, chez des patients ayant une atteinte d une bronche souche (préférentiellement la droite) mais sans atteinte ganglionnaire de type N2, de procéder à une résection complète emportant la carène tout en réanastomosant le poumon restant (généralement le gauche). La faisabilité de ces résections carénaires étant notoires, leur morbi-mortalité en est néanmoins élevée [10]. Le curage ganglionnaire La détermination préopératoire du stade clinique est actuellement loin d être parfaite. Lors de la thoracotomie, le chirurgien a le rôle important d évaluer l extension locale de la tumeur mais également le degré d atteinte ganglionnaire. Ces deux facteurs pourront être décisifs pour décider quel type de résection devra (ou ne pourra pas) être réalisé. Aussi bien le stade ganglionnaire (N) que le stade tumoral (T) sont souvent sous-estimés en préopératoire et ce n est que lors de la thoracotomie que le stade précis de la maladie devient apparent. Si tout le monde est d accord sur le fait que la mise au point préopératoire devrait aboutir à la stadification clinique la plus correcte possible, l évaluation ganglionnaire médiastinale pendant le geste chirurgical reste controversée et très variable d un centre à l autre. Un sondage bien suivi parmi la majorité des chirurgiens faisant des résections pulmonaires au Royaume-Uni a montré que 45 % de ces chirurgiens ne prélèvent jamais des ganglions qui macroscopiquement paraissent grossièrement normaux alors que seulement 23 % procédaient à une résection systématique de tous les tissus ganglionnaires médiastinaux [11]. Il existe donc une grande variabilité dans l attitude face à l exploration ganglionnaire médiastinale. La pratique chirurgicale actuelle varie d une inspection visuelle du médiastin fermé jusqu au curage médiastinal radical et systématique. La connaissance précise de la technique opératoire de chaque centre est importante si on veut analyser ses résultats thérapeutiques à la lumière des données de la littérature. En général, le terme «échantillonnage» (sampling) signifie que seuls les ganglions manifestement anormaux sont enlevés. «L échantillonnage systématique» (systematic sampling) signifie que, aux niveaux ganglionnaires spécifiés par l auteur, les ganglions sont systématiquement biopsiés. Le curage ganglionnaire médiastinal complet (mediastinal lymph node dissection) indique que tous les tissus contenant des structures ganglionnaires sont systématiquement réséqués aux stations ganglionnaires indiquées par l auteur. La stadification intra-thoracique est essentielle pour : évaluer l exactitude de la stadification préopératoire ; identifier et classer correctement des groupes de patients ayant un pronostic différent ; comparer les résultats de différents protocoles thérapeutiques ; promouvoir une utilisation rationnelle des traitements adjuvants disponibles dans le futur. Il est évident que la méthodologie actuelle de stadification clinique préopératoire n est pas optimale. Ceci est notamment illustré par le fait que dans notre centre, malgré une attitude de mise au point maximale du médiastin, 14 % des patients avaient une atteinte N2 inattendue (unforeseen) au moment de la thoracotomie [12]. Durant cette période, une médiastinoscopie cervicale était systématiquement réali- 974
5 Le traitement chirurgical du cancer bronchique non à petites cellules sée sauf chez les patients porteurs d un carcinome épidermoïde ct1-t2 sans adénopathie médiastinale significative au CT-scan. Dans la série du Brompton, bien qu une médiastinoscopie était réalisée chaque fois que le CT-scan montrait des ganglions médiastinaux élargis, une atteinte ganglionnaire N2 «inattendue» ou «imprévisible» était trouvée lors de 25 % des thoracotomies [13]. Chez environ un tiers des patients, les ganglions médiastinaux sont atteints alors que les ganglions hilaires ou intra-pulmonaires ne le sont pas [14]. Ces «sauts» de relais ganglionnaires (skip metastasis) s expliquent probablement par des lymphatiques sous-pleuraux qui se drainent directement vers le médiastin. Ceci a été suggéré par les travaux de Riquet et coll. [15] qui avaient injecté un colorant bleu dans les lymphatiques pleuraux d un segment pulmonaire. Un passage direct du colorant vers les ganglions médiastinaux a été observé à droite chez 22 % des sujets et à gauche chez 25 %, le plus fréquemment en cas d atteinte lobaire supérieure. Ces connexions lymphatiques directes avec le médiastin, par des voies souvent superficielles, sous-pleurales expliquent donc les sauts métastatiques qui rendraient nécessaire le curage ganglionnaire systématique même lorsque les ganglions interlobaires et hilaires sont indemnes. Une large variabilité technique semble aussi exister dans la technique de stadification peropératoire et même la désignation des aires ganglionnaires semble souffrir d une large variabilité entre observateurs. Dans l étude de Watanabe [16], 424 aires ganglionnaires ont été excisées chez 41 patients opérés par thoracotomie pour un cancer non-à-petites cellules. De façon indépendante, deux chirurgiens devaient attribuer les ganglions aux différentes aires ganglionnaires de la carte de Naruke [17]. Le choix de ces positions était ensuite analysé. Dans 68,5 % seulement des ganglions, la position attribuée par les deux observateurs était concordante. La variabilité entre les observateurs était lourde de conséquences puisque pour 34 % des patients elle aboutissait à un stade N1 pour l un des observateurs alors que l autre classait ces mêmes ganglions comme N2. La variabilité dans les techniques d échantillonnage ou de curage ganglionnaire et celle dans l interprétation de la localisation ganglionnaire ne doit être perdue de vue quand on veut interpréter différents résultats chirurgicaux dans la littérature. Les résultats de l étude IALT (international adjuvant lung trial) viennent récemment d être présentés [18]. Dans cette étude une chimiothérapie adjuvante à base de Cisplatine donnait un avantage de survie à 5 ans de 5 % après résection chirurgicale complète. Le sous-groupe ayant le plus bénéficié du traitement adjuvant est le groupe IIIA. Une stadification opératoire précise est donc requise afin de pouvoir bien sélectionner les patients pour un tel traitement adjuvant. Une question importante est également de savoir si le curage médiastinal influence la survie. Dans la seule étude prospective randomisée, le curage médiastinal radical n a amélioré ni la survie, ni le taux de récidives [19]. Néanmoins dans le sous-groupe des patients pn1 et pn2 qui n avaient une atteinte que d un seul niveau ganglionnaire, la survie était meilleure après lymphadénectomie radicale qu après simple échantillonage ganglionnaire. Dans une étude non-randomisée comparant l échantillonnage ganglionnaire systématique au curage radical, la survie était meilleure après curage radical [20]. Mais ceci ne s appliquait que pour des interventions à droite et des patients aux stades II et IIIA. La principale critique que l on puisse faire de cette étude repose sur le fait qu il s agissait d une étude multicentrique étudiant l effet de la chimio-thérapie adjuvante. Sur 190 chirurgiens participants, 131 n ont inclus qu un seul patient dans l étude ce qui en limite très fortement la validité. Même s il n est donc pas formellement prouvé qu un curage ganglionnaire médiastinal améliore la survie ou le taux de récidives, il est généralement admis que la résection complète d un cancer bronchique requiert une résection pulmonaire adéquate et un curage ganglionnaire médiastinal. Le curage systématique permet sans aucun doute d obtenir une stadification chirurgicale plus précise et donc une classification plus précise des patients en stades histologiques I, II et IIIA définitifs (ptnm), ce qui devrait se traduire par une amélioration de la survie dans chacun de ces stades. Depuis une réunion internationale de consensus organisé par l International Association for the Study of Lung Cancer à Londres en 1996, la façon de procéder est appelée «curage systématique» ou systematic nodal dissection [21]. Ce geste est réalisé lors de la thoracotomie, dans le but de mieux stadifier la tumeur, et consiste à réséquer et examiner de façon systématique les ganglions médiastinaux, hilaires et lobaires. La tumeur primitive étant jugée réséquable, on débute par le curage médiastinal avant la résection pulmonaire. Il est recommandé de disséquer tous les ganglions médiastinaux, au moins trois niveaux doivent être disséques, et toujours les ganglions sous-carénaires. Idéalement, pour les ganglions médiastinaux, du côté droit, les niveaux 2R (paratrachéal haut), 4R (trachéo-bronchique), 7 (sous-carénaire), 8 (para-oesophagien) et 9 (ligament pulmonaire inférieur) sont réséqués. À gauche, les ganglions des niveaux 4L, 5 (fenêtre aorto-pulmonaire), 6 (para-aortique), 7, 8 et 9 sont réséqués [22]. Dans notre propre expérience comme dans celle de beaucoup d autres équipes, ce curage systématique est réalisable sans aucune morbidité ou mortalité surajoutée [23, 24]. Une autre approche est de faire le curage ganglionnaire en fonction de la localisation bronchique de la tumeur pulmonaire. Ceci est inspiré par le travail de Naruke [17] et reflète le drainage principal de la tumeur. Ceci inclut pour les tumeurs du lobe supérieur droit les ganglions 4R (trachéobronchique), pour la tumeur du lobe moyen les ganglions 7 (sous-carénaires), pour la tumeur du lobe inférieur droit les ganglions de l aire 7 (sous-carénaire), 8 (para-oesophagien) et 9 (ligament pulmonaire inférieur). À gauche, en cas de tumeur du lobe supérieur les ganglions 4L, 5 (fenêtre aortopulmonaire) et 6 (para-aortique), pour les tumeurs du lobe inférieur les ganglions 7, 8 et SPLF, tous droits réservés 975
6 P. De Leyn, G. Decker Impact thérapeutique d une atteinte ganglionnaire N1 découverte en peropératoire Les règles chirurgicales du cancer bronchique prévoient la résection des ganglions hilaires et inter-lobaires afin de déterminer plus précisément l étendue de la résection requise. Une atteinte ganglionnaire hilaire peut obliger à une résection plus étendue que la lobectomie initialement prévue. Quand de tels ganglions envahissent l artère pulmonaire ou la bronche intermédiaire ou souche, une lobectomie élargie avec plastie de la bronche et/ou de l artère pulmonaire voire une pneumonectomie peut devenir inévitable. Pour des tumeurs situées dans les lobes supérieurs, il est généralement admis qu en cas d atteinte des ganglions à l origine du lobe ou même des ganglions hilaires, la résection pourra être complète au moyen d une lobectomie supérieure pour autant que celle-ci emporte tous ces niveaux ganglionnaires. Pour des tumeurs des lobes inférieurs la controverse persiste sur l étendue de la résection en cas d atteinte des ganglions à la racine lobaire [24]. Ces ganglions se trouvent sur la bronche intermédiaire ou l artère pulmonaire au niveau de la grande scissure. Pour une tumeur lobaire inférieure droite, en pareille situation, la plupart des centres réalisent une bi-lobectomie inférieure (c est-à-dire emportant les lobes inférieur et moyen) si la réserve respiratoire du patient le permet. Dans le passé, beaucoup d entre nous ont systématiquement réalisé une pneumonectomie quand les ganglions le long de la bronche intermédiaire étaient envahis. Actuellement, beaucoup de centres [25] ont adopté la stratégie d une lobectomie avec curage ganglionnaire quand les ganglions positifs n envahissent aucune structure et qu une résection complète peut donc être obtenue. Quand les ganglions sont fixés sur la bronche, une lobectomie de type sleeve, plutôt qu une pneumonectomie est actuellement préconisée comme traitement de choix. Dans l importante série de Deslauriers et coll. [9] comparant rétrospectivement la survie de 184 patients opérés par lobectomie et bronchoplastie avec celle de pneumonectomies réalisées dans le même centre, pour les patients ayant une atteinte N1, la survie après lobectomie-bronchoplastie était significativement meilleure qu après pneumonectomie (survie médiane 5,1 ans versus 2,8 ans ; p = 0,008) [26]. Pour les patients aux stades 1 et 2 ainsi que pour ceux classés pn0, la survie après lobectomiebronchoplastie était également significativement meilleure, illustrant l effet bénéfique de l épargne de parenchyme pulmonaire fonctionnel. Impact thérapeutique d une atteinte ganglionnaire N2 découverte de façon inattendue en peropératoire Aussi rigoureuse que soit la mise au point préopératoire du médiastin, la découverte d une atteinte N2 inattendue au cours de la thoracotomie reste toujours possible. Au Royal Brompton Hospital, la pratique du curage systématique a ainsi pu révéler une atteinte N2 chez 25 % des patients. Durant la thoracotomie, la maladie N2 était macroscopiquement visible chez 16 % des patients alors que chez 9 % l atteinte était identifiée seulement par l examen histologique de ganglions d apparence normale [13]. Durant la même période, notre taux de «maladie N2 inattendue» était de 14 %. Depuis lors, l utilisation systématique du PET-scan a modifié notre bilan préopératoire d extension. Grâce à sa valeur prédictive négative très élevée pour l atteinte médiastinale, le PET-scan a permis d abaisser notre taux de N2 «inattendus» en dessous des 10 % [27]. Les patients restants présentent généralement une atteinte N2 très limitée et toujours réséquable, avec comme conséquence que, si de façon générale la chirurgie première pour des patients avec une atteinte N2 est peu utile, ceux qui ont une telle atteinte N2 «inattendue» représentent un sous-groupe de patients qui souvent profitent d une résection primaire. Plusieurs auteurs ont ainsi rapporté des taux de réséquabilité élevés (87,4 % dans notre centre) et des taux de survie à 5 ans au-delà de 20 % en cas de résection complète et ce, sans aucun traitement adjuvant [12, 28]. Le PET-scan et sa valeur prédictive négative élevée et à défaut de PET-scan, la pratique de médiastinoscopie cervicale systématique, permettent une sélection telle que les seules atteintes N2 «inattendues» persistantes sont minimes et généralement limitées à l atteinte intra-capsulaire d une seule aire ganglionnaire. Dans ces conditions, on peut donc procéder à la résection car l atteinte ganglionnaire médiastinale «inattendue» est quasiment toujours réséquable et ne requiert que rarement un élargissement de la résection pulmonaire initialement prévue. Ce n est que dans les cas exceptionnels où la résection complète des ganglions N2 serait techniquement impossible que nous refermons la thoracotomie sans résection pulmonaire, pour ensuite administrer une chimiothérapie d induction suivie de radiothérapie voire éventuellement d une résection chirurgicale ultérieure en cas de réponse favorable. Rôle actuel de la thoracoscopie dans le traitement du cancer bronchique Il est évident que la thoracoscopie vidéo-assistée joue un rôle important dans le bilan invasif de stadification du cancer bronchique non-à petites cellules. Ainsi, des ganglions suspects de la fenêtre aorto-pulmonaire sont aisés à biopsier par thoracoscopie. Dans cette indication, la thoracoscopie représente une alternative attrayante à la médiastinotomie antérieure car elle a l avantage de permettre de mieux visualiser les structures vasculaires ou le nerf phrénique. La thoracoscopie est également utile pour le diagnostic d épanchements pleuraux quand la thoracocentèse n a permis aucun diagnostic et elle permet également une résection facile de nodules périphériques indéterminés quand un diagnostic histologique est souhaité. La résection pulmonaire par thoracoscopie est devenue faisable grâce aux avancées technologiques des années 1980 et 1990, comme l adjonction de systèmes vidéo de plus en plus performants, l amélioration progressive des optiques et 976
7 Le traitement chirurgical du cancer bronchique non à petites cellules caméras, le développement d instruments chirurgicaux dédiés à ces techniques et l essor des agrafeuses mécaniques endoscopiques. Actuellement, la lobectomie par thoracoscopie vidéo-assistée est généralement réalisée en s aidant d une petite incision accessoire (utility incision) mesurant 5 à 8 cm et la plupart des chirurgiens préconisent l absence de recours à l écartement costal. Le rôle de la thoracoscopie dans le traitement du cancer bronchique reste très débattu. Les avantages potentiels sont une moindre douleur, une moindre perturbation de la fonction pulmonaire et une moindre dépression des cytokines d où une meilleure préservation des fonctions immunitaires. Néanmoins, ces hypothèses ne sont soutenues à ce jour par aucune donnée convaincante d études prospectives randomisées. Bien que la lobectomie thoracoscopique soit techniquement difficile, sa faisabilité a été prouvée par plusieurs centres. Les survies après lobectomie thoracoscopique pour cancers de stade I ont été rapportées par plusieurs auteurs comme étant au moins aussi élevées qu après lobectomie par thoracotomie classique [29]. Sugi et coll. [30] ont rapporté une étude prospective de cancers bronchiques NSCLC de stade clinique I par lobectomie thoracoscopique (n = 48) versus lobectomie conventionnelle (n = 52). La survie à 5 ans était de 90 % dans le groupe thoracoscopique versus 85 % dans le groupe thoracotomie conventionnelle. Walker et coll. [31] ont réalisé 159 lobectomies thoracoscopiques pour des stades cliniques I et II. Tous les patients ont eu une médiastinoscopie cervicale préalable et la taille maximale des tumeurs était de 5 cm. La survie à 5 ans des patients au stade pathologique I était de 77,9 % contre 51 % pour le stade II. Une récidive fut identifiée chez 36 patients (22,6 %) et elle était locale pour neuf d entre eux. Ces chiffres sont en réalité au moins aussi bons que les résultats classiquement obtenus après lobectomie ouverte. D autres centres ont rapporté des résultats de survie aussi bons [32]. Une meilleure survie dans l option thoracoscopique pourrait s expliquer par une moindre immunodépression post-opératoire. Pour ces motifs, nous pensons qu une lobectomie par thoracoscopie vidéo-assistée se justifie actuellement pour des patients ayant une tumeur périphérique de stade I et pour lesquels un bilan par PET-scan et/ou médiastinoscopie ne retient aucun argument pour une atteinte hilaire ou médiastinale. La technique opératoire reste encore un défi et nécessite une longue courbe d apprentissage. Les potentiels avantages de l approche thoracoscopique en termes de meilleure survie ou de moindre douleur ou morbidité doivent encore être démontrés par des études randomisées. La chirurgie des stades avancés de cancer non-à petites cellules Les patients ayant une atteinte ganglionnaire médiastinale ipsilatérale (N2) et ceux ayant une tumeur T4 sont potentiellement réséquables. Ils sont regroupés sous le stade IIIA. Traitement chirurgical de l atteinte N2 Les patients ayant une atteinte des ganglions médiastinaux ipsilatéraux ou sous-carénaires ont un mauvais pronostic. Même si, techniquement, leur tumeur est souvent opérable, la survie à 5 ans est très faible. Pearson a ainsi opéré un groupe sélectionné de patients avec des ganglions positifs à la médiastinoscopie cervicale [33]. Les patients ayant une atteinte extra-capsulaire et ceux avec une atteinte des ganglions paratrachéaux hauts étaient exclus. Au total seul un cinquième des patients avec une médiastinoscopie positive furent opérés. Malgré cette sélection importante, une résection complète n a pu être obtenue que chez 64 % des patients et la survie à 5 ans des patients opérés n était que de 9 %. Dans une série japonaise rapportée par Funatsu et coll. [34], 117 patients ont été opérés malgré une atteinte N2. Une résection complète n a été obtenue que chez 11 % des patients, une résection incomplète a été réalisée chez 66 % et aucune résection chez 22 % d entre-eux. La survie à 5 ans des patients réséqués n était que de 6 %. Dans une telle situation où une résection ne permet d obtenir qu une probabilité de survie dépassant à peine le risque de mortalité opératoire, il est évident que la recommandation de ce traitement chirurgical impose la plus grande prudence. Le seul sous-groupe de patients avec atteinte N2 qui peuvent bénéficier d une résection chirurgicale primaire est celui des patients ayant une atteinte N2 «inattendue» ou imprévisible. Chez ces patients le CT-scan et/ou la médiastinoscopie ne montre aucune adénopathie envahie et ce n est que lors de la thoracotomie qu une atteinte ganglionnaire inattendue est détectée. Ce cas de figure peut concerner jusqu à 25 % des patients et la fréquence dépendra en réalité de la précision du bilan préopératoire et de l étendue de la dissection ganglionnaire peropératoire. Le sous-groupe de patients avec N2 inattendu peut profiter d une résection chirurgicale primaire comme l ont démontré plusieurs auteurs qui ont rapporté des taux de réséquabilité et de survie à 5 ans élevés atteignant 25 à 30 % en cas de résection complète [12, 17]. En Amérique du nord et Europe de l ouest, beaucoup de centres administrent une chimiothérapie ou chimio-radiothérapie d induction aux patients présentant une atteinte N2. Les avantages théoriques de cette approche dite «néoadjuvante» sont nombreux. La réduction du volume tumoral afin d en augmenter la réséquabilité et l élimination de micrométastases à distance sont les principaux buts de cette stratégie et l explication de ces avantages potentiels aux patients contribue à leur faire accepter la chimiothérapie. La littérature contient beaucoup d études non-randomisées de phase II de patients très sélectionnés traités par chimio- et/ou chimioradiothérapie suivies d une résection chirurgicale. Les résultats de ces études de phase II suggèrent que l approche néo-adjuvante pourrait améliorer les taux de réséquabilité et de survie par rapport à l approche chirurgicale seule [35]. Huit petites études randomisées étudiant les traitements adjuvants pour le stade IIIa ont été publiées. Une analyse 2004 SPLF, tous droits réservés 977
8 P. De Leyn, G. Decker exhaustive de ces séries dépasse le cadre de cet article. Les deux études les plus connues sont celles de Rossell et celle de Roth [36-39] et une description détaillée de toutes ces études vient récemment d être publiée [40]. Beaucoup de doutes persistent autour de ces études de phase III. Ceux-ci proviennent surtout du fait que souvent le bilan pré-traitement n incluait aucune mise au point invasive des ganglions médiastinaux (pas plus que de PET-scan), que les patients inclus pouvaient avoir des pronostics très divers (T3N0 et T3N1) et que la plupart de ces études ont inclus un nombre très faible de patients. Une interrogation majeure provient d une large étude randomisée européenne comparant chimiothérapie d induction suivie de chirurgie versus chirurgie seule, dans laquelle un bénéfice pour le bras chimiothérapie est suggéré pour les stades I et II mais pas pour les patients ayant une atteinte ganglionnaire médiastinale (stade IIIa) [41]. Le status des ganglions médiastinaux après chimiothérapie d induction constitue un important facteur pronostique des patients opérés après une telle chimiothérapie. Les patients présentant une guérison (downstaging) de leur atteinte médiastinale semblent avoir une bien meilleure survie que les patients dont l atteinte ganglionnaire N2 persiste. Bueno et coll. ont ainsi rapporté que les patients rétrogradés à une atteinte pathologique N0 avaient une survie à 5 ans de 35,8 % contre seulement 9 % de survie pour ceux dont l atteinte ganglionnaire persistait après chimiothérapie [42]. Le bilan clinique de réponse au traitement d induction demeure un problème majeur. Actuellement, la réévaluation des ganglions médiastinaux après chimiothérapie d induction est loin d être adéquate. Le CT-scan a été démontré comme tout à fait non fiable [43] et aussi bien le re-pet-scan que la remédiastinoscopie ont une précision de moins de 70 % [44, 45]. Sur la base de ces observations et en attendant des données plus larges de survie des patients avec atteinte N2 persistante, notre politique reste celle d explorer chirurgicalement tous les patients semblant répondeurs ou stables et de procéder à la résection avec curage ganglionnaire médiastinal radical chaque fois qu une résection complète semble faisable, indépendamment du fait que les ganglions médiastinaux demeurent positifs lors de la thoracotomie. La chirurgie pour les tumeurs T4 L extension tumorale T4 est généralement considérée comme inopérable. L atteinte T4 inclut l envahissement tumoral de la veine cave supérieure, l aorte, les vaisseaux pulmonaires intra-péricardiques, la trachée ou la carène. L envahissement du péricarde, la présence de métastases pleurales, d épanchement pleural ou péricardique malin mais également la présence de nodules satellites dans le même lobe que la tumeur primitive sont également considérés comme T4. Certaines de ces structures peuvent être réséquées et la chirurgie primaire pour traiter l envahissement de la veine cave supérieure, de la carène et des corps vertébraux a été décrite. Bien que la mortalité post-opératoire soit souvent relativement faible, la morbidité de ces interventions reste néanmoins significative [46]. Quand une résection complète peut être obtenue pour les tumeurs T4, des survies à 5 ans de 25 % peuvent être atteintes. L absence d atteinte ganglionnaire et le caractère complet de la résection sont les principaux facteurs pronostiques. De nouvelles approches telles que la voie trans-manubriale [47] et de nouvelles techniques (comme la vertébrectomie en bloc) rendent une résection complète possible dans 85 % des tumeurs T4 par envahissement du corps vertébral [46]. Dans la série de l institut Montsouris, la survie globale à 2 et 5 ans des tumeurs envahissant le corps vertébral était de 54 % et 25 % contre 73 % et 30 % après résection complète. Il est important de noter que 16 des 26 patients de cette série avaient reçu une induction par chimiothérapie. Plusieurs études ont montré, pour les tumeurs T4, la faisabilité d une radio-chimiothérapie d induction suivie d une résection chirurgicale. Stamatis et coll. [48] ont rapporté une série de 56 patients de stade IIIB traités par chimio-radiothérapie d induction. La moitié de ces patients était IIIB du fait d une tumeur T4. La réséquabilité était de 59 % et 27 patients (48 %) avaient une résection complète. La mortalité post-opératoire était de 2,9 % et la morbidité opératoire était de 50 %. Dans une étude japonaise récente [49], 27 patients de stade IIIB ont été traités par chimio-radiothérapie d induction. Vingt-deux patients avaient une atteinte clinique T4. Le taux de résection de cette série était de 81 %. La survie obtenue de 77 % à un an et 56 % à 3 ans est très prometteuse si on tient compte d une mortalité dans cette série de 4% pour un taux rapporté de complications de 36 %. Dans l étude Southwest oncology trial, d excellents résultats ont été rapportés pour la chimio-radiothérapie d induction pour des tumeurs de Pancoast [50]. Des patients avec des cancers non-à-petites cellules T3-4NO-1 de l apex pulmonaire ont été traités par deux cures de Cisplatine et Etoposide combinées à une irradiation de 45 grays. Le taux de résections complètes subséquentes était de 90,4 %. Chez 32 patients (36 %), une réponse pathologique complète a pu être constatée et il est important de noter que, chez 15 de ces patients, la tomographie computérisée ne suggérait aucune réponse tumorale. Après un suivi moyen de 3 ans, la survie globale de cette série est de 55 % et la survie à 3 ans après résection complète est de 70 %. Les rechutes surviennent principalement à distance, surtout au niveau cérébral. Ces résultats dépassent de loin ce qui a pu être obtenu par chirurgie primaire seule puisque dans la série historique du Memorial Sloan-Kettering Cancer Center, les taux de résection complète étaient de 64 % pour des tumeurs de Pancoast T3NO et 39 % pour les tumeurs T4N0. La survie actuarielle à 5 ans était de 46 % pour les T3N0 et 13 % pour les tumeurs T4N0 [51]. La littérature indique donc que la chimio-radiothérapie d induction semble être le traitement de choix pour les tumeurs de Pancoast T3-T4 N0-1. Dans des atteintes IIIB potentiellement réséquables également, la chimio-radiothérapie d induction suivie d une résection chirurgicale semble faisable [52]. 978
9 Le traitement chirurgical du cancer bronchique non à petites cellules Néanmoins, en l absence d études contrôlées prouvant une supériorité de schémas d induction associant la radiothérapie à la chimiothérapie par rapport à la chimio-induction seule, il nous semble que la lourdeur de ces schémas d induction impose actuellement leur utilisation à l intérieur de protocoles d études. Il est important de noter par ailleurs que même des patients ne montrant pas de réponse tomodensitométrique au traitement d induction méritent d être explorés chirurgicalement car la possibilité d une résection complète versus une nonréséquabilité ne peut pas toujours être prédite par les techniques d imagerie qui sont actuellement à notre disposition. Morbidité et mortalité après résection pulmonaire Malgré des progrès importants dans la mise au point préopératoire, l anesthésie, les techniques chirurgicales et les soins postopératoires, la chirurgie de résection pulmonaire reste grevée d une morbidité et mortalité opératoires. Cette morbidité dépend de l étendue de la résection pulmonaire, de la nécessité de résections associées comme la paroi thoracique ou la carène mais aussi de l âge et des comorbidités préexistantes du patient, telle que la présence ou non de bronchopneumopathie chronique obstructive [53]. Il est bien démontré que la pneumonectomie droite a une morbidité et mortalité plus importante qu une pneumonectomie gauche. Les causes exactes de cette différence restent méconnues mais sont sans doute liées au fait que le poumon droit est plus grand que le poumon gauche et que des résections complexes telles que les résections de la carène sont plus souvent réalisées du côté droit. Quand le moignon bronchique de pneumonectomie gauche est coupé court, il se rétracte vers le médiastin où il est entouré de tissus bien vascularisés. Ceci peut contribuer à expliquer que les fistules bronchopleurales surviennent plus rarement à gauche qu à droite. D autres facteurs influencent les résultats chirurgicaux. Ainsi, il n y a aucun doute que les interventions chirurgicales réalisées après thérapie «néo-adjuvante» comportent plus de défis techniques pour le chirurgien thoracique et requièrent une surveillance post-opératoire plus attentionnée. Après traitement d induction, des mortalités opératoires de 0 à 17 % après chimiothérapie seule et 4 à 15 % après chimioradiothérapie ont été rapportées [52]. Martin et coll. [54] ont rapporté l expérience du Memorial Sloan Kettering Cancer Center de 394 résections après traitement d induction dont une radiothérapie dans 18 % des cas. La mortalité globale de la série était de 4,6 %. Elle était de 2,4 % après lobectomie et atteignait 11,3 % après pneumonectomie. Les pneumonectomies droites après traitement d induction avaient une mortalité particulièrement élevée dans cette série (23,9 %). D autres auteurs ont confirmé une morbidité opératoire augmentée, surtout en cas d induction par chimioradiothérapie alors que certains centres n ont à l inverse pas trouvé d augmentation de la mortalité [52]. Ces résultats sont par ailleurs influencés par l expérience de chaque centre. La littérature démontre bien que les hôpitaux ayant un grand volume annuel de résections pulmonaires ont de meilleurs résultats que les hôpitaux à faible volume. Une étude aux États-Unis a classé les hôpitaux selon leur volume d activité croissant, depuis un faible volume (moins de 9 résections/an pour cancer bronchique) jusqu à un grand volume (plus de 67 résections/an). Les patients des hôpitaux à grand volume d activité avaient moins de complications postopératoires (20 % contre 44 %) et une moindre mortalité à 30 jours (3 % contre 6 %) que ceux des hôpitaux à faible volume d activité [55]. Birkmeyer et coll. [56] ont montré dans une autre étude que les différences absolues en taux de mortalité ajustés entre des hôpitaux à très faible volume et des hôpitaux à très fort volume d activité sont au-delà de 5 % pour une pneumonectomie et 2 % pour une lobectomie. Rôle du traitement adjuvant après résection complète Puisque même après une résection d apparence complète la survie à 5 ans des patients n est que d environ 40 %, des traitements adjuvants par radiothérapie et chimiotérapie ont été proposés. Dans la méta-analyse PORT [57], les données de patients issus de 9 études randomisées ont été analysées. Le rôle de la radiothérapie post-opératoire après une résection chirurgicale complète du cancer bronchique non-à petites cellules a été étudié. Une réduction globale de survie de 55 % à 48 % à 2 ans a été observée et l effet défavorable de la radiothérapie adjuvante prédominait pour les patients aux stades I et II. Le bénéfice d une chimiothérapie adjuvante a été démontré pour plusieurs types de cancer tels que le cancer mammaire, les cancers de l ovaire ou du colon. Pour le cancer bronchique, une méta-analyse publiée en 1995 [58] suggère qu une chimiothérapie adjuvante à base de dérivés du platine est associée à un gain de survie absolu de 5 % à 5 ans. Plusieurs groupes ont entrepris des études prospectives randomisées pour tester cette hypothèse. Dans une étude multicentrique italienne, patients avec des cancers non à petites cellules de stades I, II et IIIA étaient tirés au sort entre une chimiothérapie à base de Mitomycine, Vindésine et Cisplatine (MVP), toutes les 3 semaines (n = 606) ou l absence de traitement adjuvant après une résection chirurgicale complète de leur cancer (groupe contrôle n = 603). Aucune différence statistiquement significative de survie n était trouvée entre ces deux groupes. Cependant la toxicité de ce traitement était telle que seuls 69 % des patients avaient reçu les 3 cycles complets de MVP [59]. Une étude nord-américaine de l Intergroup a enrôlé 488 patients afin de comparer la radiothérapie adjuvante postopératoire seule avec la radiothérapie concomitante d une chimiothérapie à base d Etoposide et de Cisplatine. Ils n ont trouvé aucune différence de survie globale [60] SPLF, tous droits réservés 979
10 P. De Leyn, G. Decker L étude IALT [18] a randomisé patients après résection complète d un cancer bronchique non à petites cellules. 36,5 % avaient un stade I, 24,2 % un stade II et 33,9 % un stade III. La chimiothérapie consistait en du Cisplatine combiné à de l Etoposide (56 % des patients), de la Vinorelbine (27 % des patients), de la Vinblastine (11 % des patients) ou de la Vindésine dans 6 % des cas. Les patients recevant une chimiothérapie après une résection complète avaient une survie significativement plus longue que ceux qui n avaient pas reçu de chimiothérapie (44,5 % versus 40,4% à 5ans). Dans cette étude, le sous-groupe profitant le plus du traitment adjuvant était le stade IIIA, mais aucun sous-groupe ne bénéficiait pas de la chimiothérapie adjuvante par cisplatine. Les résultats de cette étude encouragent donc fortement l administration de 3 ou 4 cycles de chimiothérapie à base de Cisplatine à tout patient ayant eu une résection complète de son cancer bronchique non à petites cellules. Conclusions La résection chirurgicale reste le traitement de choix du cancer bronchique non à petites cellules de stades précoces. Une résection complète implique une résection anatomique (lobectomie ou pneumonectomie) et une dissection ganglionnaire systématique. Pour nombre de tumeurs centrales ou tumeurs avec ganglions N1 fixés, une lobectomie avec bronchoplastie est préférable à une pneumonectomie. Pour de petites lésions périphériques sans atteinte ganglionnaire au PET-scan et/ou une médiastinoscopie négative, une lobectomie thoracoscopique permet d obtenir une survie similaire à celle observée après chirurgie ouverte. Cependant, les avantages potentiels de la thoracoscopie pour le patient attendent toujours d être confirmés par des essais contrôlés randomisés. La résection primaire du cancer bronchique avec atteinte N2 est peu profitable pour le patient. Dans ce cas, une chimiothérapie d induction suivie d une résection en cas de réponse est devenue le traitement de choix. Seuls les patients dont l atteinte médiastinale a disparu sous l effet de l induction profitent réellement de cette chirurgie. Cependant, la réévaluation clinique de la réponse au traitement d induction par PET scan, CT scan et/ou re-médiastinoscopie reste trop imprécise. Pour les tumeurs de Pancoast et d autres T4 sélectionnés, un traitement d induction par chimio-radiothérapie suivi de résection chirurgicale améliore les taux de réséquabilité et de survie globale. La réponse au traitement comme la réséquabilité ne peuvent toujours pas être prédites par le CT-scan ou la résonance magnétique nucléaire. Pour ces raisons,tous les patients avec atteinte T4, stables ou répondeurs après chimio-radiothérapie d induction, devraient être explorés chirurgicalement. La chirurgie après traitement d induction est plus difficile et requiert une prise en charge post-opératoire attentive. Grâce à des techniques chirurgicales et post-opératoires méticuleuses, la mortalité et morbidité peuvent rester acceptables. La chimiothérapie néo-adjuvante comme la chimiothérapie adjuvante semblent améliorer le pronostic des cancers bronchiques de stades précoces. Les résultats d études randomisées en cours devront confirmer cela avant de pouvoir intégrer ces approches dans une pratique clinique journalière. Références 1 Ginsberg RJ, Rubinstein LV : Randomized trial of lobectomy versus limited resection for T1N0 non-small cell lung cancer. Ann Thorac Surg 1995 ; 60 : Landreneau RJ, Sugarbaker DJ, Mack MJ, Hazelrigg SR, Luketich JD, Fetterman L, Liptay MJ, Bartley S, Boley TM, Keenan RJ, Ferson PF, Weyant RJ, Naunheim KS : Wedge resection versus lobectomy for stage I (T1N0M0) non-small cell lung cancer. J Thorac Cardiovasc Surg 1997 ; 113 : Kodama K, Doi O, Higashiyama M, Yokouchi H : Intentional limited resection for selected patients with T1N0M0 non-small cell lung cancer: a single institution study. J Thorac Cardiovasc Surg 1997 ; 114 : De Leyn P, Rots W, Deneffe G, Nafteux P, Coosemans W, Van Raemdonck D, Decker G, Lerut T : Sleeve lobectomy for nonsmall cell lung cancer. Acta Chir Belg 2003 ; 103 : Rendina EA, Venuta F, De Giacomo T, Rossi M, Coloni GF : Parenchymal sparing operations for bronchogenic carcinoma. Surg Clin N Am 2002 ; 82 : Tronc F, Grégoire J, Rouleau J, Deslauriers J : Long-term results of sleeve lobectomy for lung cancer. Eur J Cardiothorac Surg 2000 ; 17 : Van Schil PE, Vankeirsbilck J, Brutel de la Riviere A, Van den Bosch JM : Long term survival after bronchial sleeve resection in relation to nodal involvement. Eur J Cardiothorac Surg 2000 ; 17 : Okada M, Yamagashi H, Satake S, Matsuoka H, Miyamoto Y, Yoshimura M, Tsubota N : Survival related to lymph node involvement in lung cancer after sleeve lobectomy compared with pneumonectomy. J Thorac Cardiovasc Surg 2000 ; 119 : Scott WJ, Howington J, Movsas B : Treatment of stage II non-small cell lung cancer. Chest 2003 ; 128 : 188S-201S. 10 Mitchell JD, Mathisen DJ, Wright CD, Wain JC, Donahue DM, Moncure AC,Grillo HC : Clinical experience with carinal resection. J Thorac Cardiovasc Surg 1999 ; 117 : Tsang GM, Watson DC : The practice of cardiothoracic surgeons in the perioperative staging of non-small cell lung cancer. Thorax 1992 ; 47 : De Leyn P, Schoonooghe P, Deneffe G, Van Raemdonck D, Coosemans W, Vansteenkiste J, Lerut T : Surgery for non-small cell lung cancer with unsuspected metastasis to ipsilateral mediastinal or subcarinal nodes (N2 disease). Eur J Cardiothorac Surg 1996 ; 10 : Fernando HC, Goldstraw P : The accurry of clinical evaluative intrathoracic staging as assessed by postsurgical pathological stage. Cancer 1990 ; 65 : Yoshino I, Yokoyama H, Yano T, Ueda T, Takai E, Mizutani K, Asoh H, Ichinose Y : Skip metastasis to the mediastinal lymph nodes in nonsmall cell lung cancer. Ann Thorac Surg 1996 ; 62 :
11 Le traitement chirurgical du cancer bronchique non à petites cellules 15 Riquet M, Hidden G, Debesse B : Direct lymphatic drainage of lung segments to the mediastinal nodes. J Thorac Cardiovasc Surg 1989 ; 97 : Watanabe S, Ladas G, Goldstraw P : Inter-observer variability in systematic nodal dissection: comparison of European and Japanese nodal designation. Ann Thorac Surg 2002 ; 73 : Naruke T, Tsuchiya R, Kondo H, Nakayama H, Asamura H : Lymph node sampling in lung cancer. How should it be done? Eur J Cardiothorac Surg 1999 ; 16 : The International Adjuvant Lung Cancer Trial Collaborative Group : Cisplatin-based adjuvant chemotherapy in patients with completely resected non-small cell lung cancer. N Engl J Med 2004 ; 350 : Izbicki JR, Passlick B, Pantel K, Pichlmeier U, Hosch SB, Karg O, Thetter O : Effectiveness of radical systematic mediastinal lymphadenectomy in patients with resectable non-small cell lung cancer. Ann Surg 1999 ; 227 : Keller SM, Adak S, Wagner H, Johnson DH for the eastern cooperative oncology group : Mediastinal lymph node dissection improves survival in patients with stages II and IIIa non-small cell lung cancer. Ann Thorac Surg 2000 ; 70 : Goldstraw P : Report on the international workshop on intrathoracic staging. London, October Lung Cancer 1997 ; 18 : Graham ANJ, Chan K, Pastorino U, Goldstraw P : Systematic nodal dissection in the intrathoracic staging of patients with non-small cell lung cancer. J Thorac Cardiovasc Surg 1999 ; 117 : Bollen ECM, Van Duin CJ, Theunissen PHMH, Van t Hof-Grootenboer AE, Blijham GH : Mediastinal lymph node dissection in resected lung cancer. Morbidity and accuracy of staging. Ann Thorac Surg 1993 ; 55 : Korst RJ, Ginsberg RJ : Appropriate surgical treatment of resectable non-small-cell lung cancer. World J Surg 2001 ; 25 : Asamura H, Nakayama H, Konde H, Tsuchiya R, Naruke T : Lobespecific extent of systematic lymph node dissection for non-small cell lung carcinoma according to a retrospective study of metastasis and prognosis. J Thorac Cardiovasc Surg 1999 ; 117 : Deslauriers J, Grégoire J, Jacques LF, Piraux M, Guojin L, lacasse Y : Sleeve lobectomy versus pneumonectomy for lung cancer: a comparative analysisof survival and sites of recurrences. Ann Thor Surg 2004 ; 77 : Vansteenkiste J, Stroobants S, Dupont P, De Leyn P, Verbeken E, Deneffe G, Mortelmans L, Demedts M : Prognostic importance of the standardized uptake value on F-deoxy-glucose-positron emission tomography scan in non-small-cell lung cancer: an analysis of 125 cases. J Clin Oncol 1999 ; 17 : Van Klaveren RJ, Festen J, Otten HJAM, Cox AL, De Graaf R, Lacquet LK : Prognosis of unsuspected but completely resectabe N2 non-small cell lung cancer. Ann Thorac Surg 1993 ; 56 : Kaseda S, Aoki T, Hangai N, Shimizu K : Better pulmonary function and prognosis with video-assisted thoracic surgery than with thoracotomy. Ann Thorac Surg 2000 ; 70 : Sugi K, Kaneda Y, Esato K : Video-assisted thoracoscopic lobectomy achieves a satisfactory long-term prognosis in patients with clinical satge IA lung cancer. World J Surg 2000 ; 24 : Walker WS, Codispoti M, Soon SY, Stamenkovic S, Carnochan F, Pugh G : Long-term outcomes following VATS lobectomy for nonsmall cell bronchogenic carcinoma. Eur J Cardiothorac Surg 2003 ; 23 : Gharagozloo F, Tempesta B, Margolis M : Video-assisted thoracic surgery for stage I lung cancer. Ann Thorac Surg 2003 ; 76 : Pearson FG, Delarue NC, Ilves R, Todd TRJ, Cooper JD : Significance of posterior superior mediastinal nodes identified at mediastinoscopy in patients with resectable cancer of the lung. J Thorac Cardiovasc Surg 1982 ; 83 : Funatsu T, Matsubara Y, Hatakenaka R, Kosaba S, Yasuda Y, Ikeda S : The role of mediastinoscopic biopsy in preoperative assessment of lung cancer. J Thorac Cardiovasc Surg 1992 ; 104 : Rusch VW : Surgery for stage III non-small cell lung cancer. Cancer control 1994 ; 1 : Rosell R, Gomez-Codina J, Camps C, Javier Sanchez J, Maeste J, Padilla J, Canto A, Abad A, Roig J : Preresectional chemotherapy in stage IIIA non-small cell lung cancer. Lung Cancer 1999 ; 26 : Rosell R, Gomez-Codina J, Camps C, Maestre J, Padille J, Canto A, Mate JL, Li S, Roig J, Olazabal A et al. : A randomized trial comparing preoperative chemotherapy plus surgery with surgery alone in patients with non-small cell lung cancer. N Engl J Med 1994 ; 330 : Roth JA, Atkinson EN, Fosella F, Komaki R, Bernadette Ryan M, Putnam JB Jr, Lee JS, Dhingra H, De Caro L, Chasen M, Hong WK : Long-term follow-up of patients enrolled in a randomized trial comparing perioperative chemotherapy and surgery. Lung Cancer 1998 ; 21 : Roth JA, Fossella F, Komaki R, Ryan MB, Putnam JB Jr, Lee JS, Dhingra H, De Caro L, Chasen M, McGavran M et al. : A randomized trial comparing preoperative chemotherapy plus surgery with surgery alone in resectable stage IIIA non-small cell lung cancer. J Natl Cancer Inst 1994 ; 86 : Robinson LA, Wagner H, Ruckdeschel JC : Treatment of stage IIIA non-small cell lung cancer. Chest 2003 ;123 :202S-220S. 41 Depierre A, Milleron B, Moro-Sibilot D, Chevret S, Quoix E, Lebeau B, Braun D, Breton JL, Lemarie E, Gouva S, Paillot N, Brechot JM, Janicot H, Lebas FX, Terrioux P, Clavier J, Foucher P, Monchatre M, Coetmeur D, Level Mc, Leclerc P, Blanchon F, Rodier JM, Thiberville L, Villeneuve A, Westeel V, Chastang C; French Thoracic Cooperative Group : Preoperative chemotherapy followed by surgery compared with primary surgery in respectable stage I (except T1N0), II and IIIa non-small cell lung cancer. J Clin Oncol 2002 ; 20 : Bueno R, Richards WG, Swanson SJ, Jaklitsch MT, Lukanich JM, Mentzer SJ, Sugarbaker DJ : Nodal stage after induction therapy for stage IIIA lung cancer determines patient survival. Ann Thorac Surg 200; 70 : Cerfolio RJ, Ojha B, Mukherjee S, Pask AH, Bass CS, Katholi CR : Positron emission tomography scanning with 2-fluoro-2-deoxy-Dglucose as a predictor of response of neoadjuvant treatment for nonsmall cell carcinoma. J Thorac Cardiovasc Surg 2003 ; 125 : Van Schil P : The restaging issue. Lung Cancer 2003 ; 42 : S39-S Port JL, Kent MS, Korts RJ, Keresztes R, Levin MA, Altorki NK : Positron emission tomography scanning poorly predicts response to preoperative chemotherapy in Non-small cell lung cancer. Ann Thorac Surg 2004 ; 77 : Grunenwald DM : Surgery for locally advanced non-small cell lung cancer. Sem Surg Oncol 2003 ; 21 : Grunenwald D, Spaggiari L : Trans-manubrial osteo-muscular sparing approach for apical chest tumors. Ann Thorac Surg 1997 ; 63 : Stamatis G, Eberhardt W, Stüben G, Bildat S, Dahler O, Hillejan L : Preoperative chemoradiotherapy and surgery for selected non-small cell lung cancer IIIB subgroups: long-term results. Ann Thorac Surg 1999 ; 68 : Ichinose Y, Fukuyama Y, Asoh Hiroshi, Ushijima C, Okamoto T, Ikeda J, Okamoto J, Sakai M : Induction chemoradiotherapy and sur SPLF, tous droits réservés 981
12 P. De Leyn, G. Decker gical resection for selected stage IIIB non-small cell lung cancer. Ann Thorac Surg 2003 ; 76 : Rusch VW, Giroux DJ, Kraut MJ, Crowley J, Hazuka M, Johnson D, Goldberg M, Detterbeck F, Sheperd F, Burkes R, Winton T, Deschamps C, Livingston R, Gandara D : Induction chemoradiation and surgical resection for non-small cell lung carcinomas of the superior sulcus: initial results of Southwest oncology group trial (intergroup trial 0160). J Thorac Cardiovasc Surg 2001 ; 121 : Rusch VW, Parekh KR, Leon L, Venkatram E, Bains MS, Downey RJ, Boland P, Bilsky M, Ginsberg RJ : Factors determining outcome after surgical resection of T3 and T4 lung cancers of the superior sulcus. J Thorac Cardiovasc Surg 2000 ; 119 : Eberhardt WE, Albain KS, Pass H, Putnam JB, Gregor A, Assamura H, Mornex F, Senan S, Belderbos J, Westeel V, Thomas M, Van Schil P, Vansteenkiste J, Manegold C, Mirimanoff RO, Stuschke M, Pignon J, Rocmans P, Shepherd FA : Induction treatment before surgery for nonsmall cell lung cancer. Lung cancer 2003 ; 42 : S9-S Ginsberg RJ : Lung cancer surgery: acceptable morbidity and mortality, expected results and quality control. Surg Oncol 2002 ; 11 : Martin J, Ginsberg RJ, Abolhoda A, Bains MS, Downey RJ, Korst RJ, Weigel TL, Kris MG, Venkatraman ES, Rusch VW : Morbidity and mortality after neoadjuvant therapy for lung cancer: the risks of right pneumonectomy. Ann Thorac Surg 2001 ; 72 : Bach PB, Cramer LD, Schrag D, Downey RJ, Gelfand SE, Begg CB : The influence of hospital volume on survival after resection for lung cancer. N Engl J Med 2001 ; 345 : Birkmeyer JD, Siewers AE, Finlayson EVA, Stukel TA, Lucas FL, Batista I, Welch H, Wennberg DE : Hospital volume and surgical mortality in the Unites States. N Engl J Med 2002 ; 346 : PORT meta-analysis trialists group : Postoperative radiotherapy in non-small cell lung cancer: systematic review and meta-analysis of individual patient data from nine randomised controlled trials. Lancet 1998 ; 352 : Non-small cell lung cancer collaborative group : Chemotherapy in non-small cell lung cancer: a meta-analysis using updated data on individual patients from 52 randomised clinical trials. BMJ 1995 ; 311 : Scagliotti GV, Fossati R, Torri V, Crino L, Giacconer G, Silvano G, Martelli M, Clerici M, Cognetti F, Tonato M for the Adjuvant Lung Project Italy/European organisation for research treatment of cancer- Lung cancer cooperative group investigators : Randomized study of adjuvant chemotherapy for completely resected Stage I, II, or IIA non-small cell lung cancer. J Natl Cancer Inst 2003 ; 95 : Keller SM, Adak S, Wagner H, Herskovic A, Komaki R, Brooks BJ, Perry MC, Livingston RB, Johnson DH for the Eastern Cooperative oncology Group : N Engl J Med 2000 ; 343 :
La nouvelle classification TNM en pratique
 La nouvelle classification TNM en pratique Thierry Berghmans Département des Soins Intensifs et Oncologie Thoracique Institut Jules Bordet Bruxelles, Belgique Bases historiques 1946 : Denoix invente le
La nouvelle classification TNM en pratique Thierry Berghmans Département des Soins Intensifs et Oncologie Thoracique Institut Jules Bordet Bruxelles, Belgique Bases historiques 1946 : Denoix invente le
Actualités s cancérologiques : pneumologie
 Actualités s cancérologiques : pneumologie PLAN Incidence / facteurs de risque Anatomie Symptômes Types de tumeurs Diagnostic / extension Classification Traitement Pronostic Pneumologie : incidence Belgique
Actualités s cancérologiques : pneumologie PLAN Incidence / facteurs de risque Anatomie Symptômes Types de tumeurs Diagnostic / extension Classification Traitement Pronostic Pneumologie : incidence Belgique
Prise en charge des carcinomes bronchiques selon le stade: le point de vue du chirurgien 1
 Schweiz Med Wochenschr 2000;130:679 83 A. Spiliopoulos, M. de Perrot Unité de thoracique, Département de, Hôpitaux Universitaires de Genève Prise en charge des carcinomes bronchiques selon le stade: le
Schweiz Med Wochenschr 2000;130:679 83 A. Spiliopoulos, M. de Perrot Unité de thoracique, Département de, Hôpitaux Universitaires de Genève Prise en charge des carcinomes bronchiques selon le stade: le
Pascal Thomas, pour la Société Française de Chirurgie Thoracique et Cardio-Vasculaire.
 e-mémoires de l'académie Nationale de Chirurgie, 2009, 8 (1) : 36-40 36 Recommandations de la Société Française de Chirurgie Thoracique et Cardio-Vasculaire de pratiques chirurgicales dans le traitement
e-mémoires de l'académie Nationale de Chirurgie, 2009, 8 (1) : 36-40 36 Recommandations de la Société Française de Chirurgie Thoracique et Cardio-Vasculaire de pratiques chirurgicales dans le traitement
PLACE DE L IRM DANS LE BILAN D EXTENSION DU CANCER DU RECTUM. Professeur Paul LEGMANN Radiologie A - Cochin Paris
 PLACE DE L IRM DANS LE BILAN D EXTENSION DU CANCER DU RECTUM Professeur Paul LEGMANN Radiologie A - Cochin Paris Cancer du rectum France : 15000 décès/an : 1ère cause. Pronostic souvent réservé Métastases
PLACE DE L IRM DANS LE BILAN D EXTENSION DU CANCER DU RECTUM Professeur Paul LEGMANN Radiologie A - Cochin Paris Cancer du rectum France : 15000 décès/an : 1ère cause. Pronostic souvent réservé Métastases
Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA. Doctorant: Camelia MICU (DEMETRIAN)
 UNIVERSITÉ DE MÉDECINE ET PHARMACIE DE CRAIOVA FACULTÉ DE MÉDECINE CONTRIBUTIONS A L'ÉTUDE CLINIQUE ET MORPHOLOGIQUE DES CANCERS DU POUMON Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA Doctorant:
UNIVERSITÉ DE MÉDECINE ET PHARMACIE DE CRAIOVA FACULTÉ DE MÉDECINE CONTRIBUTIONS A L'ÉTUDE CLINIQUE ET MORPHOLOGIQUE DES CANCERS DU POUMON Coordinateur scientifique: Prof. Univ. Dr. Emil PLEŞEA Doctorant:
RÉSUMÉ ABSTRACT. chirurgie thoracique
 Évolution de la prise en charge chirurgicale des cancers pulmonaires en France : lobectomie mini-invasive versus lobectomie par thoracotomie d après la base de données nationale Epithor Sophie Guinard,
Évolution de la prise en charge chirurgicale des cancers pulmonaires en France : lobectomie mini-invasive versus lobectomie par thoracotomie d après la base de données nationale Epithor Sophie Guinard,
Les différents types de cancers et leurs stades. Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07
 Les différents types de cancers et leurs stades Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07 CARCINOGENESE multiple steps, accumulation d altd altérations continuum lésionnel
Les différents types de cancers et leurs stades Dr Richard V Oncologie MédicaleM RHMS Baudour et Erasme La Hulpe 1/12/07 CARCINOGENESE multiple steps, accumulation d altd altérations continuum lésionnel
Lobectomie pulmonaire vidéo-assistée : technique, indications et résultats
 J Fran Viet Pneu 2012; 03(08): 1-65 2012 JFVP. All rights reserved. www.afvp.info JOURNAL FRANCO-VIETNAMIEN DE PNEUMOLOGIE Journal of French-Vietnamese Association of Pulmonology ARTICLE ORIGINAL Lobectomie
J Fran Viet Pneu 2012; 03(08): 1-65 2012 JFVP. All rights reserved. www.afvp.info JOURNAL FRANCO-VIETNAMIEN DE PNEUMOLOGIE Journal of French-Vietnamese Association of Pulmonology ARTICLE ORIGINAL Lobectomie
Traitements néoadjuvants des cancers du rectum. Pr. G. Portier CHU Purpan - Toulouse
 Traitements néoadjuvants des cancers du rectum Pr. G. Portier CHU Purpan - Toulouse Journées Francophones d Hépato-gastroentérologie et d Oncologie Digestive 2010 CONFLITS D INTÉRÊT Pas de conflit d intérêt
Traitements néoadjuvants des cancers du rectum Pr. G. Portier CHU Purpan - Toulouse Journées Francophones d Hépato-gastroentérologie et d Oncologie Digestive 2010 CONFLITS D INTÉRÊT Pas de conflit d intérêt
Classi cation TNM du cancer bronchique
 Revue des Maladies Respiratoires Actualités (2014) 6, 388-394 Disponible en ligne sur www.sciencedirect.com Classi cation TNM du cancer bronchique TNM classi cation for the lung cancer J.-P. Sculier Service
Revue des Maladies Respiratoires Actualités (2014) 6, 388-394 Disponible en ligne sur www.sciencedirect.com Classi cation TNM du cancer bronchique TNM classi cation for the lung cancer J.-P. Sculier Service
De la chirurgie du nodule aux ganglions
 De la chirurgie du nodule aux ganglions Docteur Xavier CARRAT Institut Bergonié Clinique Saint Augustin Chirurgie des lésions bénignes de la thyroïde problématique opératoire «simple» avec indication portée
De la chirurgie du nodule aux ganglions Docteur Xavier CARRAT Institut Bergonié Clinique Saint Augustin Chirurgie des lésions bénignes de la thyroïde problématique opératoire «simple» avec indication portée
Cancers de l hypopharynx
 Cancers de l hypopharynx A- GENERALITES 1) Epidémiologie Cancer fréquent et de pronostic grave du fait de son évolution insidieuse et de son caractère lymphophile. C est quasiment toujours un carcinome
Cancers de l hypopharynx A- GENERALITES 1) Epidémiologie Cancer fréquent et de pronostic grave du fait de son évolution insidieuse et de son caractère lymphophile. C est quasiment toujours un carcinome
Recommandations 2005. Prise en charge des patients adultes atteints d un mélanome cutané MO
 Recommandations 2005 Prise en charge des patients adultes atteints d un mélanome cutané MO Recommandations pour la Pratique Clinique : Standards, Options et Recommandations 2005 pour la prise en charge
Recommandations 2005 Prise en charge des patients adultes atteints d un mélanome cutané MO Recommandations pour la Pratique Clinique : Standards, Options et Recommandations 2005 pour la prise en charge
Recommandations régionales Prise en charge des carcinomes cutanés
 Recommandations régionales Prise en charge des carcinomes cutanés - décembre 2009 - CARCINOMES BASOCELLULAIRES La chirurgie : traitement de référence et de 1 ère intention Classification clinique et histologique
Recommandations régionales Prise en charge des carcinomes cutanés - décembre 2009 - CARCINOMES BASOCELLULAIRES La chirurgie : traitement de référence et de 1 ère intention Classification clinique et histologique
Qu est-ce qu un sarcome?
 Qu est-ce qu un sarcome? Qu est-ce qu une tumeur? Une tumeur est une prolifération anormale de cellules. Les tumeurs ne devraient donc pas automatiquement être associées à un cancer. Certaines tumeurs
Qu est-ce qu un sarcome? Qu est-ce qu une tumeur? Une tumeur est une prolifération anormale de cellules. Les tumeurs ne devraient donc pas automatiquement être associées à un cancer. Certaines tumeurs
Item 169 : Évaluation thérapeutique et niveau de preuve
 Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
Item 169 : Évaluation thérapeutique et niveau de preuve COFER, Collège Français des Enseignants en Rhumatologie Date de création du document 2010-2011 Table des matières ENC :...3 SPECIFIQUE :...3 I Différentes
INTERFERON Traitement adjuvant du mélanome à haut risque de récidive. Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper
 INTERFERON Traitement adjuvant du mélanome à haut risque de récidive Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper Pourquoi proposer un TTT adjuvant? Probabilité de survie à 10 ans en fonction
INTERFERON Traitement adjuvant du mélanome à haut risque de récidive Dr Ingrid KUPFER-BESSAGUET Dermatologue CH de quimper Pourquoi proposer un TTT adjuvant? Probabilité de survie à 10 ans en fonction
NAVELBINE voie orale
 DENOMINATION DU MEDICAMENT & FORME PHARMACEUTIQUE NAVELBINE voie orale CARACTERISTIQUES Dénomination commune : vinorelbine Composition qualitative et quantitative : Statut : A.M.M. A.T.U. Classe ATC :
DENOMINATION DU MEDICAMENT & FORME PHARMACEUTIQUE NAVELBINE voie orale CARACTERISTIQUES Dénomination commune : vinorelbine Composition qualitative et quantitative : Statut : A.M.M. A.T.U. Classe ATC :
Pierre OLIVIER - Médecine Nucléaire
 Diplôme Universitaire Corrélations anatomo-physio-pathologiques en imagerie thoracique 25 mai 2011 Imagerie TEP et pathologie tumorale bronchique Pierre OLIVIER - Médecine Nucléaire Détection en coincidence
Diplôme Universitaire Corrélations anatomo-physio-pathologiques en imagerie thoracique 25 mai 2011 Imagerie TEP et pathologie tumorale bronchique Pierre OLIVIER - Médecine Nucléaire Détection en coincidence
Métastase unique d un NPC: Une question singulière? Jean Louis Pujol - Xavier Quantin Mohammad Chakra Fabrice Barlési
 Métastase unique d un NPC: Une question singulière? Jean Louis Pujol - Xavier Quantin Mohammad Chakra Fabrice Barlési Deux grandes questions Cette modalité de présentation, requiert elle une prise en charge
Métastase unique d un NPC: Une question singulière? Jean Louis Pujol - Xavier Quantin Mohammad Chakra Fabrice Barlési Deux grandes questions Cette modalité de présentation, requiert elle une prise en charge
IRM du Cancer du Rectum
 IRM du Cancer du Rectum quels CHOIX TECHNIQUES pour quels OBJECTIFS THERAPEUTIQUES? Frank Boudghène, T. Andre, A. Stivalet, I. Frey, L. Paslaru, V. Ganthier, M. Tassart Hopital Tenon - Université Paris
IRM du Cancer du Rectum quels CHOIX TECHNIQUES pour quels OBJECTIFS THERAPEUTIQUES? Frank Boudghène, T. Andre, A. Stivalet, I. Frey, L. Paslaru, V. Ganthier, M. Tassart Hopital Tenon - Université Paris
Le cancer du poumon 2/18/2015. Radio-oncologue CSSS Gatineau. Stéphanie Ferland B.pharm, MD, MSc, FRCPC
 Objectifs Le cancer du poumon Stéphanie Ferland B.pharm, MD, MSc, FRCPC Radio-oncologue CSSS Gatineau Décrire le rôle de la thérapie générale en ce qui concerne les traitements néoadjuvants, adjuvants
Objectifs Le cancer du poumon Stéphanie Ferland B.pharm, MD, MSc, FRCPC Radio-oncologue CSSS Gatineau Décrire le rôle de la thérapie générale en ce qui concerne les traitements néoadjuvants, adjuvants
Dr Bertrand Michy Département de Pneumologie CHU de Nancy 25 octobre 2013
 Dr Bertrand Michy Département de Pneumologie CHU de Nancy 25 octobre 2013 Conflits d intérêts Aucun Introduction Constat : CB = Moins de motivation des pneumologues à obtenir le sevrage tabagique (versus
Dr Bertrand Michy Département de Pneumologie CHU de Nancy 25 octobre 2013 Conflits d intérêts Aucun Introduction Constat : CB = Moins de motivation des pneumologues à obtenir le sevrage tabagique (versus
Maladie de Hodgkin ou lymphome de Hodgkin
 Maladie de Hodgkin ou lymphome de Hodgkin Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca MALADIE DE HODGKIN Ce que vous devez savoir Même si vous entendez parler du
Maladie de Hodgkin ou lymphome de Hodgkin Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca MALADIE DE HODGKIN Ce que vous devez savoir Même si vous entendez parler du
Patho Med Cours 5. Maladie Pulmonaires Obstructives BPCO Asthme
 Patho Med Cours 5 Maladie Pulmonaires Obstructives BPCO Asthme BPCO: B: Broncho ( Bronche) P: Pneumopathie C: Chronique O: Obstructive Asthme Maladies avec des spasmes bronchiques Maladies avec des spasmes
Patho Med Cours 5 Maladie Pulmonaires Obstructives BPCO Asthme BPCO: B: Broncho ( Bronche) P: Pneumopathie C: Chronique O: Obstructive Asthme Maladies avec des spasmes bronchiques Maladies avec des spasmes
Sujets présentés par le Professeur Olivier CUSSENOT
 ANAMACaP Association Nationale des Malades du Cancer de la Prostate 17, bis Avenue Poincaré. 57400 SARREBOURG Sujets présentés par le Professeur Olivier CUSSENOT Place des nouvelles techniques d imagerie
ANAMACaP Association Nationale des Malades du Cancer de la Prostate 17, bis Avenue Poincaré. 57400 SARREBOURG Sujets présentés par le Professeur Olivier CUSSENOT Place des nouvelles techniques d imagerie
Pemetrexed, pionnier de la chimiothérapie histoguidée. Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var
 Pemetrexed, pionnier de la chimiothérapie histoguidée Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var SFPO Octobre 2009 EPIDEMIOLOGIE Incidence : 1.35 M par an dans le monde (12,4%) 28 000
Pemetrexed, pionnier de la chimiothérapie histoguidée Dr Olivier CASTELNAU Institut Arnault TZANCK ST Laurent du Var SFPO Octobre 2009 EPIDEMIOLOGIE Incidence : 1.35 M par an dans le monde (12,4%) 28 000
Le cancer dans le canton de Fribourg
 Le cancer dans le canton de Fribourg Le cancer du poumon dans le canton de Fribourg, analyses statistiques réalisées sur la base des données récoltées par le Registre fribourgeois des tumeurs depuis début
Le cancer dans le canton de Fribourg Le cancer du poumon dans le canton de Fribourg, analyses statistiques réalisées sur la base des données récoltées par le Registre fribourgeois des tumeurs depuis début
Cancers du larynx : diagnostic, principes de traitement (145a) Professeur Emile REYT Novembre 2003 (Mise à jour Mars 2005)
 Cancers du larynx : diagnostic, principes de traitement (145a) Professeur Emile REYT Novembre 2003 (Mise à jour Mars 2005) Pré-Requis : Anatomie du larynx Physiologie de la phonation et de la déglutition
Cancers du larynx : diagnostic, principes de traitement (145a) Professeur Emile REYT Novembre 2003 (Mise à jour Mars 2005) Pré-Requis : Anatomie du larynx Physiologie de la phonation et de la déglutition
VOLUMES-CIBLES Cancer Bronchique Non-à-Petites Cellules
 VOLUMES-CIBLES Cancer Bronchique Non-à-Petites Cellules Philippe GIRAUD, Nicolas POUREL, Vincent SERVOIS Romainville, le 29 septembre 2011 1 Radiothérapie et cancer du poumon La dosimétrie des cancers
VOLUMES-CIBLES Cancer Bronchique Non-à-Petites Cellules Philippe GIRAUD, Nicolas POUREL, Vincent SERVOIS Romainville, le 29 septembre 2011 1 Radiothérapie et cancer du poumon La dosimétrie des cancers
Chirurgie assistée par robot et laparoscopie en 3D à l avantage des patients?
 HigHligHts 2012: CHiRURgiE Chirurgie assistée par robot et laparoscopie en 3D à l avantage des patients? Lukasz Filip Grochola a, Hubert John b, Thomas Hess c, Stefan Breitenstein d a Clinique de chirurgie
HigHligHts 2012: CHiRURgiE Chirurgie assistée par robot et laparoscopie en 3D à l avantage des patients? Lukasz Filip Grochola a, Hubert John b, Thomas Hess c, Stefan Breitenstein d a Clinique de chirurgie
Transplantation hépatique à donneur vivant apparenté. Olivier Scatton, Olivier Soubrane, Service de chirurgie Cochin
 Transplantation hépatique à donneur vivant apparenté Olivier Scatton, Olivier Soubrane, Service de chirurgie Cochin Introduction Le prélèvement d une partie du foie chez une personne «vivante» et apparentée
Transplantation hépatique à donneur vivant apparenté Olivier Scatton, Olivier Soubrane, Service de chirurgie Cochin Introduction Le prélèvement d une partie du foie chez une personne «vivante» et apparentée
INVESTIGATEUR PRINCIPAL. Pr Alain DEPIERRE. COORDINATION IFCT Franck MORIN. PROMOTEUR C.H.U Besançon
 Essai thérapeutique randomisé comparant deux schémas de chimiothérapie préopératoire dans les cancers bronchiques non à petites cellules (CBNPC) de stades cliniques I et II. PROTOCOLE IFCT-0002 INVESTIGATEUR
Essai thérapeutique randomisé comparant deux schémas de chimiothérapie préopératoire dans les cancers bronchiques non à petites cellules (CBNPC) de stades cliniques I et II. PROTOCOLE IFCT-0002 INVESTIGATEUR
Rapport sur les nouveaux médicaments brevetés Iressa
 Rapport sur les nouveaux médicaments brevetés Iressa Au titre de son initiative de transparence, le CEPMB publie les résultats des examens des prix des nouveaux médicaments brevetés effectués par les membres
Rapport sur les nouveaux médicaments brevetés Iressa Au titre de son initiative de transparence, le CEPMB publie les résultats des examens des prix des nouveaux médicaments brevetés effectués par les membres
CHIMIOTHERAPIE DES CANCERS DU POUMON DES SUJETS AGES
 CHIMIOTHERAPIE DES CANCERS DU POUMON DES SUJETS AGES 1 EPIDEMIOLOGIE 28 000 nouveaux cas/an 4ème rang des cancers Sex ratio 6,1 Mortalité > 27 000/an Âge médian H 67 ans, F 68 ans 2 1 Taux annuel ajusté
CHIMIOTHERAPIE DES CANCERS DU POUMON DES SUJETS AGES 1 EPIDEMIOLOGIE 28 000 nouveaux cas/an 4ème rang des cancers Sex ratio 6,1 Mortalité > 27 000/an Âge médian H 67 ans, F 68 ans 2 1 Taux annuel ajusté
Radiologie Interven/onnelle sur les nodules pulmonaires. J. Palussière, X. Buy Département imagerie
 Radiologie Interven/onnelle sur les nodules pulmonaires J. Palussière, X. Buy Département imagerie Radiofréquence Interac*on courant électro- magné*que ma*ère agita*on ionique chaleur Coagula*on Nécrose
Radiologie Interven/onnelle sur les nodules pulmonaires J. Palussière, X. Buy Département imagerie Radiofréquence Interac*on courant électro- magné*que ma*ère agita*on ionique chaleur Coagula*on Nécrose
Bonnes pratiques chirurgicales
 dans le traitement du cancer bronchique primitif non à petites cellules. Données factuelles : texte de synthèse élaboré par la Société Française de Chirurgie Thoracique et Cardio-Vasculaire Coordinateur
dans le traitement du cancer bronchique primitif non à petites cellules. Données factuelles : texte de synthèse élaboré par la Société Française de Chirurgie Thoracique et Cardio-Vasculaire Coordinateur
RETOUR AU DOMICILE DES OPERES DU THORAX
 Marcelcave, le 10 février 2009 RETOUR AU DOMICILE DES OPERES DU THORA Drs Marie-Claude LELEU et Pierre DUPONT 1 PRE TEST Vrai Faux Les complications chirurgicales après chirurgie thoracique sont fréquentes.
Marcelcave, le 10 février 2009 RETOUR AU DOMICILE DES OPERES DU THORA Drs Marie-Claude LELEU et Pierre DUPONT 1 PRE TEST Vrai Faux Les complications chirurgicales après chirurgie thoracique sont fréquentes.
Essai Inter-groupe : FFCD UNICANCER FRENCH - GERCOR
 CLIMAT - PRODIGE 30 Etude de phase III randomisée évaluant l Intérêt de la colectomie première chez les patients porteurs d un cancer colique asymptomatique avec métastases hépatiques synchrones non résécables
CLIMAT - PRODIGE 30 Etude de phase III randomisée évaluant l Intérêt de la colectomie première chez les patients porteurs d un cancer colique asymptomatique avec métastases hépatiques synchrones non résécables
COMMISSION DE LA TRANSPARENCE AVIS. 4 novembre 2009
 COMMISSION DE LA TRANSPARENCE AVIS 4 novembre 2009 IRESSA 250 mg, comprimé pelliculé Boîte de 30 (CIP 395 950-7) ASTRAZENECA géfitinib Liste I Médicament soumis à prescription hospitalière. Prescription
COMMISSION DE LA TRANSPARENCE AVIS 4 novembre 2009 IRESSA 250 mg, comprimé pelliculé Boîte de 30 (CIP 395 950-7) ASTRAZENECA géfitinib Liste I Médicament soumis à prescription hospitalière. Prescription
Annick.robinson@merck.com dquirion@national.ca 514 428-2890 514 843-2302
 Communiqué de presse Relations avec les médias : Annick Robinson Dominique Quirion Merck NATIONAL Annick.robinson@merck.com dquirion@national.ca 514 428-2890 514 843-2302 Relations avec les investisseurs
Communiqué de presse Relations avec les médias : Annick Robinson Dominique Quirion Merck NATIONAL Annick.robinson@merck.com dquirion@national.ca 514 428-2890 514 843-2302 Relations avec les investisseurs
Validation clinique des marqueurs prédictifs le point de vue du méthodologiste. Michel Cucherat UMR CNRS 5558 - Lyon
 Validation clinique des marqueurs prédictifs le point de vue du méthodologiste Michel Cucherat UMR CNRS 5558 - Lyon Marqueur prédictif - Définition Un marqueur prédictif est un marqueur qui prédit le bénéfice
Validation clinique des marqueurs prédictifs le point de vue du méthodologiste Michel Cucherat UMR CNRS 5558 - Lyon Marqueur prédictif - Définition Un marqueur prédictif est un marqueur qui prédit le bénéfice
PROJET DE RECHERCHE. FSF 91 boulevard de Sébastopol 75002 Paris
 2015 PROJET DE RECHERCHE Apport de la fluorescence pour la détection des ganglions sentinelles dans les cancers du sein FLUO-BREAST Praticien Hospitalo-universitaire Chirurgie cancérologique gynécologique
2015 PROJET DE RECHERCHE Apport de la fluorescence pour la détection des ganglions sentinelles dans les cancers du sein FLUO-BREAST Praticien Hospitalo-universitaire Chirurgie cancérologique gynécologique
Revue de la littérature
 Résultats à long terme des anévrysmes traités Revue de la littérature Cours de DES de neurochirurgie Inter-région Rhône-Alpes / Auvergne Vendredi 22/04/11 Méthode (1): sélection bibliographique en fonction
Résultats à long terme des anévrysmes traités Revue de la littérature Cours de DES de neurochirurgie Inter-région Rhône-Alpes / Auvergne Vendredi 22/04/11 Méthode (1): sélection bibliographique en fonction
First Line and Maintenance in Nonsquamous NSCLC: What Do the Data Tell Us?
 Dr Jean-Charles Soria : Bonjour et bienvenue dans ce programme. Je suis Jean Charles Soria, Professeur de Médecine et Directeur du programme de développement précoce des médicaments à l université Paris
Dr Jean-Charles Soria : Bonjour et bienvenue dans ce programme. Je suis Jean Charles Soria, Professeur de Médecine et Directeur du programme de développement précoce des médicaments à l université Paris
Qui et quand opérer. au cours du traitement de l EI?
 Qui et quand opérer au cours du traitement de l EI? Gilbert Habib Département de Cardiologie - Timone Marseille 7es JNI Bordeaux, 8 juin 2006 Université de la Méditerranée Faculté de Médecine de Marseille
Qui et quand opérer au cours du traitement de l EI? Gilbert Habib Département de Cardiologie - Timone Marseille 7es JNI Bordeaux, 8 juin 2006 Université de la Méditerranée Faculté de Médecine de Marseille
Le donneur en vue d une transplantation pulmonaire
 Le donneur en vue d une transplantation pulmonaire Nicola Santelmo Chirurgie Thoracique Groupe de Transplantation Pulmonaire de Strasbourg Hôpitaux Universitaires de Strasbourg Coordinateur: Pr Gilbert
Le donneur en vue d une transplantation pulmonaire Nicola Santelmo Chirurgie Thoracique Groupe de Transplantation Pulmonaire de Strasbourg Hôpitaux Universitaires de Strasbourg Coordinateur: Pr Gilbert
Cancer du poumon chez le sujet âgé : traitement du carcinome bronchique non à petites cellules
 Cancer du poumon chez le sujet âgé : traitement du carcinome bronchique non à petites cellules M.-C. Pailler et J.-F. Morère Introduction Avec plus de 700 000 nouveaux cas annuels, le cancer bronchique
Cancer du poumon chez le sujet âgé : traitement du carcinome bronchique non à petites cellules M.-C. Pailler et J.-F. Morère Introduction Avec plus de 700 000 nouveaux cas annuels, le cancer bronchique
Evaluation de critères res de substitution de la survie globale dans les cancers bronchiques localement avancés
 Evaluation de critères res de substitution de la survie globale dans les cancers bronchiques localement avancés Evaluations de la survie sans progression et du contrôle locoregional comme critère de substitution
Evaluation de critères res de substitution de la survie globale dans les cancers bronchiques localement avancés Evaluations de la survie sans progression et du contrôle locoregional comme critère de substitution
ALK et cancers broncho-pulmonaires. Laurence Bigay-Gamé Unité d oncologie thoracique Hôpital Larrey, Toulouse
 ALK et cancers broncho-pulmonaires Laurence Bigay-Gamé Unité d oncologie thoracique Hôpital Larrey, Toulouse Toulouse, le 19 Février 2013 Adénocarcinomes : Lung Cancer Mutation Consortium Identification
ALK et cancers broncho-pulmonaires Laurence Bigay-Gamé Unité d oncologie thoracique Hôpital Larrey, Toulouse Toulouse, le 19 Février 2013 Adénocarcinomes : Lung Cancer Mutation Consortium Identification
Le cliché thoracique
 Le cliché thoracique Date de création du document 2008-2009 Table des matières * Introduction... 1 1 Nomenclature radiologique... 1 2 Le cliché thoracique de face... 2 2. 1 Qualité du cliché... 1 2. 2
Le cliché thoracique Date de création du document 2008-2009 Table des matières * Introduction... 1 1 Nomenclature radiologique... 1 2 Le cliché thoracique de face... 2 2. 1 Qualité du cliché... 1 2. 2
Cancer broncho-pulmonaire du sujet âgé. Mathilde Gisselbrecht Capacité de gériatrie- Février 2009
 Cancer broncho-pulmonaire du sujet âgé Mathilde Gisselbrecht Capacité de gériatrie- Février 2009 Généralités Cancer bronchique primitif = cancer le plus fréquent en incidence dans le monde Incidence en
Cancer broncho-pulmonaire du sujet âgé Mathilde Gisselbrecht Capacité de gériatrie- Février 2009 Généralités Cancer bronchique primitif = cancer le plus fréquent en incidence dans le monde Incidence en
COMPARAISON DE QUATRE PROTOCOLES DE CHIMIOTHERAPIE POUR DES CANCERS DU POUMON NON A PETITES CELLULES (CBP NAPC) AVANCES
 COMPARAISON DE QUATRE PROTOCOLES DE CHIMIOTHERAPIE POUR DES CANCERS DU POUMON NON A PETITES CELLULES (CBP NAPC) AVANCES Approximativement, un tiers de tous les décès dus au cancer sont en relation avec
COMPARAISON DE QUATRE PROTOCOLES DE CHIMIOTHERAPIE POUR DES CANCERS DU POUMON NON A PETITES CELLULES (CBP NAPC) AVANCES Approximativement, un tiers de tous les décès dus au cancer sont en relation avec
Peut-on ne pas reprendre des marges «insuffisantes» en cas de Carcinome canalaire infiltrant
 Peut-on ne pas reprendre des marges «insuffisantes» en cas de Carcinome canalaire infiltrant Institut Cancérologie de l Ouest CHIRURGIE Dr. Isabelle Jaffré CAS CLINIQUE 1 36 ans 90B sans CI radiothérapie
Peut-on ne pas reprendre des marges «insuffisantes» en cas de Carcinome canalaire infiltrant Institut Cancérologie de l Ouest CHIRURGIE Dr. Isabelle Jaffré CAS CLINIQUE 1 36 ans 90B sans CI radiothérapie
Votre guide des définitions des maladies graves de l Assurance maladies graves express
 Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
Votre guide des définitions des maladies graves de l Assurance maladies graves express Votre guide des définitions des maladies graves de l Assurance maladies graves express Ce guide des définitions des
Quel apport de l imagerie dans les traitements anti-angiogéniques?
 Quel apport de l imagerie dans les traitements anti-angiogéniques? L Fournier, D Balvay, CA Cuénod Service de radiologie, Hôpital Européen Georges Pompidou Laboratoire de Recherche en Imagerie, Equipe
Quel apport de l imagerie dans les traitements anti-angiogéniques? L Fournier, D Balvay, CA Cuénod Service de radiologie, Hôpital Européen Georges Pompidou Laboratoire de Recherche en Imagerie, Equipe
Place de la chirurgie pulmonaire dans les Cancers primitifs et Chirurgie de Métastasectomie Pulmonaire
 Place de la chirurgie pulmonaire dans les Cancers primitifs et Chirurgie de Métastasectomie Pulmonaire A.J. PONCELET, Ph. NOIRHOMME. Department of Cardio-Thoracic Surgery, Cliniques universitaires Saint-Luc,
Place de la chirurgie pulmonaire dans les Cancers primitifs et Chirurgie de Métastasectomie Pulmonaire A.J. PONCELET, Ph. NOIRHOMME. Department of Cardio-Thoracic Surgery, Cliniques universitaires Saint-Luc,
Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic de cancer
 Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
Information importante pour les personnes atteintes d un cancer du poumon non à petites cellules de stade avancé Les renseignements suivants sont destinés uniquement aux personnes qui ont reçu un diagnostic
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : Objectif de ce chapitre. 6.1 Introduction 86
 LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
LIGNES DIRECTRICES CLINIQUES TOUT AU LONG DU CONTINUUM DE SOINS : ÉTABLISSEMENT DE LIENS ENTRE LES PERSONNES CHEZ QUI UN DIAGNOSTIC D INFECTION À VIH A ÉTÉ POSÉ ET LES SERVICES DE SOINS ET DE TRAITEMENT
Innovations thérapeutiques en transplantation
 Innovations thérapeutiques en transplantation 3èmes Assises de transplantation pulmonaire de la région Est Le 16 octobre 2010 Dr Armelle Schuller CHU Strasbourg Etat des lieux en transplantation : 2010
Innovations thérapeutiques en transplantation 3èmes Assises de transplantation pulmonaire de la région Est Le 16 octobre 2010 Dr Armelle Schuller CHU Strasbourg Etat des lieux en transplantation : 2010
Cancer de l ovaire. traitements, soins et innovation. traitements adjuvants et de consolidation. www.e-cancer.fr. juin 2009
 traitements, soins et innovation juin 2009 recommandations professionnelles Cancer de l ovaire traitements adjuvants et de consolidation COLLECTION recommandations & référentiels RECOMMANDATIONS DE PRISE
traitements, soins et innovation juin 2009 recommandations professionnelles Cancer de l ovaire traitements adjuvants et de consolidation COLLECTION recommandations & référentiels RECOMMANDATIONS DE PRISE
Les grands syndromes. Endoscopie trachéo-bronchique. Professeur D. ANTHOINE CHU de NANCY
 Les grands syndromes Endoscopie trachéo-bronchique Professeur D. ANTHOINE CHU de NANCY 1 Endoscopie souple avec pince et brosse (fibroscopie) 2 Endoscopie Arbre bronchique normal Bifurcation trachéobronchique
Les grands syndromes Endoscopie trachéo-bronchique Professeur D. ANTHOINE CHU de NANCY 1 Endoscopie souple avec pince et brosse (fibroscopie) 2 Endoscopie Arbre bronchique normal Bifurcation trachéobronchique
UE2 CANCEROLOGIE Place de la Médecine Nucléaire
 UE2 CANCEROLOGIE Place de la Médecine Nucléaire Imagerie Imagerie de Gamma Caméra Tomographie d émission monophotoniqueou TEMP: radiopharmaceutiqueémetteurs de rayonnement Gamma Imagerie de Caméra TEP
UE2 CANCEROLOGIE Place de la Médecine Nucléaire Imagerie Imagerie de Gamma Caméra Tomographie d émission monophotoniqueou TEMP: radiopharmaceutiqueémetteurs de rayonnement Gamma Imagerie de Caméra TEP
Association lymphome malin-traitement par Interféron-α- sarcoïdose
 Association lymphome malin-traitement par Interféron-α- sarcoïdose Auteurs Cendrine Godet (*) Jean-Pierre Frat (**) Cédric Landron (*) Lydia Roy (***) Paul Ardilouze (****) Jean-Pierre Tasu (****) (*)
Association lymphome malin-traitement par Interféron-α- sarcoïdose Auteurs Cendrine Godet (*) Jean-Pierre Frat (**) Cédric Landron (*) Lydia Roy (***) Paul Ardilouze (****) Jean-Pierre Tasu (****) (*)
Lymphome non hodgkinien
 Lymphome non hodgkinien Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca LYMPHOME NON HODGKINIEN Ce que vous devez savoir Même si vous entendez parler du cancer presque
Lymphome non hodgkinien Ce que vous devez savoir Le cancer : une lutte à finir 1 888 939-3333 www.cancer.ca LYMPHOME NON HODGKINIEN Ce que vous devez savoir Même si vous entendez parler du cancer presque
CANCER DU POUMON ACTION-RÉACTION!
 CANCER DU POUMON ACTION-RÉACTION! F O R M A T I O N C O N T I N U E // M me Bouchard, 65 ans, se présente à votre cabinet pour une toux sèche et persistante depuis un mois avec une légère dyspnée. Elle
CANCER DU POUMON ACTION-RÉACTION! F O R M A T I O N C O N T I N U E // M me Bouchard, 65 ans, se présente à votre cabinet pour une toux sèche et persistante depuis un mois avec une légère dyspnée. Elle
Qu est-ce que le cancer de l œsophage?
 Cancer de l œsophage Qu est-ce que le cancer de l œsophage? Laissez-nous vous expliquer. www.fondsanticancer.org www.esmo.org ESMO/FAC Patient Guide Series basés sur les recommandations de pratique clinique
Cancer de l œsophage Qu est-ce que le cancer de l œsophage? Laissez-nous vous expliquer. www.fondsanticancer.org www.esmo.org ESMO/FAC Patient Guide Series basés sur les recommandations de pratique clinique
Document d information dans le cadre de l installation d un cyclotron. à Saint-Louis
 Document d information dans le cadre de l installation d un cyclotron à Saint-Louis Cancers & imagerie médicale Un progrès majeur pour une meilleure prise en charge des patients. Accroitre les possibilités
Document d information dans le cadre de l installation d un cyclotron à Saint-Louis Cancers & imagerie médicale Un progrès majeur pour une meilleure prise en charge des patients. Accroitre les possibilités
INFORMATION À DESTINATION DES PROFESSIONNELS DE SANTÉ LE DON DU VIVANT
 INFORMATION À DESTINATION DES PROFESSIONNELS DE SANTÉ LE DON DU VIVANT QUELS RÉSULTATS POUR LE RECEVEUR? QUELS RISQUES POUR LE DONNEUR? DONNER UN REIN DE SON VIVANT PEUT CONCERNER CHACUN /////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////
INFORMATION À DESTINATION DES PROFESSIONNELS DE SANTÉ LE DON DU VIVANT QUELS RÉSULTATS POUR LE RECEVEUR? QUELS RISQUES POUR LE DONNEUR? DONNER UN REIN DE SON VIVANT PEUT CONCERNER CHACUN /////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////////
Réflexions sur les possibilités de réponse aux demandes des chirurgiens orthopédistes avant arthroplastie
 Bull. Acad. Natle Chir. Dent., 2007, 50 113 Commission de l exercice professionnel et Groupe de réflexion Réflexions sur les possibilités de réponse aux demandes des chirurgiens orthopédistes avant arthroplastie
Bull. Acad. Natle Chir. Dent., 2007, 50 113 Commission de l exercice professionnel et Groupe de réflexion Réflexions sur les possibilités de réponse aux demandes des chirurgiens orthopédistes avant arthroplastie
Leucémies de l enfant et de l adolescent
 Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Janvier 2014 Fiche tumeur Prise en charge des adolescents et jeunes adultes Leucémies de l enfant et de l adolescent GENERALITES COMMENT DIAGNOSTIQUE-T-ON UNE LEUCEMIE AIGUË? COMMENT TRAITE-T-ON UNE LEUCEMIE
Le traitement conservateur des tumeurs malignes des membres a largement remplacé les amputations
 FACE A FACE Péroné vascularisé / Péroné non vascularisé Reconstruction après résection tumorale Dr NOURI / Dr BEN MAITIGUE SOTCOT Juin 2012 Le traitement conservateur des tumeurs malignes des membres a
FACE A FACE Péroné vascularisé / Péroné non vascularisé Reconstruction après résection tumorale Dr NOURI / Dr BEN MAITIGUE SOTCOT Juin 2012 Le traitement conservateur des tumeurs malignes des membres a
COMMISSION DE LA TRANSPARENCE. Avis. 23 mai 2007
 COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
COMMISSION DE LA TRANSPARENCE Avis 23 mai 2007 SUTENT 12,5 mg, gélule Flacon de 30 (CIP: 376 265-0) SUTENT 25 mg, gélule Flacon de 30 (CIP: 376 266-7) SUTENT 50 mg, gélule Flacon de 30 (CIP: 376 267-3)
UNE INTERVENTION CHIRURGICALE AU NIVEAU DU SEIN
 UNE INTERVENTION CHIRURGICALE AU NIVEAU DU SEIN Informations générales Pour vous, pour la vie Cette brochure vise à vous fournir des informations générales concernant l intervention chirurgicale que vous
UNE INTERVENTION CHIRURGICALE AU NIVEAU DU SEIN Informations générales Pour vous, pour la vie Cette brochure vise à vous fournir des informations générales concernant l intervention chirurgicale que vous
Qu est-ce que le cancer du sein?
 Cancer du sein Qu est-ce que le cancer du sein? Laissez-nous vous expliquer. www.fondsanticancer.org www.esmo.org ESMO/FAC Patient Guide Series basés sur les recommandations de pratique clinique de ESMO
Cancer du sein Qu est-ce que le cancer du sein? Laissez-nous vous expliquer. www.fondsanticancer.org www.esmo.org ESMO/FAC Patient Guide Series basés sur les recommandations de pratique clinique de ESMO
Charte régionale des Réunions de Concertation Pluridisciplinaire de PACA, Corse et Monaco
 Réseau Régional de Cancérologie ONCOPACA-Corse Charte régionale des Réunions de Concertation Pluridisciplinaire de PACA, Corse et Monaco 1. CONTEXTE ET OBJECTIF Contexte : Cette présente charte a été définie
Réseau Régional de Cancérologie ONCOPACA-Corse Charte régionale des Réunions de Concertation Pluridisciplinaire de PACA, Corse et Monaco 1. CONTEXTE ET OBJECTIF Contexte : Cette présente charte a été définie
Le dépistage du cancer de la prostate. une décision qui VOUS appartient!
 Le dépistage du cancer de la prostate une décision qui VOUS appartient! Il existe un test de dépistage du cancer de la prostate depuis plusieurs années. Ce test, appelé dosage de l antigène prostatique
Le dépistage du cancer de la prostate une décision qui VOUS appartient! Il existe un test de dépistage du cancer de la prostate depuis plusieurs années. Ce test, appelé dosage de l antigène prostatique
Session plénière: 1 / 4 Sessions scientifiques et poster discussions: Poster présentations: 87/1438
 CANCERS DIGESTIFS Session plénière: 1 / 4 Sessions scientifiques et poster discussions: 38/435 Poster présentations: 87/1438 The TME Trial after a Median Follow-up of 11 Years C. A. Marijnen et Al, Leiden,
CANCERS DIGESTIFS Session plénière: 1 / 4 Sessions scientifiques et poster discussions: 38/435 Poster présentations: 87/1438 The TME Trial after a Median Follow-up of 11 Years C. A. Marijnen et Al, Leiden,
Les sciences de l ingénieur appliquées à la prise en charge du
 Les sciences de l ingénieur appliquées à la prise en charge du cancer : enjeux et opportunités Début de cartographie des enjeux cliniques et technologiques gq Jean-François MENUDET, Cluster I-Care Cartographie
Les sciences de l ingénieur appliquées à la prise en charge du cancer : enjeux et opportunités Début de cartographie des enjeux cliniques et technologiques gq Jean-François MENUDET, Cluster I-Care Cartographie
Transplantation pulmonaire et mucoviscidose. Optimiser la prise en charge médicale
 Transplantation pulmonaire et mucoviscidose Optimiser la prise en charge médicale Dr Isabelle Danner-Boucher CRCM adulte de Nantes Unité de Transplantation Thoracique 11èmes Journées Scientifiques de la
Transplantation pulmonaire et mucoviscidose Optimiser la prise en charge médicale Dr Isabelle Danner-Boucher CRCM adulte de Nantes Unité de Transplantation Thoracique 11èmes Journées Scientifiques de la
TUTORAT UE 5 2012-2013 Anatomie Correction Séance n 6 Semaine du 11/03/2013
 TUTORAT UE 5 2012-2013 Anatomie Correction Séance n 6 Semaine du 11/03/2013 Appareil respiratoire-organogénèse de l appareil digestif Cours du Pr. PRUDHOMME Séance préparée par Anissa BARAKAT, Caroline
TUTORAT UE 5 2012-2013 Anatomie Correction Séance n 6 Semaine du 11/03/2013 Appareil respiratoire-organogénèse de l appareil digestif Cours du Pr. PRUDHOMME Séance préparée par Anissa BARAKAT, Caroline
Prise en charge des dysplasies et carcinomes in situ de la surface oculaire au CHT de Nouvelle-Calédonie
 Prise en charge des dysplasies et carcinomes in situ de la surface oculaire au CHT de Nouvelle-Calédonie Congrès de la SFO Mai 2011 M. Le Loir (Brest), E. Mancel (Nouméa), L.W. Hirst (Brisbane) Dysplasie
Prise en charge des dysplasies et carcinomes in situ de la surface oculaire au CHT de Nouvelle-Calédonie Congrès de la SFO Mai 2011 M. Le Loir (Brest), E. Mancel (Nouméa), L.W. Hirst (Brisbane) Dysplasie
Evaluation péri-opératoire de la tolérance à l effort chez le patient cancéreux. Anne FREYNET Masseur-kinésithérapeute CHU Bordeaux
 Evaluation péri-opératoire de la tolérance à l effort chez le patient cancéreux Anne FREYNET Masseur-kinésithérapeute CHU Bordeaux Je déclare n avoir aucun conflit d intérêt en lien avec cette présentation
Evaluation péri-opératoire de la tolérance à l effort chez le patient cancéreux Anne FREYNET Masseur-kinésithérapeute CHU Bordeaux Je déclare n avoir aucun conflit d intérêt en lien avec cette présentation
Introduction. Lésion pulmonaire dite suspecte en l absence l nignité:
 Comparaison entre scanner et morphotep dans l él évaluation du stade TNM d une d lésion l pulmonaire suspecte S Ciprian-Corby (1), L Meyer-Bisch (1), MA Muller (2), P Olivier (2), A Bertrand (2), D Régent
Comparaison entre scanner et morphotep dans l él évaluation du stade TNM d une d lésion l pulmonaire suspecte S Ciprian-Corby (1), L Meyer-Bisch (1), MA Muller (2), P Olivier (2), A Bertrand (2), D Régent
Cancer du sein. Du CA15-3 à la tomographie à émission de positons.
 Cancer du sein. Du CA15-3 à la tomographie à émission de positons. Un taux de récidive de 30% dans les dix premières années chez des patientes en rémission complète après un traitement curatif, requiert
Cancer du sein. Du CA15-3 à la tomographie à émission de positons. Un taux de récidive de 30% dans les dix premières années chez des patientes en rémission complète après un traitement curatif, requiert
Qu avez-vous appris pendant cet exposé?
 Qu avez-vous appris pendant cet exposé? Karl VINCENT, DC IFEC 2010 Diplôme Universitaire de Méthodes en Recherche Clinique Institut de Santé Publique d Epidémiologie et de développement ISPED Bordeaux
Qu avez-vous appris pendant cet exposé? Karl VINCENT, DC IFEC 2010 Diplôme Universitaire de Méthodes en Recherche Clinique Institut de Santé Publique d Epidémiologie et de développement ISPED Bordeaux
Cancer du sein in situ
 traitements et soins octobre 2009 recommandations professionnelles Cancer du sein COLLECTION recommandations & référentiels Recommandations de prise en charge spécialisée Carcinome canalaire et carcinome
traitements et soins octobre 2009 recommandations professionnelles Cancer du sein COLLECTION recommandations & référentiels Recommandations de prise en charge spécialisée Carcinome canalaire et carcinome
Document d orientation sur les allégations issues d essais de non-infériorité
 Document d orientation sur les allégations issues d essais de non-infériorité Février 2013 1 Liste de contrôle des essais de non-infériorité N o Liste de contrôle (les clients peuvent se servir de cette
Document d orientation sur les allégations issues d essais de non-infériorité Février 2013 1 Liste de contrôle des essais de non-infériorité N o Liste de contrôle (les clients peuvent se servir de cette
Essais cliniques de phase 0 : état de la littérature 2006-2009
 17 èmes Journées des Statisticiens des Centres de Lutte contre le Cancer 4 ème Conférence Francophone d Epidémiologie Clinique Essais cliniques de phase 0 : état de la littérature 2006-2009 Q Picat, N
17 èmes Journées des Statisticiens des Centres de Lutte contre le Cancer 4 ème Conférence Francophone d Epidémiologie Clinique Essais cliniques de phase 0 : état de la littérature 2006-2009 Q Picat, N
F-FLUORODÉOXYGLUCOSE EN ONCOLOGIE Expérience en Ile de France
 18F-fluorodéoxyglucose en oncologie. Expérience en Ile de France. 18 F-FLUORODÉOXYGLUCOSE EN ONCOLOGIE Expérience en Ile de France H. FOEHRENBACH 1, J. LUMBROSO 2 1 Service Médecine Nucléaire, Hôpital
18F-fluorodéoxyglucose en oncologie. Expérience en Ile de France. 18 F-FLUORODÉOXYGLUCOSE EN ONCOLOGIE Expérience en Ile de France H. FOEHRENBACH 1, J. LUMBROSO 2 1 Service Médecine Nucléaire, Hôpital
Place de la chirurgie à l heure des thérapies ciblées. The role of surgery in the era of targeted therapy. * Non ouvert en France.
 dossier thématique Place de la chirurgie à l heure des thérapies ciblées The role of surgery in the era of targeted therapy P. Bigot*, J.C. Bernhard** Points forts» En association avec l immunothérapie,
dossier thématique Place de la chirurgie à l heure des thérapies ciblées The role of surgery in the era of targeted therapy P. Bigot*, J.C. Bernhard** Points forts» En association avec l immunothérapie,
CANCER DU POUMON À PETITES CELLULES ET NON À PETITES CELLULES : DIAGNOSTIC, TRAITEMENT ET SUIVI
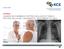 KCE REPORT 206BS SYNTHESE CANCER DU POUMON À PETITES CELLULES ET NON À PETITES CELLULES : DIAGNOSTIC, TRAITEMENT ET SUIVI 2013 www.kce.fgov.be Le Centre Fédéral d Expertise des Soins de Santé Le Centre
KCE REPORT 206BS SYNTHESE CANCER DU POUMON À PETITES CELLULES ET NON À PETITES CELLULES : DIAGNOSTIC, TRAITEMENT ET SUIVI 2013 www.kce.fgov.be Le Centre Fédéral d Expertise des Soins de Santé Le Centre
Cancer et dyspnée: comment peut-on soulager? Dr Lise Tremblay 10 mai 2010
 Cancer et dyspnée: comment peut-on soulager? Dr Lise Tremblay 10 mai 2010 Objectifs Comprendre la physiopathologie de la dyspnée Connaître les traitements disponibles pour soulager la dyspnée Définir la
Cancer et dyspnée: comment peut-on soulager? Dr Lise Tremblay 10 mai 2010 Objectifs Comprendre la physiopathologie de la dyspnée Connaître les traitements disponibles pour soulager la dyspnée Définir la
TRAITEMENT DES TUMEURS HEPATIQUES. Paul Legmann Radiologie A Pôle Imagerie
 TRAITEMENT DES TUMEURS HEPATIQUES Paul Legmann Radiologie A Pôle Imagerie TRAITEMENT DES TUMEURS HEPATIQUES Carcinome hépato-cellulaire : Sans traitement : survie à 5 ans < à 5 % (CHC sur cirrhose) Traitement
TRAITEMENT DES TUMEURS HEPATIQUES Paul Legmann Radiologie A Pôle Imagerie TRAITEMENT DES TUMEURS HEPATIQUES Carcinome hépato-cellulaire : Sans traitement : survie à 5 ans < à 5 % (CHC sur cirrhose) Traitement
Étude sur les délais de prise en charge des cancers du sein et du poumon
 Delais-Cancer Sein Poumon:32 pages 6/06/12 12:39 Page 1 Mesure 19 SOINS ET VIE DES MALADES Étude sur les délais de prise en charge des cancers du sein et du poumon DANS PLUSIEURS RÉGIONS DE FRANCE EN 2011
Delais-Cancer Sein Poumon:32 pages 6/06/12 12:39 Page 1 Mesure 19 SOINS ET VIE DES MALADES Étude sur les délais de prise en charge des cancers du sein et du poumon DANS PLUSIEURS RÉGIONS DE FRANCE EN 2011
Les traitements du cancer invasif du col de l utérus
 JUIN 2011 Les traitements du cancer invasif du col de l utérus Nom du chapitre COLLECTION GUIDES PATIENTS LE COL DE L UTÉRUS LE CHOIX DES TRAITEMENTS LA CHIRURGIE LA RADIOTHÉRAPIE LA CHIMIOTHÉRAPIE LES
JUIN 2011 Les traitements du cancer invasif du col de l utérus Nom du chapitre COLLECTION GUIDES PATIENTS LE COL DE L UTÉRUS LE CHOIX DES TRAITEMENTS LA CHIRURGIE LA RADIOTHÉRAPIE LA CHIMIOTHÉRAPIE LES
Intérêt de la TEP-FDG dans les cancers de l ovaire
 Intérêt de la TEP-FDG dans les cancers de l ovaire T. Mognetti et F. Giammarile Introduction La TEP-FDG (Tomographie par Émission de Positons après injection de 18 F- Fluoro-2-Déoxy-Glucose) est un des
Intérêt de la TEP-FDG dans les cancers de l ovaire T. Mognetti et F. Giammarile Introduction La TEP-FDG (Tomographie par Émission de Positons après injection de 18 F- Fluoro-2-Déoxy-Glucose) est un des
Cancer Bronchique «Sujet Agé» Etat de la litterature
 Cancer Bronchique «Sujet Agé» Etat de la litterature Situation en 2011 M CHAKRA Secteur Oncologie Thoracique CHU Arnaud de Villeneuve, Montpelier Qu est ce qu un sujet âgé? 70 ans est habituellement considéré
Cancer Bronchique «Sujet Agé» Etat de la litterature Situation en 2011 M CHAKRA Secteur Oncologie Thoracique CHU Arnaud de Villeneuve, Montpelier Qu est ce qu un sujet âgé? 70 ans est habituellement considéré
Découvrez L INSTITUT UNIVERSITAIRE DU CANCER DE TOULOUSE
 Découvrez L INSTITUT UNIVERSITAIRE DU CANCER DE TOULOUSE 2014 L INSTITUT UNIVERSITAIRE DU CANCER DE TOULOUSE L Institut universitaire du cancer de Toulouse (IUCT) est un nouveau modèle français d organisation
Découvrez L INSTITUT UNIVERSITAIRE DU CANCER DE TOULOUSE 2014 L INSTITUT UNIVERSITAIRE DU CANCER DE TOULOUSE L Institut universitaire du cancer de Toulouse (IUCT) est un nouveau modèle français d organisation
