Laboratoire de Biologie Médicale
|
|
|
- Carole Boudreau
- il y a 10 ans
- Total affichages :
Transcription
1 Laboratoire de Biologie Médicale Siège social : Le plan Oriental, Route départementale 562 Tel : Fax : MANUEL QUALITE Page 1 sur 36
2 SOMMAIRE INTRODUCTION 1. Objet et domaines d application 2. Glossaire et abréviations 3. Elaboration du MAQ CHAPITRE I : Présentation du laboratoire 1. Raison sociale et accès au laboratoire 2. Activité du laboratoire CHAPITRE II : Management du laboratoire 1. Organisation et management a. Déclaration de politique de qualité b. Engagement de la direction c. Organisation du laboratoire (Personnel /Locaux) 2. Système de Management de la qualité a. Organisation du SMQ b. Evaluation et Amélioration du SMQ 3. Communication a. Interne b. Externe c. Ethique d. Confidentialité CHAPITRE III : Processus de réalisation 1. Phase pré analytique 2. Phase analytique 3. Phase post analytique 4. Prestation de conseil CHAPITRE IV : Processus Supports 1. Gestion du personnel 2. Gestion documentaire 3. Informatique 4. Gestion administrative 5. Equipements (Matériel et Métrologie) 6. Achats 7. Hygiène, Sécurité et Environnement Page 2 sur 36
3 INTRODUCTION 1. Objet et domaines d application Ce manuel a pour objectif de présenter les dispositions générales mises en œuvre par le laboratoire SELARL du Lac pour garantir la qualité de ses prestations conformément à la réglementation en vigueur et aux exigences de la norme NF EN ISO (version Décembre 2012) Laboratoire de Biologie médicales : Exigences particulières concernant la qualité et la compétence. Il décrit notamment l organisation du laboratoire, ses différents types de prestations et les dispositions mises en place et appliquées systématiquement en matière d assurance de la qualité. Ce manuel s adresse à notre structure interne, aux clients, prescripteurs, auditeurs Les dispositions décrites dans le présent manuel s appliquent à l ensemble des activités pour les phases pré-analytique, analytique et post-analytique. 2. Glossaire et abréviations Examens de biologie médicale : Examens biologiques qui concourent au diagnostic, au traitement ou à la prévention des maladies humaines ou qui font apparaître toute autre modification de l état physiologique, à l exclusion des actes d anatomie et de cytologie pathologiques exécutés par les médecins spécialistes de cette discipline. Comptes rendus d analyse : Documents écrits, validés et signés par le biologiste comportant les résultats d analyses qualitatifs et/ou quantitatifs accompagnés de commentaires aussi souvent que cela est nécessaire ou prévu par la réglementation. Ces résultats doivent être présentés conformément à la réglementation en vigueur. ISO : International Organisation for Standardisation Prélèvement : Acte permettant l obtention d un échantillon biologique. Validation : Opération permettant d assurer qu un résultat a été obtenu dans des conditions techniques satisfaisantes et que celui-ci est compatible avec le dossier biologique du patient. KaliLab :nom du logiciel de gestion de la qualité utilisé par le LBM du Lac Page 3 sur 36
4 3. Gestion du MAQ Elaboration, Vérification et Approbation du manuel qualité La rédaction et la vérification du manuel qualité est sous la responsabilité du Responsable Qualité. L approbation du manuel qualité est sous la responsabilité de la direction qui s assure que les dispositions prises sont pertinentes vis à vis de la politique et des objectifs qualité édités. Diffusion du manuel qualité La direction organise la diffusion du manuel qualité. Trois types de diffusion sont en vigueur : 1) La diffusion contrôlée interne du manuel qualité à l ensemble du personnel via KaliLab permettant le suivi des attestations de lecture. Les destinataires reçoivent ainsi systématiquement des mises à jour, 2) La diffusion non contrôlée en externe du manuel qualité : elle est tracée dans KaliLab. Les destinataires ne reçoivent pas systématiquement des mises à jour, 3) La diffusion contrôlée en externe du manuel qualité : elle est tracée dans KaliLab. Les destinataires reçoivent systématiquement des mises à jour. Gestion des modifications Le manuel qualité est revu au minimum une fois par an par le Responsable Qualité qui déclenche, si nécessaire, sa mise à jour. Il est modifié suite à des modifications du système qualité (nouvelles dispositions, changements organisationnelles.). Toute modification est à nouveau ré approuvée par la direction, avant diffusion. L objet des modifications est indiqué dans KaliLab et par des annotations sur le document. Classement et archivage La version originale informatique est archivée dans KaliLab pour une durée illimitée. Les versions obsolètes papier du manuel qualité sont remises au Responsable Qualité pour destruction qui transmet ainsi la nouvelle version papier du manuel. Page 4 sur 36
5 CHAPITRE I : Présentation du laboratoire 1. Raison sociale et accès au laboratoire Historique : La SELARL BIOSIAGNE, est une société créé en 1995 par G.Zanchi, pharmacien biologiste et exploité sous N registre du commerce / SIREN / SIRET : A l origine, le laboratoire Zanchi créé en 1982, 104 chemin de Draguignan, Fayence, était exploité en nom propre, et c est lors de la création d un nouveau laboratoire à Callian, au Centre Agora Lot 26 Chemin Jean Paul Callian, qu il y a eu un changement de mode d exercice sous forme de SELARL. Le laboratoire Renassia a été dirigé par Mme Frédérique Renassia, médecin biologiste de 1995 à Durant toute ces années, la SELARL BIOSIAGNE, a travaillé en collaboration avec le laboratoire Fain, situé 13 avenue Fréderic Mistral Peymeinade. Ce laboratoire, entièrement rénové en aout 2010, a été créé en 1984 par Mme FAIN-ZANCHI et exploité en nom propre jusqu alors. La SELARL LABM DU LAC, quant à elle, a été créée en 2008 par R.ZANCHI lors de la création du laboratoire du lac, Route départementale 562 le Plan oriental à Montauroux et exploité sous le R.C.S Quatre ans plus tard la SELARL a fait l acquisition du laboratoire Fain à Peymeinade. Les laboratoires ont installés un Système d Information de Laboratoire, SIL, (SELECT INFORMATIQUE Concerto) et un logiciel qualité (KaliLab de NETIKA) communs. Les deux SELARL ont procédé à une fusion de leurs sites en une structure unique depuis fin 2013 sous le nom de SELARL LABM Du lac. En Février 2014, la SELARL fait l acquisition du laboratoire ARNAUD situé 1268 Avenue de Provence Fréjus créé par Mr Roger ARNAUD en Mars 1989, le Dr ARNAUD restant le biologiste responsable du laboratoire. Ce laboratoire fait l objet d un transfert dans des nouveaux locaux courant Juillet Page 5 sur 36
6 Le laboratoire, situé Centre Agora Lot 26 Chemin Jean Paul Callian est, quant à lui transféré dans les anciens locaux du laboratoire ARNAUD avec comme biologiste responsable le Dr ZANCHI. Le site de Montauroux passe sous la responsabilité du DR BARTOLO Aurore. Dans un souci de clarté, le laboratoire du Dr ARNAUD sera identifié VINCI et le laboratoire du Dr ZANCHI (ex laboratoire Renassia) FREJUS. En Janvier 2015, le laboratoire a pris pour nom commercial i-lab. En Juin 2015, la SELARL COLLET de Nice du Dr COLLET Guillaume, rejoint le groupement dans le cadre d une fusion acquisition. Ce laboratoire est accrédité COFRAC selon les exigences de la norme NF EN ISO (N ). Le Laboratoire de Biologie Médicale COLLET, initialement 54 Boulevard Paul Montel Nice a été créé en 1984 et autorisé par enregistrement préfectoral sous le numéro A la suite d un aménagement de nouveaux locaux, ce laboratoire est transféré au 36 Boulevard Paul Montel Résidence l Alandier NICE. Page 6 sur 36
7 Présentation des sites : Site de Montauroux : Dr BARTOLO Aurore Le plan oriental - Bâtiment B RD 562 Coordonnées : Tel : / Fax : Site de Fayence : Dr TREIL Antoine 104 Chemin de Draguignan FAYENCE Coordonnées : Tel : / Fax : Site de Fréjus : Dr ZANCHI Romain 1268 Avenue de Provence Fréjus Coordonnées : Tel : / Fax : Site de Peymeinade : Dr ALEX Stéphanie 13 avenue Fréderic Mistral Peymeinade Coordonnées : Tel : / Fax : Site de Fréjus (VINCI) : Dr ARNAUD Roger 359 avenue de Triberg FREJUS Coordonnées : Tel : / Fax : Site de Nice : Dr COLLET Guillaume 36 boulevard Paul Montel - Résidence l Alandier Nice Coordonnées : Tel : / Fax : Le laboratoire met à la disposition de ses clients un site internet Page 7 sur 36
8 Horaires d ouverture : SITE Lundi au Vendredi Samedi Montauroux 7h30-18h30 7h30-12h30 Fayence 7h30-18h30 7h30-12h30 Vinci 7h30-18h30 8h 12h00 Fréjus 7h30-18h30 8h 12h00 Peymeinade 7h30 12h et 14h -18h30 7h30-12h30 Nice 7h15-18h45 8h 12h Page 8 sur 36
9 2. Activité du laboratoire Groupement de 6 sites Laboratoire de biologie médicale i-lab Site Montauroux Directeur : Aurore BARTOLO *Plateau technique Site Fayence Directeur : Antoine TREIL Site Peymeinade Directeur : Stéphanie Alex Site Fréjus Directeur : Romain ZANCHI Site Nice Directeur : Guillaume COLLET Site Vinci Directeur : Roger ARNAUD *Plateau technique secondaire Les laboratoires traitent approximativement 415 dossiers/ jour avec comme proportion : Page 9 sur 36
10 110 dossiers/jour sont traités par le site de Fayence dont 70% (soit environ 80 dossiers) sont issus de prélèvements faits au laboratoire, 20% sont issus de prélèvements à domicile par les infirmiers et 10 % par les maisons de retraites. 70 dossiers/jour sont traités par le site de Peymeinade dont 80% sont issus de prélèvements faits au laboratoire et 20% sont issus de prélèvements à domicile par les infirmiers. 90 dossiers/ jour traités par le site de Montauroux dont 80% sont issus de prélèvements faits au laboratoire et 20% sont issus de prélèvements à domicile par les infirmiers. 85 dossiers/jours traités par le site Vinci dont 80% sont issus de prélèvements faits au laboratoire et 20% sont issus de prélèvements à domicile par les infirmiers. 60 dossiers/jours traités par le site de Nice dont 90% sont issus des prélèvements faits au laboratoire et 10% sont issus des prélèvements à domicile par les infirmiers. Le site de Fréjus étant en cours de transfert, nous n avons pas de données à jour. Les examens sont effectués sous la responsabilité des biologistes qui garantissent l indépendance de jugement, d intégrité et de confidentialité des résultats. Les secteurs d activité technique du Laboratoire sont répartis de la manière suivante : Sites techniques Montauroux (MO) Vinci (VI) Activités analytiques Secteur Hormonologie-Immunologie Secteur Sérologie infectieuse Secteur Hémato-Hémostase Secteur Biochimie Secteur Microbiologie Secteur Spermiologie Secteur Hémostase Secteur Hormonologie-Immunologie Secteur Sérologie infectieuse La répartition précise des analyses entre chaque site est consultable dans le document «Catalogue des analyses». Page 10 sur 36
11 CHAPITRE II : Management du laboratoire 1. Organisation et management a. Déclaration de politique de qualité Depuis le rapport Ballereau concernant la réforme de la biologie médicale en France, le visage de la biologie de ville se modifie considérablement. L ensemble des laboratoires devront être accrédités par le COFRAC (Comité Français d Accréditation) selon la norme qualité ISO : 2012 à l horizon A notre niveau, cette évolution n est que la suite logique de notre engagement dans la qualité. Notre politique qualité a toujours visé la satisfaction de nos clients : patients, prescripteurs, laboratoires partenaires et administrations avec lesquelles nous collaborons. Notre but : leur offrir le plus haut niveau de prestation possible avec, comme optique, un accueil de qualité, une réalisation du prélèvement optimale, la bonne exécution des examens avec une interprétation juste et fiable, ainsi que des prestations de conseils et une écoute de qualité. La qualité s accompagne d une démarche volontaire d amélioration continue. Chaque équipe managée par les biologistes a bien compris les enjeux et applique les politiques et les procédures mises en place. Nous dynamisons ainsi année après année notre système qualité, renforçons notre travail d équipe et intégrons au mieux les exigences des bonnes pratiques professionnelles ainsi que celles de la norme ISO : Les objectifs qualité en 2015 sont avant tout basés sur : - Etendre notre portée d accréditation à 50% des examens réalisés accrédités avant Octobre La poursuite dans l établissement et le suivi de notre système qualité Page 11 sur 36
12 b. Engagement de la direction La Direction du laboratoire garantit qu'elle ne subit aucune pression ou influence commerciale indue, externe ou interne, financière ou autre, susceptible de mettre en cause la qualité des examens. De même, elle met en œuvre tout moyen de disposer des éléments cliniques pertinents qui lui permettent de réaliser les examens appropriés pour répondre aux besoins des prescripteurs et des patients. Ainsi, les comptes-rendus d'examens, selon les cas, comportent l'interprétation contextuelle du résultat. Dans la perspective d'atteindre les objectifs de qualité qu'il s'est fixés, le laboratoire a entrepris une politique axée sur les thèmes suivants : une maîtrise constante de l'activité professionnelle en travaillant avec des équipes internes motivées, impliquées, évaluées, proches de la clientèle, et formées régulièrementaux bonnes pratiques professionnelles et aux exigences de la norme NF EN ISO ; l'acquisition permanente de matériel de laboratoire performant et d'évolutions informatiques. Le laboratoire a donc installé une politique de management des équipes, au travers de sa cellule Qualité, de formations, d'audits internes et externes, d'enquêtes de satisfaction, et, enfin, de traçabilité des non-conformités ou des réclamations, tous ces items étant abordés et débattus au cours de réunions qualité régulières et de revues de Direction. Cela a permis de définir des indicateurs qualité dont le but est de porter satisfaction à notre clientèle. Pour atteindre ces objectifs de rigueur et de qualité, le laboratoire s'est doté d'un système de management de la qualité (SMQ), dont la mise en œuvre repose sur : une Politique Qualité et un Manuel Qualité; un système documentaire des processus et instructions, communiqués au personnel concerné des outils techniques de contrôle de qualité des analyses (contrôles internes au laboratoire et contrôles externes auprès de sociétés savantes) des programmes de maintenances et d'étalonnage des appareillages la présence d'un personnel compétent qualifié et habilité au poste de travail (ces compétences sont réévaluées périodiquement), et bénéficiant de formations externes et internes régulières le respect des conditions d'hygiène et de sécurité des locaux pour la clientèle et le personnel. Page 12 sur 36
13 c. Organisation du laboratoire (Personnel /Locaux) Les installations des laboratoires se composent : Des installations d accueil et de prélèvements : des salles de prélèvements avec le confort nécessaire dont au moins une réservée aux prélèvements gynécologiques pour l ensemble des laboratoires. Des installations de travail lui donnant les moyens de travailler dans les conditions optimisées à ce jour permettant la réalisation des analyses ; Des équipements nécessaires à la réalisation des prestations ; Des équipements nécessaires pour la protection des personnes. Ces installations et équipements sont maintenus régulièrement. De plus, une vérification des installations électriques et des extincteurs est effectuée régulièrement conformément à la réglementation en vigueur. L organigramme détaillé des sites est décrit dans le logiciel qualité du laboratoire. Nous avons repris dans ce manuel l organigramme présentant les fonctions du laboratoire. Page 13 sur 36
14 Directeurs Responsables techniques Responsable Métrologie Responsable Commercial Biologistes Responsable qualité Pilote de processus Responsable Informatique Référents techniques Responsable Secrétariat Référents qualité Auditeurs Internes Techniciens Préleveurs Secrétaires Coursier Agent d entretien Page 14 sur 36
15 Des fonctions et des fiches de définition de fonction individuelle ont été définies. Chaque fonction du laboratoire est décrite dans une fiche de fonction présentant les responsabilités liées à cette fonction ainsi que les compétences minimales requises (la gestion et le développement des compétences et qualification du personnel est décrite dans le paragraphe 1 de la partie «Gestion du personnel» du présent manuel). Pour chaque personne du laboratoire, dans son dossier personnel, existe une définition de fonction reprenant les fonctions et les responsabilités qu elle doit assumer en tant que titulaire d une part, et en tant que suppléant d autre part (s il y a lieu). La direction du laboratoire a identifié des fonctions dites clés pour lesquelles une suppléance est prévue afin d assurer la continuité de leur exercice. Page 15 sur 36
16 Cette organisation concerne donc les fonctions suivantes : Biologiste Responsable technique Responsable qualité Responsable informatique Responsable métrologie Pilotes de processus La direction générale du laboratoire est responsable de l ensemble des activités du laboratoire et de la définition de la politique et des objectifs qualité. Elle est responsable de la conception, de la mise en œuvre, de la maintenance et de l amélioration du système de management de la qualité. Des biologistes responsables techniques par secteur ont été nommés par la direction générale. Ils ont la responsabilité générale des opérations techniques, notamment la supervision des analyses et l affectation des ressources nécessaires pour assurer la qualité requise par le laboratoire. Le responsable qualité désigné par la direction générale du laboratoire a notamment pour missions : gérer le système qualité en fonction de la politique et des objectifs définis par la direction ; sensibiliser le personnel à la démarche qualité et animer les formations qualité internes correspondantes ; s assurer de la conformité du système de management de la qualité aux exigences de la norme NF EN ISO 15189; rendre compte à la direction du fonctionnement du système qualité et de tout besoin d amélioration favoriser l amélioration du système qualité. Les Pilotes de processus définissent, organisent et mettent en œuvre le processus. Ils surveillent les indicateurs qualité associés. Lorsque des écarts sont mis en avant, ils mettent en place et suivent les actions d'amélioration éventuelles pour parvenir à l'amélioration continue du processus. Ce sont les responsables qualité et les biologistes qui se répartissent le pilotage des différents processus (cf «Cartographie des processus»). Le matériel et les équipements : Page 16 sur 36
17 Une liste des matériels et une liste des analyses effectuées dans chaque laboratoire et soustraitées (laboratoires spécialisés et/ou en contrat de collaboration) sont établies et tenues à jour dans le logiciel qualité du laboratoire par le responsable qualité. Page 17 sur 36
18 2. Système de Management de la qualité a. Organisation du SMQ Conformément à la Norme ISO Version 2012, le laboratoire a établi son système de management de la qualité autours d une approche processus. Il a défini et établi l ensemble des processus nécessaires pour répondre à sa politique et à ses objectifs qualité, ainsi qu aux besoins et exigences des utilisateurs. Plan qualité «Cartographie des processus» L organigramme mis en place afin de piloter et gérer l ensemble du système qualité est représenté ci-dessous : Cellule qualité Responsable qualité Pilotage du système qualité en accord avec les objectifs de la Direction Biologiste responsable Site Fayence Biologiste responsable Site Peymeinade Biologiste responsable Site Vinci Biologiste responsable Site Nice Biologiste responsable Site Montauroux Biologiste responsable Site Fréjus Pilotes des Référent processus qualité Site Montauroux Préleveurs Secrétaires Techniciens Coursiers Page 18 sur 36
19 b. Evaluation et Amélioration du SMQ Pour évaluer notre SMQ le laboratoire dispose de plusieurs outils : - Relevé et traitement des réclamations - Enquête de satisfaction Patient - Enquête de satisfaction Prescripteur - Indicateurs de qualité - Audits internes et audits externes L écoute des clients (patients, prescripteurs, laboratoires en collaboration, ): L écoute client s est organisée autour: du recueil et du traitement des réclamations permettant d augmenter la satisfaction des clients dans KaliLab; de la réalisation et de l analyse des enquêtes de satisfaction permettant de mesurer le taux de satisfaction de la population globale sollicitant notre laboratoire. Tous les retours des patients et prescripteurs (enquêtes et réclamations) sont analysées pour déterminer et planifier les éventuelles actions d amélioration associées. L ensemble des retours du personnel est également enregistré et traité. L ensemble des modalités de l écoute client sont décrite dans : Procédure «Ecoute client» Procédure «Gestion des non-conformités et réclamations» Gestion des indicateurs Le suivi de la politique qualité et des objectifs associés est assuré par la mise en place d indicateurs qualité pertinents suivis via un tableau de bord. Ces indicateurs sont analysés selon la fréquence définie dans le tableau de bord et un bilan annuel en revue de direction. Ils permettent : de surveiller le bon fonctionnement du laboratoire d évaluer systématiquement la qualité des prestations du laboratoire de mesurer l atteinte des objectifs fixés dans le cadre de la politique qualité du laboratoire. Page 19 sur 36
20 L atteinte des objectifs fixés est vérifiée lors de la revue de direction annuelle et permet de prendre des mesures correctives, si nécessaires. Gestion des audits internes Chaque année des audits internes sont planifiés lors de la revue de direction et réalisés par des personnes qualifiées afin de vérifier la mise en application et l efficacité du système qualité. Le programme d audit tiendra compte de l état et de l importance des processus audités et des résultats des audits précédents. Cela permet de faire remonter d éventuelles actions d amélioration. Ainsi, les résultats de ces audits sont analysés par la direction du laboratoire afin de déterminer et planifier les actions correctives et préventives appropriées. Procédure «Gestion des audits» Maîtrise des non-conformités Afin de faire évoluer notre système qualité, à chaque fois que le personnel du laboratoire constate un problème dans l exécution de la prestation ou une non-application du système qualité, des dispositions sont mises en œuvre pour enregistrer le problème dans KaliLab. Toute non-conformité détectée est donc formalisée par le personnel. Un bilan quantitatif et qualitatif de ces non conformités permet : une surveillance des récurrences, une définition et évaluation des actions correctives décidées. Une procédure décrit les modalités de gestion et de traitement des non-conformités et notamment les principes d enregistrement, le traitement effectué, l analyse des causes. Procédure «Gestion des non-conformités et réclamations» Gestion des actions d amélioration (actions correctives et préventives) Les actions d amélioration sont déclenchées suite à une analyse : des non-conformités internes ou externes, des réclamations, des résultats issus des enquêtes de satisfaction, des résultats des audits internes, des objectifs fixés lors de la revue de direction, des actions d amélioration précédentes non efficaces, des risques critiques identifiés. Page 20 sur 36
21 Ces actions sont formalisées dans KaliLab et leur suivi est assuré par le responsable qualité. Les modalités de définition et suivi des actions d amélioration sont décrites dans la : Procédure «Gestion desactions d amélioration» Revues de Direction Dans un but d évaluation du fonctionnement du laboratoire et de l adéquation du système qualité par rapport : aux besoins des clients à la politique et aux objectifs qualité définis La direction du laboratoire mène une à deux fois par an une revue de direction. Ces revues permettent à la direction, à partir de l ensemble des éléments (non-conformités, réclamations, bilan des audits ), de prendre conscience des résultats de la politique qualité, des déviations éventuelles, de décider de mesures correctives générales permettant d orienter à nouveau la politique qualité, d améliorer le système qualité et d adopter les moyens pour y parvenir. Chaque revue fait l objet d un compte rendu établi par le responsable qualité. Celui-ci est visé par la direction puis diffusé à l ensemble du personnel. Les modalités de préparation et de déroulement de la revue de direction sont décrites dans la : Procédure«Revue de Direction» Page 21 sur 36
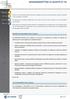
22 Objectifs Planning Plan d actions PLAN DO Actions préventives Formation Habilitation Documentation Vérification efficacité Actions d amélioration ACT CHECK Audit NC Enquête Figure 1: Roue de Deming - Amélioration continue 3. Communication a. Interne Pour s assurer que la politique, les objectifs et les résultats associés sont connus et compris par l ensemble du personnel, des actions de sensibilisation et de communication interne sont réalisées par différents moyens : -une messagerie interne par le logiciel qualité ; -les réunions avec le personnel (dont les formations internes) ; -l affichage ; -le compte-rendu de la revue de direction diffusé à l ensemble du personnel. Page 22 sur 36
23 b. Externe Communication avec les professionnels de santé La communication avec les médecins est une des tâches essentielles des biologistes du laboratoire. Les échanges sont permanents via les comptes rendus d analyses (commentaires, avis et interprétations) et les conversations téléphoniques. Communication avec les patients La communication avec les patients se fait quotidiennement au moment des contacts avec le personnel du laboratoire (accueil, prélèvement, rendu de résultats ). L interprétation des résultats aux patients est le fait exclusif des biologistes. L affichage en salle d attente permet la diffusion de l information réglementaire, administrative, organisationnelle et médicale. Un mail est à la disposition des patients afin Ces deux types de communication font parties de l obligation de Prestation de conseils c. L éthique Afin de garantir les exigences déontologiques inhérentes aux activités du laboratoire, les principes immuables suivants sont respectés : -aucune considération financière ou politique n influe sur la réalisation des analyses -l intérêt et les besoins des patients sont toujours la considération première -tous les patients sont traités équitablement et sans discrimination ; -seules les informations médicales strictement nécessaires à la réalisation de l analyse et à l interprétation des résultats sont collectées. d. Confidentialité Toute l activité du laboratoire est régie par le secret médical. Le personnel est tenu d assurer la confidentialité des informations qu il détient de par son activité au sein du laboratoire. Afin de mieux faire prendre conscience de la force de cette exigence, la fiche de définition de fonction, visée par le personnel, rappelle ce point particulier. L accès aux aires techniques d analyses est limité aux membres du personnel et aux personnes ayant signé un engagement de confidentialité de façon à garantir la sécurité des informations et des résultats. Les modalités en sont décrites de façon détaillée dans la : Page 23 sur 36
24 Procédure «Maîtrise de la confidentialité» Le laboratoire a pris les mesures nécessaires à la maitrise de l identitovigilance via la gestion des identifications des patients et échantillons. Les modalités en sont décrites de façon détaillée dans la : Procédure «Identitovigilance» Page 24 sur 36
25 CHAPITRE III : Processus de réalisation 1. Phase pré analytique a. Prise en charge d une demande d analyse Pour les demandes d analyses traitées par le laboratoire des critères d acceptation ou de refus ont été définis afin de répondre aux besoins clients, tout en respectant la réglementation en vigueur et les conditions de réalisation des analyses. Des modalités spécifiques ont été mises en œuvre pour le traitement des urgences. Dans tous les cas, si un doute subsiste, seul le biologiste est habilité à prendre la décision d acceptation de la demande. Une fois la demande acceptée, elle est enregistrée dans le système informatique afin d être traitée le plus rapidement possible selon les capacités techniques et humaines du laboratoire. Les modalités en sont décrites de façon détaillée dans les : Procédure «Traitement des demandes d examens» Procédure«Revue de contrat» Procédure «Gestion des urgences» b. Prélèvements Lorsqu un patient demande la réalisation d unexamen, les prélèvements peuvent être effectués au laboratoire, à domicile ou en maison de retraite. Cette étape est réglementée via la mise en place d un manuel de prélèvements reprenant les exigences du laboratoire. Procédure«Manuel de prélèvement» Page 25 sur 36
26 c. Gestion des échantillons Réception des échantillons Les échantillons peuvent être reçus : au secrétariat pour les prélèvements apportés par les patients et par les préleveurs externes. en technique, pour les prélèvements effectués au laboratoire (au site analytique et aux sites dits «périphériques»), en maison de retraite et les prélèvements issus d autres laboratoires. Des critères d acceptation et de refus des échantillons ont été définis à chaque niveau de réception afin de réaliser les analyses dans les conditions requises par la réglementation et les techniques utilisées. En cas de doute seul un biologiste est habilité à prendre la décision d acceptation ou de refus d un échantillon. Lorsqu un échantillon ne peut être traité, un nouveau prélèvement est effectué si cela est possible ; dans le cas contraire, le médecin prescripteur est informé par le biologiste. Les modalités en sont décrites de façon détaillée dans la : Procédure «Réception des échantillons» Modalités de transport, manipulation et conservation des échantillons Un document précise les règles de transport, manipulation et conservation des échantillons pré et post analytique. La manipulation des échantillons se fait rigoureusement de manière à éviter tout risque de contamination pour le personnel et tout risque d inversion en respectant une identification rigoureuse. Lorsqu un prélèvement réalisé à l extérieur doit être analysé en urgence ou nécessite un traitement pré analytique rapide, il est apporté immédiatement au laboratoire par le préleveur et les techniciens prennent en charge ce prélèvement. Certains échantillons nécessitent d être conservés en sérothèque conformément à la réglementation en vigueur. Les modalités en sont décrites de façon détaillée dans la : Procédure «Transport, manipulation et conservation des échantillons» Modalités de sous-traitance Le laboratoire transmet des examens à des sous-traitants dans les cas suivants : dans le cadre de transmission à des laboratoires partenaires Page 26 sur 36
27 lorsque des examens spécialisés ne peuvent être réalisées au laboratoire, en cas d impossibilité de réaliser une ou plusieurs analyses (panne d un appareil), pour un contrôle d'un résultat par une technique différente. Les résultats seront rendus sur le papier entête du laboratoire spécialisé ou une mention du lieu de réalisation de l examen sera indiquée sur le compte rendu dans le cas d un contrat de collaboration ou du règlement intérieur. Procédure «Sous-traitance des analyses» 2. Phase analytique a. Validation technique : Gestion des contrôles et des calibrations La validation technique permet de s assurer de la fiabilité de l appareil et des réactifs utilisés. Les modes opératoires par matériel décrivent les modalités techniques et fixent les périodicités de calibrations des matériels d analyse. Les modalités d analyse et de gestion des contrôles internes sont définies dans les modes opératoires par matériel. Le suivi de ces contrôles est assuré par les techniciens afin d éviter toute dérive. De plus la corrélation des résultats des examens est assurée par la participation du laboratoire à des contrôles externes. Les modalités générales en sont décrites dans la : Procédure «Validation technique Gestion des calibrations et des contrôles qualité» Le suivi des résultats des contrôles qualité est assuré par la mise en place de revues de poste mensuelles permettant l établissement d actions d amélioration. b. Validation analytique La validation analytique permet de vérifier la corrélation des valeurs trouvées avec les valeurs de référence et avec les précédents dossiers dans le cas de patient connu. Afin de garantir une homogénéité dans les conditions de contrôle des résultats, des critères de repasse ont été définis. Les modalités en sont décrites de façon détaillée dans la : Procédure «Validation analytique» Procédure «Validation des méthodes» Page 27 sur 36
28 c. Vérification des méthodes La validation technique a pour but de vérifier dans nos conditions de travail les bonnes performances analytiques de l automate ou de la technique utilisée. Procédure «Vérification des méthodes» Utilisation du matériel Un mode opératoire a été rédigé pour chaque analyseur selon les critères du fournisseur. Ces documents décrivent les modalités d utilisation du matériel. Ils sont disponibles à chaque paillasse ou consultable en ligne sur KALILAB. Pour les techniques manuelles on utilise les fiches d instructions disponibles en salle technique sous forme papier ou consultables informatiquement. Elles décrivent de manière précise les différentes étapes à suivre, le matériel, les réactifs utilisés, les limites de la technique utilisée et leur interprétation biologique. Les différentes manipulations sont effectuées dans le respect des règles d hygiène et de sécurité. La traçabilité des techniciens est faite soit dans l automate, soit sous forme d initiales sur des fiches ou cahiers de paillasses. Réalisation des examens Les examens sont effectués, par du personnel habilité, sur la base des fiches des fournisseurs ou de fiches d instruction internes pour certaines analyses manuelles (disponible à chaque paillasse et dans KaliLab). Elles décrivent, de manière précise, les différentes étapes à suivre, le matériel et les réactifs utilisés. Les différentes manipulations sont effectuées dans le respect des règles d hygiène et de sécurité. 3. Phase post analytique a. Validation biologique La validation biologique est le contrôle de la vraisemblance et de la cohérence de l ensemble des résultats des analyses d un même dossier, et leur confrontation avec les résultats antérieurs. Elle peut nécessiter la connaissance de l état clinique du patient et les traitements mis en œuvre. Seuls les biologistes peuvent réaliser cette validation. Tous les dossiers sont validés sur le système informatique central du laboratoire puis sont signés. Les modalités en sont décrites de façon détaillée dans la : Page 28 sur 36
29 Procédure «Procédure validation biologique» b. Transmission des résultats Les comptes rendus d examens ont une structure conforme à la réglementation. La présentation a été étudiée afin de faciliter la compréhension des résultats par les patients et les médecins prescripteurs. Des règles strictes ont été définies, pour le rendu des résultats, afin de garantir la confidentialité et le respect de la réglementation en vigueur. Les modalités en sont décrites de façon détaillée dans la : Procédure «Rendu des résultats» Des commentaires peuvent être nécessaires : ils peuvent être écrits ou oraux mais en aucun cas ils ne se substituent à l interprétation et au diagnostic du médecin prescripteur. c. Conservation et élimination des échantillons Les échantillons gardés en sérothèque sont conservés un an dans des congélateurs. Les autres biologiques». sont conservés selon l instruction : «Conservation des échantillons Les échantillons non conservés sont éliminés selon la procédure : Procédure «Elimination des déchets» 3. Prestation de conseil Comme le précisent la réglementation et la norme ISO NF EN :2012, les biologistes médicaux ont pour mission de réaliser des prestations de conseil aux professionnels de santé ainsi qu aux patients. Ces conseils peuvent porter sur : Le conseil en matière de choix ou de pertinence des examens biologiques (ajout ou suppression d examens) L interprétation des résultats Discussions scientifiques ou logistiques dans le but d améliorer les prestations au laboratoire lors de réunions d information avec les professionnels de santé (médecins, IDE). Les modalités en sont décrites de façon détaillée dans la : Procédure «Prestations de conseil» Page 29 sur 36
30 CHAPITRE IV : Processus Supports 1. Gestion du personnel Afin de garantir l adéquation permanente des compétences de ses équipes avec les exigences qualité du laboratoire, la direction a défini un processus de gestion du personnel qui couvre les activités suivantes : le recrutement et l intégration de nouveau personnel jusqu à l habilitation au poste la constitution et la gestion du dossier administratif de chaque salarié la conduite des entretiens individuels le maintien et l évaluation régulière des compétences la détection, la planification et le suivi des actions de formations internes et externes pour l ensemble du personnel (Plan de formation) la tenue d un planning afin de s assurer que le laboratoire dispose en permanence des moyens humains nécessaires pour la réalisation des analyses dans de bonnes conditions. Une formation spécifique en assurance et management de la qualité est suivie par l ensemble des membres du laboratoire. Les modalités en sont décrites de façon détaillée dans la : Procédure «Gestion du personnel» 2. Gestion documentaire a. La structure documentaire Le système documentaire est composé de 2 types de documentation. Les documents qualité internes au laboratoire et la documentation externe. Les documents qualité internes Il s agit de la documentation créée par le laboratoire décrivant l ensemble de l organisation et activités de celui-ci. Page 30 sur 36
31 Le système documentaire du laboratoire suit la structure pyramidale suivante conformément à la norme NF EN ISO : Norme NF EN ISO et plans qualité Décrivent les processus du SMQ Processus Quoi faire? Formulaires Décrivent les activités des processus Activités Comment faire? Instructions Décrivent les tâches des processus Tâches Procédures Servent de support aux enregistrements Enregistrements Servent de support aux enregistrements Figure 2: Structure pyramidale du système documentaire du LABM du LAC Comme représenté ci-dessus, ce système regroupe les documents suivants : Le présent manuel et les plans qualité (fiches processus), Les procédures, décrivant, si cela est nécessaire, les principes de fonctionnement et d organisation définis pour chaque chapitre du présent manuel, Les modes opératoires et fiches d instruction décrivent précisément les activités nécessaires pour assurer la qualité des prestations du laboratoire, Enfin, les preuves des activités effectuées ou des résultats obtenus peuvent être apportées par l intermédiaire du dernier niveau «formulaires d enregistrements». La flèche orange indique que chaque type de documents fait appel au type suivant. Les documents applicables «autres» La documentation applicable «autres» ou «externes» a une gestion qui lui est propre afin de Page 31 sur 36
32 conserver la cohérence avec la démarche qualité des établissements supports (établissements de santé et laboratoires en collaboration, fournisseurs). Cette documentation concerne également les documents réglementaires, législatifs et normatifs. Cette veille réglementaire est gérée grâce à un support informatique qui alerte à chaque changement ou évolution de cette documentation. b. La gestion des documents applicables Après approbation, tous les documents du système qualité sont diffusés par le responsable qualité auprès du personnel qui doit en prendre connaissance et les signer, afin que la mise en œuvre puisse être effective. Excepté le manuel qualité, les modalités de gestion des documents applicables «qualité» et «autres» sont décrites dans la : Procédure «Gestion des documents applicables» L ensemble des opérations citées ci-dessus est réalisé et maitrisé via le logiciel KaliLab. c. Maitrise des enregistrements et archivage Chaque document qualité précise les règles de classement et d archivage des enregistrements «techniques» ou qualité auxquels ils font référence. Les enregistrements sont conservés sur support papier ou informatique. Les modalités de conservation permettent de retrouver facilement les informations, et garantissent un environnement approprié pour éviter les détériorations, les endommagements, les pertes et le respect de la confidentialité. Les modalités en sont décrites de façon détaillée dans la : Procédure «Gestion des enregistrements et archivage» 3. Informatique Le système informatique général utilisé par le laboratoire a fait l objet d une déclaration auprès de la CNIL, présente dans le classeur correspondant. Le système informatique est couvert par un contrat de maintenance et de télémaintenance avec la société informatique correspondante. L accès à la télémaintenance ne peut être autorisé que par un personnel du laboratoire. Chaque intervention de cette société est tracée sur un compte rendu émis par l opérateur et permettant d identifier les raisons de l intervention et l objet des modifications. L accès au système informatique est protégé par un code utilisateur et un mot de passe personnel propre à chaque membre du personnel et donnant l accès à certaines fonctionnalités du système par rapport à la fonction de l utilisateur. Ce système est sauvegardé quotidiennement sur 2 supports distincts. Page 32 sur 36
33 La cartographie des différents systèmes informatiques est représentée sur l instruction : Instruction «Cartographie des flux des systèmes informatiques» Les modalités de maîtrise du système informatique du laboratoire sont décrites dans la : Procédure «Maîtrise du système informatique du laboratoire» 3. Gestion administrative La gestion administrative du dossier patient avant et après la réalisation de l analyse ainsi que les modalités de gestion des règlements et de télétransmission vers les organismes payeurs sont décrites dans la procédure. La procédure suivante et les documents associés décrivent toutes les dispositions prises pour maîtriser ce processus Procédure «Traitement administratif du dossier patient» 4. Équipements (Matériel et Métrologie) a. Gestiondu matériel Le matériel du laboratoire est entretenu régulièrement selon les recommandations des fournisseurs. Pour les analyseurs, il existe deux types de maintenance : La maintenance interne, réalisée par le technicien habilité travaillant sur l appareil : elle est effectuée rigoureusement a minima selon les instructions du constructeur et est enregistrée sur un formulaire prévu à cet effet. La maintenance externe, réalisée par le fournisseur : elle peut être : Curative,à la suite d une panneans ce cas une fiche de non-conformité est enregistrée et suivie dans KaliLab ; Préventive, dans le cas d un contrat de maintenanceans ce cas, un bon d intervention est remis au laboratoire par le fournisseur. Les référents des postes sont chargés de vérifier que les maintenances préventives concernant leur champ d activité, sont effectuées selon le planning prévu. Les modalités en sont décrites de façon détaillée dans la : Procédure «Gestion du matériel» Page 33 sur 36
34 b. Gestion des pannes Lorsqu un dysfonctionnement majeur est signalé sur un appareil, et que le délai d'intervention est incompatible avec la durée de conservation des échantillons et/ou le degré d'urgence de réalisation des analyses, une solution de substitution est mise en place : mise en œuvre d une technique manuelle sous-traitance des analyses à un autre laboratoire réalisation de l analyse sur un appareil de substitution Les modalités en sont décrites de façon détaillée dans chaque mode opératoire des automates. c. Gestion de la métrologie Pour les équipements de mesure et de contrôle du laboratoire un programme d étalonnage permet de s assurer de la validité de ces instruments. L étalonnage est confié à des entreprises spécialisées qui nous délivrent un certificat de conformité et/ou d'étalonnage pour chaque matériel. Les modalités en sont décrites de façon détaillée dans la : Procédure «Gestion de la Métrologie» 5. Achats Ce processus garantit la qualité, le stockage, et la traçabilité des produits et matériels achetés (notamment : date de réception, date de mise en service, date de péremption, numéro de lot, ) ainsi que la fiabilité des prestations achetées, qui peuvent avoir une influence sur la satisfaction des patients ou sur la performance du laboratoire. L ensemble de ce processus est géré via KaliLab. a. Achat de matériel Les automates et autres matériels ont été choisis selon des critères très précis. Chaque nouvelle mise en service entraîne la révision de la liste des matériels. Une procédure décrit les principes d achat, de réception et de mise en service des équipements : Procédure «Achat et mise en service des équipements» Page 34 sur 36
35 b. Achat et stockage des réactifs et produits consommables La sélection des fournisseurs est effectuée par la direction sur la base d un référencement à l aide : Des évaluations antérieures des fournisseurs Des offres faites par les fournisseurs consultés. Une évaluation annuelle des fournisseurs est réalisée lors de la revue de direction par analyse des non-conformités associées, la décision de ne pas poursuivre le référencement d un fournisseur ou de le remplacer sera tracée sur le compte rendu de cette revue de direction. Les achats peuvent se faire : sur abonnement : Dans ce cas les spécifications d achat sont retranscrites sur le contrat d abonnement. hors abonnement : Dans ce cas les spécifications d achat sont retranscrites sur le bon de commande, par le responsable de l achat. Le contrôle à la réception permet de valider la conformité du produit livré par rapport aux spécifications. Les directeurs sont ensuite chargés de la vérification de la facturation par rapport à la commande et la livraison. Des zones de stockages de différentes natures ont été définies au sein de chaque laboratoire (réfrigérées, congelées, température ambiante, zone spécifique pour les produits toxiques). Les installations d entreposage et d incubation (réfrigérateurs, congélateurs et étuves) sont vérifiées par l intermédiaire d un relevé quotidien des températures des zones de stockage. Les modalités en sont décrites de façon détaillée dans la : Procédure «Achat et stockage des réactifs et produits consommables et prestations de service» 6. Hygiène, Sécurité et Environnement a. Hygiène et sécurité des personnes Des règles d hygiène ont été définies au sein du laboratoire. D une manière générale, l opérateur doit veiller à ne jamais mettre sa personne ou son environnement en situation de risque non contrôlé. Chaque fois qu une manipulation Page 35 sur 36
36 dangereuse est mise en œuvre elle ne peut l être qu après avoir vérifié que les dispositifs de sécurité sont en place. Des mesures de sécurité incendie, gaz, électricité sont établies au sein du laboratoire dans le cadre de la gestion des locaux. Les modalités en sont décrites de façon détaillée dans la : Procédure «Hygiène et sécurité» b. Gestion des déchets Le laboratoire applique les règles de gestion des déchets exigées selon la réglementation applicable. Les déchets sont séparés en quatre groupes : Les déchets contaminés ; Les déchets toxiques ; Les déchets assimilables à des ordures ménagères ; Les déchets à caractères confidentiels. Ils sont éliminés selon des filières spécifiques, conformément à la réglementation en vigueur et au respect de la confidentialité. Les modalités en sont décrites de façon détaillée dans la : Procédure «Elimination des déchets» c. Entretien des locaux Le laboratoire applique les règles de l hygiène et sécurité du personnel conformément aux exigences de la réglementation en vigueur. L entretien et le nettoyage sont assurés par l agent d entretien de chaque laboratoire ; chaque membre du personnel est chargé cependant d assurer l ordre et la propreté dans le laboratoire. Ces modalités sont reprises dans la : Procédure «Hygiène et sécurité» Page 36 sur 36
Mise en œuvre de l accréditation dans un laboratoire de biologie médicale privé
 Mise en œuvre de l accréditation dans un laboratoire de biologie médicale privé SELARL ANALYS / SELARL ANALYS-I Une démarche d accréditation multisites Journée du 29 Juin 2010 Thierry Avellan [email protected]
Mise en œuvre de l accréditation dans un laboratoire de biologie médicale privé SELARL ANALYS / SELARL ANALYS-I Une démarche d accréditation multisites Journée du 29 Juin 2010 Thierry Avellan [email protected]
Sommaire des documents de la base documentaire 15189 v2012 01/11/2013
 La base documentaire a été complètement révisée pour être en conformité avec cette version 2012 de l ISO 15189. La cartographie des différents processus du LBM a également été modifiée (suppression du
La base documentaire a été complètement révisée pour être en conformité avec cette version 2012 de l ISO 15189. La cartographie des différents processus du LBM a également été modifiée (suppression du
Manuel qualité du laboratoire
 Laboratoire de biologie médicale des Hôpitaux Universitaires de Strasbourg Pôle de biologie 1 place de l Hôpital BP 426 67091 Strasbourg Cedex Manuel qualité du laboratoire Version 04 Rédaction : Cellule
Laboratoire de biologie médicale des Hôpitaux Universitaires de Strasbourg Pôle de biologie 1 place de l Hôpital BP 426 67091 Strasbourg Cedex Manuel qualité du laboratoire Version 04 Rédaction : Cellule
Rôle de l Assurance Qualité dans la recherche clinique
 Rôle de l Assurance Qualité dans la recherche clinique Pôle Qualité / Gestion des Risques 05 Janvier 2012 Plan La qualité d une recherche c est quoi? Bonnes Pratiques Cliniques (BPC) Responsabilités des
Rôle de l Assurance Qualité dans la recherche clinique Pôle Qualité / Gestion des Risques 05 Janvier 2012 Plan La qualité d une recherche c est quoi? Bonnes Pratiques Cliniques (BPC) Responsabilités des
Ce document est la propriété de la MAP. Il ne peut être utilisé, reproduit ou communiqué sans son autorisation. MECANIQUE AERONAUTIQUE PYRENEENNE
 MANUEL MANAGEMENT QUALITE Révision janvier 2010 Ce document est la propriété de la MAP. Il ne peut être utilisé, reproduit ou communiqué sans son autorisation. MECANIQUE AERONAUTIQUE PYRENEENNE Place d
MANUEL MANAGEMENT QUALITE Révision janvier 2010 Ce document est la propriété de la MAP. Il ne peut être utilisé, reproduit ou communiqué sans son autorisation. MECANIQUE AERONAUTIQUE PYRENEENNE Place d
Appendice 2. (normative) Structure de niveau supérieur, texte de base identique, termes et définitions de base communs
 Appendice 2 (normative) Structure de niveau supérieur, texte de base identique, termes et définitions de base communs NOTE Dans les propositions de Texte identique, XXX désigne un qualificatif de norme
Appendice 2 (normative) Structure de niveau supérieur, texte de base identique, termes et définitions de base communs NOTE Dans les propositions de Texte identique, XXX désigne un qualificatif de norme
MANAGEMENT PAR LA QUALITE ET TIC
 Garantir une organisation performante pour satisfaire ses clients et ses partenaires, telle est la finalité d une certification «qualité». On dénombre de nombreux référentiels dont le plus connu et le
Garantir une organisation performante pour satisfaire ses clients et ses partenaires, telle est la finalité d une certification «qualité». On dénombre de nombreux référentiels dont le plus connu et le
MANAGEMENT PAR LA QUALITE ET TIC
 MANAGEMENT PAR LA QUALITE ET TIC Lorraine Garantir une organisation performante pour satisfaire ses clients et ses partenaires, telle est la finalité d une certification «qualité». On dénombre de nombreux
MANAGEMENT PAR LA QUALITE ET TIC Lorraine Garantir une organisation performante pour satisfaire ses clients et ses partenaires, telle est la finalité d une certification «qualité». On dénombre de nombreux
ACCOMPAGNEMENT A LA CERTIFICATION ISO 9001 DE L AGENCE POUR LA RECHERCHE ET L INNOVATION EN CHAMPAGNE-ARDENNE - CARINNA
 1 APPEL D OFFRES ACCOMPAGNEMENT A LA CERTIFICATION ISO 9001 DE L AGENCE POUR LA RECHERCHE ET L INNOVATION EN CHAMPAGNE-ARDENNE - CARINNA JUILLET 2013 2 1. OBJET DE L APPEL D OFFRE Réalisation d un accompagnement
1 APPEL D OFFRES ACCOMPAGNEMENT A LA CERTIFICATION ISO 9001 DE L AGENCE POUR LA RECHERCHE ET L INNOVATION EN CHAMPAGNE-ARDENNE - CARINNA JUILLET 2013 2 1. OBJET DE L APPEL D OFFRE Réalisation d un accompagnement
MANUEL Q S E. Mise à jour : Mai 2014. Qualité - Sécurité - Environnement
 MANUEL Q S E Mise à jour : Mai 2014 Qualité - Sécurité - Environnement Editorial BÂTIMENTS - Privé - Public - Industriel La société RIVASI BTP est implantée dans la Drôme et les Bouches-du-Rhône. Elle
MANUEL Q S E Mise à jour : Mai 2014 Qualité - Sécurité - Environnement Editorial BÂTIMENTS - Privé - Public - Industriel La société RIVASI BTP est implantée dans la Drôme et les Bouches-du-Rhône. Elle
La gestion documentaire les bases d'un système de management de la qualité
 La gestion documentaire les bases d'un système de management de la qualité 8 ème journée professionnelle de l ANTAB - 21 Octobre 2011 Fatima TOUBAIS Ingénieur qualité Accréditation des Laboratoires Direction
La gestion documentaire les bases d'un système de management de la qualité 8 ème journée professionnelle de l ANTAB - 21 Octobre 2011 Fatima TOUBAIS Ingénieur qualité Accréditation des Laboratoires Direction
PROCEDURE ENREGISTREMENT
 Page 1 sur 7 ANNULE ET REMPLACE LES DOCUMENTS SUIVANTS référence 04/PR/001/02/V01 04/PR/001/02/V02 04/PR/001/02/V03 04/PR/001/02/V04 04/PR/001/02/V05 04/PR/001/02/V06 04/PR/001/02/V07 04/PR/001/02/V08
Page 1 sur 7 ANNULE ET REMPLACE LES DOCUMENTS SUIVANTS référence 04/PR/001/02/V01 04/PR/001/02/V02 04/PR/001/02/V03 04/PR/001/02/V04 04/PR/001/02/V05 04/PR/001/02/V06 04/PR/001/02/V07 04/PR/001/02/V08
Manuel Management Qualité ISO 9001 V2000. Réf. 20000-003-002 Indice 13 Pages : 13
 Réf. 20000-003-002 Indice 13 Pages : 13 Manuel Management Qualité ISO 9001 V2000 EVOLUTIONS INDICE DATE NATURE DE L'EVOLUTION 00 09/06/2000 Edition Originale 01 29/09/2000 Modification suite à audit interne
Réf. 20000-003-002 Indice 13 Pages : 13 Manuel Management Qualité ISO 9001 V2000 EVOLUTIONS INDICE DATE NATURE DE L'EVOLUTION 00 09/06/2000 Edition Originale 01 29/09/2000 Modification suite à audit interne
Tremplins de la Qualité. Tome 2
 Tome 2 CET OUVRAGE EST UN GUIDE D INTERPRETATION DE LA NORME NF EN ISO 9001 VERSION 2000 AVANTPROPOS Ce guide d aide à la rédaction du Manuel de Management de la Qualité a été rédigé par la Fédération
Tome 2 CET OUVRAGE EST UN GUIDE D INTERPRETATION DE LA NORME NF EN ISO 9001 VERSION 2000 AVANTPROPOS Ce guide d aide à la rédaction du Manuel de Management de la Qualité a été rédigé par la Fédération
BRANCHE DU NÉGOCE ET PRESTATIONS DE SERVICES
 Septembre 2014 CARTOGRAPHIE DES MÉTIERS DES PRESTATAIRES BRANCHE DU NÉGOCE ET PRESTATIONS DE SERVICES DANS LES DOMAINES MÉDICO-TECHNIQUES www.metiers-medico-techniques.fr CPNEFP de la branche Négoce et
Septembre 2014 CARTOGRAPHIE DES MÉTIERS DES PRESTATAIRES BRANCHE DU NÉGOCE ET PRESTATIONS DE SERVICES DANS LES DOMAINES MÉDICO-TECHNIQUES www.metiers-medico-techniques.fr CPNEFP de la branche Négoce et
Diplôme d Etat d infirmier Référentiel de compétences
 Annexe II Diplôme d Etat d infirmier Référentiel de compétences Les référentiels d activités et de compétences du métier d infirmier diplômé d Etat ne se substituent pas au cadre réglementaire. En effet,
Annexe II Diplôme d Etat d infirmier Référentiel de compétences Les référentiels d activités et de compétences du métier d infirmier diplômé d Etat ne se substituent pas au cadre réglementaire. En effet,
Accueil et Formations du personnel recruté en Stérilisation Centrale. Présenté par Dany GAUDELET et le Dr. Julien MOLINA
 Accueil et Formations du personnel recruté en Stérilisation Centrale Présenté par Dany GAUDELET et le Dr. Julien MOLINA PLAN Introduction Réglementation Circuit du personnel Procédure de Formation Accueil
Accueil et Formations du personnel recruté en Stérilisation Centrale Présenté par Dany GAUDELET et le Dr. Julien MOLINA PLAN Introduction Réglementation Circuit du personnel Procédure de Formation Accueil
MANUEL ASSURANCE QUALITE MANUEL QUALITE CENTRE DE BIOLOGIE DU LANGUEDOC
 MANUEL ASSURANCE QUALITE Ref : MAQ-COMM-TOUS-001-14 Version : 14 Applicable le : 09-01-2015 MANUEL QUALITE CENTRE DE BIOLOGIE DU LANGUEDOC BEGUIER E. - CALIEZ T. - FONTES C. -JEANE. KERDRANVAT H. - LE
MANUEL ASSURANCE QUALITE Ref : MAQ-COMM-TOUS-001-14 Version : 14 Applicable le : 09-01-2015 MANUEL QUALITE CENTRE DE BIOLOGIE DU LANGUEDOC BEGUIER E. - CALIEZ T. - FONTES C. -JEANE. KERDRANVAT H. - LE
C ) Détail volets A, B, C, D et E. Hypothèses (facteurs externes au projet) Sources de vérification. Actions Objectifs Méthode, résultats
 C ) Détail volets A, B, C, D et E Actions Objectifs Méthode, résultats VOLET A : JUMELAGE DE 18 MOIS Rapports d avancement du projet. Réorganisation de l administration fiscale Rapports des voyages d étude.
C ) Détail volets A, B, C, D et E Actions Objectifs Méthode, résultats VOLET A : JUMELAGE DE 18 MOIS Rapports d avancement du projet. Réorganisation de l administration fiscale Rapports des voyages d étude.
MINISTERE DES TECHNOLOGIES COMMUNICATION CENTRE NATIONAL DE L INFORMATIQUE DE L INFORMATION ET DE LA MANUEL DE MANAGEMENT DE LA QUALITE
 MINISTERE DES TECHNOLOGIES DE L INFORMATION ET DE LA COMMUNICATION CENTRE NATIONAL DE L INFORMATIQUE MANUEL DE MANAGEMENT DE LA QUALITE ISO 9001 VERSION 2008 V14 du 25 AVRIL 2012 CNI MANUEL DE MANAGEMENT
MINISTERE DES TECHNOLOGIES DE L INFORMATION ET DE LA COMMUNICATION CENTRE NATIONAL DE L INFORMATIQUE MANUEL DE MANAGEMENT DE LA QUALITE ISO 9001 VERSION 2008 V14 du 25 AVRIL 2012 CNI MANUEL DE MANAGEMENT
Rapport d'audit interne du processus RESSOURCES MATERIELLES NANCY
 Rapport d'audit interne du processus RESSOURCES MATERIELLES Date de l'audit : 23/03/2010 - Processus audité(s) : Système management qualité Site audité : Nancy Référentiel(s) : ISO 9001 : 2008 Équipe d'audit
Rapport d'audit interne du processus RESSOURCES MATERIELLES Date de l'audit : 23/03/2010 - Processus audité(s) : Système management qualité Site audité : Nancy Référentiel(s) : ISO 9001 : 2008 Équipe d'audit
Unité de Recherche Clinique St Louis - Lariboisière Fernand Widal Le 03 Février 2012
 Visite de pré-sélection Visite de Mise en place Murielle COURREGES-VIAUD, ARC Laurence GUERY, ARC responsable Assurance Qualité Véronique JOUIS, Coordinatrice des ARCs Responsable Logistique Unité de Recherche
Visite de pré-sélection Visite de Mise en place Murielle COURREGES-VIAUD, ARC Laurence GUERY, ARC responsable Assurance Qualité Véronique JOUIS, Coordinatrice des ARCs Responsable Logistique Unité de Recherche
D ITIL à D ISO 20000, une démarche complémentaire
 D ITIL à D ISO 20000, une démarche complémentaire www.teamup-consulting.com Teamup Consulting - 1 Certificat nºinf/2007/29319 1 ère société de conseil française certifiée ISO 20000-1:2011 Sommaire Introduction
D ITIL à D ISO 20000, une démarche complémentaire www.teamup-consulting.com Teamup Consulting - 1 Certificat nºinf/2007/29319 1 ère société de conseil française certifiée ISO 20000-1:2011 Sommaire Introduction
REFERENTIEL DE CERTIFICATION
 REFERENTIEL DE CERTIFICATION Référentiel I4 NF 285 Edition : Janvier 2015 N de révision : 4 ORGANISMES CERTIFICATEURS CNPP Cert. Route de la Chapelle Réanville CD 64 - CS 22265 F- 27950 SAINT-MARCEL Tél.
REFERENTIEL DE CERTIFICATION Référentiel I4 NF 285 Edition : Janvier 2015 N de révision : 4 ORGANISMES CERTIFICATEURS CNPP Cert. Route de la Chapelle Réanville CD 64 - CS 22265 F- 27950 SAINT-MARCEL Tél.
Certification ISO 9001 de la prise en charge médicamenteuse
 Certification ISO 9001 de la prise en charge médicamenteuse Jeudi 9 avril 2015 1 Sommaire Présentation de la Maison de santé Marie Galène La démarche de certification ISO 9001 à Marie Galène Pourquoi cette
Certification ISO 9001 de la prise en charge médicamenteuse Jeudi 9 avril 2015 1 Sommaire Présentation de la Maison de santé Marie Galène La démarche de certification ISO 9001 à Marie Galène Pourquoi cette
Système de Management par la Qualité
 Système de Management par la Qualité Rapport Technique Référence Rédigé par MAN-01 Jérémie Dhennin Nombre de pages 9 Le 23 juillet 2015 Diffusion non restreinte ELEMCA SAS / RCS Toulouse 790 447 866 425,
Système de Management par la Qualité Rapport Technique Référence Rédigé par MAN-01 Jérémie Dhennin Nombre de pages 9 Le 23 juillet 2015 Diffusion non restreinte ELEMCA SAS / RCS Toulouse 790 447 866 425,
SYSTÈME DE MANAGEMENT DE LA QUALITÉ
 SYSTÈME DE MANAGEMENT DE LA QUALITÉ Version Objet des modifications 30/10/2009 Conception initiale du manuel 10/02/2011 Amélioration n 1 du système 17/02/2012 Amélioration n 2 du système Etabli & Vérifié
SYSTÈME DE MANAGEMENT DE LA QUALITÉ Version Objet des modifications 30/10/2009 Conception initiale du manuel 10/02/2011 Amélioration n 1 du système 17/02/2012 Amélioration n 2 du système Etabli & Vérifié
RÈGLEMENT DES SERVICES DE RESTAURATION SCOLAIRE ET D ACCUEIL PÉRISCOLAIRE DE LA VILLE DE SEICHAMPS
 RÈGLEMENT DES SERVICES DE RESTAURATION SCOLAIRE ET D ACCUEIL PÉRISCOLAIRE DE LA VILLE DE SEICHAMPS Règlement approuvé par délibération du Conseil Municipal en date du 29 juin 2015 Les parents devront en
RÈGLEMENT DES SERVICES DE RESTAURATION SCOLAIRE ET D ACCUEIL PÉRISCOLAIRE DE LA VILLE DE SEICHAMPS Règlement approuvé par délibération du Conseil Municipal en date du 29 juin 2015 Les parents devront en
Références : norme ISO 15189 et documents COFRAC applicables au laboratoire. Laboratoire Benezech Delhoume
 MANUEL D ASSURANCE LABORATOIRE Références : norme ISO 15189 et documents COFRAC applicables au laboratoire Laboratoire Benezech Delhoume 1 rue Père Colombier 81000 ALBI Tel : 05 63 77 78 90 Fax : 05 63
MANUEL D ASSURANCE LABORATOIRE Références : norme ISO 15189 et documents COFRAC applicables au laboratoire Laboratoire Benezech Delhoume 1 rue Père Colombier 81000 ALBI Tel : 05 63 77 78 90 Fax : 05 63
La version électronique fait foi
 Page 1/6 Localisation : Classeur VERT Disponible sur Intranet A revoir : 10/2015 Objet : La présente procédure a pour objet de décrire les responsabilités et les principes pour la réalisation des prélèvements.
Page 1/6 Localisation : Classeur VERT Disponible sur Intranet A revoir : 10/2015 Objet : La présente procédure a pour objet de décrire les responsabilités et les principes pour la réalisation des prélèvements.
Documentation du système de management de la qualité
 Documentation du système de management de la qualité ISO/IEC 17025:2005 ISO/TR 10013:2001 Formation Assurance Qualité LNCM, Rabat 27-29 Novembre 2007 Marta Miquel, EDQM-CoE 1 ISO/TR 10013:2001 Lignes directrices
Documentation du système de management de la qualité ISO/IEC 17025:2005 ISO/TR 10013:2001 Formation Assurance Qualité LNCM, Rabat 27-29 Novembre 2007 Marta Miquel, EDQM-CoE 1 ISO/TR 10013:2001 Lignes directrices
Démarche de traçabilité globale
 Démarche de traçabilité globale Dr Chi-Dung TA* Responsable Qualité, Danone Vitapole [email protected] La traçabilité existe depuis un certain nombre d'années dans les entreprises à des niveaux plus
Démarche de traçabilité globale Dr Chi-Dung TA* Responsable Qualité, Danone Vitapole [email protected] La traçabilité existe depuis un certain nombre d'années dans les entreprises à des niveaux plus
Projet de santé. Nom du site : N Finess : (Sera prochainement attribué par les services de l ARS) Statut juridique : Raison Sociale :
 Projet de santé Nom du site : N Finess : (Sera prochainement attribué par les services de l ARS) Statut juridique : Raison Sociale : Adresse du siège social : Téléphone : Mail : Version : Etablie en date
Projet de santé Nom du site : N Finess : (Sera prochainement attribué par les services de l ARS) Statut juridique : Raison Sociale : Adresse du siège social : Téléphone : Mail : Version : Etablie en date
Montrer que la gestion des risques en sécurité de l information est liée au métier
 Montrer que la gestion des risques en sécurité de l information est liée au métier Missions de l entreprise Risques métier Solutions pragmatiques et adaptées Savoir gérer la différence Adapter à la norme
Montrer que la gestion des risques en sécurité de l information est liée au métier Missions de l entreprise Risques métier Solutions pragmatiques et adaptées Savoir gérer la différence Adapter à la norme
REGLEMENT DE CONSULTATION
 REGLEMENT DE CONSULTATION Marché publics de fournitures et services CONCEPTION, EDITION, IMPRESSION des Livrets des Hauts de Calvisson Marché n 2015 08 Marché à Procédure Adaptée selon article 28 du Code
REGLEMENT DE CONSULTATION Marché publics de fournitures et services CONCEPTION, EDITION, IMPRESSION des Livrets des Hauts de Calvisson Marché n 2015 08 Marché à Procédure Adaptée selon article 28 du Code
GUIDE OEA. Guide OEA. opérateur
 Guide > > Fiche 1 : Pourquoi être certifié? > > Fiche 2 : Les trois types de certificats et leurs critères > > Fiche 3 : La préparation de votre projet > > Fiche 4 : Le questionnaire d auto-évaluation
Guide > > Fiche 1 : Pourquoi être certifié? > > Fiche 2 : Les trois types de certificats et leurs critères > > Fiche 3 : La préparation de votre projet > > Fiche 4 : Le questionnaire d auto-évaluation
QUALIMS est votre solution!
 Vous êtes un industriel soumis à de fortes contraintes réglementaires? QUALIMS est votre solution! QUALIMS est une société internationale, présente sur le marché des éditeurs de logiciels de gestion qualité
Vous êtes un industriel soumis à de fortes contraintes réglementaires? QUALIMS est votre solution! QUALIMS est une société internationale, présente sur le marché des éditeurs de logiciels de gestion qualité
Sécurité Sanitaire des Aliments. Saint-Pierre, le 19 novembre 2013. Olivier BOUTOU. Les outils de la qualité sanitaire dans les pays du sud
 Sécurité Sanitaire des Aliments Saint-Pierre, le 19 novembre 2013 Olivier BOUTOU Les outils de la qualité sanitaire dans les pays du sud Faisons connaissance Missions au sein d AFNOR Animation de formation
Sécurité Sanitaire des Aliments Saint-Pierre, le 19 novembre 2013 Olivier BOUTOU Les outils de la qualité sanitaire dans les pays du sud Faisons connaissance Missions au sein d AFNOR Animation de formation
REF01 Référentiel de labellisation des laboratoires de recherche_v3
 Introduction Le présent référentiel de labellisation est destiné aux laboratoires qui souhaitent mettre en place un dispositif de maîtrise de la qualité des mesures. La norme ISO 9001 contient essentiellement
Introduction Le présent référentiel de labellisation est destiné aux laboratoires qui souhaitent mettre en place un dispositif de maîtrise de la qualité des mesures. La norme ISO 9001 contient essentiellement
Depuis l'an 2000, le Ministère de la Santé Publique (MSP) a mis en place une procédure d accréditation pour améliorer la qualité des services
 Depuis l'an 2000, le Ministère de la Santé Publique (MSP) a mis en place une procédure d accréditation pour améliorer la qualité des services hospitaliers. Ce projet d amélioration de la qualité porte
Depuis l'an 2000, le Ministère de la Santé Publique (MSP) a mis en place une procédure d accréditation pour améliorer la qualité des services hospitaliers. Ce projet d amélioration de la qualité porte
PROFIL DE POSTE DU CONDUCTEUR AMBULANCIER SMUR :
 PROFIL DE POSTE DU CONDUCTEUR AMBULANCIER SMUR : IDENTIFICATION DU POSTE : Titre de la fonction : Conducteur Ambulancier SMUR*. Etablissement : Centre Hospitalier Régional Universitaire de Brest. Service
PROFIL DE POSTE DU CONDUCTEUR AMBULANCIER SMUR : IDENTIFICATION DU POSTE : Titre de la fonction : Conducteur Ambulancier SMUR*. Etablissement : Centre Hospitalier Régional Universitaire de Brest. Service
Hôpital performant et soins de qualité. La rencontre des extrêmes estelle
 Hôpital performant et soins de qualité. La rencontre des extrêmes estelle possible? 18 octobre 2012 Professeur Philippe KOLH CIO, Directeur du Service des Informations Médico-Economiques CHU de LIEGE Plan
Hôpital performant et soins de qualité. La rencontre des extrêmes estelle possible? 18 octobre 2012 Professeur Philippe KOLH CIO, Directeur du Service des Informations Médico-Economiques CHU de LIEGE Plan
CENTRE HOSPITALIER DU GERS 10 Rue Michelet BP 363 32008 AUCH Cédex 8 MARCHE PUBLIC DE TRAVAUX REGLEMENT DE LA CONSULTATION
 CENTRE HOSPITALIER DU GERS 10 Rue Michelet BP 363 32008 AUCH Cédex 8 MARCHE PUBLIC DE TRAVAUX REGLEMENT DE LA CONSULTATION MARCHE DE TRAVAUX DE PEINTURE A LA MAS VILLENEUVE PROCEDURE ADAPTEE AVEC PUBLICITE
CENTRE HOSPITALIER DU GERS 10 Rue Michelet BP 363 32008 AUCH Cédex 8 MARCHE PUBLIC DE TRAVAUX REGLEMENT DE LA CONSULTATION MARCHE DE TRAVAUX DE PEINTURE A LA MAS VILLENEUVE PROCEDURE ADAPTEE AVEC PUBLICITE
Référentiel Officine
 Référentiel Officine Inscrire la formation dans la réalité et les besoins de la pharmacie d officine de demain - Ce référentiel décrit dans le cadre des missions et des activités du pharmacien d officine
Référentiel Officine Inscrire la formation dans la réalité et les besoins de la pharmacie d officine de demain - Ce référentiel décrit dans le cadre des missions et des activités du pharmacien d officine
Systèmes et réseaux d information et de communication
 233 DIRECTEUR DES SYSTÈMES ET RÉSEAUX D INFORMATION ET DE COMMUNICATION Code : SIC01A Responsable des systèmes et réseaux d information FPESIC01 Il conduit la mise en œuvre des orientations stratégiques
233 DIRECTEUR DES SYSTÈMES ET RÉSEAUX D INFORMATION ET DE COMMUNICATION Code : SIC01A Responsable des systèmes et réseaux d information FPESIC01 Il conduit la mise en œuvre des orientations stratégiques
BEP métiers des services administratifs BREVET D'ÉTUDES PROFESSIONNELLES MÉTIERS DES SERVICES ADMINISTRATIFS
 BREVET D'ÉTUDES PROFESSIONNELLES MÉTIERS DES SERVICES ADMINISTRATIFS ANNEXE I a RÉFÉRENTIEL DES ACTIVITÉS PROFESSIONNELLES I. APPELLATION DU DIPLÔME BEP métiers des services administratifs RÉFÉRENTIEL
BREVET D'ÉTUDES PROFESSIONNELLES MÉTIERS DES SERVICES ADMINISTRATIFS ANNEXE I a RÉFÉRENTIEL DES ACTIVITÉS PROFESSIONNELLES I. APPELLATION DU DIPLÔME BEP métiers des services administratifs RÉFÉRENTIEL
PRESENTATION CERTIFICATION DE SERVICE «Centres de formation pour les activités privées de sécurité et de sûreté»
 PRESENTATION CERTIFICATION DE SERVICE «Centres de formation pour les activités privées de sécurité et de sûreté» Ce référentiel s adresse à toutes les actions de formation pouvant être dispensées dans
PRESENTATION CERTIFICATION DE SERVICE «Centres de formation pour les activités privées de sécurité et de sûreté» Ce référentiel s adresse à toutes les actions de formation pouvant être dispensées dans
CATALOGUE DE FORMATIONS 2014 2015
 CATALOGUE DE FORMATIONS 2014 2015 Professionnels de l alimentation 06.47.75.88.57 HQSA Consulting [email protected] Numéro de déclaration de prestataire de formation : SIRET SIRET : 804 : 284 284 420
CATALOGUE DE FORMATIONS 2014 2015 Professionnels de l alimentation 06.47.75.88.57 HQSA Consulting [email protected] Numéro de déclaration de prestataire de formation : SIRET SIRET : 804 : 284 284 420
Eric CIOTTI Président du Conseil général des Alpes-Maritimes
 A sa création, en 2005, la FORCE 06, rattachée à l ONF, constituait une unité de forestiers-sapeurs dédiée aux travaux d entretien des infrastructures de Défense des Forêts Contre l Incendie (DFCI) et
A sa création, en 2005, la FORCE 06, rattachée à l ONF, constituait une unité de forestiers-sapeurs dédiée aux travaux d entretien des infrastructures de Défense des Forêts Contre l Incendie (DFCI) et
Catalogue d offre de services de télésanté
 Catalogue d offre de services de télésanté Document révisé 2014 12 08 Ce document est basé sur le gabarit ITIL utilisé dans la région 05 - Estrie. Table des matières DEFINITIONS... III GLOSSAIRE ET ACRONYMES...
Catalogue d offre de services de télésanté Document révisé 2014 12 08 Ce document est basé sur le gabarit ITIL utilisé dans la région 05 - Estrie. Table des matières DEFINITIONS... III GLOSSAIRE ET ACRONYMES...
Démarche Lean management
 Démarche Lean management Vers une ville INTELLIGENTE au sein d un Service de loisirs 10 octobre 2013 Objectifs de la présentation 1) Partager l expérience du Lean management au sein de l administration
Démarche Lean management Vers une ville INTELLIGENTE au sein d un Service de loisirs 10 octobre 2013 Objectifs de la présentation 1) Partager l expérience du Lean management au sein de l administration
solution technologique globale qui couvre en
 Dealer Management System solution technologique globale qui couvre en amont tous les besoins fonctionnels et techniques de l activité d un distributeur de véhicules : magasin, atelier, VN/VO. Adaptable
Dealer Management System solution technologique globale qui couvre en amont tous les besoins fonctionnels et techniques de l activité d un distributeur de véhicules : magasin, atelier, VN/VO. Adaptable
LE PROJET QUALITE-GESTION DES RISQUES- DEVELOPPEMENT DURABLE
 LE PROJET QUALITE-GESTION DES RISQUES- DEVELOPPEMENT DURABLE 1 LA POLITIQUE QUALITE-GESTION DES RISQUES Depuis 2003, la Direction s engage à poursuivre, la démarche qualité et à développer une gestion
LE PROJET QUALITE-GESTION DES RISQUES- DEVELOPPEMENT DURABLE 1 LA POLITIQUE QUALITE-GESTION DES RISQUES Depuis 2003, la Direction s engage à poursuivre, la démarche qualité et à développer une gestion
Règles de certification
 N d identification : NF212 N de révision : 7.3 Mise à jour : 04/02/2015 Et addendum n 1 du 04/02/2015 Date de mise en application : 04/02/2015 Règles de certification SERVICES DE DEPANNAGE/REMORQUAGE DE
N d identification : NF212 N de révision : 7.3 Mise à jour : 04/02/2015 Et addendum n 1 du 04/02/2015 Date de mise en application : 04/02/2015 Règles de certification SERVICES DE DEPANNAGE/REMORQUAGE DE
Référentiel Engagement de service
 Toute reproduction intégrale ou partielle faite en dehors d une demande expresse d AFNOR Certification ou de ses ayants droits ou ayants cause est illicite (code de la propriété intellectuelle artt. L122-4
Toute reproduction intégrale ou partielle faite en dehors d une demande expresse d AFNOR Certification ou de ses ayants droits ou ayants cause est illicite (code de la propriété intellectuelle artt. L122-4
SOMMAIRE 1 LA POLITIQUE GENERALE ET LA POLITIQUE QUALITE 2 UNE ORGANISATION PROFESSIONNELLE FORTE ET GARANTE DE SES MEMBRES 3 NOTRE SMQ
 Manuel Qualité 5 place du Rosoir 21000 DIJON Tél. : 03.80.59.65.20 Fax : 03.80.53.09.50 Mèl : [email protected] www.bfc.experts-comptables.fr SOMMAIRE 1 LA POLITIQUE GENERALE ET LA POLITIQUE
Manuel Qualité 5 place du Rosoir 21000 DIJON Tél. : 03.80.59.65.20 Fax : 03.80.53.09.50 Mèl : [email protected] www.bfc.experts-comptables.fr SOMMAIRE 1 LA POLITIQUE GENERALE ET LA POLITIQUE
Coordination de la Gestion des risques. Bilan - Programme
 Coordination de la Gestion des risques Bilan - Programme La démarche Mise en place en 2007 Regroupe l ensemble des Vigilances Sanitaire. Associe le programme CLIN Associe les risques liés aux vigilances
Coordination de la Gestion des risques Bilan - Programme La démarche Mise en place en 2007 Regroupe l ensemble des Vigilances Sanitaire. Associe le programme CLIN Associe les risques liés aux vigilances
Liège, le 29 juillet 2013. APPEL INTERNE et EXTERNE AUX CANDIDATURES N 2013-085
 Centre Hospitalier Universitaire de Liège Domaine Universitaire du Sart Tilman B35 4000 LIEGE 1 www.chuliege.be Département de Gestion des Ressources Humaines Service Recrutement Liège, le 29 juillet 2013
Centre Hospitalier Universitaire de Liège Domaine Universitaire du Sart Tilman B35 4000 LIEGE 1 www.chuliege.be Département de Gestion des Ressources Humaines Service Recrutement Liège, le 29 juillet 2013
Etude des possibilités de passerelles entre les CQP des Entreprises de l industrie pharmaceutique et les CQP des industries chimiques
 Etude des possibilités de passerelles entre les CQP des Entreprises de l industrie et les CQP des industries chimiques @ COPYRIGHT LEEM - Page 1 sur 51 Sommaire 1 - Finalités des passerelles... 3 2 - Principes
Etude des possibilités de passerelles entre les CQP des Entreprises de l industrie et les CQP des industries chimiques @ COPYRIGHT LEEM - Page 1 sur 51 Sommaire 1 - Finalités des passerelles... 3 2 - Principes
CAHIER DES CLAUSES PARTICULIERES. Transports sanitaires
 Marché de service CAHIER DES CLAUSES PARTICULIERES Transports sanitaires - Etablissement contractant : CENTRE HOSPITALIER 858 rue des Drs. Devillers 02120 GUISE 03.23.51.55.55 03.23.51.55.35 Procédure
Marché de service CAHIER DES CLAUSES PARTICULIERES Transports sanitaires - Etablissement contractant : CENTRE HOSPITALIER 858 rue des Drs. Devillers 02120 GUISE 03.23.51.55.55 03.23.51.55.35 Procédure
Mise en place d'une démarche qualité et maintien de la certification ISO 9001:2008 dans un système d'information
 Mise en place d'une démarche qualité et maintien de la certification ISO 9001:2008 dans un système d'information IMGT The international ImMunoGeneTics information system Joumana Jabado-Michaloud IE Bioinformatique,
Mise en place d'une démarche qualité et maintien de la certification ISO 9001:2008 dans un système d'information IMGT The international ImMunoGeneTics information system Joumana Jabado-Michaloud IE Bioinformatique,
Le 18/09/2015 à 12h00 à Pessac en Gironde (voir article 6 du présent règlement)
 LA MONNAIE DE PARIS 11, quai de Conti - 75 270 Paris cedex 06 Voie Romaine - 33 600 Pessac www.monnaiedeparis.fr Direction des Finances et de la Performance MAPA 75-15 RÈGLEMENT DE LA CONSULTATION Version
LA MONNAIE DE PARIS 11, quai de Conti - 75 270 Paris cedex 06 Voie Romaine - 33 600 Pessac www.monnaiedeparis.fr Direction des Finances et de la Performance MAPA 75-15 RÈGLEMENT DE LA CONSULTATION Version
Audit interne. Audit interne
 Définition de l'audit interne L'Audit Interne est une activité indépendante et objective qui donne à une organisation une assurance sur le degré de maîtrise de ses opérations, lui apporte ses conseils
Définition de l'audit interne L'Audit Interne est une activité indépendante et objective qui donne à une organisation une assurance sur le degré de maîtrise de ses opérations, lui apporte ses conseils
www.digitech-sa.ch PRESENTATION 2009 L'ingénierie Documentaire
 PRESENTATION 2009 L'ingénierie Documentaire 1 Historique 1992 Création de Digitech France 1993 Création de Digitech Suisse 1999 Rachat de la société DOC PLUS 2000 Rachat du département AIRS (gestion documentaire)
PRESENTATION 2009 L'ingénierie Documentaire 1 Historique 1992 Création de Digitech France 1993 Création de Digitech Suisse 1999 Rachat de la société DOC PLUS 2000 Rachat du département AIRS (gestion documentaire)
QUALITE DE SERVICE DES ENTREPRISES DE TRADUCTION
 REFERENTIEL DE CERTIFICATION DE SERVICE : QUALITE DE SERVICE DES ENTREPRISES DE TRADUCTION REF. : RE/TRAD/10 V1 08/11/2010 LE DEMANDEUR Bureau Veritas Certification Nom : Pierrick Mathieu Nom : Gilbert
REFERENTIEL DE CERTIFICATION DE SERVICE : QUALITE DE SERVICE DES ENTREPRISES DE TRADUCTION REF. : RE/TRAD/10 V1 08/11/2010 LE DEMANDEUR Bureau Veritas Certification Nom : Pierrick Mathieu Nom : Gilbert
ACCORD SUR LES ASTREINTES UES CAPGEMINI
 ACCORD SUR LES ASTREINTES UES CAPGEMINI PREAMBULE Pour répondre à la continuité du service que l entreprise doit assurer à ses clients, certaines activités pour certains rôles ou fonctions, recourent à
ACCORD SUR LES ASTREINTES UES CAPGEMINI PREAMBULE Pour répondre à la continuité du service que l entreprise doit assurer à ses clients, certaines activités pour certains rôles ou fonctions, recourent à
Marquage CE des Granulats
 REFERENTIEL SECTORIEL POUR LA Page 1 sur 11 MAÎTRISE DE LA PRODUCTION DES GRANULATS (Système d'attestation de conformité 2+) SOMMAIRE : Article 1 Objet et domaine d application Article 2 Intervenants dans
REFERENTIEL SECTORIEL POUR LA Page 1 sur 11 MAÎTRISE DE LA PRODUCTION DES GRANULATS (Système d'attestation de conformité 2+) SOMMAIRE : Article 1 Objet et domaine d application Article 2 Intervenants dans
Chapitre 1 : Introduction au contrôle de gestion. Marie Gies - Contrôle de gestion et gestion prévisionnelle - Chapitre 1
 Chapitre 1 : Introduction au contrôle de gestion Introduction 2 Contrôle de gestion : fonction aujourd hui bien institutionnalisée dans les entreprises Objectif : permettre une gestion rigoureuse et une
Chapitre 1 : Introduction au contrôle de gestion Introduction 2 Contrôle de gestion : fonction aujourd hui bien institutionnalisée dans les entreprises Objectif : permettre une gestion rigoureuse et une
Conseil en Technologie et Systèmes d Information
 Conseil en Technologie et Systèmes d Information SMQ Offre Infrastructures_AT V2 SOMMAIRE Offre de services Infogérance pour PME, TPE, Administrations & Institutions NOTRE OFFRE COMPETENCES EXPERTISE SYSTEMES
Conseil en Technologie et Systèmes d Information SMQ Offre Infrastructures_AT V2 SOMMAIRE Offre de services Infogérance pour PME, TPE, Administrations & Institutions NOTRE OFFRE COMPETENCES EXPERTISE SYSTEMES
Conditions Générales d Intervention du CSTB pour la délivrance d une HOMOLOGATION COUVERTURE
 DEPARTEMENT ENVELOPPES ET REVETEMENTS Constructions Légères et Couvertures Conditions Générales d Intervention du CSTB pour la délivrance d une HOMOLOGATION COUVERTURE Livraison Cahier V1 de Mars 2010
DEPARTEMENT ENVELOPPES ET REVETEMENTS Constructions Légères et Couvertures Conditions Générales d Intervention du CSTB pour la délivrance d une HOMOLOGATION COUVERTURE Livraison Cahier V1 de Mars 2010
Administration canadienne de la sûreté du transport aérien
 Administration canadienne de la sûreté du transport aérien Norme relative au système de gestion des fournisseurs de services de contrôle de l ACSTA Octobre 2009 La présente norme est assujettie aux demandes
Administration canadienne de la sûreté du transport aérien Norme relative au système de gestion des fournisseurs de services de contrôle de l ACSTA Octobre 2009 La présente norme est assujettie aux demandes
REGLES DE CERTIFICATION MARQUE NF DENTAIRE PARTIE 3 OBTENTION DE LA CERTIFICATION
 REGLES DE CERTIFICATION MARQUE NF DENTAIRE PARTIE 3 OBTENTION DE LA CERTIFICATION SOMMAIRE 3.1. Constitution du dossier de demande 3.2. Processus d'évaluation initiale Rev. 9 mai 2012 PROCESSUS D'OBTENTION
REGLES DE CERTIFICATION MARQUE NF DENTAIRE PARTIE 3 OBTENTION DE LA CERTIFICATION SOMMAIRE 3.1. Constitution du dossier de demande 3.2. Processus d'évaluation initiale Rev. 9 mai 2012 PROCESSUS D'OBTENTION
Accréditation des laboratoires de ais
 Accréditation des laboratoires de biologie médicale m français ais Hélène MEHAY Directrice de la section Santé Humaine Cofrac 52 rue Jacques Hillairet 75012 Paris Journée FHF Centre 30 juin 2015 1 L accréditation
Accréditation des laboratoires de biologie médicale m français ais Hélène MEHAY Directrice de la section Santé Humaine Cofrac 52 rue Jacques Hillairet 75012 Paris Journée FHF Centre 30 juin 2015 1 L accréditation
Phase 2 : Mettre en œuvre. Gestion des projets. Gestion documentaire. Gestion du changement. R Collomp - D Qualité D 2 Ges4on documentaire
 Phase 2 : Mettre en œuvre Gestion des projets Gestion Gestion du changement Gestion Plusieurs documents dans un organisme : Documentation technique Documentation sociale Documentation commerciale Documentation
Phase 2 : Mettre en œuvre Gestion des projets Gestion Gestion du changement Gestion Plusieurs documents dans un organisme : Documentation technique Documentation sociale Documentation commerciale Documentation
LABO EXPRESS - 6, avenue Charles de Gaulle - 78150 Le Chesnay 451 372 361 00027 RCS Versailles SARL au capital de 20 000 Tél. 01.39.43.78.78 / Fax.
 LABO EXPRESS - 6, avenue Charles de Gaulle - 78150 Le Chesnay 451 372 361 00027 RCS Versailles SARL au capital de 20 000 Tél. 01.39.43.78.78 / Fax. 01.39.43.78.79 www.laboexpress.fr SOMMAIRE I. PRESENTATION
LABO EXPRESS - 6, avenue Charles de Gaulle - 78150 Le Chesnay 451 372 361 00027 RCS Versailles SARL au capital de 20 000 Tél. 01.39.43.78.78 / Fax. 01.39.43.78.79 www.laboexpress.fr SOMMAIRE I. PRESENTATION
Liège, le 23 avril 2015. APPEL INTERNE et EXTERNE AUX CANDIDATURES N 2015/073
 Centre Hospitalier Universitaire de Liège Domaine Universitaire du Sart Tilman B35 4000 LIEGE 1 www.chuliege.be Département de Gestion des Ressources Humaines Service Recrutement Liège, le 23 avril 2015
Centre Hospitalier Universitaire de Liège Domaine Universitaire du Sart Tilman B35 4000 LIEGE 1 www.chuliege.be Département de Gestion des Ressources Humaines Service Recrutement Liège, le 23 avril 2015
Système Management Environnemental
 Système Management Environnemental Laboratoire de Touraine Laboratoire de Touraine Laboratoire de Touraine - Bassin Eaux Pluviales Environnemental Politique Qualité Sécurité Environnement Sommaire Norme
Système Management Environnemental Laboratoire de Touraine Laboratoire de Touraine Laboratoire de Touraine - Bassin Eaux Pluviales Environnemental Politique Qualité Sécurité Environnement Sommaire Norme
Réseau National de Laboratoires * * * * * * * * * *
 République du Sénégal Ministère de la Santé et de l Action Sociale Direction Générale de la Santé Direction des Laboratoires Réseau National de Laboratoires * * * * * * * * * * PLAN DE FORMATION DES PERSONNELS
République du Sénégal Ministère de la Santé et de l Action Sociale Direction Générale de la Santé Direction des Laboratoires Réseau National de Laboratoires * * * * * * * * * * PLAN DE FORMATION DES PERSONNELS
Nettoyage des réservoirs
 Marché à Procédure Adapté Art.146 du Code des Marchés Publics Programme 2012/2014 Entretien des ouvrages de stockage Marché. 2011.AEP.001 Nettoyage des réservoirs Règlement de la Consultation Personne
Marché à Procédure Adapté Art.146 du Code des Marchés Publics Programme 2012/2014 Entretien des ouvrages de stockage Marché. 2011.AEP.001 Nettoyage des réservoirs Règlement de la Consultation Personne
Améliorer l efficacité de votre fonction RH
 Améliorer l efficacité de votre fonction RH Des tendances accentuées par un environnement économique et social en constante évolution La fonction RH doit répondre à des exigences croissantes en termes
Améliorer l efficacité de votre fonction RH Des tendances accentuées par un environnement économique et social en constante évolution La fonction RH doit répondre à des exigences croissantes en termes
RESPONSABLE DU DEPARTEMENT ADMINISTRATIF ET FINANCIER
 RESPONSABLE DU DEPARTEMENT ADMINISTRATIF ET FINANCIER Rattaché à la Direction Générale de PORTNET S.A, le responsable du département administratif et financier a pour mission d assurer la bonne performance
RESPONSABLE DU DEPARTEMENT ADMINISTRATIF ET FINANCIER Rattaché à la Direction Générale de PORTNET S.A, le responsable du département administratif et financier a pour mission d assurer la bonne performance
Introduction au métier d ARC. en recherche clinique
 Introduction au métier d ARC en recherche clinique Déroulement d un projet de recherche clinique Idée Faisabilité Avant Pendant Après Protocole accepté Démarches réglementaires Déroulement de l étude Analyse
Introduction au métier d ARC en recherche clinique Déroulement d un projet de recherche clinique Idée Faisabilité Avant Pendant Après Protocole accepté Démarches réglementaires Déroulement de l étude Analyse
Rapport d'audit étape 2
 Rapport d'audit étape 2 Numéro d'affaire: Nom de l'organisme : CMA 76 Type d'audit : audit de renouvellement Remarques sur l'audit Normes de référence : Autres documents ISO 9001 : 2008 Documents du système
Rapport d'audit étape 2 Numéro d'affaire: Nom de l'organisme : CMA 76 Type d'audit : audit de renouvellement Remarques sur l'audit Normes de référence : Autres documents ISO 9001 : 2008 Documents du système
Notre écoute et notre réactivité
 2010 Manuel Qualité Politique qualité Notre écoute et notre réactivité sont la garantie de notre capacité à réaliser des prestations d un haut niveau de qualité. Il s agit de remplir les missions fixées
2010 Manuel Qualité Politique qualité Notre écoute et notre réactivité sont la garantie de notre capacité à réaliser des prestations d un haut niveau de qualité. Il s agit de remplir les missions fixées
L agrément des entreprises pour le conseil indépendant à l utilisation de produits phytopharmaceutiques. Ordre du jour
 L agrément des entreprises pour le conseil indépendant à l utilisation de produits phytopharmaceutiques Ordre du jour 1. Le cadre réglementaire 2. Les exigences organisationnelles et leurs applications
L agrément des entreprises pour le conseil indépendant à l utilisation de produits phytopharmaceutiques Ordre du jour 1. Le cadre réglementaire 2. Les exigences organisationnelles et leurs applications
ARRÊTÉ du. relatif au cahier des charges de santé de la maison de santé mentionné à l article L. 6323-3 du code de la santé publique.
 RÉPUBLIQUE FRANÇAISE Ministère du travail, de l emploi NOR : ARRÊTÉ du relatif au cahier des charges de santé de la maison de santé mentionné à l article L. 6323-3 du code de la santé publique. Le ministre
RÉPUBLIQUE FRANÇAISE Ministère du travail, de l emploi NOR : ARRÊTÉ du relatif au cahier des charges de santé de la maison de santé mentionné à l article L. 6323-3 du code de la santé publique. Le ministre
Liège, le 30 mars 2015. APPEL INTERNE et EXTERNE AUX CANDIDATURES N 2015/058
 Centre Hospitalier Universitaire de Liège Domaine Universitaire du Sart Tilman B35 4000 LIEGE 1 www.chuliege.be Département de Gestion des Ressources Humaines Service Recrutement Liège, le 30 mars 2015
Centre Hospitalier Universitaire de Liège Domaine Universitaire du Sart Tilman B35 4000 LIEGE 1 www.chuliege.be Département de Gestion des Ressources Humaines Service Recrutement Liège, le 30 mars 2015
Qualité et gestion des risques
 formation 2007 Qualité et gestion des risques Qualité et certification HAS Démarche qualité Qualité et certification ISO Qualité en imagerie Qualité au laboratoire Management des risques Risques spécifiques
formation 2007 Qualité et gestion des risques Qualité et certification HAS Démarche qualité Qualité et certification ISO Qualité en imagerie Qualité au laboratoire Management des risques Risques spécifiques
Journées de formation DMP
 Journées de formation DMP Le DMP dans l écosystème Chantal Coru, Bureau Etudes, ASIP Santé Mardi 26 juin 2012 Processus de coordination au centre des prises en charge Quelques exemples Maisons de santé
Journées de formation DMP Le DMP dans l écosystème Chantal Coru, Bureau Etudes, ASIP Santé Mardi 26 juin 2012 Processus de coordination au centre des prises en charge Quelques exemples Maisons de santé
Le champ d application de notre système de management
 NOS ACTIVITES NOTRE ENGAGEMENT NOTRE FONCTIONNEMENT Le périmètre de notre système de management Le périmètre du Système de Management correspond au site de Bordeaux (usine, Unité de Développement des Systèmes
NOS ACTIVITES NOTRE ENGAGEMENT NOTRE FONCTIONNEMENT Le périmètre de notre système de management Le périmètre du Système de Management correspond au site de Bordeaux (usine, Unité de Développement des Systèmes
CAHIER DES CHARGES GARDIENNAGE
 Association des Responsables de Services Généraux Facilities Managers Association CAHIER DES CHARGES GARDIENNAGE Avertissement : ce document est un exemple de cahier des charges Gardiennage établi pour
Association des Responsables de Services Généraux Facilities Managers Association CAHIER DES CHARGES GARDIENNAGE Avertissement : ce document est un exemple de cahier des charges Gardiennage établi pour
SECTION II RELATIVE AU PRÉLEVEUR
 SECTION II RELATIVE AU PRÉLEVEUR II-0 INDEX SECTION II Pages Section relative au préleveur Heures d ouvertures des laboratoires pour clients externes Requête régionale II-2 II-2 II-3 Informations requises
SECTION II RELATIVE AU PRÉLEVEUR II-0 INDEX SECTION II Pages Section relative au préleveur Heures d ouvertures des laboratoires pour clients externes Requête régionale II-2 II-2 II-3 Informations requises
Qualité Sécurité Environnement
 Qualité Sécurité Environnement FORMATION AUDIT CONSEIL EXPERTISE >> Catalogue 2014 Nos innovations: e-learning, évaluation des compétences personnalisation Formation Hygiène Alimentaire ISO 9001 : 2008...
Qualité Sécurité Environnement FORMATION AUDIT CONSEIL EXPERTISE >> Catalogue 2014 Nos innovations: e-learning, évaluation des compétences personnalisation Formation Hygiène Alimentaire ISO 9001 : 2008...
DEVENIR ANIMATEUR CERTIFIE DE LA DEMARCHE LEAN
 DEVENIR ANIMATEUR CERTIFIE DE LA DEMARCHE LEAN Certification CQPM réf : 2008 07 69 0272 Animateur de la démarche LEAN pour l amélioration de la performance et des processus. BUTS DE LA FORMATION : Etre
DEVENIR ANIMATEUR CERTIFIE DE LA DEMARCHE LEAN Certification CQPM réf : 2008 07 69 0272 Animateur de la démarche LEAN pour l amélioration de la performance et des processus. BUTS DE LA FORMATION : Etre
PREFET DES BOUCHES-DU-RHONE
 PREFET DES BOUCHES-DU-RHONE DIRECTION DEPARTEMENTALE INTERMINISTERIELLE DE LA PROTECTION DES POPULATIONS Siège : 22, Rue Borde - 13285 MARSEILLE CEDEX 08 Publipostage MARSEILLE, 03.04.2013 Téléphone :
PREFET DES BOUCHES-DU-RHONE DIRECTION DEPARTEMENTALE INTERMINISTERIELLE DE LA PROTECTION DES POPULATIONS Siège : 22, Rue Borde - 13285 MARSEILLE CEDEX 08 Publipostage MARSEILLE, 03.04.2013 Téléphone :
Programme Hôpital numérique
 Programme Hôpital numérique Boite à outils pour l atteinte des pré-requis Fiches pratiques Octobre 2012 Direction générale de l offre de soins Sommaire 1. LE PROGRAMME HOPITAL NUMERIQUE... 3 2. LE SOCLE
Programme Hôpital numérique Boite à outils pour l atteinte des pré-requis Fiches pratiques Octobre 2012 Direction générale de l offre de soins Sommaire 1. LE PROGRAMME HOPITAL NUMERIQUE... 3 2. LE SOCLE
OUVERTURE ET MISE EN PLACE
 OUVERTURE ET MISE EN PLACE Estelle Marcault 20/01/2012 URC PARIS NORD 1 Ouverture et mise en place Trois types de visites/ réunions peuvent avoir lieu : Visite de sélection Réunion investigateur Visite
OUVERTURE ET MISE EN PLACE Estelle Marcault 20/01/2012 URC PARIS NORD 1 Ouverture et mise en place Trois types de visites/ réunions peuvent avoir lieu : Visite de sélection Réunion investigateur Visite
Manuel Qualité. Satisfaire durablement et efficacement nos clients
 Q Manuel Qualité Satisfaire durablement et efficacement nos clients Politique Qualité Acteur reconnu de la sécurité des personnes et des biens et de la protection de l environnement, Apave a la volonté
Q Manuel Qualité Satisfaire durablement et efficacement nos clients Politique Qualité Acteur reconnu de la sécurité des personnes et des biens et de la protection de l environnement, Apave a la volonté
